Неорганические материалы, 2023, T. 59, № 2, стр. 216-226
Стереолитографическое формирование алюмооксидной керамики из полимеризуемых прекурсоров, содержащих хлориды алюминия
Д. С. Ларионов 1, П. В. Евдокимов 1, 2, А. В. Гаршев 1, 2, Д. А. Козлов 1, В. И. Путляев 1, 2, *
1 Московский государственный университет им. М.В. Ломоносова,
Факультет наук о материалах
119991 Москва, Ленинские горы, 1, с. 73, Россия
2 Московский государственный университет им. М.В. Ломоносова,
Химический факультет
119991 Москва, Ленинские горы, 1, с. 3, Россия
* E-mail: valery.putlayev@gmail.com
Поступила в редакцию 27.12.2021
После доработки 13.07.2022
Принята к публикации 14.07.2022
- EDN: YDPISK
- DOI: 10.31857/S0002337X23020100
Аннотация
Предложен подход к созданию полимеризуемых прекурсоров корундовой и оксинитридной керамики и их использованию в стереолитографическом формировании алюмосодержащей керамики. Исходя из однородности (оптической прозрачности) и легкости фотополимеризации, процента потери массы при термолизе отобраны три прекурсора на основе хлоридов алюминия (безводного и гексагидрата), а также основного хлорида алюминия. Охарактеризовано поведение прекурсоров при обжиге в атмосфере аммиака для синтеза оксинитридной керамики и при обжиге на воздухе для изготовления корундовой керамики из гомогенных прекурсоров. Апробирована стереолитографическая 3D-печать корундовой керамики, в т. ч. с использованием разработанных прекурсоров в виде фотополимеризуемых связок, позволяющих повысить долю оксида алюминия в фотосуспензии.
ВВЕДЕНИЕ
Для изготовления современной технической керамики активно используются методы аддитивного производства, в частности 3D-печать, позволяющая сформовать изделие любой сложной формы и внутренней архитектуры. С точки зрения пространственного разрешения и производительности практические перспективы имеет стереолитографическая 3D-печать с послойной засветкой через динамическую маску (называемая DLP, Digital Light Processing), которая характеризуется лучшим на сегодня сочетанием производительности и латерального разрешения (не хуже 50 мкм) [1, 2].
Перспективы использования полимерных прекурсоров [3] в сочетании с литографическими методами формирования керамики продемонстрированы в работе [4], в которой изготовили прототипы MEMS-устройств на основе SiCN-керамики с помощью многослойной литографии. В последние годы появляются работы, посвященные изготовлению SiOC-керамики из карбосиланов и силоксанов [5, 6]. В этой связи вполне естественен интерес к формированию стереолитографической 3D-печатью алюмооксидной и алюмо(окси)нитридной керамики с упорядоченной макропористой структурой из полимерных алюмосодержащих прекурсоров. Такая макропористая керамика со сложной проницаемой архитектурой может иметь разнообразное практическое использование, например в качестве биоинертных костных имплантатов [2, 7, 8].
Если кремнийорганические полимерные керамические прекурсоры интенсивно исследуется уже более полувека [3], то в отношении алюмосодержащих прекурсоров керамики известно значительно меньше работ. Для изготовления алюмооксидных материалов часто применяются концентрированные коллоидные растворы алюмоксанов (полимерных соединений, содержащих связи Al–O–Al и являющихся продуктами частичного гидролиза солей алюминия или его алкоксидов [9]). В качестве примера можно привести керамообразующую связку АЛЮМОКС на основе органоалюмоксанов [Al(OR)s${{\left( {{\text{OR'}}} \right)}_{x}}$(OH)pOq]m, где R = СnН2n+1, ${\text{R'}}$ = = C(CH3)=CHC(O)OСnН2n+1, n = 2–4 [10], или алюмоксаны, содержащие лактатные и цитратные анионы, используемые в золь–гель-синтезе алюмоксидного стекла [11]. Для получения алюмонитридных фаз (в основном для AlN, но возможно и для AlON) предложены алазановые соединения вида [R1 > N–Al < R2]n, которые синтезируют нагреванием алюмоиминов R1–N=Al–R2 [12, 13]. Алюмозоли были использованы также для синтеза γ‑AlON [14] и сиалонов (SiAlON) [15].
Следует отметить основную проблему использования предкерамических прекурсоров: большую потерю массы при их пиролизе и связанные с этим изменения объема. Например, для триакрилата алюминия Al(OОС–СН=СН2)3 (с учетом содержания акрилатных мономеров в фотополимеризуемой при 3D-печати смеси) потери заполимеризованной массы при термообработке сформованной модели будут превышать 80%, при этом линейная усадка керамики будет достигать 70%. Эту проблему можно частично решить за счет перехода от Al(OОС–СН=СН2)3 к основному акрилату Al(OH)2(OОС–СН=СН2) с сохранением в составе прекурсора акрилатной группы, способной к полимеризации [16]. Таким образом, среди очевидных требований, которые можно адресовать предкерамическим прекурсорам – 1) минимальная потеря массы при пиролизе, 2) сочетание высокой растворимости в фотомономере с малой вязкостью такого раствора, 3) достаточная оптическая прозрачность такого раствора, 4) наличие в составе прекурсора полимеризуемых групп (акрилатных, аллильных и др.) – наиболее важными выглядят первые два. В этой связи определенный интерес представляют концентрированные истинные растворы или золи на основе хлоридов или основных хлоридов алюминия, содержащие акрилатный мономер (например, акриламид (АА)) и сшивающий агент (например, полиэтиленгликольдиакрилат (ПЭГДА)). Такие прекурсоры могут быть использованы для формирования как алюмооксидной, так и (окси)нитридной керамики в зависимости от условий обжига. Обжиг в окислительной атмосфере приведет к образованию алюмооксидной керамики, в то время как обжиг в атмосфере азота или газообразного аммиака (т.е. в условиях восстановительного азотирования [12, 13]) может дать нитрид и оксинитриды алюминия.
Целью данной работы стала разработка подходов к созданию полимеризуемых прекурсоров корундовой и оксинитридной керамики и их использование в стереолитографическом формировании алюмосодержащей керамики. Исходя из однородности (оптической прозрачности) и легкости фотополимеризации, а также процента потери массы при термолизе отобраны три прекурсора на основе хлоридов алюминия (безводного и гексагидрата), а также основного хлорида алюминия. Охарактеризовано поведение прекурсоров при обжиге в атмосфере аммиака для синтеза оксинитридной керамики и при обжиге на воздухе для изготовления корундовой керамики из гомогенных прекурсоров. Апробирована стереолитографическая 3D-печать корундовой керамики, в т. ч. с использованием разработанных прекурсоров в виде фотополимеризуемых связок, позволяющих повысить долю оксида алюминия в фотосуспензии.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез прекурсора на основе основного хлорида алюминия. В высокий стакан с 5.81 г дистиллированной воды небольшими порциями при постоянном перемешивании добавляли порошок алюминия (0.54 г, СУАЛ-ПМ). Далее по каплям вносили 1.5 г концентрированной соляной кислоты (Сигма Тек, 14261-77); при перемешивании и нагревании до 50°C в течение 6 ч в полученную суспензию добавляли необходимое количество воды для достижения заданной массовой доли алюминия в растворе (9 мас. %). Полученный прозрачный раствор основного хлорида демонстрирует конус Тиндаля, данные динамического светорассеяния (ДСР) указывают на начинающуюся агрегацию первичных частиц золя менее 10 нм в образования с размерами до 1 мкм (рис. 1). Раствор имеет рН 3–4; с учетом доли алюминия в растворе это означает, что его основность (отношение OH/Al) близка к 0.5, т.е. основной хлорид имеет алюмоксановое строение и брутто-состав, близкий к Al2(OH)5Cl·xH2O [9]. При увеличении доли алюминия выше 14 мас. % происходит обратимое гелеобразование, описанное также в [9, 11]. Далее в раствор вносили 1.4 г АА (2L003106) и после полного растворения добавляли 0.14 г ПЭГДА (Sigma-Aldrich, 45508-500ML) и 0.016 г коммерческого фотоинициатора CPS TPO-Li. Полученную смесь оставляли перемешиваться в течение 12 ч, а затем разливали в силиконовые формы (цилиндр диаметром 5.2 мм), после чего проводили обработку раствора УФ-излучением с длиной волны 405 нм в течение 1 мин. Полученные цилиндры вынимали из формы и повторно обрабатывали УФ-излучением в течение 5 мин для окончательного затвердевания. Приготовленные образцы оставляли сушиться в течение 5 сут при комнатной температуре для удаления избыточной воды.
Синтез прекурсора на основе AlCl3·6H2O. 2.43 г гексагидрата хлорида алюминия (“ос. ч.”) вносили небольшими порциями и полностью растворяли в 1.9 г дистиллированной воды. Затем вносили 0.7 г АА (2L003106) и после полного растворения добавили 0.07 г ПЭГДА (Sigma-Aldrich, 45508-500ML) и 0.008 г CPS TPO-Li. Полученную смесь перемешивали в течение 12 ч. Полимеризация и сушка проведены аналогично предыдущему образцу.
Синтез прекурсора на основе AlCl3. 1.33 г синтезированного безводного хлорида алюминия небольшими порциями вносили в 1 мл абсолютизированного этилового спирта и интенсивно перемешивали до окончания остывания полученной смеси. Для получения равномерной суспензии доводили общий объем этилового спирта до 2 мл. В полученную полупрозрачную суспензию желтого цвета добавляли 1.6 г АА (2L003106), после чего последовательно добавляли 0.16 г ПЭГДА (Sigma-Aldrich, 45508-500ML) и 0.017 г коммерческого фотоинициатора Irgacure 819. Итоговую смесь оставляли перемешиваться в течение 12 ч. Полимеризация и сушка проведены аналогично первому образцу.
Стереолитографическая 3D-печать. Для стереолитографической печати был использован 3D-принтер Ember (Autodesk, США) со светодиодным источником с максимумом в спектре при 405 нм. В качестве геометрии модели использовался односторонний гироид. Для определения параметров трехмерной стереолитографической печати были построены зависимости глубины полимеризации Cd от дозы облучения E0.
С использованием уравнения Джейкобса
где Dp – фоточувствительность суспензии, E0 – энергия (интенсивность) УФ-излучения, Eс – критическая энергия полимеризации, были определены фоточувствительность суспензий и их критическая энергия полимеризации.Рентгенофазовый анализ (РФА) проводили на рентгеновском дифрактометре Rigaku D/Max-2500 с вращающимся анодом (Япония). Съемка осуществлялась в режиме на отражение (геометрия Брегга–Брентано) в кварцевых кюветах без усредняющего вращения с использованием CuKср-излучения. Качественный анализ полученных рентгенограмм проводили с использованием базы данных ICDD PDF-2.
Распределение частиц по размерам определяли методом ДСР на приборе Zetasizer Nano ZS в диапазоне 0.3 нм–10 мкм, а также на приборе лазерной дифракции Fritsch Analysette-22 в диапазоне 0.2–100 мкм.
Растровая электронная микроскопия (РЭМ) и рентгеноспектральный микроанализ (РСМА) проведены на растровых электронных микроскопах с автоэмиссионным источником LEO SUPRA 50VP. Ускоряющее напряжение электронной пушки составляло 2–21 кВ. Изображения получали во вторичных электронах при увеличениях до 200 000×. Для оценки однородности распределения фаз и элементного состава образцов проводили РСМА при помощи электронного микроскопа Leo SUPRA 50VP, оснащенного системой энергодисперсионного микроанализа INCA Energy 300 (Oxford Instruments, Великобритания) при ускоряющих напряжениях 15–21 кВ.
Дифференциальный термический (ДТА) и термогравиметрический (ТГ) анализ образцов проводили с использованием синхронного термоанализатора с вертикальной загрузкой образцов STA 409 PC Luxx (Netzsch, Германия). Измерения проводили в атмосфере воздуха или аммиака в интервале температур от комнатной до 1300°С со скоростью нагрева 10°С/мин. Навески образцов составляли до 100 мг.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Исследование прекурсоров для получения нитридной и оксинитридной керамики. Предварительно была изучена возможность использования прекурсоров, содержащих концентрированные растворы AlX3 (где Х – изопропилатная, формиатная или акрилатная группы, хлор; или продукты гидролиза этих соединений) в воде или абсолютированном спирте. В качестве азотосодержащего компонента использовался или только АА (который вместе с ПЭГДА присутствовал в составе любого образца), или в состав прекурсора дополнительно вводили аллиламин либо этилендиамин. Исходя из соображений потери массы при термообработке (зависит от молекулярной массы группы Х и концентрации AlХ3 в растворе); оптической прозрачности прекурсора (визуальная оценка); легкости фотополимеризации (время гелеобразования не более 5 мин) для дальнейшей работы были отобраны три следующих образца с АА в качестве азотосодержащего компонента: на основе водного коллоидного раствора основного хлорида алюминия (обозначение Al(OH)2Cl), на основе водного раствора гексагидрата хлорида алюминия (обозначение AlCl3_wat), на основе спиртового раствора безводного AlCl3 (обозначение AlCl3_EtOH); процесс их приготовления описан выше.
Термодинамический анализ. Для понимания возможностей синтеза нитридной и оксинитридной керамики с использованием предложенных прекурсоров в атмосфере азота или аммиака были простроены диаграммы Эллингхама $\left( {{{\Delta }_{r}}G_{T}^{^\circ } = {{\Delta }_{r}}H_{{298}}^{^\circ } - T{{\Delta }_{r}}S_{{298}}^{^\circ }} \right)$ для целого ряда реакций, представленных в табл. 1 и на рис. 2. Для AlNкр взяты рекомендуемые NIST [17] значения ${{\Delta }_{f}}H_{{298}}^{^\circ }$ = = –317.98 кДж/моль, $S_{{298}}^{^\circ }$ = 20.14 Дж/(моль К). Для шпинели γ-AlON (состава Al23O27N5) использованы значения ΔfH° = –16339 кДж/моль, S° = = 3045 Дж/(моль К) [18, 19], которые близки данным Кауфмана [20]. Реакция 2AlCl3 кр + 3Н2Ог = = Al2O3 кр + 6HClг (${{\Delta }_{r}}H_{{298}}^{^\circ }$ = –93 кДж, ${{\Delta }_{r}}S_{{298}}^{^\circ }$ = = 387 Дж/К) термодинамически вероятна при любой температуре; в реальности протекает уже при температуре выше 170°C [21]. Следовательно, в случае водосодержащих прекурсоров AlCl3_wat и Al(OH)2Cl восстановлению подвергается оксид алюминия. Применительно к задачам данной работы можно сделать следующие выводы.
Таблица 1.
Возможные химические реакции, протекающие при восстановительном обжиге прекурсоров
| № | Химическая реакция |
|---|---|
| (1) | Al2O3 кр + 3Cграфит + 2NH3 г = 2AlNкр + 3COг + 3H2 г |
| (2) | Al2O3 кр + 4.5Cграфит + 2NH3 г = 2AlNкр + 3COг + 1.5CH4 г |
| (3) | Al2O3 кр + 2NH3 г = 2AlNкр + 3H2Oг |
| (4) | Al2O3 кр + 3Cграфит + N2 г = 2AlNкр + 3COг |
| (5) | AlCl3 кр + NH3 г = AlNкр + 3HClг |
| (6) | 11.5 Al2O3 кр + 7.5Cграфит + 2.5N2 г = Al23O27N5 кр + 7.5COг |
| (7) | 11.5 Al2O3 кр + 7.5Cграфит + 2.5NH3 г = Al23O27N5 кр + 7.5COг + 3.75Н2 г |
| (8) | 23AlCl3 кр + 27Н2Ог + 5NH3 г = Al23O27N5 кр + 69HClг |
1. Более отрицательные энергии Гиббса реакций с образованием γ-AlON по сравнению с AlN говорят о том, что γ-AlON может рассматриваться как полупродукт при образовании нитрида алюминия. В безводном прекурсоре (AlCl3_EtOH), где в качестве алюмосодержащего компонента выступает безводный хлорид алюминия, равновесие в реакциях образования нитрида и оксинитрида достигается при температурах более низких, чем в случае использования оксида алюминия. Следует, однако, иметь в виду, что существует консенсус относительно термодинамической неустойчивости γ-AlON ниже 1600–1700°C [18, 19, 22] (согласно [18], это зависит и от p(N2)/p(O2)).
2. Использование аммиака в качестве атмосферы обжига оправдано его хорошими восстановительными свойствами (в т. ч. за счет энтропийного фактора соответствующих реакций); его способностью удалять излишки углерода (в противовес обжигу в атмосфере азота), поскольку для реакции Cграфит + 4/3NH3 г = CH4 г + 2/3N2 г ${{\Delta }_{r}}H_{{298}}^{^\circ }$ = –13.27 кДж (<0), ${{\Delta }_{r}}S_{{298}}^{^\circ }$ = 56.92 Дж/К (>0), т.е. ${{\Delta }_{r}}G_{T}^{^\circ }$ < 0 для любых Т. Следует подчеркнуть, что полное удаление углеродного пиролизованного остатка не требуется, т.к. углерод расходуется в реакциях типа (1), (2), (4), (6), (7) (табл. 1). С точки зрения термодинамики, для образования нитридной фазы в реакциях типа (1) и (2) (табл. 1, рис. 2) температура обжига в аммиаке должна быть не ниже 1100°C.
Синхронный термический анализ (СТА) прекурсоров в атмосфере NH3. Наиболее сильно отличались по термическому поведению прекурсоры Al(OH)2Cl и AlCl3_EtOH. В диапазоне до 1300°C разложение прекурсоров протекает в три заметных стадии.
1-я стадия – до 300°C для Al(OH)2Cl и до 200°C для AlCl3_EtOH – связана с удалением хемосорбированной воды или спирта. Меньше всего массы теряется на этой стадии у прекурсора Al(OH)2Cl (до 15%) и более всего у прекурсора AlCl3_wat) (до 50%).
2-я стадия – до 500°C, это в основном пиролиз полимера и пирогидролиз с удалением HCl/NH4Cl. На данной стадии теряется 40–45% массы, больше для прекурсора AlCl3_wat, меньше – для Al(OH)2Cl.
3-я стадия – до 1100°С, связана с восстановлением оксида алюминия и нитридизацией. На этой стадии инвариантно теряется до 15% массы прекурсора.
Следует обратить внимание на увеличение содержания водорода в отходящих газах после 600°C за счет заметного разложения аммиака и его уменьшение (равно как и основного потока аммиака) за счет вступления в реакции восстановления/нитридизации после 850°C с одновременным ростом СО (см. реакции (1), (2), а также термодинамический анализ). Кривые СТА для прекурсора Al(OH)2Cl представлены на рис. 3.
Рис. 3.
Результаты СТА для прекурсора Al(OH)2Cl в токе аммиака: кривые ТГ/ДСК (а), кривая ТГ и значения ионных токов при параллельном масс-спектрометрическом исследовании отходящих газов (цифрами указаны массовые числа: М = 17 (аммиак), М = 14 (азот), М = 2 (водород), М = 28 (СО)) (б).

Обжиг сформованных прекурсоров в атмосфере NH3. Были проведены три отжига указанных трех прекурсоров при температурах 1000°C (1 ч), 1100°C (1 ч) и 1300°C (после термоанализа). Образцы после отжига при 1000°C имели серо-черный цвет, что говорит о большом количестве оставшегося углерода. Несмотря на значительную усадку (табл. 2), наилучшую сохранность формы после обжигов показали образцы прекурсора Al(OH)2Cl. Мы связываем этот факт с золь–гель-переходом [9, 11], который протекает при сушке (концентрировании) алюмоксанового золя, составляющего данный прекурсор. По сравнению с ним образец AlCl3_wat с наименьшей усадкой очень пористый, ломкий; не все образцы этого прекурсора сохранили свою форму после обжига. Образцы после обжига при 1100°C более светлые, с чуть заметным серым или желтым оттенком (Al(OH)2Cl); образцы после обжига при 1300°C практически белые, что подтверждает декарбонизацию в атмосфере аммиака с повышением температуры.
Таблица 2.
Усадка (±2%) и состав образцов прекурсоров после сушки и обжига
| Прекурсор | AlCl3_wat | Al(OH)2Cl | AlCl3_EtOH |
|---|---|---|---|
| Усадка после сушки, % | 14 | 29 | 10 |
| Усадка после обжига при 1100°С, % | 11 | 49 | 38 |
| Общая усадка, % | 23 | 64 | 44 |
РСМА, РЭМ и РФА обожженных образцов прекурсоров. РСМА образцов обожженных прекурсоров (табл. 3) указывает на наибольшее содержание азота в образце AlCl3_EtOH, где, как предполагается, содержится льюисов аддукт хлорида алюминия с акриламидом, в котором азотсодержащая молекула удерживается в координационной сфере хлорида более прочно по сравнению с другими прекурсорами. Увеличение содержания азота с увеличением температуры отжига не вполне очевидно, по крайней мере для прекурсоров AlCl3_wat и Al(OH)2Cl. Для прекурсора AlCl3_EtOH заметно нарастание доли азота (по N/Al и O/N) с повышением температуры; причем этот прекурсор содержит больше остаточного углерода, чем остальные, что говорит о принципиальной возможности протекания более глубокой нитридизации при повышении температуры обжига. Максимальное содержание азота в этом обожженном прекурсоре не превышает 9 ат. %. Большое содержание кислорода в используемых для фотополимеризации акрилатных мономерах приводит к тому, что при высоких температурах образцы содержат определенное количество оксида алюминия, для перевода которого в (окси)нитрид требуется карбонитридизация в среде аммиака или азота при более высоких температурах. С учетом неизбежности проведения этой стадии прекурсор Al(OH)2Cl на основе золя основного хлорида алюминия выглядит приемлемо с точки зрения сохранности формы изделий после обжига.
Таблица 3.
Состав обожженных образцов по данным РСМА
| Температура, °С |
C/Al | N/Al | O/N | C/Al | N/Al | O/N | C/Al | N/Al | O/N |
|---|---|---|---|---|---|---|---|---|---|
| AlCl3_wat | Al(OH)2Cl | AlCl3_EtOH | |||||||
| 1000 | 0.3 | 0.1 | 25.7 | 0.2 | 0.2 | 25.9 | 0.3 | 0.1 | 23.5 |
| 1100 | 0.3 | 0.1 | 27.0 | 0.2 | 0.1 | 38.5 | 0.5 | 0.2 | 17.9 |
| 1300 | 0.3 | 0.1 | 26.1 | 0.2 | 0.1 | 30.8 | 0.3 | 0.3 | 10.8 |
Микроструктура обожженных образцов прекурсоров Al(OH)2Cl и AlCl3_EtOH представлена на рис. 4а. Образец Al(OH)2Cl имеет небольшое количество трещин, что связано с его большой усадкой; на остальных участках он выглядит достаточно плотным, образованным субмикронными частицами. Образец AlCl3_EtOH содержит большое количество пор с размерами 1–2 мкм и выглядит более аморфным по сравнению с предыдущим прекурсором. По данным РФА, образцы прекурсоров, обожженных при 1000°C, представляют собой нанокристаллические тела с очень широкими налагающимися пиками (рис. 4б). Точная фазовая идентификация в данном случае вряд ли возможна, однако центры широких перекрывающихся линий можно соотнести как с корундом, так и с (окси)нитридами. Можно заключить, что прекурсоры представляют собой плохо закристаллизованные оксинитридные фазы с малым содержанием азота. С повышением температуры начинается кристаллизация фаз (по-видимому, с расслоением рентгеноаморфной оксинитридной фазы); становится заметна фаза корунда, а при 1300°С, по крайней мере для прекурсора AlCl3_EtOH, становятся заметными и линии оксинитрида.
Рис. 4.
Микроструктура (а–г) и дифрактограммы (д, е) обожженных в атмосфере аммиака заполимеризованных прекурсоров.

Таким образом, в процессе обжига прекурсоров при более высоких температурах в атмосфере аммиака (или азота) потенциально могут образоваться фазы нитрида и оксинитридов алюминия, что не противоречит известным данным (например, [12, 18, 19]). Обжиг на воздухе исследованных прекурсоров позволяет сформировать корундовую керамику, в т. ч. сложной формы, с использованием приемов 3D-печати. С учетом сохранности формы образца наибольший интерес представляет прекурсор Al(OH)2Cl, на котором и был сделан акцент во второй части данной работы.
Отработка режимов стереолитографической печати корундовой керамики из прекурсоров
Исследование фоточувствительности суспензий для стереолитографической 3D-печати. Среда на основе золя основного хлорида алюминия демонстрирует высокие значения фоточувствительности и низкую критическую энергию полимеризации (табл. 4), т.к. является прозрачным раствором с характерным размером частиц золя на два порядка меньше длины волны излучения, которое используется для полимеризации. Такая высокая фоточувствительность не позволяет напрямую использовать данную суспензию для стереолитографической печати, в которой характерные толщины полимеризуемого слоя составляют от 50 до 200 мкм. Для уменьшения фоточувствительности был использован водорастворимый краситель Е104 (хинолиновый желтый), его использование позволило снизить фоточувствительность до 377 мкм. При использовании порошка оксида алюминия в качестве наполнителя (высокочистый порошок корунда марки TCPLSDBM, Baikowski®, Франция) критическая энергия полимеризации возрастает до 40.7 мДж/см2, что связано с рассеянием света на частицах Al2O3 со средним размером 400 нм; это сопоставимо с длиной волны источника, который используется в примененном стереолитографическом принтере Ember.
Таблица 4.
Параметры печати для исследуемых суспензий
| Суспензия | Ес, мДж/см2 | Dp, мкм |
|---|---|---|
| Золь Al(OH)2Cl | 11.5 | 2476 ± 135 |
| Золь Al(OH)2Cl + E104 | 29.4 | 377 ± 17 |
| Золь Al(OH)2Cl + Al2O3 + E104 | 40.7 | 291 ± 44 |
На основе данных о фоточувствительности суспензий (табл. 4, рис. 5) было выбрано итоговое значение толщины слоя для полимеризации в 200 мкм. В результате стереолитографической печати были получены модели с заданной трехмерной архитектурой типа гироид с размером пор 1 мм и долей пор 70% (рис. 6а, 6б). На рис. 6а представлены предкерамические композиты, которые были получены из суспензии на основе золя основного хлорида алюминия и суспензии на основе золя, дополнительно наполненной порошком оксида алюминия (20 об. %). На рис. 6б представлены предкерамические композиты на основе золя до и после температурной обработки при 1200 и 1700°C на воздухе, которая проводилась по специально разработанному термическому режиму для плавного удаления полимерной составляющей.
Рис. 5.
Зависимости глубины полимеризации от дозы облучения для суспензий на основе прекурсора Al(OH)2Cl (1), прекурсора Al(OH)2Cl с добавлением красителя E104 (2), прекурсора Al(OH)2Cl с добавлением 20 об. % оксида алюминия и красителя E104 (3).

Рис. 6.
Композиты на основе прекурсора Al(OH)2Cl (слева) и прекурсора Al(OH)2Cl, наполненного частицами оксида алюминия (справа), изготовленные стереолитографической 3D-печатью (а); композит на основе прекурсора Al(OH)2Cl после 3D-печати (слева), керамика после термической обработки на воздухе при 1200°C (по центру) и 1700°C (справа) (б); результаты ТГ/ДСК-анализа прекурсора Al(OH)2Cl на воздухе (в); дифрактограмма корундовой керамики, полученной из прекурсора Al(OH)2Cl обжигом при 1700°C в токе воздуха (штрих-диаграмма соответствует карточке № 10-173 ICDD PDF-2) (г); микроструктрура корундовой керамики, полученной из прекурсора Al(OH)2Cl, наполненного частицами оксида алюминия (обжиг на воздухе при 1700°C) (д).
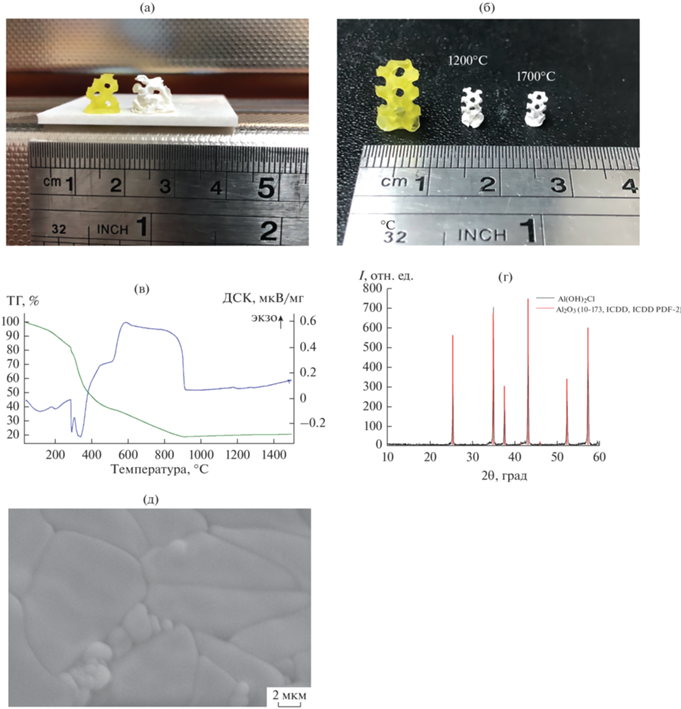
Обжиг напечатанных моделей. В соответствии с данными ТГ/ДСК/масс-спектрометрии (рис. 6в) отпечатанные модели нагревали на воздухе со скоростью 5°C/мин до 1200°C с изотермическими выдержками в интервалах интенсивной потери массы (300 и 700°C) в течение 1 ч. Спекание осуществлялось при 1200 и 1700°C в течение 3 ч. По данным РФА, обожженные после 1500°C образцы представляют собой хорошо закристаллизованный корунд (рис. 6г). Спеченные при 1700°C образцы достаточно прочные, в то время как обожженные при 1200°C требуют осторожности при манипуляции с ними. Микроструктура керамики, спеченной при 1700°C, из суспензии прекурсора с порошком корунда имеет бимодальный характер с зернами 1–2 и 5–7 мкм (рис. 6д). Это говорит о необходимости оптимизации условий спекания, поскольку частицы оксида алюминия, введенные первоначально для наполнения прекурсора и возникшие при термолизе предкерамической алюмоксановой связки, могут иметь различную кинетику роста. Вместе с тем бимодальная микроструктура может представлять определенный интерес в плане улучшения трещиностойкости керамики [23].
ЗАКЛЮЧЕНИЕ
В качестве гомогенных предкерамических прекурсоров для изготовления алюмооксидной и оксинитридной керамики предложены растворы солей AlCl3·6H2O и AlCl3 (водный и спиртовый раствор соответственно), а также коллоидный раствор алюмоксанового гидроксохлорида Al(OH)3–хClх (х ~ 0.5), содержащие растворимые мономер (акриламид, одновременно выполняющий функцию азотсодержащего вещества) и сшивающий агент (диакрилат полиэтиленгликоля). Несмотря на значительную потерю массы при термообработке (до 80%), прекурсор на основе Al(OH)3–хClх сохраняет исходную форму и обладает перспективой для использования в качестве фотополимеризуемой связки при наполнении его дисперсным порошком оксида алюминия.
Термолиз прекурсоров в атмосфере аммиака протекает в три стадии, причем сохранность формы изделия определяет потеря массы на первой стадии – до 300°C (меньше всего массы теряется на этой стадии у прекурсора Al(OH)3–хClх и более всего у прекурсора на основе AlCl3·6H2O); в то время как стадия, связанная с восстановлением оксида алюминия и нитридизацией, протекает выше 800°C. Наибольшее количество азота содержит нитридизованный прекурсор на основе спиртового раствора AlCl3 вследствие более сильной связи Al–N в аддукте.
На гомогенной алюмоксановой связке Al(OH)3–хClх методом стереолитографической печати сформована корундовая керамика из суспензии, содержащей 20 об. % порошкового корунда и до 5% оксида алюминия, содержащегося в алюмоксановой связке. Обжиг такого изделия на воздухе при температурах выше 1200°C позволяет сформировать корундовую керамику с бимодальной микроструктурой.
Список литературы
Zocca A., Colombo P., Gomes C.M., Günster J. Additive Manufacturing of Ceramics: Issues, Potentialities, and Opportunities // J. Am. Ceram. Soc. 2015. V. 98. № 7. P. 1983–2001. https://doi.org/10.1111/jace.13700
Ievlev V.M., Putlyaev V.I., Safronova T.V., Evdokimov P.V. Additive Technologies for Making Highly Permeable Inorganic Materials with Tailored Morphological Architectonics for Medicine // Inorg. Mater. 2015. V. 51. № 13. P. 1295–1313. https://doi.org/10.1134/S0020168515130038
Colombo P., Mera G., Riedel R., Sorarù G.D. Polymer-Derived Ceramics: 40 Years of Research and Innovation in Advanced Ceramics // J. Am. Ceram. Soc. 2010. V. 93. № 7. P. 1805–1837. https://doi.org/10.1111/j.1551-2916.2010.03876.x
Liew L.A., Liu Y., Luo R., Cross T., An L., Bright V.M., Dunn M.L., Daily J.W., Raj R. Fabrication of SiCN MEMS by Photopolymerization of Preceramic Polymer // Sens. Actuators, A. 2002. V. 95. № 2–3. P. 120–134. https://doi.org/10.1109/MEMSYS.2002.984340
Heimann R.B. Silicon Nitride, a Close to Ideal Ceramic Material for Medical Application // Ceramics. 2021. V. 4. P. 208–223. https://doi.org/10.3390/ceramics4020016
Rey C., Combes C., Drouet C. Bioinert Ceramics: State-of-the-Art // Key Eng. Mater. 2017. V. 758. P. 3–13. doi:10.4028/www.scientific.net/KEM.758.3
Eckel Z.C., Zhou C., Martin J.H., Jacobsen A.J., Carter W.B., Schaedler T.A. Additive Manufacturing Of Polymer-Derived Ceramics // Science. 2016. V. 351. № 6268. P. 58–62. https://doi.org/10.1126/science.aad2688
De Hazan Y., Penner D. SiC and SiOC Ceramic Articles Produced by Stereolithography of Acrylate Modified Polycarbosilane Systems // J. Eur. Ceram. Soc. 2017. V. 37. № 16. P. 5205–5212. https://doi.org/10.1016/j.jeurceramsoc.2017.03.021
Новаков И.А., Радченко Ф.С. Наноразмерные алюмоксановые частицы-прекурсоры органо-неорганических гибридных полимерных композиций // Изв. ВолгГТУ. 2013. № 4 (107). С. 5–20.
Стороженко П.А., Щербакова Г.И., Цирлин А.М., Муркина А.С., Варфоломеев М.С., Кузнецова М.Г., Полякова М.В., Трохаченкова О.П. Органоалкоксиалюмосиликаты и бескремнеземное связующее на их основе // Неорган. материалы. 2007. Т. 43. № 3. С. 373–382. https://doi.org/10.1134/S0002337X19100130
He J., Avnir D., Zhang L. Sol–Gel Derived Alumina Glass: Mechanistic Study of Its Structural Evolution // Acta Mater. 2019. V. 174 P. 418–426. https://doi.org/10.1016/j.actamat.2019.05.062
Baixia L., Yinkui L., Yi. L. Preparation of Aluminium Nitride from Organometallic/Polymeric Precursors // J. Mater. Chem. 1993. V. 3. № 2. P. 117–127. https://doi.org/10.1039/JM9930300117
Jensen J.A. Organoaluminum Precursor Polymers for Aluminum Nitride Ceramics // Inorganic and Organometallic Polymers II. ACS Symposium Series, Ch. 32. Washington, DC: Am. Chem. Soc., 1994. P. 428–439. https://doi.org/10.1021/bk-1994-0572.ch032
Naderi-beni B., Alizadeh A. Preparation of Single Phase AlON Powders Aided by the Nitridation of Sol-Gel-Derived Nanoparticles // Ceram. Int. 2019. V. 45. P. 7537–7543. https://doi.org/10.1016/j.ceramint.2019.01.047
Ивичева С.Н., Овсянников Н.А., Лысенков А.С., Климашин А.А., Каргин Ю.Ф. Синтез оксонитридоалюмосиликатов золь-гель методом // Журн. неорган. химии. 2020. Т. 65. № 12. С. 1614–1625. https://doi.org/10.1134/S0036023620120050
Орлов Н.К., Евдокимов П.В., Милькин П.А., Тихонов А.А., Тихонова С.А., Климашина Е.С., Зуев Д.М., Капитанова О.О., Путляев В.И. Синтез прекерамического прекурсора на основе органических солей алюминия для стереолитографической 3D-печати корундовой керамики // Перспективные материалы. 2021. № 4. С. 67–80. https://doi.org/10.30791/1028-978X-2021-4-67-80
Chase M.W. NIST–JANAF Thermochemical Tables, Fourth Edition // J. Phys. Chem. Ref. Data. Monograph 9. 1998. P. 1–1951.
Willems H.X., Hendrix M.M.R.M., Metselaar R., de With G. Thermodynamics of Alon I: Stability at Lower Temperatures // J. Eur. Ceram. Soc. 1992. V. 10. P. 327–337. https://doi.org/10.1016/0955-2219(92)90088-U
Corbin N.D. Aluminum Oxynitride Spinel: a Review // J. Eur. Ceram. Soc. 1989. V. 5. P. 143–154. https://doi.org/10.1016/0955-2219(89)90030-7
Kaufman L. Calculation of Quasibinary and Quasiternary Oxynitride Systems – III // Calphad. 1979. V. 3. P. 275–291.
Валеев Д.В., Лайнер Ю.А., Самохин А.В., Синайский М.А., Михайлова А.Б., Куцев С.В., Гольдберг М.А. Физико-химические исследования процесса термогидролиза хлорида алюминия // Перспективные материалы. 2016. № 1. С. 64–73. https://doi.org/10.1134/S2075113316050269
Tabary P., Servant C. Thermodynamic Reassessment of the AlN-A12O3 System // Calphad. 1999. V. 22. № 2. P. 179–201. https://doi.org/10.1016/S0364-5916(98)00023-6
Becher P. Microstructural Design of Toughened Ceramics // J. Am. Ceram. Soc. 1991. V. 74. № 2. P. 255–269. https://doi.org/10.1111/j.1151-2916.1991.tb06872.x
Дополнительные материалы отсутствуют.
Инструменты
Неорганические материалы




