БИОХИМИЯ, 2023, том 88, вып. 11, с. 2206 - 2220
УДК 577.27;576.5;602.9
ИММУННЫЕ ПРИВИЛЕГИИ КАК РЕЗУЛЬТАТ ВЗАИМНОЙ
РЕГУЛЯЦИИ ИММУННОЙ И СТВОЛОВОЙ СИСТЕМ
Обзор
© 2023 Д.В. Карпенко
ФГБУ «Национальный медицинский исследовательский центр гематологии» Минздрава России,
лаборатория эпигенетической регуляции кроветворения,
125167 Москва, Россия; электронная почта: d_@list.ru
Поступила в редакцию 19.06.2023
После доработки 09.10.2023
Принята к публикации 10.10.2023
Иммунные привилегии раковых стволовых клеток - хорошо известная и широко изучаемая про-
блема, поскольку наличие таких клеток в опухолях ассоциируется с рефрактерностью, рециди-
вированием и метастазированием. Накапливающиеся данные также свидетельствуют о наличии
иммунных привилегий у непатологических стволовых клеток в дополнение к другим механизмам
их защиты от повреждающих факторов. Такое сходство между патологическими и нормальными
стволовыми клетками ставит вопрос о том, почему стволовые клетки обладают таким потенциаль-
но опасным свойством. Регуляции жизненно важных процессов контроля аутоиммунитета и реге-
нерации при взаимодействии между иммунными клетками, стволовыми клетками и их микроокру-
жением рассматриваются в обзоре как определяющие для формирования иммунных привилегий
стволовых клеток. Отмечается глубокая взаимная интеграция в регуляции стволовых и иммунных
клеток. Исходя из многообразия и сложности взаиморегуляции стволовых клеток, их микроокру-
жения и иммунной системы, я предлагаю использовать термин «стволовая система».
КЛЮЧЕВЫЕ СЛОВА: аутоиммунитет, регенерация, стволовая клетка, раковая стволовая клетка, стволо-
вая система, иммунные привилегии, нестин.
DOI: 10.31857/S0320972523110131, EDN: MMKBQY
ВВЕДЕНИЕ
другие ткани. Другая работа [4] показала, что
подсадка фрагмента аутологичной селезёнки в
Развитие хирургии и, в частности, техник
головной мозг вместе с опухолевыми клетками
по трансплантациям привело к необходимо-
приводит к гибели последних. Также было по-
сти обучаться на моделях животных. Это при-
казано, что предварительная иммунизация ре-
вело естественным образом к обнаружению
ципиента приводит к отторжению трансплан-
реакций отторжения аллогенных трансплан-
тата кожи в мозге мыши [5]. Трансплантации
татов и обнаружению иммунных привилегий.
до сих пор являются важным звеном, позво-
Так, первые упоминания по иммунопривиле-
ляющим in vivo изучение деталей иммунных
гированности относятся к концу XIX века [1, 2],
привилегий во взаимодействии сложных си-
когда офтальмолог заметил, что трансплантат
стем организма, дополняющим методы совре-
кожи мыши, посаженный в переднюю каме-
менной молекулярной биологии и биоинфор-
ру глаза собаки, демонстрировал более дли-
матики.
тельное выживание. В своей работе Shirai [3]
Изначально основной гипотезой, объясня-
показал приживление раковых клеток, под-
ющей формирование иммунных привилегий
саженных от стороннего донора в головной
в органах, являлось существование области,
мозг, в противовес отторжению при подсадке в изолированной от клеток иммунной системы.
Принятые сокращения: CSC - раковые стволовые клетки; GFP - зеленый флуоресцентный белок; HSC - стволо-
вые кроветворные клетки; MC - мезенхимные клетки; MHC - главный комплекс гистосовместимости; MSC - мезен-
химные стволовые клетки; MUSE - мультилинейно-дифференцирующиеся стрессоустойчивые клетки; T-reg - регу-
ляторные Т-лимфоциты.
2206
ИММУННЫЕ ПРИВИЛЕГИИ В СТВОЛОВОЙ СИСТЕМЕ
2207
Однако показанная миграция периферических
но участие в формировании иммунных приви-
иммунных клеток через целостный гемато-
легий при онкологических заболеваниях, тре-
энцефалический барьер и активная регуля-
бует отдельного рассмотрения.
ция макрофагов и лимфоцитов нейронами
Накопленные экспериментальные данные
и глией [6] заставила пересмотреть взгляд на
позволяют выделить широкий спектр как ме-
иммунопривилегированность как на свойство
ханизмов иммунных привилегий, так и обла-
изолированной от иммунной системы области
стей организма с иммунными привилегиями,
органа. Более того, территория мозга может
не ограничивающихся барьерными органами.
быть выделена как особая иммунная терри-
Сила иммунных привилегий при этом явля-
тория [7]. Также широко известно, что нару-
ется не абсолютным понятием и может в зна-
шение целостности одного глаза может при-
чительной степени варьироваться и находится
вести к возникновению иммунной реакции и
в зависимости от многих факторов [29, 30].
атаке на контралатеральный глаз [8]. Помимо
В зависимости от силы иммунных привилегий
барьерных механизмов, особое внимание уде-
могут выделяться промежуточные термины.
ляется микроокружению внутри глаза, а также
Например, способность иммунного усколь-
участию иммунных клеток и, в частности, ре-
зания (immune evasive) отражает способность
гуляторных Т-лимфоцитов (T-reg) в качестве
временно избегать иммунного ответа, что
ключевых факторов формирования иммуно-
выражается в относительно более длительной
привилегированной территории глаза [9, 10].
выживаемости аллогенного трансплантата, но
Согласно современным данным, в формиро-
неспособности избежать воздействия иммуни-
вании иммунных привилегий глаза участвуют
тета полностью [31].
субпопуляции CD8 и CD4 T-reg как в передней
камере самого глаза, так и в селезёнке [10]. Для
плаценты и плода одна из теорий их иммуно-
ИММУННЫЕ ПРИВИЛЕГИИ
привилегированности также ассоциируется со
СТВОЛОВЫХ КЛЕТОК
слоем регуляторных T-клеток, экспрессирую-
щих факторы HO-1, LIF, TGF-β и IL-10 [11].
Более ранние исследования демонстрируют
Иммуногенность аутологичной спермы, по-
ускользание стволовых клеток от цитотокси-
казанная на свинье [12], также означает, что
ческого действия иммунных клеток для крове-
семенники являются иммунопривилегирован-
творных стволовых клеток [32], эмбриональных
ными. К механизмам иммунной привилегиро-
стволовых клеток [33], а далее - для мезенхим-
ванности семенников относят как клеточные
ных [34] и нейральных стволовых клеток [35].
барьеры, выстроенные клетками Сертоли [13],
Работы показывают, что снижение экспрессии
так и механизмы цитокиновых регуляций,
молекул главного комплекса гистосовмести-
супрессирующих иммунную реакцию [14, 15].
мости (MHC) снимает надзор от цитотоксиче-
Меланоциты способны мигрировать в волося-
ских (CD8+) Т-лимфоцитов, а также, что есте-
ные фолликулы, где они не подвергаются уни-
ственные киллеры (NK) не атакуют стволовые
чтожению иммунной системой при гетероти-
клетки независимо от экспрессии MHC.
пической трансплантации [16]. Это позволяет
Недавняя работа Agudo et al. [36] демон-
отнести волосяные фолликулы к иммунопри-
стрирует иммунную привилегированность как
вилегированным областям организма [16, 17].
собственное свойство рассмотренных в ра-
Механизмы иммунной привилегированности
боте стволовых клеток. В работе были ис-
обнаруживают также в суставных хрящах [18-20].
пользованы трансгенные мыши, экспресси-
Отдельный интерес представляют случаи
рующие зеленый флуоресцентный белок (GFP)
использования механизмов иммунной приви-
в LGR5+ стволовых клетках, и CD8+ T-клетки
легии опухолями [21-24]. Иммуносупрессив-
с Т-клеточным рецептором, аффинным к пеп-
ное микроокружение рака может значительно
тидам GFP, в составе комплекса MHC I, т.е.
варьироваться, используя широкий спектр ре-
уничтожающие GFP-продуцирующие клетки
гуляции, включающий экспрессию сигналь-
in vivo. Авторы проделали тщательную работу
ных цитокинов, метаболическое изменение
и показали, что можно выделить субпопу-
микроокружения, иммунные контрольные точ-
ляции стволовых клеток, не подверженных
ки на раковых клетках и вовлечение иммун-
иммунному надзору в волосяных фоллику-
ных клеток, поляризованных в противовоспа-
лах и мышцах, но не в кишечнике, яичниках
лительные [23, 25-28]. При этом изученность
или молочной железе. Состояние покоя было
механизмов и количество литературных дан-
выделено как определяющее свойство суб-
ных по ним сильно варьируется, полный обзор
популяций стволовых клеток, ускользающих
механизмов, для которых продемонстрирова-
от иммунного надзора. В покоящихся стволо-
БИОХИМИЯ том 88 вып. 11 2023
2208
КАРПЕНКО
вых клетках снижена экспрессия MHC I и
типа клетки с иммунными привилегиями [48].
β2-микроглобулина (B2m). Также было пока-
В нашей недавней работе мы показали иммун-
зано значительное снижение экспрессии ре-
ные привилегии MSC [49]. Мы использовали
цепторов и транскрипционных факторов Irf3,
модель очагов эктопического кроветворения,
Irf5, Stat1 и Stat3, отвечающих на воспаление.
взяв в качестве донора костного мозга транс-
Авторы показали, что данная субпопуляция
генных мышей Nestin-GFP, экспрессирующих
стволовых клеток не активирует эффектор-
GFP в стволовых клетках под промоторной ак-
ные Т-клетки и не подвергается воздействию
тивностью нестина, и сажая трансплантат под
иммунной системы, однако при стимулах, ак-
капсулу почки изогенных мышей дикого типа
тивирующих пролиферацию покоящихся ство-
с полной нескомпрометированной иммуной
ловых клеток, эти свойства утрачиваются. От-
системой. Иммунные привилегии также отме-
сутствие или значительное снижение MHC I
чаются для мультилинейно-дифференцирую-
на поверхности клеток должно приводить к
щихся стрессоустойчивых клеток (MUSE), вы-
активации NK и уничтожению ими таких кле-
деляемых как SSEA-3+ субпопуляция MC [50].
ток, чего не наблюдалось в описываемой рабо-
Было показано выживание в течение несколь-
те. Это подразумевает существование и иных
ких недель аллогенных и ксеногенных MUSE,
механизмов защиты покоящихся стволовых
введённых внутривенно кроликам без иммун-
клеток от иммунитета.
ной супрессии [51]. Несмотря на различия в
Исходя из приведённых результатов [36],
подходах к фенотипированию субпопуляций,
особый интерес представляют длительно-репо-
сходство функциональных характеристик
пулирующие стволовые кроветворные клетки
SSEA-3+ MUSE и NES-GFP+ MSC [40, 49, 50]
(HSC), которые редко делятся и в основном
даёт основания предпологать, что они пред-
пребывают в покоящемся состоянии [37]. Им-
ставляют одну общую субпопуляцию. Согласно
муногенность общей массы клеток аллоген-
литературным данным, MUSE экспрессируют
ного костного мозга не вызывает сомнений [31,
нестин [52]. Ранее, основываясь на наших ре-
38], однако это не исключает возможности при-
зультатах и литературных данных, мы указы-
сутствия минорных клеточных популяций, об-
вали на связь между экспрессией нестина и по-
ладающих иммунопривилегированностью. Так,
пуляцией иммунопривилегированных клеток.
в работе на мышах показано, что нишевые
Такие нестин-экспрессирующие стволовые
CD150high T-reg участвуют в формировании им-
клетки обнаруживаются в различных частях
мунных привилегий аллогенных HSC [39]. Од-
взрослого организма и органах различного эм-
новременно с этим авторы показывают участие
брионального происхождения: как на примере
нишевых T-reg в защите HSC от оксидативно-
изученных нами иммунопривилегированных
го стресса и удержании их в состоянии покоя
клеток, в частности MSC, так и других имму-
посредством аденозина, генерируемого рецеп-
нопривилегированных стволовых клеток, та-
торами CD39 на поверхности T-reg. Однако ав-
ких как мышечные стволовые клетки и стволо-
торы не связывают состояние покоя стволовых
вые клетки волосяного фолликула [49], а также
клеток и иммунную привилегированность как
стволовых клеток других иммунопривилегиро-
причину и следствие.
ванных территорий: яичка [53], хряща [54], го-
Значительный интерес вызывает также
ловного мозга [55] и сетчатки глаза [56]. Вопрос
субпопуляция мезенхимных стволовых клеток
участия нестина в механизмах иммунных при-
(MSC), которые служат источником стромы
вилегий не затрагивался в работе напрямую,
как в костном мозге, так и органах, и тканях
как и вопрос механизмов иммунных привиле-
по всему организму, из-за их иммуносупрес-
гий в целом.
сивной активности и склонности находиться
Нестин
- промежуточный филамент
в покоящемся состоянии in vivo [40, 41]. Науч-
VI типа [57]. Нестин известен как маркер ство-
ная позиция относительно иммунных приви-
ловых клеток [57]. Наряду с другими проме-
легий мезенхимных клеток (MC) неоднознач-
жуточными филаментами, нестин участвует в
на. Несмотря на предпосылки и демонстрацию
ряде сигнальных путей, ключевых для стволо-
значительного иммуномодулирующего потен-
вых клеток как нормальных, так и раковых [58].
циала [34], MC и MSC классифицировались
Повышение экспрессии нестина выделяют как
как клетки, не имеющие иммунных привиле-
негативный прогностический фактор для ряда
гий [31, 42-45]. Вместе с тем работы, демон-
видов рака эпителиального, мезенхимного и
стрирующие иммунные привилегии покоящих-
нейрального происхождений: колоректального
ся стволовых клеток [36, 39], в том числе и ра-
рака, гепатоцеллюлярной карциномы, различ-
ковых [46, 47], приводят к обратному заклю-
ных видов рака центральной нервной системы,
чению и ассоциации мезенхимного фено-
немелкоклеточного рака лёгкого, рака молочной
БИОХИМИЯ том 88 вып. 11 2023
ИММУННЫЕ ПРИВИЛЕГИИ В СТВОЛОВОЙ СИСТЕМЕ
2209
железы, меланомы и множественной миело-
которой выполняется множеством механизмов
мы [59]. Более того, нестин ассоциируется с не-
и связана с функциями самоподдержания,
зрелым фенотипом опухолей и раковыми ство-
дифференцировки и активации в ответ на по-
ловыми клетками (CSC) [60]. Гиперэкспрессия
вреждение [65, 74-79]. Нарушение регуляции
нестина ассоциируется с более агрессивным
состояния покоя стволовых клеток зачастую
течением и метастазированием опухолей, их
сопровождается их истощением и ассоцииру-
рефрактерностью к терапии [61]. Вопрос о
ется с дегенеративными патологиями и старе-
том, является ли нестин прямым регулятором в
нием [80-83]. Таким образом, связь состояния
процессах формирования иммунных привиле-
покоя стволовых клеток с иммунными привиле-
гий или лишь является пассивным маркером,
гиями [36] и, более того, участие T-reg в поддер-
ассоциированным с регуляцией стволового
жании состояния покоя [39] свидетельствуют
состояния, остается открытым.
о глубокой интеграции механизмов иммунных
Дополнительные аргументы об общности
привилегий в регуляцию стволовых клеток.
стволовых клеток различных тканей происхо-
дят из работ, посвящённых плюрипотентным
стволовым клеткам взрослого организма [62-
СТВОЛОВАЯ СИСТЕМА
65]. Такие плюрипотентные клетки имеют на-
сыщенную событиями историю их изучения с
Описанные выше функции и характеристи-
использованием различных протоколов и упо-
ки стволовых клеток в значительной степени
минаются в литературе под различными назва-
определяются эндогенно - эпигенетическими
ниями: MAPCs/spore-like cells/STAP/MUSE/
метками, продуктами метаболизма, внутрен-
VSEL [62]. VSEL - очень малые эмбрионопо-
ними сигнальными каскадами, РНК-интер-
добные стволовые клетки и позиционируют-
ференцией и другими клеточными механизма-
ся как предшественники тканеспецифичных
ми [58, 84-86]. Вместе с тем стволовая клетка
стволовых клеток. Для таких клеток показано
и её окружение представляют собой сложную
участие в репаративных процессах: увеличе-
систему взаимной их регуляции [87, 88]. Прак-
ние их числа и выход в периферическую кровь
тическое отделение стволовой клетки от ниши
под действием факторов повреждения тканей.
затруднительно ввиду нарушения клеточных
MUSE демонстрируют способность к кросс-
регуляций [36, 63, 89-92]. Культивирование вы-
дифференцировке между направлениями за-
деленной субпопуляции стволовых клеток тре-
родышевых листков [52, 66]. Так, для малой
бует специальных решений [93]. Например,
субпопуляции MSC, которые можно найти в
демонстрируется эффективность использова-
соединительных тканях почти всех органов, ав-
ния методов культивирования, направленных
торы продемонстрировали способность клеток
на удержание стволовых клеток мышц в со-
к дифференцировке во всех трёх направлениях
стоянии покоя, для увеличения последующего
зародышевых листков, их самоподдержание
терапевтического эффекта на мышах [94]. Эти
и их миграцию к областям повреждения [52].
методы включают в себя локальную регуляцию
Показано, что такие стволовые клетки мигри-
стволовых клеток за счёт ниши, включающей
руют в ткани при эмбриогенезе, не принимают
в себя матрикс и специальную ростовую сре-
непосредственного участия в формировании
ду. Продукты метаболизма вносят существен-
ткани и остаются покоящимися во взрос-
ный вклад в регуляцию стволовых клеток и их
лом организме [64, 67-70]. При этом такие
окружения [39, 95]. Лиганд-рецепторные меж-
стволовые клетки обладают устойчивостью к
клеточные контакты и нанотрубки, обеспечи-
облучению и химиотерапевтическому воздей-
вающие прямой обмен цитоплазматическим
ствию [71-73]. В экспериментах по аллоген-
содержимым, также играют важную роль в
ной и ксеногенной трансплантациии MUSE
регуляции стволовых клеток и их окружения
показано наличие у них иммунных привиле-
[96-99]. Помимо потомства стволовых клеток,
гий [50, 51]. Таким образом, можно обобщить,
важную роль в поддержании стволовых кле-
что субпопуляции стволовых клеток различных
ток играют иммунные и другие клетки ниши
органов и тканей взрослого организма имеют
стволовых клеток [39, 100, 101]. Микровезику-
множество общих функций и характеристик.
лы, секретируемые MSC, содержат как мем-
Маловероятно, что для одинаковых функций
бранный репертуар рецепторов и лигандов,
эволюционно возникло множество различных
способных к взаимодействию на поверхности
и независимых механизмов, однако необходи-
клетки, так и внутреннее содержимое с его
ма строгая проверка этой гипотезы.
внутриклеточным разнообразием сигнальных
Состояние покоя стволовых клеток выде-
молекул и способны взаимодействовать с
ляется как ключевая характеристика, регуляция
мишенями в других частях тела [102-104].
12
БИОХИМИЯ том 88 вып. 11 2023
2210
КАРПЕНКО
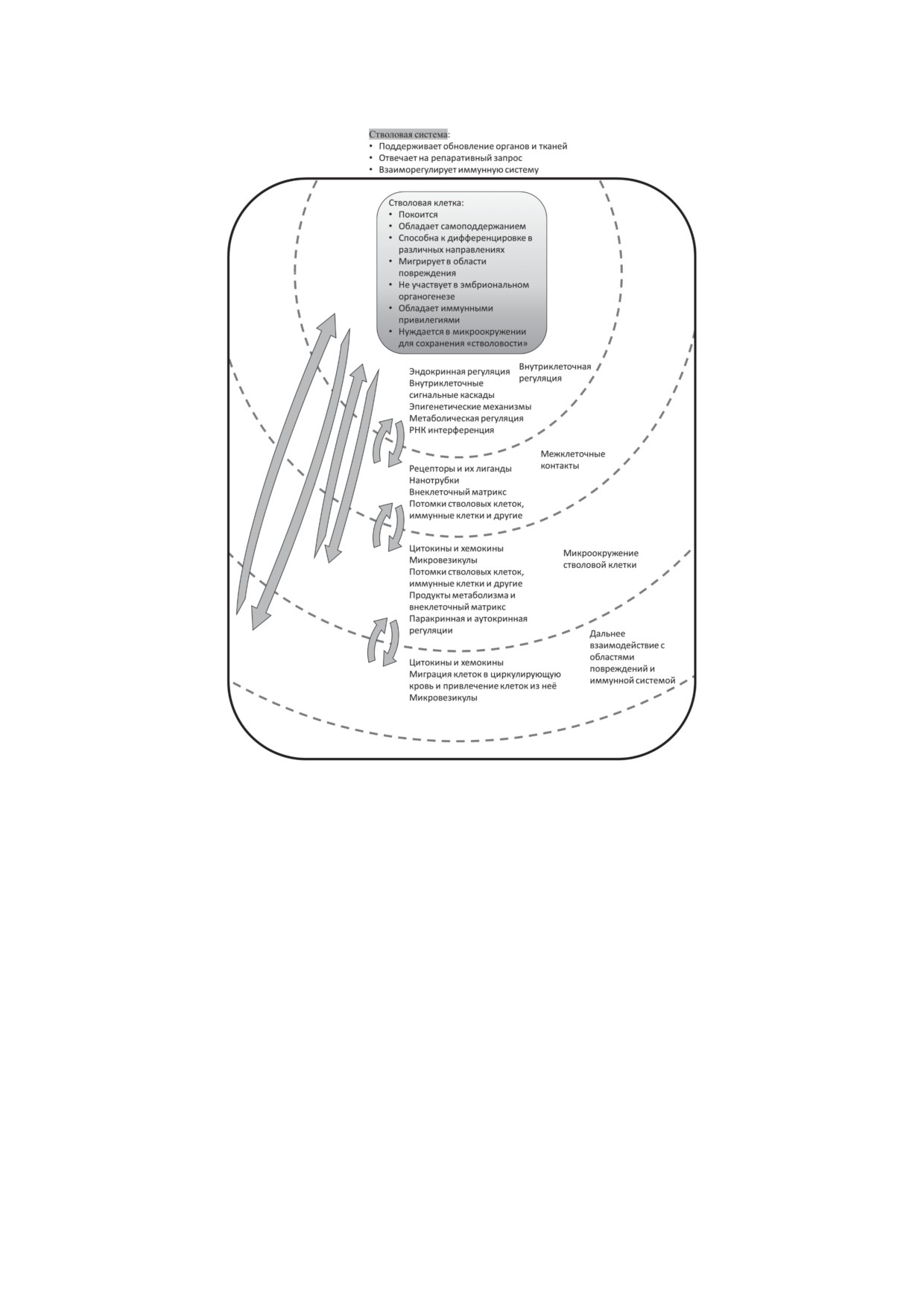
Рис. 1. Схема показывает идею обобщения стволовых клеток, их микроокружения и механизмов их регуляций в ство-
ловую систему. Пунктирные линии разделяют области взаимодействий, подписанные в правой части. В центральных
подписях указаны основные элементы, участвующие во взаимодействии, включая как клетки, так и различные некле-
точные компоненты. Стрелки в левой части указывают на процессы, происходящие между выделенными областями
взаимодействия
На примере стволовых клеток мышц демон-
позволит более точно отражать структуру объ-
стрируется их переход в состояние готовности
екта изучения, что должно благоприятно ска-
как реакция на повреждение в другой части
зываться на общем представлении. Вместе с тем
организма, а для VSEL - выход в перифериче-
разделение понятий «стволовая клетка» и «ниша
скую кровь [69, 105]. Приведённые примеры
стволовых клеток» имеет принципиальное зна-
упоминают лишь небольшую часть изученных
чение в понимании их функционирования.
механизмов, при этом демонстрируют суще-
Схемы экспериментов, способных различать
ствование сложной сети регуляции, связанной
вклад индивидуальных клеток или их субпопу-
с функциями стволовых клеток (рис. 1). Терми-
ляций, способны предложить принципиально
нологически уместно говорить о существовании
новый взгляд на объект изучения [49, 65, 88].
стволовой системы, отвечающей за регуляцию
Так, например, сокращение MC предоставля-
её клеточных и иных компонент. Эта система
ет лучшее отличие от сокращения MSC. Такое
выполняет функцию поддержки клеточного
различие мы выделили как ключевой момент,
состава органов взрослого организма, реагирует
позволивший показать иммунные привилегии
репаративным ответом в случае повреждения,
мезенхимных стволовых клеток среди общей
осуществляет взаиморегуляцию с иммунной
популяции мезенхимных клеток, не обладаю-
системой (рис. 1). Термин «стволовая система»
щих иммунными привилегиями [49].
БИОХИМИЯ том 88 вып. 11 2023
ИММУННЫЕ ПРИВИЛЕГИИ В СТВОЛОВОЙ СИСТЕМЕ
2211
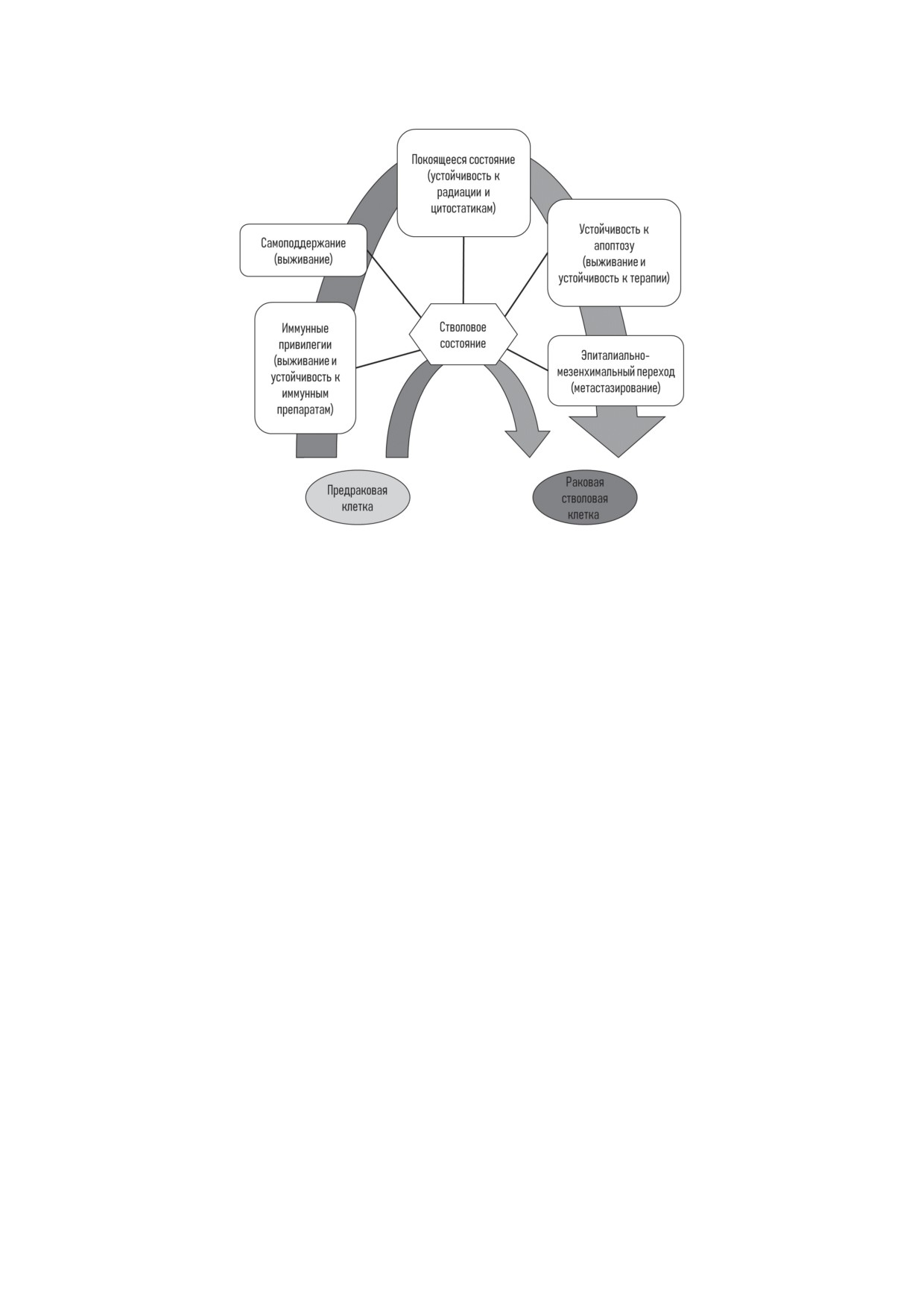
Рис. 2. Показана идея, что в ряде случаев рака, возможно, происходит получение комплекса признаков, необходимых
для выживания раковой стволовой клетки через стволовое состояние нежели через независимые события
Обобщение признаков стволовых клеток
вое состояние вместо независимого последова-
организма и признание иммунных привилегий
тельного их накопления (рис. 2).
как основного свойства субпопуляций стволо-
Отдельным фактором риска, связанным с
вых клеток даёт новый взгляд на процессы кан-
иммунными привилегиями, является возмож-
церогенеза. Известно, CSC ассоциируются с
ность их использования инфекционными па-
рефрактерностью к терапии, метастазировани-
тогенами для укрытия от действия иммунной
ем, рецидивированием [106, 107]. В литературе
системы [112]. Инфицирование стволовых кле-
демонстрируется системное сходство между
ток и их ниш приводит к нарушению функций
CSC и нормальными стволовыми клетками,
стволовой системы и выражается клинически-
выраженное в состоянии глубокого покоя,
ми патологиями в виде фиброзов, нарушения
способности к миграции и дифференцировке,
кроветворения, нарушений костной и хряще-
устойчивости к гипоксии, самоподдержанию
вой тканей, повреждения барьерных функций
и экспрессии нестина [49, 57, 58, 60, 64, 66,
в сосудах мозга [112].
106]. Иммунная система способна оказывать
Наличие столь потенциально опасного ме-
подавляющее действие на раковые клетки и
ханизма, как иммунные привилегии стволовых
тормозить развитие рака [108, 109]. Наличие
клеток, должно быть эволюционно уравнове-
иммунных привилегий у CSC как стволовых
шено не менее значимыми причинами, чтобы
предоставляет патологическим клеткам зна-
не быть отвергнутым в процессе эволюции.
чимые преимущества, что демонстрируется в
Контроль над аутоиммунитетом - подходящая
экспериментах [46, 110]. Как и в нашей работе
значимая причина. В дополнение к механиз-
с непатологичными стволовыми клетками [49],
мам центрального контроля аутоиммунитета в
демонстрируется длительное выживание рако-
организме представлены механизмы перифе-
вых стволовых клеток и сохранение их функ-
рического контроля [113, 114]. Основными ис-
ций давать метастазы при подавлении иммун-
полнителями периферического контроля счи-
ной системы [46]. Как и для непатологических
таются Т-reg, однако отмечается также участие
стволовых клеток в исследованиях отмечается
и других механизмов контроля иммунитета.
роль T-reg и состояния покоя CSC в форми-
Иммунные привилегии стволовых клеток мо-
ровании иммунных привилегий CSC [46, 47,
гут быть частью таких механизмов [29] (рис. 3).
110, 111]. Таким образом, раковые клетки могут
Это предположение подтверждается тем, что
получить целый набор преимуществ, характер-
во время воспалительного процесса MSC не
ных стволовым клеткам, включая иммунные
просто уклоняются от действия иммунных кле-
привилегии, посредством смещения в стволо-
ток, но и активизируются, выделяя хемокины,
БИОХИМИЯ том 88 вып. 11 2023
12*
2212
КАРПЕНКО
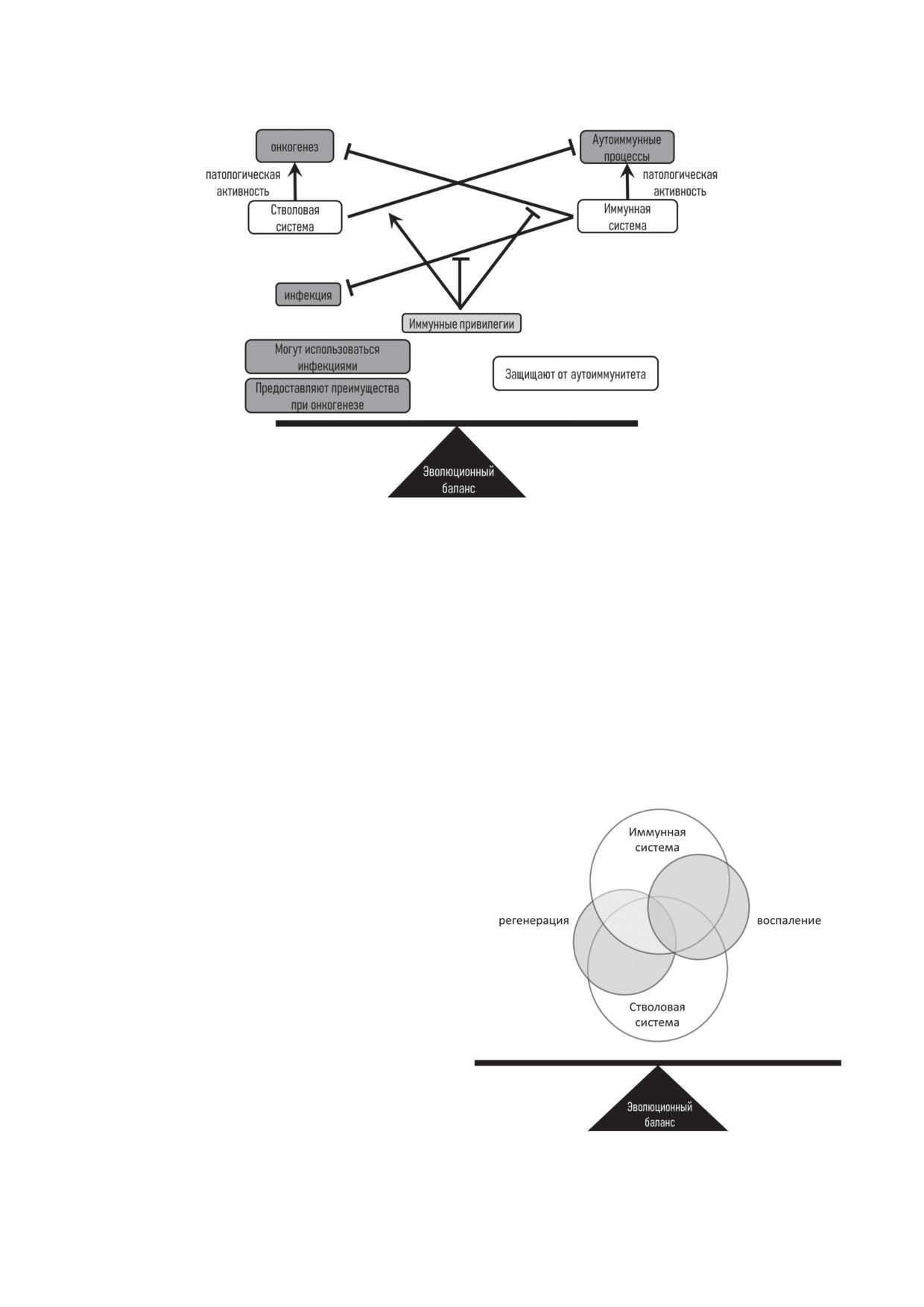
Рис. 3. Схема показывает возможную роль иммунных привилегий в регуляции стволовой и иммунной систем как ре-
зультат эволюционного баланса
которые привлекают иммунные клетки [115,
ференцировки [39, 121, 122]. Для T-reg рези-
116]. Вовлечение стволовых клеток в процесс
дентов стволовых ниш волосяных фолликулов
периферического контроля иммунитета может
показана экспрессия JAG1-сигнала, что де-
быть обусловлено высокой ценностью таких
монстрирует участие передачи Notch-сигнала
клеток и необходимостью их защиты. Также
как в иммуных регуляциях, так и в регуляции
периферический контроль может быть необ-
стволовых клеток [123-126]. Для макрофагов
ходим в дополнение к центральному контролю,
показана их роль в процессах восстановле-
особенно для сложных долгоживущих орга-
ния различных тканей, а их дисфункция при-
низмов, которые могут накопить мутационные
водит к нарушению регуляции дифференци-
различия в геноме периферических тканей
ровки стволовых клеток и фиброзу [119, 127,
и центральной иммунной системы в течение
128]. Макрофаги также оказывают поддержку
жизни [117].
В дополнение к аутоиммунному контролю,
взаимодействие стволовой системы и иммун-
ной системы необходимо в месте поврежде-
ния [118]. Правильно оркестрированная акти-
вация восстановительных и воспалительных
программ является важной биологической ре-
гуляцией [102, 119, 120]. Взаимодействие меж-
ду этими функциями представляется еще бо-
лее весомым для эволюционного равновесия,
и оно может использовать те же механизмы,
что и контроль аутоиммунитета (рис. 4).
Участие иммунной системы в регуляции
стволовой системы отмечается не только в ак-
тивных патологических процессах, но и в нор-
ме с участием T-reg и макрофагов. Для T-reg
продемонстрировано существование тканевых
T-reg с профилем экспрессии и транскрип-
томом, сходным с таковым у стволовых кле-
ток [120]. Показано участие T-reg в процессах
Рис. 4. Схема отображает баланс между регенерацией
восстановления тканей, поддержания покоя-
и воспалением как часть эволюционного баланса между
щегося состояния стволовых клеток и их диф-
механизмами стволовой и иммунной систем
БИОХИМИЯ том 88 вып. 11 2023
ИММУННЫЕ ПРИВИЛЕГИИ В СТВОЛОВОЙ СИСТЕМЕ
2213
MSC в борьбе с оксидативным стрессом по-
мы, которая, как уже отмечалось, регулирует-
средством утилизации деполяризованных ми-
ся различными механизмами, действующими
тохондрий [101]. Участие иммунных клеток
как при межклеточном контакте, так и через
в поддержании стволовых клеток в норме де-
системные и локальные механизмы, вклю-
монстрирует глубину взаимной интеграции
чающие в качестве промежуточных звеньев
стволовой и иммунной систем.
иммунные и другие клетки, образуя сложную
В свою очередь, стволовые клетки, наряду
систему, рассматриваемую в обзоре (рис. 1).
с иммуносупрессивным воздействием, способ-
Подробное рассмотрение механизмов заслу-
ны стимулировать воспалительный ответ. Так,
живает отдельного обзора, а наиболее изучен-
MSC, активированные воспалительными сиг-
ные механизмы могут стать предметом отдель-
налами, выделяют хемокины, привлекающие
ных обзоров.
иммунные клетки к области повреждения,
Важным обобщением является то, что
где стволовые клетки способны модулировать
между стволовой и иммунной системами
их дальнейшую активность [115, 116]. Гормон
существует тесная и сложная взаимосвязь.
прокальцитонин, вырабатываемый MSC, яв-
Понимание механизмов этой связи позволит
ляется одним из лучших и самых ранних мар-
применять комплексные подходы в транс-
керов различных групп инфекционных забо-
ляционной медицине и в уже существующих
леваний [112, 129]. Уровень прокальцитонина
видах терапии. Таким примером может быть
значительно повышается задолго до повыше-
использование мезенхимальных клеток и их
ния уровня С-реактивного белка, что исполь-
продуктов для подавления аутоиммунных па-
зуется в отделениях интенсивной терапии.
тологий [50, 103, 135]. В трансплантологии для
MSC также экспрессируют функциональные
профилактики и лечения реакций «трансплан-
Toll-подобные рецепторы (TLR), активирую-
тат против хозяина» могут использоваться ме-
щие миграцию, дифференцировку, секрецию
зенхимальные клетки и их неклеточные про-
цитокинов и хемокинов в ответ на патоген-
дукты [115, 136]. Другим примером является
ассоциированные лиганды [130]. Было пока-
стимуляция стволовых ниш и их механизмов
зано, что такие MSC в зависимости от сигна-
периферической защиты от аутоиммунитета
лов окружения могут утрачивать способность
вместо общей иммуносупрессии, которая мо-
к ингибированию Т-лимфоцитов вследствие
жет сопровождаться инфекционными ослож-
нарушения сигнального пути Notch посред-
нениями [137]. Эксперименты на мышах с
ством активации TLR3 и TLR4 [131]. Более
T-reg, несущими искусственный химерный ан-
того, набор генов, специфически активируе-
тигенный рецептор против заданного MHC I,
мый в стволовых клетках, предоставляет соб-
демонстрируют потенциал в борьбе с оттор-
ственную защиту от вирусных инфекций [86].
жением трансплантата [138]. Воспалительные
Таким образом, MSC имеют сложный паттерн
процессы играют ключевую роль в запуске ре-
поведения и могут как блокировать иммунный
генерации, однако их избыточная активность
ответ, так и активно участвовать в нём.
замедляет восстановление [133]. Понимание
Представленные примеры взаимной регу-
механизмов иммунной регуляции процессов
ляции стволовой и иммунной систем не явля-
регенерации может предложить инструменты
ются исчерпывающими. Например, отмеча-
для терапевтического управления иммунной
ется влияние гипоксии, часто следующей за
системой и новые решения для регенератив-
повреждением, как на подавление иммуните-
ной медицины [133, 139, 140]. Поскольку нали-
та, так и на поддержание стволовых клеток [95,
чие иммунных привилегий в норме является
111, 132]. Также аденозин играет важную роль в
результатом сложной корегуляции различных
регуляции обеих систем [133]. Причем в меха-
механизмов, в случае рака может потребо-
низмах регуляции участвуют различные клет-
ваться ингибирование различных сигнальных
ки, в том числе потомки стволовых клеток или
путей в зависимости от конкретного пациента
дендритные клетки [88, 134]. Как видно из об-
для достижения большей эффективности пер-
зора литературы, иммунные привилегии ство-
сонализированной терапии [27, 141, 142].
ловых клеток обусловлены рекрутированием
Интеграция нового механизма в систему
Т-лимфоцитов из циркулирующей крови, их
создаёт потенциальную точку поломки. Для
перепрограммированием, состоянием покоя и
каждого механизма существуют причины, ко-
другими механизмами, которые одновременно
торые перевешивают связанные с ним риски,
регулируют как иммунный ответ, так и поддер-
иначе он отвергается естественным отбором.
жание стволовых клеток. Таким образом, им-
Такая глубокая интеграция стволовой системы
мунные привилегии стволовых клеток глубоко
и иммунной системы означает наличие эво-
интегрированы в регуляцию стволовой систе-
люционной необходимости и сложной тонко
БИОХИМИЯ том 88 вып. 11 2023
2214
КАРПЕНКО
настроенной регуляции. Как видно из обзора,
клеток с иммунными клетками свидетельству-
фундаментальное значение иммунных приви-
ет о существовании сложной сети взаимного
легий непатологических стволовых клеток и
регулирования, нарушение которой может
особенно MSC трудно переоценить. Ведь MSC
привести к раку, аутоиммунным патологиям,
распространены по всему организму и демон-
дисфункции тканей органов и ускоренному
стрируют сильный вклад в иммунную регу-
старению. Исходя из наличия сложной сети
ляцию [67, 102, 103, 115, 116]. Взаимодействие
регуляции стволовых клеток, я предлагаю ис-
стволовых и иммунных систем играет важную
пользовать термин «стволовая система», ко-
роль для различных аспектов регенерации
торый включает в себя как регуляцию самих
повреждений и контроля аутоиммунитета [17,
стволовых клеток и их микроокружения, так
39, 66, 101, 103, 119, 122]. Иммунорегулирующие
и механизмы их взаимодействия с иммунной
свойства MSC используются для поддержи-
системой. Термин «стволовая система» позво-
вающей трансплантационной терапии, а ре-
ляет более точно отражать структуру объекта
генеративный потенциал MSC применяется
изучения, что будет благоприятно сказываться
в регенеративной медицине [66, 102, 104, 115,
на общем представлении. Изучение механиз-
136]. Также иммунные привилегии могут быть
мов регуляции стволовой и иммунной систем
вовлечены в развитие рака и инфекционных
открывает широкие возможности для изуче-
заболеваний [46, 47, 110, 112]. Таким образом,
ния, результаты которого позволят лучше по-
предмет обзора затрагивает широкий круг ме-
нять биологию и применить полученные ре-
дицинских проблем, в том числе и тех, кото-
зультаты в медицине.
рые не рассматриваются в данном обзоре.
Финансирование. Исследование выпол-
нено при финансовой поддержке Российского
ЗАКЛЮЧЕНИЕ
научного фонда (грант № 22-25-00459; https://
rscf.ru/project/22-25-00459/).
Ассоциация иммунных привилегий с ос-
Благодарности. Автор благодарит Бигиль-
новным свойством покоящихся стволовых
деева Алексея, заведующего лабораторией
клеток предлагает точку зрения на вопросы
эпигинетической регуляции кроветворения
регуляции аутоиммунитета, инфекционных
НМИЦ гематологии, за критическое прочте-
заболеваний, регенеративной медицины, транс-
ние работы.
плантации и онкологии. Таким образом, в
Конфликт интересов. Автор объявляет об
ряде случаев наличие у раковых клеток стволо-
отсутствии финансового или иного конфликта
вого состояния может предоставить целый ряд
интересов в представленной работе.
преимуществ, включая защиту от иммунитета.
Соблюдение этических норм. Настоящая
Это понимание может оказаться важным для
статья не содержит описания выполненных ав-
лечения случаев рака, осложнённых наличи-
тором исследований с участием людей или ис-
ем CSC. Изучение взаимодействия стволовых
пользованием животных в качестве объектов.
СПИСОК ЛИТЕРАТУРЫ
1. Van Dooremaal, J. C. (1873) The development of
6. Carson, M. J., Doose, J. M., Melchior, B., Schmid,
living tissue transplanted to foreign soil [in German],
C. D., and Ploix, C. C. (2006) CNS immune privilege:
Arch. Ophthalmol., 19, 358-373.
hiding in plain sight, Immunol. Rev., 213, 48-65,
2. Niederkorn, J. Y. (2006) See no evil, hear no evil,
doi: 10.1111/j.1600-065X.2006.00441.x.
do no evil: the lessons of immune privilege, Nat.
7. Negi, N., and Das, B. K. (2018) CNS: not an im-
Immunol., 7, 354-359, doi: 10.1038/NI1328.
munoprivilaged site anymore but a virtual second-
3. Shirai, Y. (1921) On the transplantation of the rat
ary lymphoid organ, Int. Rev. Immunol., 37, 57-68,
sarcoma in adult heterogeneous animals, Japan Med.
doi: 10.1080/08830185.2017.1357719.
World, 1, 14-15.
8. Chang, G. C., and Young, L. H. (2011) Sympathetic
4. Murphy, J. B., and Sturm, E. (1923) Conditions
ophthalmia, Semin. Ophthalmol.,
26,
316-320,
determining the transplantability of tissues in the brain,
doi: 10.3109/08820538.2011.588658.
J. Exp. Med., 38, 183-197, doi: 10.1084/jem.38.2.183.
9. Hori, J., Yamaguchi, T., Keino, H., Hamrah, P., and
5. Medawar, P. B. (1948) Immunity to homologous
Maruyama, K. (2019) Immune privilege in corneal
grafted skin; the fate of skin homografts, Br. J. Exp.
transplantation, Prog. Retin. Eye Res., 72, 100758,
Pathol., 29, 58-69.
doi: 10.1016/j.preteyeres.2019.04.002.
БИОХИМИЯ том 88 вып. 11 2023
ИММУННЫЕ ПРИВИЛЕГИИ В СТВОЛОВОЙ СИСТЕМЕ
2215
10.
Keino, H., Horie, S., and Sugita, S. (2018) Immune
testicular germ cell tumors, Adv. Exp. Med. Biol., 1226,
privilege and eye-derived T-regulatory cells, J. Immu-
111-121, doi: 10.1007/978-3-030-36214-0_9.
nol. Res., 2018, 1679197, doi: 10.1155/2018/1679197.
24.
Nguyen, P. H. D., Wasser, M., Tan, C. T., Lim, C. J.,
11.
Zenclussen, A. C., Schumacher, A., Zenclussen,
Lai, H. L. H., et al. (2022) Trajectory of immune
M. L., Wafula, P., and Volk, H. D. (2007) Immunology
evasion and cancer progression in hepatocellular
of pregnancy: cellular mechanisms allowing fetal
carcinoma, Nat. Commun., 13, 1441, doi: 10.1038/
survival within the maternal uterus, Expert Rev. Mol.
S41467-022-29122-W.
Med., 9, 1-14, doi: 10.1017/S1462399407000294.
25.
Duan, Q., Zhang, H., Zheng, J., and Zhang, L.
12.
Katsh, S. (1957) In vitro demonstration of uter-
(2020) Turning cold into hot: firing up the tumor
ine anaphylaxis in guinea pigs sensitized with ho-
microenvironment, Trends Cancer,
6,
605-618,
mologous testis or sperm, Nature, 180, 1047-1048,
doi: 10.1016/J.TRECAN.2020.02.022.
doi: 10.1038/1801047a0.
26.
Lim, A. R., Rathmell, W. K., and Rathmell, J. C.
13.
Kaur, G., Thompson, L. A., and Dufour, J. M.
(2020) The tumor microenvironment as a metabolic
(2014) Sertoli cells - immunological sentinels of
barrier to effector T cells and immunotherapy, eLife, 9,
spermatogenesis, Semin. Cell Dev. Biol., 30, 36-44,
1-13, doi: 10.7554/ELIFE.55185.
doi: 10.1016/j.semcdb.2014.02.011.
27.
Li, B., Chan, H. L., and Chen, P. (2019) Im-
14.
Kern, S., Robertson, S. A., Mau, V. J., and Maddocks, S.
mune checkpoint inhibitors: basics and challeng-
(1995) Cytokine Secretion by macrophages in the
es, Curr. Med. Chem., 26, 3009-3025, doi: 10.2174/
rat testis, Biol. Reprod., 53, 1407-1416, doi: 10.1095/
0929867324666170804143706.
biolreprod53.6.1407.
28.
Xia, L., Oyang, L., Lin, J., Tan, S., Han, Y., et al.
15.
O’Bryan, M. K., Gerdprasert, O., Nikolic-Paterson,
(2021) The cancer metabolic reprogramming and
D. J., Meinhardt, A., Muir, J. A., Foulds, L. M.,
immune response, Mol. Cancer, 20, 28, doi: 10.1186/
Phillips, D. J., De Kretser, D. M., and Hedger, M. P.
S12943-021-01316-8.
(2005) Cytokine profiles in the testes of rats treated
29.
Ichiryu, N., and Fairchild, P. J. (2013) Immune
with lipopolysaccharide reveal localized suppression
privilege of stem cells, Methods Mol. Biol., 1029, 1-16,
of inflammatory responses, Am. J. Physiol. Regul.
doi: 10.1007/978-1-62703-478-4_1.
Integr. Comp. Physiol., 288, 1744-1755, doi: 10.1152/
30.
Agudo, J. (2021) Immune privilege of skin stem
ajpregu.00651.2004.
cells: what do we know and what can we learn? Exp.
16.
Billingham, R. E., and Silvers, W. K. (1971) A biolo-
Dermatol., 30, 522-528, doi: 10.1111/EXD.14221.
gist’s reflections on dermatology, J. Invest. Dermatol.,
31.
Ankrum, J. A., Ong, J. F., and Karp, J. M. (2014) Mes-
57, 227-240, doi: 10.1111/1523-1747.ep12261543.
enchymal stem cells: immune evasive, not immune
17.
Paus, R., Bulfone-Paus, S., and Bertolini, M. (2018)
privileged, Nat. Biotechnol., 32, 252-260, doi: 10.1038/
Hair follicle immune privilege revisited: the key to
nbt.2816.
alopecia areata management, J. Invest. Dermatol.
32.
Aguila, H. L., and Weissman, I. L. (1996) Hematopoi-
Symp. Proc., 19, 12-17, doi: 10.1016/j.jisp.2017.10.014.
etic stem cells are not direct cytotoxic targets of natural
18.
Sun, Z., Zhang, M., Zhao, X. H., Liu, Z. H., Gao, Y.,
killer cells, Blood, 87, 1225-1231, doi: 10.1182/blood.
Samartzis, D., Wang, H. Q., and Luo, Z. J. (2013)
V87.4.1225.bloodjournal8741225.
Immune cascades in human intervertebral disc: the
33.
Drukker, M., Katz, G., Urbach, A., Schuldiner, M.,
pros and cons, Int. J. Clin. Exp. Pathol., 6, 1009-1014.
Markel, G., Itskovitz-Eldor, J., Reubinoff, B.,
19.
Fujihara, Y., Takato, T., and Hoshi, K. (2014) Mac-
Mandelboim, O., and Benvenisty, N. (2002) Charac-
rophage-inducing FasL on chondrocytes forms im-
terization of the expression of MHC proteins in human
mune privilege in cartilage tissue engineering, enhanc-
embryonic stem cells, Proc. Natl. Acad. Sci. USA, 99,
ing in vivo regeneration, Stem Cells, 32, 1208-1219,
9864-9869, doi: 10.1073/PNAS.142298299.
doi: 10.1002/stem.1636.
34.
Rasmusson, I., Ringdén, O., Sundberg, B., and Le
20.
Sun, Z., Liu, B., and Luo, Z. J. (2020) The immune
Blanc, K. (2003) Mesenchymal stem cells inhib-
privilege of the intervertebral disc: implications for
it the formation of cytotoxic T lymphocytes, but not
intervertebral disc degeneration treatment, Int. J. Med.
activated cytotoxic T lymphocytes or natural killer
Sci., 17, 685-692, doi: 10.7150/ijms.42238.
cells, Transplantation, 76, 1208-1213, doi: 10.1097/
21.
Joyce, J. A., and Fearon, D. T. (2015) T cell exclusion,
01.TP.0000082540.43730.80.
immune privilege, and the tumor microenvironment,
35.
Mammolenti, M., Gajavelli, S., Tsoulfas, P., and
Science, 348, 74-80, doi: 10.1126/science.aaa6204.
Levy, R. (2004) Absence of major histocompatibility
22.
Chen, D. S., and Mellman, I. (2013) Oncology meets
complex class I on neural stem cells does not permit
immunology: the cancer-immunity cycle, Immunity,
natural killer cell killing and prevents recognition by
39, 1-10, doi: 10.1016/j.immuni.2013.07.012.
alloreactive cytotoxic T lymphocytes in vitro, Stem
23.
Kalavska, K., Kucerova, L., Schmidtova, S.,
Cells, 22, 1101-1110, doi: 10.1634/stemcells.22-6-1101.
Chovanec, M., and Mego, M. (2020) Cancer stem cell
36.
Agudo, J., Park, E. S., Rose, S. A., Alibo, E.,
niche and immune-active tumor microenvironment in
Sweeney, R., et al. (2018) Quiescent tissue stem cells
БИОХИМИЯ том 88 вып. 11 2023
2216
КАРПЕНКО
evade immune surveillance, Immunity, 48, 271-285,
48.
Babaei, G., Aziz, S. G. G., and Jaghi, N. Z. Z. (2021)
doi: 10.1016/j.immuni.2018.02.001.
EMT, cancer stem cells and autophagy; the three
37.
Bernitz, J. M., Kim, H. S., MacArthur, B., Sieburg, H.,
main axes of metastasis, Biomed. Pharmacother., 133,
and Moore, K. (2016) Hematopoietic stem cells count
110909, doi: 10.1016/J.BIOPHA.2020.110909.
and remember self-renewal divisions, Cell, 167, 1296-
49.
Karpenko, D., Kapranov, N., and Bigildeev, A. (2022)
1309, doi: 10.1016/j.cell.2016.10.022.
Nestin-GFP transgene labels immunoprivileged
38.
Fürst, D., Neuchel, C., Tsamadou, C., Schrezen-
bone marrow mesenchymal stem cells in the model
meier, H., and Mytilineos, J. (2019) HLA matching in
of ectopic foci formation, Front. Cell Dev. Biol., 10,
unrelated stem cell transplantation up to date, Transfus.
993056, doi: 10.3389/FCELL.2022.993056.
Med. Hemother., 46, 326-336, doi: 10.1159/000502263.
50.
Kuroda, Y., Oguma, Y., Hall, K., and Dezawa, M.
39.
Hirata, Y., Furuhashi, K., Ishii, H., Li, H. W.,
(2022) Endogenous reparative pluripotent muse
Pinho, S., Ding, L., Robson, S. C., Frenette, P. S.,
cells with a unique immune privilege system: hint
and Fujisaki, J. (2018) CD150 high bone marrow Tregs
at a new strategy for controlling acute and chronic
maintain hematopoietic stem cell quiescence and
inflammation, Front. Pharmacol.,
13,
1027961,
immune privilege via adenosine, Cell Stem Cell, 22,
doi: 10.3389/FPHAR.2022.1027961.
445-453, doi: 10.1016/j.stem.2018.01.017.
51.
Yamada, Y., Wakao, S., Kushida, Y., Minatoguchi, S.,
40.
Méndez-Ferrer, S., Michurina, T. V., Ferraro, F.,
Mikami, A., et al. (2018) S1P-S1PR2 axis mediates
Mazloom, A. R., Macarthur, B. D., Lira, S. A.,
homing of muse cells into damaged heart for long-
Scadden, D. T., Ma’ayan, A., Enikolopov, G. N.,
lasting tissue repair and functional recovery after acute
and Frenette, P. S. (2010) Mesenchymal and haema-
myocardial infarction, Circ. Res., 122, 1069-1083,
topoietic stem cells form a unique bone marrow niche,
doi: 10.1161/CIRCRESAHA.117.311648.
Nature, 466, 829-834, doi: 10.1038/nature09262.
52.
Li, H., Wei, J., Liu, X., Zhang, P., and Lin, J. (2022)
41.
Naji, A., Eitoku, M., Favier, B., Deschaseaux, F., Rouas-
Muse Cells: ushering in a new era of stem cell-based
Freiss, N., and Suganuma, N. (2019) Biological func-
therapy for stroke, Stem Cell Res. Ther., 13, 421,
tions of mesenchymal stem cells and clinical implica-
doi: 10.1186/S13287-022-03126-1.
tions, Cell. Mol. Life Sci., 76, 3323-3348, doi: 10.1007/
53.
Jiang, M. H., Cai, B., Tuo, Y., Wang, J., Zang, Z. J.,
S00018-019-03125-1.
et al. (2014) Characterization of nestin-positive stem
42.
Zangi, L., Margalit, R., Reich-Zeliger, S., Bachar-
leydig cells as a potential source for the treatment of
Lustig, E., Beilhack, A., Negrin, R., and Reisner, Y.
testicular leydig cell dysfunction, Cell Res., 24, 1466-
(2009) Direct imaging of immune rejection and
1485, doi: 10.1038/CR.2014.149.
memory induction by allogeneic mesenchymal stromal
54.
Jaramillo-Rangel, G., Chávez-Briones, M. D. L.,
cells, Stem Cells, 27, 2865-2874, doi: 10.1002/stem.217.
Ancer-Arellano, A., and Ortega-Martínez, M. (2021)
43.
Miura, Y., Yoshioka, S., Yao, H., Takaori-Kondo, A.,
Nestin-expressing cells in the lung: the bad and the
Maekawa, T., and Ichinohe, T. (2013) Chimerism of
good parts, Cells, 10, 3413, doi: 10.3390/cells10123413.
bone marrow mesenchymal stem/stromal cells in allo-
55.
Li, L., Mignone, J., Yang, M., Matic, M., Penman, S.,
geneic hematopoietic cell transplantation: is it clinically
Enikolopov, G., and Hoffman, R. M. (2003) Nestin
relevant? Chimerism, 4, 78-83, doi: 10.4161/chim.25609.
expression in hair follicle sheath progenitor cells, Proc.
44.
Badillo, A. T., Beggs, K. J., Javazon, E. H., Tebbets,
Natl. Acad. Sci. USA, 100, 9958-9961, doi: 10.1073/
J. C., and Flake, A. W. (2007) Murine bone marrow
PNAS.1733025100.
stromal progenitor cells elicit an in vivo cellular and hu-
56.
Bhatia, B., Singhal, S., Lawrence, J. M., Khaw, P. T.,
moral alloimmune response, Biol. Blood Marrow Trans-
and Limb, G. A.
(2009) Distribution of Müller
plant., 13, 412-422, doi: 10.1016/j.bbmt.2006.12.447.
stem cells within the neural retina: evidence for the
45.
Berglund, A. K., Fortier, L. A., Antczak, D. F., and
existence of a ciliary margin-like zone in the adult
Schnabel, L. V. (2017) Immunoprivileged no more:
human eye, Exp. Eye Res., 89, 373-382, doi: 10.1016/J.
measuring the immunogenicity of allogeneic adult
EXER.2009.04.005.
mesenchymal stem cells, Stem Cell Res. Ther., 8, 288,
57.
Bernal, A., and Arranz, L. (2018) Nestin-expressing
doi: 10.1186/s13287-017-0742-8.
progenitor cells: function, identity and therapeutic
46.
Malladi, S., MacAlinao, D. G., Jin, X., He, L.,
implications, Cell. Mol. Life Sci.,
75,
2177-2195,
Basnet, H., Zou, Y., De Stanchina, E., and
doi: 10.1007/S00018-018-2794-Z.
Massagué, J. (2016) Metastatic latency and immune
58.
Sharma, P., Alsharif, S., Fallatah, A., and Chung,
evasion through autocrine inhibition of WNT, Cell,
B. M. (2019) Intermediate filaments as effectors of
165, 45, doi: 10.1016/J.CELL.2016.02.025.
cancer development and metastasis: a focus on kera-
47.
Galassi, C., Musella, M., Manduca, N., Maccafeo, E.,
tins, vimentin, and nestin, Cells, 8, 497, doi: 10.3390/
and Sistigu, A. (2021) The immune privilege of
CELLS8050497.
cancer stem cells: a key to understanding tumor
59.
Szymańska-Chabowska, A., Świątkowski, F., Jan-
immune escape and therapy failure, Cells, 10, 2361
kowska-Polańska, B., Mazur, G., and Chabowski, M.
doi: 10.3390/CELLS10092361.
(2021) Nestin expression as a diagnostic and prognostic
БИОХИМИЯ том 88 вып. 11 2023
ИММУННЫЕ ПРИВИЛЕГИИ В СТВОЛОВОЙ СИСТЕМЕ
2217
marker in colorectal cancer and other tumors, Clin. Med.
72.
Anand, S., Bhartiya, D., Sriraman, K., and Mallick, A.
Insights Oncol., 15, doi: 10.1177/11795549211038256.
(2016) Underlying mechanisms that restore spermato-
60.
Neradil, J., and Veselska, R. (2015) Nestin as a
genesis on transplanting healthy niche cells in busul-
marker of cancer stem cells, Cancer Sci., 106, 803-811,
phan treated mouse testis, Stem Cell Rev. Rep., 12,
doi: 10.1111/CAS.12691.
682-697, doi: 10.1007/S12015-016-9685-1.
61.
Ishiwata, T., Matsuda, Y., and Naito, Z. (2011) Nestin
73.
Ratajczak, J., Wysoczynski, M., Zuba-Surma, E.,
in gastrointestinal and other cancers: effects on cells
Wan, W., Kucia, M., et al. (2011) Adult murine bone
and tumor angiogenesis, World J. Gastroenterol., 17,
marrow-derived very small embryonic-like stem cells
409-418, doi: 10.3748/WJG.V17.I4.409.
differentiate into the hematopoietic lineage after co-
62.
Bhartiya, D.
(2017) Pluripotent stem cells in
culture over OP9 stromal cells, Exp. Hematol., 39, 225-
adult tissues: struggling to be acknowledged over
237, doi: 10.1016/j.exphem.2010.10.007.
two decades, Stem Cell. Rev. Rep.,
13,
713-724,
74.
Sousa-Victor, P., García-Prat, L., and Muñoz-
doi: 10.1007/S12015-017-9756-Y.
Cánoves, P. (2021) Control of satellite cell function in
63.
Ratajczak, M. Z., Ratajczak, J., and Kucia, M. (2019)
muscle regeneration and its disruption in ageing, Nat.
Very small embryonic-like stem cells (VSELs), Circ.
Rev. Mol. Cell Biol., 23, 204-226, doi: 10.1038/s41580-
Res., 124, 208-210, doi: 10.1161/circresaha.118.314287.
021-00421-2.
64.
Ratajczak, M. Z., Ratajczak, J., Suszynska, M.,
75.
Chen, Z., Guo, Q., Song, G., and Hou, Y. (2022)
Miller, D. M., Kucia, M., and Shin, D. M. (2017)
Molecular regulation of hematopoietic stem cell
A novel view of the adult stem cell compartment from
quiescence, Cell. Mol. Life Sci., 79, 218, doi: 10.1007/
the perspective of a quiescent population of very small
S00018-022-04200-W.
embryonic-like stem cells, Circ. Res., 120, 166-178,
76.
Cavallucci, V., Fidaleo, M., and Pani, G.
(2016)
doi: 10.1161/CIRCRESAHA.116.309362.
Neural stem cells and nutrients: poised between
65.
Bhartiya, D., Jha, N., Tripathi, A., and Tripathi, A.
quiescence and exhaustion, Trends Endocrinol. Metab.,
(2023) Very small embryonic-like stem cells have the
27, 756-769, doi: 10.1016/J.TEM.2016.06.007.
potential to win the three-front war on tissue damage,
77.
Ancel, S., Stuelsatz, P., and Feige, J. N. (2021) Muscle
cancer, and aging, Front. Cell. Dev. Biol., 10, 1061022,
stem cell quiescence: controlling stemness by staying
doi: 10.3389/FCELL.2022.1061022.
asleep, Trends Cell Biol., 31, 556-568, doi: 10.1016/
66.
Dezawa, M. (2016) Muse cells provide the pluripotency
J.TCB.2021.02.006.
of mesenchymal stem cells: direct contribution of
78.
Ayyaz, A., Kumar, S., Sangiorgi, B., Ghoshal, B.,
muse cells to tissue regeneration, Cell Transplant., 25,
Gosio, J., Ouladan, S., Fink, M., Barutcu, S.,
849-861, doi: 10.3727/096368916X690881.
Trcka, D., Shen, J., Chan, K., Wrana, J. L., and
67.
Isern, J., García-García, A., Martín, A. M., Arranz, L.,
Gregorieff, A. (2019) Single-cell transcriptomes of the
Martín-Pérez, D., Torroja, C., Sánchez-Cabo, F.,
regenerating intestine reveal a revival stem cell, Nature,
and Méndez-Ferrer, S. (2014) The neural crest is a
569, 121-125, doi: 10.1038/S41586-019-1154-Y.
source of mesenchymal stem cells with specialized
79.
Dias, I. B., Bouma, H. R., and Henning, R. H. (2021)
hematopoietic stem cell niche function, eLife, 3,
Unraveling the big sleep: molecular aspects of stem
03696, doi: 10.7554/ELIFE.03696.
cell dormancy and hibernation, Front. Physiol., 12,
68.
Gleiberman, A. S., Michurina, T., Encinas, J. M.,
624950, doi: 10.3389/FPHYS.2021.624950.
Roig, J. L., Krasnov, P., Balordi, F., Fishell, G.,
80.
Ibrayeva, A., Bay, M., Pu, E., Jörg, D. J., Peng, L.,
Rosenfeld, M. G., and Enikolopov, G.
(2008)
Jun, H., Zhang, N., Aaron, D., Lin, C., Resler, G.,
Genetic approaches identify adult pituitary stem cells,
Hidalgo, A., Jang, M. H., Simons, B. D., and
Proc. Natl. Acad. Sci. USA, 105, 6332, doi: 10.1073/
Bonaguidi, M. A.
(2021) Early stem cell aging
PNAS.0801644105.
in the mature brain, Cell Stem Cell, 28, 955-966,
69.
Dumont, N. A., Wang, Y. X., and Rudnicki, M. A.
doi: 10.1016/J.STEM.2021.03.018.
(2015) Intrinsic and extrinsic mechanisms regulating
81.
Choi, K., Park, S. H., Park, S. Y., and Yoon, S. K.
satellite cell function, Development, 142, 1572-1581,
(2022) The stem cell quiescence and niche signaling is
doi: 10.1242/DEV.114223.
disturbed in the hair follicle of the hairpoor mouse, an
70.
Neo, W. H., Lie-A-Ling, M., Fadlullah, M. Z. H., and
MUHH model mouse, Stem Cell Res. Ther., 13, 211,
Lacaud, G. (2021) Contributions of embryonic HSC-
doi: 10.1186/S13287-022-02898-W.
independent hematopoiesis to organogenesis and the
82.
Chakkalakal, J. V., Jones, K. M., Basson, M. A.,
adult hematopoietic system, Front. Cell Dev. Biol., 9,
and Brack, A. S. (2012) The aged niche disrupts
631699, doi: 10.3389/FCELL.2021.631699.
muscle stem cell quiescence, Nature, 490, 355-360,
71.
Shaikh, A., Bhartiya, D., Kapoor, S., and Nimkar, H.
doi: 10.1038/nature11438.
(2016) Delineating the effects of 5-fluorouracil and
83.
Singh, S., Jakubison, B., and Keller, J. R.
(2020)
follicle-stimulating hormone on mouse bone marrow
Protection of hematopoietic stem cells from stress-
stem/progenitor cells, Stem Cell Res. Ther., 7, 59,
induced exhaustion and aging, Curr. Opin. Hematol.,
doi: 10.1186/S13287-016-0311-6.
27, 225-231, doi: 10.1097/MOH.0000000000000586.
БИОХИМИЯ том 88 вып. 11 2023
2218
КАРПЕНКО
84.
Zhang, Z., Zhuang, L., and Lin, C. P. (2019) Roles
cy of the skeletal muscle-derived stem cells in mice,
of microRNAs in establishing and modulating stem
Stem Cell Res. Ther., 13, 56, doi: 10.1186/S13287-
cell potential, Int. J. Mol. Sci., 20, 3643, doi: 10.3390/
022-02730-5.
IJMS20153643.
96. Kann, A. P., Hung, M., and Krauss, R. S. (2021)
85.
Ren, R., Ocampo, A., Liu, G. H., and Izpisua
Cell-cell contact and signaling in the muscle stem cell
Belmonte, J. C. (2017) Regulation of stem cell aging by
niche, Curr. Opin. Cell. Biol., 73, 78-83, doi: 10.1016/
metabolism and epigenetics, Cell Metab., 26, 460-474,
J.CEB.2021.06.003.
doi: 10.1016/J.CMET.2017.07.019.
97. Zamfirescu, A. M., Yatsenko, A. S., and Shcherbata,
86.
Wu, X., Dao Thi, V. L., Huang, Y., Billerbeck, E.,
H. R.
(2022) Notch signaling sculpts the stem
Saha, D., et al. (2018) Intrinsic immunity shapes
cell niche, Front. Cell. Dev. Biol.,
10,
1027222,
viral resistance of stem cells, Cell, 172, 423-438,
doi: 10.3389/FCELL.2022.1027222.
doi: 10.1016/J.CELL.2017.11.018.
98. Whitehead, J., Zhang, J., Harvestine, J. N., Kotham-
87.
Fuchs, E., and Blau, H. M. (2020) Tissue stem cells:
bawala, A., Liu, G. Yu, and Leach, J. K. (2020) Tun-
architects of their niches, Cell Stem Cell, 27, 532-556,
neling nanotubes mediate the expression of senescence
doi: 10.1016/J.STEM.2020.09.011.
markers in mesenchymal stem/stromal cell spheroids,
88.
Cancedda, R., and Mastrogiacomo, M. (2023) Transit
Stem Cells, 38, 80-89, doi: 10.1002/stem.3056.
Amplifying Cells (TACs): a still not fully understood
99. Jackson, M. V., Morrison, T. J., Doherty, D. F.,
cell population, Front. Bioeng. Biotechnol.,
11,
McAuley, D. F., Matthay, M. A., Kissenpfennig, A.,
1189225, doi: 10.3389/FBIOE.2023.1189225.
O’Kane, C. M., and Krasnodembskaya, A. D. (2016)
89.
Chertkov, J. L., Drize, N. J., and Gurevitch, O. A.
Mitochondrial transfer via tunneling nanotubes is an
(1983) Hemopoietic stromal precursors in long-term
important mechanism by which mesenchymal stem
culture of bone marrow: II. Significance of initial
cells enhance macrophage phagocytosis in the in vitro
packing for creating a hemopoietic microenvironment
and in vivo models of ARDS, Stem Cells, 34, 2210-
and maintaining stromal precursors in the culture,
2223, doi: 10.1002/STEM.2372.
Exp. Hematol., 11, 243-248.
100. Yamazaki, S., Ema, H., Karlsson, G., Yamaguchi, T.,
90.
Nie, Y., Han, Y.-C., and Zou, Y.-R. (2008) CXCR4 is
Miyoshi, H., Shioda, S., Taketo, M. M., Karlsson, S.,
required for the quiescence of primitive hematopoietic
Iwama, A., and Nakauchi, H. (2011) Nonmyelinating
cells, J. Exp. Med.,
205,
777-783, doi:
10.1084/
schwann cells maintain hematopoietic stem cell
jem.20072513.
hibernation in the bone marrow niche, Cell, 147, 1146-
91.
Greenbaum, A., Hsu, Y. M. S., Day, R. B.,
1158, doi: 10.1016/J.CELL.2011.09.053.
Schuettpelz, L. G., Christopher, M. J., Borgerding,
101. Phinney, D. G., Di Giuseppe, M., Njah, J., Sala, E.,
J. N., Nagasawa, T., and Link, D. C. (2013) CXCL12
Shiva, S., et al. (2015) Mesenchymal stem cells use ex-
in early mesenchymal progenitors is required for
tracellular vesicles to outsource mitophagy and shuttle
haematopoietic stem-cell maintenance, Nature, 495,
microRNAs, Nat. Commun., 6, 8472, doi: 10.1038/
227-230, doi: 10.1038/nature11926.
ncomms9472.
92.
Boyd, A. L., Campbell, C. J. V., Hopkins, C. I.,
102. Toh, W. S., Zhang, B. I. N., Lai, R. C., and Lim, S.
Fiebig-Comyn, A., Russell, J., Ulemek, J., Foley, R.,
K. (2018) Immune regulatory targets of mesenchymal
Leber, B., Xenocostas, A., Collins, T. J., and
stromal cell exosomes/small extracellular vesicles
Bhatia, M. (2014) Niche displacement of human
in tissue regeneration, Cytotherapy, 20, 1419-1426,
leukemic stem cells uniquely allows their competitive
doi: 10.1016/J.JCYT.2018.09.008.
replacement with healthy HSPCs, J. Exp. Med., 211,
103. Kahmini, F. R., and Shahgaldi, S. (2021) Therapeutic
1925-1935, doi: 10.1084/jem.20140131.
potential of mesenchymal stem cell-derived extracel-
93.
Lahlil, R., Scrofani, M., Barbet, R., Tancredi, C.,
lular vesicles as novel cell-free therapy for treatment
Aries, A., and Hénon, P. (2018) VSELs maintain their
of autoimmune disorders, Exp. Mol. Pathol., 118,
pluripotency and competence to differentiate after
104566, doi: 10.1016/J.YEXMP.2020.104566.
enhanced ex vivo expansion, Stem Cell Rev. Rep., 14,
104. Nakazaki, M., Lankford, K. L., Yamamoto, H.,
510-524, doi: 10.1007/S12015-018-9821-1.
Mae, Y., and Kocsis, J. D. (2023) Human mesen-
94.
Quarta, M., Brett, J. O., DiMarco, R., De Morree, A.,
chymal stem-derived extracellular vesicles improve
Boutet, S. C., Chacon, R., Gibbons, M. C., Garcia,
body growth and motor function following severe spi-
V. A., Su, J., Shrager, J. B., Heilshorn, S., and
nal cord injury in rat, Clin. Transl. Med., 13, 1284,
Rando, T. A. (2016) An artificial niche preserves the
doi: 10.1002/CTM2.1284.
quiescence of muscle stem cells and enhances their
105. Ratajczak, M. Z., Liu, R., Marlicz, W., Blogowski, W.,
therapeutic efficacy, Nat. Biotechnol., 34, 752-759,
Starzynska, T., Wojakowski, W., and Zuba-Surma, E.
doi: 10.1038/nbt.3576.
(2011) Identification of very small embryonic/epiblast-
95.
Elashry, M. I., Kinde, M., Klymiuk, M. C., Eldaey, A.,
like stem cells (VSELS) circulating in peripheral blood
Wenisch, S., and Arnhold, S. (2022) The effect of
during organ/tissue injuries, Methods Cell Biol., 103,
hypoxia on myogenic differentiation and multipoten-
31-54, doi: 10.1016/B978-0-12-385493-3.00003-6.
БИОХИМИЯ том 88 вып. 11 2023
ИММУННЫЕ ПРИВИЛЕГИИ В СТВОЛОВОЙ СИСТЕМЕ
2219
106. Barbato, L., Bocchetti, M., Di Biase, A., and Regad, T.
119. Vannella, K. M., and Wynn, T. A. (2017) Mechanisms
(2019) Cancer stem cells and targeting strategies, Cells,
of organ injury and repair by macrophages, Annu.
8, 926, doi: 10.3390/CELLS8080926.
Rev. Physiol.,
79,
593-617, doi:
10.1146/annurev-
107. Mantovani, A., Marchesi, F., Malesci, A., Laghi, L.,
physiol-022516-034356.
and Allavena, P. (2017) Tumour-associated macro-
120. Zhang, R., Xu, K., Shao, Y., Sun, Y., Saredy, J.,
phages as treatment targets in oncology, Nat. Rev. Clin.
et al. (2021) Tissue Treg secretomes and transcription
Oncol., 14, 399-416, doi: 10.1038/nrclinonc.2016.217.
factors shared with stem cells contribute to a Treg
108. Rollan, M. P., Cabrera, R., and Schwartz, R. A.
niche to maintain Treg-ness with 80% innate immune
(2022) Current knowledge of immunosuppression
pathways, and functions of immunosuppression
as a risk factor for skin cancer development, Crit.
and tissue repair, Front. Immunol.,
11,
632239,
Rev. Oncol. Hematol., 177, 103754, doi: 10.1016/
doi: 10.3389/FIMMU.2020.632239.
j.critrevonc.2022.103754.
121. Cho, I., Lui, P. P., and Ali, N. (2020) Treg regulation
109. Dugué, P. A., Rebolj, M., Garred, P., and Lynge, E.
of the epithelial stem cell lineage, J. Immunol. Regen.
(2013) Immunosuppression and risk of cervical cancer,
Med., 8, 100028, doi: 10.1016/J.REGEN.2020.100028.
Expert Rev. Anticancer Ther., 13, 29-42, doi: 10.1586/
122. Li, J., Tan, J., Martino, M. M., and Lui, K. O.
ERA.12.159.
(2018) Regulatory T-cells: potential regulator of tissue
110. You, Y., Li, Y., Li, M., Lei, M., Wu, M., Qu, Y.,
repair and regeneration, Front. Immunol., 9, 585,
Yuan, Y., Chen, T., and Jiang, H. (2018) Ovarian
doi: 10.3389/FIMMU.2018.00585.
cancer stem cells promote tumour immune privilege
123. Liu, J., Sato, C., Cerletti, M., and Wagers, A. (2010)
and invasion via CCL5 and regulatory T cells, Clin.
Notch signaling in the regulation of stem cell self-
Exp. Immunol., 191, 60-73, doi: 10.1111/CEI.13044.
renewal and differentiation, Curr. Top. Dev. Biol., 92,
111. Baldominos, P., Barbera-Mourelle, A., Barreiro, O.,
367-409, doi: 10.1016/S0070-2153(10)92012-7.
Huang, Y., Wight, A., et al. (2022) Quiescent cancer
124. Ali, N., Zirak, B., Rodriguez, R. S., Pauli, M. L.,
cells resist T cell attack by forming an immunosup-
Truong, H. A., et al. (2017) Regulatory T cells in skin
pressive niche, Cell, 185, 1694-1708, doi: 10.1016/
facilitate epithelial stem cell differentiation, Cell, 169,
j.cell.2022.03.033.
1119-1129, doi: 10.1016/J.CELL.2017.05.002.
112. Lebeau, G., Ah-Pine, F., Daniel, M., Bedoui, Y.,
125. Golub, R.
(2021) The Notch signaling pathway
Vagner, D., Frumence, E., and Gasque, P. (2022)
involvement in innate lymphoid cell biology,
Perivascular mesenchymal stem/stromal cells, an
Biomed. J., 44, 133-143, doi: 10.1016/J.BJ.2020.12.004.
immune privileged niche for viruses? Int. J. Mol. Sci.,
126. Meng, J., Jiang, Y.-Z., Zhao, S., Tao, Y., Zhang, T.,
23, 8038, doi: 10.3390/IJMS23148038.
et al. (2022) Tumor-derived Jagged1 promotes cancer
113. Theofilopoulos, A. N., Kono, D. H., and Baccala, R.
progression through immune evasion, Cell Rep., 38,
(2017) The Multiple pathways to autoimmunity, Nat.
110492, doi: 10.1016/J.CELREP.2022.110492.
Immunol., 18, 716-724, doi: 10.1038/NI.3731.
127. Chazaud, B. (2020) Inflammation and skeletal muscle
114. Legoux, F. P., Lim, J. B., Cauley, A. W., Dikiy, S.,
regeneration: leave it to the macrophages! Trends Im-
Ertelt, J., Mariani, T. J., Sparwasser, T., Way, S. S.,
munol., 41, 481-492, doi: 10.1016/J.IT.2020.04.006.
and Moon, J. J. (2015) CD4+ T cell tolerance to tissue-
128. Oishi, Y., and Manabe, I. (2018) Macrophages in
restricted self antigens is mediated by antigen-specific
inflammation, repair and regeneration, Int. Immunol.,
regulatory T Cells rather than deletion, Immunity, 43,
30, 511-528, doi: 10.1093/INTIMM/DXY054.
896-908, doi: 10.1016/J.IMMUNI.2015.10.011.
129. Velissaris, D., Zareifopoulos, N., Lagadinou, M.,
115. Sergeant, E., Buysse, M., Devos, T., and Sprangers, B.
Platanaki, C., Tsiotsios, K., Stavridis, E. L., Kasar-
(2021) Multipotent mesenchymal stromal cells in kid-
tzian, D. I., Pierrakos, C., and Karamouzos, V. (2021)
ney transplant recipients: the next big thing? Blood
Procalcitonin and sepsis in the emergency department:
Rev., 45, 100718, doi: 10.1016/J.BLRE.2020.100718.
an update, Eur. Rev. Med. Pharmacol. Sci., 25, 466-
116. López-García, L., and Castro-Manrreza, M. E. (2021)
479, doi: 10.26355/EURREV_202101_24416.
TNF-α and IFN-γ participate in improving the im-
130. Lombardo, E., and Delarosa, O. (2010) Modula-
munoregulatory capacity of mesenchymal stem/stro-
tion of adult mesenchymal stem cells activity by toll-
mal cells: importance of cell-cell contact and extracel-
like receptors: implications on therapeutic poten-
lular vesicles, Int. J. Mol. Sci., 22, 9531, doi: 10.3390/
tial, Mediators Inflamm., 2010, 865601, doi: 10.1155/
IJMS22179531.
2010/865601.
117. Blokzijl, F., De Ligt, J., Jager, M., Sasselli, V.,
131. Raicevic, G., Rouas, R., Najar, M., Stordeur, P.,
Roerink, S., et al. (2016) Tissue-specific mutation
Id Boufker, H., Bron, D., Martiat, P., Goldman, M.,
accumulation in human adult stem cells during life,
Nevessignsky, M. T., and Lagneaux, L. (2010) Inflam-
Nature, 538, 260-264, doi: 10.1038/nature19768.
mation modifies the pattern and the function of Toll-
118. Cooke, J. P. (2019) Inflammation and its role in
like receptors expressed by human mesenchymal stro-
regeneration and repair, Circ. Res., 124, 1166-1168,
mal cells, Hum. Immunol., 71, 235-244, doi: 10.1016/
doi: 10.1161/CIRCRESAHA.118.314669.
J.HUMIMM.2009.12.005.
БИОХИМИЯ том 88 вып. 11 2023
2220
КАРПЕНКО
132. Wu, Q., You, L., Nepovimova, E., Heger, Z., Wu, W.,
damage, Front. Immunol., 12, 713631, doi: 10.3389/
Kuca, K., and Adam, V. (2022) Hypoxia-inducible
fimmu.2021.713631.
factors: master regulators of hypoxic tumor immune
138. Proics, E., David, M., Mojibian, M., Speck, M.,
escape, J. Hematol. Oncol., 15, 77, doi: 10.1186/
Lounnas-Mourey, N., et al. (2023) Preclinical assess-
S13045-022-01292-6.
ment of antigen-specific chimeric antigen receptor
133. Newman, H., Shih, Y. V., and Varghese, S. (2021) Res-
regulatory t cells for use in solid organ transplanta-
olution of inflammation in bone regeneration: from un-
tion, Gene Ther., 30, 309-322, doi: 10.1038/S41434-
derstandings to therapeutic applications, Biomaterials,
022-00358-X.
277, 121114, doi: 10.1016/j.biomaterials.2021.121114.
139. Alanazi, R. F., Alhwity, B. S., Almahlawi, R. M.,
134. Song, X., Zhang, Y., Zhang, L., Song, W., and Shi, L.
Alatawi, B. D., Albalawi, S. A., Albalawi, R. A.,
(2018) Hypoxia enhances indoleamine 2,3-dioxygenase
Albalawi, A. A., Abdel-Maksoud, M. S., and
production in dendritic cells, Oncotarget, 9, 11572-
Elsherbiny, N. (2023) Multilineage differentiating stress
11580, doi: 10.18632/ONCOTARGET.24098.
enduring (Muse) cells: a new era of stem cell-based
135. Matheakakis, A., Batsali, A., Papadaki, H. A., and
therapy, Cells, 12, 1676, doi: 10.3390/cells12131676.
Pontikoglou, C. G. (2021) Therapeutic implications
140. Kushioka, J., Chow, S. K. H., Toya, M., Tsubosaka, M.,
of mesenchymal stromal cells and their extracellular
Shen, H., Gao, Q., Li, X., Zhang, N., and Goodman,
vesicles in autoimmune diseases: from biology to
S. B. (2023) Bone regeneration in inflammation with
clinical applications, Int. J. Mol. Sci., 22, 10132,
aging and cell-based immunomodulatory therapy, In-
doi: 10.3390/IJMS221810132.
flamm. Regen., 43, 29, doi: 10.1186/S41232-023-00279-1.
136. Petinati, N., Kapranov, N., Davydova, Y., Bigildeev, A.,
141. Akhbariyoon, H., Azizpour, Y., Esfahani, M. F.,
Pshenichnikova, O., Karpenko, D., Drize, N.,
Firoozabad, M. S. M., Rad, M. R., Esfahani, K. S.,
Kuzmina, L., Parovichnikova, E., and Savchenko, V.
Khoshavi, N., Karimi, N., Shirinisaz, A., Abedi, F.,
(2020) Immunophenotypic characteristics of multipo-
Rad, M. R., and Sharifi, P. (2021) Immune checkpoint
tent mesenchymal stromal cells that affect the efficacy
inhibition for the treatment of cancers: an update and
of their use in the prevention of acute graft vs host dis-
critical review of ongoing clinical trials, Clin. Immu-
ease, World J. Stem Cells, 12, 1377-1395, doi: 10.4252/
nol., 232, 108873, doi: 10.1016/J.CLIM.2021.108873.
WJSC.V12.I11.1377.
142. Kong, X.
(2020) Discovery of new immune
137. Ara, T., and Hashimoto, D. (2021) Novel insights
checkpoints: family grows up, Adv. Exp. Med. Biol.,
into the mechanism of GVHD-induced tissue
1248, 61-82, doi: 10.1007/978-981-15-3266-5_4.
IMMUNE PRIVILEGES AS A RESULT OF MUTUAL REGULATION
OF THE IMMUNE AND STEM SYSTEMS
Review
D. V. Karpenko
Laboratory of Epigenetic regulation of hematopoiesis, National Medical Research Center for Hematology,
125167 Moscow, Russia; e-mail: d_@list.ru
The immune privileges of cancer stem cells are a well-known and widely studied problem, as the presence
of such cells in tumors is associated with refractoriness, recurrence, and metastasis. Accumulating evidence
also suggests the presence of immune privileges for non-pathologic stem cells in addition to their other
defense mechanisms against damaging factors. This similarity between pathologic and normal stem cells
raises the question of why stem cells have such a potentially damaging property. The regulation of vital pro-
cesses of autoimmunity control and regeneration by interactions between immune cells, stem cells and their
microenvironment are reviewed as determinants of stem cell immune privilege formation. A deep mutual
integration in the regulation of stem and immune cells is noted. Based on the diversity and complexity of
the mutual regulation of stem cells, their microenvironment and the immune system, I propose to use the
term “stem system”.
Keywords: autoimmunity, regeneration, stem cell, cancer stem cell, stem system, immune privileges, nestin
БИОХИМИЯ том 88 вып. 11 2023