БИОХИМИЯ, 2023, том 88, вып. 8, с. 1313 - 1336
УДК 577.25
ВЛИЯНИЕ СВЕРХЭКСПРЕССИИ ДОФАМИНОВОГО
НЕЙРОТРОФИЧЕСКОГО ФАКТОРА МОЗГА (CDNF)
В ГИППОКАМПЕ НА ПОВЕДЕНИЕ МЫШЕЙ
С ГЕНЕТИЧЕСКОЙ ПРЕДРАСПОЛОЖЕННОСТЬЮ
К ДЕПРЕССИВНО-ПОДОБНОМУ ПОВЕДЕНИЮ
© 2023 Я.П. Каминская, Т.В. Ильчибаева, Н.В. Хоцкин, В.С. Науменко, А.С. Цыбко*
Федеральный исследовательский центр Институт цитологии и генетики СО РАН,
630090 Новосибирск, Россия; электронная почта: antoncybko@mail.ru
Поступила в редакцию 08.04.2023
После доработки 08.06.2023
Принята к публикации 09.06.2023
Дофаминовый нейротрофический фактор мозга (CDNF) является перспективным средством для
лечения болезни Паркинсона. Однако его роль в регуляции немоторного поведения, в том числе
в разного рода психопатологиях, остаётся неясной. В связи с этим целью настоящей работы
было изучение влияния сверхэкспрессии CDNF в гиппокампе на поведение мышей линии ASC
(Antidepressant Sensitive Cataleptics) с генетической предрасположенностью к депрессивно-подоб-
ному поведению. Сверхэкспрессию CDNF в нейронах гиппокампа мышей индуцировали с помо-
щью аденоассоциированного вирусного вектора (AAV). Через 4 недели после стереотаксической
инъекции вектора AAV-CDNF в дорсальный гиппокамп оценивалось поведение в условиях домаш-
ней клетки, исследовательское, тревожно-подобное и депрессивно-подобное поведение, а также
пространственное и ассоциативное обучение. Мы обнаружили значительные улучшения в дина-
мике пространственного обучения в водном лабиринте Морриса у животных со сверхэкспрес-
сией CDNF. В то же время не было обнаружено эффекта CDNF на другие исследованные формы
поведения. Поведение опытных животных в условиях домашней клетки не отличалось от такового
в контрольной группе, за исключением снижения общего количества съеденной пищи и некоторо-
го увеличения количества эпизодов сна в светлую фазу суток. В данном исследовании также была
предпринята попытка определить молекулярную основу упомянутых выше изменений посредством
экспрессионного анализа. Нами не было обнаружено значительных изменений в уровне мРНК
генов, кодирующих рецепторы основных нейротрансмиттерных систем, вовлечённых в нейроплас-
тичность, выживание нейронов, а также ключевых киназ. Однако у животных со сверхэкспрессией
CDNF было выявлено повышение уровня мРНК сплайсированной формы Xbp, что может гово-
рить об активации Ire1α/Xbp1-пути, традиционно ассоциируемого со стрессом эндоплазматиче-
ского ретикулума (ЭПР). С помощью иммуногистохимического анализа было показано, что СDNF
колокализован с маркером ЭПР кальретикулином. Таким образом, обнаруженные нами эффекты
CDNF на поведение могут быть опосредованы специфическим молекулярным каскадом, что под-
чёркивает его отличие от классических нейротрофических факторов.
КЛЮЧЕВЫЕ СЛОВА: нейротрофические факторы, дофаминовый нейротрофический фактор мозга
CDNF, депрессивно-подобное поведение, обучение, стресс ЭПР, реакция несвёрнутых белков UPR.
DOI: 10.31857/S0320972523080031, EDN: IHUIUU
ВВЕДЕНИЕ
но, в 2007 году, но с тех пор привлёк большое
внимание исследователей. Известно, что CDNF
Дофаминовый нейротрофический фак-
значительно отличается от других нейро-
тор мозга (cerebral dopamine neurotrophic fac-
трофических факторов (НТФ). Так, его го-
tor, CDNF) был открыт относительно недав- мология с астроцитарным мезэнцефальным
Принятые сокращения: БП - болезнь Паркинсона; НТФ - нейротрофические факторы; ЭПР - эндоплазматический
ретикулум; AAV - аденоассоциированный вирусный вектор; ASC - линия мышей с генетической предрасположенно-
стью к депрессивно-подобному поведению; CDNF - дофаминовый нейротрофический фактор мозга; IRE1α - эндори-
бонуклеаза инозитол-требующий фермент 1 α; MANF - мезэнцефалический астроцитарный нейротрофический фактор;
UPR - реакция развёрнутых белков; XBP1 - X-box-связывающий белок.
* Адресат для корреспонденции.
1313
3
1314
КАМИНСКАЯ и др.
НТФ (MANF) составляет 59%, а с другими
мального и патологического поведения. Было
НТФ гомология не прослеживается; CDNF
проведено небольшое количество исследова-
не связывается с общими для остальных НТФ
ний, призванных установить влияние CDNF
рецепторами, не имеет проформы [1]. Кроме
на поведение животных, но зачастую исследо-
того, для него не были идентифицированы
ватели ограничивались лишь оценкой мотор-
рецепторы на клеточной мембране, что позво-
ного поведения на различных моделях БП.
лило выделить его и MANF в отдельное семей-
Интересно, что нокаут гена Cdnf на мышах
ство. Оба этих белка имеют двойственную
не привёл к существенным различиям в базо-
природу и могут как секретироваться клеткой,
вой двигательной активности, привыкании к
так и оказывать протективное действие изну-
новой среде, депрессивно-подобном или тре-
три, «заякореваясь» в мембране эндоплазмати-
вожно-подобном поведении [12]. В то время
ческого ретикулума (ЭПР) [2].
как у рыбок Danio rerio нокаут гена Cdnf вызы-
Повышенный интерес к CDNF связан в
вает нарушение социального поведения, сни-
первую очередь с его нейропротекторными
жение тревожности и повышение судорожной
свойствами. Принято выделять два механизма,
активности. Более того, у таких мутантных по
которые их обеспечивают. Первый обуслов-
гену Cdnf рыбок были зафиксированы наруше-
лен нахождением белка в просвете ЭПР и
ния не только со стороны дофаминовой систе-
заключается в модуляции реакции несвёрну-
мы, но и дефицит ГАМКергических и гиста-
тых белков (unfolded protein response, UPR),
минергических нейронов, что подтверждает
которая позволяет избежать стресса ЭПР и
роль CDNF как универсального регулятора
нейровоспаления. Второй же механизм пред-
нейрогенеза, необходимого для формирования
полагает высвобождение CDNF и его связы-
медиатор-специфических типов нейронов [13].
вание с неидентифицированным рецептором,
Ранее было показано, что введение в гиппо-
активирующим внутриклеточные сигналь-
камп CDNF или трансгена CDNF улучшает
ные каскады. Рекомбинантный белок CDNF
долговременную память, не влияя на исследо-
проявил выраженное нейропротекторное дей-
вательское поведение, неофобию и простран-
ствие на дофаминергические нейроны сред-
ственное обучение в экспериментальной мо-
него мозга в двух фармакологических моделях
дели болезни Альцгеймера - у мышей линии
болезни Паркинсона (БП): на получавших
APP/PSI [14]. Кроме того, было показано, что
6-гидроксидофамин (6-OHDA) крысах [1, 3]
CDNF способен активировать PI3K/Akt-сиг-
и получавших 1-метил-4-фенил-1,2,3,6-тетра-
нальный путь как in vitro, так и in vivo, причём
гидропиридин (MPTP) мышах [4]. Позже ней-
даже в неповреждённом мозге [15]. Поскольку
ропротекторный эффект CDNF был показан
указанный сигнальный путь является необ-
также на получавших 6-OHDA мармозетках,
ходимым компонентом процесса долговремен-
однако он оказался менее выраженным, чем
ной потенциации, можно предположить, что
у грызунов [5].
CDNF принимает самое активное участие в
Описанные выше отличительные особен-
процессах нейропластичности, связанных с
ности CDNF продиктованы его молекуляр-
обучением и памятью. Учитывая, что гиппо-
ной структурой. В структуре CDNF выделяют
камп, особенно его дорсальная часть, - кри-
неструктурированный C-конец и глобулярный
тически важная структура для обучения [16],
N-конец, которые соединены гибким линке-
памяти [17], пространственной навигации [18]
ром [6]. N-Конец содержит сигнальную по-
и регуляции настроения [19] - большой инте-
следовательность, необходимую для трансля-
рес представляет изучение функций CDNF в
ции в ЭПР, а также сапозиноподобный домен,
регуляции гиппокамп-зависимого поведения.
способный контактировать с мембранами и
Однако на сегодняшний день этот аспект оста-
липидами [2, 7]. На C-конце, в свою очередь,
ётся малоизученным. Также ничего не извест-
у CDNF находится последовательность, ответ-
но об участии CDNF в механизмах депрессии
ственная за удержание CDNF в просвете ЭПР
и действия антидепрессантов.
(ER retention sequence; ERS) [8, 9]. C-Конце-
Линия мышей ASC (Antidepressant Sensi-
вой мотив CXXC традиционно ассоциируют
tive Catalepsy) была выведена путём длитель-
с цитопротекторным и антиапоптотическим
ной селекции на высокую предрасположен-
действием, в то время как наличие N-терми-
ность к каталепсии популяции беккроссов
нального домена предполагает нейротрофные
(СВА × (СВА × AKR)) от скрещивания чувстви-
функции [10, 11].
тельной (СВА) и устойчивой (AKR) к каталеп-
Однако нейротрофические функции CDNF
сии линий [20, 21]. Мыши линии ASC демон-
остаются слабо изученными. В первую оче-
стрировали каталептическое замирание [22], ко-
редь это касается его роли в регуляции нор-
торое значительно снижалось при хроническом
БИОХИМИЯ том 88 вып. 8 2023
CDNF КАК РЕГУЛЯТОР ПОВЕДЕНИЯ
1315
введении классических антидепрессантов ими-
В группе, получавшей AAV-EGFP, - 11 жи-
прамина и флуоксетина [23, 24]. Было установ-
вотных; в группе, получавшей AAV-СDNF, -
лено, что, в отличие от родительских линий,
11 животных.
для ASC характерно увеличение неподвиж-
Второй этап: введение вирусного вектора,
ности в тестах «принудительное плавание» и
кодирующего целевой белок или флуорес-
тесте «подвешивание за хвост», а также сни-
центную метку, и тестирование животных для
жение двигательной активности, что интер-
определения депрессивно-подобного, тревож-
претируется как депрессивно-подобное пове-
но-подобного, исследовательского поведения,
дение [25]. Подтверждением валидности моде-
а также пространственного обучения. Размер
ли ASC является также снижение депрессивно-
выборки в каждой группе n ≥ 8.
подобного поведения в ответ на внутрижелудоч-
Дополнительно было оценено депрессив-
ковое введение рекомбинантного BDNF [26],
но-подобное поведение в тесте принудительно-
которому в настоящее время отводится одно
го плавания, и так как этот тест обладает выра-
из ключевых мест в механизме депрессивных
женным стрессирующим воздействием, данный
расстройств [27-29]. Кроме того, мыши ли-
тест был проведён отдельно - третьим этапом.
нии ASC демонстрируют повышенную тре-
В группе, получавшей AAV-EGFP, - 6 живот-
вожность по сравнению с родительской ли-
ных; в группе, получавшей AAV-СDNF, - 7 жи-
нией [30]. Таким образом, линия мышей ASC
вотных.
была предложена в качестве новой живот-
Животные. Эксперименты проводились на
ной модели для изучения механизмов депрес-
взрослых самцах мышей линии ASC, которая
сии [26], действия антидепрессантов и хорошо
была выведена путём длительной селекции на
подходит для исследования эффектов CDNF в
предрасположенность к каталепсии в лабора-
контексте патологий поведения.
тории нейрогеномики поведения Института
Целью настоящей работы являлось иссле-
цитологии и генетики СО РАН. Инъекцию
дование эффектов сверхэкспрессии CDNF в
обеим группам животных осуществляли в воз-
гиппокампе на поведение и экспрессию ряда
расте 2 мес.
ключевых генов, вовлечённых в процессы ней-
Животных содержали в ЦКП «SPF-вива-
рональной пластичности у мышей линии ASC
рий» ИЦиГ СО РАН по 4-5 особей в стандарт-
с генетической предрасположенностью к де-
ных лабораторных условиях со свободным до-
прессивно-подобному поведению. Гены-канди-
ступом к воде и пище. За 2 дня до проведения
даты (согласно базе данных KEGG; https://
поведенческих тестов животных рассаживали
в отдельные клетки для снятия групповых эф-
mmu) включали следующие группы: рецепторы
фектов.
основных нейромедиаторных систем (серото-
Плазмиды. В лаборатории был создан и ве-
ниновые, дофаминовые, глутаматные); белки,
рифицирован аденоассоциированный вирусный
вовлечённые в нейропластичность (Arc, c-Fos,
вектор, несущий плазмиду pAAV-Syn-CDNF-
Syn, Bdnf); белки, регулирующие выживание
EGFP, которая кодируeт ген Cdnf мыши, а также
нейронов (Bax, Bcl-xl); белки системы протео-
зелёный флуоресцентный белок (EGFP), необ-
стаза (Atf6, Grp78, Perk, Ire1α); транскрипцион-
ходимый для контроля эффективности экс-
ные факторы (Creb, Nfκb, Xbp1); а также кина-
прессии плазмиды в нейронах млекопитающих.
зы (Akt1, Mapk3, Pik3r1, Kalrn).
Контрольная группа получала аналогичный век-
тор, кодирующий только EGFP. Карты плазмид
AAV-Syn-Cdnf-EGFP и AAV-Syn-EGFP, исполь-
МАТЕРИАЛЫ И МЕТОДЫ
зованных в настоящем исследовании, показаны
на рис. 2, а. Все этапы клонирования были про-
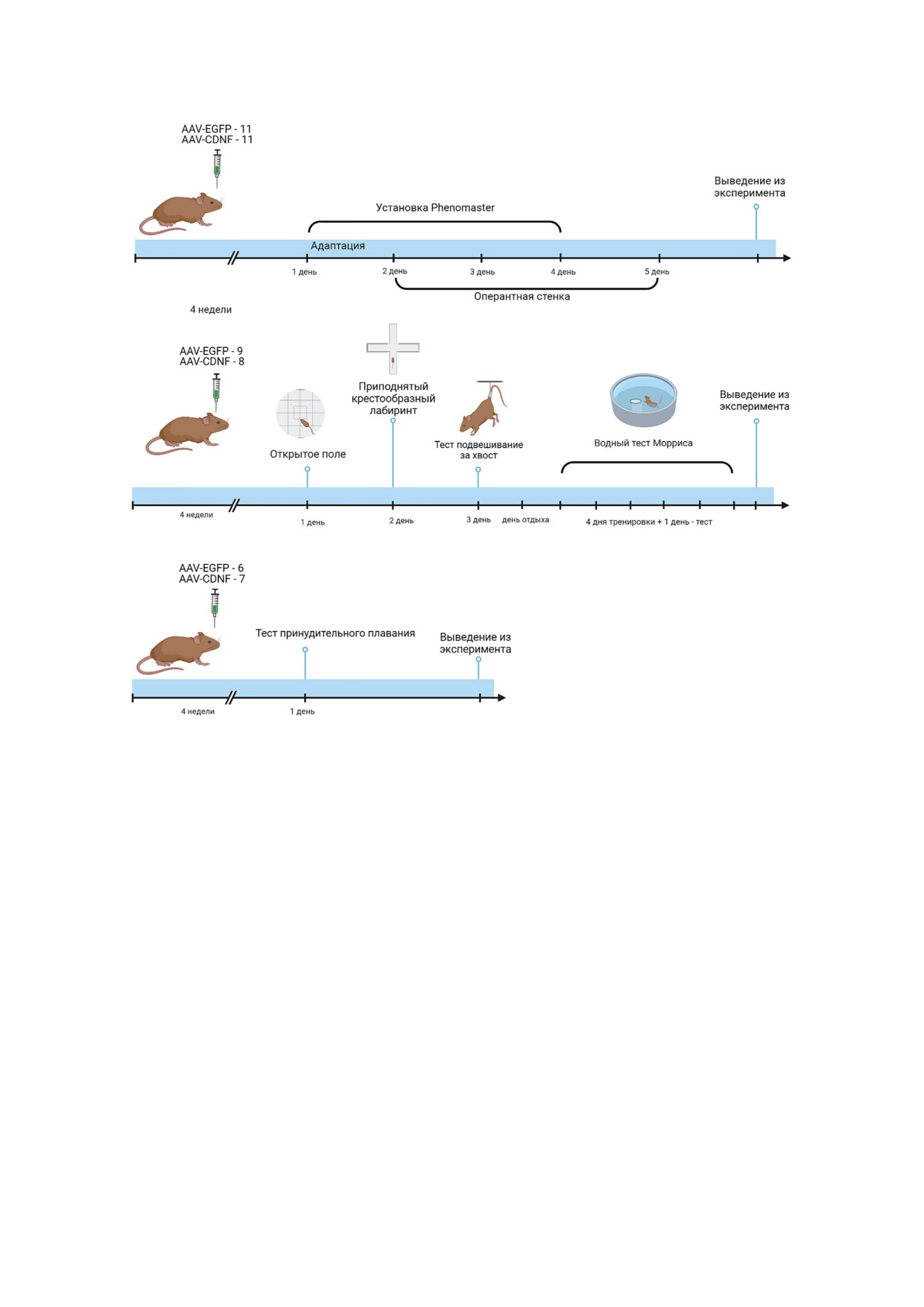
Дизайн эксперимента. Эксперимент про-
верены секвенированием по Сэнгеру.
изводился в три этапа (рис. 1). Первый этап:
Клеточная культура и трансфекция. Клетки
введение аденоассоциированного вирусного
HEK 293FT # PTA-5077 («ATCC», США) ис-
вектора (AAV), кодирующего целевой белок
пользовали для получения векторов рекомби-
или флуоресцентную метку, и тестирование
нантного аденоассоциированного вируса.
животных в условиях домашней клетки спустя
Линию клеток поддерживали в среде
4 недели с момента инъекции. Такой времен-
DMEM, содержащей 10% FBS («Sigma-Aldrich»,
ной промежуток после введения AAV являет-
США) и 100 ед./мл пенициллина/стрептоми-
ся оптимальным для достаточной наработки
цина («Sigma-Aldrich»), при 37 °C в атмосфере
исследуемого белка и подобран на основании
5% CO2. Клетки пассировали при конфлюент-
литературных данных
[31] и исследований,
ности не менее 70%, и культуральную среду
проводившихся в нашей лаборатории [32, 33].
обновляли каждые 2-3 дня.
БИОХИМИЯ том 88 вып. 8 2023
3*
1316
КАМИНСКАЯ и др.
Рис. 1. Дизайн эксперимента. Мышам опытной группы стереотаксически вводили в гиппокамп pAAV-Syn-Cdnf-EGFP
(экспрессирующую Cdnf), в гиппокамп мышей контрольной группы вводили pAAV-Syn-EGFP (экспрессирующую
только EGFP). Через 4 недели мышей изолировали в индивидуальные клетки и затем проводили поведенческие тесты
Аденоассоциированные вирусы. Упаковку
ляли в месте инъекции ещё на 2 мин, чтобы
AAV-Syn-Cdnf-EGFP и AAV-Syn-EGFP в кап-
минимизировать утечку вирусной суспензии
сиды AAV проводили путём котрансфекции
при извлечении иглы. До начала эксперимента
с плазмидами AAV-DJ и pHelper («Cell Bio-
6 животным линии ASC была сделана пробная
labs Inc.», США) в HEK-клетки. Количество
стереотаксическая инъекция AAV-EGFP в гип-
полученных вирусных частиц определяли ме-
покамп, чтобы с помощью дальнейшего мор-
тодом количественной ПЦР (кПЦР).
фологического контроля убедиться в правиль-
Стереотаксическое введение в гиппокамп.
ности выбранных координат.
Перед проведением процедуры животных нар-
Экстракция образцов мозга. Мыши были
котизировали смесью
2,2,2-трибромэтанола
декапитированы через 24 ч после тестирова-
и 2-метил-2-бутанола; после разрезания кожи
ния поведения. Мозг был извлечён в тот же
на черепе помещали в стереотаксическую уста-
день (12:00-14:00) на льду, образцы целого
новку («TSE Systems», Германия). Далее че-
гиппокампа были выделены в соответствии
реп билатерально просверливали, согласно ко-
с онлайн-атласом мышиного мозга (https://
ординатам AP: -2,0 мм; ML: 1,5 мм; DV: 2,0 мм
scalablebrainatlas.incf.org/mouse/ABA_v3), замо-
рожены в жидком азоте и хранились при темпе-
1.5&ap=-2&dv=2). Вирусные частицы (1 мкл),
ратуре -80 °C до процедур выделения РНК или
разведённые в 1× PBS до концентрации 109 ви-
вестерн-блот-анализа. Для анализа экспрес-
русных частиц в мкл, медленно вводили микро-
сии генов интереса использовались образцы
шприцем в гиппокамп со скоростью 0,1 мкл/мин
мозга животных второго этапа, прошедших по-
в течение 10 мин. После инъекции иглу остав-
веденческое тестирование. Так как инъекции
БИОХИМИЯ том 88 вып. 8 2023
CDNF КАК РЕГУЛЯТОР ПОВЕДЕНИЯ
1317
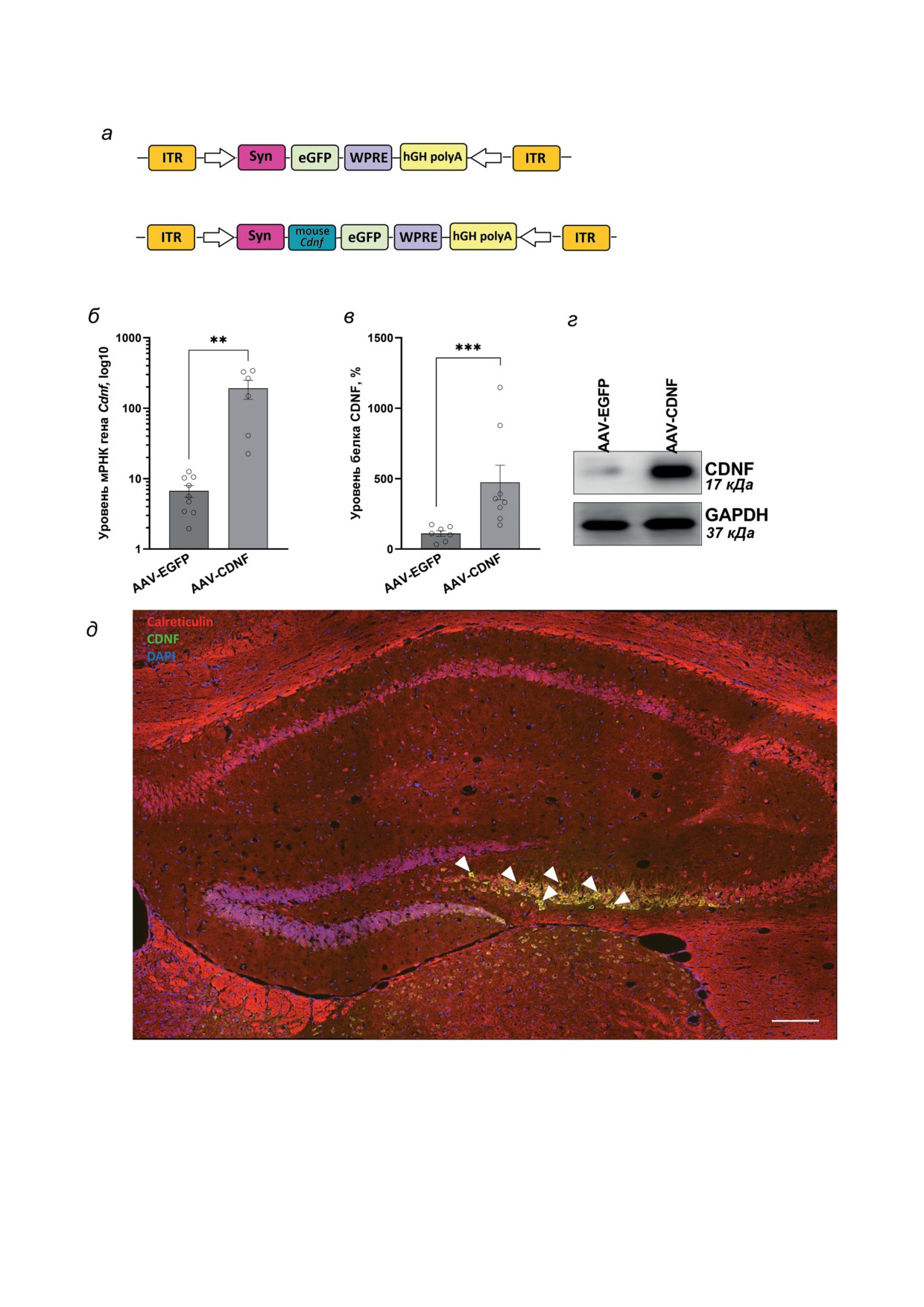
Рис. 2. Сверхэкспрессия CDNF в гиппокампе мышей ASC. а - Карты плазмид pAAV-Syn-EGFP и pAAV-Syn-Cdnf-EGFP.
б - Уровень мРНК гена Cdnf. в - Количественная оценка интенсивности хемилюминесцентного сигнала для бел-
ка CDNF, и результат иммуноблота на мембране (г). Число копий кДНК гена отнесено на 100 копий кДНК rPol2.
Уровни белка представлены в относительных единицах, нормализованных на соответствующий уровень GAPDH.
** p < 0,01; *** p < 0,005 - по сравнению с контролем. д - Совместная локализация кальретикулина и трансдуци-
рованного CDNF в CA3-области и зубчатой извилине гиппокампа (масштабная линейка - 100 мкм). Срезы гиппо-
кампа подвергали иммуногистохимическому окрашиванию для обнаружения CDNF (зелёный) и кальретикулина (крас-
ный) с последующей конфокальной микроскопией. Ядра показаны синим цветом. Колокализация показана жёлтым
цветом, наиболее репрезентативные клетки отмечены стрелками
БИОХИМИЯ том 88 вып. 8 2023
1318
КАМИНСКАЯ и др.
вирусного вектора осуществлялись билате-
Экспрессию генов представляли как отноше-
рально, определение уровней мРНК и белка
ние количества копий кДНК анализируемого
проводили по отдельности, используя левую
гена к 100 копиям гена rPol2, выполняющего
или правую половины гиппокампа. Образцы
функцию внутреннего стандарта [34-36]. Для
гиппокампа животных первого и третьего эта-
сплайсированной (sXbp) и несплайсирован-
пов эксперимента использовали только для
ной (uXbp) форм Xbp расчёт производился по
определения уровня мРНК с целью подтвер-
методу ΔΔCt с помощью программного обес-
ждения сверхэкспрессии CDNF.
печения амплификатора.
Суммарную РНК выделяли с помощью
Вестерн-блот-анализ. Для определения уров-
ExtractRNA («Евроген», Россия), обрабатывали
ня общего белка образцы ткани гомогенизиро-
ДНКазой без РНКазной активности (RNase
вали («Kimble Chase», США) в 300 мкл лизирую-
free DNase, 1000 о.е./мл; «Promega», США) в
щего буфера, содержащего 100 мМ Tris-HCl
соответствии с протоколами производителей.
(pH 8,4), 300 мМ NaCl, 4мМ EDTA, 0,2% (w/v)
Концентрацию РНК оценивали с помощью
Triton X-100; 1мМ NaVO4, 2 мМ PMSF, 1 мМ
спектрофотометра Eppendorf Nanodrop 2000C
смеси ингибиторов протеаз (химостатин, лей-
(«Thermo Fisher Scientific Inc.», США). РНК раз-
пептин, антипаин, пепстатин; «Sigma-Aldrich»)
водили водой до концентрации 0,125 мкг/мкл и
и ингибиторы фосфотаз (PhosSTOP; «Roche»)
хранили при -80°С.
из расчёта одна таблетка на 10 мл буфера. Го-
Реакция обратной транскрипции. Получен-
могенат инкубировали на льду 60 мин и цен-
ную общую РНК в количестве 1 мг смешивали
трифугировали (12 000 g, 15 мин). Супернатант
с рандомными гексануклеотидными прайме-
белка переносили в чистые пробирки и хра-
рами (конечная концентрация праймера соста-
нили при температуре
-80 °C. Количество
вила 5 мкМ) и 2,25 мкмолями стерильного KCl.
общего белка было измерено по методу BCA
На амплификаторе («БИС», Россия) произво-
с использованием коммерческого набора
дили денатурацию при 94 °C в течение 5 мин и
Pierce BCA Protein Assay Kit («Thermo Fisher
отжиг - при 41 °C в течение 15 мин, после чего
Scientific Inc.»). Пробы разводились до кон-
на льду непосредственно добавляли по 15 мкл
центрации 1500 мкг/мл с помощью 2-кратно-
смеси, содержащей обратную транскриптазу
го буфера Лэммли (2,5 мл буфера Лэммли
M-MLV (200 ед.), а также Tris-HCl (pH 8,3;
получали смешиванием 147 мкл 1 М Tris-HCl
0,225 мкмоль), смесь dNTP (0,015 мкмоль каждо-
(pH 6,8), 470 мкл 10%-ного SDS, 235 мкл гли-
го), DTT (0,225 мкмоль) и MnCl2 (0,03 мкмоль).
церола, 117 мкл 5%-ного β-меркаптоэтанола
Полученную смесь инкубировали при 41 °C в те-
и 1,5 мл воды) и хранились при температуре
чение 60 мин. Синтезированную кДНК хранили
-20 °С. Проводили термическую обработку
при температуре -20 °C.
проб для денатурации белка (5 мин, 95 °С).
Количественная ОТ-ПЦР в реальном вре-
Экстракты белка (15 мкг на дорожку) раз-
мени. ПЦР проводили на амплификаторе
деляли с помощью 10%-ного разделяющего
LightCycler 480 System («Roche», Швейцария).
SDS-PAGE. Для электрофореза использова-
кДНК (1 мкл) смешивали с 19 мкл смеси Master
лась камера Hoefer SE 600 («Hoefer Inc.», США)
mix («Синтол», Россия), приготовленной со-
и источник питания EPS
301
(«Amersham
гласно инструкции производителя. Праймеры,
Pharmacia Biotech», Великобритания). Затем
используемые для амплификации кДНК ис-
белки переносили на нитроцеллюлозную мем-
следуемых генов (табл. 1), разработаны на ос-
брану («Bio-Rad», США) с помощью системы
нове последовательностей, опубликованных в
для полусухого электроблоттинга Trans-Blot
базе данных EMBL Nucleotide database, и син-
Turbo Transfer System («Bio-Rad») в течение
тезированы в компании «БИОССЕТ» (Ново-
2 ч при силе тока 0,9 А. В качестве маркера
сибирск). Серия разведений геномной ДНК с
использовалась смесь Precision Plus Protein
концентрацией 0,0625, 0,125, 0,25, 0,5, 1, 2, 4,
Kaleidoscope Standards («Bio-Rad»).
8, 16, 32, 64 и 128 нг/мкл была амплифициро-
Для иммунодетекции белка мембрану бло-
вана одновременно в отдельных пробирках
кировали 5%-ным сухим обезжиренным моло-
и была использована как внешний экзоген-
ком, разведённом в буфере TBS-T (Tris Bufferd
ный стандарт для построения калибровочной
Saline, «Bio-Rad Laboratories Inc.», США) с до-
кривой. Для контроля специфичности ампли-
бавлением 0,05% (v/v) Tween 20, в течение часа
фикации использовался анализ кривой плав-
при комнатной температуре и инкубировали
ления для каждого прогона каждой пары прай-
с первичными антителами при 4 °C в течение
меров. Калибровочная кривая была построена
ночи (табл. 2).
автоматически программным обеспечением
После первичных антител мембрану отмы-
LightCycler
480
(«Roche Applied Science»).
вали 5 раз по 5 мин буфером TBS-T и инку-
БИОХИМИЯ том 88 вып. 8 2023
CDNF КАК РЕГУЛЯТОР ПОВЕДЕНИЯ
1319
Таблица 1. Нуклеотидные последовательности праймеров и их характеристики
Температура отжига,
Длина ПЦР продукта,
Ген
Нуклеотидная последовательность (5′→3′)
°C
п.н.
F: CTGTGACCTGTTTATCGCCCTG
Htr1a
62
109
R: GTAGTCTATAGGGTCGGTGATTGC
F: AGAAGCCACCTTGTGTGTGA
Htr2a
61
169
R: TTGCTCATTGCTGATGGACT
F: AGAAAAGGTGGCAATGCTGG
Htr2b
59
120
R: TTAGAAATGGTTTGGGCTGATCT
F: GGCTACACGATCTACTCCACCG
Htr7
65
198
R: CGCACACTCTTCCACCTCCTTC
F: TGCCAGCTGATGAAGACAGA
Akt-1
60
120
R: CCATTCTTCCCGCTCCTCAG
F: ATCTGTTGACCGAAGTGTCCAAG
Arc
64
218
R: GAAGACCTCCCTCCACACGT
F: CTCAAACCAATGCCAGTGTCC
Atf6
59
94
R: ATGCTGATAATCGACTGCTGC
F: GACATCACCTACCGCTTCCG
Avpr1a
60
192
R: CCAAGAGGCGGCGATCAT
F: CATCTTTGTGGCTGGAGTCCTC
Bax
64
216
R: AAGTGGACCTGAGGTTTATTGGC
F: TGGATCTCTACGGGAACAATGC
Bcl-xl
64
197
R: GTGGCTGAAGAGAGAGTTGTGG
F: TAGCAAAAAGAGAATTGGCTG
Bdnf
59
255
R: TTTCAGGTCATGGATATGTCC
F: CGGTGGACCTGTGGAAGATG
Cdnf
60
130
R: ACATATTTGGGGGCCAGCTC
F: AAAGAGAAGGAAAAACTGGAG
c-Fos
58
264
R: CGGAAACAAGAAGTCATCAA
F: GCTGGCTAACAATGGTACGGAT
Creb
64
140
R: TGGTTGCTGGGCACTAGAAT
F: GGAAACCCTGTCGAATGCTCTC
Drd1
64
195
R: CAGCCAAACCACACAAATACATCG
F: TCCGCCACTTCTTGACATACATTG
Drd2
64
132
R: CCCATCCACAGCCTCCTCTAAG
F: CAATGAAGCCATACGGACATCG
Gria1
60
121
R: GGATTGCATGGACTTGGGGA
F: GTGTTTGTGAGGACTACGGC
Gria2
60
125
R: TTCATGGTGTCGCAAGGCT
F: GACTCGCTGGAAACACCCTT
Grik1
60
141
R: TCTTCGTACACCACCGTCAC
F: AGGAGACAGTCTGTGCTTGTC
Grik2
60
137
R: CCACCAATCTGCGTGAGGT
F: TTTTCTCCTGCTCCTTCGCC
Grin1
60
124
R: TGTCGCTTATTGGCCTGGTT
F: TGAACCGCACTGACCCTAAG
Grin2a
60
107
R: CACAGCCTCTTGGTCCGTAT
БИОХИМИЯ том 88 вып. 8 2023
1
320
КАМИНСКАЯ и др.
Таблица 1 (продолжение)
Температура отжига,
Длина ПЦР продукта,
Ген
Нуклеотидная последовательность (5′→3′)
°C
п.н.
F: CTATCACCATCACCACCGGC
Grin2b
60
210
R: TCATCATGGCCACTGTAGCG
F: CGCACACTCGGACAAAATCT
Grm1
59
177
R: AGTGAGAACTCTCCCACGAC
F: GGAACAACAGCAGGAACCCT
Grm2
60
146
R: CACGGCATTGACCACAAACAT
F: AGCAAGGCTACGCAACATCT
Grm3
60
196
R: CACCCAGGTGAAGGAAGCAT
F: GAGCGGAAGAAGACGGTGAA
Grm4
60
157
R: TGACAATGGGTATGGGCTGG
F: CCCACACTCTTGCCCAACAT
Grm5
60
141
R: ACAGCGTACCAAGCCTTCTT
F: CGCTCTACCATGAAGCCTGT
Grp78
60
174
R: AGCCTCATCGGGGTTTATGC
F: TCTGGGGATGTCCTGTGGAT
Ire1α
60
195
R: CTTGGCCTCTGTCTCCTTGG
F: CATGGTGTCTGTGGAGGGC
Kalrn
60
137
R: CCGCACTGTTGAAGAACTCC
F: TGCCCTCGAAAACCAAGGTG
Mapk3
61
195
R: CGAAGGTGAATGGCTCCTCG
F: CGTCTGTCTGCTCTCTCTCGAC
Nfκb1
62
152
R: CTCGCCTCGGTACTTCTCTCTC
F: ACAACAGTGACTCAGCGGAC
Perk
60
194
R: GCAGCCAGAGTCCTCAAACA
F: TCCGAAAGACTCTAGCCTTGG
Pik3r1
60
132
R: CATGCTGCTTGATGGTGTGG
F: TTCTACTCCAAGAAGTCGCAGC
Plcg1
61
104
R: GACCCCTCGATTTTGTCCGC
F: GTTGTCGGGCAGCAGAATGTAG
rPol2
61
188
R: TCAATGAGACCTTCTCGTCCTCC
sXbp1
F: GCTGAGTCCGCAGCAGGT
60
130
(кДНК)
R: CAGGGTCCAACTTGTCCAGAAT
F: GTTGGTGACTACTCCTCCTCG
Syp
60
127
R: GCCCTTTGTTGTTCTCTCGGTA
F: CAGACTACGTGCACCTCTGC
uXbp1
60
139
R: CAGGGTCCAACTTGTCCAGAAT
бировали со вторичными поликлональными
соответствии с инструкцией производителя, и
антителами (табл. 2), конъюгированными с
сканера C-Digit Blot Scanner («Li-Cor», США).
пероксидазой хрена, при комнатной темпера-
Для каждой мембраны проводилось измере-
туре в течение часа. Затем мембрану снова от-
ние конститутивного белка GAPDH в каче-
мывали 5 раз по 5 мин буфером TBS-T.
стве внутреннего стандарта для дальнейшей
Связанные антитела визуализировались с
нормировки. Экспрессия белка выражалась в
помощью Clarity Western ECL («Bio-Rad»), в относительных единицах. Плотность бендов
БИОХИМИЯ том 88 вып. 8 2023
CDNF КАК РЕГУЛЯТОР ПОВЕДЕНИЯ
1321
Таблица 2. Характеристики используемых в работе антител
Первичные антитела
Вторичные антитела:
Белок
разведение, шифр производителя
Разведение
Шифр производителя
CDNF
1 : 500
Pag458Mu01 («CloudClone», США)
CREB
1 : 1000
Ab 3138 («Abcam», Великобритания)
Против кролика 1 : 10 000
pCREB
1 : 1000
Ab 32096 («Abcam»)
G-21234 («Invitrogen», США)
MAPK
1 : 1000
Ab 17942 («Abcam»)
p-MAPK
1 : 1000
9101 («Cell Signaling Technology», США)
сFos
1 : 500
Sc-52 («Santa Cruz», США)
Против кролика 1 : 8000
G-21234 («Invitrogen»)
p-cFos
1 : 1000
D82c12 («Cell Signaling Technology»)
GAPDH
1 : 10000
Ab 8245 («Abcam»)
Против мыши 1 : 30 000 ab6728 («Abcam»)
определялась с помощью денситометрии для
Поведенческие тесты. Тесты в условиях
количественной оценки содержания белка при
домашней клетки. В течение 96 ч с помощью
помощи программы Image Studio Lite 5.2.
установки PhenoMaster («TSE Systems») авто-
Иммунофлуоресцентный анализ. Спустя
матически регистрировались такие физиологи-
4 недели после инъекции животных транскар-
ческие показатели, как: пройденный путь (м),
диально перфузировали фосфатно-солевым бу-
потребление пищи (г) и воды (мл), время и
фером (PBS) и 4%-ным раствором параформ-
число эпизодов сна (мин). Неподвижность
альдегида. Мозг извлекали и постфиксировали
животного оценивалась периодами по 10 с, и
4%-ным параформальдегидом на 6 ч, затем по-
программа считала животное спящим, если
гружали в 30%-ный раствор сахарозы в PBS
фиксировала 4 периода неподвижности под-
на 2 дня. Последовательные срезы толщиной
ряд (равнозначно одному эпизоду сна). Таким
8 мкм делали в криостате («Thermo Scientific»,
образом, программное обеспечение установки
США). Пермеабилизацию проводили погруже-
PhenoMaster определяло состояние сна как не-
нием в 0,3%-ный раствор Triton X-100 (T8787,
подвижность в течение 40 с и более.
«Sigma-Aldrich») на 30 мин. Неспецифическое
В течение 3 дней у животных исследо-
связывание блокировали
5%-ной нормаль-
вали когнитивные способности с помощью
ной ослиной сывороткой («Sigma-Aldrich») и
теста «оперантная стенка». Начало теста все-
0,1%-ным Triton X-100 в PBS в течение 1 ч при
гда совпадало с началом периода активного
комнатной температуре. Инкубацию с анти-
бодрствования животных, сигналом служил
телами anti-Calreticulin
[FMC 75]
(1 : 1000,
свет лампочки, встроенной в модуль. Модуль
ab22683,
«Abcam») и anti-CDNF
(1 : 1000;
был запрограммирован таким образом, что
«Icosagen AS», Эстония), разведённым в PBS,
на первый день животное получало простей-
проводили в течение ночи при 4 °C. После про-
шую задачу - получить вознаграждение в виде
мывания в PBS наносили вторичные антитела
сладкой гранулы, совершая тычок носом в
с флуоресцентными метками на 1 ч при ком-
отверстие, помеченное горящей лампочкой.
натной температуре (1 : 400, #711-545-152 Alexa
На второй день задача усложнялась - теперь,
Fluor® 488 AffiniPure Donkey Anti-Rabbit IgG и
чтобы получить вознаграждение, необходимо
1 : 200 #A-21203 Donkey anti-Mouse IgG (H + L)
было выполнить тычки носом в 2 помеченных
Highly Cross-Adsorbed Secondary Antibody, Alexa
светом отверстия. На третий день задача не
Fluor 594). Ядра клеток окрашивали раство-
отличалась от предыдущего, однако отверстия
ром бис-бензимида (краситель Hoechst 33258
уже не были помечены светом - животное
(5 мкг/мл в PBS); «Sigma-Aldrich»). Срезы по-
должно было само вспомнить необходимую
мещали в монтирующую среду (Fluoromount G;
последовательность действий.
«Associates Biotechnology Southern», США) с
Продолжительность тестирования каждый
последующим микроскопическим анализом с
день составляла не более 120 мин. Окончание
использованием конфокального микроскопа
теста наступало, когда животное получало все
Olympus IX83P2ZF («Olympus Corp.», Япония).
гранулы (всего 10 штук), либо автоматически,
БИОХИМИЯ том 88 вып. 8 2023
1
322
КАМИНСКАЯ и др.
по истечении указанного интервала. Запись
закрытых рукавах, а также исследованная пло-
параметров начиналась после первого тычка в
щадь рукавов. Число выглядываний из закры-
отверстие.
того рукава и свешивания с края арены под-
Для нижеописанных тестов для снятия
считывались вручную.
групповых эффектов за 2 дня до эксперимен-
Тест принудительного плавания (forced swim
тов животных рассаживали в индивидуальные
test). Мышь помещали в прозрачный стеклян-
клетки.
ный цилиндр диаметром 15 и высотой 25 см,
Тест «открытое поле» (open field). Уста-
наполненный водой (t = 25 °С). После 2-минут-
новка для этого теста представляет собой аре-
ного периода адаптации, в течение 4 мин авто-
ну с диаметром 40 см и высотой стенок 25 см.
матически регистрировалась подвижность, а
Полупрозрачный пол освещался снизу двумя
также вручную регистрировалась неподвиж-
галогеновыми лампами мощностью
12 Вт,
ность животного с помощью оригинального
расположенными на 40 см ниже. Испытуе-
программного обеспечения «EthoStudio». Для
мое животное помещали около стенки арены
расчёта уровня подвижности программа изме-
и тестировали в течение 5 мин. С помощью
ряла скорость изменения силуэта животного,
оригинального программного обеспечения
которая определялась как количество пиксе-
«EthoStudio» проводилась автоматическая ре-
лей, связанных с животным, изменённых ме-
гистрация общей длины пройденного пути,
жду двумя соседними кадрами [38, 39].
площади покрытия арены и времени, прове-
Водный лабиринт Морриса (Morris water
дённого в центре арены (диаметр 20 см) [37].
maze). Установка для теста представляла собой
Число вертикальных стоек и эпизоды умыва-
круглый бассейн диаметром 110 см со стенками
ния подсчитывались вручную.
высотой 30 см. Бассейн заполняли водой (тем-
Тест «подвешивание за хвост» (tail suspension
пература - 25 °C, высота столба воды - ~15 см)
test). Установка представляет собой горизон-
и добавляли сухое молоко для непрозрачности.
тальную штангу, расположенную на высоте
В программе «EthoStudio» установка делилась
30 см, на которой с помощью липкой ленты
на 4 сектора. Стеклянная платформа диамет-
животные фиксируются за хвост. В этом по-
ром 6 см помещалась в геометрический центр
ложении животные не могут сбежать или же
нижнего правого сектора так, что она оказы-
ухватиться за ближайшие поверхности. Чтобы
валась на 0,5 см ниже уровня воды, становясь
предотвратить карабканье животных по хво-
невидимой для животных. На ближайшую
сту, на него надевается пластиковый гладкий
к платформе стену бассейна клеили чёрный
цилиндр. При подвешивании мыши за хвост
прямоугольник размером 6 × 12 см, который
регистрировалось время неподвижности и
служил визуальным ориентиром. Животное
число эпизодов неподвижности. Подвижность
автоматически трассировалось при помощи
в этом тесте определялась как любые произ-
веб-камеры, и его поведение анализировалось
вольные движения животных: попытки дотя-
в программе «EthoStudio».
нуться до стенок установки и перекладины,
Обучение животных проводилось в тече-
сильная тряска или движения конечностей,
ние 4 дней, по 3 тестирования каждый раз.
похожие на бег; маятникообразные раскачи-
При обучении животное помещали в центр
вания, возникающие в связи с предыдущими
одного из секторов, кроме целевого, и в тече-
движениями, подвижностью не считались.
ние 60 с оно искало платформу. Вне зависи-
Продолжительность тестирования составляла
мости от того, была найдена платформа или
6 мин, производилась видеорегистрация теста.
нет, в конце каждого тестирования мышь
Приподнятый крестообразный лабиринт
помещали на платформу и удерживали (если
(elevated plus maze) - это пересекающиеся под
требовалось) там в течение 15 с. Параметры,
прямым углом рукава, два из которых откры-
которые измерялись в течение тестирования:
ты и два закрыты. Длина рукавов составляла
латентное время нахождения платформы (с),
30 см, ширина - 6 см, расстояние над уровнем
пройденный путь (см) и суммарное расстоя-
пола - 60 см. Закрытые рукава имели стен-
ние до платформы (см), которое вычислялось
ки из непрозрачного пластика высотой 20 см
как сумма расстояний от мыши до платформы
(безопасные рукава). Животное помещали
в каждый момент времени. Считалось среднее
на место пересечения четырёх рукавов лаби-
по трём тестированиям.
ринта, лицом по направлению к открытому
На пятый день проводили контрольное
рукаву. В последующие 5 мин с использова-
тестирование для проверки качества форми-
нием оригинального программного обеспече-
рования пространственной памяти у живот-
ния «EthoStudio» фиксировались следующие
ных. Для этого платформу убирали, животное
показатели: время пребывания в открытых и
помещали в центр бассейна и фиксировали
БИОХИМИЯ том 88 вып. 8 2023
CDNF КАК РЕГУЛЯТОР ПОВЕДЕНИЯ
1323
его перемещение в течение 60 с. Оценивали
денный путь у групп AAV-EGFP и AAV-CDNF
время нахождения в целевом секторе (%), по-
(t = 0,9; p > 0,05) не отличался (рис. 3, б).
том считали среднее по трём тестированиям.
Динамика потребления пищи досто-
Статистически значимое превышение времени
верно различалась у разных групп животных
нахождения в целевом секторе над случай-
(F(1,19) = 6,18; p < 0,05; рис. 3, в). Апостериор-
ным (25%) свидетельствовало о том, что мышь
ное сравнение выявило достоверную разни-
помнит расположение платформы.
цу между животными из групп AAV-EGFP и
Статистический анализ. Все полученные
AAV-CDNF на четвёртый день (p < 0,01). Эф-
результаты проверялись на соответствие нор-
фект дня достоверно отмечается у всех групп
мальному распределению по критерию Кол-
(F(3,57) = 39,53; p < 0,001). Однако взаимодей-
могорова-Смирнова и Диагостини-Пирсо-
ствия факторов сверхэкспрессия × день тести-
на. Экстремальные значения исключались с
рования не выявлено (F(3,57) = 1,4; p > 0,05).
помощью критерия Диксона. Динамические
Общее потребление пищи оказалось досто-
результаты поведенческого тестирования в
верно ниже у животных со сверхэкспрессией
домашней клетке (потребление воды, пищи,
CDNF (t = 2,079; p = 0,05; рис. 3, г).
пройденный путь), а также такие показатели,
Сверхэкспрессия CDNF не повлияла ни
как латентное время нахождения платформы,
на динамику потребления воды (F(1,18) = 0,003;
расстояние до платформы и пройденный путь
p > 0,05; рис. 3, д), ни на общее количество по-
в водном тесте Морриса, обрабатывались дис-
треблённой воды (t = 1,59; p > 0,05; рис. 3, е).
персионным анализом (ANOVA) для повтор-
Для обеих групп отмечается эффект дня те-
ных измерений. Также проводилось апосте-
стирования (F(3,54) = 4,33; p < 0,001). При апо-
риорное сравнение по Фишеру. Остальные
стериорном сравнении установлено, что ос-
результаты поведенческих тестов, а также все
новной вклад в «эффект дня» осуществляет
результаты молекулярных методик обраба-
разница, возникающая к четвёртому дню в
тывались с помощью t-критерия Стьюдента
группе AAV-EGFP (p < 0,01). Взаимодействия
или U-критерия Манна-Уитни. Все значения
факторов не выявлено (F(3,54) = 0,3; p > 0,05).
представлены как m ± SEM.
Сверхэкспрессия CDNF не оказала влия-
ния на цикл сон/бодрствование. Анализ дина-
мики длительности эпизодов сна и их количе-
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
ства не выявил отличий между исследуемыми
группами животных (F(1,20) = 0,01; p > 0,05 и
Сверхэкспрессия CDNF. Интрагиппокам-
F(1,20) = 3,46; p > 0,05 соответственно). Однако
пальная инъекция AAV-CDNF вызвала повы-
как длительность эпизодов сна, так и коли-
шение уровня мРНК Cdnf более чем в 10 раз
чество эпизодов достоверно отличаются в
(t = 2,752; p = 0,0015; рис. 2, б). Вестерн-блот-
зависимости от времени суток (F(89,18) = 18,74;
анализ также показал, что уровень белка
p < 0,001 и F(89,18) = 13,82; p < 0,001 соответ-
CDNF в гиппокампе экспериментальных жи-
ственно; рис. 4). При этом животные всех
вотных значительно вырос (U = 1; p = 0,0006;
групп проявляют меньшую активность в свет-
рис. 2, в и г). Таким образом, была достигнута
лое время, что было подтверждено при ана-
сверхэкспрессия CDNF в гиппокампе экспе-
лизе средней продолжительности эпизодов сна
риментальных животных, что также было под-
и их количества в зависимости от фазы суток
тверждено данными флуоресцентной мик-
(F(1,4) = 97,25; p < 0,001 и F(1,4) = 198,1; p < 0,001
роскопии (рис. 2, д). По результатам иммуно-
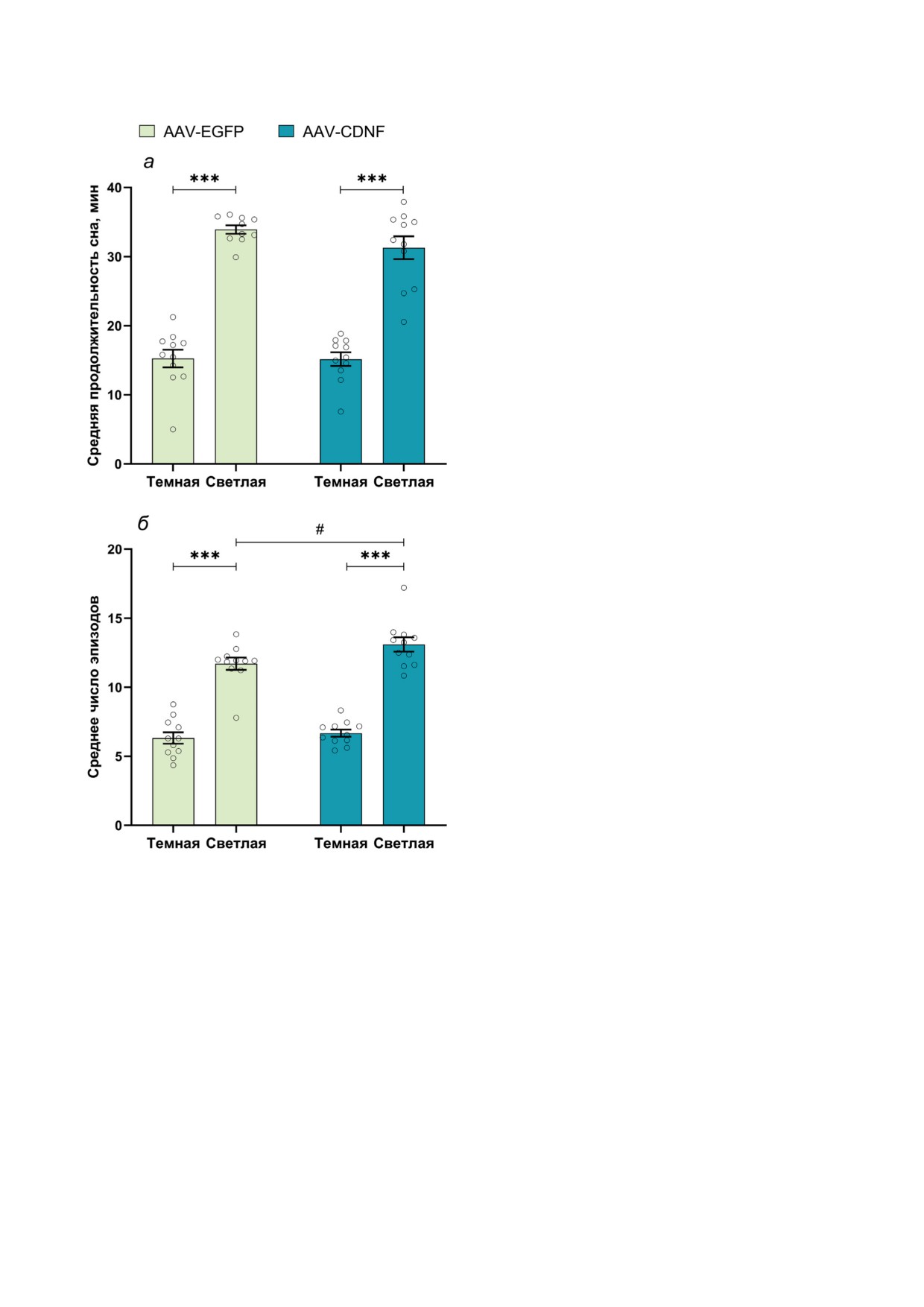
соответственно; рис.
4). Эффект сверхэкс-
гистохимического анализа с кальретикулином,
прессии отмечался для количества эпизодов
проведённому на срезах гиппокампа, было
сна (F(1,4) = 4,32; p < 0,05), но не их средней
обнаружено, что экспрессируемый CDNF пре-
продолжительности (F(1,4) = 0,02; p > 0,05) при
имущественно локализуется в ЭПР (рис. 2, д).
оценке с учётом фазы суток. Разница объ-
Эффекты сверхэкспрессии CDNF на пове-
ясняется большим количеством эпизодов в
дение в условиях домашней клетки. Сверхэкс-
группе AAV-CDNF в светлое время суток, вы-
прессия CDNF не повлияла на общую фи-
явленным при апостериорном тестировании
зическую активность животных, которая оце-
(p < 0,05). Взаимодействия факторов сверхэкс-
нивалась по изменению пройденной дистан-
прессия × фаза суток не выявлено для обоих
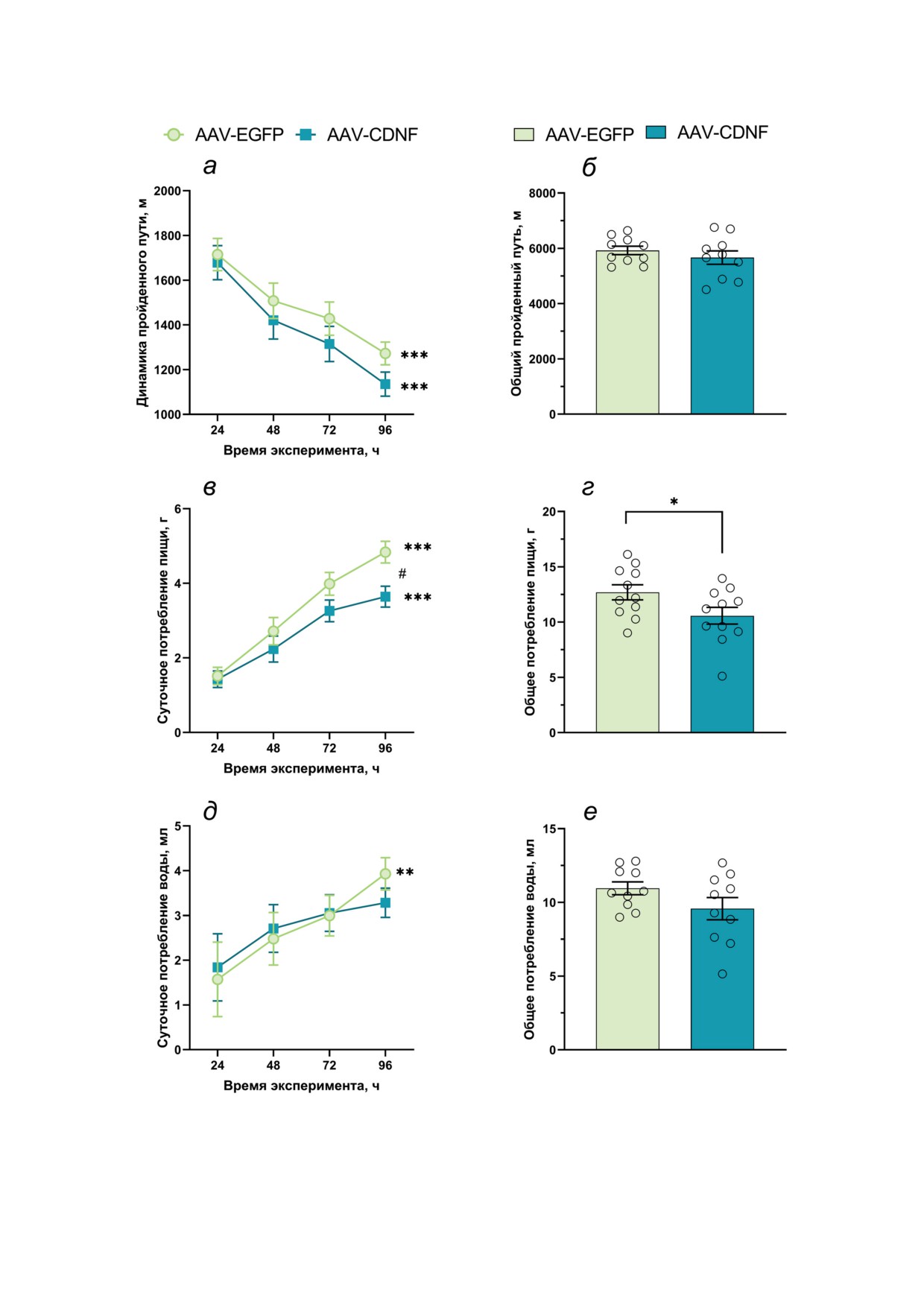
ции (F(1,17) = 1,81; p > 0,05). В то же время здесь
параметров (F(1,4) = 0,006; p > 0,05 и F(1,4) = 1,54;
отмечается эффект дня тестирования (F(3,51) =
p > 0,05 соответственно).
= 22,58; p < 0,001), то есть к четвёртому дню жи-
Сверхэкспрессия CDNF не повлияла на тре-
вотные проходили меньшее расстояние вне за-
вожность, депрессивно-подобное и исследова-
висимости от группы (рис. 3, а). Общий прой-
тельское поведение. Сверхэкспрессия CDNF
БИОХИМИЯ том 88 вып. 8 2023
1324
КАМИНСКАЯ и др.
Рис. 3. Поведение животных со сверхэкспрессией CDNF и животных контрольной группы в домашней клетке:
а - динамика пройденного пути; б - общий пройденный путь; в - динамика суточного потребления пищи; г - общее
потребление пищи; д - динамика суточного потребления воды; е - общее потребление воды. *** p < 0,001; ** p < 0,01;
* p = 0,05 - для обеих групп по сравнению с первым днём; # p < 0,01 - для группы AAV-CDNF по сравнению
с AAV-EGFP
БИОХИМИЯ том 88 вып. 8 2023
CDNF КАК РЕГУЛЯТОР ПОВЕДЕНИЯ
1325
риса показало, что животные эксперимен-
тальной группы обучались быстрее. Анализ
повторных измерений ANOVA для динамики
обучения мышей выявил эффект сверхэкс-
прессии на латентное время нахождения плат-
формы (F(1,15) = 4,45; p = 0,05; рис. 5, а) и на
суммарное расстояние до платформы в каж-
дый момент времени (F(1,15) = 6,23; p < 0,05;
рис. 5, б). Влияние дня тестирования также от-
мечалось в обоих случаях (F(3,45) = 7,14; p < 0,001
и F(3,45) = 6,92; p < 0,001 соответственно). В свою
очередь, на пройденный путь влияла только
принадлежность животных к той или иной
группе (F(1,15) = 8,45; p = 0,0109), а эффекта дня
не наблюдалось (F(3,45) = 2,57; p > 0,05; рис. 5, в).
Апостериорное сравнение показало, что жи-
вотные из группы AAV-CDNF уже на второй
день тестирования достоверно уменьшали рас-
стояние до платформы по сравнению с первым
днём тестирования (p < 0,05), в то время как
для контрольной группы достоверное отличие
появляется только к последнему дню тестиро-
вания (p < 0,05; рис. 5, б). Также апостериор-
ное сравнение показало уменьшение общего
пройденного пути по сравнению с первым
днём тестирования только для группы AAV-
CDNF (p < 0,05), также на второй день выяв-
ляется разница по сравнению с контрольной
группой (p < 0,05; рис. 5, в).
День контрольного теста (без платформы)
показал, что животные всех групп провели
больше времени в целевой четверти (где ранее
располагалась платформа). Этот показатель
статистически выше в сравнении с 25%-ной
вероятностью случайного нахождения в целе-
вом секторе, что означает устойчивое форми-
рование пространственной памяти у всех экс-
периментальных животных (рис. 5, г).
Также в условиях домашней клетки был
проведён тест «оперантная стенка». Сверхэкс-
Рис. 4. Средняя продолжительность (а) и среднее коли-
прессия CDNF не повлияла на такие показа-
чество (б) эпизодов сна животных со сверхэкспрессией
тели, как количество тычков носом, количе-
CDNF и животных контрольной группы в зависимости
ство съеденных гранул и общее время тычков
от фазы суток. *** p < 0,001 - по сравнению с тёмной
фазой; # p < 0,05 - для группы AAV-СDNF по сравнению
носом (табл. 3).
с AAV-EGFP
Таким образом, нами впервые показано,
что сверхэкспрессия CDNF в гиппокампе
улучшает пространственное обучение у мы-
не повлияла на исследовательское и тревож-
шей с генетической предрасположенностью к
но-подобное поведение ни в тесте «откры-
депрессивно-подобному поведению. Вместе с
тое поле», ни в тесте «приподнятый кресто-
тем CDNF не оказал влияния на ассоциатив-
образный лабиринт». По результатам тестов
ное обучение, что может указывать на раз-
«подвешивание за хвост» и «принудительное
личную роль CDNF в механизмах, контроли-
плавание» также не было обнаружено эффек-
рующих пространственное и ассоциативное
тов CDNF на депрессивно-подобное поведе-
обучение.
ние (табл. 3).
Влияние сверхэкспрессии CDNF на экс-
Эффекты сверхэкспрессии CDNF на обуче-
прессию генов нейропластичности. Учитывая
ние. Тестирование в водном лабиринте Мор-
выявленные изменения в поведении мышей,
БИОХИМИЯ том 88 вып. 8 2023
1
326
КАМИНСКАЯ и др.
Таблица 3. Результаты поведенческих тестов
M ± SEM
Параметр
p-значение
AAV-EGFP
AAV-CDNF
Тест «оперантная стенка»
Количество тычков носом
94,40 ± 15,47
54,64 ± 15,63
0,08
Количество съеденных гранул
6,00 ± 1,24
4,10 ± 1,12
0,32
Общее время тычков носом (с)
62,46 ± 16,35
41,32 ± 11,86
0,44
Тест «открытое поле»
Время, проведенное в центре арены (%)
3,74 ± 1,33
4,49 ± 1,60
0,72
Исследованная площадь арены (%)
66,26 ± 4,28
64,32 ± 6,56
0,80
Пройденный путь (м)
14,27 ± 0,24
14,32 ± 0,57
0,93
Количество вертикальных стоек
2,67 ± 0,82
4,00 ± 1,33
0,39
Количество умываний
0,50 ± 0,19
0,75 ± 0,16
0,61
Тест «приподнятый крестообразный лабиринт»
Время, проведенное в открытых рукавах (%)
4,05 ± 0,98
4,35 ± 0,66
0,89
Время, проведенное в закрытых рукавах (%)
87,88 ± 2,62
88,44 ± 1,02
0,86
Исследованная площадь открытых рукавов (%)
17,56 ± 2,78
23,96 ± 1,32
0,07
Исследованная площадь закрытых рукавов (%)
87,55 ± 0,88
87,67 ± 0,68
0,91
Число свешиваний с края установки
4,44 ± 1,12
3,88 ± 0,55
0,67
Число выглядываний из закрытых рукавов
11,44 ± 1,82
15,43 ± 0,90
0,09
Тест «подвешивание за хвост»
Время неподвижности (с)
79,29 ± 8,34
66,29 ± 3,85
0,19
Количество эпизодов неподвижности
13,44 ± 0,80
14,5 ± 0,70
0,34
Тест «принудительное плавание»
Мобильность (степень изменения силуэта животного), %
11,26 ± 0,50
11,1 ± 0,44
0,83
мы оценили уровень экспрессии ключевых
и воздействуя на
синаптическую
пластич-
генов, связанных с процессами обучения и
ность [40]. Принимая во внимание вышеопи-
памяти. Результаты обобщены в табл. 4. Среди
санные данные и локализацию CDNF в ЭПР,
исследованных генов достоверное отличие в
мы решили сфокусироваться на экспрессии
экспрессии было выявлено только для Htr2a
генов UPR (рис. 6).
(t = 2,210; p = 0,04), кодирующего серотонино-
Было обнаружено увеличение экспрессии
вый 5-НТ2А-рецептор.
сплайсированной формы Xbp (sXbp) (рис. 6, д;
Известно, что CDNF может выступать в
t = 2,624; p = 0,017), а также Ire1α (рис. 6, в) на
роли регулятора UPR [15], а UPR, в свою оче-
уровне тенденции (p = 0,0616). При этом отно-
редь, может влиять на когнитивные функции
шение сплайсированной формы Xbp (sXbp) к
в моделях нейродегенеративных заболеваний,
несплайсированной (uXbp) отличается досто-
не только модулируя ответ на стресс ЭПР, но
верно (t = 2,604; p = 0,018; рис. 6, ж).
БИОХИМИЯ том 88 вып. 8 2023
CDNF КАК РЕГУЛЯТОР ПОВЕДЕНИЯ
1327
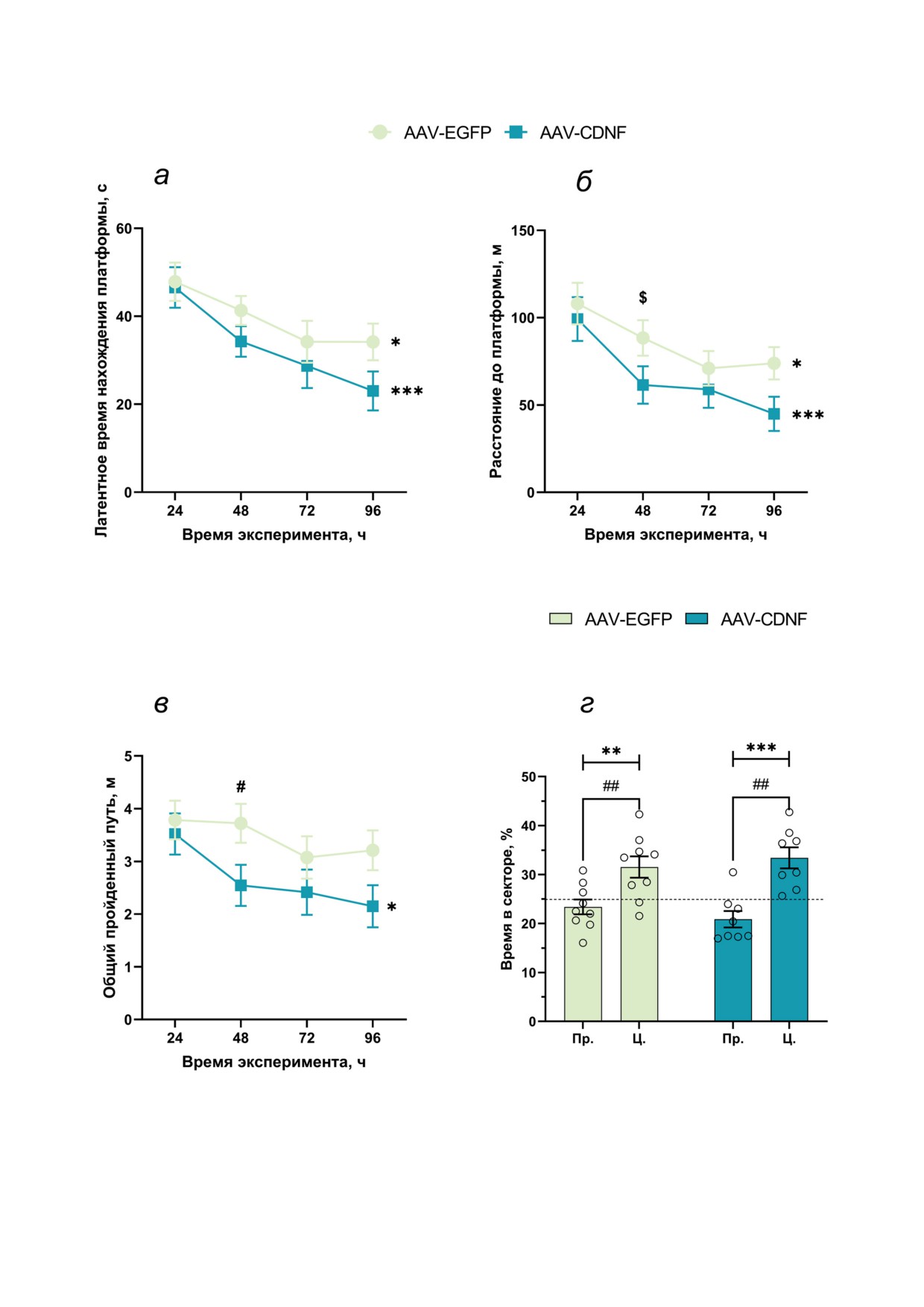
Рис. 5. Латентное время нахождения платформы (а), расстояние до платформы (б) и общий пройденный путь (в)
в тесте «водный лабиринт Морриса» для животных со сверхэкспрессией CDNF и животных контрольной группы.
* p < 0,05; *** p < 0,001 - по сравнению с первым днём тестирования; $ p < 0,05 - для группы AAV-CDNF по сравне-
нию с первым днём тестирования; # p < 0,05 - по сравнению с контрольной группой. г - Контрольное тестирование
для проверки качества формирования пространственной памяти. Время (%), проведённое в целевом секторе (Ц.):
** p < 0,01, *** p < 0,001 - по сравнению с противоположным сектором (Пр.); ## p < 0,01 - по сравнению с 25%-ной
вероятностью случайного нахождения в целевом секторе (обозначено пунктирной линией)
БИОХИМИЯ том 88 вып. 8 2023
1
328
КАМИНСКАЯ и др.
Таблица 4. Профиль экспрессии генов в гиппокампе для животных со сверхэкспрессией CDNF (AAV-CDNF) и живот-
ных контрольной группы (AAV-EGFP)
m ± SEM
Ген
p-значение
Характеристика гена
AAV-EGFP
AAV-CDNF
Htr1a
119,372 ± 14,9095
136,9180 ± 16,0019
0,4329
1A-подтип серотониновых рецепторов
Htr2a
31,5110 ± 1,3773
37,6930± 2,4348
0,0403
2A-подтип серотониновых рецепторов
Htr2b
11,2980 ± 1,2811
15,5690 ± 2,8993
0,1903
2B-подтип серотониновых рецепторов
Htr7
12,6867 ± 0,4399
13,2297 ± 1,0833
0,6479
7-подтип серотониновых рецепторов
RAC-alpha serine/threonine-protein
Akt-1
493,3750 ± 89,2579
425,3310 ± 42,6366
0,5003
kinase - ключевой фермент
PI3/Akt-сигнального пути
activity regulated cytoskeleton associated
protein - ген раннего ответа,
Arc
33,0988 ± 6,7011
57,1540 ± 13,3297
0,1554
один из главных регуляторов
синаптической пластичности
Avpr1a
0,0118± 0,0003
0,0137± 0,0027
0,4698
1A-рецептор аргинин-вазопрессина
Bax
10,0878 ± 1,6144
8,9317 ± 1,4453
0,8639
BCL2 Associated X - активатор апоптоза
Bcl-xl
31,3613 ± 3,2143
30,0603 ± 3,0493
0,7962
Bcl-2-Like Protein 1 - ингибитор апоптоза
Bdnf
92,5860 ± 7,4267
85,8040 ± 7,2094
0,5206
нейротрофический фактор мозга
c-Fos
14,1278 ± 2,1041
12,4967 ± 1,8462
0,5958
ген раннего ответа
cAMP response element binding protein -
Creb
32,3000 ± 4,7879
33,3883 ± 2,8045
0,8665
транскрипционный фактор
Drd1
2,6805 ±0,2429
3,4728 ± 0,5516
0,2799
D1-дофаминовый рецептор
Drd2
1,5910 ± 0,2287
2,5990 ± 0,6282
0,2556
D2-дофаминовый рецептор
глутаматный ионотропный
Gria1
1110,5000 ± 91,0357
1056,7080 ± 116,4134
0,7201
AMPA1-рецептор (α1-субъединица)
глутаматный ионотропный
Gria2
1056,9540 ± 144,9108
1077,4820 ± 110,9364
0,5787
AMPA2-рецептор (α2-субъединица)
глутаматный ионотропный
Grik1
21,0377 ± 1,1859
19,7733 ± 1,7413
0,3527
каинатный рецептор (1-субъединица)
глутаматный ионотропный
Grik2
112,1920 ± 12,8476
110,4676 ± 8,9398
0,6305
каинатный рецептор (β2-субъединица)
глутаматный ионотропный
Grin1
773,9467 ± 40,1829
766,6870 ± 75,0227
0,9330
NMDA1-рецептор (z1-субъединица)
глутаматный ионотропный
Grin2a
501,7465 ± 63,7042
469,2562 ± 37,8923
0,6664
NMDA2A-рецептор (ε1-субъединица)
глутаматный ионотропный
Grin2b
327,4900 ± 22,9015
320,2550 ± 18,8293
0,8100
NMDA2B-рецептор (ε2-субъединица)
Grm1
96,7208 ± 5,0159
109,4579 ± 11,9102
0,3374
глутаматный метаботропный рецептор 1
Grm2
80,5865 ± 5,6277
79,4585 ± 5,9721
0,8922
глутаматный метаботропный рецептор 2
БИОХИМИЯ том 88 вып. 8 2023
CDNF КАК РЕГУЛЯТОР ПОВЕДЕНИЯ
1329
Таблица 4 (продолжение)
m ± SEM
Ген
p-значение
Характеристика гена
AAV-EGFP
AAV-CDNF
Grm3
120,8930 ± 5,9356
132,7440 ± 11,1860
0,5288
глутаматный метаботропный рецептор 3
Grm4
0,7130 ± 0,1083
1,0190 ± 0,2466
0,3930
глутаматный метаботропный рецептор 4
Grm5
218,2150 ± 13,8453
227,5493 ± 18,4510
0,6905
глутаматный метаботропный рецептор 5
Kalrn
194,6956 ± 5,8838
201,5212 ± 10,6467
0,5816
калирин - киназа-активатор Rho-ГТФаз
Mapk3
1,0560 ± 0,0948
0,9830 ± 0,1292
0,3427
митоген-активируемая протеинкиназа 3
Nfκb
9,2062 ± 1,013
9,5600 ± 0,8037
0,7958
транскрипционный фактор
регуляторная субъединица 1
Pik3r1
53,4200 ± 3,2130
52,0680 ± 4,4137
0,8072
фосфатидилинозитол-3-киназы
Plcg1
67,5700 ± 7,3740
69,980 ± 15,0900
0,5288
фосфолипаза С гамма 1
rPol2
5,4170 ± 0,9583
3,6736 ± 0,7517
0,1647
РНК-полимераза II субъединица А
Syp
20,1800 ± 2,3135
23,8340 ± 2,4439
0,2919
синаптофизин
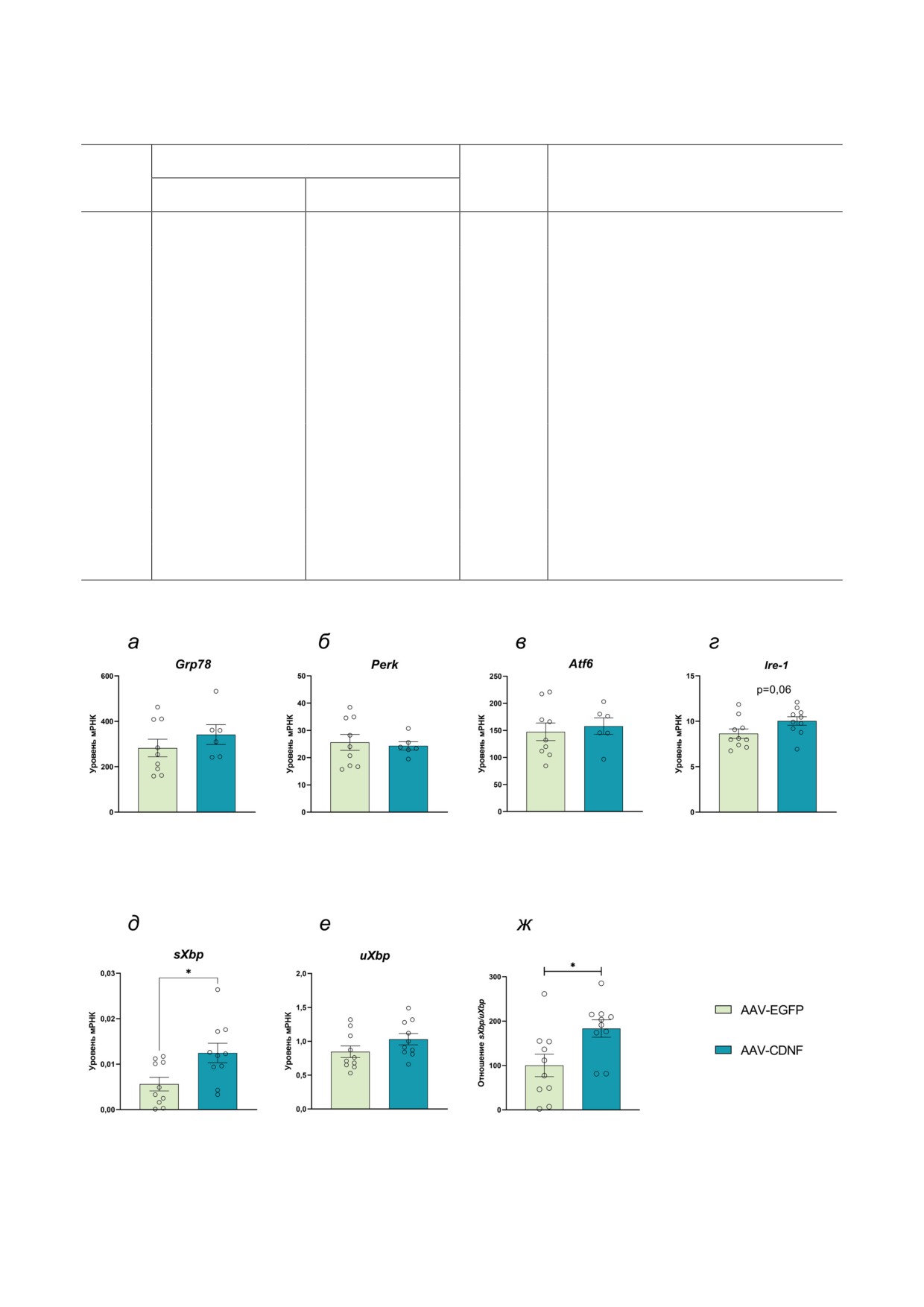
Рис. 6. Уровень экспрессии генов UPR: Grp78 (а), Perk (б), Atf6 (в), Ire1α (г), sXbp (д), uXbp (е) и соотношение sXbp/
uXbp (ж). Уровень мРНК (а-г) представлен как число копий гена, отнесённое на 100 копий rPol2. Для панелей (д)
и (е) экспрессия представлена как отношение уровней экспрессии sXbp и uXbp к уровню экспрессии rPol2. *p < 0,05 -
для CDNF относительно группы AAV-EGFP
4
БИОХИМИЯ том 88 вып. 8 2023
1330
КАМИНСКАЯ и др.
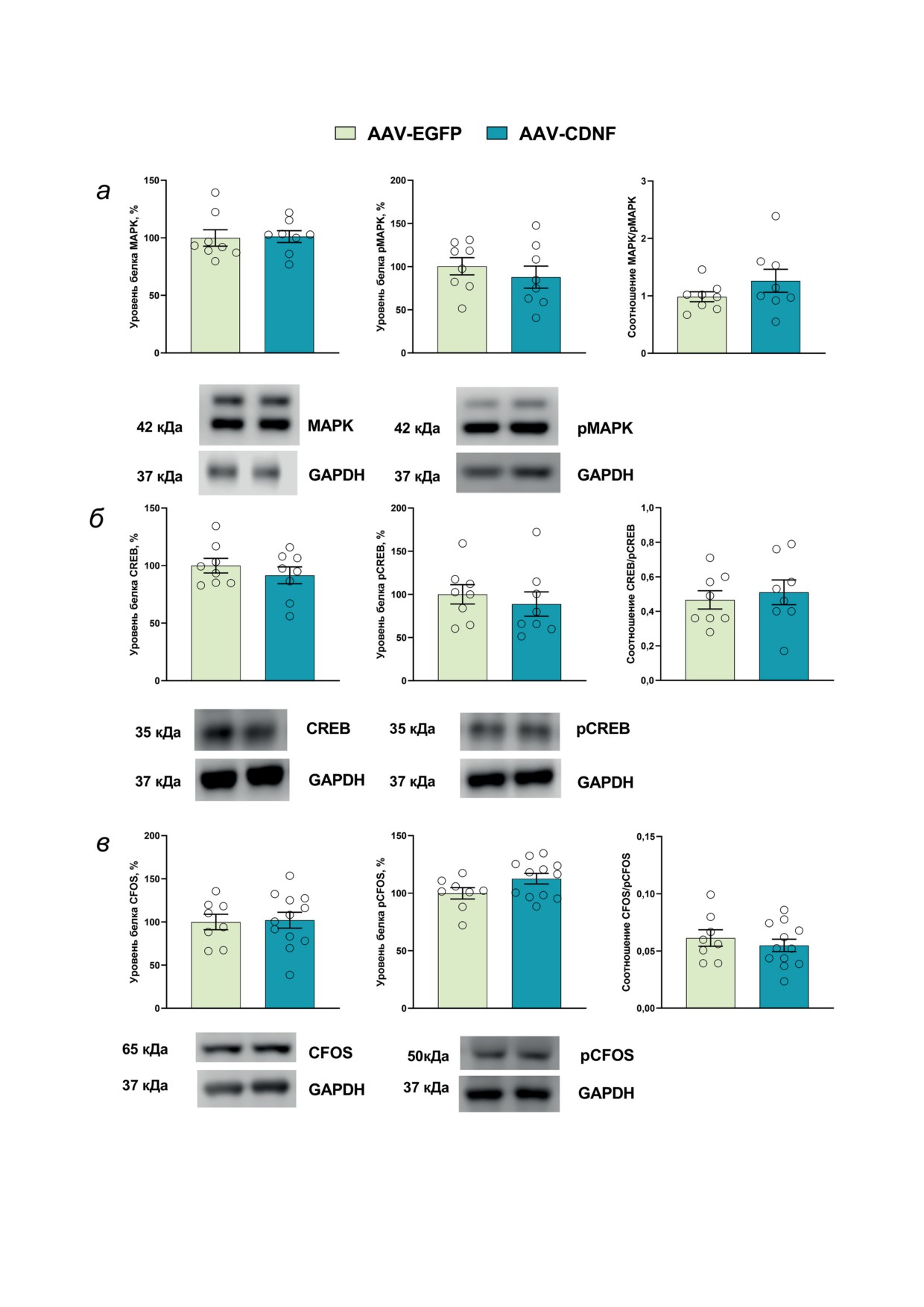
Рис. 7. Количественная оценка интенсивности хемилюминесцентного сигнала для белка, его фосфорилированной
формы и их соотношение, а также результаты иммуноблота на мембранах для MAPK/pMAPK (а), СREB/pCREB (б)
и CFOS/pCFOS (в). Уровни белка представлены в относительных единицах, нормализованных на соответствующий
уровень GAPDH
БИОХИМИЯ том 88 вып. 8 2023
CDNF КАК РЕГУЛЯТОР ПОВЕДЕНИЯ
1331
Ввиду того, что активность каскадов зача-
депрессивно-подобное поведение мышей, оце-
стую изменяется не на уровне экспрессии, а на
нённое в тестах «принудительное плавание» и
уровне посттрансляционных модификаций, в
«подвешивание за хвост». На этой же линии
первую очередь фосфорилирования, было ре-
мышей в том же тесте ранее был продемон-
шено оценить не только количество белка, но
стрирован антидепрессантный эффект цен-
и отношение между обычной и фосфорилиро-
трального введения рекомбинантного белка
ванной формой белков раннего ответа CREB и
BDNF [26], однако глиальный нейротрофи-
CFOS, а также MAP-киназы. Однако сверхэкс-
ческий фактор GDNF при центральном вве-
прессия CDNF в гиппокампе не повлияла на
дении не оказал влияния на неподвижность
уровень вышеперечисленных белков, фосфо-
в тесте «подвешивание за хвост» [30]. В то же
рилированных форм этих белков или их соот-
время и BDNF, и GDNF оказывали значитель-
ношение (рис. 7).
ный антидепрессантный эффект в тесте «при-
нудительное плавание». Вероятно, CDNF не
влияет на депрессивно-подобное поведение
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
«депрессивных» мышей ASC, что отличает его
от классических нейротрофических факторов
В результате данной работы было обна-
BDNF и GDNF. Однако следует принимать
ружено, что сверхэкспрессия CDNF в гиппо-
во внимание, что в упомянутых работах мы
кампе не влияет на двигательную активность,
вводили белок BDNF или GDNF системно, в
потребление воды, а также исследовательское
желудочек мозга, тогда как в настоящем иссле-
и тревожно-подобное поведение. Ранее было
довании увеличение количества CDNF осу-
показано, что как трансгенные мыши APP/PS1
ществлялось локально, только в гиппокампе.
(являются моделью болезни Альцгеймера), так
Ранее было показано нарушение угаса-
и мыши дикого типа совершали больше под-
ния памяти страха у мышей линии ASC, и
ходов как к новым, так и к старым объектам
было предположено, что данное нарушение
в тесте «новый объект» после микроинъек-
может играть важную роль в формировании
ции CDNF, то есть проявляли бо льшую ис-
депрессивно-подобного фенотипа этих жи-
следовательскую активность [14]. Стоит отме-
вотных [43]. Также была показана устойчи-
тить, что тест «новый объект» лучше подходит
вость мышей этой линии к амнестической
для описания неофобии, а в более специфич-
стимуляции [44]. Сверхэкспрессия CDNF в
ном тесте на спонтанное исследовательское
нейронах гиппокампа мышей ASC улучши-
поведение обнаруженная разница не подтвер-
ла пространственное обучение животных.
дилась. Поэтому авторы приходят к выводу,
Можно предположить, что данное улучшение
что ни микроинъекция белка, ни эндогенный
связано с повышенной устойчивостью памя-
CDNF не вызывает побочных эффектов в виде
ти у мышей данной линии. Однако в работе
усиления тревожности, гипо- или гиперак-
Kemppainen et al. [14] было продемонстриро-
тивности, и наши данные согласуются с этим
вано, что индукция сверхэкспрессии CDNF
выводом [14].
в гиппокампе улучшала пространственную
Ранее было установлено, что как фар-
память как у мышей линии APP/PS1, так и у
макологическое (мусцимол) [41], так и опто-
мышей дикого типа. Здесь стоит отметить два
генетическое
[42] ингибирование глутамат-
момента. Во-первых, в указанном исследова-
ергических нейронов дорсального гиппокампа
нии в AAV был встроен ген CDNF человека,
нарушает консолидацию памяти о недавнем
а во-вторых, транскрипция осуществлялась
приёме пищи, сокращает время до наступле-
под контролем промотора цитомегаловиру-
ния следующего приёма пищи и увеличивает
са (CMV), что не позволяло достичь специфи-
его объём. Также установлено, что вентраль-
ческой экспрессии в нейронах. Если первое
ный гиппокамп участвует в восприятии таких
обстоятельство вряд ли играет большую роль в
важных нейроэндокринных регуляторов, как
силу высокой консервативности CDNF среди
лептин, грелин и глюкагоноподобный пеп-
млекопитающих, второе существенно ослож-
тид-1 (GLP-1). Обнаруженное нами снижение
няет картину. В созданной нами плазмиде
потребления пищи под действием сверхэкс-
экспрессия гена Cdnf контролируется синап-
прессии CDNF в гиппокампе подтверждает
синовым промотором (Syn), обеспечивающим
участие CDNF в регуляции пищевого поведе-
избирательную экспрессию целевого гена в
ния, однако механизм данного эффекта ещё
нервных клетках. Таким образом, мы впервые
предстоит установить.
показали, что именно сверхэкспрессия нейро-
Повышение экспрессии CDNF в гиппо-
нального CDNF улучшает пространственное
кампе не оказало существенного влияния на
обучение животных. Поскольку изменилась
БИОХИМИЯ том 88 вып. 8 2023
4*
1
332
КАМИНСКАЯ и др.
динамика обучения, мы можем предполагать
сии Bdnf не отмечалось. Другой механизм, объ-
эффект на кратковременную память, не обна-
ясняющий изменение когнитивных функций,
руженный в исследовании Kemppainen et al. [14].
предполагает в качестве ключевого посред-
Более того, эффект сверхэкспрессии CDNF в
ника благоприятных эффектов sXBP1 - кали-
нейронах, вероятно, зависит от генотипа. Это
рин (Kal7) [50]. В нашем эксперименте под-
поднимает важный вопрос о том, изменена
тверждений активации данного пути также не
ли функция CDNF при тех или иных нейро-
было найдено. Не исключено и существование
патологиях. Пока что исследование данной
альтернативных каскадов, вовлекающих, на-
проблемы находится в зачаточном состоянии.
пример, KIF17.
Имеется лишь несколько работ, в которых
Несмотря на выраженный эффект сверх-
попытались оценить связь полиморфизмов в
экспрессии CDNF на обучение в водном лаби-
гене CDNF с развитием БП, шизофренией или
ринте Морриса, её влияния на ассоциативное
кокаиновой зависимостью [45-47].
обучение обнаружено не было, что может ука-
На данном этапе мы не можем проследить
зывать на различную роль CDNF в механиз-
всю последовательность молекулярных собы-
мах, контролирующих пространственное и
тий, ведущих к поведенческим изменениям,
ассоциативное обучение.
однако нам удалось выявить несколько потен-
Нами установлено достоверное увеличе-
циальных «ключевых игроков». Одним из них,
ние экспрессии
2А-подтипа серотониновых
безусловно, является транскрипционный фак-
рецепторов (5-HT2А) в группе со сверхэкспрес-
тор Xbp1 (X-box binding protein-1). Наличие
сией CDNF. Представляется маловероятным,
связи экспрессии Cdnf и Xbp1, а также увеличе-
что данное обстоятельство могло привести к
ние образования его сплайсированной формы
столь существенному изменению динамики
уже были показаны ранее на клеточной куль-
обучения животных в водном лабиринте Мор-
туре в контексте изучения UPR [48]. Известно,
риса. Действительно, существует целый ряд
что активная форма белка XBP1 образуется
исследований на различных модельных объ-
только со сплайсированного транскрипта при
ектах, указывающий на взаимосвязь 5-HT2A-
участии IRE1. С помощью иммуногистохими-
рецепторов и процессов памяти [51], однако их
ческого анализа мы подтвердили, что CDNF
результаты достаточно противоречивы. В це-
локализуется в ЭПР, откуда прямо или опо-
лом, существующие данные показывают, что
средованно может влиять на экспрессию Ire1α.
активация 5-HT2А-рецепторов при системной
Действительно, нами была замечена сильная
инъекции или при местной микроинфузии,
тенденция к увеличению экспрессии Ire1α в
по-видимому, усиливают у мышей две формы
опытной группе. Можно предположить, что
памяти, зависящей от гиппокампа: память
in vivo существуют механизмы, вовлечённые
объекта и условно-рефлекторную память стра-
в клеточный ответ на стресс ЭПР, однако при
ха. При этом в отношении заданий, связанных
отсутствии стресса эти же механизмы, вероят-
с пространственным обучением, результат,
но, выполняют другие функции. В пользу этой
скорее, обратный. Так, при подкожной инъек-
гипотезы выступает и тот факт, что у нокаут-
ции псилоцина, который является агонистом
ных по Cdnf животных не наблюдалось изме-
5-HT2А-рецепторов, у крыс нарушалось про-
нений в базальной экспрессии генов UPR [12].
странственное обучение в карусельном тесте
Влияние экспрессии Xbp1 на формирование
и память о нахождении платформы в водном
пространственной памяти и гиппокамп-зави-
лабиринте Морриса, но не было эффекта на
симое обучение было показано в исследова-
консолидацию памяти [52].
нии Martinez et al. [49]. Было установлено,
Ранее высказывалось мнение, что основ-
что животным с кондиционным нокаутом
ным свойством CDNF, которое отличает его от
по Xbp1 (XBP1Nes-/-) требовалось больше попы-
классических НТФ, является то, что его влия-
ток, чтобы выполнить задание в тесте гибко-
ние на неповреждённые нейроны слабое или
сти памяти, а также они показывали меньший
даже отсутствует [1, 53]. Однако накаплива-
процент замираний в тесте контекстуального
ются данные, свидетельствующие, что CDNF
условно-рефлекторного пассивного избегания.
может не только способствовать выживанию
Животные со сверхэкспрессией XBP1, напро-
специфической популяции нейронов в усло-
тив, демонстрировали улучшение во всех вы-
виях угрозы, но также запускает некоторые
шеперечисленных тестах. Основным эффек-
молекулярные каскады в неповреждённом
тором изменений был назначен BDNF, так
мозге, осуществляет тонкую регуляцию нор-
как имеются данные, подтверждающие его
мального поведения, а также вовлечён в меха-
роль мастера-регулятора. Однако в нашем
низмы формирования различных типов пато-
исследовании изменений на уровне экспрес-
логического поведения. В ходе нашей работы
БИОХИМИЯ том 88 вып. 8 2023
CDNF КАК РЕГУЛЯТОР ПОВЕДЕНИЯ
1333
было обнаружено, что нейрональный CDNF
Финансирование. Работа выполнена при
участвует в механизмах формирования про-
финансовой поддержке Российского научного
странственной памяти у мышей линии ASC с
фонда (грант № 22-15-00011). Содержание жи-
генетически-детерминированным депрессив-
вотных было поддержано бюджетным проек-
но-подобным поведением. Было показано, что
том № FWNR-2022-0023.
избыточно экспрессирующийся в гиппокампе
Благодарности. Исследование было осущест-
CDNF локализуется в ЭПР и приводит к акти-
влено на базе Центра генетических ресурсов
вации Ire1α/Xbp1-пути, традиционно ассо-
лабораторных животных Института цитологии
циируемого со стрессом ЭПР. Таким образом,
и генетики Сибирского отделения Российской
несмотря на то что CDNF активирует уникаль-
академии наук (ИЦиГ СО РАН), поддержанно-
ные молекулярные каскады, что отличает его
го Министерством науки и высшего образова-
от классических нейротрофических факто-
ния России (уникальный идентификационный
ров, он тем не менее обладает существенным
номер проекта: RFMEFI62119X0023).
нейротрофным потенциалом, реализуемым на
Конфликт интересов. Авторы заявляют об
уровне поведенческой пластичности.
отсутствии конфликта интересов.
Соблюдение этических норм. Все экспери-
Вклад авторов. Я.П. Каминская - про-
ментальные процедуры были проведены в соот-
ведение экспериментов, анализ результатов,
ветствии с международными правилами обраще-
написание текста; Т.В. Ильчибаева - созда-
ния с животными (Guide for the Care and Use of
ние вирусных конструктов, визуализация;
Laboratory Animals, the Eighth Edition, Committee
Н.В. Хоцкин - проведение экспериментов;
for the Update of the Guide for the Care and Use
А.С. Цыбко - концепция, проведение экс-
of Laboratory Animals; National Research Council
периментов, редактирование текста статьи;
© 2020 National Academy of Sciences (USA)) и
В.С. Науменко - редактирование текста ста-
одобрены этическим комитетом ИЦиГ СО РАН
тьи, общее руководство проектом.
(заключение № 34 от 15 июня 2016 г.).
СПИСОК ЛИТЕРАТУРЫ
1. Lindholm, P., Voutilainen, M. H., Laurén, J.,
model of Parkinson’s disease, PLoS One,
11,
Peränen, J., Leppänen, V.-M., Andressoo, J.-O.,
e0149776, doi: 10.1371/journal.pone.0149776.
Lindahl, M., Janhunen, S., Kalkkinen, N., Timmusk, T.,
6. Raykhel, I., Alanen, H., Salo, K., Jurvansuu, J., Van,
Tuominen, R. K., and Saarma, M. (2007) Novel
D. N., Latva-Ranta, M., and Ruddock, L. (2007)
neurotrophic factor CDNF protects and rescues
A molecular specificity code for the three mammalian
midbrain dopamine neurons in vivo, Nature, 448,
KDEL receptors, J. Cell Biol.,
179,
1193-1204,
73-77, doi: 10.1038/nature05957.
doi: 10.1083/jcb.200705180.
2. Parkash, V., Lindholm, P., Peränen, J., Kalkkinen, N.,
7. Lindholm, P., and Saarma, M. (2010) Novel CDNF/
Oksanen, E., Saarma, M., Leppänen, V.-M, and
MANF family of neurotrophic factors, Dev. Neurobiol.,
Goldman, A. (2009) The structure of the conserved
70, 360-371, doi: 10.1002/dneu.20760.
neurotrophic factors MANF and CDNF explains
8. Apostolou, A., Shen, Y., Liang, Y., Luo, J., and
why they are bifunctional, Protein Eng. Des. Sel., 22,
Fang, S. (2008) Armet, a UPR-upregulated protein,
233-241, doi: 10.1093/protein/gzn080.
inhibits cell proliferation and ER stress-induced cell
3. Voutilainen, M. H., Bäck, S., Peränen, J., Lindholm, P.,
death, Exp. Cell Res., 314, 2454-2467, doi: 10.1016/
Raasmaja, A., Männistö, P. T., Saarma, M., and
j.yexcr.2008.05.001.
Tuominen, R. K. (2011) Chronic infusion of CDNF
9. Bruhn, H. (2005) A short guided tour through func-
Prevents 6-OHDA-induced deficits in a rat model
tional and structural features of saposin-like proteins,
of Parkinson’s disease, Exp. Neurol., 228, 99-108,
Biochem. J., 389, 249-257, doi: 10.1042/BJ20050051.
doi: 10.1016/j.expneurol.2010.12.013.
10. Mätlik, K., Yu, L., Eesmaa, A., Hellman, M.,
4. Lindholm, D., Wootz, H., and Korhonen, L. (2006)
Lindholm, P., Peränen, J., Galli, E., Anttila, J.,
ER stress and neurodegenerative diseases, Cell Death
Saarma, M., Permi, P., Airavaara, M., and Arumäe, U.
Differ., 13, 385-392, doi: 10.1038/sj.cdd.4401778.
(2015) Role of two sequence motifs of mesencephalic
5. Garea-Rodríguez, E., Eesmaa, A., Lindholm, P.,
astrocyte-derived neurotrophic factor in its survival-
Schlumbohm, C., König, J., Meller, B., Krieglstein, K.,
promoting activity, Cell Death Dis.,
6, e2032,
Helms, G., Saarma, M., and Fuchs, E.
(2016)
doi: 10.1038/cddis.2015.371.
Comparative analysis of the effects of neurotrophic
11. Božok, V., Yu, L., Palgi, J., and Arumäe, U. (2018)
factors CDNF and GDNF in a nonhuman primate
Antioxidative CXXC peptide motif from mesencephalic
БИОХИМИЯ том 88 вып. 8 2023
1
334
КАМИНСКАЯ и др.
astrocyte-derived neurotrophic factor antagonizes
22.
Kulikov, A. V., Kozlachkova, E. Y., Maslova,
programmed cell death, Front. Cell Dev. Biol., 6, 106,
G. B., and Popova, N. K. (1993) Inheritance of
doi: 10.3389/fcell.2018.00106.
predisposition to catalepsy in mice, Behav. Genet., 23,
12.
Lindahl, M., Chalazonitis, A., Palm, E., Pakarinen, E.,
379-384, doi: 10.1007/BF01067439.
Danilova, T., Phamb, T. D., Setlikb, W., Rao, M.,
23.
Tikhonova, M. A., Lebedeva, V. V., Kulikov, A. V.,
Võikar, V., Huotari, J., Kopra, J., Andressooa, J.-O.,
Bazovkina, D. V., and Popova, N. K. (2006) Effect
Piepponend, P. T., Airavaaraa, M., Panhelainen, A.,
of imipramine on the behavior and cerebral 5-HT1A
Gershon, M. D., and Saarma, M. (2020) Cerebral
serotonin receptors in mice genetically predisposed
dopamine neurotrophic factor-deficiency leads to
to catalepsy, Bull. Exp. Biol. Med.,
141,
48-50,
degeneration of enteric neurons and altered brain
doi: 10.1007/s10517-006-0090-7.
dopamine neuronal function in mice, Neurobiol. Dis.,
24.
Tikhonova, M. A., Alperina, E. L., Tolstikova, T. G.,
134, 104696, doi: 10.1016/j.nbd.2019.104696.
Bazovkina, D. V., Di, V. Y., Idova, G. V., Kulikov,
13.
Chen, Y.-C. C., Baronio, D., Semenova, S.,
A. V., and Popova, N. K. (2010) Effects of chronic
Abdurakhmanova, S., and Panula, P. (2020) Cerebral
fluoxetine treatment on catalepsy and the immune
dopamine neurotrophic factor regulates multiple
response in mice with a genetic predisposition to
neuronal subtypes and behavior, J. Neurosci., 40,
freezing reactions: the roles of types 1A and 2A
6146-6164, doi: 10.1523/JNEUROSCI.2636-19.2020.
serotonin receptors and the Tph2 and SERT genes,
14.
Kemppainen, S., Lindholm, P., Galli, E., Lahtinen,
Neurosci. Behav. Physiol., 40, 521-527, doi: 10.1007/
H.-M. M., Koivisto, H., Hämäläinena, E., Saarmab, M.,
s11055-010-9291-7.
and Tanila, H. (2015) Cerebral dopamine neurotrophic
25.
Базовкина Д. В., Куликов А. В., Кондаурова Е. М.,
factor improves long-term memory in APP/PS1
Попова Н. К. (2005) Селекция на предрасполо-
transgenic mice modeling Alzheimer’s disease as well
женность к каталепсии усиливает депрессивно-
as in wild-type mice, Behav. Brain Res., 291, 1-11,
подобные характеристики поведения у мышей,
doi: 10.1016/j.bbr.2015.05.002.
Генетика, 41, 1222-1228.
15.
Voutilainen, M. H., De Lorenzo, F., Stepanova, P.,
26.
Naumenko, V. S., Kondaurova, E. M., Bazovkina,
Bäck, S., Yu, L.-Y., Lindholm, P., Pörsti, E.,
D. V., Tsybko, A. S., Tikhonova, M. A., Kulikov,
Saarma, M., Männistö, P. T., and Tuominen, R. K.
A. V., and Popova, N. K. (2012) Effect of brain-derived
(2017) Evidence for an additive neurorestora-
neurotrophic factor on behavior and key members of
tive effect of simultaneously administered CDNF
the brain serotonin system in genetically predisposed
and GDNF in hemiparkinsonian rats: implications
to behavioral disorders mouse strains, Neuroscience,
for different mechanism of action, eNeuro,
214, 59-67, doi: 10.1016/j.neuroscience.2012.04.031.
4, ENEURO.0117-16.2017, doi: 10.1523/ENEURO.
27.
Björkholm, C., and Monteggia, L. M. (2016) BDNF -
0117-16.2017.
a key transducer of antidepressant effects, Neuro-
16.
Kesner, R. P. (2018) An analysis of dentate gyrus
pharmacology, 102, 72-79, doi: 10.1016/j.neuropharm.
function (an update), Behav. Brain Res., 354, 84-91,
2015.10.034.
doi: 10.1016/J.BBR.2017.07.033.
28.
Caviedes, A., Lafourcade, C., Soto, C., and
17.
Papp, G., Witter, M. P., and Treves, A. (2007) The CA3
Wyneken, U. (2017) BDNF/NF-ΚB signaling in the
network as a memory store for spatial representations,
neurobiology of depression, Curr. Pharm. Des., 23,
Learn. Mem., 14, 732-744, doi: 10.1101/LM.687407.
3154-3163, doi: 10.2174/1381612823666170111141915.
18.
Fredes, F., and Shigemoto, R.
(2021) The role
29.
Mondal, A. C., and Fatima, M. (2019) Direct and
of hippocampal mossy cells in novelty detection,
indirect evidences of BDNF and NGF as key mod-
Neurobiol. Learn. Mem., 183, 107486, doi: 10.1016/
ulators in depression: role of antidepressants treat-
J.NLM.2021.107486.
ment, Int. J. Neurosci., 129, 283-296, doi: 10.1080/
19.
Sun, D., Mei, L., and Xiong, W. C. (2023) Dorsal
00207454.2018.1527328.
dentate gyrus, a key regulator for mood and psy-
30.
Naumenko, V. S., Bazovkina, D. V., Semenova, A. A.,
chiatric disorders, Biol. Psychiatry, 93, 1071-1080,
Tsybko, A. S., Il’chibaeva, T. V., Kondaurova, E. M.,
doi: 10.1016/J.BIOPSYCH.2023.01.005.
and Popova, N. K. (2013) Effect of glial cell line-de-
20.
Kondaurova, E. M., Bazovkina, D. V., Kulikov,
rived neurotrophic factor on behavior and key members
A. V., and Popova, N. K. (2006) Selective Breeding
of the brain serotonin system in mouse strains geneti-
for catalepsy changes the distribution of microsatellite
cally predisposed to behavioral disorders, J. Neurosci.
D13Mit76 alleles linked to the 5-HT1A serotonin
Res., 91, 1628-1638, doi: 10.1002/jnr.23286.
receptor gene in mice, Genes, Brain Behav.,
5,
31.
Chen, S.-H., Haam, J., Walker, M., Scappini, E.,
596-601, doi: 10.1111/j.1601-183X.2006.00212.x.
Naughton, J., and Martin, N. P. (2019) Recombinant
21.
Kulikov, A. V., Bazovkina, D. V., Kondaurova,
viral vectors as neuroscience tools, Curr. Protoc.
E. M., and Popova, N. K. (2008) Genetic structure of
Neurosci., 87, e67, doi: 10.1002/cpns.67.
hereditary catalepsy in mice, Genes Brain Behav., 7,
32.
Kondaurova, E. M., Plyusnina, A. V., Ilchibaeva,
506-512, doi: 10.1111/j.1601-183X.2008.00387.x.
T. V., Eremin, D. V., Rodnyy, A. Y., Grygoreva, Y. D.,
БИОХИМИЯ том 88 вып. 8 2023
CDNF КАК РЕГУЛЯТОР ПОВЕДЕНИЯ
1335
and Naumenko, V. S. (2021) Effects of a Cc2d1a/
passive avoidance response in mice with high levels of
Freud-1 knockdown in the hippocampus on behavior,
predisposition to catalepsy, Neurosci. Behav. Physiol.,
the serotonin system, and BDNF, Int. J. Mol. Sci., 22,
39, 475-480, doi: 10.1007/s11055-009-9152-4.
13319, doi: 10.3390/ijms222413319.
44.
Sinovyev, D. R., Dubrovina, N. I., and Kulikov,
33.
Kondaurova, E. M., Belokopytova, I. I., Kulikova,
A. V. (2009) Development of amnesia in different
E. A., Khotskin, N. V., Ilchibaeva, T. V., Tsybko,
mouse strains, Bull. Exp. Biol. Med., 147, 557-559,
A. S., Popova, N. K., and Naumenko, V. S. (2023)
doi: 10.1007/S10517-009-0583-2.
On the role of serotonin
5-HT(1A) receptor in
45.
Lohoff, F. W., Bloch, P. J., Ferraro, T. N., Berrettini,
autistic-like behavior: cross talk of 5-HT and BDNF
W. H., Pettinati, H. M., Dackis, C. A., O’Brien,
systems, Behav. Brain Res., 438, 114168, doi: 10.1016/
C. P., Kampman, K. M., and Oslin, D. W. (2009)
j.bbr.2022.114168.
Association analysis between polymorphisms in the
34.
Kulikov, A. V., Naumenko, V. S., Voronova, I. P.,
conserved dopamine neurotrophic factor (CDNF)
Tikhonova, M. A., and Popova, N. K.
(2005)
gene and cocaine dependence, Neurosci. Lett., 453,
Quantitative RT-PCR assay of 5-HT1A and 5-HT2A
199-203, doi: 10.1016/j.neulet.2009.02.026.
serotonin receptor MRNAs using genomic DNA as an
46.
Choi, J. M., Hong, J. H., Chae, M. J., Hung, N. P.,
external standard, J. Neurosci. Methods, 141, 97-101,
Kang, H. S., Ma, H.-I., and Kim, Y. J. (2011) Analy-
doi: 10.1016/J.JNEUMETH.2004.06.005.
sis of mutations and the association between polymor-
35.
Naumenko, V. S., and Kulikov, A. V. (2006) Quan-
phisms in the cerebral dopamine neurotrophic factor
titative assay of 5-HT1A receptor gene expression
(CDNF) gene and Parkinson’s disease, Neurosci.
in the brain, Mol. Biol., 40, 30-36, doi: 10.1134/
Lett., 493, 97-101, doi: 10.1016/j.neulet.2011.02.013.
S0026893306010067/METRICS.
47.
Yang, Y., Yu, H., Li, W., Liu, B., Zhang, H., Ding, S.,
36.
Naumenko, V. S., Osipova, D. V., Kostina, E. V., and
Lu, Y., Jiang, T., and Lv, L. (2018) Association between
Kulikov, A. V. (2008) Utilization of a two-standard
cerebral dopamine neurotrophic factor (CDNF)
2
system in real-time PCR for quantification of gene
polymorphisms and schizophrenia susceptibility and
expression in the brain, J. Neurosci. Methods, 170,
symptoms in the han chinese population, Behav. Brain
197-203, doi: 10.1016/j.jneumeth.2008.01.008.
Funct., 14, 1, doi: 10.1186/s12993-017-0133-4.
37.
Kulikov, A. V., Tikhonova, M. A., and Kulikov, V. A.
48.
Arancibia, D., Zamorano, P., and Andrés, M. E. (2018)
(2008) Automated measurement of spatial preference
CDNF Induces the adaptive unfolded protein response
in the open field test with transmitted lighting,
and attenuates endoplasmic reticulum stress-induced
J. Neurosci. Methods, 170, 345-351, doi: 10.1016/
cell death, Biochim. Biophys. Acta Mol. Cell Res., 1865,
j.jneumeth.2008.01.024.
1579-1589, doi: 10.1016/j.bbamcr.2018.08.012.
38.
Khotskin, N. V., Plyusnina, A. V., Kulikova,
49.
Martínez, G., Vidal, R. L., Mardones, P., Serrano,
E. A., Bazhenova, E. Y., Fursenko, D. V., Sorokin,
F. G., Ardiles, A. O., Wirth, C., Valdés, P., Thielen, P.,
I. E., Kolotygin, I., Mormedec, P., Tereninac,
Schneider, B. L., Kerr, B., Valdés, J. L., Palacios,
E. E., Sheveleva, O. B., and Kulikov, A. V. (2019)
A. G., Inestrosa, N. C., Glimcher, L. H., and Hetz, C.
On association of the lethal yellow (AY) mutation in
(2016) Regulation of memory formation by the
the agouti gene with the alterations in mouse brain
transcription factor XBP1, Cell Rep., 14, 1382-1394,
and behavior, Behav. Brain Res.,
359,
446-456,
doi: 10.1016/j.celrep.2016.01.028.
doi: 10.1016/j.bbr.2018.11.013.
50.
Cissé, M., Duplan, E., Lorivel, T., Dunys, J., Bauer, C.,
39.
Kulikov, A. V., Morozova, M. V., Kulikov, V. A.,
Meckler, X., Gerakis, Y., Lauritzen, I., and Checler, F.
Kirichuk, V. S., and Popova, N. K. (2010) Automated
(2017) The transcription factor XBP1s restores hip-
analysis of antidepressants’ effect in the forced swim
pocampal synaptic plasticity and memory by control
test, J. Neurosci. Methods, 191, 26-31, doi: 10.1016/
of the kalirin-7 pathway in Alzheimer model, Mol.
j.jneumeth.2010.06.002.
Psychiatry, 22, 1562-1575, doi: 10.1038/mp.2016.152.
40.
Hetz, C., and Saxena, S. (2017) ER stress and the un-
51.
Zhang, G., and Stackman, R. W. (2015) The role
folded protein response in neurodegeneration, Nat. Rev.
of serotonin
5-HT2A receptors in memory and
Neurol., 13, 477-491, doi: 10.1038/nrneurol.2017.99.
cognition, Front. Pharmacol., 6, 225, doi: 10.3389/
41.
Henderson, Y. O., Smith, G. P., and Parent, M. B.
fphar.2015.00225.
(2013) Hippocampal neurons inhibit meal onset,
52.
Rambousek, L., Palenicek, T., Vales, K., and
Hippocampus, 23, 100-107, doi: 10.1002/hipo.22062.
Stuchlik, A. (2014) The effect of psilocin on memo-
42.
Hannapel, R., Ramesh, J., Ross, A., Lalumiere, R. T.,
ry acquisition, retrieval, and consolidation in the rat,
Roseberry, A. G., and Parent, M. B. (2019) Postmeal
Front. Behav. Neurosci., 8, 1-7, 180, doi: 10.3389/
optogenetic inhibition of dorsal or ventral hippocampal
fnbeh.2014.00180.
pyramidal neurons increases future intake, eNeuro, 6,
53.
Lindholm, P., and Saarma, M. (2022) Cerebral dopa-
457-475, doi: 10.1523/ENEURO.0457-18.2018.
mine neurotrophic factor protects and repairs dopa-
43.
Dubrovina, N. I., Zinov’ev, D. R., Zinov’eva, D. V.,
mine neurons by novel mechanism, Mol. Psychiatry,
and Kulikov, A. V. (2009) Learning and extinction of a
27, 1310-1321, doi: 10.1038/s41380-021-01394-6.
БИОХИМИЯ том 88 вып. 8 2023
1
336
КАМИНСКАЯ и др.
THE EFFECT OF HIPPOCAMPAL OVEREXPRESSION OF DOPAMINE
NEUROTROPHIC FACTOR (CDNF) ON THE BEHAVIOR OF MICE
WITH GENETIC PREDISPOSITION TO DEPRESSIVE-LIKE BEHAVIOR
Y. P. Kaminskaya, T. V. Ilchibaeva, N. V. Khotskin, V. S. Naumenko, and A. S. Tsybko*
Federal research center Institute of Cytology and Genetics, Siberian Branch of the Russian Academy of Sciences,
630090 Novosibirsk, Russia; e-mail: antoncybko@mail.ru
Cerebral dopamine neurotrophic factor (CDNF) is the promising tool for treatment of Parkinson’s disease.
However, its role in the regulation of non-motor behavior, including various psychopathologies, remains
unclear. In this regard, the aim of present work was to study the effect of CDNF overexpression in the
hippocampus on the behavior of ASC mice (Antidepressant Sensitive Cataleptics) with a genetic predis-
position to depression-like behavior. CDNF overexpression in mouse hippocampal neurons was induced
using an adeno-associated viral vector. Four weeks after stereotaxic injection of the AAV-CDNF construct
into the dorsal hippocampus, home cage behavior, exploratory, anxiety and depressive-like behaviors,
as well as spatial and associative learning were assessed. We found significant improvements in the dynamics
of spatial learning in the Morris water maze in CDNF-overexpressing animals. At the same time, no effect
of CDNF was found on other studied behaviors. The behavior of the experimental animals in the home cage
conditions did not differ from that in the control group, except for a decrease in the total amount of food
eaten and a slight increase in the number of sleep episodes in the light phase of the day. In the present study
we also attempted to determine the molecular basis for the above mentioned changes by genes expression
assessment. We did not find significant changes in the mRNA level of key kinases, genes involved in neuro-
plasticity and neuronal survival as well as genes encoding receptors for the main neurotransmitter systems.
However, animals overexpressing CDNF show increased lever of spliced Xbp indicating activation of the
Ire1α/Xbp1 pathway traditionally associated with ER stress. Immunohistochemical analysis showed that
CDNF was co-localized with the ER marker calreticulin. Thus, the effects of endogenous CDNF on behav-
ior that we have found may be mediated by a specific molecular cascade, which emphasizes its difference
from classical neurotrophic factors.
Keywords: neurotrophic factors, cerebral dopamine neurotrophic factor CDNF, depressive-like behavior, learning,
ER stress, unfolded protein response UPR
БИОХИМИЯ том 88 вып. 8 2023