НЕФТЕХИМИЯ, 2021, том 61, № 3, с. 291-310
УДК 66.074.5.081.3
ОПТИМИЗАЦИЯ МЕТОДОВ ОЧИСТКИ ГАЗОВЫХ СМЕСЕЙ
ОТ ДИОКСИДА УГЛЕРОДА (ОБЗОР)
© 2021 г. Э. Г. Новицкий1,*, С. Д. Баженов1, А. В. Волков1
1 Институт нефтехимического синтеза им. А.В. Топчиева РАН, Москва, 119991 Россия
*E-mail: ednov@ips.ac.ru
Поступила в редакцию 18 декабря 2020 г.
После доработки 10 марта 2021 г.
Принята к публикации 12 апреля 2021 г.
Проведен анализ современных технологий очистки от диоксида углерода различных газовых смесей
(природный газ, газы конверсии углеводородов в производствах аммиака и синтез-газа), а также дымовых
газов, образующихся при сжигании углеродсодержащего сырья в энергетике. Обсуждены различные
направления совершенствования процессов сорбции-десорбции, как с точки зрения расширения круга
применяемых аминовых абсорбентов, так и возможности применения аппаратов нового типа - мем-
бранных контакторов с половолоконными мембранами или керамическими трубчатыми элементами.
Рассмотрен вариант процесса декарбонизации насыщенного раствора амина при температуре не выше
90оС с применением растворов с концентрацией моноэтаноламина (МЭА) 12%, позволяющий избежать
его термоокислительной деструкции.
Ключевые слова: абсорбция, десорбция, амины, деструкция термоокислительная, мембраны полимер-
ные, половолоконные, керамические, контакторы мембранные
DOI: 10.31857/S0028242121030011
В обзоре рассматриваются проблемы оптимиза-
абсорбция водными растворами алканоламинов, в
ции технологий очистки от диоксида углерода газо-
первую очередь МЭА, применяемыми уже почти
вых смесей (природный газ, газы конверсии угле-
сто лет [4]. Этот базовый процесс успешно исполь-
водородов в производствах аммиака и синтез-газа),
зуется и в настоящее время, естественно, постоян-
а также дымовых газов, образующихся при сжига-
но совершенствуясь как с точки зрения технологии
нии углеродсодержащего сырья в энергетике. Ак-
(расширение перечня применяемых аминов, совер-
туальность этих проблем по-прежнему остается
шенствование параметров процесса), так и аппа-
достаточно острой, поскольку эмиссия диоксида
ратурного оформления (конструкция абсорберов и
углерода в атмосферу постоянно возрастает, до-
десорберов диоксида углерода) [5-9]. Несмотря на
стигнув в 2018 г. значений около 35 Гт. Лидерами
очевидные проблемы, характерные для этих про-
являются КНР (9.4 Гт), США (5.1 Гт); РФ находит-
цессов (термическая и термоокислительная дегра-
ся на 5 месте (1.5 Гт) [1]. При этом важно отметить,
дация аминов, коррозия оборудования и трубопро-
что в США, например, около половины годовых
водов), существует обоснованная точка зрения, что
выбросов диоксида углерода приходится на дымо-
они будут востребованы до 30-х годов текущего
вые газы энергетического сектора [2, 3]. Хотя по
столетия [10, 11].
некоторым данным в 2019 г. мировая эмиссия оста-
К настоящему времени сложилось устойчивое
лась на уровне 2018 г. (Financial Times. 11.02.2020.),
представление о механизме процессов термиче-
проблема ее снижения остается актуальной.
ской и термоокислительной деградации и составе
Наиболее распространенным способом очист-
образующихся продуктов [12-14]. Согласно [12] в
ки различных газовых смесей от кислых приме-
процессе деградации МЭА образуются такие кор-
сей (сероводород, диоксид углерода) является их
розионно-активные продукты как 2-оксазолидон,
291
292
НОВИЦКИЙ и др.
Таблица 1. Состав термостабильных солей (ТСС)
накоплению смолообразных продуктов. Согласно
Термостабильные соли
Содержание, мас. % (мг/л)
[14] потери МЭА уже при 120°C могут достигать
Оксалаты
0.025 (250)
55.7% за 5000 ч работы, что соответствует практи-
Сульфатыa
0.050 (500)
чески полной его потере за год (8520 ч) эксплуа-
Формиаты
0.050 (500)
тации. Это означает, что систему ежегодно необ-
Ацетаты
0.100 (1000)
ходимо перезагружать свежим раствором МЭА (в
Тиосульфатыa
0.100 (1000)
скобках отметим, что именно так и происходит на
Хлоридыa
0.050 (500)
практике). По данным [12, 14] для исключения та-
a Накапливаются при очистке дымовых газов.
ких потерь температура в кубе десорбера должна
быть не больше 110°C.
дигидроксиэтилмочевина,
1-(2-гидроксиэтил)-2-
В более поздних обзорах [18, 19] также представ-
имидазолидон и N-(2-гидроксиэтил)-этилендиа-
лены результаты работ по идентификации продук-
мин. Кроме того, при очистке газов, содержащих
тов деструкции алканоламинов и методов очистки
кислород (дымовые газы), в системе происходит
от них рабочих растворов абсорбентов. Следует
образование и накопление продуктов окисления
отметить, что в литературе системно освещены и
аминов (табл. 1), также инициирующих коррозион-
вопросы коррозии аппаратуры и трубопроводов,
ные процессы [15, 16]. Следует отметить, что обра-
обусловленные появлением в растворах аминовых
зование всех вышеперечисленных продуктов (они
абсорбентов коррозионно-активных продуктов
получили название термостабильных солей «ТСС»,
термо- и термоокислительной деструкции [20-25].
или «heat stable salts - HSS» в англоязычной лите-
В указанных работах последовательно рассмотре-
ратуре) характерно и для процессов с применением
ны все блоки технологической схемы процессов
в качестве абсорбента растворов других алканола-
абсорбции-десорбции, обозначены коррозион-
минов (диэтаноламин, метилдиэтаноламин и др.).
но-опасные аппараты и узлы. В [25] показано, что
Вклад ТСС в общие потери МЭА в процессе
наиболее опасными участками являются нижняя
цикла «абсорбция-десорбция» может достигать
часть абсорбера, где происходит экзотермический
2.2 кг МЭА/кг поглощенного СО2 [17].
процесс поглощения диоксида углерода и темпе-
Дальнейшие эволюции состава абсорбцион-
ратура максимально насыщенного абсорбента мо-
ных растворов при температурах в кубовой части
жет достигать 80°C. Далее с точки зрения корро-
десорбера 115-135°C приводят к образованию и
зии опасным является десорбер (кубовая часть) и
затем весь тракт от десорбера до возврата тощего
раствора абсорбента в обратный теплообменник,
где температура абсорбента составляет 110-135°C.
Лабораторные исследования влияния условий про-
цесса на скорость коррозии углеродистой стали
[26] показали, что концентрация некарбонизиро-
ванного (α = 0) амина слабо влияет на его коррози-
онную активность; аналогичная зависимость была
показана в [23] на примере нержавеющей стали
(рис. 1). Это противоречит общепризнанному мне-
нию о том, что концентрация амина в абсорбционном
растворе должна составлять не более 20-30 мас. %
[27, 28].
Очевидно, что в исследованном диапазоне тем-
ператур скорость коррозии линейно возрастает с
увеличением температуры карбонизированного
раствора МЭА. Так, даже при сравнительно уме-
Рис. 1. Влияние температуры и степени карбонизации
ренной температуре (50°C) и низкой степени кар-
α = МСО
/ММЭА 30%-ного раствора МЭА на корро-
2
зию нержавеющей стали [23]: ■ - α = 0.5; ○ - α = 0.25;
бонизации раствора (α = 0.25), скорость коррозии
Δ - α = 0.
углеродистой стали составляет около 0.1 мм/г.
НЕФТЕХИМИЯ том 61 № 3 2021
ОПТИМИЗАЦИЯ МЕТОДОВ ОЧИСТКИ ГАЗОВЫХ СМЕСЕЙ
293
CO2
Очищенный газ
Конденсатор
на компрессию
Холодильник
тощего амина
Возвратный
конденсат
Насос конденсата
Насос
Емкость
Десорбер
Абсорбер
Теплообменник
Дымовой газ
Na2CO3
МЭА
регенерация
Шлам
Рис. 2. Принципиальная технологическая схема очистки газов от диоксида углерода [39].
Что же касается значений реальных температур
схеме (1), относятся к быстрым. Однако они прохо-
(120-135°C) и концентраций диоксида углерода,
дят через стадию образование карбамата, для чего
то, как показали пилотные испытания, коррозия в
необходим атом водорода при атоме азота, поэтому
случае углеродистой стали может составлять не-
они возможны только для первичных и вторичных
сколько мм/г [29]. Это приводит к тому, что 25%
аминов [34-39]. Обобщенная схема очистки дымо-
эксплуатационных затрат составляют расходы на
вых газов представлена на рис. 2.
борьбу с коррозией оборудования и трубопроводов
Типичный состав дымового газа для ТЭЦ, рабо-
[30-33].
тающей на угле, имеет следующий состав, об. %:
Общепринятый механизм процесса очистки
CO2-14, O2 -5, N2-81; ppm: SOx -300-3000, NOx -
технологических газов от диоксида углерода пред-
100-1000, а также 1000-10000 мг/м3 частиц лету-
полагает наличие двух основных реакций:
чей сажи. Типичный состав дымового газа при ра-
боте на природном газе содержит, об. %: CO2 - 4,
(1)
O2 - 5, N2 - 1; ppm: SОх - 300-3000, NOx - 100-500
(2)
и ~10 мг/м3 твердых частиц.
Дымовой газ поступает в нижнюю часть аб-
где R1, R2, и R3 - алкильные группы или водород.
сорбера. Давление газа 1-9 атм. Сверху абсор-
Реакции, протекающие по механизму (2), яв- бера выходит очищенный от СО2 дымовой газ
ляются медленными, поскольку контролируются (степень извлечения СО2 >90%), а снизу - на-
медленной диссоциацией угольной кислоты с об- сыщенный СО2 абсорбент. Этот абсорбент про-
разованием бикарбоната. Поэтому они мало при- ходит через обратный теплообменник, тепло-
годны для процесса очистки дымовых газов. Это носитель
- возвратный тощий (очищенный)
связано с тем обстоятельством, что парциальное абсорбент после десорбера. Нагретый до
давление диоксида углерода в них низкое, а ско-
90-110°C насыщенный абсорбент поступает в
рости потока большие, поэтому абсорбент должен
верхнюю часть десорбера. В этой части десорбе-
обеспечивать очень высокую скорость абсорбции
ра насыщенный СО2 раствор имеет температуру,
. Этим требованиям отвечают именно первич- которая поддерживается подачей в кубовую часть
СО2
десорбера через выносной кипятильник пара с тем-
ные амины. Напротив, реакции, протекающие по
НЕФТЕХИМИЯ том 61 № 3 2021
294
НОВИЦКИЙ и др.
пературой 120-130°C. При этом происходит выде-
торов применяются, главным образом, все те же
ление СО2. Таким образом на выходе из верхней
органические амины [42-50]. Так в [48] исследо-
части десорбера абсорбент содержит минимальное
вана возможность получения эффективных адсор-
количество СО2. Выделенный CO2 через холодиль-
бентов диоксида углерода по достаточно типичной
ник-конденсатор поступает в линию всасывания
для этих работ схеме. На первом этапе проводит-
компрессора, затем при давлениях до 100 атм за-
ся конденсация аминосиланов в порах адсорбен-
качивается, например, в нефтяные скважины для
та, например, силикагелей и на втором - гидролиз
увеличения их отдачи.
аминосиланов, обеспечивающий их прививку с
фиксацией на внутренней поверхности пор. В ра-
При очистке природного газа общая конфигу-
боте исследованы два аминосилана: (3-аминопро-
рация технологической схемы сохраняется, од-
пил) триметоксисилан и N-[3-(триметоксисилил)-
нако технологические параметры, естественно,
пропил]этилендиамин. Состав и структура моди-
отличаются. Это определяется, с одной стороны,
фицированных адсорбентов были подтверждены
составом и исходным давлением очищаемого при-
данными элементного состава, рентгеновской и
родного газа, а с другой - требованиями к составу
ИК-спектроскопии. Удельная адсорбционная ем-
очищенного газа. Абсорбция кислых газов (H2S и
кость модифицированных силикагелей по диок-
CO2) проводится при давлениях до 100 атм, а их
сиду углерода возрастала в среднем в 10-12 раз и
содержание может составлять несколько десятков
достигала высоких значений 470-700 мкмол/г. Сле-
процентов (например, природный газ астраханско-
дует отметить, что указанные данные авторам уда-
го месторождения содержит сероводорода около 30
лось получить только при температуре десорбции
и диоксид углерода - около 20 об. %). Главная цель
600°C, а в области температур ≤150°C десорбция
очистки - минимизация содержания кислых га-
практически не наблюдалась (отметим в скобках,
зов. Количественное извлечение Н2S до следовых
что десорбцию осуществляли в потоке инертного
значений его концентрации обычно происходит, в
газа). Конечный результат выглядит очень привле-
то время как остаточное содержание СО2 может
кательным, но его практические перспективы сом-
составлять 2-3% для обычных применений и 50-
нительны. Характерно, что и другие публикации на
100 ppm для производства сжиженного природного
эту тему связаны с модификацией исходных адсо-
газа (СПГ, LNG - Liquefied Natural Gas). В этом слу-
рбентов различными комбинациями органических
чае применяют вторичные или третичные амины [26].
аминов, поэтому трудно представить, что такая
Естественно, что с учетом существенных
технология сможет составить конкуренцию абсор-
«родовых» недостатков абсорбционно-десорбци-
бционным технологиям с применением напрямую
онной технологии очистки от СО2 различных про-
растворов аминов. Авторы [51] исследовали альтер-
мышленно важных газовых смесей с применением
нативный процесс адсорбции диоксида углерода с
водных растворов аминов (главным образом, моно-
применением в качестве адсорбентов активирован-
этаноламина), продолжаются поиски либо новой
ных углей, полученных из различных целлюлозо-
технологии, либо способов модернизации имею-
содержащих отходов сельскохозяйственных про-
щейся. Анализ литературных данных показывает,
изводств. Экспериментальные значения величины
что это касается, с одной стороны, поиска новых
энергии активации процесса (≤ 42 кДж/мол СО2)
аминовых абсорбентов, а с другой - адаптации
свидетельствуют по мнению авторов о физическом
мембранных технологий и аппаратов.
характере адсорбции.
АДСОРБЦИЯ
АБСОРБЦИЯ РАСТВОРАМИ АМИНОВ
Судя по содержанию публикаций процесс адсо-
Как уже отмечалось выше, наиболее распростра-
рбции по-прежнему остается интересным с пози-
ненными представителями класса аминов в процес-
ций расширения круга применяемых адсорбентов
сах очистки газовых смесей от диоксида углерода
[40, 41]. Однако в основном эти публикации посвя-
являются моноэтаноламин, диэтаноламин и метил-
щены исследованию химически модифицирован-
диэтаноламин. Отмечалось также, что применение
ных адсорбентов, в которых в качестве модифика-
этих аминов неизбежно связано с необходимостью
НЕФТЕХИМИЯ том 61 № 3 2021
ОПТИМИЗАЦИЯ МЕТОДОВ ОЧИСТКИ ГАЗОВЫХ СМЕСЕЙ
295
Таблица 2. Перечень аминов-абсорбентов [52], а также концентрация амина и удельная нагрузка CO2
МЭА
30; (2.5)
0.58, 0.79; (0.47)
Диэтилентриамин
(2.5)
1.83
ДЭА
30
0.50
Триэтилентетрамин
(2.5)
2.1
МДЭА
50; (2.0)
0.52; (0.97)
Тетраэтиленпентамин
(0.5)
3.03
АМП
30
0.80; 0.63
N-(2-Гидроксиэтил)этилендиамин
(2.5)
1.36
ТЭА
30
0,39; 0.27
N,N'-бис(2-Гидроксиэтил)этилендиамин
(2.5)
1.21
3-Амино-1-пропанол
(2.5)
0.83
Пиперидин
(0.5)
1.40
2-Амино-1-бутанол
(2.5)
1.34
2-Метилпиперидин
(0.5)
1.14
1-Амино-2-пропанол
30; (0.5)
0.54; (0.89)
4-Аминопиперидин
(0.5)
1.90
4-Амино-1-бутанол
30; (2.5)
0.59; 0.89
Пиперазин
(0.5)
1.30
5-Амино-1-пентанол
(2.5)
0.83
1-Метил пиперазин
(0.5)
1.19
Этиламин
(2.5)
0.69
транс-2,5-Диметилпиперазин
(0.5)
1.36
Пропиламин
(2.5)
0,97
N-этилпиперазин
(1.0)
1.43
Бутиламин
(2.5)
1.07
2-(1-Пиперазинил)этиламин
(1.0)
1.90
втор-Бутиламин
(2.5)
0.85
2-(1-Пиперазинил)этан
(1.0)
0.90
Изобутиламин
(2.5)
0.73
Азетидин
(0.24)
2.43
N-пентиламин
(2.5)
0.90
1,4-Диазобицикло [2.2.2] октан
(2.5)
0.83
Гексиламин
(0.1)
2.36
4-(Диметиламино)-2-бутанол
(2.0)
0.98
Этилендиамин
(2.5)
1.28
4-(Дпропиламино)-2-бутанол
(2.0)
0.56
1,3-Диаминопропан
(2.5)
1.27
4-(Дибутиламино)-2-бутанол
(2.0)
0.35
1,2-Диаминопропан
(2.5)
1.16
4-[(2-Гидроксиэтил)(метил)амино]-2-бутанол
(2.0)
0.91
1,4-Диаминопропан
(2.5)
1.42
4-[(2-Гидроксилэтил)(этил)амино]-2-бутанол
(2.0)
0.95
Гексаметилендиамин
(1.5)
1.52
МДЭА
(2.0)
0.83
1,7-Диаминогептан
(2.5)
1.35
Соль аминокислоты (глицина)
(2.0)
0.32
проведения десорбции СО2 при температурах
тически идеальной селективностью абсорбции
≥120°C, что приводит к увеличению расхода аминов
СО2/СН4 180-1000 (этилендиамин, диэтилентри-
(обусловленному их термической и термоокисли-
амин) могут быть интересны при очистке природ-
тельной деградацией), увеличению энергетических
ного газа. С точки зрения поиска термостойких
затрат на стадии десорбции и коррозии оборудова-
аминов, в первую очередь представляют интерес
ния. Эти обстоятельства определяли направление
так называемые стерически затрудненные амины,
активных поисков аминовых абсорбентов, которые
содержащие разветвленные заместители у атома
являются более термостойкими и одновременно
азота.
позволяющими понижать температуру десорбции.
Анализ литературы последнего десятилетия
К настоящему времени известны результаты иссле-
свидетельствует, что самым востребованным
дований по применению водных растворов более
классом таких соединений являются различные
пятидесяти аминов, включая и довольно экзотиче-
пропаноламины и их комбинации с моноэтанола-
ские (табл. 2) [52]. Данные таблицы свидетельству-
мином, метилдиэтаноламином и некоторыми дру-
ют не только о широте номенклатуры аминов, но
гими реально применяемыми аминами [53-58].
также и об их возможностях по удельной нагруз-
В [53] представлены результаты исследований
ке СО2 (МСО2/Мамин) при температурах абсорбции
термоокислительной деградация водных раство-
22-40°C. Выборочные данные для аминов с прак-
ров следующих аминов:
2-амино-2-гидроксиме-
НЕФТЕХИМИЯ том 61 № 3 2021
296
НОВИЦКИЙ и др.
тил-1,3-пропандиола (АГМПД), пиперазина (Пз),
СО2. На основании полученных результатов авто-
2-амино-1,3-пропандиола (ПД), смеси
2-амино-
ры полагают, что оптимальным составом раствора
2-метил-1-пропанола (АМП), моноэтаноламина
абсорбента, обеспечивающим сочетание макси-
(МЭА) и водного раствора смеси (АГМПД + Пз),
мальной скорости абсорбции СО2 с его конечной
а также водных растворов этих же аминов в кар-
концентрацией в насыщенном растворе, является
бонизированной форме. Общий вывод из анализа
смесь состава 3ММЭА и 3МАМП. Эффективность
приведенных данных состоит в том, что присут-
насыщения такого раствора диоксидом углерода
ствие кислорода и диоксида углерода существенно
выше, чем раствора с суммарной концентрацией
влияет на степень термоокислительной деструкции
5ММЭА.
различных аминов и их смесей. Так, установлено,
Эффективность АМП как абсорбента СО2 была
что стерически затрудненные амины (АГМПД и
оценена и в работе [60], где представлены результа-
АМП) в наибольшей мере устойчивы к термоокис-
ты сравнительных исследований процессов абсор-
лительной деструкции, чем амины с линейными
бции и десорбции диоксида углерода растворами
заместителями у атома азота. Однако эти же ами-
моноэтаноламина, диэтаноламина, метилдиэтано-
ны в некарбонизированной форме более подвер-
ламина и 2-амино-2-метил-1-пропанола. Десорб-
жены термоокислительной деструкции. В то же
цию растворов исследовали в интервале темпера-
время смеси с пиперазином, например, АГМПД,
тур 60-110°C в зависимости от удельной нагрузки
оказались более устойчивыми к термоокислитель-
по СО2 в аппарате насадочного типа. Наиболее ак-
ной деструкции. Поэтому водные растворы смеси
тивным в процессе десорбции был раствор АМП с
2-амино-2-гидроксиметил-1,3-пропандиола с пипе-
исходной нагрузкой 0.4МCO2/МАМП при температу-
разином по мнению авторов могут быть использова-
ре 110°C, скорость десорбции которого составила
ны в качестве абсорбентов вместо растворов МЭА
85×10-3 ммол/с (в скобках отметим, что десорбция
в процессах очистки различных газовых смесей от
активировалась продувкой раствора потоком влаж-
диоксида углерода. Авторы статьи [59] показали,
ного азота). Очевидно, что водные растворы ами-
что смеси третичных аминов - 2-(диметиламино)-
нопропанолов, включая и их смеси с другими (уже
этанола и 3-диметиламно-1-пропанола - с пер-
широко известными) аминами, в последние годы
вичными и вторичными аминами являются более
являются популярными объектами исследований.
активными абсорбентами с точки зрения нагрузки
Так, Wang T. и Jens K.J. [61-63] провели серию
по диоксиду углерода, теплоты абсорбции и имеют
работ, посвященных процессам абсорбции, десор-
более быструю кинетику абсорбции, чем метилди-
бции и деградации как самого АМП так и его сме-
этаноламин.
сей с другими аминами, в т.ч. моноэтаноламином и
пиперазином. Особняком, на наш взгляд, стоит пу-
В работе [55] исследована возможность улучше-
бликация [57], в которой представлены результаты
ния абсорбции диоксида углерода с применением
исследований процессов абсорбции и десорбции
смесей аминов, включающих МЭА и различные
диоксида углерода растворами АМП, проведенных
третичные амины (третамин), такие как N,N-диме-
на пилотной установке (табл. 3 и 4).
тилэтаноламин (ДМЭА), N,N-диэтилэтаноламин
(ДЭЭА) и
2-амино-2-метил-1-пропанол (АМП).
Привлекает внимание очень высокое соотноше-
Данные по скорости абсорбции диоксида углеро-
ние высоты насадки к диаметру - 30 раз (обычно
да растворами указанных смесей оказались выше,
не превышает значения 5-10 раз) [11].
чем у растворов соответствующих аминов, незави-
Температура в абсорбере находится на уровне
симо от типа третичного амина в смеси. При этом
45-50°C. В десорбере температура составляет око-
наибольшая скорость наблюдалась для смеси со-
ло 118оС в кубовой части и стабилизируется на зна-
става 3ММЭА/3Мтрет-амин и на нее практически не
чениях ≈ 100-102°C на высоте насадки около 4 м.
влиял тип третичного амина. Более того, скорость
Здесь привлекают внимание два обстоятельства.
абсорбции СО2 для указанных смесей состава
Первое - превышение потерь на стадии абсорбции
3ММЭА/3Мтрет-амин практически не отличается от
за счет деградации АМП, второе - значительные
скорости абсорбции в растворе состава 5ММЭА при
потери АМП на стадии абсорбции за счет эмиссии
аналогичной температуре и степени нагрузки по
(унос амина с отходящим очищенным газом). Все
НЕФТЕХИМИЯ том 61 № 3 2021
ОПТИМИЗАЦИЯ МЕТОДОВ ОЧИСТКИ ГАЗОВЫХ СМЕСЕЙ
297
Таблица 3. Характеристики насадочных аппаратов - абсорбера и десорбера [57]
Аппараты пилотной
Абсорбер
Десорбер
установки (насадочные)
Диаметр, м
0.15
0.10
Высота насадки
4.36
3.89
Насадка
«Sulzer Mellapak 250Y»
«Sulzer Mellapak 250Y»
ТИП, VАПП - 0.019 м3
Структурированная (удельная поверхность
Структурированная (удельная
250 м2/м3), S насадки = 4.75 м2
поверхность 250 м2/м3)
Таблица 4. Потери от деградации и эмиссии АМП в процессах абсорбции и десорбции
Параметры
Единица измерения
Абсорбция
Десорбция
Всего
Деградация
АМП
кг/т СО2
2.09×10-3
8.10×10-4
2.90×10-3
В том
частей ацетона
-
1.34×10-6
1.36×10-6
2.70×10-6
числе
4-оксазолидинон
-
2.7×10-6
2.65×10-6
5.35×10-6
2,4-лутидин
-
4.24×10-4
4.29×10-6
4.26×10-4
Эмиссия
АМП
кг/т СО2
1.25×10-3
2.45×10-6
1.25×10-3
В том
частей ацетона
-
7.88×10-9
1.70×10-15
7.88×10-9
числе
4-оксазолидинон
-
1.56×10-8
3.37×10-15
1.56×10-8
2,4-лутидин
-
1.11×10-5
1.90×10-8
1.11×10-5
эти данные серьезно отличаются от известных дан-
части снижения энергопотребления и удельного
ных по МЭА, в первую очередь это относится к по-
расхода абсорбента (7-8 л/м3) не удалось. Лучшим
терям при десорбции, которые в десятки раз ниже
абсорбентом оказался 40%-ный раствор МЭА, ис-
известных данных для МЭА. Авторы объясняют
следованный в тех же условиях.
это маломасштабностью эксперимента и полагают,
Применение солей глицина для этих же целей
что необходимы исследования с применением бо-
описано и в патенте [65]: «Поглотительный рас-
лее крупных аппаратов.
твор для абсорбции диоксида углерода и способ
И, наконец, следует отметить, что есть данные
ускорения абсорбции посредством диоксида гер-
о попытках применения в качестве абсорбентов и
мания». Водный раствор содержит абсорбент диок-
соединений, не относящихся к классу алканолами-
сида углерода на основе солей аминокислоты и до-
нов. Например, в [64] представлены результаты ис-
бавку, активирующую скорость абсорбции, которая
следования по применению в качестве абсорбента
представляет собой, например, диоксид германия.
растворов натриевой соли глицина. Исходное сооб-
В процессе абсорбции диоксид германия оказы-
ражение состоит в том, что такой абсорбент (соль
вает каталитическое действие на стадии реакции
аминоуксусной кислоты) исключит его потери за
диоксида углерода с солью аминокислоты. Концен-
счет уноса как на стадии абсорбции так и десорб-
трация соли аминокислоты составляет 30%, а соот-
ции. На основе данных лабораторных исследований
ношение концентраций между солью аминокисло-
очистки дымового газа с применением растворов
ты и диоксидом германия находиться в интервале
различной концентрации была сделана попытка ре-
(мас. %): 99.9/0.1-90.0/10.0. По мнению авторов,
ализации этого процесса в промышленных услови-
преимущество предлагаемого способа состоит и
ях на ТЭЦ в городе Dürnrohr (Австрия), исходя из
в том, что абсорбенты - соли аминокислот - неле-
полученных лабораторных данных по снижению
тучи, в то время как гетероциклические амины и
энергозатрат. Применяли водные растворы с кон-
алканоламины летучи и сбрасываются в окружа-
центрацией глицината натрия 15, 25 и 40 мас. %.
ющую среду вместе с очищенным дымовым газом
Однако подтвердить лабораторные результаты в
(унос), что ведет к их потере и нежелательному
НЕФТЕХИМИЯ том 61 № 3 2021
298
НОВИЦКИЙ и др.
загрязнению окружающей среды. И, наконец, поя-
Таблица 5. Состав и свойства полиамидинов
вились сообщения о применении в качестве абсор-
№ п/п
R1
R2
R3
Mn
Tg, °C
бентов соединений класса амидинов [66, 67, 68]. В
1
(CH2)6
Me
Et
2740
6
[66] синтез полиамидина осуществляли в два эта-
2
(CH2)6
Et
Me
6260
0
па. На первом этапе [реакция (3)]
3
(CH2)6
i-Pr
Me
3910
-11
4
(CH2)6
Ph
Me
2160
14
5
[(CH2)2O]2
Ph
Me
5730
1
(CH2)2
R2C(OR3)3 + H2N-R1-NH2
R2
H+, 140-220°C
(3)
R1
N
N
−R3OH
H
n
(5)
смесь αω-диамина
(23.8
ммол), ортоэфира
(25 ммол) и р-крезола (20 ммол, растворитель)
нагревается в реакторе с мешалкой и под азотной
подушкой в течение 20 мин при 80°C. Затем тем-
пература повышается до 140°C и перемешивание
продолжается в течение двух часов для удале-
ния образующихся при поликонденсации спиртов
R3OH. После чего давление в реакторе понижают
до 0.2 кПа и в течение одного часа смесь выдержи-
Абсорбцию проводили при 40°C, а десорбцию -
вают при 180°C. Финальная процедура - удаление
при 80°C при постоянной продувке системы азо-
п-крезола - проводится при температуре 200°C.
том. Степень извлечения СО2 устойчиво состав-
Полученный таким образом олигоамидин исполь-
ляла ~80%, что обеспечивает преимущество пе-
зуется на втором этапе для синтеза полиамидина
ред аминами и амидинами с низкой молекулярной
методом сополиконденсации с, например, полиэти-
массой при получении стабильных и регенерируе-
ленгликолем ([(CH2)mO]n [(CH2)2]) по реакции (4):
мых абсорбентов диоксида углерода. Данные ана-
логичного характера были представлены и в [67].
В этой работе исследовали абсорбцию СО2 с при-
R2
менением не линейных, а циклических амидинов,
+
O
содержащих силатранильные
(2,8,9-триоксаси-
R
N
N
1
HO
H
H
латрициклоундекановые) группы на основе три-
n
n
этаноламинов. Абсорбцию проводили при 25°C, а
R2
десорбцию - при 60°C, причем десорбцию прово-
дили в условиях сдувки СО2 аргоном. Одновремен-
O
(4)
R1
N
N+
H
но было показано, что пятичленные циклические
H
n
амидины, содержащие силатрановые группы типа
n
R-Si(OCH2 CH2)3N, также абсорбируют СО2 в ука-
занных условиях, хотя и не столь активно. И, на-
Фрагменты полиэтиленгликоля в макромолеку-
против, ациклические амидины с силатрановыми
лах полиамидинового абсорбента обеспечивают
группами вообще не поглощают СО2. И, наконец,
его пластичность (см. значения Тg в табл. 5).
в [68] было показано, что амидины циклической
С применением полученных полиамидинов
структуры реагируют с диоксидом углерода с об-
было проведено несколько циклов абсорбции-де-
разованием (только в присутствии хотя бы следов
сорбции СО2
в течение 1500 мин. Механизм про-
воды) устойчивого цвиттерион-аддукта с последу-
цесса абсорбции представлен реакцией (5):
ющим преобразованием его в бикарбонат амидина
НЕФТЕХИМИЯ том 61 № 3 2021
ОПТИМИЗАЦИЯ МЕТОДОВ ОЧИСТКИ ГАЗОВЫХ СМЕСЕЙ
299
(подтверждено данными ИК-спектроскопии) по ре-
следований и успех этого направления. Типичная
акции (6):
публикация работа содержит все характерные эта-
пы исследований [71].
N
N
Выбор материала. Сначала были выбраны пло-
-
+
+
HCO3
ские (листовые) мембраны по 10 образцов коммер-
(6)
N
N
чески доступных плоских мембран на основе 4
H
различных типов полимеров, а именно: полипро-
O
-
O
пилена (ПП), поливинилдиенфторида (ПВДФ), по-
В отсутствие следов воды реакция не идет. По-
литетрафторэтилена (ПТФЭ) и нейлона. Для этих
добные попытки найти замену классу алканолами-
мембран были определены газопроницаемость (N2,
нов столь экзотическими и недешевыми абсорбен-
CO2) и краевой угол смачивания для исходных об-
разцов и после выдержки в 30%-ном растворе мо-
тами (сегодня 0.1 л линейного амидина стоит около
4 $, т.е. ~40 тыс. $/т) лишний раз свидетельствуют
ноэтаноламина в течение 2 мес. при температурах
об остроте проблемы.
293.15, 313.15 и 353.15 К. Было установлено, что
ПТФЭ (5 образцов) показал отличную стабиль-
ность во времени по газопроницаемости и несма-
МЕМБРАННЫЕ КОНТАКТОРЫ ДЛЯ
чиваемости при температурах 313.15 и 353.15 К.
ПРОЦЕССОВ АБСОРБЦИИ-ДЕСОРБЦИИ
ПП (один образец) и ПВДФ ( три образца) были
ДИОКСИДА УГЛЕРОДА
устойчивы лишь при 313.15 К и заметно дегради-
Энергичное развитие мембранных технологий
ровали при 353.15 К. Нейлон оказался нестабиль-
предопределило активизацию исследований воз-
ным во всем диапазоне температур. Для дальней-
можности реализации процессов абсорбции-де-
ших исследований были выбраны половолоконные
сорбции диоксида углерода с применением мем-
мембраны из ПТФЭ.
бранных контакторов. Априори такие аппараты
Модули. С применением полых волокон из
имеют в разы более высокие значения величин
ПТФЭ были изготовлены лабораторный и пилот-
удельной поверхности контакта на единицу объе-
ный модули для проведения исследований процес-
ма. Еще одно существенное преимущество таких
са абсорбции. Параметры аппаратов представлены
аппаратов состоит в том, их конструкция обеспечи-
в табл. 6.
вает возможность независимого управления пото-
Удельная поверхность для пилотного аппара-
ками жидкости и газа, что невозможно в случае ап-
та составила 1329 м2/м3. Напомним, что для на-
паратов колонного типа, где происходит смешение
садочного абсорбера, описанного выше (стр. 16
фаз. Впервые идея применить мембранный кон-
[57]), оснащенного современной насадкой «Sulzer
тактор с половолоконной мембраной из полипро-
Mellapak 250Y», удельная поверхность составляет
пилена была предложена еще в 1985 г. [69, 70] для
всего лишь 250 м2/м3. Методом ртутной пороме-
удаления диоксида углерода. За прошедшие с тех
трии было установлено, что внутренняя поверх-
пор три с половиной десятка лет эта проблема пре-
ность волокон содержит макропоры размером 1-
вратилась в самостоятельное направление, которое
10 мкм (средний размер при этом составлял 5-
сегодня включает две обширные ветви - мембран-
6 мкм, а средняя пористость 0.28 мл/г). Параметры
ные контакторы с мембранами на основе органиче-
проведения экспериментов: лабораторный модуль -
ских (включая элементоорганические) полимеров
скорость подачи абсорбента до 0.05 л/мин, газа -
и мембранные контакторы на основе керамических
3 л/мин; пилотный модуль - 0.5-3.3 л/мин и 5-
мембран. О популярности этого направления сви-
30 л/мин соответственно. Общая рабочая поверх-
детельствует, например, и такой факт: в течение
ность мембран в пилотном модуле 11.5 м2. С при-
одного года (июль и декабрь 2019 г.) опубликованы
менением таких установок авторы верифициро-
два обзора на эту тему, содержащих ссылки на 350
вали разработанные модели процесса абсорбции.
публикаций.
Результаты экспериментов показали, что модель,
Мы остановимся на некоторых публикациях,
предназначенная для описания процесса в лабо-
которые определяют, на наш взгляд, алгоритм ис-
раторном абсорбере, оказалось корректной. В то
НЕФТЕХИМИЯ том 61 № 3 2021
300
НОВИЦКИЙ и др.
Таблица 6. Параметры контакторов
Тип
Лабораторный контактор
Пилотный контактор
Параметры модуля
Диаметр, Dвн, м
1.24×10-2
0.105
Длина, L эффективная, м
0.30
0.88
Длина, L общая, м
0.35
1.0
Число волокон
119
8521
Удельная поверхность, м2/м3
1331
1329
Параметры волокна
Диаметр Dвн, м
4.30×10-4
4.30×10-4
Dнар, м
8.70×10-4
8.70×10-4
Пористость
0.336
0.336
же время результаты экспериментов на пилотной
технологические параметры процесса (скорости
установке оказались неадекватными. По мнению
потоков, температуры) должны исключить воз-
авторов, это объясняется тем обстоятельством, что
можность капиллярной конденсации паров воды,
предложенная ими плоская 2D модель процесса не
что может привести к изменению состава раствора
учитывает распределение потоков внутри и вокруг
абсорбента и необходимости постоянной коррек-
волокон пилотного аппарата и нуждается в дора-
тировки этого состава. Однако, главный параметр,
ботке.
исключающий перспективность рассмотренной
технологии, состоит в том, что она предусматри-
В отличие от приведенного примера в большин-
вает все те же минимум 120°C на стадии регене-
стве работ рассматриваются проблемы применения
мембранных контакторов и на стадии десорбции.
рации МЭА. В большинстве работ этот недостаток
предлагается устранить, обеспечив движущую
Так, в [72] исследована возможность применения
силу процесса выделения абсорбированного диок-
половолоконных мембранных контакторов при
сида углерода применением вакуума, либо продув-
абсорбционной очистке технологических потоков
от CO2 водными растворами алканоламинов как
ки десорбируемого СО2 инертными газами (азот,
или даже аргон). Таких публикаций много, они
на стадии абсорбции, так и на стадии десорбции.
представлены, например, в подробном и объемном
В качестве материала мембран (в первую очередь
обзоре [52]. В качестве типичного примера приве-
с точки зрения термостойкости) рассматривали
дем уже давнюю публикацию [73], в которой опи-
политриметилсилилпропин и политетрафторэти-
сана интенсификация десорбции СО2 из раствора,
лен (ПТФЭ). Выбрали последний, как более при-
карбонизированного МЭА путем продувки током
емлемый по цене. Было проведено моделирование
процессов абсорбции и десорбции на основе экспе-
азота. Применение вакуума при десорбции СО2 в
мембранном контакторе представлено, например,
риментальных данных, полученных на лаборатор-
в [74] на примере карбонизированного раствора
ной установке. Результаты показали возможность
МЭА, или в [75] - для растворов ДЭА, а в [76] на
уменьшения удельной степени объема аппаратов
приблизительно в 4 раза (по сравнению с аппара-
примере карбонизированного раствора МДЭА. Как
правило, давление в межволоконном пространстве
тами насадочного типа) как на стадии абсорбции,
контактора составляло 10-35 кПа.
так и десорбции с применением сухих мембран
при линейной скорости подачи раствора абсорбен-
Интересный подход к проблеме был изложен в
та 10-4-10-3 м/с. Применение таких контакторов
работе [77]. Авторы поставили задачу выяснить,
на стадии десорбции диоксида углерода из насы-
как влияют продукты термоокислительной дегра-
щенного раствора амина может быть возможным
дации МЭА, такие как щавелевая, уксусная и му-
лишь при наличии мембран, устойчивых при тем-
равьиная кислоты (компоненты ТСС) на работу
пературах выше 120°C к действию компонентов
мембранного контактора с половолоконными мем-
абсорбционных растворов, включая ТСС. При этом
бранами из полипропилена на стадии абсорбции.
отмечается, что качество полых волокон (материа-
Когда ПП половолоконную мембрану, предвари-
лы волокон, соотношение внутреннего и внешне-
тельно подвергнутую воздействию продуктов раз-
го диаметров, наличие-отсутствие пористости) и
ложения амина, используют в мембранном контак-
НЕФТЕХИМИЯ том 61 № 3 2021
ОПТИМИЗАЦИЯ МЕТОДОВ ОЧИСТКИ ГАЗОВЫХ СМЕСЕЙ
301
торе абсорбции газа, скорость массопереноса CO2
снижается по сравнению с применением неэкспо-
нированного предварительно ПП-волокна. Было
обнаружено, что присутствие щавелевой кислоты
снижает скорость массопереноса CO2 в MЭA, за
которой следует муравьиная кислота, а затем ук-
сусная кислота. Авторы считают, что эти кислоты
адсорбируются в ПП, изменяя свойства поверхно-
сти и уменьшая гидрофобность мембраны. Это, в
свою очередь, увеличивает степень смачивания
пор мембраны. Циклические эксперименты с при-
менением мембранного контактора-десорбера и
раствора, карбонизированного МЭА, содержащего
компоненты ТСС, показали, что смачивание пор
мембраны увеличивается на 22-31% после 69 ч
Рис. 3. Схема процесса с совмещением процессов аб-
непрерывного эксперимента. Данные электронной
сорбции/десорбции в одном аппарате.
и рентгеновской спектроскопии ПП мембран до и
после экспонирования в компонентах ТСС пока-
зали, что увеличение смачивания может быть обу-
в рецикл. Удельный поток извлекаемого диоксида
словлено как морфологическими так и химически-
углерода составлял 1.1×10-3 см3/cм2·с·cм Hg. Эти
ми изменениями в мембране.
параметры выделения диоксида углерода были не-
изменны в течение 4 мес. На рис. 3 представлено
В работах [78, 79] описаны процессы сорбции-
схематическое изображение реализации на при-
десорбции в контакторах с капиллярными мем-
мере одного волокна. К сожалению, авторы не по-
бранами. В [80] теми же авторами представлен
казали, каким образом можно избежать перетека-
необычный вариант применения мембранного кон-
ния раствора амина вместе с диоксидом углерода
тактора, а именно, реализация стадий абсорбции
в межволоконное пространство и масштаба этого
диоксида углерода и его последующей десорбции
процесса.
в одном мембранном контакторе. В качестве абсор-
бента применяли водные растворы аминов (моно-
Еще один пример, заслуживающий внимания,
этаноламин, диэтаноламин, 2-метиламино-этанол
представлен в работе [81], где описан метод формо-
и
2-амино-2-метил-1-пропанол). Контактор был
вания половолоконных мембран из полисульфона и
оснащен ультрафильтрационными мембранами из
представлены параметры мембранного контактора,
полиэфирсульфона. На стадии абсорбции внутрь
оснащенного полученными мембранами. Формова-
волокон (напорная сторона) подавался раствор аб-
ние половолоконных мембран проводили с приме-
сорбента и модельный газ: смесь СО2 (5-15 об. %)
нением раствора полисульфона в водном N-метил-
и остальное N2). Внутри волокон поддержива-
пирролидоне с добавлением 2% этанола. Главное
лось атмосферное давление, а снаружи (в корпусе
преимущество полученных таким образом полых
контактора) остаточное давление составляло 10-
волокон состоит в том, что они имеют повышенные
27 кПа. По утверждению авторов, через некоторое
значения общей пористости (74.9%), но меньшие
время (0.28 с) после смешения потоков и движения
значения размера пор (øср - 19.3 нм против 24.5 нм).
их внутри волокна снизу-вверх при температуре
С применением таких волокон были изготовлены
60°C начинается процесс десорбции. По всей вы-
контакторы для исследования абсорбции диоксида
соте контактора диоксид углерода диффундирует
углерода водным раствором моноэтаноламина и
через пористую стенку в межволоконное простран-
последующей десорбции карбонизированного рас-
ство. Одновременно туда же перетекает и некото-
твора. Краткая характеристика модулей: внутрен-
рое количество абсорбента. Таким образом извле-
ний диаметр 15 мм, высота - 250 мм, число волокон
кается 76% диоксида углерода. Основная масса
30. Параметры волокон, мм: внутренний диаметр
абсорбента, содержащая 24% СО2, возвращается
0.45-0.50; наружный 0.9-1.0; эффективная длина
НЕФТЕХИМИЯ том 61 № 3 2021
302
НОВИЦКИЙ и др.
Таблица 7. Параметры полых волокон и модулей [84]
Параметры
Модуль 1
Модуль 2
Модуль 3
Диаметр D модуля, см
1.27
1.27
1.27
Диаметр d наружный волокна, см
0.11
0.20
0.11
Диаметр d внутренний волокна, см
0.08
0.16
0.08
Количество волокон
20.00
10.00
35.00
Рабочая длина волокна, см
18.00
18.00
18.00
Сечение модуля, см2
1.27
1.27
1.27
Сечение потока жидкости, см2
0.10
0.20
0.18
Сечение потока газа, см2
1.08
0.95
0.95
Пористость
0.86
0.75
0.75
Удельная поверхность, м2/м3
431.00
472.00
806.00
180. Общая поверхность контакта ~85 см2. Опти-
жидкости, значения коэффициента массоперено-
мальные параметры работы контактора в процессе
са и удельной поверхности. Модуль 3, имеющий
абсорбции были достигнуты при скорости течения
самые высокие значения удельной поверхности и
раствора МЭА 300 мл/мин и скорость абсорбции
фактора упаковки, оказался наиболее эффектив-
СО2 составила 3.9×10-3 мол/м2·с, а при десорбции -
ным, поскольку сопротивление массопереносу в
при скорости подачи насыщенного раствора
жидкой фазе для этого модуля оказалось ниже, чем
200 мл/мин - 2.0×10-4 мол/м2·с.
в других, где оно достигало 90% от общего значе-
ния. В изученных контакторах объединены лучшие
Следует отметить, что в последние годы стано-
параметры полых волокон (высокие удельные по-
вятся актуальными и половолоконные контакторы
верхности) и высокая химическая и термическая
с применением полых волокон из керамических
стабильность, характерная для керамики.
материалов. Это объясняется их термической и хи-
В [85] представлены интересные результаты ис-
мической стабильностью, а также механической
следований влияния размера пор и толщины стен-
прочностью. В [82] мембранные контакторы с ке-
ки коммерческих микрофильтрационных (МФ)
рамическими полыми волокнами были примене-
половолоконных мембран, а также керамических
ны для десорбции СО2 из насыщенных растворов
половолоконных мембран из оксида алюминия
МЭА при высоких температурах, когда полимер-
(глинозем), изготовленных авторами в рамках ци-
ные мембраны неприемлемы. Керамические по-
тируемой работы, на скорость десорбции СО2 из
ловолоконные мембраны на основе оксидов алю-
карбонизированного раствора моноэтаноламина.
миния формовали при температуре 1400°C, они
В качестве рабочей жидкости применяли 30% во-
обладают высокой прочностью и гидрофобностью.
дный раствор МЭА со степенью карбонизации
Подробности изложены в [83, 84]. Эксперимент по
0.5МCO2/ММЭА. Исходный раствор подавался
десорбции проводили с применением водного рас-
внутрь половолоконных мембран при атмосфер-
твора МЭА (концентрация 2.5 М/л), концентрация
ном (98 кПа) давлении, остаточное давление в кор-
СО2 составляла 0.45МCO2/ММЭА.
пусе модуля (выход диоксида углерода) составля-
Характеристики модулей и керамических воло-
ло 1-40 кПа. Температура во всех экспериментах
кон представлены в табл. 7.
была 40°C скорость подачи раствора составляла
Исследования процесса десорбции показали,
300 мл/мин. В табл. 8 представлены характеристики
что такие проблемы как захлебывание или нагрузка
половолоконных мембран, исследованных в работе.
по газу при использовании контакторов отсутству-
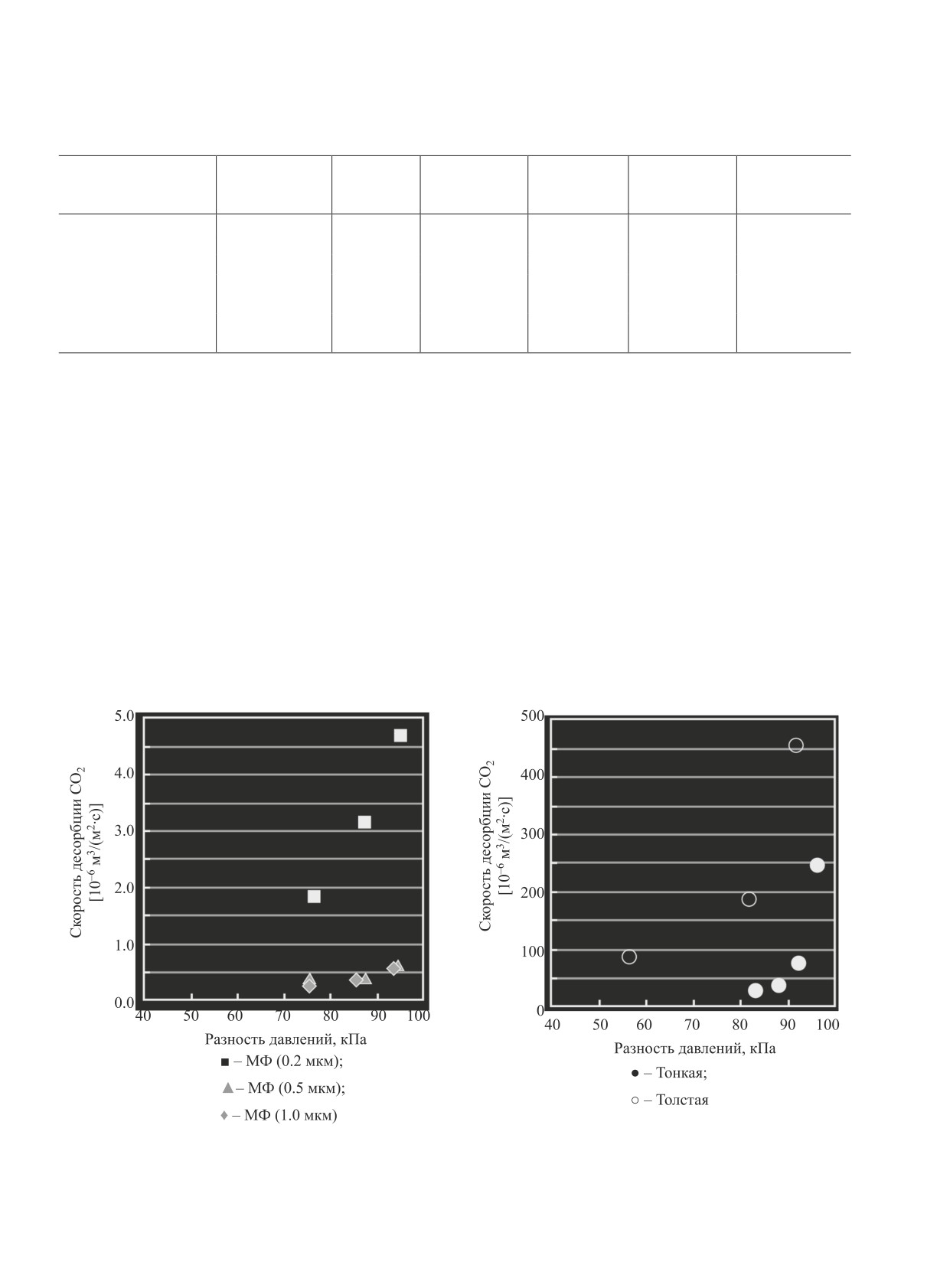
Здесь следует отметить, что коммерческие МФ
ют, поскольку потоки газа и жидкости разделены
мембраны отличаются только размером пор при
мембраной. Эффективность модуля характеризо-
полной идентичности геометрических размеров, а
вали как высоту теоретической тарелки «HTU».
полученные в цитируемой работе - отличаются и
Для половолоконного модуля «HTU» зависит от
размерами геометрических параметров. Влияние
нескольких величин, а именно от скорости потока
этих различий иллюстрируется данными рис. 4 и 5.
НЕФТЕХИМИЯ том 61 № 3 2021
ОПТИМИЗАЦИЯ МЕТОДОВ ОЧИСТКИ ГАЗОВЫХ СМЕСЕЙ
303
Таблица 8. Характеристики половолоконных мембран
Толщина
Диаметр
Диаметр
Длина
Диаметр пор
Пористость,
Название мембран
мембран,
внутренний,
наружный,
эффективная,
мембран, мкм
%
мм
мм
мм
мм
МФ
0.2а
1.5
7.0
10.0
35.0б
65
МФ
0.5а
1.5
7.0
10.0
35.0б
65
МФ
1.0а
1.5
7.0
10.0
35.0б
55
Получена согласно
1.6
1.8
8.0
11.6
35.7
52
работев (тонкая)
Получена согласно
1.6
2.9
8.0
13.8
30.8
62
работев (толстая)
а Коммерческие мембраны.
б Приведены значения по наружной части трубок.
в Согласно «Мембранной Терминологии» это трубчатые мембраны.
Анализ этих данных свидетельствует, что в слу-
шего диаметра создается наибольшая поверхность
чае МФ мембран наибольший перенос СО2 наблю-
контакта между материалом мембраны и насы-
дается для мембраны с меньшим диаметром пор
щенным раствором. Таким образом, скорость де-
(0.2 мкм), в то время как два образца с большими
сорбции СО2 зависит не только (и не столько) от
размерами пор имеют практически одинаково бо-
диаметра пор, сколько от интегральной их характе-
лее низкие значения (рис. 4). Более того, в экспе-
ристики - поверхности контакта «раствор-мембра-
риментах с мембраной МФ 0.2 наблюдалось пено-
на», а, следовательно, еще и толщины мембраны,
образование на наружной поверхности мембраны
в данном случае от толщины ее стенки. Данные
при разности давлений 94 кПа, что указывает на
по десорбции диоксида углерода с применением
то, что десорбция СО2 происходит уже внутри пор
толстостенных мембран, полученных в этой ра-
мембранной стенки. Поскольку все МФ мембраны
боте (рис. 5), подтверждают это. Более того, оче-
отличаются только размером пор, в порах наимень-
видно, что такие мембраны обеспечивают скорость
Рис. 5. Скорость десорбции CO2 для мембран согласно
Рис. 4. Скорость десорбции CO2 для МФ-мембран.
работе.
НЕФТЕХИМИЯ том 61 № 3 2021
304
НОВИЦКИЙ и др.
Таблица 9. Результаты промышленных испытаний десорбера тарельчатого
Содержание МЭА в водном растворе, мас. % (моль/л)
Характеристики процесса
23 (3.77)
17.0
(2.78)
Нагрузка СО2 исходного раствора, г/л
60.0
60.0
Нагрузка СО2 после десорбции г/л
33.0
20.0
Степень удаления СО2, %
45.0
66.6
Таблица 10. Эффективность десорбции СО2 из карбонизированных растворов МЭА различной концентрации [87]
Содержание МЭА в водном растворе, мас. % (моль/л)
Характеристики процесса: десорбция СО2 при Т = 90°C
7.5
(1.23)
12.0
(1.97)
30.0
(4.92)
Нагрузка СО2 исходного раствора
г/л
40.90
65.10
125.60
моль СО2/моль МЭА
0.74
0.74
0.58
Нагрузка СО2 после десорбции
г/л
15.00
14.00
69.00
моль СО2/моль МЭА
0.27
0.16
0.32
Степень удаления СО2, %
62.50
78.50
45.00
десорбции СО2 на 1-2 порядка выше, чем у МФ-
ние 24 недель, т.е. почти полгода. Но у этого мате-
мембран.
риала имеются два недостатка: он дорог и, кроме
того, есть серьезные проблемы при формовании
Рассмотренные варианты применения мембран-
из него волокон малого диаметра, поскольку этот
ных половолоконных контакторов в процессах аб-
материал нерастворим. Наибольший интерес пред-
сорбции и десорбции диоксида углерода водными
ставляют разделительные элементы из керамиче-
растворами аминов позволяют сделать некоторые
ских материалов, благодаря, в первую очередь, их
общие выводы. В отличие от типичных мембран-
высокой термостойкости и технологичности при-
ных процессов, например, газоразделения, мате-
менения.
риал для мембранных контакторов рассматривае-
мого назначения не должен обладать селективной
В заключение необходимо представить еще одно
газопроницаемостью. Более того, в этом случае
направление модернизации технологии десорбции
предпочтительными являются пористые мембра-
раствора карбонизированного абсорбента. В [11,
ны с асимметричной структурой: микропористый
стр. 285] приведены данные по десорбции диок-
несущий слой (условно с порами микроразмеров
сида углерода из насыщенных диоксидом углерода
на наружной поверхности полого волокна) и тон-
растворов моноэтаноламина производительностью
копористый (условно с порами ультраразмеров на
360 м3/ч. Процесс проводили в промышленном де-
внутренней поверхности). Такая конструкция по-
сорбере тарельчатого типа диаметром 3.0 м и вы-
ловолоконной мембраны позволяет отделять газо-
сотой около 10 м. Были исследованы два раствора
вую фазу от жидкой в условиях возрастающей по-
с концентрацией МЭА 23% и 17%. Температурные
верхности межфазного контакта, что обеспечивает
параметры работы десорбера были следующие: на-
достаточную величину газового потока. Важным
сыщенный раствор - 78°C, температура в кубовой
преимуществом половолоконных контакторов яв-
части - 115°C температура верхней части - 102°C.
ляется и то обстоятельство, что в отличие от при-
Результаты представлены в табл. 9.
меняемых массообменных аппаратов насадочного
Приведенные результаты интересны тем, что
или тарельчатого типа, в контакторах жидкий и
для 23%-ного раствора МЭА характерна та же сте-
газовый потоки разделены, что является важным
пень удаления СО2, что и для 30%-ного [10, 12]. Но
технологическим преимуществом. С точки зрения
в случае 17%-ного раствора МЭА степень удаления
материалов полых волокон, наилучшим является
почти в 1.5 раза выше. Влияние концентрации рас-
политетрафторэтилен, благодаря высокоустойчи-
творов МЭА на эффективность процесса декарбо-
вой несмачиваемости. Так, в [86] сообщалось, что
низации было изучено в [87]. Полученные резуль-
волокна из ПТФЭ сохраняют устойчивость в тече-
таты представлены в табл. 10.
НЕФТЕХИМИЯ том 61 № 3 2021
ОПТИМИЗАЦИЯ МЕТОДОВ ОЧИСТКИ ГАЗОВЫХ СМЕСЕЙ
305
Таблица 11. Равновесное давление СО2 (кПа) над водными растворами МЭА различной концентрации и степени
карбонизации (взято из [88])
Температура °C
α
80
90
100
110
120
МСО2/ММЭА
12% (1.97 М/л) МЭА
0.12
0.193
0.441
0.965
1.97
3.93
0.72
358.8
484.0
652.2
901.2
1188
15% (2.26 М/л) МЭА
0.12
0.180
0.441
1.11
2.54
5.56
0.70
350.6
462.2
623.5
860.7
1135
30% (4.91 М/л) МЭА
0.2
0.359
0.750
1.60
3.35
6.53
0.5а
58.19
103.5
188.3
298.4
495.3
a Максимальное применяемое значение.
Сопоставление данных табл. 9 и 10 позволя-
ции методов декарбонизации насыщенных диок-
ет сделать вывод, что уменьшении концентрации
сидом углерода абсорбционных водных растворов
МЭА в растворе абсорбента позволяет увеличить
различных аминов можно выделить следующие на-
степень десорбции диоксида углерода даже при
правления реализации этих процессов.
90°C. Более того, этот эффект наблюдается при
Расширение круга применяемых аминов с по-
более низкой температуре десорбции и наиболее
зиций увеличения их термостабильности. На этом
выражен в случае 12%-ного раствора МЭА. Эти
направлении очень популярны исследования рас-
данные хорошо согласуются со значениями вели-
творов т.н. «стерически» затрудненных аминов,
чин равновесного давления диоксида углерода над
содержащих в качестве заместителей у атома азо-
растворами МЭА различной концентрации и степе-
та пропильные радикалы изостроения а также их
ни карбонизации табл. 11.
комбинации с традиционно применяемыми моно-,
Полученные результаты авторы объясняют об-
диэтанол- и метиддиэтаноламинами. Следует так-
разованием в концентрированных (> 20%) раство-
же отметить, что амины с практически идеальной
рах МЭА надмолекулярных структур (мицелляр-
селективностью поглощения СО2/СН4 800-1000
ного типа) состава [МЭА-СО2-Н2О] с наличием
могут оказаться востребованными при очистке
водородных связей. Поэтому десорбции диоксида
природного газа.
углерода предшествует стадия разрушения этих
Актуальной становится тема аппаратурно-
структур, что увеличивает затраты энергии и, сле-
го оформления процессов абсорбции-десорбции
довательно, необходимость применения высоких
с применением мембранных контакторов двух
(≥ 115°C) температур.
типов - половолоконных и трубчатых. Эти аппара-
Сделанный анализ проблемы оптимизации
ты имеют в разы более высокие значения величин
очистки различных газовых смесей методом аб-
удельной поверхности контакта на единицу объе-
сорбции диоксида углерода растворами аминов по-
ма, чем насадочные, а их конструкция обеспечивает
зволяет предположить, что успех может быть до-
возможность независимого управления потоками
стигнут расширением ассортимента применяемых
жидкости и газа, что невозможно в случае аппара-
аминов при одновременном снижении их концен-
тов колонного типа, где происходит смешение фаз.
трации и реализации процессов адсорбции/десорб-
Предпочтительными являются пористые мем-
ции в мембранных контакторах.
браны с асимметричной структурой: микропори-
стый несущий слой (условно с порами микрораз-
ЗАКЛЮЧЕНИЕ
меров на наружной поверхности полого волокна) и
На основе анализа публикаций главным образом
тонкопористый (условно с порами ультраразмеров
последнего десятилетия, посвященных оптимиза-
на внутренней поверхности). Такая конструкция
НЕФТЕХИМИЯ том 61 № 3 2021
306
НОВИЦКИЙ и др.
половолоконной мембраны позволяет отделять га-
7.
Sreenivasulu B., Gayatri D.V., Sreedhar I., Ragha-
зовую фазу от жидкой в условиях возрастающей
van K.V. A journey into the process and engineering
aspects of carbon capture technologies // Renewable
поверхности межфазного контакта, что обеспечи-
Sustainable Energy Reviews. 2015. V. 41. P. 1324-1350.
вает достаточную величину газового потока.
8.
Abu-Zahra M.R.M., Niederer J.P.M., Feron P.H.M.,
ИНФОРМАЦИЯ ОБ АВТОРАХ
Versteeg G.F. CO2 capture from power plants Part I.
Новицкий Эдуард Григорьевич ORCID: http://
A parametric study of the technical performance based
on monoethanolamine // Intern. J. of Greenhouse Gas
orcid.org/0000-0001-9009-2073
Баженов Степан Дмитриевич ORCID: http://
S1750-5836(06)00007-7
orcid.org/0000-0002-2010-5294
9.
Wang T., Hovland J., Jens K.J. Amine reclaiming
Волков Алекcей Владимирович ORCID: http://
technologies in post-combustion carbon dioxide capture //
orcid.org/0000-0003-4524-4597
J. of Environ. Science. 2015. V. 27. P. 276-289. https://
doi.org/10.1016/j.jes.2014.06.037
10.
Rochelle G.T. Amine scrubbing for CO2 capture //
ФИНАНСИРОВАНИЕ РАБОТЫ
Science. 2009. V. 325. № 5948. P. 1652-1654. https://
Работа выполнена в рамках Государственного
doi.org/10.1126/science.1176731
задания ИНХС РАН.
11.
Вакк Э.Г., Шуклин Г.В., Лейтес И.Л. Получение
технологического газа в производствах аммиака,
метанола, водорода и высших углеводородов. Теоре-
КОНФЛИКТ ИНТЕРЕСОВ
тические основы, технология, катализаторы, обору-
Авторы заявляют об отсутствии конфликта ин-
дование, системы управления. М.: ISBN 978-5-98801-
тересов, требующего раскрытия в данной статье.
33-3, 2011. 285 с.
12.
Davis J., Rochelle G. Thermal degradation of
monoethanolamine at stripper conditions // Energy
СПИСОК ЛИТЕРАТУРЫ
1. British Petrolеum Statistical Review of World Energy //
org/10.1016/j.egypro.2009.01.045
2019. P. 2.
13.
Dutcher B., Fan M., Russell A.G. Amine-based CO2
2. Inventory of US Greenhouse Gas Emissions and Sinks:
capture technology development from the beginning
1990-2015 // United States Environmental Protection
of 2013 // ACS Applied Materials & Interfaces.
Agency: Washington, DC. 2017.
3. Psarras P.C., Comello S., Bains P., Charoensawadpong P.,
am507465f
Reichelstein S., Wilcox J. Carbon capture and utilization
14.
Moser P., Schmidt S., Stahl K. Investigation of trace
in the industrial sector // Environ. Science Technology.
elements in the inlet and outlet streams of a MEA-
based post-combustion capture process results from
org/10.1021/acs.est.7b01723
the test programme at the Niederaussem pilot plant //
4. Bottoms R.R. Process for separating acidig gases // Patent
US № 1783901. 1930. P. 1-6.
org/10.1016/j.egypro.2011.01.077
5. Bailey B.W., Feron P.H.M. Post-combustion decarbo-
nisation processes // Oil & Gas Science and Technology.
15.
Butwell K.F., Kubek D.J., Sigmund P.W. Alkanolamine
treating // Hydrocarbon Processing. 1982. V. 61. № 3.
ogst:2005028
P. 108. OSTI: 5220672.
6. Liang Z., Rongwong W., Liu H., Fu K., Gao H., Cao F.,
16.
Thompson G.J., Frimpong R., Remias J.E., Neathery
Zhang R., Sema T., Henni A., Sumon K., Nath D., Gelo-
J.K., Liu K. Heat stable salt accumulation and solvent
witz D., Srisang W., Saiwan C., Benamord A., Al-Marri M.,
degradation in a pilot-scale CO2 capture process
Shi H., Supap T., Chan C., Zhou Q., Abu-Zahra M.,
using coal combustion flue gas // Aerosol and Air
Wilson M., Olson W., Idem R., Tontiwachwuthikul P.
Recent progress and new developments in post-
org/10.4209/aaqr.2013.05.0150
combustion carbon-capture technology with amine
17.
Kohl A., Nielsen R. Gas Purification. Fifth Ed. Houston:
based solvents // Intl. J. of Greenhouse Gas Control.
Gulf Publishing Company, 1993. P. 41-186.
18.
Gouedard C., Picq D., Launay F., Carrette P.L. Amine
ijggc.2015.06.017
degradation in CO2 capture. I. A review // Intl. J. of
НЕФТЕХИМИЯ том 61 № 3 2021
ОПТИМИЗАЦИЯ МЕТОДОВ ОЧИСТКИ ГАЗОВЫХ СМЕСЕЙ
307
Greenhouse Gas Control. 2012. V. 10. P. 244-270.
30.
Tems R., Al-Zahrani A. Cost of corrosion in gas
sweetening and fractionation plants // NACE Intl.,
Corrosion. 2006. Paper № 444. P. 1-12.
19.
Dumee L., Scholes C., Stevens G., Kentish S. Purification
31.
Léonard G., Voice A., Toye D., Heyen G. Influence
of aqueous amine solvents used in post combustion CO2
of dissolved metals and oxidative degradation
capture: A review // Intl. J. of Greenhouse Gas Control.
inhibitors on the oxidative and thermal degradation of
monoethanolamine in postcombustion CO2 сapture //
ijggc.2012.07.005
Industrial & Engineering Chemistry Research. 2014.
20.
Nielsen R.B., Lewis K.R., McCullough J.G., Hansen D.A.
Corrosion in refinery amine systems // NACE Intl.,
ie5036572
Corrosion 95. 1995. Paper № 571. P. 1-26. OSTI:
32.
Xiao J., Li C.-W., Li. M.-H. Kinetics of absorption of
128737.
carbon dioxide into aqueous solutions of 2-amino-2-
21.
Soosaiprakasam I.R., Amornvadee V. Corrosion and
methyl-1-propanol + monoethanolamine // Chemical
polarization behavior of carbon steel in MEA-based CO2
Engineering Science. 2000. V. 55. № 1. P. 161-175.
capture process // Intl. J. of Greenhouse Gas Control.
33.
Stowe H.M., Hwang G.S. Fundamental understanding of
ijggc.2008.02.009
CO2 capture and regeneration in aqueous amines from
22.
Veldman R.R. Alkanolamine solution corrosion
first-principles studies: recent progress and remaining
mechanisms and inhibition from heat stable salts and
challenges // Industrial & Engineering Chemistry
CO2 // NACE Intl., Corrosio. 2000. Paper № 496.
P. 1-13.
org/10.1021/acs.iecr.7b00213
23.
Vazquez R.C., Rios G., Trejo A., Rincon R.E., Uruchurtu J.,
34.
Blauwhoff P.P.M., Versteeg G.F., van Swaaij W.P.M. A
Malo J.M. The effect of diethanolamine solution
study on the reaction between CO2 and alkanolamines
concentration in the corrosion of steel // NACE Intl.,
in aqueous solutions // Chemical Engineering
Corrosion. 2000. Рaper № 696. P. 1-11.
24.
Tanthapanichakoon W., Veawab A., McGarvey B.
org/10.1016/0009-2509(84)80021-4
Electrochemical investigation on the effect of heat-stable
35.
Ma’mun S., Svendsen H.F., Hoff K.A., Juliussen O.
salts on corrosion in CO2 capture plants using aqueous
Selection of new absorbents for carbon diоxide
solution of MEA // Industrial Engineering Chemistry
capture // Energy Conversion and Management. 2007.
org/10.1021/ie050575a
enconman.2006.04.007
25.
Kittel J., Gonzalez S. Corrosion in CO2 post-combustion
36.
Liao C.-H., Li M.-H. Kinetics of absorption of carbon
capture with alkanolamines. A review // Oil & Gas
dioxide into aqueous solutions of monoethanolamine +
Science Technology. 2014. V. 65. № 5. P. 915-929.
N-methyldiethanolamine // Chem. Engineering
26.
Kittel J., Fleury E., Vuillemin B., Gonzalez S., Ropital F.,
org/10.1016/S0009-2509(02)00395-0
Oltra R. Corrosion in alkanolamine used for acid gas
37.
Hossain M.M., de Lasa H.I. Chemical-looping combustion
removal: From natural gas processing to CO2 capture //
(CLC) for inherent CO2 separations, a review //
Materials and Corrosion. 2012. V. 63. № 3. P. 223-230.
Chem. Engineering Science. 2008. V. 63. P. 4433-4451.
27.
Nielsen R.B., Lewis K.R., McCullough J.G., Hansen
38.
Jones C.W. Capture from dilute gases as a component
D.A. Controlling corrosion in amine treating plants //
of modern global carbon management // Annual
Proceedings of the 45th Laurance Reid Gas Conditioning
Review of Chemical and Biomolecular Engineering.
Conference, Norman, OK. 1995. P. 1-33.
28.
Wagner R., Judd B. Fundamentals - Gas sweetening //
chembioeng-061010-114252
Proceedings of the 56th Laurance Reid Gas Conditioning
39.
Rashid H., Khan K., Yaseen M., Umar M.N. Solvent
Conference, Norman, OK. 2006.
degradation in 8 capture process from power plant flue
29.
Kittel J., Idem R., Gelowitz D., Tontiwachwuthikul P.,
gas // Theoretical and Experimental Chemistry. 2014.
Parrain G., Bonneau A. Corrosion in MEA units
for CO2 capture: Pilot plant studies // Energy Procedia.
014-9337-y
40.
Zhang Z., Yao Z.-Z., Xiang S., Chen B. Perspective of
egypro.2009.01.105
microporous metal-organic frameworks for CO2 capture
НЕФТЕХИМИЯ том 61 № 3 2021
308
НОВИЦКИЙ и др.
and separation // Energy Environ. Science. 2014. V. 7.
51.
Rashidi A., Yusup S., Hameed B.H. Kinetic studies on
carbon dioxide capture using lignocellulosic based
41.
Lu X., Jin D., Wei S., Wang Z., An C., Guo W. Strategies
activated carbon // Energy. 2013. V. 61. P. 440-446.
to enhance CO2 capture and separation based on
engineering absorbent materials // J. of Materials
52.
Xu Y., Goh K., Wang R., Bae T.-H. A review on polymer-
based membranes for gas-liquid membrane contacting
org/10.1016/S1001-0742(08)60002-9
processes: Current challenges and future direction //
42.
Choi S., Drese J.H., Eisenberger P.M., Jones C.
Separation and Purification Technology. 2019. V. 229.
Application of amine-tethered solid sorbents for direct
CO2 capture from the ambient air // Environ. Science
53.
Bougie F., Iliuta M.C. Stability of aqueous amine
solutions to thermal and oxidative degradation in the
org/10.1021/es102797w
absence and the presence of CO2 // Intl. J. of Greenhouse
43.
Goeppert A., Czaun M., May R.B., Prakash G.K.S.,
Olah G.A., Narayanan S.R. Carbon dioxide capture
org/10.1016/j.ijggc.2014.07.008
from the air using a polyamine based regenerable solid
54.
Dugay J., Bontemps D., Louis-Louisy M., Vial J.
adsorbent // J. of the American Chemical Society. 2011.
Analytical methods for the monitoring of post-
combustion CO2 capture process using amine solvents: A
ja2100005
review // Int. J. of Greenhouse Gas Control. 2018. V. 72.
44.
Goeppert A., Zhang H., Czaun M., May R.B., Pra-
kash G.K.S., Olah G.A, Narayanan S.R. Easily
55.
Conway W., Bruggink S., Beyad Y., Luo W., Melián-
regenerable solid adsorbents based on polyamines for
Cabrera I., Puxty G., Feron P. CO2 absorption
carbon dioxide capture from the air // ChemSus Chem.
into aqueous amine blended solutions containing
monoethanolamine (MEA), N,N-dimethylethanolamine
cssc.201301114
(DMEA), N,N-diethylethanolamine (DEEA) and
45.
Belmabkhout Y., Serna-Guerrero R., Sayari A. Amine-
2-amino-2-methyl-1-propanol (AMP) for post-
bearing mesoporous silica for CO2 removal from dry
combustion capture processes // Chem. Engineering
and humid air // Chemical Engineering Science. 2010.
org/10.1016/j.ces.2014.12.053
ces.2010.02.044
56.
Kierzkowska-Pawlak H. Kinetics of CO2 absorption in
46.
Serna-Guerrero R., Belmabkhout Y., Sayari A. Modeling
aqueous N,N-diethylethanolamine and its blend with
CO2 adsorption on amine-functionalized mesoporous
N-(2-aminoethyl)ethanolamine using a stirred cell
silica: 1. A semi-empirical equilibrium model // Chem.
reactor // Intl. J. of Greenhouse Gas Control. 2015. V.
Engineering J. 2010. V. 161. № 1-2. P. 173-181. https://
doi.org/10.1016/j.cej.2010.04.024
57.
Osagie E., Biliyok C., Di Lorenzo G., Manovic V. Process
47.
Qi G., Fu L., Choi B.H., Giannelis E.P. Efficient CO2
modelling and simulation of degradation of 2-amino-
sorbents based on silica foam with ultra-large mesopores //
2-methyl-1-propanol (AMP) capture plant // Energy
Energy Environ. Science. 2012. V. 5. P. 7368-7375.
org/10.1016/j.egypro.2017.03.1324
48.
Titinchi J.J.S., Piet M., Abbo H.S., Bolland O., Schwie-
58.
Liang Y., Liu H., Rongwong W., Liang Z., Idem R.,
ger W. Chemically modified solid adsorbents for CO2
Tontiwachwuthikul P. Solubility, absorption heat and
capture // Energy Procedia. 2014. V. 63. P. 8153-8160.
mass transfer studies of CO2 absorption into aqueous
49.
Dantas T.L.P., Luna F.M.T., Silva I.J. jr., de Aze-
solution of 1-dimethylamino-2-propanol // Fuel.
vedo D.C.S., Grande C.A., Rodrigues A.E., Moreira F.P.M.
Carbon dioxide-nitrogen separation through adsorption
fuel.2014.11.098
on activated carbon in a fixed bed // Chem. Engineering
59.
Hadri E.L.N., Quang D.V., Abu-Zahra M.R.M. Study
of Novel Solvent for CO2 Post-combustion Capture //
cej.2010.08.026
50.
Kowles G.P., Graham J.V., Delaney S.W., Chaffe A.L.
org/10.1016/j.egypro.2015.07.414
Aminopropyl-functionalized mesoporous silicas as CO2
60.
Jamal A., Meisen A., Lim C.J. Kinetics of carbon dioxide
adsorbents // Fuel Processing Technology. 2005. V. 86.
absorption and desorption in aqueous alkanolamine
solutions using a novel hemispherical contactor-
fuproc.2005.01.014
II: Experimental results and parameter estimation //
НЕФТЕХИМИЯ том 61 № 3 2021
ОПТИМИЗАЦИЯ МЕТОДОВ ОЧИСТКИ ГАЗОВЫХ СМЕСЕЙ
309
Chemical Engineering Science. 2006. V. 61. № 19.
Energies Nouvelles. 2014. V. 69. № 6. P. 1035-1045.
61.
Wang T., Jens K.-J. Oxidative degradation of aqueous
72.
Zaidiza D.A., Belaissaoui B., Rode S., Favre E.
2-amino-2-methyl-1-propanol solvent for post
intensification potential of hollow fiber membrane
combustion CO2 capture // Industrial and Engineering
contactors for CO2 chemical absorption and stripping
Chemistry Research. 2012. V. 51. № 18. P. 6529-6536.
using monoethanolamine solutions // Separation and
Purification Technology. 2017. V. 188. P. 38-51. https://
62.
Wang T., Jens K.-J. Oxidative degradation of AMP/
doi.org/10.1016/j.seppur.2017.06.074
MEA blends for post-combustion CO2 capture //
73.
Teramoto M., Kitada S., Ohnishi N., Matsuyama H.,
Matsumiya N. Separation and concentration of CO2 by
org/10.1016/j.egypro.2013.05.116
capillary-type facilitated transport membrane module
63.
Wang T., Jens K.-J. Oxidative degradation of aqueous PZ
with permeation of carrier solution // J. of Membrane
solution and AMP/PZ blends for post-combustion carbon
dioxide capture // Intl. J. of Greenhouse Gas Control.
org/10.1016/j.memsci.2003.12.023
74.
Fang M., Wang Z., Yana S., Cen Q., Luo Z. CO2
ijggc.2014.03.003
desorption from rich alkanolamine solution by using
64.
Rabensteiner M., Kinger G., Koller M., Gronald G.,
membrane vacuum regeneration technology // Intl. J. of
Unterberger S., Hochenauer C. Investigation of the
Greenhouse Gas Control. 2012. V. 9. P. 507-521. https://
suitability of aqueous sodium glycinate as a solvent for
doi.org/10.1016/j.ijggc.2012.05.013
post combustion carbon dioxide capture on the basis of
75.
Okabe K., Kodama S., Mano H., Fujioka Y. Separa-
pilot plant studies and screening methods // Intl. J. of
tion and recovery of carbon dioxide by a membrane
Greenhouse Gas Control. 2014. V. 29. P. 1-15. https://
flash process utilizing waste thermal energy // Energy
doi.org/10.1016/j.ijggc.2014.07.011
65.
Шнайдер Р., Кюттель Д., Кинцль М., Йох Р.,
org/10.1016/j.egypro.2009.01.168
Фишер Б.П. Поглотительный раствор для абсорб-
76.
Lv P.P., Wang F., Guo Y.H., Tang H.Y. CO2 desorption
ции диоксида углерода и способ ускорения абсор-
by hydrophilic PTFE hollow fiber membranes via a
бции посредством диоксида германия. // Патент РФ
membrane flash process // Key Engineering Materials.
№ 2638663. Опубликован 2017.12.15.
66.
Furusho Y., Endo T. Reversible capture and release of
scientific.net/KEM.671.293
carbon dioxide by binary system of polyamidine and
77.
Franco J.A., Montigny D., Kentisha S.E., Perera J.M.,
polyethylene glycol // Polymer Bulletin. 2017. V. 74.
Stevens G.W. Effect of amine degradation products
on the membrane gas absorption process // Chemical
67.
Aoyagi N., Endo T. CO2 capture capacity of five- and
Engineering Science. 2009. V. 64. № 18. P. 4016-4023.
six-membered cyclic amidines bearing silatranyl group
under dry conditions // Tetrahedron. 2017. V. 73. № 12.
78.
Kazuhiro Okabe, Satoshi Kodama, Hiroshi Mano,
Yuichi Fujioka. Separation and recovery of carbon
68.
Heldebrant D.J., Jessop P.G., Thomas C.A., Eckert C.A.,
dioxide by a membrane flash process utilizing waste
Liotta C.L. The reaction of 1,8-diazabicyclo[5.4.0]-
thermal energy // Energy Procedia. 2009. V. 1. P. 1281-
undec-7-ene (DBU) with carbon dioxide // J. Organic
1288. https:// doi.org 10.1016/j.egypro.2009.01.168
79.
Teramoto M., Kitada S., Ohnishi N., Matsuyama H.,
org/10.1021/jo0503759
Matsumiya N. Separation and concentration of CO2 by
69.
Qi Z., Cussler E.L. Microporous hollow fibers for
capillary-type facilitated transport membrane module
gas absorption: I. Mass transfer in the liquid // J. of
with permeation of carrier solution // J. of Membrane
Membrane Science. 1985. V. 23. № 3. P. 321-322.
org/10.1016/j.memsci.2003.12.023
70.
Qi Z., Cussler E.L. Microporous hollow fibers for
80.
Teramoto M., Ohnishi N., Takeuchi N., Kitada S.,
gas absorption: I. Mass transfer in the liquid // J. of
Matsuyama H., Matsumiya N., Mano H. Separation and
enrichment of carbon dioxide by capillary membrane
org/10.1016/S0376-7388(00)83149-X
module with permeation of carrier solution // Separation
71.
Chabanon E., Kimball E., Favre E., Lorain O., Goetheer E.,
and Purification Technology. 2003. V. 30. № 3. P. 215-
Ferre D., Gomez A., Broutin P. Hollow fiber membrane
contactors for post-combustion CO2 capture: A
81.
Kianfar E., Pirouzfar V., Sakhaeinia H. An experimental
scale-up study from laboratory to pilot plant // IFP
study on absorption/stripping CO2 using mono-ethanol
НЕФТЕХИМИЯ том 61 № 3 2021
310
НОВИЦКИЙ и др.
amine hollow fiber membrane contactor // J. of the
properties on CO2 desorption from chemical absorbents
Taiwan Institute of Chemical Engineers. 2017. V. 80.
using a membrane flash process // Energy Procedia.
82. Koonaphapdeelert S., Wu Z., Li K. Carbon dioxide
egypro.2013.05.202
stripping in ceramic hollow fibre membrane contactors //
86. Guo Y. Long-term stability of polytetrafluoroethylene
Chemical Engineering Science. 2009. V. 64. № 1. P. 1-8.
(PTFE) hollow fiber membranes for CO2 capture //
83. Koonaphapdeelert S., Li K. Preparation and
org/10.1021/acs.energyfuels.5b01789
characterization of hydrophobic ceramic hollow
87. Novitskii E.G., Vasilevskii V.P., Vasil’eva V.I.,
fibre membrane // J. of Membrane Science. 2007.
Goleva E.A., Grushevenko E.A., Volkov A.V. Effect
of composition and structure of aqueous mono-
memsci.2006.12.039
ethanolamine solutions on carbon dioxide sorption
84. Koonaphapdeelert S., Tan X., Wu Z., Li K. Solvent
and desorption in purification of gas mixtures //
distillation by ceramic hollow fibre membrane contac-
tors // J. of Membrane Science. 2008. V. 314. № 1-2.
Russian J. of Applied Chemistry. 2018. Vol. 91. № 5.
85. Takahashi N., Matsuzaki K., Funai T., Wada T., Fukuna-
88. Мельников Е.Я. Справочник азотчика. М.: Химия.
ga H., Takatsuka T., Mano H. Effects of membrane
1986. 235 с.
НЕФТЕХИМИЯ том 61 № 3 2021