НЕФТЕХИМИЯ, 2023, том 63, № 1, с. 56-66
УДК: 547.313-542.97
ЭКСПЕРИМЕНТАЛЬНОЕ И КИНЕТИЧЕСКОЕ МОДЕЛИРОВАНИЕ
ГИДРОПРЕВРАЩЕНИЯ н-ГЕПТАНА НА МЕЗОПОРИСТОМ
КАТАЛИЗАТОРЕ Pt/MSU. ВЛИЯНИЕ АКТИВНОСТИ ЦЕНТРОВ И
ВРЕМЕНИ КОНТАКТА
© 2023 г. Mohammad Javad Asadinasab1, Touba Hamoule2,*
1 Department of Chemical Engineering, Amirkabir University of Technology, Tehran, 15914 Iran
2 Department of Basic Science, Petroleum University of technology, Ahvaz, 63431 Iran
*E-mail: t.hamoule@put.ac.ir
Поступила в редакцию 10 сентября 2021 г.
После доработки 18 марта 2022 г.
Принята к публикации 8 декабря 2022 г.
Синтезированы мезоструктурированные молекулярные сита на основе цеолита MSU с последующим
описанием его свойств и характеристик, который был использован при приготовлении катализаторов
на основе Pt (0.6 и 1.0 мас. %) для гидроконверсии н-гептана (условия опытов: температура 300-450°С,
давление 760 мм рт. ст.). Характеристики проб были определены методами рентгеноструктурного
анализа (XRD), построением изотермы адсорбции-десорбции N2 и термопрограммированной десорб-
ции аммиака (NH3-TPD). Показано, что в данном гетерогенно-каталитическом процессе катализаторы
обладают хорошей активностью и селективностью в отношении реакции изомеризации. Кроме того,
с увеличением количества металлических центров катализатора повышается селективность реакции
ароматизации. По результатам эксперимента была построена кинетическая модель этой реакции. На
основании других публикаций и с учетом полученных характеристик была предложена схема реакции.
Преимущество построенной модели реакции состоит в четком определении кинетических параметров
источника изомеров, ароматических продуктов и продуктов крекинга в зависимости от числа активных
центров катализатора и времени пребывания субстрата на его металло-кислотных центрах.
Ключевые слова: мезопора, селективность, кинетическое моделирование, изомеры
DOI: 10.31857/S0028242123010057, EDN: UBPVIF
Преобразование линейных алканов в развет-
таллических активных центров в гидроконверсии.
вленные изомеры приводит к более высокому окта-
Бифункциональные катализаторы содержат или
новому числу бензина по сравнению с результатами
благородные, или переходные металлы, нанесен-
использования бифункциональных катализаторов
ные на кислотный носитель - цеолит; такие моди-
[1]. Этот процесс является одним из способов ре-
фицированные носители
- важные катализаторы
гулирования нормы расходования ископаемого
процесса перегруппировки [2-11].
топлива и уменьшения количества выбросов вред-
Использование цеолита в качестве носителя ка-
ных соединений в окружающую среду. Среди про-
тализаторов гидроконверсии ограничено низкой
цессов перегруппировки гидроконверсия известна
селективностью изомеризации из-за малого раз-
как один из наиболее важных и экономичных ка-
мера пор микропористых цеолитов. Кроме того,
талитических процессов в нефтеперерабатываю-
открытие мезоструктурированных молекулярных
щей промышленности. В последние годы большое
сит с большой площадью поверхности, высокой
внимание уделяется использованию би- и триме-
проницаемостью и однородными гексагональными
56
ЭКСПЕРИМЕНТАЛЬНОЕ И КИНЕТИЧЕСКОЕ МОДЕЛИРОВАНИЕ
57
структурами цилиндрических мезопор позволило
структуры BEA, а также тетраэтилортосиликата
получить катализаторы (или носители катализато-
(TEOS, Merck) и изопропоксида алюминия (AIP,
ров) для перегруппировки объемных молекул [12].
Merck) в качестве источников кремния и алюминия
Мезопористые молекулярные сита, полученные
соответственно. Кроме того, используют бромид
прямой сборкой нанокластерных прекурсоров це-
цетилтриметиламмония (CTAB, Merck) в качестве
олитного типа, обозначаются как MSU-S или MAS.
поверхностно-активного вещества. Обычно синтез
Данные структуры, повышающие гидротермиче-
MSU состоит из смешивания трех растворов A, B и
скую стабильность и кислотность мезопористого
C по схеме: 0.408 г AIP + 20.41 г TEOS (А), 22.5 мл
материала, улучшают характеристики этих мате-
воды + 27.24 г TEAOH (В), 9.11 г CTAB + 228.6 мл
риалов при их использовании в качестве носите-
воды (С).
ля катализаторов гидроконверсии [13, 14]. Основ-
Раствор, полученный путем смешивания компо-
ные преимущества этих катализаторов - большая
нентов A и B, выдерживали при температуре окру-
площадь поверхности, определенная по методу
жающей среды в течение 2 ч. Затем его помещали
Брунауэра-Эммета-Теллера (BET), и высокая кис-
в автоклав из нержавеющей стали с футеровкой из
лотность, что позволяет широко использовать их
политетрафторэтилена объемом 200 мл при темпе-
в качестве кислотного катализатора и носителя
ратуре 100°С на 3 ч. Кроме того, после гидротер-
[15, 16]. Кинетическая модель реакции - важный
мической обработки добавляли раствор С и дово-
фактор при разработке, оптимизации и управлении
дили рН конечного геля до 9 введением по каплям
процессом перегруппировки. Была изучена кине-
серной кислоты. Окончательный гидротермальный
тика процесса конверсии на катализаторах, нане-
раствор выдерживали при 150°С в течение 48 ч.
сенных на цеолит, и получена новая информация о
Катализатор несколько раз промывали деионизиро-
степени влияния различных параметров на актив-
ванной водой, сушили при 110°С в течение ночи и
ность и селективность катализаторов [17-20].
прокаливали при 600°С в течение 4 ч со скоростью
В данном исследовании впервые разрабатывает-
изменения температуры 1°С/мин.
ся кинетическая модель гидроконверсии н-гептана
Методом пропитки готовили катализаторы с
на катализаторах, нанесенных на MSU, с исполь-
одним металлом, содержащие 0.6 и 1.0 мас. % Pt
зованием мезопористого материала на основе цео-
на носителе MSU при соответствующей концен-
лита. Кинетика гидроконверсии включает реакции
трации раствора H2PtCl6·6H2O, используемого в
изомеризации, крекинга и ароматизации н-гептана
качестве источника платины Pt. После выпарива-
в указанных условиях. В качестве преимуществ
ния растворителя и сушки при 80°С в течение 24 ч
разработанного метода кинетического моделирова-
прокаливали катализатор Pt-MSU при температуре
ния можно выделить четкую характеристику энер-
300°С в течение 24 ч.
гии активации всех продуктов, определить констан-
Каталитическую конверсию н-гептана в присут-
ты реакции по уравнению Аррениуса, конверсии и
ствии водорода проводили в интервале температур
селективности всех продуктов, а также источник
300-450°С, WHSV = 1 ч-1, P = 1 атм. в микроре-
образования сходных продуктов крекинга из раз-
акторе непрерывного действия с неподвижным
ных изомеров. Особое внимание в данной работе
слоем, в который было загружено 0.5 г катализа-
уделяется активности центров и времени контакта
тора. После обработки катализаторов в потоке Н2
карбениевых ионов на кислотных и металлических
(60 мл/мин) в реактор подавали н-гептан. Для по-
центрах.
лучения наилучшей селективности по конкретным
продуктам и предотвращения образования кокса
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
вводили водород в оптимизированном количестве
Приготовление катализатора. Синтезируют
(H2/HC = 10). Рабочие характеристики катализатора
мезоструктурированный (MSU) алюмосиликат с
проверяли после 30 мин его работы в потоке (TOS)
использованием затравок цеолита Beta по ранее
при температурах, указанных для каждого экспери-
описанной методике [21, 22]. Затравки цеолита
мента. Продукты анализировали с помощью встро-
Beta готовят с применением гидроксида тетраэтил-
енного газового хроматографа (YL6100), оснащен-
аммония (TEAOH, Merck) в качестве регулятора
ного пламенно-ионизационным детектором (FID).
НЕФТЕХИМИЯ том 63 № 1 2023
58
MOHAMMAD JAVAD ASADINASAB, TOUBA HAMOULE
Таблица 1. Анализ синтезированных катализаторов
Характеристика катализатора
NH3-TPD
Образец
площадь
объем пор,
температура
десорбированный
катализатора
поверхности ВЕТ,
диаметр пор, Å
см3/гкат
десорбции, °С
NH3, ммоль/г
кат
м2/гкат
MSU
917
0.87
28.5
215
0.25
Результаты определения характеристик и
рованной мезопористой структуры, полученные
проверки активности. Для определения харак-
методом NH3-TPD. Температура десорбции явля-
теристик мезопористых материалов использовали
ется показателем силы кислоты катализатора; ко-
прибор рентгеноструктурного анализа (XRD), ос-
личество десорбированного аммиака характери-
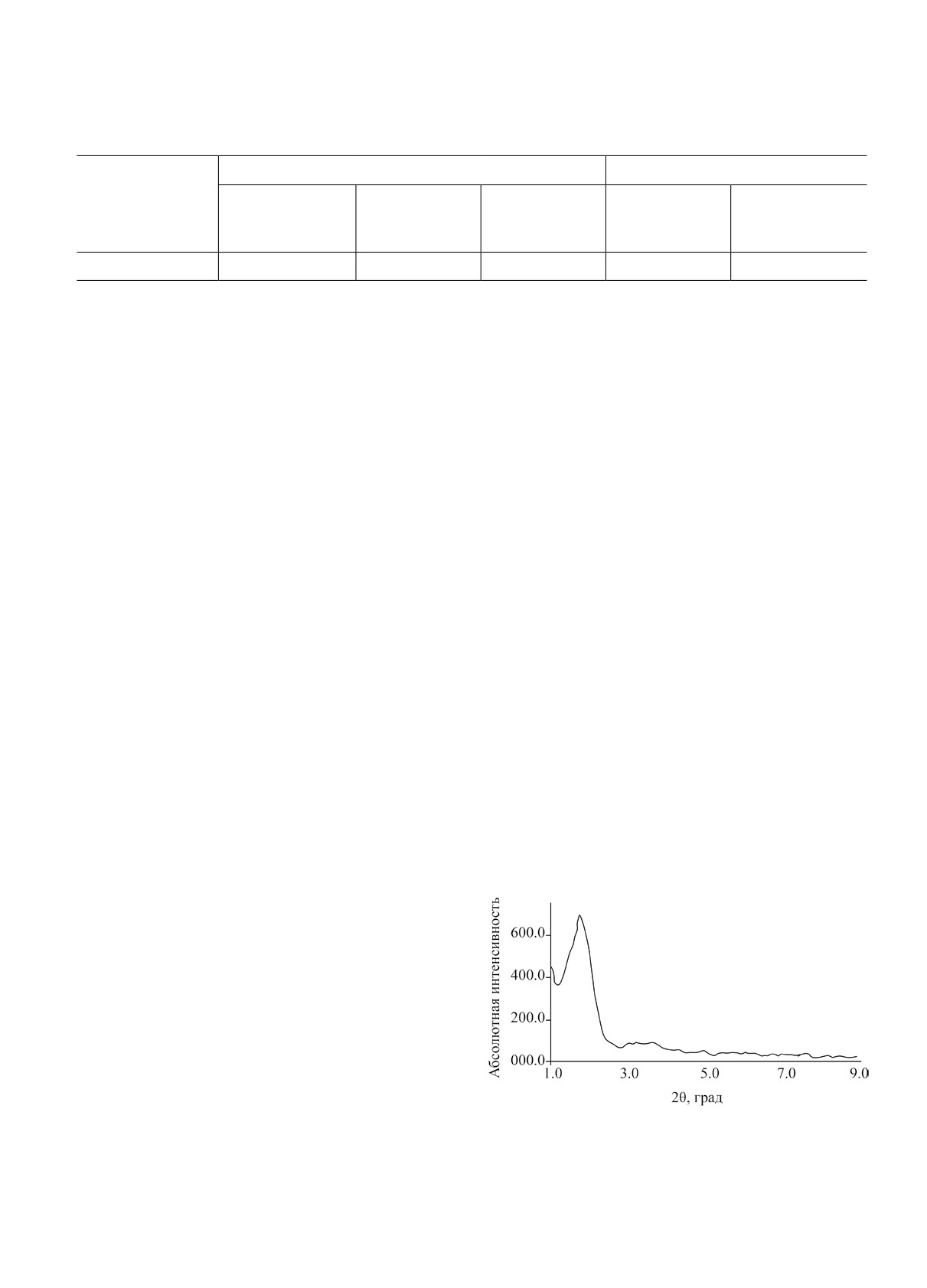
нащенный дифрактометром STOE. На рис. 1 пред-
зует величину кислотности, которую оценивают
ставлена рентгенограмма XRD синтезированного
по площади под каждым из профилей десорбции.
катализатора. Интенсивный пик MSU при 2θ =
Результат показывает, что максимальная темпера-
1°-1.85° отражает плоскость (100) и свидетель-
тура составляет 215°С, это связано с кислотным
ствует о гексагональной мезопористой структуре,
центром умеренной силы. В табл. 2 приведены
описанной в работе Kostas и др. [22]. Для опреде-
общая конверсия н-гептана и селективность по
ления площади поверхности и объема пор приме-
различным продуктам. Основными продуктами
няли изотермы адсорбции-десорбции N2 при 77 K,
являются моноразветвленные изомеры (МОВ),
полученные с помощью прибора ASAP-2010
многоразветвленные изомеры (MUB), продукты
Micrometrics USA (табл. 1). Большая площадь по-
крекинга и ароматизации. Как правило, повыше-
верхности катализатора MSU хорошо согласуется с
ние температуры увеличивает общую конверсию,
предыдущими исследованиями [22, 23]. Для оцен-
селективность крекинга и отношение количества
ки прочности и накопления кислотных центров
многоразветвленных изомеров к количеству мо-
использовали метод термопрограммированной
норазветвленных изомеров, но уменьшает общую
десорбции аммиака (NH3-TPD) с помощью микро-
селективность изомеризации. Селективность ката-
метрического анализатора TPD/TPR Analyzer 2900
лизатора по продуктам изомеризации снижалась
(см. табл. 1).
с повышением температуры и из-за термодина-
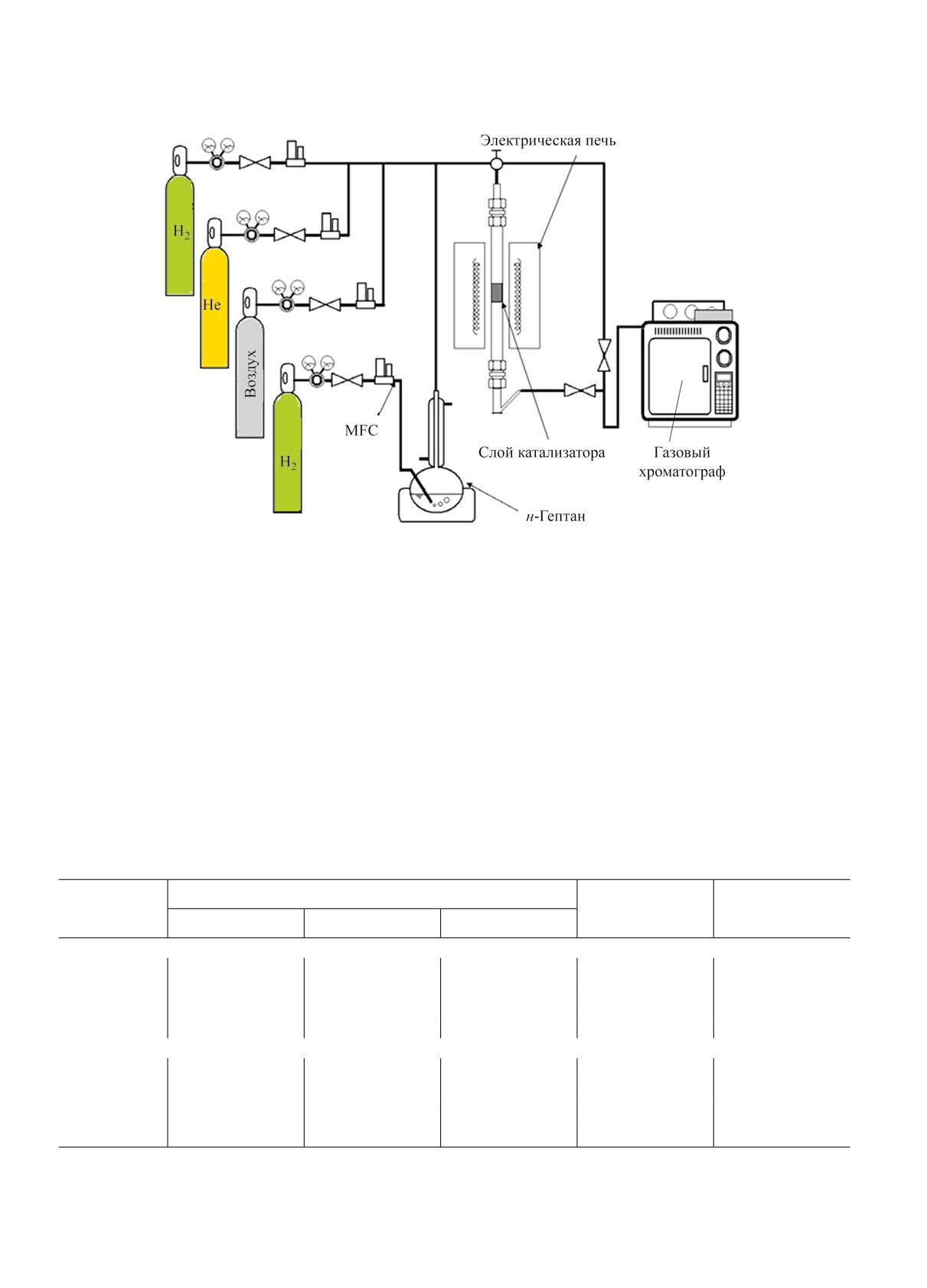
На рис. 2 представлена схема процесса гидро-
мических ограничений [24]. Здесь 2-метилгексан
конверсии. После обработки катализатора в пото-
(2MC6), 3-метилгексан (3MC6) являются монораз-
ке водорода 60 мл/мин в реактор подают н-гептан.
Кроме того, в реактор вводят водород в оптимизи-
рованном количестве (H2/HC = 10) для получения
наилучшей селективности по конкретным продук-
там. Следовательно, время работы катализаторов
(TOS), составляющее 0.5 ч-1, при заданной темпе-
ратуре характеризует их эффективность в каждом
эксперименте. Для анализа продуктов реакции
применяли газовую хроматографию с пламенно-
ионизационным детектором FID 6100 в реальном
времени.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Результаты эксперимента. В табл. 1 представ-
Рис. 1. Рентгенограмма рентгено-структурного анализа
катализатора MSU.
лены количество центров и кислотность синтези-
НЕФТЕХИМИЯ том 63 № 1 2023
ЭКСПЕРИМЕНТАЛЬНОЕ И КИНЕТИЧЕСКОЕ МОДЕЛИРОВАНИЕ
59
Рис. 2. Схематическое изображение процесса гидроконверсии.
ветвленными продуктами, а
2,3-диметилпентан
му (PCP) с соотношением 2MC6/3MC6, равным 0.5.
(2,3DMC5), 2,4-диметилпентан (2,4DMC5) и 2,2-ди-
Таким образом, отношение 2MC6/3MC6 близко к
метилпентан (2,2DMС5) - многоразветвленными.
термодинамическому значению 0.81 при темпера-
Результаты показывают, что селективность моно-
туре 350°С. Падение селективности изомера 3MC6
разветвленных изомеров 2MC6 и 3MC6 снижается
больше, чем у изомера 2MC6. По результатам ис-
с повышением температуры и конверсии на двух
следования, в этих катализаторах температура по-
каталитических системах. Согласно Vazquez и др.
давляет более быстрый 1,2-алкилгидридный сдвиг,
[25], при перегруппировке алкилкарбений-иона об-
разование 2- и 3-метилгексанов происходит только
который обычно приводит к конверсии изомера
по протонированному циклопропановому механиз-
2MC6 в изомер 3MC6.
Таблица 2. Селективность катализатора и конверсия н-гептпана на катализаторе Pt/MSU
Селективность по реакциям, мас. %
Температура,
Всего, %
Конверсия, мас. %
°C
изомеризации
крекинга
ароматизации
0.6% Pt
300
69.9
14.6
15.5
100.0
3.3
350
68.2
16.2
15.6
100.0
15.3
400
49.9
29.2
20.9
100.0
47.9
450
31.6
36.9
31.5
100.0
65.2
1.0% Pt
300
55.9
11.0
33.1
100.0
43.0
350
7.3
36.3
56.4
100.0
93.0
400
4.4
35.5
60.1
100.0
74.0
450
0.0
32.1
67.9
100.0
88.0
НЕФТЕХИМИЯ том 63 № 1 2023
60
MOHAMMAD JAVAD ASADINASAB, TOUBA HAMOULE
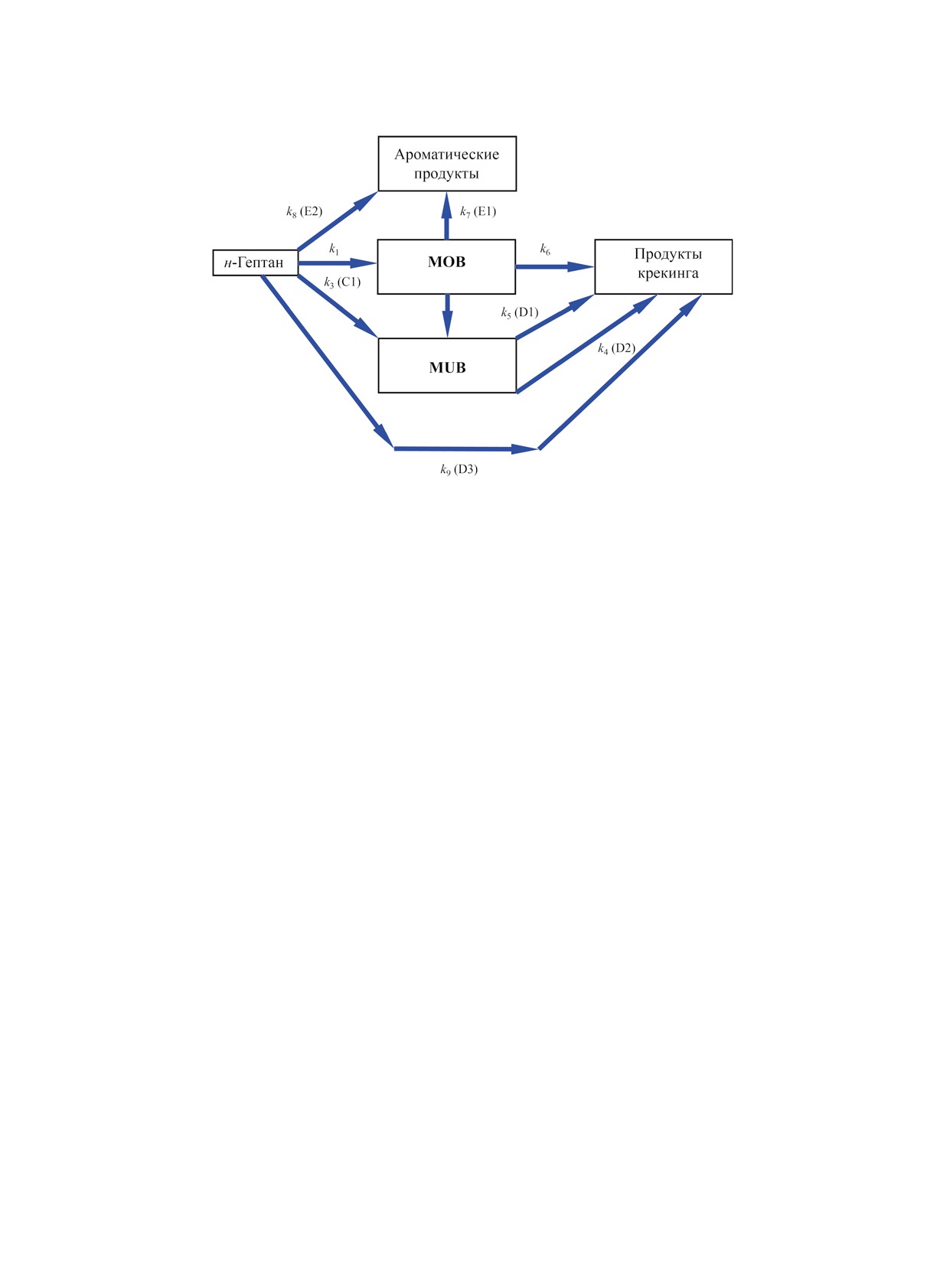
Рис. 3. Предлагаемая кинетическая схема реакции гидроконверсии н-гептана.
Среди многоразветвленных изомеров селектив-
тается, что реакции крекинга при высоких темпе-
ность изомера 2,3DMC5 оказывается выше, чем у
ратурах происходят на кислотных центрах. В этом
других многоразветвленных изомеров. Увеличе-
процессе протонирование алканов на кислотных
ние образования многоразветвленных изомеров с
центрах Брэнстеда является стадией, определяю-
повышением температуры и конверсии указывает
щей скорость реакции для всех алканов. Таким об-
на то, что они являются вторичными продуктами,
разом, ароматизация и крекинг - конкурирующие
образующимися из первичных моноразветвленных
реакции [27].
изомеров благодаря формированию промежуточ-
Кинетика. Кинетика реакций гидроконверсии
ного соединения протонированного циклопропана
была рассмотрена путем определения модели в со-
[26].
ответствии с характеристиками катализатора и экс-
Результаты показывают, что продукты крекин-
периментальными результатами. Все реакции счи-
га при низких температурах почти родственны
тали реакциями первого порядка, а термической
семействам С3 и С4. С повышением температуры
конверсией пренебрегали [28, 29]. На рис. 3 показа-
селективность семейств С1 и С2 увеличивается, ве-
на предлагаемая схема кинетической реакции для
роятно, за счет вторичного крекинга при высоких
гидроконверсии н-гептана, который превращается
температурах и подходящих условиях для гидроге-
в изомеры MOB, MUB, ароматические углеводоро-
нолиза.
ды и продукты крекинга. MOB производит толуол,
а MUB в основном 2,3DMC5 или продукты крекин-
Ароматические углеводороды образуются из
дигидроформирующего кольца парафина. В этом
га. Кинетические параметры определяются с помо-
щью компьютерной программы в пакете MATLAB,
двухфакторном механизме реакции гидрирования-
дегидрирования (HDH) на металлических центрах
использующей метод Рунге-Кутты четвертого по-
рядка с фиксированным размером интервала.
протекают быстрее, чем реакции изомеризации на
кислотных центрах, так что эта стадия регулирует
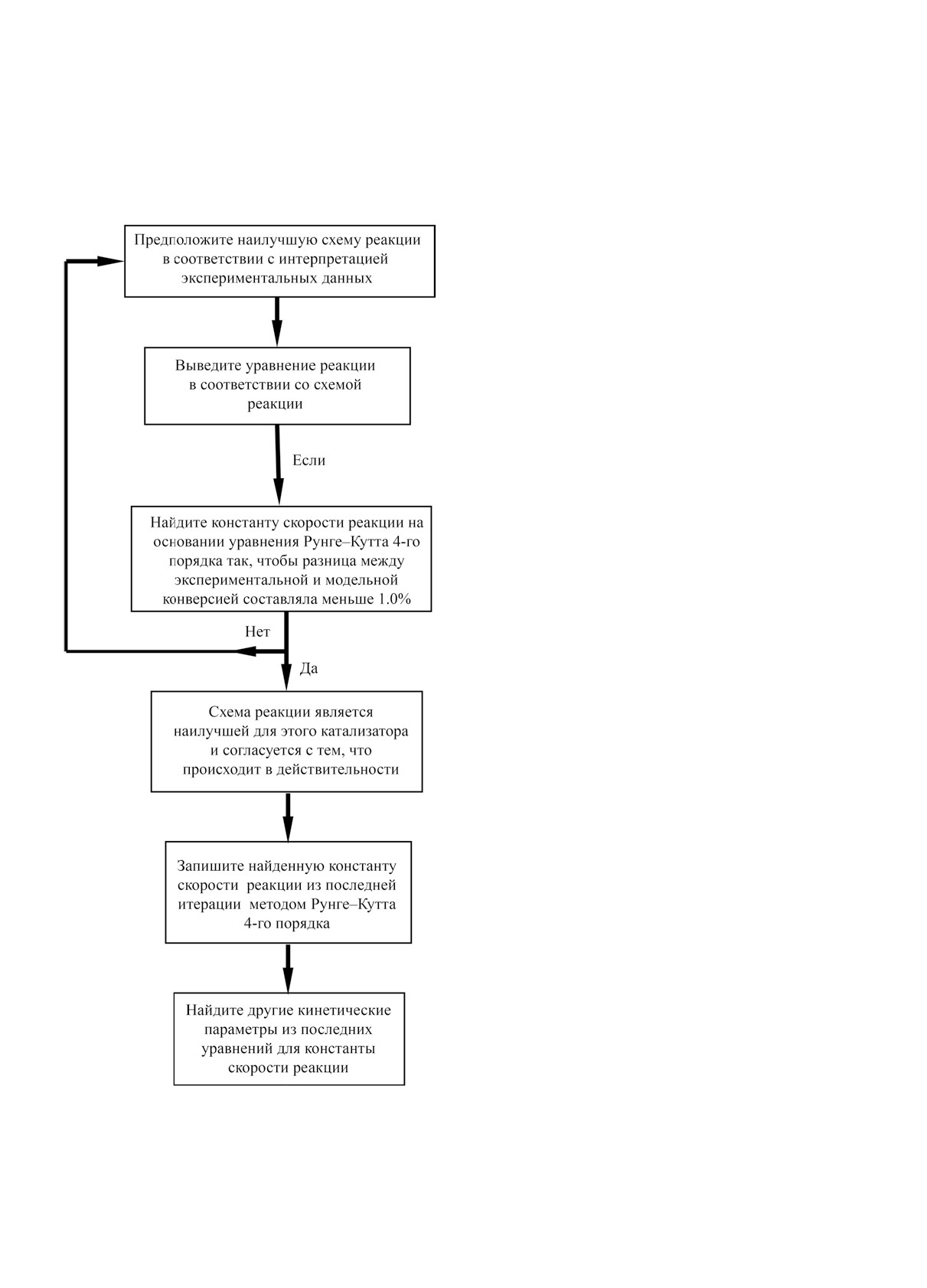
Определение алгоритма. Путем определения
скорость реакции. Благодаря подходящей кислот-
алгоритма, приведенного на рис. 4, были рассчи-
ности синтезированных катализаторов в данном
таны константа скорости реакции, энергия актива-
исследовании они имели благоприятную селектив-
ции, предэкспоненциальный множитель процесса
ность в процессе ароматизации. Кроме того, счи-
перегруппировки, конверсия и селективность с ис-
НЕФТЕХИМИЯ том 63 № 1 2023
ЭКСПЕРИМЕНТАЛЬНОЕ И КИНЕТИЧЕСКОЕ МОДЕЛИРОВАНИЕ
61
пользованием метода Рунге-Кутты четвертого по-
рядка с фиксированным размером интервала. Как
показано на рис. 4, сначала в соответствии с описа-
нием эксперимента предполагается схема реакции,
подобная той, что представлена на рис. 3. Все урав-
нения скорости реакции, а также уравнения (1)-(9)
были получены в соответствии с последним опре-
делением указанной схемы:
Ca = exp (t(k1 + k3 + k8 + k9)),
(1)
где Ca
- концентрация непрореагировавшего
сырья;
Cb = (k1/(k1 + k3 + k8 + k9 - (k2 + k6 + k7)))·
(exp - t(k2 + k6 + k7) - exp - t(k1 + k3 + k8 + k9)),
(2)
где Cb - концентрация моноразветвленного про-
дукта;
CC1 = (k3/(k5 - (k1 + k3 + k8 + k9)))·
(exp - t(k1 + k3 + k8 + k9) - exp - t(k5))),
(3)
где CC1 - концентрация 2,2-диметилпентана;
CC2 = (k1·k2/((k1 + k3 + k8 + k9-(k2 + k6 + k7))·
(k4-(k2 + k6 + k7)))·(exp t(k2 + k6 + k7) - exp t(k4)) +
(k1·k2/(k2 + k6 + k7·(k1 + k3 + k8 + k9))·
(k1 + k3 + k8 + k9 - k4))·
(exp - t(k1 + k3 + k8 + k9) - exp - t(k4)),
(4)
где CC2 - концентрация 2,2- и 2,4-диметилпентана;
CD1 = (k3·k5/(k5 - (k1 + k3 + k8 + k9)))·
(((1- exp t(k1 + k3 + k8 + k9)) / (k1 + k3 + k8 + k9)) -
((1- exp -t·k5)/k5)) + (k1·k6/(k1 + k3 + k8 + k9 -
(k2 + k6 + k7)))·(((1- exp- t(k2 + k6 + k7) / (k2 + k6 + k7)) -
(1- exp-t(k1 + k3 + k8 + k9))/(k1 + k3 + k8 + k9)),
(5)
где CD1 - концентрация пропана и н-бутана;
CD2 = (k1·k2·k4/((k1 + k3 + k8 + k9 - (k2 + k6 + k7))·
(k4(k2 + k6 + k7)))·(((1 - exp - t(k2 + k6 + k7))/(k2 + k6 + k7)) -
((1- exp t(k4))/k4)) + (k1·k2·k4/(k2 + k6 + k7 - (k1 + k3 + k8 +
k9))·(k1 + k3 + k8 + k9 - k4))·
(((1- exp-t(k1 + k3 + k8 + k9)/(k1 + k3 + k8 + k9)) -
((1- exp - t(k4))/k4)),
(6)
где CD2 - концентрация пропана и изобутана;
CD3 = (k9/(k1 + k3 + k8 + k9)) -
(1- exp- t(k1 + k3 + k8 + k9)),
(7)
Рис. 4. Схематический алгоритм процесса перегруппи-
где CD3 - концентрация метана, этана и циклобу-
ровки н-гептана.
тана;
НЕФТЕХИМИЯ том 63 № 1 2023
62
MOHAMMAD JAVAD ASADINASAB, TOUBA HAMOULE
Таблица 3. Кинетические параметры гидроконверсии н-гептана на катализаторе 0.6% Pt/MSU
Номер реакции
Параметры
1
2
3
4
5
6
7
8
9
Тип реакции
гидроизомеризация
крекинг
ароматизация
крекинг
Еа, ккал/моль
34.45
27.38
26.95
40.7
37.95
38.34
20.24
26.1
39.14
K0
49.2
30.6
26.9
13.9
14.45
15.25
37.6
35.15
14.42
Таблица 4. Кинетические параметры гидроконверсии н-гептана на катализаторе 1.0% Pt/MSU
Номер реакции
Параметры
1
2
3
4
5
6
7
8
9
Тип реакции
гидроизомеризация
крекинг
ароматизация
крекинг
Еа, ккал/моль
34.45
27.38
26.95
40.70
37.95
38.34
20.24
26.10
39.14
K0
49.21
30.60
26.90
13.92
14.45
15.25
37.6
35.15
14.42
CE1 = (k1·k7/(k1 + k3 + k8 + k9 - (k2 + k6 + k7))·
личных продуктов. Результаты моделирования и
(((1- exp - t(k2 + k6 + k7))/(k2 + k6 + k7)) -
эксперимента совпадают друг с другом и наилуч-
шим образом согласуются с тем, что происходит в
((1- exp -t(k1 + k3 + k8 + k9))/(k1 + k3 + k8 + k9))) +
действительности, поэтому данная схема идеально
(k8/(k1 + k3 + k8 + k9))·(1- exp- t(k1 + k3 + k8 + k9)), (8)
подходит для этой кинетической конверсии.
где CE1 - концентрация толуола;
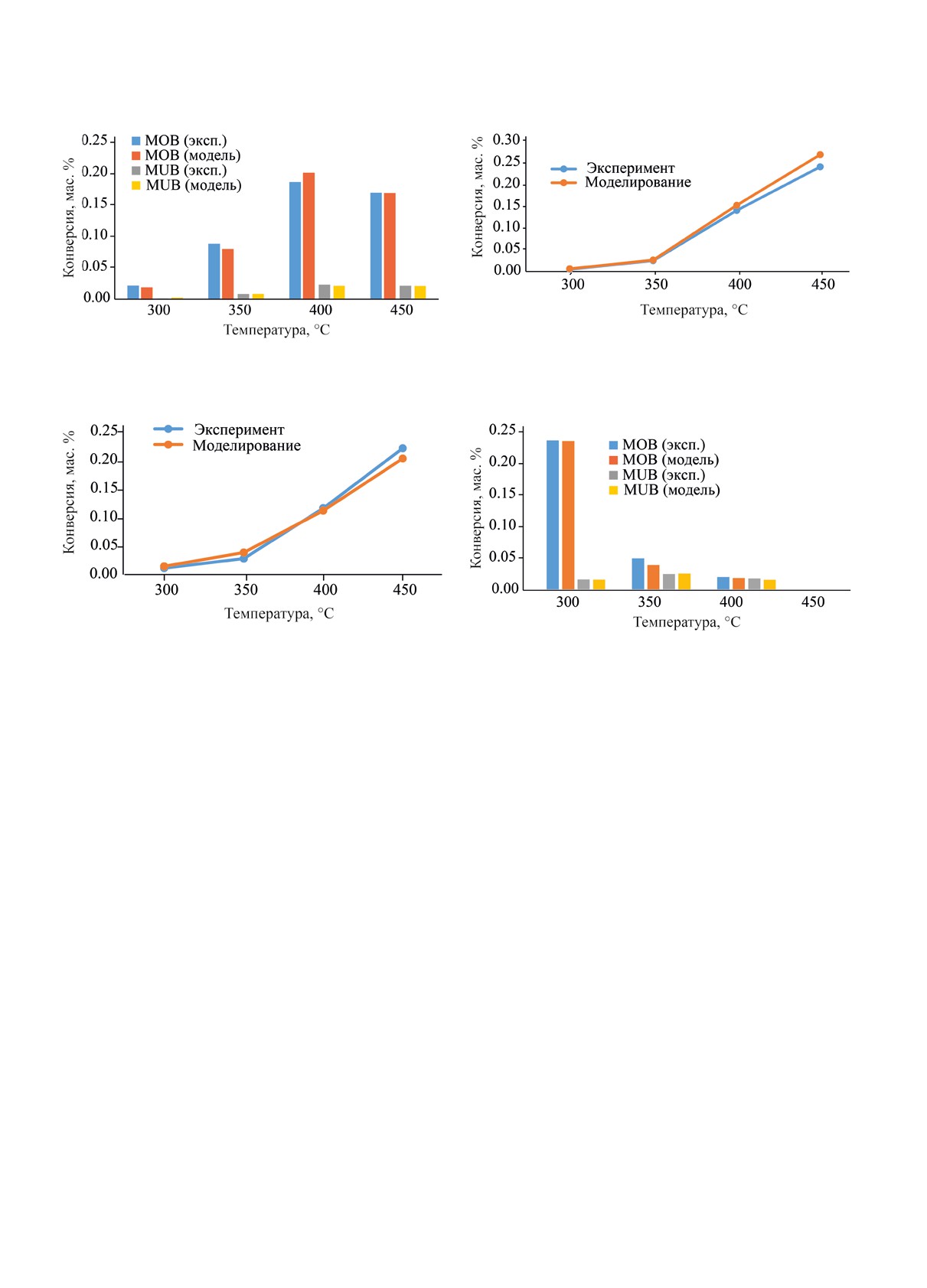
Как показано на рис. 5, значение модельной
CE2 = (k8/(k1 + k3 + k8 + k9)) (1- exp -
конверсии изомеров MOB при температуре 300°С
t(k1 + k3 + k8 + k9)),
(9)
ниже значения конверсии экспериментальной. Со-
где CE2 - концентрация бензола, ксилола и цикло-
ответственно, незначительная разница при посто-
пентана.
янной массовой объемной скорости (WHSV) обу-
словлена высоким потенциалом кислотного центра
В соответствии с этой моделью четко рассчиты-
ваются указанные параметры. Если селективность
для образования изомера MOB при низких темпе-
и конверсия, полученные на основе расчетных па-
ратурах. По мере повышения температуры экспе-
раметров, подтверждаются экспериментальными
риментальные результаты изомеров MUB стано-
результатами, значит эта схема хорошо согласуется
вятся выше, чем результаты моделирования, в то
с экспериментом; в противном случае надо менять
время как экспериментальные результаты MOB
предварительную оценку схемы.
становятся ниже, чем результаты моделирования.
Чтобы найти константу скорости реакции, со-
Это явление происходит из-за двух факторов. Было
ответствующую реакции на схеме, алгоритм необ-
предположено, что зависимость между температу-
ходимо преобразовать в код MATLAB с использо-
рой и активностью центра является линейной, од-
ванием метода Рунге-Кутты четвертого порядка.
нако экспериментальные результаты показывают,
Если рассчитанный параметр согласуется с экспе-
что эта зависимость не является линейной. При по-
риментальными данными, вычисляются другие ки-
вышении температуры вторичная перегруппировка
нетические параметры. В табл. 3 и 4 представлены
изомеров MOB находится в хорошем равновесии
кинетические параметры, полученные в результате
между металлическими и кислотными центрами.
этого моделирования.
При этом образование изомеров MUB ускоряется
На рис. 5-10 представлено сравнение экспе-
и создает незначительную разницу с результатами
риментальной и модельной конверсии для раз- моделирования [29].
НЕФТЕХИМИЯ том 63 № 1 2023
ЭКСПЕРИМЕНТАЛЬНОЕ И КИНЕТИЧЕСКОЕ МОДЕЛИРОВАНИЕ
63
Рис. 6. Конверсия сырья в продукт крекинга
Рис. 5. Конверсия сырья в изомер (0.6% Pt/MSU).
(0.6% Pt/MSU).
Рис. 7. Конверсия сырья в ароматические продукты
Рис. 8. Конверсия сырья в изомер (1.0% Pt/MSU).
(0.6% Pt/MSU).
На рис. 6 показано сравнение эксперименталь-
центрами разница между этими двумя наборами
ных результатов и результатов моделирования по
результатов была незначительной, что свидетель-
получению продуктов крекинга. Причина расхож-
ствует о надежности предложенной модели.
дения между ними (экспериментальные данные
Экспериментальные результаты и результа-
ниже, чем модельные) объясняется следующим
ты моделирования для продуктов MOB и MUB
образом.
(рис. 8) хорошо совпадают, что и в этом случае под-
Обычно пропан получают из изомеров MUB.
тверждает надежность предложенной модели.
Поэтому было высказано предположение, что
Как видно, для катализатора с 0.6% Pt равнове-
вклад изомера 2,3DMC5 в производство С3 сос-
сие кислотных и металлических центров является
тавляет 40%, а изомеров 2,2- и 2,4DMC5 - 60%.
приемлемым, и существует лишь незначительная
Однако результаты эксперимента показывают, что
разница между результатами, полученными для
это соотношение было неправильным. Решение
продуктов крекинга и ароматических углеводоро-
данной проблемы было достигнуто благодаря тому,
дов. Однако с увеличением количества металли-
что разница между этими двумя факторами стала
ческих центров это равновесие исчезает, и синтез
незначительной за счет изменения указанного со-
ароматических углеводородов превалирует над
отношения до оптимального значения.
синтезом продуктов крекинга.
На рис. 7 показано сравнение эксперименталь-
По мере повышения температуры структура
ных результатов и результатов моделирования для
бифункциональных участков катализатора (и ка-
ароматических продуктов. Благодаря хорошему
налов между ними) становится более плотной. В
равновесию между кислотными и металлическими
результате этого явления пористость катализатора
НЕФТЕХИМИЯ том 63 № 1 2023
64
MOHAMMAD JAVAD ASADINASAB, TOUBA HAMOULE
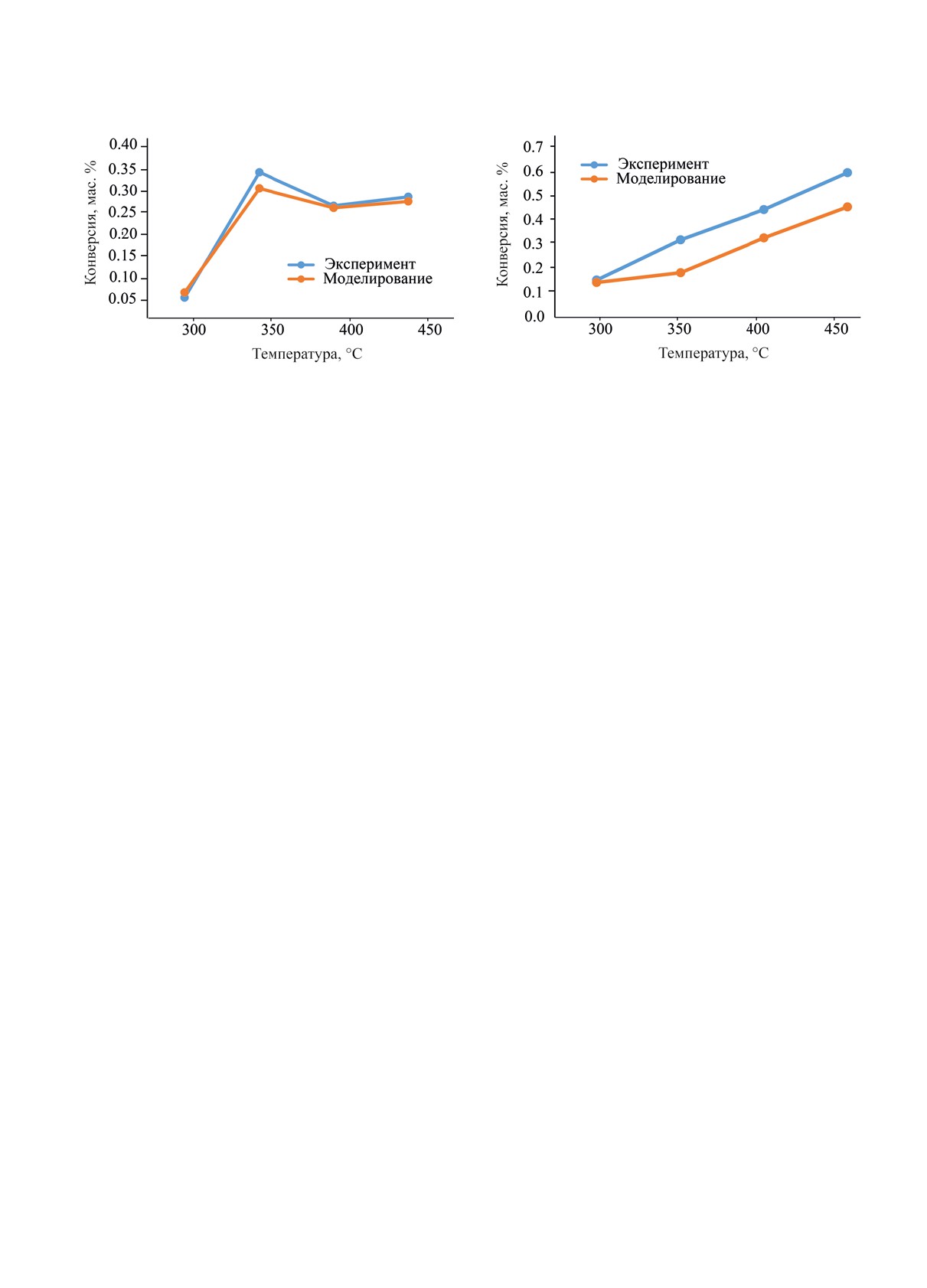
Рис.
9. Конверсия сырья в продукт крекинга
Рис. 10. Конверсия сырья в ароматический продукт
(1.0% Pt/MSU).
(1.0% Pt/MSU).
стремится к минимальному значению, так что ко-
ускоряется реакция гидрирования-дегидрирова-
личество эффективных путей между металлом и
ния, поэтому при высоких температурах не хватает
кислотным центром уменьшается.
времени для протекания реакции изомеризации.
Как показано на рис. 9, разница в конверсии
Увеличение дисперсности металлических центров
между экспериментальными результатами и ре-
связано с уменьшением времени контакта на над-
зультатами моделирования по продуктам крекин-
кислотных центрах. Результаты показывают, что
га незначительна. Следовательно, можно предпо-
с увеличением скорости реакции гидрирования-
ложить, что пористость структуры катализатора
дегидрирования выход изомеров при высоких тем-
1% Pt/VSU с увеличением температуры не меняет-
пературах падает до нуля, а выход ароматических
ся, т.е. катализатор остается стабильным при высо-
соединений увеличивается. Следовательно, повы-
ких температурах.
шение количества металлических центров ограни-
чивает вторичную реакцию изомеризации.
На рис. 10 представлено сравнение эксперимен-
тальных результатов и результатов моделирования
для ароматических продуктов. Увеличение коли-
ВЫВОДЫ
чества металлических центров до 1% Pt вызыва-
Сравнение результатов эксперимента и модели-
ет ускорение реакции гидрирования-дегидриро-
рования показывает, что модель, представленная
вания. На основании обзора литературы влияние
в данной работе, хорошо согласуется с процессом
доступности и дисперсности металлических цен-
перегруппировки, происходящим при эксперименте.
тров играет важную роль в отклонении пути реак-
Энергия активации реакции получения изо-
ции из-за уменьшения времени контакта субстрата
меров MOB и MUD из MOB для катализатоа с
на катализаторе для взаимодействия с другой ча-
1.0% Pt выше, чем у катализатора, содержащего
стью центров [30-32]. Таким образом, при посто-
0.6% Pt. Увеличение дисперсности металлических
янной дисперсности кислотных центров не хва-
центров уменьшает время пребывания субстрата
тало времени для изомеризации на этих центрах.
на каталитических надкислотных центрах. Это,
Кинетические параметры показывают, что энергия
в конечном счете, связано с ускорением реакции
активации реакции ароматизации ниже, чем у ре-
гидрирования-дегидрирования, что ограничивает
акции изомеризации, а энергия активации реак-
реакцию вторичной изомеризации.
ции изомеризации ниже, чем у реакции крекинга.
Следовательно, на кислотных центрах происходит
При высоких температурах создается конкурен-
реакция циклизации, затем реакция изомеризации
ция между реакциями крекинга и ароматизации.
и, наконец, реакция крекинга. Таким образом, при
Результаты моделирования процесса для катали-
увеличении дисперсности металлических центров
заторов с более высоким содержанием металли-
НЕФТЕХИМИЯ том 63 № 1 2023
ЭКСПЕРИМЕНТАЛЬНОЕ И КИНЕТИЧЕСКОЕ МОДЕЛИРОВАНИЕ
65
ческих центров показали, что ароматизация прева-
лирует над крекингом; это связано с увеличением
org/10.1016/j.jiec.2013.09.055
4.
Hajimirzaee S., Mehr A.S., Ghavipour M., Vatankhah
активности реакции гидрирования-дегидриро-
M., Behbahani R.M. Effect of metal loading on catalytic
вания на высокопрочном катализаторе. Согласно
activity and selectivity of ZSM-5 zeolite catalyst in
обзору литературы, одной из основных проблем,
conversion of methanol to olefins and aromatics // Petrol.
связанных с отклонением селективности катализа-
тора, является прочность структуры. Это означает,
org/10.1080/10916466.2016.1258413
что любое изменение селективности катализатора
5.
Kluksdahl H.E. Reforming a sulfur-free naphtha with a
обусловлено балансом центров и их активностью.
platinum-rhenium catalyst. Patent US3415737A, 1968.
Мы приходим к выводу, что структура нашего ка-
6.
Zhua L., DePristo A.E. Microstructures of bimetallic
тализатора отличается прочностью и не изменяется
clusters: Bond order metal simulator for disordered
при повышении температуры.
org/10.1006/jcat.1997.1586
Кинетические параметры конверсии н-гептана
7.
Qi W., Ran J., Zhang Z., Niu J., Zhang P., Fu L.,
в толуол показывают, что катализатор с большим
Hu B., Li Q. Methane combustion reactivity during the
количеством металлических центров оказывается
metal→metallic oxide transformation of Pd-Pt catalysts:
эффективнее, что связано с увеличением скорости
Effect of oxygen pressure // Appl. Surf. Sci. 2018. V. 435.
протекания реакции гидрирования-дегидрирова-
ния и уменьшением времени контакта субстрата
8.
Liu H., Lei G.D., Sachtler W.M.H. Pentane and butane
на активных кислотных центрах. Согласно иссле-
isomerization over platinum promoted sulfated zirconia
дованию реакции гидроконверсии, селективность
catalysts // Appl. Catal. A: Gen. 1998. V. 146. P. 165-
изомера может быть оптимизирована за счет уве-
личения числа кислотных центров.
9.
Balakrishnan J.H., Schwank J. A chemisorption and
XPS study of bimetallic Pt-Sn/Al2O3 catalysts // J. Catal.
КОНФЛИКТ ИНТЕРЕСОВ
9517(91)90227-U
Авторы заявляют об отсутствии конфликта
10.
Ponec V., Bond G.C. Reactions of alkanes and reforming
интересов, требующих раскрытия в данной статье.
of naphtha // Stud. Surf. Sci. Catal. 1995. V. 95. № C.
P. 583-677.
11.
Barbiera J., Marécot P., Del Angel G., Bosch P.,
ИНФОРМАЦИЯ ОБ АВТОРАХ
Boitiaux J.P., Didillon B., Dominguez J.M., Schiftef I.,
Mohammad Javad Asadinasab, ORCID: https://
Espmosa G. Preparation of platinum-gold bimetallic
orcid.org/0000-0002-0666-8285
catalysts by redox reactions // Appl. Catal. A: Gen. 1994.
860X(94)80288-2
0002-1738-6785
12.
Siegmund Greulich-Weber H.M. Ordered Porous
Nanostructures and Applications, ed. by R. Wehrspohn. -
СПИСОК ЛИТЕРАТУРЫ
New York: Kluwer Academic Plenum, 2005. P. 350-351.
1. van de Runstraat A., Kamp J.A., Stobbelaar P.J., van
13.
Zhao D., Feng J., Huo Q., Melosh N., Fredrickson G.H.,
Grondelle J., Krijnen S., van Santen R.A. Kinetics
Chmelka B.F., Stucky G.D. Triblock copolymer synthesis
of hydro-isomerization of n-hexane over platinum
of mesoporous silica with periodic 50 to 300 angstrom
containing zeolites // J. Catal. 1997. V. 171. № 1.
pores // Science. 1998. V. 279. № 5350. P. 548-552.
2. Zhang A., Nakamura I., Aimoto K., Fujimoto K.
14.
Sachtler W.M.H., Liu H., Lei G.D. Selectivity and rate
Isomerization of n-pentane and other light hydrocarbons
of activity decline of bimetallic catalysts. The viscosity
on hybrid catalyst. Effect of hydrogen spillover // Ind.
of concentrated suspensions and solutions // Appl. Catal.
A: Gen. 1976. V. 14. P. 1-12.
org/10.1021/ie00043a008
15.
Bagshaw S.A., Kemmitt T., Milestone N.B. Mesoporous
3. Mishra G.S., Machado K., Kumar A. Highly selective
[M]-MSU-x metallo-silicate catalysts by non-ionic
n-alkanes oxidation to ketones with molecular oxygen
polyethylene oxide surfactant templating1: Acid
catalyzed by SBA-15 supported rhenium catalysts // J.
[N0(N+)X-I+] and base (N0M+I-) catalysed pathways //
НЕФТЕХИМИЯ том 63 № 1 2023
66
MOHAMMAD JAVAD ASADINASAB, TOUBA HAMOULE
Microporous Mesoporous Mater. 1998. V. 22. P. 419-
25.
Vazquez M.I., Escardino A., Corma A. Activity and
selectivity of nickel-molybdenum/HY ultrastable zeolites
16.
Liu L., Li H., Zhang Y. Effect of synthesis parameters on
for hydroisomerization and hydrocracking of alkanes //
the chromium content and catalytic activities of meso-
Ind. Eng. Chem. Res. 1987. V. 26. № 8. P. 1495-1500.
porous Cr-MSU-x prepared under acidic conditions // J.
Phys. Chem. B. 2006. V. 110. P. 15478-15485. https://
26.
Patrigeon A., Benazzi E., Travers Ch., Bernhard J.Y.
doi.org/10.1021/jp061875o
Influence of the zeolite structure and acidity on the
17.
von Aretin T., Hinrichsen O. Single-event kinetic model
hydroisomerization of n- heptane // Catal. Today. 2001.
for cracking and isomerization of 1-hexene on ZSM-5 //
Ind. Eng. Chem. Res. 2014. V. 53. № 50. P. 19460-
5861(00)00558-7
27.
Mokaya R., Jones W., Moreno S., Poncelet G. n-heptane
18.
von Artein T., Schallmoser S., Standle S., Tonigold M.,
hydroconversion over aluminosilicate mesoporous
Lercher J.A., Hinrichsen O. Single event kinetic model
molecular sieves // Catal. Letters. 1997. V. 49. P. 87-94.
for 1-pentane cracking on ZSM-5 // Ind. Eng. Chem.
28.
Wang Z., Guo Y., Lin R. Effect of triethylamine on the
org/10.1021/acs.iecr.5b02629
cracking of heptane under a supercritical condition and
19.
Ying L., Zhu J., Cheng Y., Wang L., Li, X. Kinetic
the kinetic study on the cracking of heptane // Energ.
modeling of C2-C7 olefins interconversion over
ZSM-5 catalyst // J. Ind. Eng. Chem. 2016. V. 33.
Convers. Manage. 2008. V. 49. № 8. P. 2095-2099.
20.
Huang X., Aihemaitijiang D., Xiao W.D. Reaction
29.
Maloncy M.L., Maschmeyer T., Jansen J.C. Technical
pathway and kinetics of C3-C7 olefin transformation
and economical evaluation of zeolite membrane based
over high-silicon HZSM-5 zeolite at 400-490°C //
heptane hydroisomerization process // Chem. Eng. J.
org/10.1016/j.cej.2015.05.124
CEJ.2004.11.011
21.
Liu Y., Zhang W., Pinnavaia T.J. Steam-stable
30.
Kadiev K.M., Maximov A.L., Kadieva M.K. The
aluminosilicate mesostructures assembled from zeolite
effect of MoS2 active site dispersion on suppression
type Y seeds // J. Am. Chem. Soc. 2000. V. 122. № 36.
of polycondensation reactions during heavy oil
hydroconversion // Catalysts. 2021. V. 11. № 6. P. 676.
22.
Triantafyllidis K.S., Iliopoulou E.F., Antonakou E.V.,
Lappas A.A., Wang H., Pinnavaia T.J. Hydrothermally
31.
van der Wal L.I., Oenema J., Smulders L.C.J.,
stable mesoporous aluminosilicates (MSU-S) assembled
Samplonius N.J., Nandpersad K.R., Zečević J.,
from zeolite seeds as catalysts for biomass pyrolysis //
de Jong K.P. Control and impact of metal loading
Microporous Mesoporous Mater. 2007. V. 2007. P. 132-
heterogeneities at the nanoscale on the performance
of Pt/zeolite Y catalysts for alkane hydroconversion //
23.
Gagea B.C., Lorgouilloux Y., Altintas Y., Jacobs P.A.,
Martens J.A. Bifunctional conversion of n-decane over
org/10.1021/acscatal.1c00211
HPW heteropoly acid incorporated into SBA-15 during
32.
Gutierrez-Acebo E., Leroux C., Chizallet C., Schuurman Y.,
synthesis // J. Catal. 2009. V. 265. P. 99-108. https://doi.
org/10.1016/j.jcat.2009.04.017
Bouchy C. Metal/acid bifunctional catalysis and intimacy
24.
Maxwell I.E. Zeolites catalysis in hydroprocessing
criterion for ethylcyclohexane hydroconversion: When
technology // Catal. Today. 1987. V. 1. № 4. Р. 385-413.
proximity does not matter // ACS Catal. 2018. V. 8.
НЕФТЕХИМИЯ том 63 № 1 2023