НЕФТЕХИМИЯ, 2023, том 63, № 6, с. 809-837
УДК 541.64+544.476.2
ДВОЙНЫЕ МЕТАЛЛОЦИАНИДНЫЕ (DMC) КАТАЛИЗАТОРЫ:
СИНТЕЗ, СТРОЕНИЕ И МЕХАНИЗМ ДЕЙСТВИЯ (ОБЗОР)
© 2023 г. Д. А. Пятаков1,*, И. Э. Нифантьев1,2
1 Институт нефтехимического синтеза им. А.В. Топчиева РАН, Москва, 119991 Россия
2 Московский государственный университет имени М.В. Ломоносова, химический факультет, Москва, 119991 Россия
*Е-mail: dinamitry06@gmail.com
Поступила в редакцию 27 октября 2023 г.
После доработки 8 декабря 2023 г.
Принята к публикации 10 декабря 2023 г.
Двойные металлоцианидные (double metal cyanide, DMC) катализаторы безальтернативны для использо-
вания в промышленном процессе полимеризации пропиленоксида (PO) с целью получения полипропи-
леноксида (PPO) со свойствами, необходимыми для специализированных применений: низкой степенью
ненасыщенности, высокими молекулярными массами и гидроксильными числами. Современные про-
мышленные образцы демонстрируют высокую эффективность, давая возможность проводить процесс с
экстремально низкими загрузками - до 25 ppm, что не требует регенерации катализатора и не приводит
к ухудшению свойств полимеров. Главными недостатками этих материалов являются относительно
сложный синтез и чувствительность к влаге. Несмотря на то, что DMC-катализаторы известны еще с
1960-х гг., их гибридный характер и переменный состав до сих пор затрудняют исследование и выявление
взаимосвязи между способом получения, составом и свойствами этих материалов. Данный литературный
обзор призван систематизировать и проанализировать информацию по синтезу, строению и механизму
действия DMC-катализаторов. Подробно рассмотрен как традиционный синтез, так и нетрадиционные
методы получения DMC-катализаторов. Большое внимание уделено вопросам строения каталитическо-
го центра и механизма полимеризации, а также физико-химическим свойствам этих материалов, как
гетерогенных катализаторов.
Ключевые слова: DMC-катализаторы, гибридные материалы, гетерогенный катализ, полимеризация с
раскрытием цикла, полипропиленоксид
DOI: 10.31857/S0028242123060023, EDN: RSSHIA
Двойные металлоцианидные (double metal
выступают многоатомные спирты и получаемые
cyanide, DMC) катализаторы - уникальные мате-
PPO представляют собой PPO-полиолы, которые в
риалы, используемые в качестве гетерогенных ка-
свою очередь служат мономерами в последующей
тализаторов в производстве полипропиленоксида
поликонденсации с ди- и триизоцианатами для по-
(PPO) путем полимеризации пропиленоксида (PO).
лучения PU.
PPO относится к простым полиэфирам и является
В промышленности широко распространена
крупнотоннажным продуктом, который находит
анионная полимеризация PO в присутствии KOH,
применение в качестве неионогенного поверхност-
однако, она сопряжена с перегруппировкой моно-
но-активного вещества и для получения других ши-
мера в аллиловый спирт, который выступает ини-
роко востребованных полимеров - полиуретанов
циатором (схема 2).
(PU) [1-3]. PPO получают полимеризацией с рас-
крытием цикла (ring-opening polymerization, ROP)
Данная перегруппировка не только приводит
PO в присутствии катализатора и инициатора, или
к появлению ненасыщенных групп в полимере и
«стартера» (схема 1). Чаще всего инициаторами
снижает его гидроксильное число (ГЧ), но и огра-
809
810
ПЯТАКОВ, НИФАНТЬЕВ
OH
O
HO
OH
O
H
n
инициатор
Me
полиизоцианат
Me
O
O
O
PU
кат., T, P
O
O
H
H
n
n
PO
Me
Me
PPO-полиол
Схема 1. Получение полипропиленоксид-полиолов из пропиленоксида.
H
n PO
Me
O
O
K
OH
+
O K
O
H
O
n
Me
Me
Растущая
полимерная цепь
Схема 2. Побочная реакция изомеризации мономера при KOH-катализируемой полимеризации PO.
ничивает молекулярную массу, делая невозмож-
Zn-Co DMC-катализаторы высокоэффективны,
ным получение полимеров с Mn свыше 6 кДа [1].
они позволяют синтезировать полимеры со значи-
Помимо этого, после проведения полимеризации
тельно более высокими молекулярными массами,
требуется дополнительная стадия нейтрализации и
которые при этом содержат на порядок меньшее
отделения неорганических солей от полимера.
число ненасыщенных групп и характеризуются
Недостатки такой анионной полимеризации
более высоким ГЧ. Эти уникальные материалы
позволяют преодолеть DMC-катализаторы, ко-
эффективно катализируют полимеризацию PO при
торые представляют собой гибридные (органо-
загрузках в десятки и сотни ppm, а современные
неорганические) материалы, получаемые из водо-
промышленные образцы предполагают проведение
растворимой соли металла и водорастворимой ме-
полимеризации с экстремально низкими загрузка-
таллоцианидной соли другого металла в присутс-
ми - до 25 ppm [1]. При столь низких загрузках
твии органического(их) лиганда(ов). Состав таких
отсутствует необходимость в пост-синтетической
катализаторов можно выразить формулой [4]:
обработке реакционной массы для отделения ката-
лизатора от полимера, что является несомненным
Ma[M′(CN)b]c · xMXd · yL · zH2O,
технологическим преимуществом, даже несмотря
где M = Zn, Fe(II), Ni(II) и др., M′ = Co(III), Fe(II),
на отсутствие регенерации катализатора.
Fe(III) и др.; MXd - соль металла M, используемая
К недостаткам DMC-катализаторов можно от-
в синтезе; L - органический(ие) лиганд(ы); x, y и z
нести достаточно сложную технологию синтеза и
зависят от способа получения катализатора.
чувствительность к влаге. Также полимеризация
Наиболее доступными и активными явля-
PO в присутствии данных катализаторов сопро-
ются цинк-кобальтовые катализаторы (M = Zn,
вождается образованием очень малых количеств
M′ = Co(III)), получаемые из ZnCl2 и K3[Co(CN)6].
(60-400 ppm) так называемых «высокомолекуляр-
НЕФТЕХИМИЯ том 63 № 6 2023
ДВОЙНЫЕ МЕТАЛЛОЦИАНИДНЫЕ (DMC) КАТАЛИЗАТОРЫ
811
L, H2O
ZnCl2 + K3[Co(CN)6]
Zn3[Co(CN)6]2 xZnCl2 yL zH2O
-KCl
(большой
DMC катализатор
избыток)
L = лиганд(ы)
Схема 3. Общая схема синтеза DMC-катализаторов на примере Zn-Co-материалов.
ных хвостов» («high molecular weight tails») - высо-
лучаемых материалов, а вопрос природы активных
комолекулярной фракции полимера (100-400 кДа),
центров катализатора и механизм полимеризации
наличие которой негативно сказывается на эксплуа-
PO еще до конца не прояснены.
тационных свойствах PU, получаемых из подоб-
Цель данного обзора - систематизация данных
ных PPO-полиолов [3].
о синтезе, строении, механизме каталитического
DMC-комплексы Ma[M′(CN)b]c · xH2O, состав-
действия и физико-химических свойствах рассма-
ляющие неорганическую
«основу» гибридных
триваемых материалов.
DMC-материалов, также известны как аналоги
берлинской лазури Fe3[Fe(CN)6]2 (Prussian blue
СИНТЕЗ DMC-КАТАЛИЗАТОРОВ
analogs, PBA). Берлинская лазурь вошла в историю
как ценный синтетический краситель синего цвета,
широко используемый в 18 и 19 вв. Позднее в 20 в.,
Традиционные методы синтеза
с началом промышленного производства синтети-
DMC-катализаторов
ческого индиго, подобное применение берлинской
Общая характеристика. Подавляющее коли-
лазури сошло на нет, а исследователи стали откры-
чество статей и патентов посвящено Zn-Co DMC-
вать новые грани этого соединения вместе с PBA.
катализаторам как наиболее активным предста-
Например, интригует возможная роль берлинской
вителям данного класса материалов. В основе их
лазури в химической эволюции на Земле [5, 6].
синтеза лежит обменная реакция в водном раство-
PBA интересны как катодные материалы [7, 8],
ре между K3[Co(CN)6] и ZnCl2, взятом в большом
адсорбенты для радиоактивного цезия [9] и газов
избытке, в присутствии органического(их) лиган-
[10, 11], а также своими магнитными свойствами
да(ов). В результате реакции образуется гексациа-
[12]. Самым заметным приложением PBA стал
нокобальтат(III) цинка, который вместе с избытком
синтез на их основе DMC-материалов - уникаль-
ZnCl2, лигандом(ами) и молекулами воды форми-
ных катализаторов, разработанных компанией
руют гибридный материал (схема 3).
General Tire в 1960-х гг. [13]. Однако, за уникаль-
Данные материалы имеют переменный состав,
ностью каталитических свойств скрывается слож-
т.е. x, y и z в формуле DMC-катализатора на схеме 3
ность строения: переменный состав и аморфный
зависят от способа его получения. Следует отме-
характер затрудняют исследование этих матери-
тить, что синтез предполагает варьирование мно-
алов, в результате чего долгое время их описание
жества параметров (соотношение реагентов, при-
можно было прочитать лишь в патентной литера-
рода и количество лигандов, условия промывок,
туре. Публикации в академической среде, посвя-
режим сушки и др.), которые влияют на состав,
щенные DMC-катализаторам, стали появляться
строение и микроструктуру материалов и которые,
лишь в 2000-x гг., что совпало с интересом к про-
в конечном счете, определяют свойства катализа-
цессу сополимеризации эпоксид/CO2 и развитием
тора (период индукции, активность) и продуктов
физико-химических методов анализа и кванто-
полимеризации - PPO-полиолов.
во-химического моделирования. Следствие этого -
недостаток фундаментальных данных о влиянии
Наряду с Zn-Co-катализаторами, к тради-
различных факторов (природа лигандов, реакци-
ционным DMC-катализаторам можно отнес-
онные условия, условия промывки, режим сушки и
ти цинк-железные материалы, полученные из
пр.) на строение и каталитическую активность по-
ZnCl2 и K3[Fe(CN)6] (Zn-Fe(III) материалы) или
НЕФТЕХИМИЯ том 63 № 6 2023
812
ПЯТАКОВ, НИФАНТЬЕВ
K4[Fe(CN)6] (Zn-Fe(II) материалы). Если не сказано
(parallel-flow dropping method, PFDM) [17]. В слу-
иное, в данном обзоре под DMC-катализаторами
чае «RDM» [17-19] катализаторы имеют другую
понимаются Zn-Co-материалы.
кристаллическую структуру, более низкую степень
аморфности и содержат больше калия, что при-
Типичный синтез DMC-катализатора предпола-
водит к меньшей активности (см. ниже) в сравне-
гает медленное (в течение 15-30 мин) добавление
раствора K3[Co(CN)6] к раствору ZnCl2 при ин-
нии с образцами, полученными в режиме «FDM»
[17, 19]. Напротив, «PFDM» продемонстрировал
тенсивном перемешивании и небольшом нагреве
многообещающие результаты с точки зрения ката-
(30-50°C). При этом лиганд и солиганды (при на-
личии) добавляются либо в виде раствора (смеси)
литической активности DMC-материалов [17], но
пока не получил должного внимания в академиче-
сразу после смешения двух исходных растворов,
либо добавляется в сами исходные растворы. Вы-
ской или патентной литературе.
падающий осадок отделяют фильтрованием под
Неорганические прекурсоры. В отличие от
давлением или центрифугированием, после чего
органических лигандов (см. ниже), неоргани-
диспергируют его в водном растворе лиганда и пе-
ческие прекурсоры Zn-Co DMC-катализаторов
ремешивают в течение некоторого времени, а затем
слабо подвержены варьированию. В качестве
снова фильтруют или центрифугируют. Такую ста-
источника цинка применяли ацетат [20, 21], сульфат
дию промывки повторяют еще несколько раз, а за-
[20, 22, 23], трифлат [22, 23] и различные галогениды
тем катализатор подвергают сушке.
[24-26], но во всех случаях полученные на их осно-
Большой избыток ZnCl2 по сравнению со сте-
ве материалы уступали по свойствам тем, что полу-
хиометрическим количеством (1.5 моль на 1 моль
чены из ZnCl2. Исключением являются материалы
K3[Co(CN)6], 1 экв.) критически важен в синтезе
на основе TBA и PTMEG (poly(tetramethylene ether)
DMC-катализаторов, независимо от строения ли-
glycol), описанные в статье [25], где было показано,
гандов и остальных параметров синтеза. Так, в
что ZnBr2 является наилучшим прекурсором с точ-
случае высокоэффективных катализаторов количе-
ки зрения активности катализатора и свойств по-
ство ZnCl2 может составлять до ~16 экв. [14, 15],
лиэфиров. Chen и др. [27, 28] осуществили синтез
что соответствует 24 молям ZnCl2. Совсем недав-
DMC-катализаторов из нерастворимых цинк-со-
но опубликованные результаты in situ мониторинга
держащих прекурсоров - ZnO, Zn(OH)2 и ZnCO3 по
процесса синтеза DMC-катализаторов с помощью
реакции с водорастворимой кислотой H3[Co(CN)6]
рамановской спектроскопии поясняют эту особен-
в присутствии TBA с последующим вымачиванием
ность [16]. Снижение количества ZnCl2 с 23.6 до
в HCl (aq) для удаления непрореагировавших пре-
7.6 моль (≈ в 3 раза) на 1 моль K3[Co(CN)6] и от-
курсоров. Несмотря на несколько более высокую
сутствие трет-бутанола (tert-butyl alcohol, TBA)
активность полученных материалов, данный под-
на стадии смешения неорганических прекурсоров
ход более трудоемок, чем традиционный синтез.
(он добавляется сразу после этой стадии) приво-
В патенте [29] представлен способ получения ма-
дит к существенному увеличению времени, необ-
териалов из смеси ZnCl2 и CaCl2. Также сообща-
ходимого для образования гибридного материала,
лось [30], что допирование крайне малыми количе-
с 0.5 до 10 ч. Таким образом, TBA необходимо
ствами CaCl2 приводит к увеличению активности
добавлять к раствору одной из солей или в оба
материалов, однако никаких объяснений роли соли
раствора солей. Кроме этого, на строение и свой-
кальция ни в патенте, ни в этой статье не приво-
ства рассматриваемых материалов влияет способ
дится. В патенте [31] предложен способ получения
смешения солей. Наиболее распространено до-
катализаторов посредством добавления NaCN к
бавление раствора K3[Co(CN)6] к раствору ZnCl2
смеси ацетата Zn(OAc)2 и CoCl2 при одновремен-
(forward dropping method, FDM), что обеспечива-
ной обработке ультразвуком. В качестве цианид-
ет постоянный локальный избыток соли цинка, но
ной соли в нескольких китайских патентах [32-34]
возможны и другие варианты смешения реагентов:
заявляется смесь достаточно редкого гексациано-
добавление K3[Co(CN)6] к ZnCl2 (reverse dropping
кобальтата(II) - феррата(II) калия K2[CoFe(CN)6]
method, RDM) и одновременное добавление рас-
и традиционного K3[Co(CN)6], однако, вопросы
творов ZnCl2 и K3[Co(CN)6] к раствору лиганда
вызывает плохая растворимость в воде такого пре-
НЕФТЕХИМИЯ том 63 № 6 2023
ДВОЙНЫЕ МЕТАЛЛОЦИАНИДНЫЕ (DMC) КАТАЛИЗАТОРЫ
813
O
O
Me
Me
OH
Me
O
O
OR
OH
O
Me
Me
OR
HO
OR
Me
Me
O
O
O
O
R = Me, Et, Pr, Bu
R = Me, Bu [61],
Me
O O
Et [62, 63]
[59, 60]
O
Me
[61]
O
O
Me
O
Me
O
O
OR
R N
X
N
Me
OH
Me
Me
Me
Me
O
N
R = Me, Et [64], i-Pr, Bu
R = H [65, 66], Me [65]
X = C, S
[40]
[65]
O
O
O O
O
O
HOOC
Me
OR
Y
Y
N
COONa
X
X
n
NaOOC
N
R = Me, Et, t-Bu
X = Et, OH, OEt Y = Me, OH, OEt
COOH
n = 1-3
[69, 70]
[42, 67, 68]
Me
Me
Me3Si OR
MeSi(OEt)3
Me CN
CN
Me
CN
CN
n
NC
R = H [73], Et, SiMe3
Me
R
n = 0-2
R = Me [71, 72], Et [72]
[74]
[72]
Рис. 1. Соединения, используемые в синтезе DMC-катализаторов как альтернатива TBA.
курсора. Вместо гексацианокобальтата(III) калия
TBA в качестве лиганда, который стал «атрибутом»
применяли комплексы K3[Co(CN)5X], где X = Cl,
высокоэффективных катализаторов. При этом, для
Br, I, NO2 или N3, но они демонстрировали лишь
достижения выдающейся активности в синтезе
умеренную или низкую активность [28]. В целом,
применяют солиганды, среди которых наиболее
несмотря на возможность менять природу неор-
популярны олигомерные простые полиэфиры - по-
ганических прекурсоров, существующие способы
лиэтиленгликоль (PEG) [15, 35], PPG [14, 36, 37],
получения DMC-катализаторов ограничены до-
PTMEG [25, 38, 39], P123 (Pluronic® P123, коммер-
ступностью реагентов.
ческий триблок-сополимер этиленоксида (EO) и
Лиганды. В качестве лигандов (L) в синтезе пер-
PO) [22, 23, 40-42] и сверхразветвленный полигли-
вых DMC-катализаторов были использованы глим
цидол (HBP) [38] (рис. 1). В качестве солигандов
(1,2-диметоксиэтан, диметиловый эфир этилен-
предложены также краун-эфиры [43-45], фталаты
гликоля), 1,2-диэтоксиэтан и 1,4-диоксан, т.е. про-
[46], фосфиноксиды [15], циклодекстрины [47, 48],
стые эфиры [13]. Однако позже была обнаружена
циклические карбонаты [49], алкилполигликозиды
высокая каталитическая активность материалов с
[50] и др. [51-54].
НЕФТЕХИМИЯ том 63 № 6 2023
814
ПЯТАКОВ, НИФАНТЬЕВ
В синтезе DMC-катализаторов также могут
к частичному удалению амина и дает активирован-
использоваться поверхностно-активные веще-
ные катализаторы, для которых индукционный пе-
ства (ПВА), которые представлены производными
риод отсутствует или крайне мал (<1 мин).
холевых кислот [55], полиакриламидом [56, 57],
Температура синтеза. Традиционно используе-
Tween® 80 и его аналогами [47, 58], и сложными
мые температуры синтеза (30-50°C) обеспечивают
эфирами глицерина [58]. ПВА оказывают двой-
необходимую растворимость исходных неоргани-
ственное влияние на свойства данных материалов.
ческих прекурсоров и побочного KCl (зачастую
Во-первых, они способны препятствовать агрега-
применяют достаточно концентрированные рас-
ции частиц в процессе синтеза, уменьшая их сред-
творы). По всей видимости, более высокие тем-
ний размер и влияя тем самым на удельную поверх-
пературы нежелательны с точки зрения гидролиза
ность и пористость [38]. Во-вторых, они входят в
исходного ZnCl2 и DMC-катализатора, а также уве-
состав катализаторов и выступают солигандами,
личения скорости образования твердой фазы (при
т.к. содержат группы COO--, COOR-, CONH2-, OH-
увеличении скорости роста кристаллов увеличива-
и др., за счет которых осуществляется координация
ется количество дефектов, связанных с окклюзией
по атомам цинка.
ионов калия).
Следует упомянуть, что изучаются и катализа-
Промывка катализатора. Промывка катали-
торы без TBA в составе. Среди соединений, при-
затора водными растворами TBA необходима для
менявшиеся в синтезе DMC-материалов как аль-
удаления примесного KCl, потому что ионы калия
тернатива TBA, например алкоксиспирты [59, 60],
снижают активность катализатора [13]. Причины
сложные эфиры алкоксиспиртов или гликолей
такого влияния до конца не ясны, но само появление
[61-63], алкиллактаты [40, 64], базовые органиче-
ионов калия в составе DMC-катализатора связыва-
ские растворители типа амидов [65, 66], α-, β-, γ- и
ют с окклюзией на стадии роста основной фазы и
δ-дикарбонильные соединения [42, 67, 68], дина-
и образованием KZn[Co(CN)6] в качестве побоч-
триевая соль этилендиаминтетрауксусной кислоты
ной фазы [76]. При этом содержащая в катализа-
[69, 70] и др. (рис. 1). Полученные с использовани-
торе влага также негативно влияет на активность,
ем таких лигандов материалы изучаются не только
поэтому обычно используют не только растворы с
в синтезе PPO, но и других реакциях ROP. Напри-
постоянной концентрацией, но и растворы с посте-
мер, материалы, полученные группой под руковод-
пенно увеличивающейся концентрацией, вплоть до
ства Il Kim с использованием 1,3-дикетонов или
чистого TBA. В то же время, авторы работы [77]
1,3-кетоэфиров и добавок P123, превосходят по
утверждают, что для получения высокоэффектив-
свойствам аналогичные материалы, полученные с
ных катализаторов не требуется тщательная про-
применением TBA [42] в полимеризации PO. Ката-
мывка катализаторов до полного исчезновения ио-
лизаторы, синтезированные с применением изобу-
нов K+: хорошая активность наблюдалась ими при
тиронитрила или N-метилпирролидона и добавок
содержании K+ до 1 мас. %. По мнению авторов,
P123, показали высокую активность в полимери-
это наблюдение поможет снизить затраты на про-
зации ε-капролактона (ε-CL) [65, 71, 72]. Этой же
изводство DMC-материалов.
группой впервые в качестве основных лигандов
Сушка катализатора. От условий сушки зави-
предложены такие кремнийорганические соеди-
сит конечный состав и свойства катализатора. В по-
нения, как триметилсиланол, ди(триметилсилило-
давляющем большинстве случаев сушку проводят
вый)эфир и алкоксисиланы [73, 74].
при 50 или 60°С в вакууме (~30 торр) до постоян-
Отдельно стоит упомянуть про модифицирова-
ной массы [1]. В сравнении с такой традиционной
ние DMС-катализаторов алифатическими аминами
сушкой, распылительная или лиофильная сушка
с длинным углеводородным радикалом, например,
позволяют получать катализатор со значительно
октадециламином [75]. При приготовлении таких
меньшим размером частиц, но лишь с незначитель-
но большей активностью [78].
катализаторов на стадии синтеза берется смесь эта-
нола и воды, поэтому в качестве лиганда выступает
Инициаторы полимеризации. Помимо вышерас-
не только амин, но и спирт. Последующее нагрева-
смотренных характеристик традиционного синтеза
ние этих материалов в вакууме при 130°С приводит
DMC-материалов, имеет смысл также остановить-
НЕФТЕХИМИЯ том 63 № 6 2023
ДВОЙНЫЕ МЕТАЛЛОЦИАНИДНЫЕ (DMC) КАТАЛИЗАТОРЫ
815
ся на инициаторах, используемых в DMC-катали-
вирующий эффект аминов наблюдается и в гидро-
зируемой (со)полимеризации PO. Применяющи-
аминировании алкинов, где они выступают реа-
еся инициаторы также характеризуют свойства
гентами: в случае ароматических аминов (менее
DMC-катализаторов и процесса (со)полимериза-
нуклеофильных) DMC-катализаторы демонстри-
ции в целом.
руют более высокую активность, по сравнению с
Известным недостатком DMC-катализаторов
алифатическими аминами (более нуклеофильны-
является невозможность использования низкомо-
ми) [22]. В то же время, некоторые алифатические
лекулярных «стартеров», в качестве которых обыч-
дикарбоновые кислоты [90, 91] и ароматические
но выступают гликоли, например пропиленгликоль
многоосновные кислоты успешно применяются-
и глицерин. Считается, что гликоли образуют проч-
лись в сополимеризации эпоксидов и CO2 [92-94],
ные хелаты с атомами цинка, препятствуя коорди-
причем сила кислот влияла на каталитическую
нации мономера и тем самым дезактивируя катали-
систему. Было обнаружено, что слабые кислоты
тические центры [79]. При возрастании расстояния
(pKa1 4.43-4.72) выступают инициаторами, а силь-
между OH-группами в диоле склонность к образо-
ные кислоты (pKa1 1.87-4.2) действуют как иници-
ванию хелатов сильно затрудняется из-за стериче-
аторы-передатчики цепи («chain initiation-transfer
ских препятствий, поэтому в качестве инициаторов
agents»), т.е. инициируют катионную ROP эпокси-
используют олигомерные PPO-полиолы, предвари-
да, а in situ образующийся PPO-полиол выступает
тельно полученные с помощью KOH-катализиру-
инициатором сополимеризации. Используя в каче-
емой конденсации PO и гликолей (полунепрерыв-
стве «стартеров» полидиметилсилоксаны (PDMS) с
ный процесс). Сравнительно недавно компанией
концевыми группами Si-OH [95], можно получать
Bayer MaterialScience был разработан DMC-ката-
блок-сополимеры PPO-PDMS-PPO.
лизатор, толерантный к небольшим количествам
низкомолекулярных «стартеров» [80]. Технология
Нетрадиционные методы синтеза
синтеза PPO с использованием такого катализатора
DMC-катализаторов
получила название CAOS (Continuous Addition оf
Синтез с помощью метода обратной эмульсии.
Starter). В CAOS-процессе в качестве инициатора
В работах [22, 23, 96] описан способ получения
используется смесь олигомерного PPO-полиола и
наноразмерного катализатора с помощью метода
небольшого количества гликоля; при этом гликоль
обратной эмульсии («вода в масле»), при котором
непрерывно добавляется в процессе синтеза. Такой
реакция протекает в каплях воды, диспергирован-
процесс позволяет получать PPO с лишь незначи-
тельно большим молекулярно-массовым распреде-
ных в неполярном растворителе (циклогексан). К
раствору TBA в циклогексане в присутствии эмуль-
лением (ММР) в сравнении с полунепрерывными
гатора, выступающего одновременно и солигандом
технологиями. Сохранение узкого ММР реализу-
ется благодаря эффекту «догоняющей кинетики»
[IGEPAL® CO-520, поли(оксиэтилен)5-(4-изоок-
(«catch-up kinetics»), способствующей преимуще-
тилфенил)эфир] прибавляли по каплям при интен-
ственной полимеризации с участием более корот-
сивном перемешивании водный раствор ZnCl2, а
ких полимерных цепей и нарушающей принцип
затем - водный раствор K3[Co(CN)6] (мольное со-
Флори [81, 82].
отношение ZnCl2 : K3[Co(CN)6] = 5 : 1). Синтезиро-
ванный таким образом катализатор показал боль-
Помимо олигомеров на основе пропиленгликоля
шую активность в реакции гидроаминирования
и глицерина, в качестве «стартеров» могут приме-
алкенов и алкинов в сравнении с образцами, по-
няться, например, параформ [83], фенолы [84, 85]
лученными классическим способом (солиганды -
и полиолы на основе касторового масла [86-88].
PTMEG, PEG или P123), а также отличался от них
Хорошо координирующиеся амины (например, ди-
по размеру частиц (см. ниже).
этаноламин и диэтилентриамин, способные хела-
тировать ионы Zn2+), мочевина и низкомолекуляр-
Механохимический синтез. Механохимический
ные карбоновые кислоты (муравьиная, уксусная и
синтез привлекает внимание исследователей в раз-
масляная) выступают ингибиторами и их нельзя
личных областях неорганической и органической
использовать в роли инициаторов [89]. Дезакти-
химии и имеет потенциал для применения в про-
НЕФТЕХИМИЯ том 63 № 6 2023
816
ПЯТАКОВ, НИФАНТЬЕВ
мышленности [97]. В отличие от традиционного
сульфоксид, ацетонитрил, метанол и хлороформ;
синтеза, этот подход является более экологически
при этом наилучшими свойствами характеризовал-
чистым («зеленым») и предполагает перемалы-
ся Zn-Co-катализатор, синтезированный с приме-
вание смеси реагентов в отсутствие растворителя
нением DFP. Следует отметить, что растворители
(«solvent-free») или в очень малом его количестве.
могут не только опосредованно влиять на состав и
Механохимический синтез DMC-катализаторов бо-
свойства материалов, но и выступать солигандами,
лее распространен, чем метод обратной эмульсии,
т.е. входить в состав материалов. В работе [98] из-
и представлен в целом ряде статей [21, 98-104]. На
учили влияние строения полиэфирного солиганда
примере Zn-Co-материалов такой синтез заклю-
(PEG, PPG или PTMEG) в цинк-железных матери-
чался в перемалывании в шаровой мельнице сме-
алах на каталитические свойства в реакциях ци-
си ZnCl2 и K3[Co(CN)6] с небольшим количеством
клоприсоединения и сополимеризации между PO и
TBA и, при наличии, солиганда и прочих добавок,
CO2. Наибольшую активность показал PTMEG-со-
после чего полученную смесь промывали смесью
держащий катализатор, но он существенно уступал
воды и TBA для удаления побочных продуктов и
в активности аналогичному катализатору, синтези-
непрореагировавших солей, а катализатор подвер-
рованному традиционным способом, однако, не-
гали сушке.
сколько превосходил его в селективности.
Получение Zn-Co-материалов способом, пред-
Катализаторы, не являющиеся Zn-Co- или
ставленным выше (в качестве лиганда был TBA),
Zn-Fe-материалами. Помимо традиционных
представлено всего в двух работах [101, 104], тогда
цинк-кобальтовых и цинк-железных материалов,
как цинк-железных материалов - бóльшим количе-
в полимеризации PO были изучены цинк-нике-
ством примеров [21, 98, 99, 101, 103], в том числе
левые материалы на основе Zn[Ni(CN)4], полу-
с использованием ионных жидкостей (ionic liquids,
ченные из Zn(OAc)2 и NiCl2 [111], и материалы
IL) или четвертичных солей аммония (quaternary
на основе Co[M(CN)4], где M = Ni, Pd и Pt [100,
ammonium salts, QAS) в качестве добавок на ста-
112-115], Fe(II) и Fe(III) [114], а также ряд цинк-
дии синтеза. IL способствуют увеличению актив-
содержащих материалов Znx[M(CN)4]y, где в каче-
ности DMC-катализаторов [105] и способны ме-
стве центрального атома в цианидном комплексе
нять селективность в реакции эпоксидов и CO2
выступали Cr(III) [28, 102], Ni(II) [28, 100, 116],
[41, 98, 99, 106-110]. Авторами исследования [99]
Mo(IV), Mn(III), Fe(II) и Cd(II) [28], а прекурсором
продемонстрирован синтез с применением бромида
был хлорид цинка. Во всех вышеописанных случа-
цетилтриметиламмония (cetyltrimethylammonium
ях единственным лигандом в составе материалов
bromide, CTAB) и показано, что CTAB входит в
был TBA, за исключением катализаторов на основе
состав полученных материалов, частицы которых
Zn[Ni(CN)4] [116], синтезированных с использова-
имели наноразмерный характер (25-79 нм). Zhang
нием и других лигандов (глим, 2-метоксиэтанол,
и др. получили цинк-железные материалы, исполь-
1-метоксипропанол-2 и пр.), и Co[Ni(CN)4] [115],
зуя в качестве прекурсоров ZnCl2 или Zn(OAc)2
синтезированного с применением TBA и PTMEG.
[21]. Материалы на основе Zn(OAc)2 были менее
активны в сополимеризации PO и CO2, но получен-
СОСТАВ, СТРОЕНИЕ И МЕХАНИЗМ
ные полимеры имели меньшие коэффициенты по-
ДЕЙСТВИЯ DMC-КАТАЛИЗАТОРОВ
лидисперсности (D). В работе [103] синтезированы
Состав. Формула на схеме 3 лишь упрощенно
цинк-железные материалы с добавками солей 1-бу-
отражает состав DMC-катализаторов. По данным
тил-3-метилимидазолия в качестве IL ([BMIM]X,
X = PF6, BF4, Br, Cl), среди которых наиболее ак-
рентгенофазового анализа, фазы свободных ZnCl2
и Zn3[Co(CN)6]2 в них отсутствуют [117]. В иссле-
тивными были материалы на основе [BMIM]PF6.
довательских работах состав этих материалов за-
Zhang и др. [101] исследовали влияние природы
растворителя в механохимическом синтезе Zn-Co
частую выражается в более сложными формулами,
которые точнее передают состав, например:
и цинк-железных материалов с TBA в качестве
единственного лиганда. Среди растворителей были
Zn2.67[Co(CN)6]1.0·0.24ME·0.30H2O·1.49Cl-
1,1,1,2,3,4,4,5,5,5-декафторпентан (DFP), диметил-
(ME = 2-метоксиэтанол) [59];
НЕФТЕХИМИЯ том 63 № 6 2023
ДВОЙНЫЕ МЕТАЛЛОЦИАНИДНЫЕ (DMC) КАТАЛИЗАТОРЫ
817
N
N
R
C
C
O
N
N
N
N
H
Cl
C
C
C
C
Zn
Co
Zn
Co
Zn
C
C
C
C
t-Bu
t-BuO
N
N
N
N
O
C
C
H
N
N
Активный центр
Неактивный центр
Активный центр
Рис. 2. Схематичное строение DMC-катализаторов с TBA и ROH в качестве лиганда и солиганда соответственно.
Zn1.94Co(CN)5.71 · 0.62HD · 0.03P123 · 0.26H2O ·
анионов [Co(CN)6]3-, являющихся координацион-
· 0.41Cl- (HD = 2,5-гександион, P123 - триблок-со-
ными вакансиями. Такие вакансии образуют сеть
полимер EO20PO70EO20) [42].
«скрытых» микропор, характер которой сильно за-
висит от условий синтеза [119].
Такой нестехиометрический состав, очевид-
но, является следствием комплексного характера
Известно, что чистая фаза Zn3[Co(CN)6]2 мало-
химических процессов, протекающих при приго-
активна в катализе, поэтому предполагают, что ка-
товлении DMC-катализаторов, являющихся ги-
тионы цинка из ZnCl2 координированы по атомам
бридными материалами. Кроме обменной реакции
азота CN-групп на периферии, неся также лиган-
между ZnCl2 и K3[Co(CN)6], могут протекать по-
ды в виде ионов хлора (или OH-), молекул TBA
бочные реакции гидролиза и сольволиза фрагмен-
или воды [39]. Такие периферийные атомы цинка
тов ZnCl, в результате чего в составе образующейся
рассматриваются как активные центры (рис. 2).
фазы появляются фрагменты Zn-OR (R = H от H2O,
Эти выводы были сделаны на основе результатов
трет-Bu от TBA, алкил от солиганда). Протекание
работ [20, 120], в которых изучалось влияние спо-
гидролиза и сольволиза косвенно подтверждается
соба получения DMC-катализаторов на их катали-
отсутствием зарядового баланса в приведенных
тическую активность. Например, импрегнирова-
выше брутто-формулах. Как минимум часть H2O
ние ZnCl2 (в присутствии или отсутствие TBA) в
является скрытым анионом OH-: наличие фраг-
предварительно полученный Zn3[Co(CN)6]2 не по-
ментов Zn-OH в составе материалов подтвержда-
зволяет получить DMC-катализатор. Материалы,
ют данные ИК-спектроскопии [42]. Помимо этого,
полученные из K3[Co(CN)6] по обменной реакции
причиной отсутствия зарядового баланса может
с избытком ZnCl2, но в отсутствие TBA также де-
быть неверная интерпретация результатов TGA
монстрируют низкую каталитическую активность.
(см. ниже).
Таким образом, «свободный» ZnCl2 и TBA оказы-
Строение. DMC-катализаторы характеризуются
вают синергетический эффект на каталитическую
высокой аморфностью, что затрудняет их фазовый
активность. Этот эффект может быть связан с из-
анализ, основанный на порошковой рентгеновской
менением морфологии: органический лиганд за-
дифракции. При этом ряд авторов полагает, что в
трудняет образование кристаллической (упорядо-
основе материалов лежит кристаллическая струк-
ченной) фазы [121] и способствует образованию
тура Zn3[Co(CN)6]2. Для Zn3[Co(CN)6]2 · 12H2O
аморфной фазы, которая характеризуется меньшим
характерна кубическая кристаллическая решетка
размером частиц и большей удельной поверхно-
с октаэдрическим окружением ионов цинка, а для
стью (в том числе за счет пористости). Подобным
безводного Zn3[Co(CN)6]2 - ромбоэдрическая кри-
образом влияет и «свободный» ZnCl2: при увели-
сталлическая решетка с тетраэдрическим лиганд-
чении его количества растет содержание аморф-
ным окружением [118]. В этих кристаллических
ной фазы [20, 120]. По всей видимости, развитая
упаковках соотношение катионов и анионов равно
поверхность DMC-катализаторов обеспечивает
1 : 1, вследствие чего отсутствует одна третья часть
доступность большего количества каталитических
НЕФТЕХИМИЯ том 63 № 6 2023
818
ПЯТАКОВ, НИФАНТЬЕВ
центров, в сравнении с Zn3[Co(CN)6]2. В то же са-
до ~3.7 Å. Для сравнения, экспериментально най-
мое время, электронное состояние атомов цинка в
денные контакты Zn-Zn в Zn3[Co(CN)6]2·12H2O
DMC-катализаторах должно отличаться от таково-
значительно больше - 7.3 Å [118]. Длина контактов
го в Zn3[Co(CN)6]2. Польскими учеными [117, 122,
Zn-Zn может играть важную роль, если в активный
123] были получены данные спектроскопии EXAFS
центр входят два атома цинка (см. ниже).
(extended X-ray absorption fine structure, исследова-
Интересным является также вопрос о термиче-
ние дальней тонкой структуры рентгеновских спек-
ских превращения DMC-катализаторов. Несмотря
тров поглощения), согласно которым часть атомов
на почти полувековую историю успешного приме-
цинка должна иметь координационное окружение
нения этих материалов в промышленности и много-
как в ромбоэдрической форме Zn3[Co(CN)6]2 (ли-
численные исследовательские работы, лишь в 2016 г.
гандное окружение из четырех атомов азота), а
была опубликована статья [130], авторы которой
часть - другое лигандное окружение (включающее
попытались ответить на вопрос, что же происходит
в части случаев хлор, но ZnCl2 при этом отсутству-
с DMC-катализаторами при нагревании. Для этого
ет). Эти данные подтверждают изображенное на
на примере нескольких TBA- или глим-содержа-
рис. 2 схематичное строение DMC-материалов. Ха-
щих образцов цинк-кобальтовых катализаторов
рактеризация с помощью твердотельной спектро-
был проведен анализ выделяемых газов (evolved
скопии ЯМР 13С [19, 69, 70, 124, 125] и раманов-
gas analysis, EGA) с применением масс-спектромет-
ской спектроскопии [16, 126, 127] ограничивается
рии (EGA-MS) и ИК- спектроскопии (EGA-FTIR).
единичными случаями не дает дополнительной ин-
Примечательно, что потеря массы для TBA-содер-
формации о строении этих материалов.
жащих образцов наблюдалась в широком интерва-
Существует и другой взгляд на строение DMC-ка-
ле температур 110-400°С, что существенно выше
тализаторов. Неорганическую «основу» этих ма-
температуры кипения TBA (82°С). Неожиданно
териалов может составлять смешанный гекса-
оказалось, что потеря массы обусловлена не испа-
цианокобальтат(III)-хлорид цинка Zn2[Co(CN)6]Cl -
рением лиганда, которое фиксировалось в очень
его образованию способствует большой избыток
малых количествах, а его разложением на изобути-
ZnCl2 в синтезе, когда замещению подвергается
лен и воду:
один атом хлора. Косвенно это подтверждается
(CH3)3C-OH → (CH3)2C=CH2 + H2O.
данными статьи [120], согласно которым, увели-
чение формального количества ZnCl2 по отноше-
Для чистого TBA в некаталитических условиях
нию к Zn3[Co(CN)6]2 приводит к резкому росту
подобная дегидратация протекает при температу-
каталитической активности до определенного пре-
рах свыше 400°С [131], поэтому представляется,
дела - 1 : 1 по молям (1Zn3[Co(CN)6]2 + 1ZnCl2 ≡
что столь низкие температуры в случае DMC-ма-
≡ 2Zn2[Co(CN)6]Cl), а при дальнейшем увеличении
териалов обусловлены присутствием атомов цинка,
количества ZnCl2 активность растет незначитель-
способных выступать кислотами Льюиса и катали-
но. Кроме этого, в статьях [128, 129] проведено мо-
зировать процесс. В то же время, термическое раз-
делирование кристаллической структуры DMC-ка-
ложение глим-содержащих материалов не сопро-
тализаторов на основании фазы Zn2[Co(CN)6]Cl.
вождалось деструкцией лиганда. Помимо этого,
Авторы работы [129] также выполнили модели-
по данным дифференциальной сканирующей ка-
рование фаз Zn2[Co(CN)6]L, где L = Cl, OH, EtO,
лориметрии для TBA-содержащих материалов на-
трет-BuO, и установили, что в случае L = трет-
блюдается фазовый переход в интервале 90-180°С
BuO поверхностная энергия граней (001) и (100)
[130, 132]. Заметное разложение TBA и изменение
должна быть минимальна. Эти данные говорят о
химической природы DMC-материалов наблюда-
том, что при использовании TBA (трет-BuOH) в
ется в температурном интервале 80-150°С, тогда
синтезе должны получаться частицы с развитой по-
как полимеризация PO обычно проводится при
верхностью и пористостью. Примечательно также,
130-180°С. Зачастую также практикуется предак-
что по данным расчетов для L = Cl самые корот-
тивация катализатора, заключающаяся в нагре-
кие контакты Zn-Zn составляют 4.4 Å, тогда как в
вании его вместе со «стартером» при 80-150°С в
случае L = OH, EtO, трет-BuO они сокращаются
вакууме (<200 торр) перед добавлением мономера
НЕФТЕХИМИЯ том 63 № 6 2023
ДВОЙНЫЕ МЕТАЛЛОЦИАНИДНЫЕ (DMC) КАТАЛИЗАТОРЫ
819
[133]. Следует отметить, что вследствие вышеу-
PO и CO2, был установлен механизм, в котором ак-
казанной в данном разделе реакции DMC-матери-
тивным центром служат два близкорасположенных
алы могут содержать фрагменты Zn-OH, наличие
атома цинка, один из которых активирует эпоксид,
которых роднит их с цинк-содержащим фермен-
а другой является источником нуклеофильного ал-
том карбоангидраза [134]. В карбоангидразе атом
коголята [139]. Ключевым моментом для этих ката-
цинка связан с тремя атомами азота имидазольных
лизаторов представляется молекулярная структура:
циклов (в остатках гистидина) и молекулой воды.
на основе расчетных данных было предсказано, что
Под действием активных участков пептидной
«идеальная» длина контактов Zn-Zn для карбокси-
цепи происходит депротонирование L3Zn-OH+ до
латов должна составлять 4.3-5.0 Å, что объясняет
L3Zn-OH и взаимодействие с CO2 (гидратация до
низкую активность сукцината цинка в сравнении с
HCO–). Сходство карбоангидразы и DMC-катализа-
выcшими гомологами (ZnGA и др.) [140]. Расчет-
торов проявляется и в O/S-обменных реакциях, т.к.
ная длина контактов Zn-Zn для Zn2[Co(CN)6]Cl
она превращает CS2 в COS, а COS - в CO2 [135]. При
(4.4 Å, см. выше) соответствует этому требованию,
этом чистый гидроксид-гексацианокобальтат(III)
что позволяет предположить, что кооперативное
цинка Zn2[Co(CN)6]OH обладает низкой активно-
действие двух атомов цинка реализуется и в DMC
стью в сравнении с DMC-материалами, содержа-
катализаторах [141]. Неясным остается вопрос с
щими в качестве лиганда 1,2-диметоксиэтан [136].
лигандным окружением атома(ов) цинка и как оно
Таким образом, структурные превращения
сочетается с различным качественным и количе-
DMC-катализаторов возможны как в процессе,
ственным составом материалов. При этом в пользу
так и до полимеризации, что оставляет пробелы
одной природы активных центров DMC-катали-
в нашем понимании природы этих материалов и
заторов говорят низкие величины коэффициентов
заставляет с осторожностью относиться к обще-
полидисперности Đ получаемого PPO (менее 1.1).
принятому механизму ROP. Данные о химических
С целью прояснения механизма полимеризации
превращениях при термической предактивации
группой под руководством D. Darensbourg были по-
TBA-содержащих катализаторов и тщательное ис-
лучены растворимые аналоги DMC-материалов -
следование состава активированных катализаторов
биметаллические комплексы цинка и железа(II)/
могут послужить ключом к разгадке механизма их
кобальта(III) [142-144], в которых лигандами при
действия. Также, насколько нам известно, подоб-
тетраэдрических катионах Zn2+ выступали циа-
ное исследование состава продуктов термическо-
но-группы, ион I- и тетрагидрофуран. In situ-мо-
го разложения для DMC-катализаторов с другими
ниторинг реакции полимеризации α-пиненоксида
лигандами не проводили, что поднимает вопрос об
с помощью ИК-спектроскопии позволил доказать,
адекватности интерпретации результатов TGA в
что координация между атомами цинка и CN-груп-
контексте установления состава материалов.
пами не нарушается: никакого изменения положе-
Строение каталитического центра и механизм
ния и интенсивности сигнала этих групп не про-
действия. Каталитическое действие рассматривае-
исходит, а также не появляется дополнительных
мых материалов обеспечивается льюисовской кис-
подобных сигналов [143]. Координация CN-групп
лотностью атомов цинка. Считается, что механизм
с кобальтом также не нарушается, о чем свиде-
полимеризации пропиленоксида на DMC-катали-
тельствует EXAFS-анализ лигандного окружения
заторах является катионно-координационным, о
атомов кобальта [122]. Соответственно, цианоко-
чем свидетельствует региоселективность полиме-
бальтат-анионы не лабильны и механизм катализа
ризации по типу «голова к хвосту»; при этом по-
неразрывно связан с лабильностью Zn-O и Zn-Cl
лимеризация не является стереоспецифической и
связей. Однако, лиганды [Co(CN)6]3- неизбежно
приводит к атактическим полимерам [89, 137, 138].
«настраивают» льюисовскую кислотность Zn2+,
внося свой вклад в активность DMC-катализаторов.
Принято считать, что в данных материалах ак-
тивными центрами являются отдельные атомы цин-
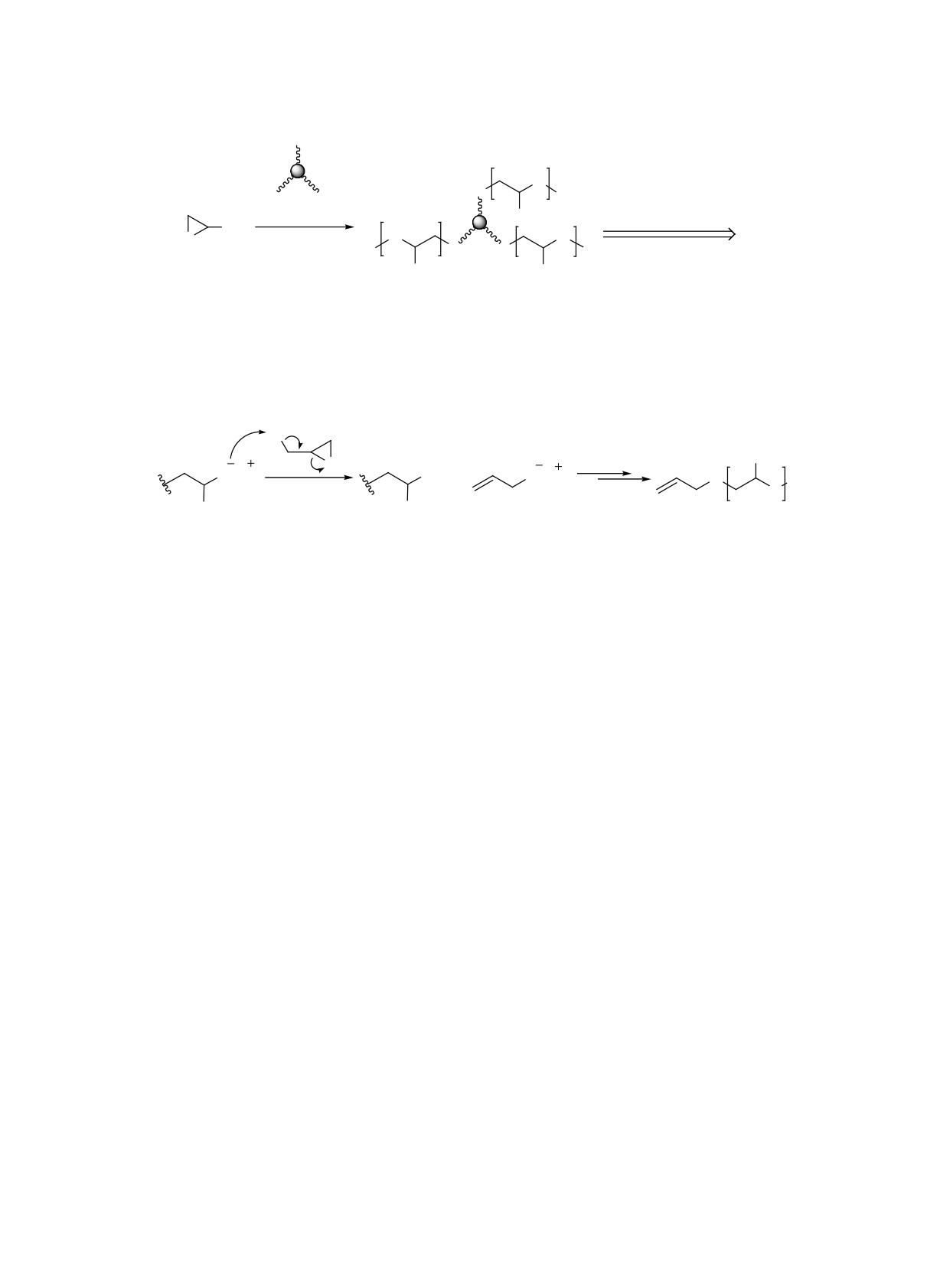
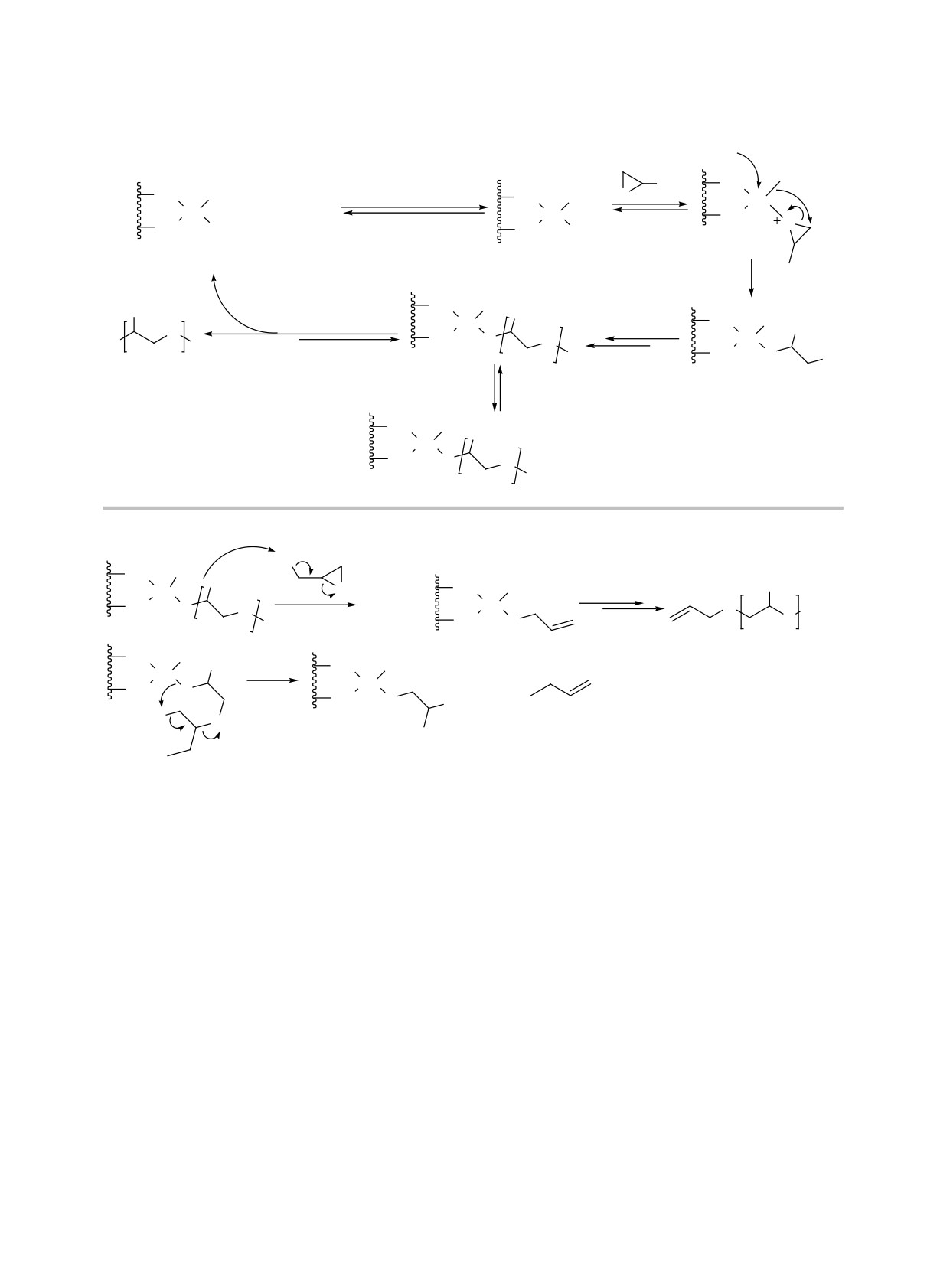
Принципиальный механизм полимеризации PO
ка (см., например, [30, 39, 120]), хотя, к примеру,
с участием отдельного атома цинка изображен на
для глутарата цинка ZnGA (и других карбоксила-
схеме 4a. На стадии инициирования (реакции (1)-
тов), гетерогенного катализатора сополимеризации
(3)) происходит превращение неактивных центров
НЕФТЕХИМИЯ том 63 № 6 2023
820
ПЯТАКОВ, НИФАНТЬЕВ
Cl
(a)
OR
Me
CN
CN
Cl (or R′OH, H2O) инициатор (ROH)
CN
OR O
Zn
Zn
Zn
-Cl-
CN O
CN Cl
- HCl (или R′OH, H2O)
CN Cl
R′OH = лиганд
(1)
(2)
«Cпящий» центр
Активный центр
Me
(3)
Me
CN
Cl Me
HCl (или R′OH, H2O)
Zn
(n - 1) PO
CN
Cl
Me
O
CN O
Zn
HO
R
O
n
R
CN
O
OR
(5)
(4)
n
PnOH
PmOH
(6)
CN
Cl Me
Zn
+ PnOH
CN O
O
R
m
(б)
H
CN
Cl Me
Me
Zn
O
CN Cl
n PO
CN
O
+
Zn
O
H
O
PnOH
CN O
O
R
(7)
n
n
CN
Cl
Me
CN
Cl
Zn
Zn
CN
O
(8)
CN O
+ R′′Ο
OH
H
O
Me
Pn-1OAll
R′′Ο
Схема 4. Механизмы DMC-катализируемой полимеризации: (а) - принципиальный механизм DMC-катализируемой
полимеризации PO; (б) - возможные побочные реакции, приводящие к появлению ненасыщенных групп в PPO.
CN-Zn-Cl в активные под действием инициатора
лизатора и полимер с концевой OH-группой PnOH
ROH и мономера. Сначала ROH замещает Cl- в
(реакция (5)). Однако эти полимерные цепи не яв-
неактивных центрах (реакция (1)), затем происхо-
ляются «мертвыми» и участвуют в передаче цепи
дит координация PO по атому цинка и его актива-
при взаимодействии с растущими полимерными
ция (реакция (2)) с последующей нуклеофильной
цепями (реакция (6)). Авторы работы [120] выска-
атакой соседней группы OR с раскрытием цикла
зали предположение, что инициирование включа-
(реакция (3)). Стадия (4) представляет собой рост
ет перенос H+ с лиганда ROH на мономер, однако
цепи: PO замещает Cl- (или R′OH, H2O и т.д.) и вне-
это представляется маловероятным, поскольку при
дряется в полимерную цепь, т.е. повторяются реак-
этом должна нарушаться координация с атомом
ции (2) и (3). Обрыв цепи возможен, когда расту-
цинка и региоселективность полимеризации (как
щая полимерная цепь взаимодействует с Cl- (или
при катализе протонными кислотами или кисло-
R′OH, H2O и т.д.), давая неактивный центр ката-
тами Льюиса [145, 146]). Более разумным являет-
НЕФТЕХИМИЯ том 63 № 6 2023
ДВОЙНЫЕ МЕТАЛЛОЦИАНИДНЫЕ (DMC) КАТАЛИЗАТОРЫ
821
ся высказанное в статье [141] предположение, что
мера на этой стадии подтверждается эксперимен-
акцептором протона выступает Cl-. Замена Cl- на
тальными данными [42]. Вследствие индукционно-
более основный противоанион NO– в составе ката-
го периода стадию инициирования еще называют
лизатора приводит к ускорению ROP, что косвенно
активацией DMC-катализатора.
подтверждает эту гипотезу.
Сотрудниками Dow Chemical Company предло-
Появление аллильных групп в PPO может про-
жена кинетическая модель с несколькими актив-
исходить двумя путями (схема 4б). Первый (реак-
ными центрами, основанная на том, что константы
ция (7)) предполагает перегруппировку PO в ал-
скорости стадий полимеризации зависят от длины
лиловый спирт аналогично KOH-катализируемой
полимерной цепи [148]. Согласно этой модели, в
анионной полимеризации (схема 2), а второй за-
процессе полимеризации могут существовать не-
ключается в депротонировании CH3-группы пред-
сколько типов каталитических центров, которые
концевого звена с образованием макромолекулы
необратимо переходят друг в друга. На примере
Pn-1OCHCH=CH2 (реакция (8)). Представляется,
двух типов таких центров проведено моделирова-
что вклад реакции 8 должен быть существенно
ние, в соответствии с которым полимерные цепи
меньше из-за стерических препятствий со стороны
от активных центров типа 1 составляют более
матрицы материала (вращение полимерных цепей
низкомолекулярную фракцию и 70 мас. % всех ма-
в порах катализатора заторможено) и энергетиче-
кромолекул, а от активных центров типа 2 - более
ского фактора (связь С-O в эпоксидах менее проч-
высокомолекулярную фракцию и 30 мас. % всех
ная, чем в простых эфирах). На порядок более низ-
макромолекул. Эти фракции имеют узкое ММР,
кое содержание непредельных групп в полимере
но различные коэффициенты полидисперности Đ,
в случае DMC-катализаторов, по-видимому, объ-
и их смесь также дает узкое ММР, которое хоро-
ясняется меньшей основностью алкоголята цинка
шо согласуется с экспериментальными данными.
по сравнению с алкоголятом калия из-за меньшей
Впрочем, несмотря на интересный результат, эта
полярности связи Zn-O.
работа никак не проясняет природу возможных ак-
Полимеризация PO на DMC-катализаторах яв-
тивных центров.
ляется примером «бессмертной» полимеризации
При увеличении концентрации инициатора
[147]. Количество инициатора намного превышает
скорость полимеризации снижается [79, 89], т.е.
количество активных центров катализатора, поэто-
инициатор оказывает депрессионный эффект. Ве-
му в «бессмертной» полимеризации, в отличие от
роятно, это связано с тем, что он влияет на равнове-
«живой», количество растущих полимерных це-
сие (2), соперничая с мономером в координации по
пей намного меньше, чем количество инициатора.
атому цинка и затрудняя ее. Учитывая такое вли-
Иными словами, имеет место постоянная переда-
яние инициатора и возможность полимеризации в
ча цепи между «мертвыми» полимерными цепями
его отсутствие, Wu и др. [79] считают, что спирт
PmOH и растущими макромолекулами (схема 4,
ROH правильно рассматривать не как инициа-
реакция (6)), тогда как в «живой» полимериза-
тор или «стартер», а как регулятор молекулярной
ции все макромолекулы являются растущими
массы (агент передачи цепи). Эти авторы также
и их количество равно количеству инициатора.
детально изучили кинетику полимеризации PO и
Величины коэффициента полидисперсности Đ,
установили, что ее скорость подчиняется формуле
близкие к 1, также говорят о том, что передача
цепи происходит значительно быстрее, чем рост
RP = KM2C/(1 + kTr),
(2)
цепи. При этом, молекулярная масса полиме-
где K и k - константы скорости полимеризации и
ра находится в хорошем согласии с отношением
передачи цепи; M, С и Tr - концентрации мономе-
[PO]/[ROH] (но не [PO]/[катализатор], как в «жи-
ра, катализатора и регулятора, соответственно.
вой» полимеризации) [20, 89]. Также полимериза-
ция PO характеризуется индукционным периодом,
Вода, содержащаяся в мономере и «стартере»
что, по-видимому, связано с установлением равно-
как примесь, также выступает регулятором, если
весия в реакция (1) и (2). Замещение органических
ее количество невелико. Увеличение концентрации
лигандов координирующимися молекулами моно-
воды приводит к увеличению индукционного пери-
НЕФТЕХИМИЯ том 63 № 6 2023
822
ПЯТАКОВ, НИФАНТЬЕВ
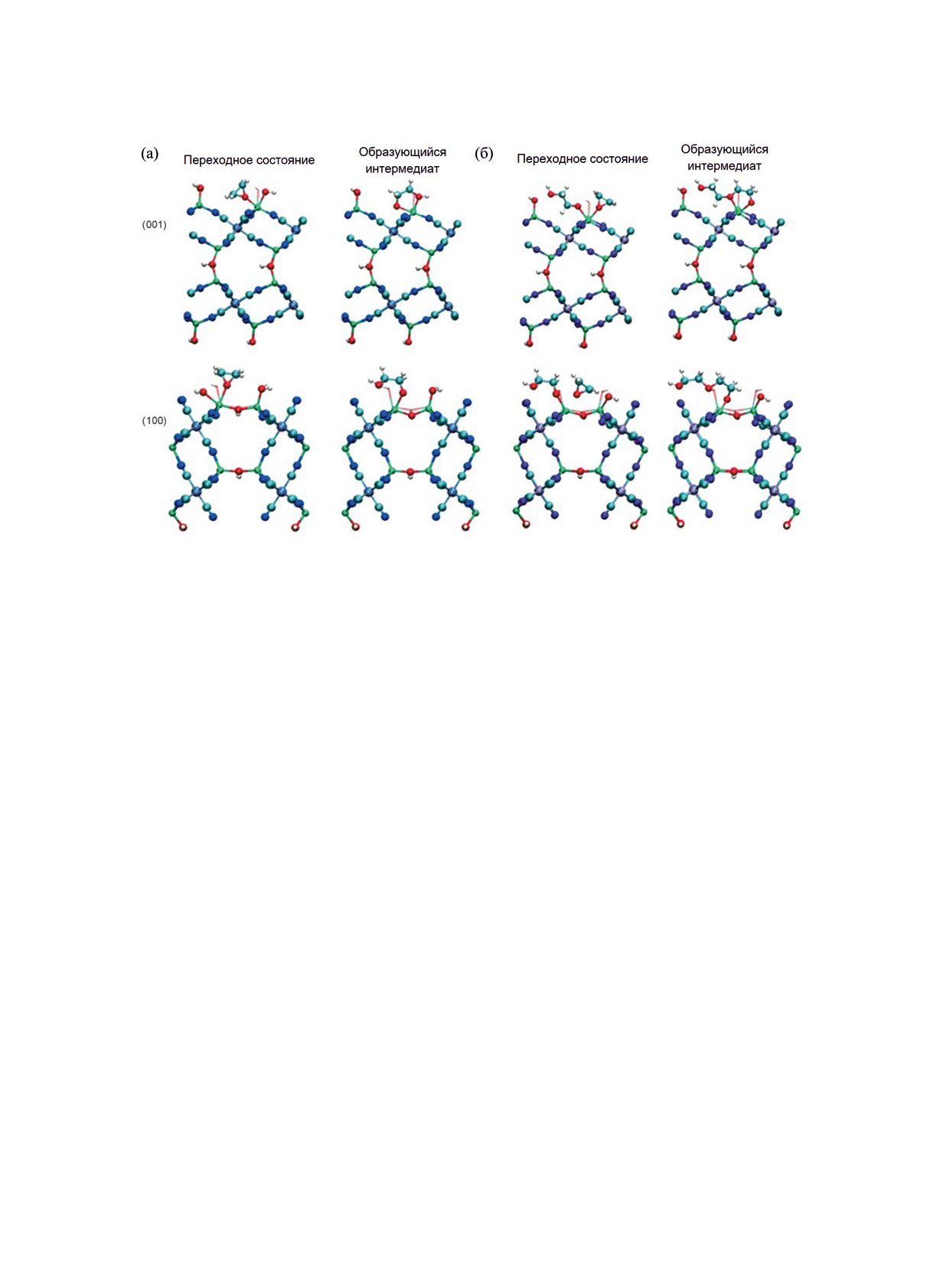
Рис. 3. Строение переходного состояния и образующегося интермедиата для стадий инициирования (а) и роста цепи (б)
модельной реакции полимеризации EO на фазе Zn2[Co(CN)6]OH. Цветовое обозначение атомов: Co - большие серо-синие,
Zn - зеленые, Cl - желтые, C - бирюзовые, N - синие, O - красные, H - белые.
ода, а слишком большое ее количество полностью
(001). Такое различие в активности может быть
дезактивирует катализатор (например, для приме-
следствием различного лигандного окружения,
нявшегося в статье [79] катализатора ~3500 ppm и
влияющего на положительный заряд атомов цинка:
более). Вследствие этого, все используемые в поли-
на гранях (100) они связаны с тремя атомами кис-
меризации реагенты должны быть тщательно осу-
лорода, тогда как на гранях (001) - лишь с двумя.
шены. Однако Wei и др. показали [41], что добавка
Авторы работы
[56] исследовали кинетику
небольших количеств QAS, например CTAB, при-
полимеризации, а также влияние концентрации
водит к снижению чувствительности катализатора
катализатора на ГЧ, степень ненасыщенности и
к количеству влаги до сотен ppm при сохранении
полидисперсность PPO. Было показано, что ГЧ и
высокой активности.
степень ненасыщенности практически не зависят
К сожалению, механизм полимеризации на
от концентрации катализатора, в то время как ко-
DMC-материалах страдает от недостатка модели-
эффициент полидисперсности уменьшается при
рования, что характерно для многих гетерогенных
возрастании концентрации. Такое изменение ММР
катализаторов [149]. В статье [129] предпринята
может быть объяснено на основании кинетиче-
попытка смоделировать стадии инициирования и
ской модели [150]. При более низкой концентра-
роста цепи (присоединение одной молекулы мо-
ции (меньшем количестве активных центров) ниже
номера) для EO (модельный мономер) на неорга-
вероятность эффективного столкновения молекул
нической фазе Zn2[Co(CN)6]OH (рис. 3). Расчеты
на ранних стадиях полимеризации, т.е. соответ-
предсказывают, что полимеризация с участием ато-
ствующие ki (константы скорости роста цепи на
мов цинка граней (100) должна быть более выгод-
i-ой ступени присоединения) меньше, чем при бо-
на: энергии активации (Ea) стадий инициирования
лее высокой концентрации катализатора. Далее ki
и роста цепи меньше на 60 и 50 кДж/моль, соот-
склонны увеличиваться с ростом конверсии моно-
ветственно, нежели в случае атомов цинка граней
мера, т.е. ki+1/ki > 1 при более низкой концентрации
НЕФТЕХИМИЯ том 63 № 6 2023
ДВОЙНЫЕ МЕТАЛЛОЦИАНИДНЫЕ (DMC) КАТАЛИЗАТОРЫ
823
CN Cl (или ROH, H2O)
Me
CN
Cl
CN Cl
Me
O
X
n PO
Zn
Zn
Zn
X
PPO
CN Cl
CN
O
CN
O
-Cl-
ROH = лиганд
X = анион IL или QAS
Me
Схема 5. Предполагаемая роль IL и QAS в механизме DMC-катализируемой полимеризации PO в присутствии дан-
ных добавок [105].
катализатора, что и приводит к уширению ММР.
[129]. Кроме этого, ключевую роль может играть де-
Помимо этого, важную роль в достижении низкого
градация катализатора. Almora-Barrios и колл. [129]
коэффициента полидисперсности играет интенсив-
выполнили моделирование альтернативной стадии
ное перемешивание, которое определяет скорость
инициирования с участием Zn-OH из линкерного
диффузии макромолекул. Недостаточно интенсив-
фрагмента Zn-O(H)-Zn на поверхности (100) ката-
ное перемешивание приводит к уширению ММР и
лизатора (рис. 4). Подобное инициирование должно
даже к бимодальному распределению [151].
сопровождаться разрушением матрицы материала.
Закономерно, Ea такого процесса несколько выше,
Kim и др. [105] показали, что добавки IL поло-
чем для инициирования с участием нелинкерного
жительно влияют на полимеризацию PO, приводя
Zn-OH (рис. 3а), но он может иметь место благо-
к существенному сокращению индукционного пе-
даря высокой температуре (~130°С) и давлению
риода и увеличению скорости ROP, а также умень-
(~4 бар) в условиях синтеза [129].
шению количества аллильных групп в PPO. Анало-
гичным образом влияют и добавки QAS [152, 153].
Деградация DMC материалов имеет экспери-
ментальное подтверждение. С помощью мето-
Полагают, что IL и QAS могут влиять на стадию
инициирования, способствуя раскрытию коорди-
да динамического светорассеяния (dynamic light
scattering, DLS) показано, что активация катализа-
нированного эпоксида за счет нуклеофильной ата-
тора сопровождается существенным уменьшением
ки аниона (схема 5). Авторы работы [105] также
среднего размера частиц катализатора и увеличени-
считают, что IL могут стабилизировать активные
ем их неоднородности по размерам, т.е. фрагмента-
центры и препятствовать их гибели, хотя их рас-
суждения выглядят весьма умозрительными.
Механизм появления
«высокомолекулярных
хвостов» и деградация катализатора. Несмо-
тря на низкую полидисперсность, получаемые на
DMC-катализаторах полимеры содержат «высоко-
молекулярные хвосты», фракция которых может
составлять до 2-3% [154]. Эта полимерная фрак-
ция проявляет нежелательные гидрофобные свой-
ства, препятствуя образованию стабильных пен в
синтезе PU из PPO-полиолов и изоцианатов [155].
Полагают [154], что образование этой фракции
связано с наличием фрагментов Zn-OH в струк-
туре материалов. Если рост цепи инициируется
Zn-OH, то макромолекулы будут иметь две кон-
Рис. 4. Строение переходного состояния и образую-
цевые OH-группы. Участвуя в переносе цепи
щегося интермедиата для альтернативного варианта
(схема 4, реакция (6)), такие макромолекулы мо-
инициирования модельной реакции полимеризации EO
гут получить два растущих конца, что закономерно
на поверхности (100) фазы Zn2[Co(CN)6]OH. Цветовое
обозначение атомов такое, как на рис. 3.
может кратно увеличить их молекулярные массы
НЕФТЕХИМИЯ том 63 № 6 2023
824
ПЯТАКОВ, НИФАНТЬЕВ
цией [42]. Фрагментация приводит к разрушению
затрудняет определение влияния отдельных факто-
матрицы материала (деградации) и «высвобожде-
ров на каталитическую активность.
нию» атомов цинка из объема на поверхность, пре-
Элементный состав поверхности. Элементный
вращая их в активные центры. В процессе поли-
анализ поверхности (слой толщиной ~10-100 Å)
меризации растущие полимерные цепи вызывают
позволяет осуществлять рентгеновская фотоэ-
дальнейшую фрагментацию, и частицы катализа-
лектронная спектроскопия (X-ray photoelectron
тора образуют мелкую дисперсию в реакционной
spectroscopy, XPS), которая используются наравне
массе, что визуально выглядит как растворение.
с элементным анализом в объеме материала («in
На примере сополимеризации PO и CO2 продемон-
bulk»): атомно-эмиссионной (AES), атомно-абсор-
стрировано, что ультразвуковая обработка реакци-
бционной (AAS), рентгенофлуоресцентной (XRF)
онной смеси способствует увеличению активности
или энергодисперсионной рентгеновской спек-
катализатора, как предполагается, за счет фрагмен-
троскопией (Energy-dispersive X-ray spectroscopy,
тации частиц катализатора и их диспергирования
EDX). Кроме этого, с помощью EDX-мэппинга
[156]. «Высвобождение» каталитических центров
можно получить информацию о возможных одно-
из объема на поверхность материалов в результате
родном или неоднородном распределении элемен-
фрагментации является одним из факторов, обу-
тов по образцу [161].
славливающих высокую активность DMC-катали-
Например, работа
[24] позволяет сравнить
заторов. Вероятно, Zn-Co- и Zn-Fe-катализаторы
DMС-материалы, полученные на основе различных
должны иметь различную склонность к фрагмента-
галогенидов цинка и солигандов при фиксирован-
ции вследствие разной энергии связей Zn-O (менее
ном соотношении Zn : Co = 10 на стадии синтеза.
прочная) и Fe-O (более прочная). В то же время со-
По данным XPS соотношение Zn : Co на поверх-
общалось, что в ROP ε-CL деградация Zn-Co-ката-
ности синтезированных образцов варьировалось в
лизатора при загрузке ~10 ppm происходила только
пределах 1.9-56.2, в то время как по данным AES
после пяти циклов регенерации, до этого заметной
соотношение Zn : Co оказалось в пределах 1.58-
дезактивации катализатора не наблюдалось [71].
1.64. В работе [117] поверхность материалов была,
Обработка катализатора протонными кислота-
наоборот, обеднена цинком в сравнении с объемом,
ми, например, уксусной, может снизить количество
т.к. соотношение Zn : Co составило 2.40 по данным
«высокомолекулярных хвостов» за счет превраще-
EDX-анализа, а по данным спектров XPS - 1.90. В
ния фрагментов Zn-OH в Zn-OAc [154]. Положи-
то же время, EDX-анализ сам по себе порой дает
тельный эффект в борьбе с образованием этой по-
нерелевантные данные вследствие известных огра-
лимерной фракции имеет введение в ее состав EO,
ничений метода [162]. К примеру, для полученных
т.е. уменьшение количества PO в ней [157]. Пред-
в статье [163] катализаторов соотношение Zn : Co =
1.34, что меньше теоретического значения 1.5 для
ложены и другие решения [158, 159], в том числе
Zn3[Co(CN)6]2 и противоречит здравому смыслу.
снижающие содержание
«высокомолекулярных
Столь различные данные элементных анализов на
хвостов» до менее чем 60 ppm [160].
поверхности и в объеме материалов лишний раз
подчеркивают важность всестороннего анализа
ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА
DMC-катализаторов, как гибридных материалов, с
DMC-КАТАЛИЗАТОРОВ
целью выявления закономерностей между их при-
DMC-материалы являются гетерогенными ка-
родой и каталитической активностью.
тализаторами, поэтому помимо состава и строения
В статье [117] проведена деконволюция экспе-
на «молекулярном уровне», должны учитываться
риментальных спектров XPS и оценен вклад раз-
характеристики, относящиеся непосредственно к
личных электронных состояний в наблюдаемый
частицам материала. Это значительно расширяет
сигнал атомов цинка. Содержание фрагментов
перечень параметров, характеризующих катали-
Zn-NC, Zn-Cl и Zn-O на поверхности составля-
заторы. Изменение одного из параметров синтеза
ет 69, 20 и 11% соответственно, что противоречит
приводит к изменению сразу нескольких физи-
особенной роли кислород-содержащих лигандов
ко-химических параметров этих материалов, что
[39]. Данные XPS помогли установить природу
НЕФТЕХИМИЯ том 63 № 6 2023
ДВОЙНЫЕ МЕТАЛЛОЦИАНИДНЫЕ (DMC) КАТАЛИЗАТОРЫ
825
лигандов в DMC-катализаторах, синтезированных
Zn3[Co(CN)6]2 · xH2O [19], что не коррелирует с их
в работе [42]. В этой статье были получены мате-
эффективностью в (со)полимеризации с участием
риалы с использованием α-, β- и γ-дикетонов или
эпоксидов. Zn-Co-материалы обладают наиболь-
β-кетоэфиров, как лигандов, и добавок солиганда -
шей кислотностью среди катализаторов, получен-
P123. Характер фотоэлектронных спектров, содер-
ных из K3[Co(CN)6] и MCl2 (M = Zn, Fe, Co, Ni, Cu),
жащих по два сигнала электронов Zn2p1/2 и Zn2p3/2,
но наиболее эффективными в обменной реакции
свидетельствовал о том, что в случае 1,3-дикетонов
между карбоновыми кислотами и нитрилом оказа-
или 1,3-кетоэфиров лиганды входят в структуру
лись кобальт-кобальтовые материалы [171].
материала как в кетонной, так и енольной тауто-
Зависимость кислотности материала от способа
мерных формах. Эти результаты также подтвер-
получения была изучена на примере цинк-кобаль-
ждались данными ИК-спектроскопии. Интересные
товых DMC-катализаторов с TBA и PEG-4000 в ка-
результаты дала деконволюция спектров XPS для
честве лигандов [19]. При использовании солиган-
марганец-железных материалов, синтезированных
да в дополнение к TBA кислотность существенно
из K4[Fe(CN)6], MnCl2, TBA и P123 [161]. Помимо
повышается, с 1.34 до 2.29 ммоль/г, если PEG-4000
ожидаемого аниона [Fe(CN)6]4-, железо присут-
добавляется после стадии смешения неорганиче-
ствует в малых количествах в виде [Fe(CN)6H2O]3-,
ских реагентов и TBA. В то же время, катализатор
марганец - в виде [Mn(CN)6]4-, MnO и MnO2, а кис-
содержащий только ТВА, проявлял наибольшую
лород - в виде MnO2, C=O и С-OH. Таким образом,
активность в сополимеризации циклогексеноксида
природа металлов в DMC-материалах влияет на их
(CHO) и CO2, что коррелировало с общей кислот-
качественный состав: в отличие от цинк-кобальто-
ностью. В случае цинк-кобальтовых материалов,
вых, в марганец-железных материалах нет хлора.
полученных с использованием TBA и P123 в каче-
Льюисовская кислотность. Для DMC-катали-
стве лигандов [167], способ добавления P123 также
заторов характерна только льюисовская кислот-
влияет на кислотность: этот показатель составляет
ность [124, 126]. Льюисовская кислотность харак-
1.79 или 1.51 ммоль/г, если P123 присутствует или
теризуется суммарным количеством кислотных
отсутствует на стадии смешения неорганических
центров на поверхности материала и определяет-
прекурсоров и TBA, соответственно, что практиче-
ся на основании данных по адсорбции/десорбции
ски не отражается на каталитической активности в
аммиака с помощью метода термопрограммируе-
сополимеризации CHO и CO2.
мой десорбции. Обычно такая кислотность выра-
Аналогичная картина наблюдается и для
жается в ммоль/г или ммоль/м2 (количество NH3,
цинк-железных материалов. Наличие солиганда
адсорбируемое 1 г или 1 м2 поверхности катали-
(P123 [124, 165, 169, 170] или PEG-5800 [166]) в
затора соответственно). Среди представленных
дополнение к TBA обуславливает наибольшую
в литературе данных в подавляющем количестве
общую кислотность и наибольшую эффектив-
случаев кислотность определялась для цинк-же-
ность в переэтерификации триглицеридов. Также
лезных DMC-катализаторов [124, 164-170] и лишь
было показано, что способ добавления солиганда
в нескольких случаях - для цинк-кобальтовых
(PEG-4000) в процессе синтеза цинк-железных
[19, 161, 167, 171] или нетрадиционных катализа-
DMC-катализаторов, практически не влияет на их
торов [161, 171].
эффективность в поликонденсации с образованием
Кислотность не учитывает фрагментацию ка-
сверхразветвленных полиэфиров, а их кислотность
тализатора и
«высвобождение» каталитических
при этом изменяется в пределах 3.14-8.23 ммоль/г
[168].
центров в процессе синтеза (см. раздел выше).
Вследствие этого каталитическая активность мо-
Satyarthi и др. [172-174] сравнили цинк-желез-
жет коррелировать как с кислотностью, отнесен-
ные материалы и широко используемые образцы
ной к массе материала (общая кислотность), так и
кислотных катализаторов, сульфатированный ди-
с кислотностью, отнесенной к поверхности мате-
оксид циркония и цеолит Al-MCM-41. Среди этих
риала (плотность кислотных центров). Так, Zn-Co
катализаторов DMC-материалы имели наиболь-
DMC-материалы имеют меньшую кислотность,
шую «суммарную» кислотность (0.84 ммоль/г) и
чем цинк-железные [167], но большую, чем чистый
плотность кислотных центров, что подтверждалось
НЕФТЕХИМИЯ том 63 № 6 2023
826
ПЯТАКОВ, НИФАНТЬЕВ
их высокой активностью в процессе этерификации
териала с SBET 486 м2/г и средним диаметром пор
и в обратной реакции гидролиза. При этом, мар-
2.1 нм, а если солиганд добавляется после стадии
ганец-железные материалы характеризуются еще
смешения неорганических прекурсоров, SBET по-
большей кислотностью, чем цинк-железные [170],
лученного материала снижается на порядок - до
и проявляют более высокую активность в метано-
~48 м2/г, но средний диаметр пор возрастает до
лизе пропиленкарбоната [161].
~10 нм [19].
Удельная поверхность и пористость. DMC-ма-
По сравнению с Zn-Co-материалами, Zn-Fe(III)
териалы отличаются от Zn3[Co(CN)6]2 не только
или Zn-Fe(II) материалы имеют значительно мень-
различным составом, влияющим на электронные
шую удельную поверхность - до 165 м2/г [164], и
свойства атомов цинка, но и на уровне морфоло-
для них наблюдается другой характер зависимости
гии. Чистый гексацианокобальтат(III) цинка высо-
BET
от условий синтеза. TBA- и TBA/P123-содержа-
щие материалы характеризуются большей удель-
кокристалличен и характеризуется микропористо-
ной поверхностью по сравнению с чистым гекса-
стью с размером пор ~5 Å [22], что слишком мало
цианоферратом(II) цинка; при этом наибольшей
для диффузии реагентов к каталитическим цен-
SBET обладал TBA/P123-содержащий катализатор
трам и поэтому процесс может протекать лишь на
[124]. В другой работе [178] показано, что удель-
внешней поверхности частиц. Напротив, DMC-ма-
ная поверхность и пористость уменьшаются при
териалы в значительной степени аморфны и обла-
увеличении молекулярной массы солиганда (PEG).
дают мезопористостью, что позволяет им иметь
Влияние порядка добавления TBA и PEG-4000 на
высокую удельную поверхность, желанную для
удельную поверхность Zn-Fe(II) катализаторов из-
любого гетерогенного катализатора. Для лучших
учено в статье [168]. Наибольшая SBET (160 м2/г)
образцов величины SBET, определяемые на основе
наблюдается, если раствор ZnCl2, TBA и PEG-4000
изотерм адсорбции жидкого азота по методу BET,
добавляется к раствору K4[Fe(CN)6], а наименьшая
превосходят 500 м2/г и сопоставимы с таковыми
(37 м2/г) - при добавлении раствора ZnCl2 и TBA к
для некоторых видов цеолитов и силикагеля [175].
раствору K4[Fe(CN)6], TBA и PEG-4000.
Значительно реже для DMC-материалов определя-
Для увеличения удельной поверхности пред-
ется внешняя удельная поверхность SEXT, не учи-
тывающая поверхность пор.
ложены нанесение DMC-материалов на силика-
гель [179-182], γ-Al2O3 в сочетании с механохи-
Наибольшую удельную поверхность среди
мическим синтезом [183] или PU-пену [184-186].
цинк-кобальтовых катализаторов, 730 м2/г, имеет
Получение композитов DMC/SiO2 возможно как
TBA-содержащий образец, синтез которого пред-
с помощью золь-гель метода, заключающегося в
ставлен в статье [163]. Природа лиганда оказывает
соосаждении DMC-материала и SiO2 [180, 182],
влияние на удельную поверхность и пористость.
так и путем осаждения DMC-материала на уже
Например, при использовании TBA, тетрагидро-
существующий SiO2 [179, 181]. Полученные в ра-
фурана или 2-метоксиэтанола в качестве лиган-
боте [180] с помощью золь-гель метода компози-
дов SBET составила 653, 561 и 614 м2/г, а средний
ты имели высокую удельную поверхность (SBET
размер пор - 2.9, 10.1 и 12.0 нм соответственно
составила от 648 до 736 м2/г), но были компози-
[176, 177]. Кроме этого, данный TBA-содержа-
ционно неоднородны: кроме частиц DMC/SiO2,
щий катализатор демонстрирует и большую SEXT -
присутствовали частицы практически чистого си-
290 м2/г [176].
ликагеля и частицы DMC-материала. Однако, Sun
Наличие солиганда и способ его добавления
и колл. [182] удалось получить однородный нано-
(порядок смешения реагентов) влияют на удель-
ламмелярный композит, удельная поверхность ко-
ную поверхность и пористость. Так, использова-
торого была значительно больше (431 м2/г), чем
ние солиганда (PEG-10000) приводит к уменьше-
у ненанесенного DMC-катализатора (232 м2/г).
нию SBET с 730 до 448 м2/г и увеличению объема
Наноламеллярной формой частиц обусловлена и
пор, если солиганд добавляет вместе с K3[Co(CN)6]
большая SBET (784 м2/г), которую имел комплекс
и TBA к раствору ZnCl2 и TBA [163]. Присутствие
Zn2[Co(CN)6]OAc, полученный из Zn(OAc)2 и
солиганда (PEG-4000) на стадии смешения неорга-
K3[Co(CN)6] в отсутствие органических лигандов
нических прекурсоров приводит к получению ма-
и родственный DMC-материалам [125].
НЕФТЕХИМИЯ том 63 № 6 2023
ДВОЙНЫЕ МЕТАЛЛОЦИАНИДНЫЕ (DMC) КАТАЛИЗАТОРЫ
827
Дополнительными опциями для увеличения
агрегации частиц и их неконтролируемому росту,
удельной поверхности DMC-материалов является
способствуя получению материалов с развитой по-
синтез по методу обратной эмульсии или с приме-
верхностью и пористостью. Форма и размер частиц
нением «PFDM» (см. раздел 1). Так, катализатор
при этом зависят от строения полиэфира.
DMC-Igepal, полученный методом обратной эмуль-
Способ смешения неорганических прекур-
сии, превосходит по величине общей и внешней
соров, «PFDM», «FDM» или «RDM», оказыва-
удельной поверхности TBA/PTMEG-содержащий
ет влияние на морфологию цинк-кобальтовых
катализатор, синтезированный классическим спо-
TBA-содержащих катализаторов
[17]. Во всех
собом: SBET - 552 против 464 м2/г, SEXT - 170 против
трех случаях наблюдалась ламеллярная структу-
21 м2/г соответственно. Использование «PFDM»
ра, но расположение ламелей различалось. В слу-
для синтеза TBA/PEG-3000-содержащих катализа-
чае «PFDM» образуются однородные по размерам
торов дает материалы с наибольшей SBET (~37 м2/г)
частицы, похожие на цветок («flower-like», срост-
в сравнении с образцами, полученными с помощью
ки ламелей), тогда как для «FDM» и «RDM» -
«FDM» и «RDM» (в обоих случаях ~13 м2/г).
частицы более неправильной формы с большей
Морфология. Морфология (размер частиц и их
областью сращивания отдельных ламелей, размер
форма, (не)однородность по размерам) является
таких частиц больше, чем для «PFDM». Различие в
важной характеристикой, зависящей от способа
морфологии для этих режимов является следстви-
получения и влияющей на каталитические свой-
ем различной макрокинетики процессов.
ства DMC-материалов. В недавно опубликованном
исследовании подчеркивается важность размера
DMC-катализаторы могут образовывать нано-
частиц катализатора для достижения низких значе-
ламеллярную структуру. Такая морфология наблю-
ний коэффициента полидисперсности получаемого
дается в разных по происхождению материалах и,
PPO [151]. В то же время, ранее сообщалось, что
по всей видимости, определяется температурой
степень аморфности не связана напрямую с ак-
синтеза, как в случае работ [180, 182, 187], в кото-
тивностью и селективностью DMC-катализаторов
рых синтез проводили при 75°С (в статье [182, 187]
[127].
это был TBA-содержащий катализатор, в статьях
Результаты сканирующей электронной микро-
[180, 182] - гибридный DMC/SiO2). Сходная мор-
скопии (СЭМ) показывают, что использование ор-
фология, однако, наблюдалась в случае TBA/
ганических лигандов приводит к увеличению сте-
PEG-содержащего катализатора, полученного при
пени аморфности и уменьшению размера частиц
50°С [77].
в сравнении с чистым Zn3[Co(CN)6]2 · xH2O, кото-
В работе [23] приведено сравнение катализато-
рый является высококристаллическим [23]. Более
ров, полученных традиционным способом (DMC-
конкретно влияние природы солиганда на мор-
PTMEG) и катализатора, полученного по методу
фологию материалов показано в работах [23, 38].
обратной эмульсии DMC-Igepal. Последний отли-
Катализатор без солиганда (содержал только TBA)
чался наноразмерным характером частиц (<200 нм)
имел большие частицы (> 1.5 мкм) неправильной
и большей однородностью в сравнении с материа-
формы с большим разбросом по размерам. Добав-
лами, полученными традиционным способом (рис. 5).
ка солиганда, в качестве которых использовались
Цинк-железные катализаторы, синтезирован-
полиэфиры (PEG, PPG, PTMEG, P123 или HBP),
ные с использованием TBA и P123 при 50°С, пред-
приводит к уменьшению размера частиц (< 300 нм)
ставляли собой сферические частицы размером
и увеличению однородности по размерам. В случае
1-3 мкм и их агломераты [170]. Kotwal и колл. [164]
PTMEG, P123 или HBP получаются хорошо раз-
деленные частицы сферической формы, PPG - ку-
установили влияние температуры на морфологию
бической формы, PEG - агломераты сферических
цинк-железных катализаторов: при 10°С части-
частиц. Вследствие полимерной природы, полиэ-
цы имеют сферическую форму (средний диаметр
фирные солиганды эффективно координируются
~2 мкм), при 25°С - кубическую (~1 × 1 мкм), при
по атомам цинка растущей частицы, «обволаки-
50°С - кубическую (~1 × 1 мкм) и гексагональную
вая» их. Таким образом, солиганды препятствуют
(длина ~3 мкм), а при 80°С - неправильную.
НЕФТЕХИМИЯ том 63 № 6 2023
828
ПЯТАКОВ, НИФАНТЬЕВ
материалов и соответствующих PBA, является ме-
зопористость. Цинк-железные материалы имеют
большую общую кислотность, но характерная для
них микропористость затрудняет доступность кис-
лотных центров, делая эти катализаторы менее ак-
тивными. Фрагментация также может вносить свой
вклад в различие активности двух этих видов DMC-
катализаторов.
ЗАКЛЮЧЕНИЕ
В заключение, в этом обзоре собраны и про-
анализированы данные по синтезу, строению, ме-
ханизму действия и физико-химическим свойствам
DMC-материалов, как катализаторов. Несмотря на
появление все новых и новых знаний, в академичес-
кой литературе до сих пор нет ответа на вопрос,
каковы строение активного центра и механизм
DMC-катализируемой полимеризации PO. По-ви-
димому, определяющую роль играют фрагменты
L3Zn-OH, наличие которых роднит между собой
DMC-материалы, созданные человеком, и карбоан-
гидразу - высокоэффективный катализатор гидра-
тации CO2, созданный природой. Одним из фак-
торов, обуславливающих высокую эффективность
DMC-катализаторов, является разрушение матри-
цы материала (фрагментация) и «высвобождение»
активных центров из объема на поверхность. Не-
ясными остаются превращения, которые возможны
еще до полимеризации и которые сопровождают
катализатор в процессе нее. На наш взгляд, боль-
шие надежды в решении этих вопросов возлагают-
ся на квантово-химическое моделирование. Одна-
ко, невзирая на белые пятна в нашем понимании их
природы и механизма действия, ведется активная
разработка новых подходов к синтезу DMC-мате-
риалов, в том числе не содержащих TBA в составе.
Рис. 5. СЭМ-фотографии DMC-PTMEG (a), чистого
(б) и DMC-Igepal (в).
Zn3[Co(CN)6]2
ФИНАНСИРОВАНИЕ РАБОТЫ
Работа выполнена при финансовой поддержке
Российского научного фонда, грант 21-73-30010.
Таким образом, физико-химическими свой-
ствами DMC-материалов, а, следовательно, и их
КОНФЛИКТ ИНТЕРЕСОВ
каталитическими свойствами, можно управлять в
Нифантьев И.Э. - член редколлегии журнала
широких пределах, варьируя параметры синтеза.
«Нефтехимия», Пятаков Д.А. заявляет об отсут-
Важной характеристикой, отличающей цинк-ко-
ствии конфликта интересов, требующего раскры-
бальтовые DMC-материалы от цинк-железных
тия в данной статье.
НЕФТЕХИМИЯ том 63 № 6 2023
ДВОЙНЫЕ МЕТАЛЛОЦИАНИДНЫЕ (DMC) КАТАЛИЗАТОРЫ
829
ИНФОРМАЦИЯ ОБ АВТОРАХ
blue analogues with well-controlled morphologies for
the efficient sorption of cesium // J. Mater. Chem. A.
Пятаков Дмитрий Александрович, к.х.н.,
C6TA10016C .
Нифантьев Илья Эдуардович, д.х.н., ORCID:
10.
Takahashi A., Tanaka H., Parajuli D., Nakamura T.,
Minami K., Sugiyama Y., Hakuta Y., Ohkoshi S.-I.,
Kawamoto T. Historical pigment exhibiting ammonia
gas capture beyond standard adsorbents with adsorption
СПИСОК ЛИТЕРАТУРЫ
sites of two kinds // J. Am. Chem. Soc. 2016. V. 138.
1.
Ionescu M. Chemistry and Technology of Polyols for
Polyurethanes. Shropshire: Rapra Technology, 2005.
11.
Kaye S.S., Long J.R. Hydrogen storage in the dehydrat-
2.
Brocas A.-L., Mantzaridis C., Tunc D., Carlotti S. Poly-
ed Prussian blue analogues M3[Co(CN)6]2 (M = Mn,
ether synthesis: from activated or metal-free anion-
Fe, Co, Ni, Cu, Zn) // J. Am. Chem. Soc. 2005. V. 127.
ic ring-opening polymerization of epoxides to func-
tionalization // Prog. Polym. Sci. 2013. V. 38. № 6.
12.
Ferlay S., Mallah T., Ouahès R., Veillet P., Verdaguer M.
A room-temperature organometallic magnet based on
ci.2012.09.007
Prussian blue // Nature. 1995. V. 378. № 6558. P. 701-
3.
Herzberger J., Niederer K., Pohlit H., Seiwert J.,
Worm M., Wurm F.R., Frey H. Polymerization of
13.
Milgrom J. Method of making a polyether using a dou-
ethylene oxide, propylene oxide, and other alkylene
ble metal cyanide complex compound // Patent US
oxides: synthesis, novel polymer architectures, and
№ 3278457. 1966.
bioconjugation // Chem. Rev. 2016. V. 116. № 4.
14.
Le-Khac B., Wang W. Double-metal cyanide catalysts
which can be used to prepare polyols and the processes
rev.5b00441
related thereto // Patent US № 6696383. 2004.
4.
Valvekens P., De Vos D. Chapter 1. Double metal cya-
15.
Le-Khac B. Highly active double metal cyanide cata-
nides as heterogeneous catalysts for organic reactions.
lysts // Patent US № 5693584. 1997.
In: New Materials for Catalytic Applications / Eds.
16.
Chen X., Kumbhalkar M., Fisk J., Murdoch B. In situ
V.I. Parvulescu, E. Kemnitz. Amsterdam: Elsevier,
monitoring of double metal cyanide (DMC) catalyst
2016. P. 1-12.
synthesis by raman spectroscopy // Raman Technol-
5.
Ruiz-Bermejo M., Menor-Salván C., Osuna-Esteban S.,
ogy for Today’s Spectroscopists. 2023. V. 38. № S6.
Veintemillas-Verdaguer S. The effects of ferrous and
other ions on the abiotic formation of biomolecules
nq1471w5
using aqueous aerosols and spark discharges // Orig.
17.
An N., Li Q., Yin N., Kang M., Wang J. Effects of addi-
Life Ev. Biosph. 2007. V. 37. № 6. P. 507-521. https://
tion mode on Zn-Co double metal cyanide catalyst for
doi.org/10.1007/s11084-007-9107-0
synthesis of oligo(propylene-carbonate) diols // Appl.
6.
Ruiz-Bermejo M., Rogero C., Menor-Salván C.,
Organomet. Chem. 2018. V. 32. № 11. P. e4509. https://
Osuna-Esteban S., Martín-Gago J.Á., Veintemillas-
doi.org/10.1002/aoc.4509
Verdaguer S. Thermal wet decomposition of Prussian
18.
Le-Khac B., Bowman P.T., Hinney H.R. Highly active
blue: implications for prebiotic chemistry // Chem.
double metal cyanide complex catalysts // Patent US
№ 5712216. 1998.
org/10.1002/cbdv.200900024
19.
Sebastian J., Srinivas D. Effects of method of prepa-
7.
Fu H., Liu C., Zhang C., Ma W., Wang K., Li Z., Lu X.,
ration on catalytic activity of Co-Zn double-metal
Cao G. Enhanced storage of sodium ions in Prussian
cyanide catalysts for copolymerization of CO2 and ep-
blue cathode material through nickel doping // J. Mater.
oxide // Appl. Catal. A: Gen. 2014. V. 482. P. 300-308.
org/10.1039/C7TA00132K
20.
Huang Y.J., Qi G.R., Chen L.S. Effects of morphology
8.
Liu S., Pan G.L., Li G.R., Gao X.P. Copper hexacyano-
and composition on catalytic performance of double
ferrate nanoparticles as cathode material for aqueous
metal cyanide complex catalyst // Appl. Catal. A: Gen.
Al-ion batteries // J. Mater. Chem. A. 2015. V. 3. № 3.
S0926-860X(02)00452-0
9.
Liu J., Li X., Rykov A.I., Fan Q., Xu W., Cong W.,
21.
Zhang W., Lin Q., Cheng Y., Lu L., Lin B., Pan L.,
Jin C., Tang H., Zhu K., Ganeshraja A.S., Ge R.,
Xu N. Double metal cyanide complexes synthesized
Wang X., Wang J. Zinc-modulated Fe-Co Prussian
by solvent-free grinding method for copolymerization
НЕФТЕХИМИЯ том 63 № 6 2023
830
ПЯТАКОВ, НИФАНТЬЕВ
of CO2 and propylene oxide // J. Appl. Polym. Sci.
thesizing a double metal cyanide catalyst // Patent US
№ 6921737. 2005.
aP.34544
32.
Shaobo Z., Hui J., Zhihua Z. Polymetallic cyanide com-
22.
Peeters A., Valvekens P., Ameloot R., Sankar G.,
plex catalyst and preparation method and application
Kirschhock C.E.A., De Vos D.E. Zn-Co double metal
thereof // Patent CN № 110684187. 2020.
cyanides as heterogeneous catalysts for hydroamina-
33.
Jin H., Wang R., Zhang H., Tu J. Multi-metal cyanide
tion: a structure-activity relationship // ACS Catal.
complex catalyst // Patent CN № 101302286. 2010.
34.
Shaobo Z., Hui J., Zhihua Z. Supported metal cyanide
cs300805z
complex catalyst as well as preparation method and
23.
Peeters A., Valvekens P., Vermoortele F., Ameloot R.,
application thereof // Patent CN № 113881032. 2022.
Kirschhock C., De Vos D. Lewis acid double metal cya-
35.
Hofmann J., Ooms P., Gupta P., Schaefer W. Improved
nide catalysts for hydroamination of phenylacetylene //
double metal cyanide catalysts for producing polyether
Chem. Commun. 2011. V. 47. № 14. P. 4114-4116.
polyols // Patent WO № 1999/046042. 1999.
36.
Le-Khac B. Highly active double metal cyanide cata-
24.
Dharman M.M., Ahn J.-Y., Lee M.-K., Shim H.-L.,
lysts // Patent US № 5482908. 1996.
Kim K.-H., Kim I., Park D.-W. Moderate route for
37.
Le-Khac B. Polyether-containing double metal cyanide
the utilization of CO2-microwave induced copoly-
catalysts // Patent US № 5545601. 1996.
merization with cyclohexene oxide using highly effi-
38.
Lee I.K., Ha J.Y., Cao C., Park D.-W., Ha C.-S., Kim I.
cient double metal cyanide complex catalysts based
Effect of complexing agents of double metal cya-
on Zn3[Co(CN)6]2 // Green Chem. 2008. V. 10. № 6.
nide catalyst on the copolymerizations of cyclohex-
ene oxide and carbon dioxide // Catal. Today. 2009.
25.
Kim I., Byun S.H., Ha C.-S. Ring-opening polymer-
izations of propylene oxide by double metal cyanide
cattod.2009.07.073
catalysts prepared with ZnX2 (X = F, Cl, Br, or I) // J.
39.
Kim I., Ahn J.-T., Ha C.S., Yang C.S., Park I. Polym-
Polym. Sci., Part A: Polym. Chem. 2005. V. 43. № 19.
erization of propylene oxide by using double metal
cyanide catalysts and the application to polyurethane
26.
Kim I., Yi, M.J., Lee K.J., Park D.-W., Kim B.U.,
elastomer // Polymer. 2003. V. 44. № 11. P. 3417-3428.
Ha C.-S. Aliphatic polycarbonate synthesis by copo-
lymerization of carbon dioxide with epoxides over
40.
Yoon J.H., Lee I.K., Choi H.Y., Choi E.J., Yoon J.H.,
double metal cyanide catalysts prepared by using ZnX2
Shim S.E., Kim I. Double metal cyanide catalysts bear-
(X = F, Cl, Br, I) // Catal. Today. 2006. V. 111. № 3.
ing lactate esters as eco-friendly complexing agents
for the synthesis of highly pure polyols // Green Chem.
27.
Chen S., Zhang X., Lin F., Qi G. Preparation of double
metal cyanide compleces from water-insoluble zinc
C0GC00554A
compounds and their catalytic performance for co-
41.
Wei R.-J., Zhang X.-H., Du B.-Y., Fan Z.-Q., Qi G.-R.
polymerization of epoxide and CO2 // React. Kinet.
Highly active and selective binary catalyst system for
the coupling reaction of CO2 and hydrous epoxides //
org/10.1007/s11144-007-4891-0
J. Mol. Catal. A: Chem. 2013. V. 379. №. P. 38-45.
28.
Zhang X.H., Chen S., Wu X.M., Sun X.K., Liu F.,
Qi G.R. Highly active double metal cyanide complex-
42.
Tran C.H., Pham L.T.T., Lee Y., Jang H.B., Kim S.,
es: effect of central metal and ligand on reaction of
Kim I. Mechanistic insights on Zn(II)-Co(III) double
epoxide/CO2 // Chin. Chem. Lett. 2007. V. 18. № 7.
metal cyanide-catalyzed ring-opening polymerization
of epoxides // J. Catal. 2019. V. 372. P. 86-102. https://
29.
Combs G. Double metal cyanide complex catalysts
doi.org/10.1016/j.jcat.2019.02.028
modified with group IIA compounds // Patent WO
43.
Schaefer W., Hofmann J., Ooms P. Double metal cya-
№ 1999/048607. 1999.
nide catalysts for producing polyether polyols // WO
30.
Huang Y.-J., Zhang X.-H., Hua Z.-J., Chen S.-L.,
Patent № 2003/020796. 2003.
Qi G.-R. Ring-opening polymerization of propyl-
44.
Mellado M.M., Gonzalez M.D.B. Double metal cyanide
ene oxide catalyzed by a calcium-chloride-modified
(DMC) catalysts with crown ethers, process to produce
zinc-cobalt double metal-cyanide complex // Macro-
them and applications // Patent US № 2007/0135298.
mol. Chem. Phys. 2010. V. 211. № 11. P. 1229-1237.
2007.
45.
Zhang M., Yang Y., Chen L. Preparation of crown ether
31.
Dexheimer E.M., Wildeson J., Hinz W. Method of syn-
complexing highly active double metal cyanide catalysts
НЕФТЕХИМИЯ том 63 № 6 2023
ДВОЙНЫЕ МЕТАЛЛОЦИАНИДНЫЕ (DMC) КАТАЛИЗАТОРЫ
831
and copolymerization of CO2 and propylene oxide //
60.
O’Connor J.M., Grieve R.L. Double metal cyanide
Chinese J. Catal. 2015. V. 36. № 8. P. 1304-1311.
catalysts containing polyglycol ether complexing
agents // Patent US № 2001/0046940. 2001.
46.
Lili Y., Shaobo Z., Hui J., Wang W. Preparation method
61.
Lim J., Yun S.H., Kim M.-R., Kim I. Synthesis of poly-
of aliphatic polycarbonate catalyzed by DMC catalyst //
carbonate polyols by double-metal cyanide catalyzed
Patent CN № 104927040. 2015.
copolymerization of epoxide with carbon dioxide //
47.
Liu H., Wang X., Gu Y., Guo W. Preparation and charac-
J. Nanosci. Nanotechnol. 2017. V. 17. № 10. P. 7507-
terization of double metal cyanide complex catalysts //
62.
Jang J.H., Ha J.H., Kim I., Baik J.H., Hong S.C. Facile
org/10.3390/80100067
room-temperature preparation of flexible polyurethane
foams from carbon dioxide based poly(ether carbonate)
48.
Ooms P., Hofmann J., Gupta P., Groenendaal L. Dou-
polyols with a reduced generation of acetaldehyde //
ble metal cyanide catalysts for preparing poly-ether-
ACS Omega. 2019. V. 4. № 5. P. 7944-7952. https://
polyols // Patent US № 6204357. 2001.
doi.org/10.1021/acsomega.9b00808
49.
Hsu Y.-C., Tsai H.-C. High-activity double-metal-cya-
63.
Lee D.H., Ha J.H., Kim I., Baik J.H., Hong S.C. Carbon
nide catalyst // Patent US № 2021/0205799. 2021.
dioxide based poly(ether carbonate) polyol in bi-poly-
50.
Ooms P., Hofmann J., Gupta P., Schaefer W. Dou-
ol mixtures for rigid polyurethane foams // J. Polym.
ble-metal-cyanide catalysts used for preparing poly-
ether polyols // Patent US № 6391820. 2002.
org/10.1007/s10924-020-01668-0
51.
Hofmann J., Gupta P., Kumpf R.-J., Ooms P., Schae-
64.
Jang E.H., Kim S.A., Kim H., Tran C.H., Song H.Y.,
fer W., Schneider M. Crystalline double metal cyanide
Hyun K., Seo W.J., Kim I. Access to ultra-high molecu-
catalysts for producing polyether polyols // Patent WO
lar weight poly(propylene glycol)-based polyols using
№ 1999/019063. 1999.
double metal cyanide catalyst // Macromol. Res. 2020.
52.
Schaefer W., Hofmann J., Ooms P. Double metal
cyanide catalysts for the production of polyetherpolyols //
020-8008-1
Patent WO № 2003/020422. 2003.
65.
Tran C.-H., Lee, M.-W., Lee S.-J., Choi J.-H.,
53.
Ooms P., Hofmann J., Dobler M. Double metal cyanide
Lee E.-G., Choi H.-K. Kim I. Highly active heteroge-
catalysts for the preparation of polyether polyols //
neous double metal cyanide catalysts for ring-open-
Patent US № 2004/0092389. 2004.
ing polymerization of cyclic monomers // Polymers.
54.
Le-Khac B. Double-metal cyanide catalysts for prepar-
ing polyether polyols // Patent US № 2003/0211935.
polym14122507
2003.
66.
He Z., Yu S., Cai Z., Cao X., Zhang L., Huang K. Modifi-
55.
Hofmann J., Ooms P., Gupta P., Schaefer W., Lohrenz J.
cation of ZnCoPBA by different organic ligands and its
Double metal cyanide catalysts for producing polyether
application in the cycloaddition of CO2 and epoxides //
polyols // Patent WO № 2000/047649. 2000.
56.
Chruściel A., Hreczuch W., Janik J., Czaja K.,
org/10.1007/s12039-022-02034-4
Dziubek K., Flisak Z., Swinarew A. Characterization
67.
Tran C.H., Kim S.A., Moon Y., Lee Y., Ryu H.M.,
of a double metal cyanide (DMC)-type catalyst in the
Baik J.H., Hong S.C., Kim I. Effect of dicarbonyl com-
polyoxypropylation process: effects of catalyst con-
plexing agents on double metal cyanide catalysts to-
centration // Ind. Eng. Chem. Res. 2014. V. 53. № 16.
ward copolymerization of CO2 and propylene oxide //
57.
Le-Khac B. Double metal cyanide catalysts containing
org/10.1016/j.cattod.2020.01.008
functionalized polymers // Patent WO № 1998/016310.
68.
Tran C.H., Pham L.T.T., Jang H.B., Kim S.A., Kim I.
1998.
Effect of α-, β-, γ-, and δ-dicarbonyl complexing agents
58.
Ooms P., Hofmann J., Gupta P. Bimetallic cyanide
on the double metal cyanide-catalyzed ring-opening
catalysts for producing polyether polyols // Patent WO
polymerization of propylene oxide // Catal. Today.
№ 2000/015337. 2000.
59.
Lee S.H., Lee I.K., Ha J.Y., Jo J.K., Park I., Ha C.-S.,
cattod.2020.01.001
Suh H., Kim I. Tuning of the activity and induction
69.
Verma A., Saini S., Sharma B., Verma V., Behera B.,
period of the polymerization of propylene oxide cat-
Singh R., Ganguly S.K., Ray A., Vorontsov A., Kumar U.
alyzed by double metal cyanide complexes bearing
EDTA incorporated Fe-Zn double metal cyanide cat-
β-alkoxy alcohols as complexing agents // Ind. Eng.
alyst for the controlled synthesis of polyoxypropylene
Chem. Res. 2010. V. 49. № 9. P. 4107-4116. https://
glycol // J. Polym. Res., 2023. V. 30. № 2. P. 62. https://
doi.org/10.1021/ie1000967
doi.org/10.1007/s10965-022-03407-6
НЕФТЕХИМИЯ том 63 № 6 2023
832
ПЯТАКОВ, НИФАНТЬЕВ
70.
Verma A., Sharma B., Saini S., Behera B., Saran S.,
propagation constant and segments // Macromol. The-
Ganguly S.K., Kumar U. Oligomeric heterogeneous
double metal cyanide catalyst for one-pot ring-opening
org/10.1002/mats.202100012
polymerization // ChemistrySelect. 2023. V. 8. № 6.
82.
Klinger M., Bachmann R., Jupke A. Molecular weight
distribution in di metal cyanide catalyzed polymeriza-
71.
Tran C.-H., Lee M.-W., Park S.-W., Jeong J.-E.,
tion 2: numerical simulation of chain activation/deacti-
Lee S.-J., Song W., Huh P., Kim I. Heterogeneous dou-
vation and diffusion effects // Macromol. Theory Simul.
ble metal cyanide catalyzed synthesis of poly(ε-capro-
lactone) polyols for the preparation of thermoplastic
mats.202100013
elastomers // Catalysts. 2021. V. 11. № 9. P. 1033.
83.
Langanke J., Hofmann J., Gürtler C., Wolf A. Facile
synthesis of formaldehyde-based polyether(-carbonate)
72.
Tran C.H., Lee S.J., Moon B.-r., Lee E.-g., Choi H.-k.,
polyols // J. Polym. Sci., Part A: Polym. Chem. 2015.
Kim I. Organonitriles as complexing agents for the
double metal cyanide-catalyzed synthesis of polyether,
pola.27687
polyester, and polycarbonate polyols // Catal. Today.
84.
Ma K., Bai Q., Zhang L., Liu B. Synthesis of flame-re-
tarding oligo(carbonate-ether) diols via double metal
tod.2023.114125
cyanide complex-catalyzed copolymerization of PO
73.
Tran C.H., Choi H.-K., Lee E.-G., Moon B.-R., Song W.,
and CO2 using bisphenol A as a chain transfer agent //
Kim I. Prussian blue analogs as catalysts for the fixa-
RSC Adv. 2016. V. 6. № 54. P. 48405-48410. https://
tion of CO2 to glycidol to produce glycerol carbonate
doi.org/10.1039/C6RA07325E
and multibranched polycarbonate polyols // J. CO2
85.
Zhang, X., Dong, J., Su, Y., Lee, E.G., Duan, Z., Kim, I.,
Liu, B. Construction and arm evolution of trifunction-
jcou.2023.102530
al phenolic initiator-mediated polycarbonate polyols
74.
Kim I., Kim S.A. Double metal cyanide catalyst, prepa-
produced by using a double metal cyanide catalyst //
ration method therefor, and method for preparing
Polym. Chem. 2023. V. 14. № 11. P. 1263-1274. https://
polyol // Patent WO № 2021/137632. 2021.
doi.org/10.1039/D3PY00009E
75.
Luinstra G.A., Nörnberg B. Process for preparing dou-
86.
Mijolovic D., Haunert A., Kunst A., Bauer S., Miao Q.,
ble metal cyanide catalysts and their use in polymer-
Eling B. // Раtent WO № 2009/095363. 2009.
ization reactions // Patent WO № 2016/202838. 2016.
87.
Kunst A., Eling B., Loeffler A., Lutter H.-D., Han W.,
76.
Chen S., Qi G.-R., Hua Z.-J., Yan H.-Q. Double metal
Mueller J. Polyether polyols, process for preparing
cyanide complex based on Zn3[Co(CN)6]2 as highly
polyether polyols and their use for producing polyure-
active catalyst for copolymerization of carbon dioxide
thanes // Patent US № 2011/0269863. 2011.
and cyclohexene oxide // J. Polym. Sci., Part A: Polym.
88.
Hager S.L., Moore M.N., Reese J.R., Neal B.L.
Polyols suitable for hot molded foam production
org/10.1002/pola.20334
with high renewable resource content // Patent US
77.
Pinilla-de Dios M., Andrés-Iglesias C., Fernández A.,
№ 2013/0210951. 2013.
Salmi T., Galdámez J.R., García-Serna J. Effect of Zn/
89.
Huang Y.-J., Qi G.-R., Wang Y.-H. Controlled
Co initial preparation ratio in the activity of double
ring-opening polymerization of propylene oxide cat-
metal cyanide catalysts for propylene oxide and CO2
alyzed by double metal-cyanide complex // J. Polym.
copolymerization // Eur. Polym. J. 2017. V. 88. P. 280-
Sci., Part A: Polym. Chem. 2002. V. 40. № 8. P. 1142-
78.
Ahmad S.-A., Le-Khac B., Bullano G.A. Double metal
90.
Gao Y., Gu L., Qin Y., Wang X., Wang F. Dicarboxylic
cyanide catalysts // Patent US № 5900384. 1999.
acid promoted immortal copolymerization for controlla-
79.
Wu L.-C., Yu A.-F., Zhang M., Liu B.-H., Chen L.-B.
ble synthesis of low-molecular weight oligo(carbonate-
DMC catalyzed epoxide polymerization: induction
ether) diols with tunable carbonate unit content //
period, kinetics, and mechanism // J. Appl. Polym.
J. Polym. Sci., Part A: Polym. Chem. 2012. V. 50.
org/10.1002/aP.20089
la.26366
80.
McDaniel K.G. High productivity alkoxylation process-
91.
Liu S., Qin Y., Qiao L., Miao Y., Wang X., Wang F.
es // Patent US № 2008/0167501. 2008.
Cheap and fast: oxalic acid initiated CO2-based poly-
81.
Bachmann R., Klinger M., Jupke A. Molecular weight
ols synthesized by a novel preactivation approach //
distribution in di metal cyanide catalyzed polymeriza-
tion 1: fundamental distribution for length dependent
org/10.1039/C5PY01338K
НЕФТЕХИМИЯ том 63 № 6 2023
ДВОЙНЫЕ МЕТАЛЛОЦИАНИДНЫЕ (DMC) КАТАЛИЗАТОРЫ
833
92.
Liu S., Miao Y., Qiao L., Qin Y., Wang X., Chen X.,
103. Shi J., Shi Z., Yan H., Wang X., Zhang X., Lin Q.,
Wang F. Controllable synthesis of a narrow polydisper-
Zhu L. Synthesis of Zn-Fe double metal cyanide com-
sity CO2-based oligo(carbonate-ether) tetraol // Polym.
plexes with imidazolium-based ionic liquid cocatalysts
via ball milling for copolymerization of CO2 and pro-
org/10.1039/C5PY00556F
pylene oxide // RSC Adv. 2018. V. 8. № 12. P. 6565-
93.
Liu S., Qin Y., Chen X., Wang X., Wang F. One-pot con-
trollable synthesis of oligo(carbonate-ether) triol using
104. Liu N., Gu C., Wang Q., Zhu L., Yan H., Lin Q. Fab-
a Zn-Co-DMC catalyst: the special role of trimesic acid
rication and characterization of the ternary composite
as an initiation-transfer agent // Polym. Chem. 2014.
catalyst system of ZnGA/RET/DMC for the terpolym-
erization of CO2, propylene oxide and trimellitic an-
C4PY00578C
hydride // RSC Adv. 2021. V. 11. № 15, P. 8782-8792.
94.
Li X.-J., Wen Y.-F., Wang Y., Peng H.-Y., Zhou X.-P.,
Xie X.-L. CO2-based biodegradable supramolecular
105. Kim I., Anas K., Lee S., Ha, C.-S., Park, D.-W. Tuning
polymers with well-tunable adhesive properties // Chin.
of the activity and induction period of double met-
al cyanide catalyzed ring-opening polymerizations
org/10.1007/s10118-021-2641-9
of propylene oxide by using ionic liquids // Catal.
95.
Haider K.W., Chung J.Y.J., Dormish J.F., Starcher R.V.,
Yano I.L., Hortelano E.R. Polyether-polysiloxane poly-
org/10.1016/j.cattod.2007.10.067
ols // Patent US № 2008/0171829. 2008.
106. Tharun J., Dharman M.M., Hwang Y., Roshan R.,
96.
Yi M.J., Byun S.-H., Ha C.-S., Park D.-W., Kim I. Copo-
Park M.S., Park D.-W. Tuning double metal cyanide
lymerization of cyclohexene oxide with carbon dioxide
catalysts with complexing agents for the selective pro-
over nano-sized multi-metal cyanide catalysts // Solid
duction of cyclic carbonates over polycarbonates //
Appl. Catal. A: Gen. 2012. V. 419-420. P. 178-184.
org/10.1016/j.ssi.2004.04.031
97.
Friščić T., Mottillo C., Titi H.M. Mechanochemistry for
107. Wei R.-j., Zhang X.-h., Du B.-y., Fan Z.-q., Qi G.-r.
Synthesis // Angew. Chem. Int. Ed. 2020. V. 59. № 3.
Synthesis of bis(cyclic carbonate) and propylene car-
bonate via a one-pot coupling reaction of CO2, bisepox-
98.
Guo Z., Lin Q. Coupling reaction of CO2 and propylene
ide and propylene oxide // RSC Adv. 2013. V. 3. № 38.
oxide catalyzed by DMC with co-complexing agents
incorporated via ball milling // J. Mol. Catal. A: Chem.
108. Dharman M.M., Yu J.-I., Ahn J.-Y., Park D.-W. Selec-
tive production of cyclic carbonate over polycarbonate
cata.2014.03.006
using a double metal cyanide-quaternary ammonium
99.
Guo Z., Lin Q., Wang X., Yu C., Zhao J., Shao Y., Peng T.
salt catalyst system // Green Chem. 2009. V. 11. № 11.
Rapid synthesis of nanoscale double metal cyanide
catalysts by ball milling for the cycloaddition of CO2
109. Zhang Y.-Y., Li Y., Zhou X.-J., Zhang X.-H., Du B.-Y.,
and propylene oxide // Mater. Lett. 2014. V. 124.
Fan Z.-Q. Synthesis of an amphiphilic brush copo-
lymer by a highly efficient “grafting onto” approach
100. Guo Z., Lin Q., Zhu L., Wang X., Niu Y., Yu C., Fang T.
via CO2 chemistry // Macromol. Rapid Commun.
Nanolamellar Zn-Ni/Co-Ni catalysts introduced by
ball milling for the copolymerization of CO2 with pro-
marc.201400718
pylene oxide // Nanosci. Nanotechnol. Lett. 2014. V. 6.
110. Liu B., Zhang Y.-Y., Zhang X.-H., Du B.-Y., Fan Z.-Q.
Fixation of carbon dioxide concurrently or in tandem
101. Zhang W., Lu L., Cheng Y., Xu N., Pan L., Lin Q.,
with free radical polymerization for highly transparent
Wang Y. Clean and rapid synthesis of double metal
polyacrylates with specific UV absorption // Polym.
cyanide complexes using mechanochemistry // Green
org/10.1039/C6PY00525J
org/10.1039/C1GC15557A
111. Garcia J.L., Jang E.J., Alper H. New heterogeneous
102. Qiang L., Zhifang G., Lisha P., Xue X. Zn-Cr double
catalysis for the synthesis of poly(ether polyol)s // J.
metal cyanide catalysts synthesized by ball milling for
Appl. Polym. Sci. 2002. V. 86. № 7. P. 1553-1557.
the copolymerization of CO2/propylene oxide, phthalic
anhydride/propylene oxide, and CO2/propylene oxide/
112. Robertson N.J., Qin Z., Dallinger G.C., Lobkov-
phthalic anhydride // Catal. Commun. 2015. V. 64.
sky E.B., Lee S., Coates, G.W. Two-dimensional double
metal cyanide complexes: highly active catalysts for
НЕФТЕХИМИЯ том 63 № 6 2023
834
ПЯТАКОВ, НИФАНТЬЕВ
the homopolymerization of propylene oxide and copo-
123. C h r u ś c i e l A . , H re c z u c h W. , C z a j a K . ,
lymerization of propylene oxide and carbon dioxide //
Ławniczak-Jabłońska K., Janik J. The complementary
structural studies of the double metal cyanide type
org/10.1039/B607963F
catalysts for the ring opening polymerization of the
113. Hofmann J. Double metal cyanide catalysts for
oxiranes // Polimery. 2016. V. 61. № 6. P. 421-432.
the preparation of polyether polyols // Patent US
№ 2008/0177025. 2008.
124. Sreeprasanth P.S., Srivastava R., Srinivas D., Rat-
114. Yu S.J., Liu Y., Byeon S.J., Park D.W., Kim I. Ring-open-
nasamy P. Hydrophobic, solid acid catalysts for
ing polymerization of propylene oxide by double metal
production of biofuels and lubricants // Appl. Catal.
cyanide catalysts prepared by reacting CoCl2 with var-
ious metal cyanide salts // Catal. Today. 2014. V. 232.
org/10.1016/j.apcata.2006.08.012
125. Marquez C., Simonov A., Wharmby M.T., Van
115. Alferov K., Wang S., Li T., Xiao M., Guan S., Meng Y.
Goethem C., Vankelecom I., Bueken B., Krajnc A.,
Co-Ni cyanide bi-metal catalysts: copolymerization of
Mali G., De Vos, D., De Baerdemaeker T. Layered
carbon dioxide with propylene oxide and chain transfer
Zn2[Co(CN)6](CH3COO) double metal cyanide: a
two-dimensional DMC phase with excellent catalytic
org/10.3390/catal9080632
performance // Chem. Sci. 2019. V. 10. № 18. P. 4868-
116. Chen S., Xiao Z., Ma M. Copolymerization of carbon
dioxide and epoxides with a novel effective Zn-Ni dou-
126. Sebastian J., Darbha S. Structure-induced catalytic
ble-metal cyanide complex // J. Appl. Polym. Sci. 2008.
activity of Co-Zn double-metal cyanide complexes
for terpolymerization of propylene oxide, cyclohex-
app.25064
ene oxide and CO2 // RSC Adv. 2015. V. 5. № 24.
117. Lawniczak-Jablonska K., Dynowska E., Lisowski W.,
Sobczak J.W., Chruściel A., Hreczuch W., Libera J.,
127. Sebastian J., Srinivas D. Factors influencing catalytic
Reszka A. Structural properties and chemical bonds
activity of Co-Zn double-metal cyanide complexes
in double metal cyanide catalysts // X-ray Spectrom.
for alternating polymerization of epoxides and CO2 //
Appl. Catal. A: Gen. 2015. V. 506. P. 163-172. https://
xrs.2636
doi.org/10.1016/j.apcata.2015.09.010
118. Mullica D.F., Milligan W.O., Beall G.W., Reeves W.L.
128. Wojdeł J.C., Bromley S.T., Illas F., Jansen J.C. Devel-
Crystal structure of Zn3[Co(CN)6]2·12H2O // Ac-
opment of realistic models for double metal cyanide
ta Crystallogr. B. 1978. V. 34. № 12. P. 3558-3561.
catalyst active sites // J. Mol. Model. 2007. V. 13. № 6.
119. Simonov A., De Baerdemaeker T., Boström H.L.B.,
129. Almora-Barrios N., Pogodin S., Bellarosa L., García-
Ríos Gómez M.L., Gray H.J., Chernyshov D., Bosak A.,
Melchor M., Revilla-López G., García-Ratés, M.,
Bürgi H.-B., Goodwin A.L. Hidden diversity of vacancy
Vázquez-García A.B., Hernández-Ariznavarreta P.,
networks in Prussian blue analogues // Nature. 2020.
López N. Structure, activity, and deactivation mecha-
nisms in double metal cyanide catalysts for the pro-
s41586-020-1980-y
duction of polyols // ChemCatChem. 2015. V. 7. № 6.
120. Zhang X.-H., Hua Z.-J., Chen S., Liu, F., Sun X.-K.,
Qi G.-R. Role of zinc chloride and complexing agents
130. Chruściel A., Hreczuch W., Czaja K., Sacher-Majew-
in highly active double metal cyanide catalysts for
ska B. On thermal behaviour of DMC catalysts for ring
ring-opening polymerization of propylene oxide //
opening polymerization of epoxides // Thermochim.
Appl. Catal. A: Gen. 2007. V. 325. № 1. P. 91-98.
tca.2016.02.009
121. Chen S., Zhang P., Chen L. Fe/Zn double metal
131. Barnard J.A. The pyrolysis of tert-butanol // Trans.
cyanide (DMC) catalyzed ring-opening polymerization
of propylene oxide: Part 3. Synthesis of DMC cata-
org/10.1039/TF9595500947
lysts // Prog. Org. Coat. 2004. V. 50. № 4. P. 269-272.
132. Kisielowski C., Specht P., Rozeveld S., Freitag B.,
Kieft E.R., Kang J., Fielitz A.J., Fielitz T.R., van
122. Lawniczak-Jablonska K., Chrusciel A. Estimation of
Dyck D., Yancey D.F. Exploring functional materials
the catalytic centre in double metal cyanide catalysts by
by understanding beam-sample interactions // Adv.
XAS // J. Phys. Conf. Ser. 2016. V. 712. № 1. P. 012062.
Funct. Mater. 2022. V. 32. № 27. P. 2201112. https://
doi.org/10.1002/adfm.202201112
НЕФТЕХИМИЯ том 63 № 6 2023
ДВОЙНЫЕ МЕТАЛЛОЦИАНИДНЫЕ (DMC) КАТАЛИЗАТОРЫ
835
133. Hayes J.E., Langsdorf L.J., Isaacs B.H., Armellini F.J.
complexes derived from the CpCo(CN)− anion // Inorg.
Process for rapid activation of double metal cyanide
Chim. Acta. 2004. V. 357. № 5. P. 1603-1607. https://
catalysts // Patent US № 5844070. 1998.
doi.org/10.1016/j.ica.2003.11.016
134. Schenk S., Notni J., Köhn U., Wermann K., Anders E.
145. Kubisa P., Penczek S. Cationic activated monomer
Carbon dioxide and related heterocumulenes at zinc
polymerization of heterocyclic monomers // Prog.
and lithium cations: bioinspired reactions and princi-
Polym. Sci. 1999. V. 24. № 10. P. 1409-1437. https://
ples // Dalton Trans. 2006. № 35. P. 4191-4206. https://
doi.org/10.1016/S0079-6700(99)00028-3
doi.org/10.1039/B608534B
146. Raghuraman A., Babb D., Miller M., Paradkar M.,
135. Li Y., Zhang Y.-Y., Liu B., Zhang X.-H. HCAII-inspired
Smith B., Nguyen A. Sequential DMC/FAB-catalyzed
catalysts for making carbon dioxide-based copolymers:
alkoxylation toward high primary hydroxyl, high
the role of metal-hydroxide bond // Chin. J. Polym. Sci.
molecular weight polyether polyols // Macromole-
s10118-018-2047-5
org/10.1021/acs.macromol.6b01363
136. Kuyper J., Boxhoorn G. Hexacyanometallate salts used
147. Inoue S. Immortal polymerization: the outset, develop-
as alkene-oxide polymerization catalysts and molecu-
ment, and application // J. Polym. Sci., Part A: Polym.
lar sieves // J. Catal. 1987. V. 105. № 1. P. 163-174.
org/10.1002/1099-0518(20000815)38:16<2861::AID-
137. Chen S., Xu N., Shi J. Structure and properties of
POLA20>3.0.CO;2-1
polyether polyols catalyzed by Fe/Zn double metal
148. Zhang M., Villa C., Thompson L., Weston J. Mul-
cyanide complex catalyst // Prog. Org. Coat. 2004.
tisite model of polyol preparation in continuous pro-
cesses using heterogeneous double metal cyanide
coat.2003.08.021
138. Chen S., Chen L. Sequence structure of polyether cat-
aiche-2004/pdffiles/papers/353b.pdf.
alyzed by Fe-Zn double-metal cyanide complex cat-
149. Grajciar L., Heard C.J., Bondarenko A.A., Polyn-
alysts // Colloid. Polym. Sci. 2003. V. 281. № 3. P.
ski M.V., Meeprasert J., Pidko E.A., Nachtigall P. To-
wards operando computational modeling in heteroge-
139. Luinstra G.A., Molnar F. Poly(propylene carbonate),
neous catalysis // Chem. Soc. Rev. 2018. V. 47. № 22.
old CO2 copolymer with new attractiveness // Macro-
150. Natta G., Mantica E. The distribution of products in
org/10.1002/masy.200751324
a series of consecutive competitive reactions // J. Am.
140. Klaus S., Lehenmeier M.W., Herdtweck E., Degl-
Chem. Soc. 1952. V. 74. № 12. P. 3152-3156. https://
mann P., Ott A.K., Rieger B. Mechanistic insights in-
doi.org/10.1021/ja01132a057
to heterogeneous zinc dicarboxylates and theoretical
151. Stahl S.-F., Wietzer M., Luinstra G.A. DMC-mediat-
considerations for CO2-epoxide copolymerization // J.
ed propoxylation in semibatch with an external loop:
Am. Chem. Soc. 2011. V. 133. № 33. P. 13151-13161.
insights into the catalytic action // Ind. Eng. Chem.
141. Stahl S.-F., Luinstra G.A. DMC-Mediated copoly-
org/10.1021/acs.iecr.3c01313
merization of CO2 and PO - mechanistic aspects de-
152. Lee S., Baek S.T., Anas K., Ha C.-S., Park D.-W.,
rived from feed and polymer composition // Catalysts.
Lee J.W., Kim I. Tuning of activity, induction period
and polymer properties of double metal cyanide cata-
catal10091066
lyzed ring-opening polymerizations of propylene oxide
142. Darensbourg D.J., Adams M.J., Yarbrough J.C. Toward
by using quaternary ammonium salts // Polymer. 2007.
the design of double metal cyanides for the copoly-
merization of CO2 and epoxides // Inorg. Chem. 2001.
polymer.2007.05.072
153. Lee S.H., Ha C.-S., Kim I. Modified montmorillonite
ic0155941
as a tuner of propylene oxide polymerization behavior
143. Darensbourg D.J., Adams M.J., Yarbrough J.C.,
catalyzed by double metal cyanide compound // Mac-
Phelps A.L. Synthesis and structural characterization
of double metal cyanides of iron and zinc: catalyst
org/10.1007/BF03218775
precursors for the copolymerization of carbon diox-
154. Le-Khac B., Wang W., Faraj M.K. Acid-treated dou-
ide and epoxides // Inorg. Chem. 2003. V. 42. № 24.
ble metal cyanide complex catalysts // Patent US
№ 6063897. 2000.
144. Darensbourg D.J., Phelps A.L. Mixed metal cyanide
155. Safina L.R., Kharlampidi K.E., Safin D.K. Molecu-
НЕФТЕХИМИЯ том 63 № 6 2023
836
ПЯТАКОВ, НИФАНТЬЕВ
lar-weight characteristics and deemulsifying activity
166. Kumar P., Srivastava V.C., Jha M.K. Synthesis of bio-
of oligourethanes based on alkylene oxide block copo-
diesel from transesterification of Jatropha oil with
lymers and propylene oxide homopolymers prepared
methanol using double metal cyanide as catalyst //
in the presence of a double metal cyanide catalyst //
J. Clean Energy Technol. 2017. V. 5. № 1. P. 23-26.
Russ. J. Appl. Chem. 2012. V. 85. № 10. P. 1610-1616.
167. Sebastian J., Darbha S. Solid, double-metal cyanide
156. Dai C., Zhu Q., Pang H., Zhu L., Lin Q. Rapid copo-
catalysts for synthesis of hyperbranched polyesters
lymerization of carbon dioxide and propylene oxide
and aliphatic polycarbonates // J. Chem. Sci. 2014.
catalyzed by double metal cyanide complexes in an
ultrasonic field // Mater. Lett. 2016. V. 180. P. 89-92.
s12039-014-0573-4
168. Sebastian J., Srinivas D. Influence of method of prepa-
157. Lear J.J., Sloan O.D., Pazos J.F. Method for decreas-
ration of solid, double-metal cyanide complexes on
ing the propensity for phase-out of the high molecular
their catalytic activity for synthesis of hyperbranched
weight component of double metal cyanide-catalyzed
polymers // Appl. Catal. A: Gen. 2013. V. 464-465.
high secondary hydroxyl polyoxypropylene polyols //
Patent US № 6083420. 2000.
169. Srinivas D., Satyarthi J.K. Biodiesel production from
158. Laitar D.S., Babb D.A., Villa C.M., Keaton R., Masy
vegetable oils and animal fat over solid acid dou-
J.-P. Alkylene oxide polymerization using a double
ble-metal cyanide catalysts // Catal. Surv. from Asia.
metal cyanide catalyst complex and a magnesium,
Group 3-Group 15 metal or lanthanide series metal
s10563-010-9108-2
compound // Patent US № 9040657. 2015.
170. Srivastava R., Srinivas D., Ratnasamy P. Fe-Zn dou-
159. McDaniel K.G., Combs G.G. Catalyst for the produc-
ble-metal cyanide complexes as novel, solid trans-
tion of polyols having lower amounts of high molecular
esterification catalysts // J. Catal. 2006. V. 241. № 1.
weight tail // Patent US № 9562134. 2017.
160. Eleveld M.B., Grotenbreg R.A.W., Van Kempen R.
171. Marquez C., Corbet M., Smolders S., Marion P., De
Preparation of a double metal cyanide catalyst // Patent
Vos D. Double metal cyanides as heterogeneous Lewis
US № 6977236. 2005.
acid catalysts for nitrile synthesis via acid-nitrile ex-
161. Song Z., Subramaniam B., Chaudhari R.V. Transester-
change reactions // Chem. Commun. 2019. V. 55. № 86.
ification of propylene carbonate with methanol using
Fe-Mn double metal cyanide catalyst // ACS Sustain.
172. Satyarthi J.K., Radhakrishnan S., Srinivas D. Factors
influencing the kinetics of esterification of fatty acids
org/10.1021/acssuschemeng.8b04779
over solid acid catalysts // Energy & Fuels. 2011. V. 25.
162. Hamuyuni J., Daramola M.O., Oluwasina O.O.
Energy-Dispersive X-ray Spectroscopy: Theory and
173. Satyarthi J.K., Srinivas D., Ratnasamy P. Influence of
Application in Engineering and Science in Encyclope-
surface hydrophobicity on the esterification of fatty ac-
dia of Physical Organic Chemistry / Eds. Wang. Z. John
ids over solid catalysts // Energy & Fuels. 2010. V. 24.
Wiley & Sons, 2017. P. 1-23.
163. Jadhav A.R., Bandal H.A., Kim H. Synthesis of substi-
174. Satyarthi J.K., Srinivas D., Ratnasamy P. Hydrolysis
tuted amines: catalytic reductive amination of carbonyl
of vegetable oils and fats to fatty acids over solid acid
compounds using Lewis acid Zn-Co-double metal
catalysts // Appl. Catal. A: Gen. 2011. V. 391. № 1.
cyanide/polymethylhydrosiloxane // Chem. Eng. J.
175. De Gisi S., Lofrano G., Grassi M., Notarnicola M.
cej.2016.02.067
Characteristics and adsorption capacities of low-cost
164. Kotwal M., Deshpande S.S., Srinivas D. Esterifica-
sorbents for wastewater treatment: a review // Sus-
tion of fatty acids with glycerol over Fe-Zn double-
metal cyanide catalyst // Catal. Commun. 2011. V. 12.
org/10.1016/j.susmat.2016.06.002
176. Luo M., Zhang X.-H., Du B.-Y., Wang Q., Fan Z.-Q.
com.2011.05.008
Alternating copolymerization of carbonyl sulfide and
165. Kumar P., Matoh L., Srivastava V.C., Štangar U.L. Syn-
cyclohexene oxide catalyzed by zinc-cobalt double
thesis of zinc/ferrocyanide nano-composite catalysts
metal cyanide complex // Polymer. 2014. V. 55. № 16.
having a high activity for transesterification reaction //
mer.2014.05.065
org/10.1016/j.renene.2019.10.178
177. Wei R.-J., Zhang X.-H., Du B.-Y., Sun X.-K., Fan Z.-Q.,
НЕФТЕХИМИЯ том 63 № 6 2023
ДВОЙНЫЕ МЕТАЛЛОЦИАНИДНЫЕ (DMC) КАТАЛИЗАТОРЫ
837
Qi G.-R. Highly Regioselective and alternating co-
catalyzed by silicon dioxide/Zn-CoIII double metal
polymerization of racemic styrene oxide and carbon
cyanide complex hybrid catalysts with a nanolamellar
dioxide via heterogeneous double metal cyanide com-
structure // J. Polym. Sci., Part A: Polym. Chem. 2008.
plex catalyst // Macromolecules. 2013. V. 46. № 9.
pola.22666
178. Yan F., Yuan Z., Lu P., Luo W., Yang L., Deng L.
183. Zhu L., Zhu Q., Wang Q., Gu C., Tang A., Liu T.,
Fe-Zn double-metal cyanide complexes catalyzed bio-
Dai C., Li H. CO2 copolymerization catalyzed by the
diesel production from high-acid-value oil // Renew.
double metal cyanide catalysts Zn-Fe(III)/Zn-Co(III)
org/10.1016/j.renene.2010.10.032
with nanometer-sized γ-Al2O3 as co-catalyst // Nanosci.
179. Cao X., Wang K., Mao Q., Gu Z., Wang F.
Nanotechnol. Lett. 2018. V. 10. № 11. P. 1515-1522.
MCM-41-supported double metal cyanide nanocom-
posite catalyst for ring-opening polymerisation of pro-
184. Le-Khac B. Polyurethane foam-supported double met-
pylene oxide // J. Nanopart. Res. 2022. V. 24. № 3.
al cyanide catalysts for polyol synthesis // Patent US
№ 5426081. 1995.
180. Dienes Y., Leitner W., Müller M.G.J., Offermans
185. Le-Khac B. Plastic foam-supported double metal cya-
W.K., Reier T., Reinholdt A., Weirich T.E., Müller T.E.
nide catalysts for polyether polyol synthesis // Patent
Hybrid sol-gel double metal cyanide catalysts for the
copolymerisation of styrene oxide and CO2 // Green
US № 5523386. 1996.
186. Le-Khac B. Polyurethane foam-supported double met-
org/10.1039/C2GC16485J
al cyanide catalysts for polyether polyol synthesis //
181. Marquez C., Rivera-Torrente M., Paalanen P.P., Weck-
Patent US № 5527880. 1996.
huysen B.M., Cirujano F.G., De Vos D., De Baerde-
187. Zhang X.-H., Wei R.-J., Sun X.-K., Zhang J.-F.,
maeker T. Increasing the availability of active sites
Du B.-Y., Fan Z.-Q., Qi G.-R. Selective copolymer-
in Zn-Co double metal cyanides by dispersion onto a
ization of carbon dioxide with propylene oxide cata-
SiO2 support // J. Catal. 2017. V. 354. P. 92-99. https://
lyzed by a nanolamellar double metal cyanide com-
doi.org/10.1016/j.jcat.2017.08.008
plex catalyst at low polymerization temperatures //
182. Sun X.-K., Zhang X.-H., Liu F., Chen S., Du B.-Y.,
Wang Q., Fan Z.-Q., Qi G.-R. Alternating copoly-
merization of carbon dioxide and cyclohexene oxide
org/10.1016/j.polymer.2011.09.040
НЕФТЕХИМИЯ том 63 № 6 2023