ЖУРНАЛ ОБЩЕЙ ХИМИИ, 2021, том 91, № 9, с. 1453-1458
УДК 546.881;546.881.5
КОМПЛЕКСЫ ВАНАДИЯ(V) С УГЛЕВОДАМИ
И СПИРТАМИ
© 2021 г. Г. В. Горкуша*, Г. Э. Литосов, Д. О. Рузанов
Санкт-Петербургский государственный технологический институт (технический университет),
Московский пр. 26, Санкт-Петербург, 190013 Россия
*e-mail: grigorygor2014@yandex.ru
Поступило в Редакцию 16 июня 2021 г.
После доработки 20 августа 2021 г.
Принято к печати 22 августа 2021 г.
Получены продукты взаимодействия цитратного биядерного комплекса ванадия(IV) с глюкоза-6-фос-
фатом, глюкозой, мальтозой и монофосфатом глицерина. Изучено строение полученных комплексов.
Ключевые слова: ванадий, глюкоза-6-фосфат, комплексы ванадия, углеводы
DOI: 10.31857/S0044460X21090171
Координационные соединения играют важную
зуется в моноклинной сингонии в пространствен-
роль в живых организмах, участвуя в важнейших
ной группе P21/c с параметрами элементарной
процессах жизнедеятельности. Комплексные сое-
ячейки a 8.9440(6), b 15.2560(10), c 9.2970(6) Å,
динения ванадия(IV) и (V) - подтвержденные ин-
β 107.4370(10)°, V 1210.28(14) Å3, Z 2. Исходный
сулиномиметики - используются при лечении са-
комплекс ванадия(IV) 1 состоит из биядерного
аниона [(VO)2Citr2]4-, четырех внешнесферных ка-
харного диабета, а также в целях кардиозащиты и
иммуномодуляции в ультрамалых концентрациях
тионов калия и четырех сольватных молекул воды.
Структура комплексных катионов представляет
[1-3].
собой два катиона оксованадия(IV), связанных
Координационные соединения ванадия с ор-
между собой двумя остатками лимонной кислоты.
ганическими лигандами имеют преимущества пе-
Каждый остаток лимонной кислоты в нейтральной
ред свободными ионами ванадия в растворе ввиду
и слабощелочной средах связывает попарно фраг-
устойчивости комплекса и возможности контроля
менты V=O. Установлено антигликемическое дей-
над ионным замещением окружения металла [1].
ствие комплекса 1.
Комплексы воздействуют на компоненты фермен-
Ванадий в высших валентностях и фосфор
тов, отвечающих за углеводный обмен в организ-
сходны по свойствам и могут взаимодействовать с
ме. Важной задачей остается выяснение процессов
различными координационными рецепторами, ко-
замещения или координации комплексов ванадия
торые функционализированы фосфатной группой
при взаимодействии с фосфатами углеводов и их
(АДФ, АТФ). Фосфатная группа в составе углево-
влияние на сами ферменты.
да или β-глицерофосфата обладает высокой селек-
Модельные реакции с углеводами и сложны-
тивностью к соединениям ванадия, и это можно
ми спиртами могут раскрыть способ взаимодей-
использовать для построения модельных реакций.
ствия, если использовать в реакциях комплекс ва-
Фосфатные группы некоторых соединений в гомо-
надия K4[(VO)2Citr2]∙4H2O 1, структура которого
генной водной среде способны присоединяться к
подтверждена методом РСА. По данным рентге-
комплексам ванадия (V+5O+). Биядерные комплек-
ноструктурного анализа, комплекс 1 кристалли-
сы ванадия (V+4O2+) в меньшей степени способны
1453
1454
ГОРКУША и др.
Схема 1.
K4[V2O2(C6H6O7)2]·4H2O + Углевод (Rn) → K4[V2O2(C6H6O7)2Rn]
2а-г
1
OH
O
OCH2
O
P
OCH2
H
O
H
H
O
H
O
R=
(2a),
(2б),
OH
H
OH
H
O
R
O
O
OH
OH
OH
OH
OH
O
O
H OH
H OH
V
V
O
O
O
O
O
O
R
OCH2
HOCH2
H
O
H
H
O
H
O
(2в),
OH
H
OH
H
O
OH
O
OH
H OH
H OH
HO
1
HO
O
P
OH
(2г).
O
O
OH
присоединять фосфатную группу, координиру-
1226, 1341, 1378, 1460, 2924, 3311, 3411) и ком-
ясь через кислород к фосфорсодержащим ионам.
плекса 2а следует, что глюкоза в исходном виде и
Окислительно-восстановительная биокаталитиче-
в полученном соединении находится в цикличе-
ская способность соединений ванадия исследова-
ской форме (полоса 916 см-1 [7]), изменения по-
на в ряде работ [4–6].
лосы при 996 см-1, а также полоса при 1650 см-1
и смещение полосы при 777 см-1 в комплексе 2а
Нами получены ванадий-углеводные и вана-
дий-спиртовые комплексы, установлен их состав.
свидетельствуют о присоединении комплекса 1
Комплекс ванадия(IV) 1 чувствителен к рН раство-
к спиртовой группе СH2OH глюкозы с образова-
ра. Слабокислая среда активирует металлоцентры
нием связи CH2O-V. Металлоцентры биядерного
и увеличивает способность присоединения к фос-
цитратного комплекса ванадия проявляются поло-
фатным группам углеводов и спиртов c образова-
сами при 775, 553 см-1 [8].
нием комплексов 2a-г (схема 1), а в нейтральной
В комплексе с глюкоза-6-фосфатом 2б глюкоза
или слабощелочной среде происходит их отрыв от
также находится в циклической форме (916 см-1),
фосфатной и гидроксильной групп углеводов.
присоединение происходит по фосфатной группе.
Результаты ЯМР 1H, 13С, ИК, УФ спектроско-
Образовавшаяся группировка ROPO-V характери-
пии комплексов 2a-г указывают на их устойчивый
зуется полосами при 1047 (P-O-C), 1224 (P-O-H),
состав. Биядерный остов комплекса остается без
1076 см-1 (P-O-V).
изменения. Атомы ванадия становятся V-валент-
Присоединение комплекса 1 к β-глицерофосфа-
ными.
ту идет по фосфатной группе, что подтверждается
Сопоставление ИК спектров исходных углево-
сопоставлением спектральных данных реагентов
дов и комплексов 2a-г показало, что комплекс 1
и продукта реакции [полосы в ИК спектре при
может координироваться как к глюкоза-6-фосфа-
1049 (P-O-C), 1240 (P-O-H), 1068 см-1 (P-O-V) и
ту (R-O-P-O-V) (2б), так и к глюкозе, и мальто-
в электронном спектре при 270 нм].
зе (R-O-V) (2a, в). Комплекс 1 присоединяется к
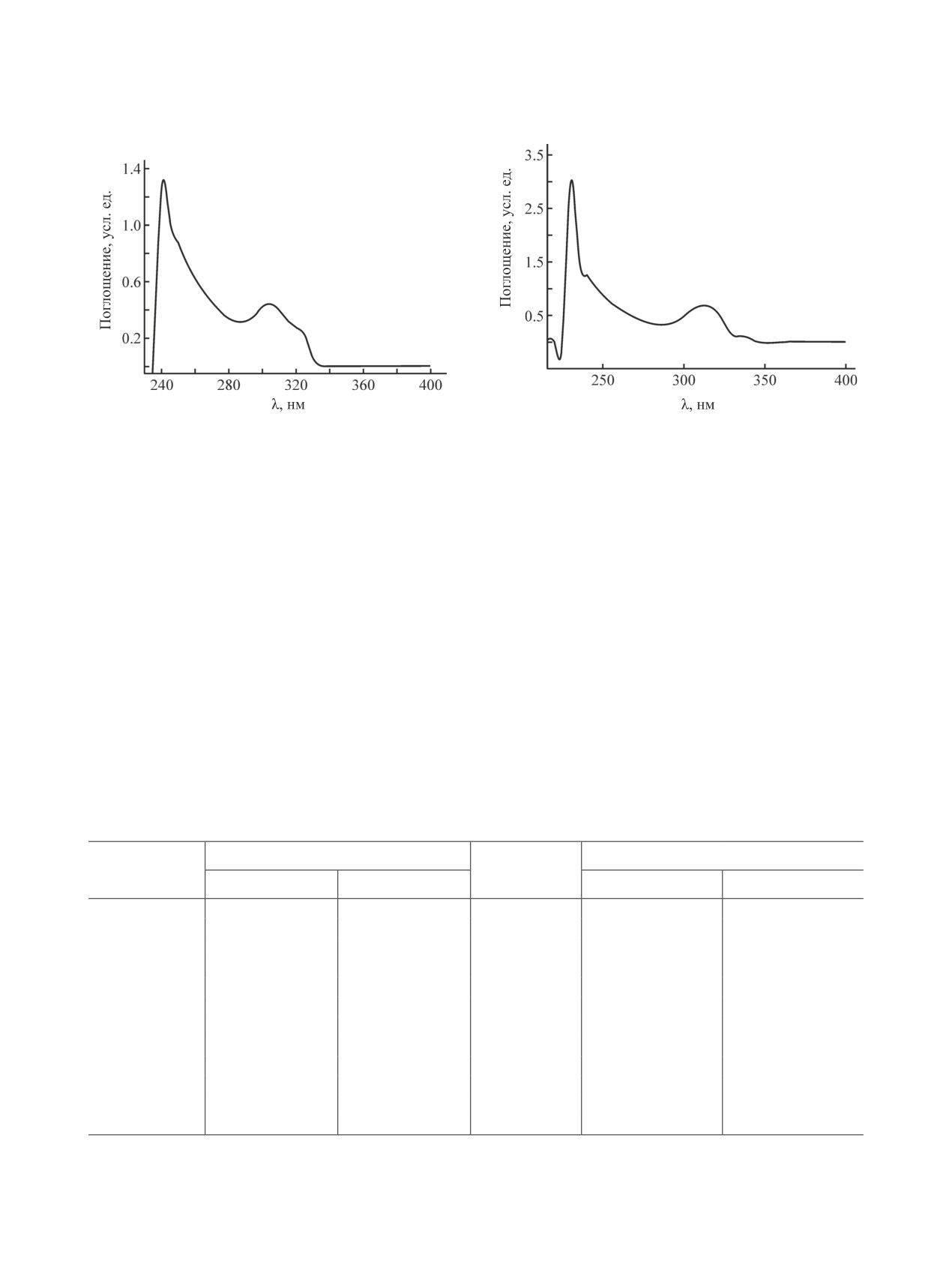
Согласно данным электронной спектроскопии,
группе (НO)2P=O через кислород ОН-группы.
в каждом из полученных комплексов присутствует
Из сравнения ИК спектров глюкозы (ν, см-1:
ион VO2+, которому соответствуют длины волн от
623, 777, 916, 996, 1024, 1051, 1112, 1149, 1204,
270 до 350 нм [9] (рис. 1, 2).
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 9 2021
КОМПЛЕКСЫ ВАНАДИЯ(V) С УГЛЕВОДАМИ И СПИРТАМИ
1455
Рис. 1. Электронный спектр комплекса 2а (306,
Рис. 2. Электронный спектр комплекса 2б (315,
323 нм).
341 нм).
Все полученные соединения были охаракте-
фате комплекс ванадия присоединен к фосфатной
ризованы данными ЯМР 1H и 13С. Основные раз-
группе, о чем свидетельствует сдвиг сигнала атома
личия наблюдаются в положениях сигналов про-
С2 на 3 м. д. (табл. 1, 2).
тонов и атомов углерода в молекулах углеводов
Для уточнения структуры полученных соеди-
и β-глицерофосфата в области 90-60 (13С) и 6-
нений были использованы методы гетероядерной
3 м. д. (1H). Сигналы атомов углерода углеводного
корреляционной спектроскопии 1H-13C HMBC и
остатка комплекса 2б смещены на 3 м. д., комплек-
HSQC. Сдвиги сигналов атомов углерода (в сред-
са 2a - на 2 м. д. относительно исходного углевода.
нем на 3 м. д.) и протонов (на 0.1-0.3 м. д.) сви-
Структура двух соединенных между собой моле-
детельствуют о взаимодействии углеводных ли-
кул глюкозы в мальтозе остается без изменения,
гандов с комплексом ванадия 1. Сопоставление
ионное присоединение приводит к сильному сдви-
с ИК и электронными спектрами показывает, что
гу (4-5 м. д.) сигналов в спектре ЯМР 13С комплек-
комплекс V(IV) не оказывает каталитическое вли-
са 2в по сравнению с мальтозой. В β-глицерофос-
яние на углеводы и глицерофосфат. Координация
Таблица 1. Сравнение параметров спектров ЯМР исходной глюкозы и комплекса 2а
δС, м. д.
δ, м. д.
Атом углерода
Атом водорода
глюкоза
комплекс 2а
глюкоза
комплекс 2а
С1
94.84
92.05
Н1
5.22
5.13
С2
74.15
71.38
Н2
5.22
5.12
С3
75.58
72.72
Н3
3.53
3.34
С4
74.29
71.44
Н4
3.73
3.63
С5
72.40
69.60
Н5
3.40
3.31
С6
63.40
60.54
Н6
3.82
3.72
С1′
94.84
95.87
Н1′
5.22
5.12
С2′
74.15
75.90
Н2′
5.22
5.13
С3′
75.58
75.72
Н3′
3.53
3.60
С4′
74.29
74.10
Н4′
3.73
3.58
С5′
72.40
69.55
Н5′
3.40
3.29
С6′
63.40
60.70
Н6′
3.82
3.75
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 9 2021
1456
ГОРКУША и др.
Таблица 2. Сравнение параметров спектров ЯМР β-глицерофосфата и комплекса 2га
δС, м. д.
δ, м. д.
Атом углерода
Атом водорода
β-глицеро-фосфат
комплекс 2г
β-глицеро-фосфат
комплекс 2г
С1
75.81
74.83
Н1
4.15
4.03
С1′
75.61
74.81
Н2
3.69
3.57
С2
63.29
62.33
Н3
3.67
3.56
С2′
63.12
62.30
С1α
75.81
74.81
Н1′
4.15
3.97
С1α′
75.61
74.79
Н2′
3.69
3.51
С2α
63.29
62.29
Н3′
3.67
3.48
С2α′
63.12
62.22
а Сигнал центрального атома углерода в глицерофосфате имеет два пика - С1, С1α. Сигналы первого и третьего угле-
родов обозначены С2, С2α соответственно. Сигналы второй молекулы обозначены штрихом.
происходит с участием гидроксильной и фосфат-
монной кислоты (2.41 г, 11.5 ммоль), раствор ох-
ной групп углеводов, а также фосфатной группы
лаждали до комнатной температуры и подщелачи-
β-глицерофосфата.
вали 12 мл 1 М. KОН до pH ≈ 5.5, затем добавляли
Таким образом, на примере взаимодействия
50 мл этанола. После выдерживания при 2-4°С в
цитратного биядерного комплекса ванадия(IV) с
течение недели образовывались синие кристаллы,
глюкоза-6-фосфатом, глюкозой, мальтозой и моно-
которые отфильтровывали, промывали спиртом и
фосфатом глицерина показано, что присоединение
сушили на воздухе. Выход 97%. УФ спектр (H2O):
комплекса протекает селективно по фосфатной
λ 300 нм.
группе в фосфатах углеводов и по гидроксильной
Бис(D-глюконато)бис[(μ2-цитрато)оксована-
группе индивидуальных углеводов.
дий(V)]тетракалий (2а). 0.1 г. (0.13 ммоль) ком-
плекса 1 растворяли в 20 мл H2O и добавляли 0.08
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
г D-глюкозы (0.30 ммоль). Полученный раствор
Спектры ЯМР 1Н и 13С снимали на спектроме-
кипятили 25 мин, затем упаривали. Полученный
тре Bruker Avance III HD 400 NanoBay на рабочих
серо-фиолетовый осадок отфильтровывали, про-
частотах 400.17 и 100.63 МГц соответственно. Для
мывали этанолом и сушили. Выход 0.07 г (40%),
отнесения сигналов в спектрах ЯМР 1H и 13C ис-
т. пл. 178°С. ИК спектр, ν, см-1: 3253, 2942, 2912,
пользовали методы двумерной гомо- и гетероядер-
2891, 1650 (C=O), 1369, 1302, 1287, 1224 (C-O),
ной спектроскопии ЯМР HMBC и HSQC. ИК спек-
1201 (C-O), 1145, 1103, 1082, 1041 (C-O-C), 1020,
тры записывали на ИК спектрометре Shimadzu
991, 916, 839, 775 (V=O), 702, 646, 601, 553 (V=O),
IR Tracer-100 с приставкой Quest на длинах волн
433, 405. УФ спектр, λ, нм: 315, 341. Спектр ЯМР
4000-400 см-1. Электронные спектры поглощения
1H (D2O), δ, м. д.: 5.13 д (2H, CH2O, 3JHH 7.4 Гц),
записывали на спектрофотометре СФ-56. Количе-
5.12 д (2H, CH2O, 3JHH 8.1 Гц), 4.54 с (1Н, CHO),
ство ванадия в комплексах определяли гравиме-
4.52 с (1H, CHO), 3.81 д (2Н, CH2, 3JHH 8.8 Гц), 3.78
трически.
д (2Н, CH2, 3JHH 10.7 Гц), 3.75 с (1Н, CHO), 3.72 с
Тетракалий бис[(μ2-цитрато)оксованадий-
(1Н, CHO), 3.63 д (2Н, CH2, 3JHH 11.2 Гц), 3.60 с
(IV)] тетрагидрат, K4[(VO)2Citr2]∙4H2O (1) полу-
(1Н, CHO), 3.58 с (1H, CHO), 3.40 д (2Н, CH2, 3JHH
чен по модифицированной нами методике [10]. К
10.3 Гц), 3.34 м (1Н, COOH), 3.31 с (1Н, CHO), 3.29
водному раствору V2O5 (0.6 г. 3.33 ммоль) добав-
с (1Н, CHO). Спектр ЯМР 13С (D2O), δС, м. д.: 95.87
ляли твердый KОН (0.81 г. 14.4 ммоль). Реакцион-
(C1′), 92.05 (C1), 75.90 (C2′), 75.72 (C3′), 72.72 (C3),
ную массу нагревали до 90°С. После образования
71.44 (C4), 71.38 (C2), 74.10 (C4′), 69.60 (C5), 69.55
прозрачного раствора добавляли моногидрат ли-
(C5′), 60.70 (C6′), 60.54 (C6). Найдено, % C 33.02; H
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 9 2021
КОМПЛЕКСЫ ВАНАДИЯ(V) С УГЛЕВОДАМИ И СПИРТАМИ
1457
3.91; V 11.72. C24H34O28V2. Вычислено, %: C 33.02;
(1Н, CHO), 3.53 с (1Н, CHO), 3.50 с (1Н, CHO), 3.44
H 3.89; V 11.69
с (1Н, CHO), 3.39 с (1Н, CHO), 3.31 с (1Н, CHO),
3.26 м (1Н, COOH), 3.25 с (1Н, CHO). Спектр ЯМР
Бис(D-глюконато-6-фосфат)бис[(μ2-цитрато)
оксованадий(V)]тетракалий (2б) получали ана-
13С (D2O), δС, м. д.: 99.58 (C1), 99.50 (C1′), 95.74
(C2′), 93.32 (С2), 74.51 (C3), 74.25 (C4), 74.32 (C3′),
логично из 0.1 г. (0.13 ммоль) комплекса 1 и 0.1 г
(0.38 ммоль) глюкоза-6-фосфата. Выход 0.14 г
74.17 (C4′), 73.13 (C5), 73.08 (C5′), 72.85 (C6), 72.80
(70%), светло-синий кристаллический порошок,
(C7), 72.65 (C7′), 72.61 (C6′), 71.27 (C8), 71.24 (C9),
т. пл. 192°С. ИК спектр, ν, см-1: 3253, 2942, 2912,
71.14 (C8′), 71.11 (C10), 70.90 (C9′), 70.83 (C10′),
2891, 2364, 1602, 1460, 1408, 1369, 1340, 1300,
67.30 (С11), 67.05 (C11′), 61.87 (C12′), 61.71 (C12).
Найдено, % C 36.14; H 4.46; V 8.52. C36H54O38V2.
1224 (P-O-H), 1201, 1145, 1103, 1076 (P-O-V),
1047 (P-O-C), 1020, 991, 916, 839, 775 (V=O),
Вычислено, %: C 36.12; H 4.51; V 8.52.
702, 646, 601, 553 (V=O), 433, 405. УФ спектр, λ,
Бис(β-глицеро-6-фосфато)бис[(μ2-цитрато)-
нм: 306, 323. Спектр ЯМР 1H (D2O), δ, м. д.: 5.24
оксованадий(V)]тетракалий
(2г).
0.1
г
д (2H, CH2O, 3JHH 7.1 Гц), 5.20 д (2H, CH2O, 3JHH
(0.13 ммоль) комплекса 1 растворяли в 30 мл H2O,
7.3 Гц), 4.81 с (1Н, CHO), 4.76 д (2Н, CH2OP, 3JHP
раствор нагревали до 90°С, затем добавляли 0.09 г
12.2 Гц), 4.52 с (1H, CHO), 4.01 с (1Н, CHO), 3.97
(0.52 ммоль) β-глицерофосфата натрия и кипятили
с (1H, CHO), 3.92 д (2Н, CH2, 3JHH 11.5 Гц), 3.87
при перемешивании 40 мин. Pаствор упаривали,
д (2Н, CH2, 3JHH 8.6 Гц), 3.79 с (1Н, CHO), 3.69 д
образовавшийся осадок отфильтровывали, про-
(2Н, CH2, 3JHH 9.3 Гц), 3.59 с (1Н, CHO), 3.51 д (2Н,
мывали этанолом и сушили. Выход 0.06 г (32%),
CH2, 3JHH 10.7 Гц), 3.46 с (1Н, CHO), 3.36 м (1Н,
голубой порошок, т. пл. 129 °С. ИК спектр, ν, см-1:
COOH), 3.30 с (1Н, CHO). Спектр ЯМР 13С (D2O),
3346, 3217, 2945, 2804, 1666, 1585, 1475, 1444,
δС, м. д.: 94.67 (C1), 94.37 (C1′), 77.29 (C2), 74.22
1398, 1354, 1334, 1284, 1269, 1240 (P-O-H), 1120,
(C3′), 73.97 (C3), 73.30 (C2′), 73.12 (C4′), 72.98 (C4),
1068 (P-O-V), 1049 (P-O-C), 983, 954, 912, 893,
66.41 (C5′), 65.23 (C5), 61.65 (C6′), 61.68 (C6). Най-
771, 700, 621, 518. УФ спектр: λ 270 нм. Спектр
дено, % C 27.94; H 3.46; V 9.90. V2C24H36O34P2 Вы-
ЯМР 1H (D2O), δ, м. д.: 4.03 м (2Н, CH2O), 3.97 м
числено, %: C 27.90; H 3.48; O 52.71; P 6.00; V 9.88.
(2Н, CH2O), 3.57 с (1Н, CHOP), 3.56 д (2Н, CH2O,
Бис(D-мальтолато)бис[(μ2-цитрато)оксова-
3JHH 8.9 Гц), 3.51 д (2Н, CH2O, 3JHH 9.4 Гц), 3.48 с
надий(V)]тетракалий (2в). 0.1 г (0.13 ммоль)
(1Н, CHOP). Спектр ЯМР 13С (D2O), δС, м. д.: 74.86
комплекса
1 растворяли в
25 мл H2O, рас-
(C1), 74.83 (C1′), 74.81 (C1α), 74.79 (C1α′), 62.33 (C2).
твор нагревали до 50°С, затем добавляли 0.07 г
62.30 (C2′), 62.29 (C2α), 62.22 (C2α′). Найдено, % C
(0.20 ммоль) мальтозы и кипятили при перемеши-
25.24; H 3.27; V 11.90. C18H28O28P2V2. Вычислено.
вании 10 мин. Раствор упаривали, образовавший-
%: C 25.23; H 3.27; P 7.24; V 11.91.
ся осадок отфильтровывали, промывали этанолом
ИНФОРМАЦИЯ ОБ АВТОРАХ
и сушили. Выход 0.06 г (20%), серо-фиолето-
вый кристаллический порошок, т. пл. 178°С. ИК
Горкуша Григорий Владимирович, ORCID:
спектр, ν, см-1: 3292, 2924, 2358, 2341, 1589 (C=O),
1446, 1404, 1359, 1199 (C-O), 1143, 1102 (C-O),
Литосов Герман Эдгарович, ORCID: https://
1070, 1014, 990, 920, 900, 844, 669, 781 (V=O), 754,
orcid.org/0000-0001-7851-0148
549 (V=O), 509. УФ спектр: λ 305 нм. Спектр ЯМР
1H (D2O), δ, м. д.: 5.30 д (2H, CH2O, 3JHH 8.1 Гц),
org/0000-0002-8567-4578
5.21 д (2H, CH2O, 3JHH 8.5 Гц), 5.13 д (2H, CH2O,
3JHH 7.9 Гц), 5.10 д (2H, CH2O, 3JHH 6.1 Гц), 4.77
БЛАГОДАРНОСТИ
с (1Н, CHO), 4.56 д (2Н, CH2, 3JHH 9.8 Гц), 4.42 с
(1Н, CHO), 4.12 с (1Н, CHO), 3.95 д (2Н, CH2, 3JHH
Авторы выражают благодарность Инжинирин-
8.7 Гц), 3.93 с (1Н, CHO), 3.87 д (2Н, CH2, 3JHH
говому центру Санкт-Петербургского государ-
10.1 Гц), 3.84 с (1Н, CHO), 3.77 с (1Н, CHO), 3.69
ственного технологического института (техни-
с (1Н, CHO), 3.65 д (2Н, CH2, 3JHH 11.0 Гц), 3.57 с
ческого университета) за проведение ИК и ЯМР
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 9 2021
1458
ГОРКУША и др.
спектральных исследований, а также преподава-
№ 7. С. 516; Fedorova E.V., Rybakov V.B.,
телям кафедры органической химии Санкт-Пе-
Senyavin V.M., Aslanov L.A., Anisimov A.V. // Russ.
тербургского государственного технологического
J. Coord. Chem. 2002. Vol. 28. N 7. P. 483. doi
института (технического университета) и А.А. Фе-
10.1023/A:1016201311785
доришкиной за помощь в написании рукописи.
5. Marzban L., McNeill H. J. // J. Trace Elem. Exp.
Med. 2003. Vol. 16. N 4. P. 253. doi 10.1016/j.
КОНФЛИКТ ИНТЕРЕСОВ
ica.2020.120057
6. Kaliva M., Kyriakakis E., Salifoglou A. // Inorg. Chem.
Авторы заявляют об отсутствии конфликта
2002. Vol. 41. P. 7015. doi 10.1021/ic020323r
интересов.
7. Driss H., Bannani F., Thouvenot R., Debbabi M. // J.
СПИСОК ЛИТЕРАТУРЫ
Soc. Chim. Tunisie. 2010. Vol. 12. P. 173.
8. Neves A., Romanowski S., Bortoluzzi A.J., Mang-
1. Воробьева Н.М., Федорова Е.В., Баранова. Н.И. //
rich A.S. // Inorg. Chim. Acta. 2001. Vol. 313. P. 137.
Биосфера. 2013. Т. 5. №1. С. 77.
doi 10.1016/s0020-1693(00)00379-0
2. Kaliva М., Gabriel С., Raptopoulou A.T., Salifoglou A. //
9. Maurya M.R., Kumar A., Bhat A., Azam A., Bader C.,
Inorg. Chim. Acta. 2008. Vol. 361. P. 2631. doi
Rehder D. // Inorg. Chem. 2006. Vol. 45. P. 1260. doi
10.1016/j.ica.2007.11.014
10.1021/ic050811
3. Shechter Y., Karlish S.J, Karlish D. // Nature. 1980.
Vol. 284. P. 556. doi 10.1038/284556a0
10. Tsaramyrsi M., Kaliva M., Salifoglou A., Raptopoulou
4. Федорова Е.В., Рыбаков В.Б., Сенявин В.М., Асла-
C.P., Terzis A., Tangoulis V., Giapintzakis J. // Inorg.
нов Л.А., Анисимов А.В. // Коорд. хим. 2002. Т. 28.
Chem. 2001. Vol. 40. P. 5772. doi 10.1021/ic010276n
Vanadium(V) Complexes with Some Carbohydrates
and Alcohols
G. V. Gorkusha*, H. E. Litosov, and D. O. Ruzanov
St. Petersburg State Institute of Technology (Technical University), St. Petersburg, 190013 Russia
*e-mail: grigorygor2014@yandex.ru
Received June 16, 2021; revised August 20, 2021; accepted August 22, 2021
The products of the reaction of a citrate binuclear vanadium(IV) complex with glucose-6-phosphate, glucose,
maltose, and glycerol monophosphate were obtained. Structure of the obtained complexes was studied.
Keywords: vanadium, glucose-6-phosphate, vanadium complexes, carbohydrates
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 91 № 9 2021