ЖУРНАЛ ОБЩЕЙ ХИМИИ, 2022, том 92, № 8, с. 1232-1239
УДК 547.24/.259.8
ТИОФОСФОРИЛЗАМЕЩЕННЫЕ НАТРИЕВЫЕ СОЛИ
РИЦИНОЛЕВОЙ КИСЛОТЫ
© 2022 г. Н. П. Шапкина,*, И. Г. Хальченкоа, Н. В. Масловаа, В. Г. Савченкоа,
Э. А. Токарьа,b, Е. М. Заяцa
a Дальневосточный федеральный университет, о. Русский, п. Аякс 10, 690922 Россия
b Институт химии Дальневосточного отделения Российской академии наук, Владивосток, 690022 Россия
*е-mail: npshapkin@gmail.com
Поступило в редакцию 24 февраля 2022 г.
После доработки 28 марта 2022 г.
Принято к печати 29 марта 2022 г.
Исследовано взаимодействие рицинолеата натрия с тиофосфорилтрихлоридом в различных условиях.
При высокой концентрации рицинолеата натрия с тиофосфорилтрихлоридом взаимодействует в первую
очередь спиртовая ОН-группа, в выделенном соединении присутствует натрийацильная группа, что
подтверждено данными ИК, ЯМР 1Н, 13С, 31Р спектроскопии и элементным анализом. При разбавлении
раствора соли в 5 раз реакция протекает по механизму нуклеофильного замещения как по карбоксилат-
ной, так и по спиртовой группе. По данным гель-хроматографии, молекулярная масса продукта реакции
близка к трехзамещенному тиофосфату, состав и структура которого подтверждены элементным анали-
зом и данными ИК, ЯМР 1Н, 13С, 31Р спектроскопии и дифрактометрии. При хроматографировании на
силикагеле он распадается, как при гидролизе в слабокислой среде.
Ключевые слова: рицинолеат натрия, трихлортиофосфат, механизм нуклеофильного замещения, тио-
фосфорилзамещенные полирицинолеаты
DOI: 10.31857/S0044460X22080091, EDN: IOXMAX
Касторовое масло получают из клещевины,
мое для равновесия между реагентом и продуктом
на 90-95% оно состоит из глицерида рициноле-
реакции в системе. Максимальная полимериза-
вой кислоты. Благодаря гидроксильной группе и
ция наблюдается в присутствии 5% катализатора.
двойной связи касторовое масло служит сырьем
Сложный полидодецилат рицинолевой кислоты
для производства косметических и смазочных ма-
получен из касторового масла с довольно высо-
териалов [1]. Из касторового масла в присутствии
ким выходом в две стадии [5]. При его выдержива-
различных катализаторов получают полимеры и
нии при 160°С в атмосфере СО при повышенном
композиты [2, 3]. Были разработаны способы син-
давлении в присутствии кобальтопиридинового
теза полирицинолевой кислоты с использованием
катализатора образуется полимер с высокой мо-
2-этилгексаноата олова(II) в качестве катализатора
лекулярной массой. На основе касторового масла
[4]. Исследована зависимость выделения конден-
получены термопластичные полимеры с исполь-
сационной воды и рекуперации полимера в зави-
зованием катализатора октакарбонилдикобальта
симости от продолжительности реакции, темпера-
Со2(СО)8, а из производных касторового масла и
титаната бария - новые наноструктурированные
туры, природы катализатора. На заключительном
этапе получен полимер с превосходными функци-
пьезоэлектрики [6].
ональными свойствами, который может быть ре-
Касторовое масло и рицинолевая кислота при-
комендован в качестве природного биополимера.
влекают внимание многих исследователей не толь-
Рассчитано количество катализатора, необходи-
ко возможностью получения из них композитов и
1232
ТИОФОСФОРИЛЗАМЕЩЕННЫЕ НАТРИЕВЫЕ СОЛИ
1233
Схема 1.
CH2CH=CH(CH2)7COONa
(S)PCl3 + NaOOC(CH2)7CH=CHCH2CH(OH)(CH2)5CH3
P(S)
O
−3HCl
(CH
2)5CH3
3
полимеров, но также перспективой использования
Нами исследовано взаимодействие натрие-
при производстве биотоплива [7-10], которое по
вой соли рицинолевой кислоты с тиофосфорил
сравнению с петродизелем способно к восстанов-
трихлоридом, которое предположительно проте-
лению, имеет более высокую биоразлагаемость,
кает с образованием сложноэфирной связи по ги-
чем ископаемые виды топлива, нетоксично, харак-
дроксильной группе (схема 1).
теризуется смазочными свойствами, не содержит
Реакцию проводили в спиртово-бензольных
серы и ароматических соединений, не приводит к
растворах при 50°C при соотношениях спирт-бен-
увеличению уровня углекислого газа в атмосфере.
зол 1:1 и 5:1. В обоих случаях выпадал осадок хло-
Сведения об элементоорганических эфирах
рида натрия. После удаления растворителей выде-
рицинолевой кислоты довольно ограничены. При
лены продукты реакции 1 и 2, которые очищали
взаимодействии с силанами рицинолевая кислота
экстракцией петролейным эфиром. Для каждого
образует эфирную связь Si-O-C [11], соли рици-
продукта реакции было выделено по две фракции:
нолевой кислоты, растворимые в органических
А, Б (1) и В, Г (2). Фракции A и В представляли
растворителях, взаимодействуют с тетрахлоридом
собой белые воскообразные вещества, нераство-
кремния с образованием рицинолеатов кремния
римые в петролейном эфире. Фракции Б и Г - бес-
[12, 13].
цветные жидкости, хорошо растворимые в орга-
нических растворителях. В табл. 1 представлены
Эфиры фосфорных кислот достаточно хоро-
выход, элементный анализ и брутто-формулы всех
шо изучены [14-18], в то время как образование
фракций.
эфиров тиофосфорных кислот с высшими жирны-
ми кислотами практически не изучено. Органиче-
Определение молекулярно-массового распре-
ские тиофосфаты относятся к превосходным три-
деления растворимых фракций Б и Г проводили
бодобавкам в машинное масло [14]. Касторовое
в толуоле. Главное соединение фракции B имеет
масло - один из компонентов смазок, но сведения
молярную массу 800-900 ед., на хроматограмме
о тиофосфорилпроизводных касторового масла
фракции Г наблюдаются два максимума с масса-
отсутствуют.
ми 1000 и 600 ед. (рассчитанная молярная масса
Таблица 1. Элементный состав фракций A-Г продуктов синтеза 1 и 2
Найдено, %
Вычислено, %
Фракция
Выход, %
Формула
Na
C
S
P
Na
C
S
P
А
64.5
5.0
58.3
2.9
2.9
5.1
57.9
2.9
2.8
[NaОС(О)С17Н32О]2.5
(ОС17Н32СОО)0.5РS∙6Н2О
Б
18.6
1.4
62.7
3.0
2.7
1.1
62.5
3.1
3.0
(ОС17О32СОО)2.5
[NaOC(OC17Н32О)]0.5∙2Н2О
В
32.8
5.2
62.7
3.0
2.7
5.5
61.8
3.0
2.9
[(NaОС(О)С17Н32О]2.7
(ОС17Н32СОО)0.3РS∙2Н2О
Г
45.9
1.5
62.5
3.1
2.8
1.0
61.8
3.0
2.9
[NaОС(О)С17Н32О]0.4
(ОС17Н32СОО)2.6∙4Н2О
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 92 № 8 2022
1234
ШАПКИН и др.
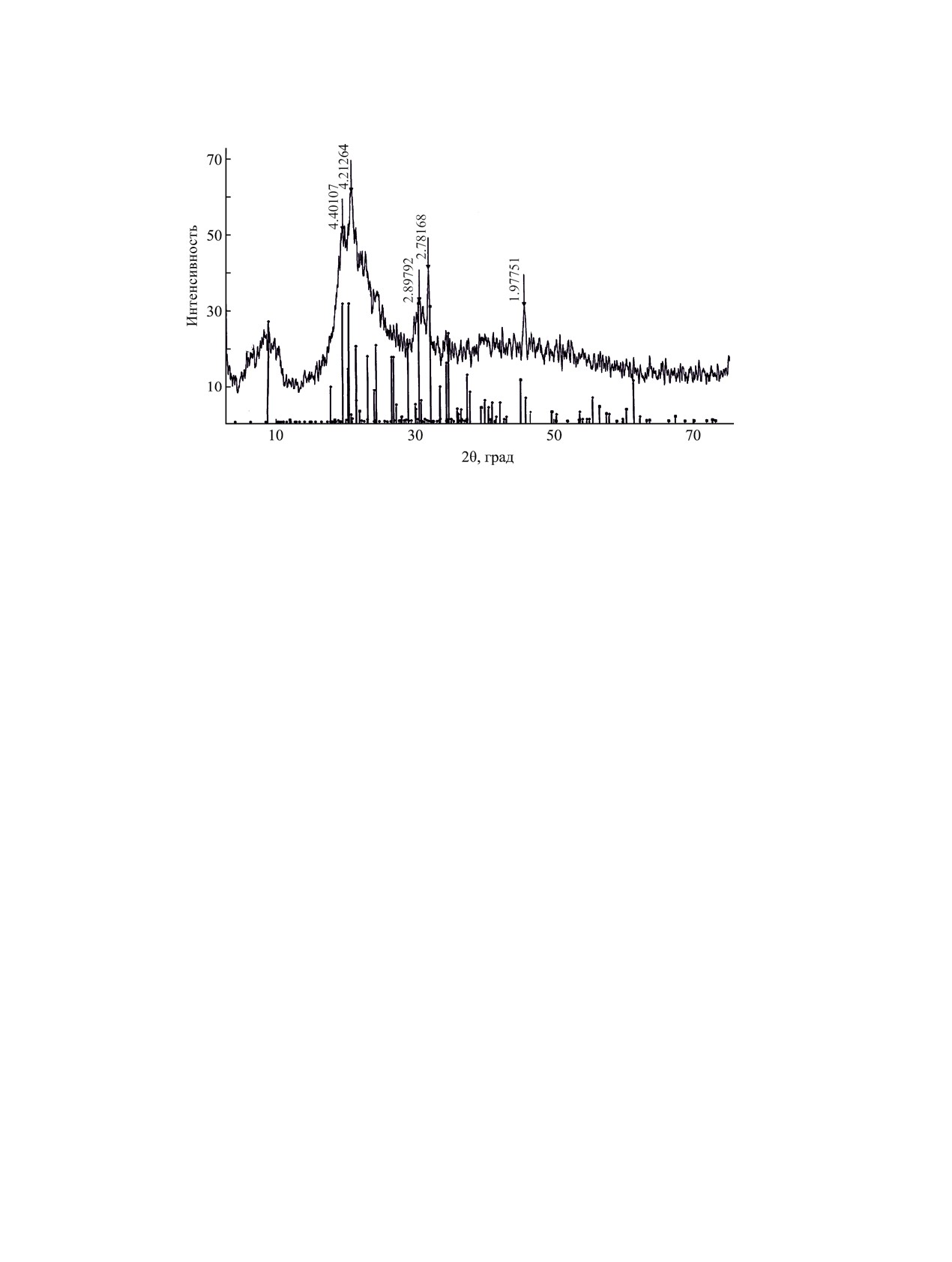
Рис. 1. Дифрактограмма фракции А.
для фракций Б и Г 1050-1130 ед. в зависимости
Для фракций А и Б записаны спектры ЯМР
от количества воды и атомов натрия). Второй пик
23Na в ДМСО. В спектре ЯМР 23Na нераствори-
соответствует молярной массе ди(рицинолеато)ти-
мой фракции А наблюдается сигнал при 2.5 м. д.,
офосфорной кислоте.
в спектре растворимой фракции Б резонанс ядер
натрия наблюдается при 0.5 м. д. Сдвиг в сторону
Для нерастворимой фракции А проведен рент-
генофазовый анализ. Характер дифрактограммы
слабого поля связан с уменьшением координации
соответствует кристаллической соли рицинолеата
иона натрия с карбоксильной группой в тририци-
натрия [13], но количество отражений значительно
нолеат-анионе.
больше (как в слоистой структуре муллита, рис. 1).
Спектры ЯМР 1Н, 13С и 31Р растворимых фрак-
Дифрактограммы воскообразных фракций А и В
ций Б и Г идентичны. В спектрах ЯМР 1Н фрак-
аналогичны между собой [13].
ций Б и Г наблюдается сигнал в диапазоне 0.86-
ИК спектры нерастворимых фракций А, В
0.88 м. д. с интенсивностью 9Н, принадлежащий
идентичны друг другу. В спектрах наблюдаются
протонам группы СН3. В диапазоне 1-4 м. д. на-
полосы поглощения при 645-650 см-1 (валентные
блюдается сигнал протонов алифатических групп
колебания связи P=S), 960-1033 см-1 (колебания
в цепи рицинолевого фрагмента, сигналы в обла-
связи S=P-O-C), 2856-2920 см-1 (валентные ко-
сти 6-5.4 м. д. соответствуют резонансу протонов
лебания связей С-Н в группах СН2 и СН3), 1245,
при двойной связи.
1299, 1375 см-1 (деформационные колебания связи
В спектрах ЯМР 13С фракций Б и Г сигналы в
С-Н). Валентные колебания связи С=О в связан-
области 14.0-36.3 м. д принадлежат атомам угле-
ной эфирной карбоксильной группе наблюдаются
рода в группах СН3 и СН2. В области 60-63 м. д.
в области 1735 см-1, полоса при 1560 см-1 принад-
наблюдается резонанс атома углерода в группе
лежит колебаниям связи С=О в координированной
С-ОН, в области 125, 128-132.5, 132.9 м. д. реги-
группе с ионом натрия [15, 19].
стрируются сигналы групп атомов углерода в двух
ИК спектры растворимых фракций Б и Г так-
различных фрагментах с двойными связями, при
же идентичны друг другу. Главная особенность их
173.7 м. д. - сигнал атома углерода карбоксигруп-
спектров - отсутствие полос поглощения при 1735
пы. В спектре ЯМР 31Р фракции Б фиксируются
и 1560 см-1; полоса при 1710 см-1 соответствует
два сигнала при 67.7 и 57.5 м. д. с соотношением
валентным колебаниям связи С=О в свободной
0.1:1.0. Это свидетельствует о присутствии приме-
карбоксильной группе.
си в количестве 10%.
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 92 № 8 2022
ТИОФОСФОРИЛЗАМЕЩЕННЫЕ НАТРИЕВЫЕ СОЛИ
1235
Схема 2.
S
S
S
HO
P1
OC18
HO
P2
OC18
C18O
P3
OC18
OH
OC18
OC18
O
C18 = CH3(CH2)5CHCH2CH=CH(CH2)7COOH
Схема 3.
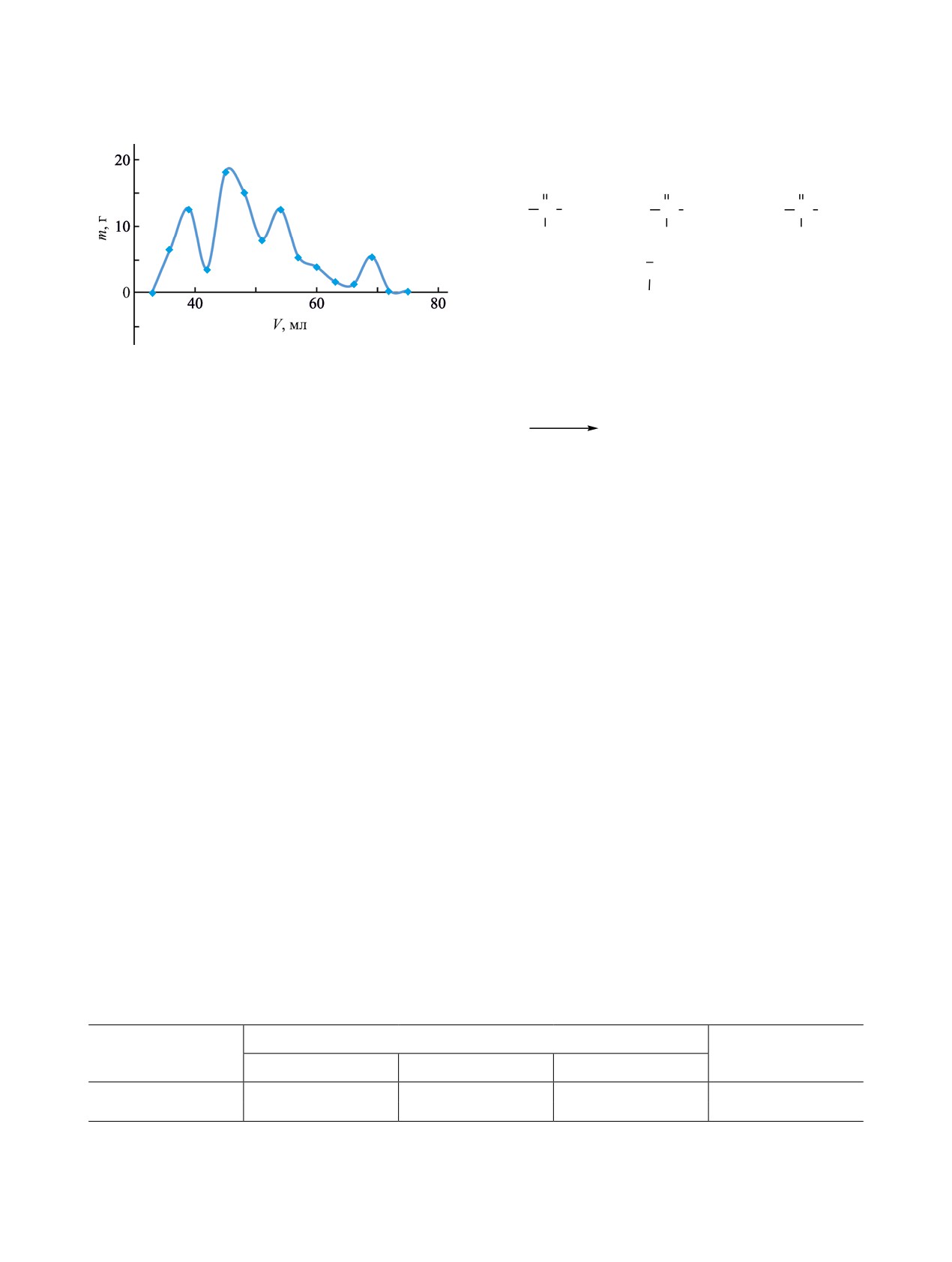
Рис. 2. Гель-хроматограмма фракции Д.
(C18H32O3Na)3P(S) + H2O
3HCl
Для нерастворимых фракций А и В записаны
(C18H32O3H)2P(S)OH + C18H34O3
-3NaCl
твердотельные спектры ЯМР 31Р. В спектре наблю-
дается интенсивный сигнал при 57 м. д. и слабый
сигнал при 68.3 м. д. Исходя из данных ЯМР 31Р,
1735-1560 см-1 наблюдается полоса свободной
можно предположить несколько вариантов окру-
карбоксильной группы при 1710 см-1. Интенсив-
жения атома фосфора: Р1 - 67-68, Р2 - 63-64,
ность полосы колебаний связи P=S [14] снижает-
Р3 - 57 м. д. (схема 2).
ся, и появляется полоса связи P=О при 1282 см-1
Для определения состава фракций Б и Г, рас-
[18], т. е. после взаимодействия фракций Д и Е с
творимых в толуоле, проведена тонкослойная хро-
поверхностью силикагеля протекает гидролиз с
матография. На хроматограмме наблюдались два
перераспределением атомов в окружении атома
пятна: одно оставалось на старте, второе имело Rf
фосфора.
0.3. После пропускания фракций Б и Г через слой
Для выяснения строения нерастворимых фрак-
силикагеля выделены фракции Д и Е (табл. 2).
ций А и В был проведен гидролиз фракции А 2%-
На гель-хроматограмме фракции Д наблюдалось
ным раствором соляной кислоты (схема 3) с после-
большое число пиков (рис. 2). Такое количество
дующей экстракцией эфиром продукта гидролиза.
пиков на гель-хроматограмме связано с разруше-
нием эфирной связи С-О-Р(S) при взаимодей-
После отгонки эфира был выделен продукт ги-
ствии с гидроксильными группами на поверхно-
дролиза Ж (найдено, %: С 66.9; S 2.9; Р 1.9). Из
сти силикагеля, так как связь элемент-кислород в
фракции В аналогично получен гидролизат З. По
карбоксигруппе легко разрушается под действием
данным гель-хроматографии продукта гидролиза
кислоты [13]. Это подтверждается снижением со-
Ж, молекула тиофосфорилпроизводного рицино-
отношения серы к фосфору, которое колеблется
левой кислоты разрушается, о чем свидетельству-
от 1.5 до 2 (табл. 2), и образованием соединений с
ет образование нескольких соединений с различ-
различными молярными массами.
ными молярными массами.
ИК спектры фракций Д и Е имеют более про-
В ИК спектре гидролизата Ж появляется по-
стую структуру. Вместо трех полос в области
лоса С=О в свободной карбоксильной группе
Таблица 2. Элементный состав фракций Д и Е
Найдено, %
Фракция
Выход, %
С
Р
S
Д
69.9
1.4
2.2
43.3
Е
69.2
1.5
2.2
25.1
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 92 № 8 2022
1236
ШАПКИН и др.
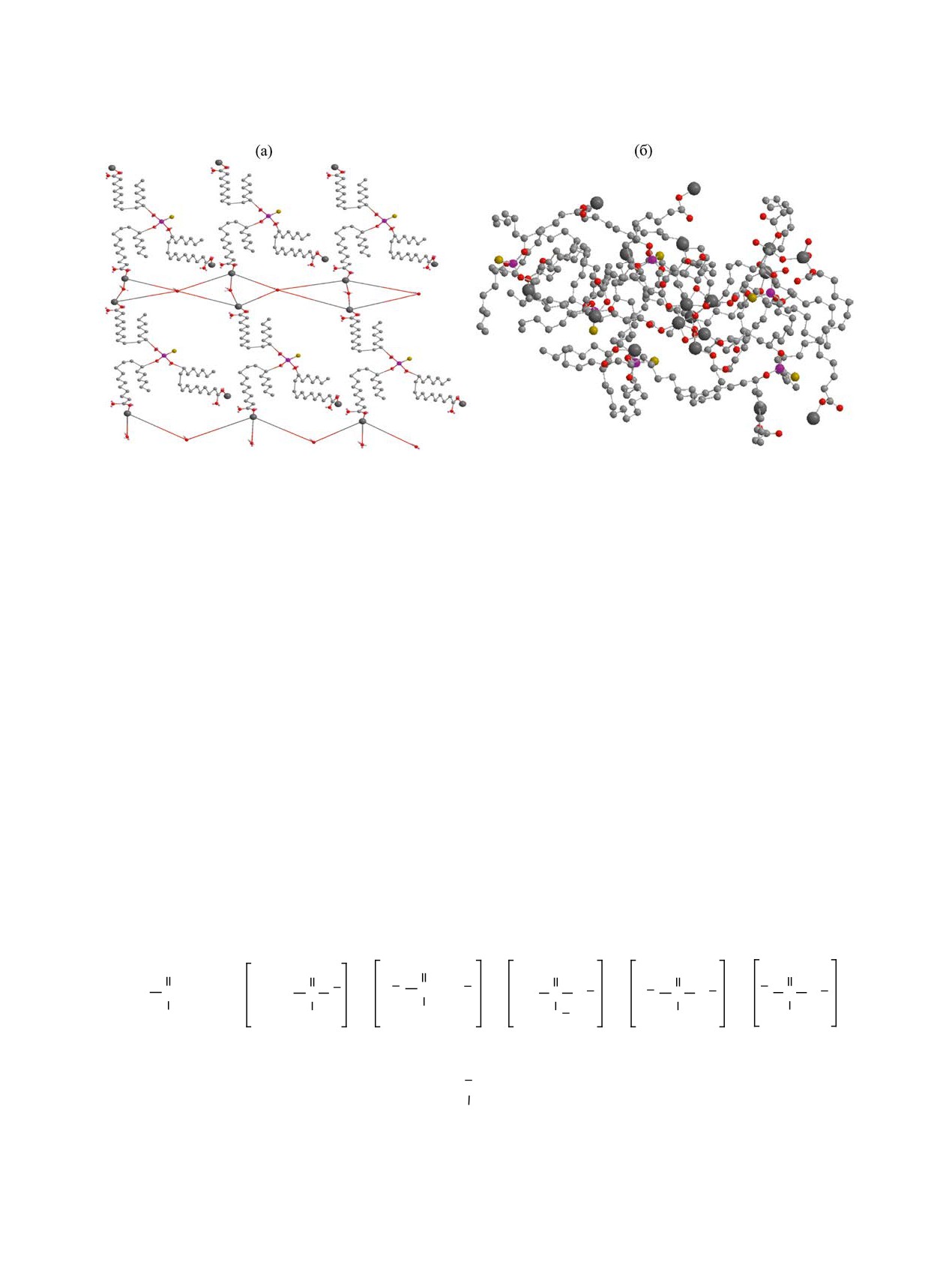
Рис. 3. Структура поли-12О,12О′,12О′′-тиофосфорилтрис(рицинолеата натрия). (а) - упаковка в двухмерном пространстве,
(б) - упаковка в трехмерном пространстве.
при 1708-1710 см-1 в результате разрыва связи
лиэфирной конденсации [4], при этом получаются
(S)P-C(O), а также полоса при 1280-1290 см-1
фрагменты полимерной цепи (рис. 3). Различие
(связь P=О [18]). В спектрах ЯМР 31Р гидролиза-
полимеров, образовавшихся после гидролиза или
тов Ж и З наблюдаются сигналы при 63.8, 67.0 м. д.
хроматографирования, заключается в количестве
рицинолеатных групп в брутто-формуле (схема 6).
и сигналы меньшей интенсивности при 29, 19, 0.9,
0.36 м. д., которые принадлежат атомам фосфора в
Таким образом, при взаимодействии тиофос-
различном окружении (схема 4).
форилтрихлорида с натриевой солью рицинолевой
кислоты в смесях спирт-бензол, 1:1 и 5:1, полу-
Появление в спектре ЯМР 31Р сигналов при
чены два полимера, которые различается количе-
26, 20, 19, 0.9, 0.4 м. д. обусловлено протеканием
ством натрия, уменьшающимся с увеличением
побочных реакций (схема 5) [14, 21, 22]. Присо-
соотношения спирт-бензол, и вариантами окруже-
единение интермедиата HSC18 по двойной связи
ния пятивалентного атома фосфора в тригональ-
в рицинолеат-ионе [22] приводит к образованию
ной пирамиде. Реакция протекает как по спирто-
сульфанилпроизводных.
вому гидроксилу, так и по натрийкарбоксигруппе.
В результате гидролиза или пропускания через
Полимеры, содержащие натрий, имеют слоистую
слой силикагеля образуются полимеры за счет по-
структуру, легко гидролизуются в слабокислой
Схема 4.
S
S
O
O
O
O
C18
P SC18
C
18Na
P C18Na
C18Na
P
O
HO
P
C18
C18
P
C18
O
P
C18
OH
OH
18
C
C18
OH
OH
n
n
n
n
n
63.8-64.0 м. д.
67.0 м. д.
29.0 м. д.
19.0 м. д.
0.9 м. д.
0.4 м. д.
O
C18 = CH3(CH2)5CHCH2CH=CH(CH2)7COOH
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 92 № 8 2022
ТИОФОСФОРИЛЗАМЕЩЕННЫЕ НАТРИЕВЫЕ СОЛИ
1237
Схема 5.
NaC18PS + H2O → NaOH + (HC18O)2PSOH + C18H
R1
O
S
R1
R2
R2
(C18)2
P
H+
C18
P S
O
C18
O
O
S
P
C18
+
NaOH
C18
P OH+
HSC18
C
18
C
18
C18
X
X
P
+
HSC18
P
(R2HC=HCR1)2
OH
[R2(C18S)HCH2CR1]2
OH
O
C18 = CH3(CH2)5CHCH2CH=CH(CH2)7COOH; X = S, O; R1 = C7(OH)CH2,
R2 = C7COONa, CH=CHCOOH.
Схема 6.
{[(C18)x(SC18)2 P(O)9]y[(C18)x P(S)]1-y}n
OH
x = 2, 3, 4.
Для полимера c х = 4, у = 0.33 (0.2 до 1) найдено, %: С 70.5; S 1.8; Р 1.3; вычислено, %: С 69.9; S 2.2; Р 1.5. Для
полимера c х = 6, у = 0.5 найдено, %: С 68.5; S 2.2; Р 1.4; вычислено, %: С 68.5; S 2.5; Р 1.6.
среде с образованием полимеров с сульфанильны-
ент - толуол. Калибровку колонки проводили по
ми группами, различающихся вариантами окруже-
триметилтрифенилциклотрисилоксану (408 ед.),
ния атомов фосфора.
трис(ацетилацетату) хрома (350 ед.), октавинил-
циклосилсесквиоксану (632 ед.), октафенилцикло-
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
силсесквиоксану (1030 ед.).
Реактивы: ацетон (ЧДА), касторовое масло, то-
Рицинолеат натрия. Использовали касторовое
луол, диэтиловый эфир - перед синтезом перего-
масло высокой чистоты медицинского назначения.
няли, этиловый спирт сушили над металлическим
К 60 мл (0.058 моль) триглицирида рицинолевой
кальцием.
кислоты приливали 100 мл водного раствора ще-
ИК спектры образцов в KBr записаны на при-
лочи (4.6 г, 0.12 моль) и 200 мл ацетона. Раствор
боре PerkinElmer-1000. Рентгенофазовый анализ
нагревали и перемешивали несколько минут. Если
(РФА) проводили на приборе Advance D-8. Спек-
масло не растворялось полностью, добавляли во-
тры ЯМР записывали на приборе Bruker для ядер
дный раствор NaOH (2.3 г в 50 мл воды). Получен-
1Н (400.13МГц), 13С (100.61 МГц) в ДМСO-d6.
ный раствор приливали к 800 мл ацетона. Выпав-
Для гель-хроматографии использовали колонку
шие бесцветные кристаллы отделяли вакуумным
высотой 1 м и диаметром 1 см. Колонку заполняли
фильтрованием, промывали ацетоном. После про-
полистиролом, сшитым 2% дивинилбензола, элю-
мывания из фильтрата продолжали выпадать кри-
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 92 № 8 2022
1238
ШАПКИН и др.
сталлы. Общий выход 15.3 г (85%). Количество
КОНФЛИКТ ИНТЕРЕСОВ
натрия определяли обратным титрованием. Най-
Авторы заявляют об отсутствии конфликта
дено, %: С 60.2; Na 6.8. C18H33NaO3∙2H2O. Вычис-
интересов.
лено, %: С 60.6; Na 6.4.
Тиофосфорилтрихлорид. К 62.41 г (0.3 моль)
СПИСОК ЛИТЕРАТУРЫ
PCl5 порциями прибавляли 22.2 г пентасульфида
1.
Danlami J.M., Arsad A.В., Zaini M.A.A. // J. Taiwan
дифосфора и нагревали, пока смесь не станови-
Inst. Chem. Eng. 2015. Vol. 47. P. 99. doi 10.1016/j.
лась жидкой. Полученный PSCl3 перегоняли при
jtice.2014.10.012
120-129°С, затем еще раз при 124-125°С. Выход
2.
Scholz V., da Silva J.N. // Biomass & Bioenergy. 2008.
80%.
Vol. 32. N 2. P. 95. doi 10.1016/j.biombioe.2007.08.004
Трис(рицинолеат) тиофосфата. а. В 50 мл
3.
Долгов Б.Н. // ЖОХ. 1954. T. 24. С. 861.
спирта растворяли 19.2 г рицинолеата натрия при
4.
Vadgama R.N., Anil A., Lali A.M. // Heliyon. 2019. N 5.
нагревании до 50°С и интенсивном перемешива-
P e01944. doi 10.1016/j.heliyon.2019.e01944
нии. После полного растворения соли приливали
по каплям 3.39 г. (0.02 моль) PSCl3, растворенного
5.
Quinzler D., Mecking S. // Chem. Commun. 2009. N 36.
в 50 мл бензола, в течение 1 ч. Раствор оставляли на
P. 5400. doi 10.1039/b912294j
18 ч. Образовавшийся эфир пятивалентного фос-
6.
Tang D., Liangsheng Q., Zheng J., Weimin C. // J. Appl.
фора 1 хорошо растворим в смеси бензол-спирт,
Polymer Sci. 2002. Vol. 84. N 4. P. 709. doi 10.1002/
1:1. Осадок хлорида натрия отфильтровывали и
app.10024.abs
взвешивали. Масса хлорида натрия 2.7 г, выход
7.
Martini N., Sсhell J.S. // Plant Oils as Fuels. Berlin:
70%. Растворитель упаривали на роторном испа-
Spinger, 1998. P. 276.
рителе при пониженном давлении, остаток высу-
8.
Demirbas А. // Energy Convers. Manage. 2009. Vol. 50.
шивали в вакуумном шкафу до постоянной массы.
P. 14. doi 10.1016/j.enconman.2008.09.001
б. Реакцию в смеси бензол-спирт, 1:5, проводи-
9.
Ma F., Hanna M.A. // Bioresour. Technol. 1999.
ли аналогично. Смешивали 19.2 г рицинолеата на-
Vol. 70. P. 1.
трия и 250 мл спирта. После полного растворения
10.
Keera S.T., El Sabagh S.M., Taman A.R. // Egypt.
соли к раствору приливали раствор 3.39 г PSCl3
J. Petrol. 2018. Vol. 27. P. 979. doi 10.1016/j.
в бензоле. Раствор оставляли на 18 ч. Образовав-
ejpe.2018.02.007
шийся эфир пятивалентного фосфора 2 хорошо
11.
Boyer F., Post H.J. // Org. Chem. 1952. Vol. 17.
растворим в смеси бензол-спирт, 1:1. Осадок хло-
P. 1389. doi 10.1021/jo50010a019
рида натрия отфильтровывали и взвешивали. Мас-
12.
Pat. 1918338 (1933). Germany.
са хлорида натрия 2.7 г, выход 70%. Растворитель
упаривали на роторном испарителе при понижен-
13.
Шапкин Н.П., Хальченко И.Г., Маслова Н.В., Грибо-
ном давлении, остаток высушивали в вакуумном
ва В.В., Савченко В.Г. // Изв. АН. Сер. xим. 2020.
шкафу до постоянной массы.
№ 7. С. 1385; Shapkin N.P., Khalchenko I.G., Maslova
N.V., Gribova V.V., Savchenko V.G. // Russ. Chem.
ИНФОРМАЦИЯ ОБ АВТОРАХ
Bull. 2020. Vol. 69. N 7. P. 1385. doi 10.1007/s11172-
020-2913-5
Шапкин Николай Павлович, ORCID: https://
14.
Пурдела Д., Вылчану Р. Химия органических соеди-
orcid.org/0000-0002-4287-8917
нений фосфора. М.: Химия, 1972. 752 с.
Хальченко Ирина Григорьевна, ORCID: https://
15.
Исмаилов В.М., Зыкова Т.В., Москва В.В., Новру-
orcid.org/0000-0002-5541-2200
зов С.А., Разумов А.И., Ахмедов Ш.Т., Салахутди-
Маслова Наталья Валерьевна, ORCID: https://
нов Р.А. // ЖОХ. 1973. Т. 43. № 6. С. 1247.
orcid.org/0000-0002-1814-0234
16.
Ismailov V.M., Aydin A., Kantaeva M.M. / /
Савченко Вячеслав Георгиевич, ORCID: https://
Phosphorous, Sulfur, Silicon. 1999. Vol. 149. P. 137.
orcid.org/0000-0001-8430-6194
doi 10.1080/10426509908037028
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 92 № 8 2022
ТИОФОСФОРИЛЗАМЕЩЕННЫЕ НАТРИЕВЫЕ СОЛИ
1239
17. Аллахвердиева Г.Э., Исмаилов В.М., Мамедов И.А.,
20. Кутырев Г.А., Кашура А.А., Черкасов Р.А., Пудо-
Гасымов Р.А., Ахундова М.А., Юсубов Н.Н. // Kimya
вик А.Н. // ЖОХ. 1985. T. 55. Вып. 10. С. 2162.
Problemleri. 2019. Vol. 17. N 3. P. 450.
18. Lira L.M., Vasilev D., Pilli R.A., Wessjohann L.A. //
21. Кабачник М.И., Мастрюкова Т.А., Курочкин Н.И. //
Tetrahedron Lett. 2013. Vol. 54. P. 1690. doi 10.1016/j.
ЖОХ. 1956. Т. 26. С. 2228.
tetlet.2013.01.059
19. Казицина Л.А., Куплетская Н.Б. Применение ИК,
22. Оаэ С. Химия органических соединений серы. М.:
ЯМР-спектроскопии в органической химии. М.: ВШ,
1971. 264 с.
Химия, 1975. 512 с.
Thiophosphorus-Containing Sodium Salts of Ricinoleic Acid
N. P. Shapkina,*, I. G. Khal’chenkoa, N. V. Maslovaa, V. G. Savchenkoa,
E. A. Tokara,b, and E. M. Zayatsa
a Far Eastern Federal University, Vladivostok, 690922 Russia
b Institute of Chemistry, Far Eastern Branch of the Russian Academy of Sciences, Vladivostok, 690022 Russia
*e-mail: npshapkin@gmail.com
Received February 24, 2022; revised March 28, 2022; accepted March 29, 2022
The reaction of sodium ricinoleate with thiophosphoryl trichloride under various conditions was studied. At
a high concentration of sodium ricinoleate, thiophosphoryl trichloride reacts primarily with the alcohol OH
group, and the isolated compound contains a sodium acyl group, which was confirmed by IR, 1H, 13C, 31P NMR
spectroscopy and elemental analysis data. When the salt solution is diluted 5 times, the reaction proceeds by
the mechanism of nucleophilic substitution both on the carboxylate and on the alcohol group. According to gel
chromatography data, the molecular weight of the reaction product is close to trisubstituted thiophosphate, the
composition and structure of which are confirmed by elemental analysis and IR, 1Н, 13С, 31Р NMR spectroscopy
and diffractometry data. During chromatography on silica gel, it decomposes, as during hydrolysis in a slightly
acidic medium.
Keywords: sodium ricinoleate, trichlorothiophosphate, nucleophilic substitution mechanism, thiophosphor-
yl-substituted polyricinoleates
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 92 № 8 2022