ЖУРНАЛ ОБЩЕЙ ХИМИИ, 2023, том 93, № 4, с. 507-515
УДК 547.883
СИНТЕЗ ТЕТРАЗИНИЛЬНЫХ БИРАДИКАЛОВ,
СОДЕРЖАЩИХ п-ФЕНИЛЕНОВЫЙ ФРАГМЕНТ
© 2023 г. С. Г. Кострюков1,*, А. А. Буртасов1, А. В. Долганов1, А. Ш. Козлов1,
И. А. Конушкин1, Н. А. Малов1, А. Д. Краснов1, А. Ю. Асфандеев1
1 Национальный исследовательский Мордовский государственный университет имени Н. П. Огарёва,
ул. Большевистская 68, Саранск, 430005 Россия
*e-mail: kostryukov_sg@mail.ru
Поступило в редакцию 21 декабря 2022 г.
После доработки 25 февраля 2023 г.
Принято к печати 1 марта 2023 г.
Перхлораты 3,3′-(1,4-фенилен)бис[1-(4-R-фенил)-5-фенил-5,6-дигидро-1,2,4,5-тетразиния] действием
D-глюкозы в слабощелочной среде (NH4OH) в присутствии кислорода воздуха были превращены в
соответствующие тетразинильные бирадикалы, которые были выделены в индивидуальном состоянии
и охарактеризованы данными циклической вольтамперометрии, элементного анализа, ИК, УФ, ЭПР
спектроскопии.
Ключевые слова: 5,6-дигидро-1,2,4,5-тетразинийперхлорат, 1,2,3,4-тетрагидро-1,2,4,5-тетразинил,
вердазильный радикал, циклическая вольтамперометрия, спектроскопия ЭПР
DOI: 10.31857/S0044460X23040029, EDN: ATFBUF
Тетразинильные радикалы (вердазилы), впер-
внутримолекулярными обменными взаимодей-
вые описанные в 1964 г. Куном и Тришманом [1],
ствиями и магнитными свойствами имеют зна-
продолжают привлекать внимание исследовате-
чительный потенциал для современных техноло-
лей своей высокой химической стабильностью,
гических приложений и фундаментальной науки
структурным разнообразием и разностороннему
[10]. Стабильные ди- и полирадикалы могут ис-
применению [2, 3]. Так, на основе вердазильных
пользоваться в качестве рабочих элементов спин-
радикалов получены координационные соедине-
тронных устройств [11, 12], многофункциональ-
ния с различными металлами [4, 5]. Интерес к ме-
ных магнитных материалов на основе молекул и
таллокомплексам вердазилов обусловлен тем, что
квантовых машин [13], но несмотря на очевидные
гибкость молекулярных орбиталей в вердазиль-
успехи в химии бирадикалов, стабильные на воз-
ном радикале позволяет настраивать молекуляр-
духе три- и полирадикалы все еще являются экзо-
ные магнитные взаимодействия, а введение атома
тическими соединениями.
металла дает возможность значительно менять
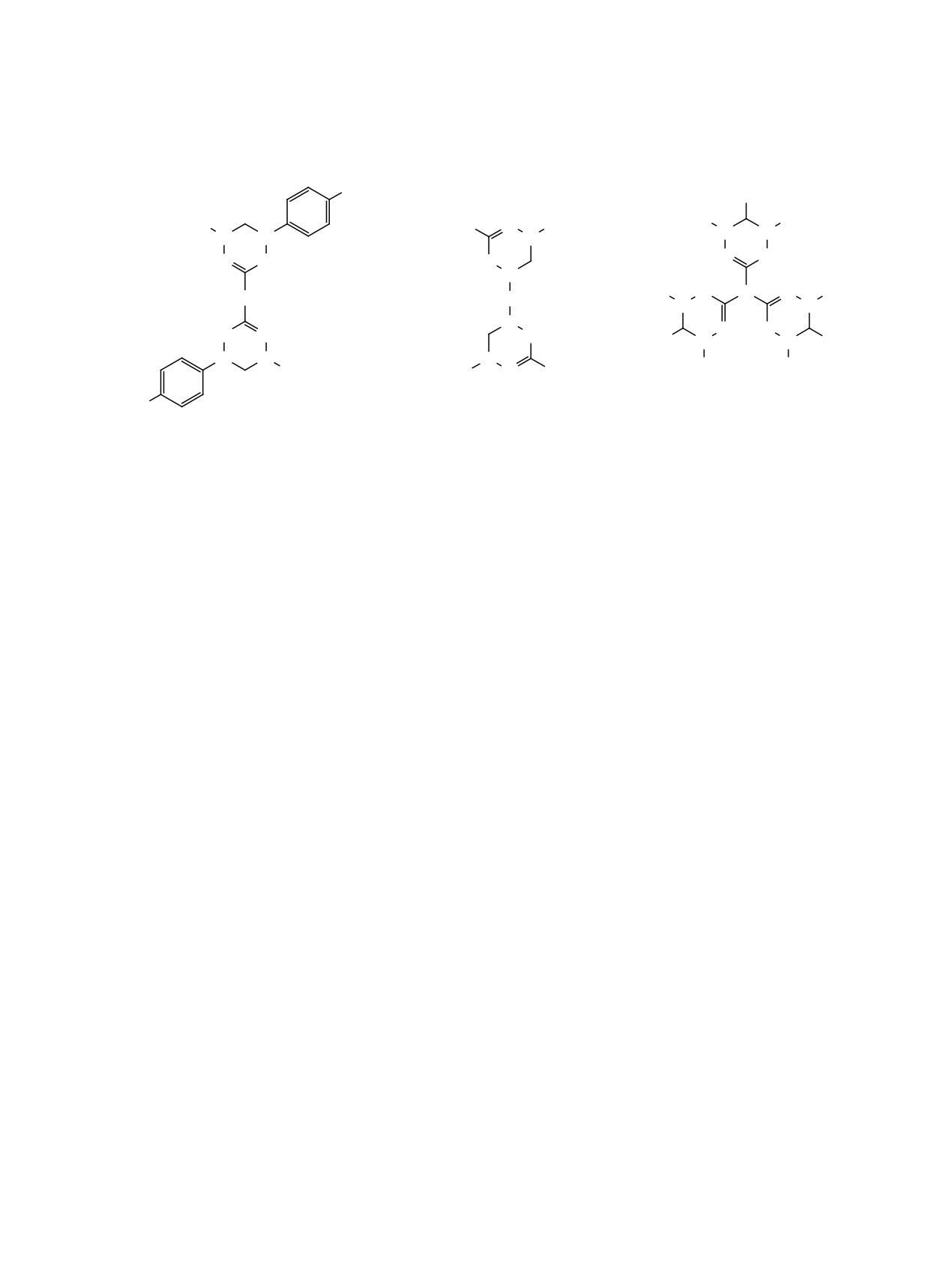
Впервые стабильные вердазильные би- и три-
магнитное поведение лигандов и получать си-
радикалы были получены Куном и сотр. [14]
стемы новыми свойствами [5, 6]. Бирадикальные
(схема 1).
системы перспективны благодаря наличию в них
дополнительных центров координации, что позво-
В дальнейшем данные радикалы являлись
ляет использовать их для синтеза мультиспиновых
объектами квантово-химических исследований
структур [7--9].
[15-17] и экспериментальных исследований маг-
π-Сопряженные органические высокоспиновые
нитных свойств [18, 19], а также изучалось при-
молекулы (ди- и полирадикалы) с существенными
менение одного из них в качестве бирадикального
507
508
КОСТРЮКОВ и др.
Схема 1.
R1
R2
Ph
Ph
Ph
Ph
N
Ph
N
N
N
N
N
•
N
N•
N N•
N
N
Ph
N•
Z
N
Ph
X
Y
N
N
•
N
•
N
N•
HN
N
N
R2
N
N
R2
N N
N
Ph
Ph
Ph
Ph
N
Ph
Z = 1,3,5-C6H3;
R1
Y = 4,4'-бифенил
R2 = H, Me, Bn
X = p-C
6H4, m-C6H4; R1 = H, Me, MeO
зонда для резонансного исследования фосфоли-
на суспензию перхлоратов
5,6-дигидро-1,2,4,5-
пидных мембран [20].
тетразиния 2a-е D-глюкозы в присутствии NH4OH
(схема 3).
Следует отметить, что бирадикалы Куна с дру-
гими заместителями в настоящее время не описа-
Данная реакция сопровождалась постепен-
ны. Таким образом, было бы интересно синтези-
ным изменением цвета: в большинстве случаев
ровать ряд подобных бирадикалов с различным
с темно-фиолетового на изумрудно-зеленый, за
набором заместителей, с целью исследования
исключением солей 2д, е, содержащих циано- и
влияния природы заместителя, например, на их
нитрогруппы (в этих случаях цвет изменялся на
электрохимические свойства. Тем более, что ранее
коричневый). Все вердазильные бирадикалы 1a-е
было показано [21], что заместители в фенильных
были выделены в индивидуальном виде с помо-
щью флеш-хроматографии, охарактеризованы с
фрагментах вердазилов Куна влияют на величину
использованием ИК, УФ и ЭПР спектроскопии.
электрохимической щели, которая важным пара-
Соединения 1a-г представляют собой мелкокри-
метром, определяющим емкость аккумулятора на
сталлические вещества темно-зеленого цвета,
основе нейтральных радикалов [22].
кроме циано- (1д) и нитропроизводных (1е), име-
В данной работе мы обратились к синтезу и из-
ющих темно-коричневую окраску. В ИК спектрах
учению электрохимических свойств вердизильных
вердазилов 1a-е присутствует полоса колебаний в
бирадикалов, имеющих в качестве спейсера, раз-
области ~1150-1160 см-1, характерная для тетраз-
деляющего вердазильные фрагменты, п-фенилено-
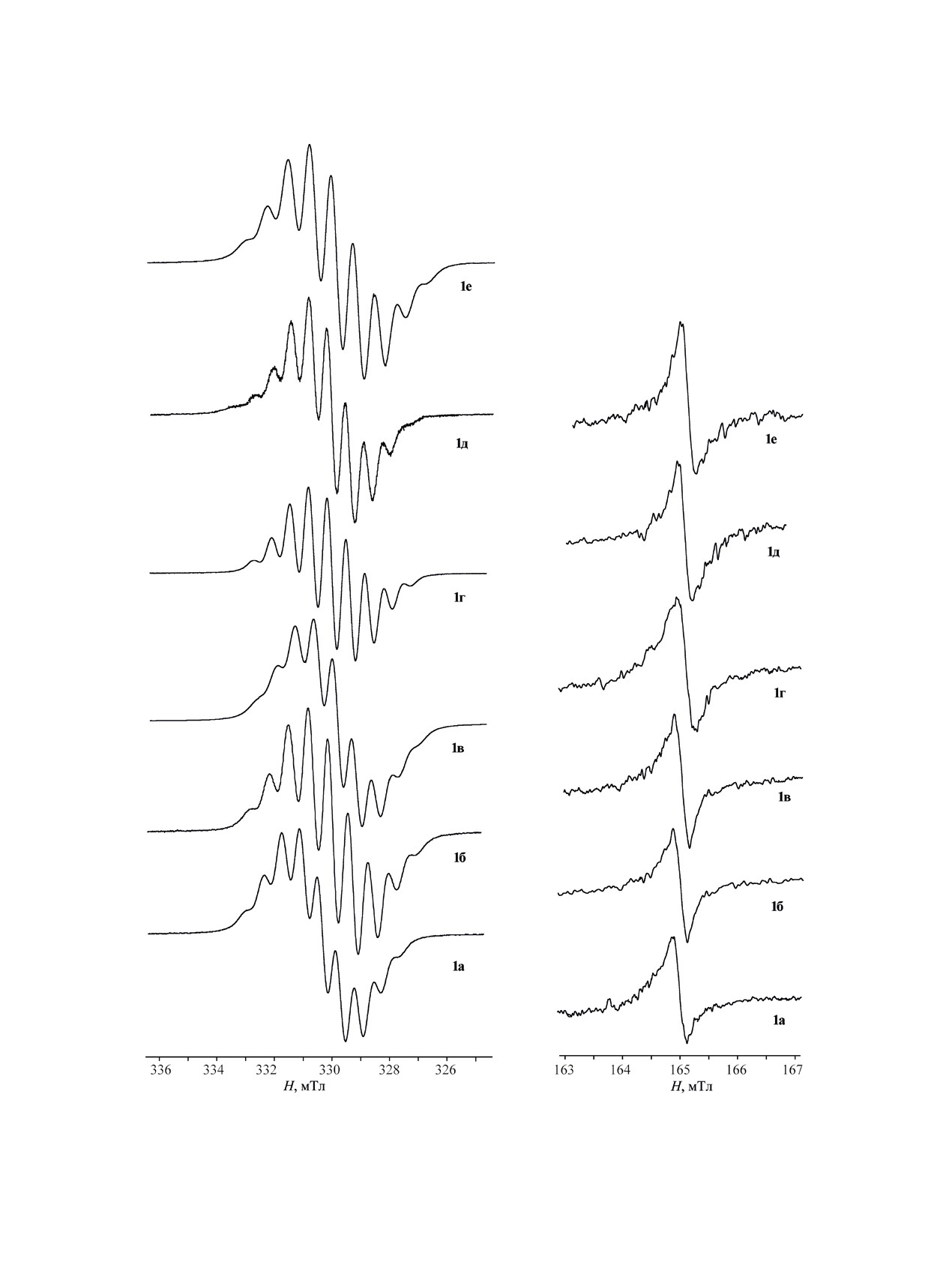
инильного фрагмента [1]. Бензольные растворы
вый фрагмент. В качестве объектов исследования
радикалов 1a-е дают устойчивые во времени спек-
была выбрана серия вердазильных бирадикалов
тры ЭПР, содержащие 9 широких линий, вызван-
1a-е, различающихся заместителями в пара-поло-
ным взаимодействием неспаренного электрона с
жениях фенильных фрагментов у атома N2 3,4-ди-
четырьмя атомами азота тетразинового кольца [1]
гидро-1,2,4,5-тетразинильного цикла.
(рис. 1). Бирадикальная природа соединений 1a-е
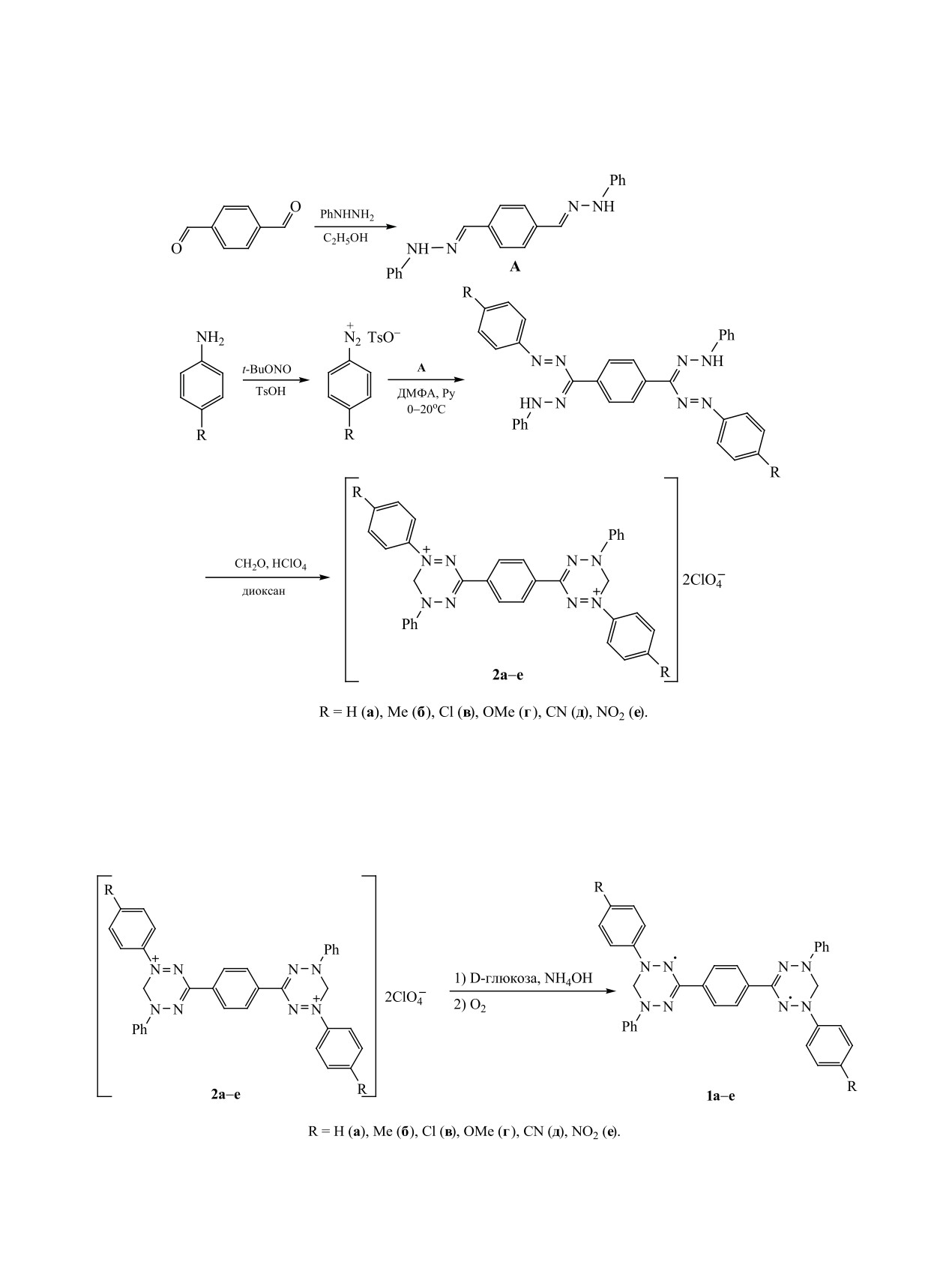
Вердазильные радикалы
1a-е получали по
дополнительно подтверждается обнаружением
методике [23] из соответствующих биядерных
слабых ЭПР сигналов отвечающих запрещенным
перхлоратов тетразиния 2a-е, синтез которых был
∆Ms = 2 переходам.
описан ранее [24] (схема 2).
Электрохимические свойства радикалов 1a-е
Вердазильные бирадикалы 1а-е получали в
исследовали методом циклической вольтамперо-
двухфазной системе EtOAc-H2O при действии
метрии в ацетонитриле с использованием в каче-
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 93 № 4 2023
СИНТЕЗ ТЕТР
АЗИНИЛЬНЫХ БИРАДИКАЛОВ
509
Схема 2.
Схема 3.
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 93 № 4 2023
510
КОСТРЮКОВ и др.
Рис. 1. Спектры ЭПР вердазилов 1а-е в бензоле при 25°C.
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 93 № 4 2023
СИНТЕЗ ТЕТР
АЗИНИЛЬНЫХ БИРАДИКАЛОВ
511
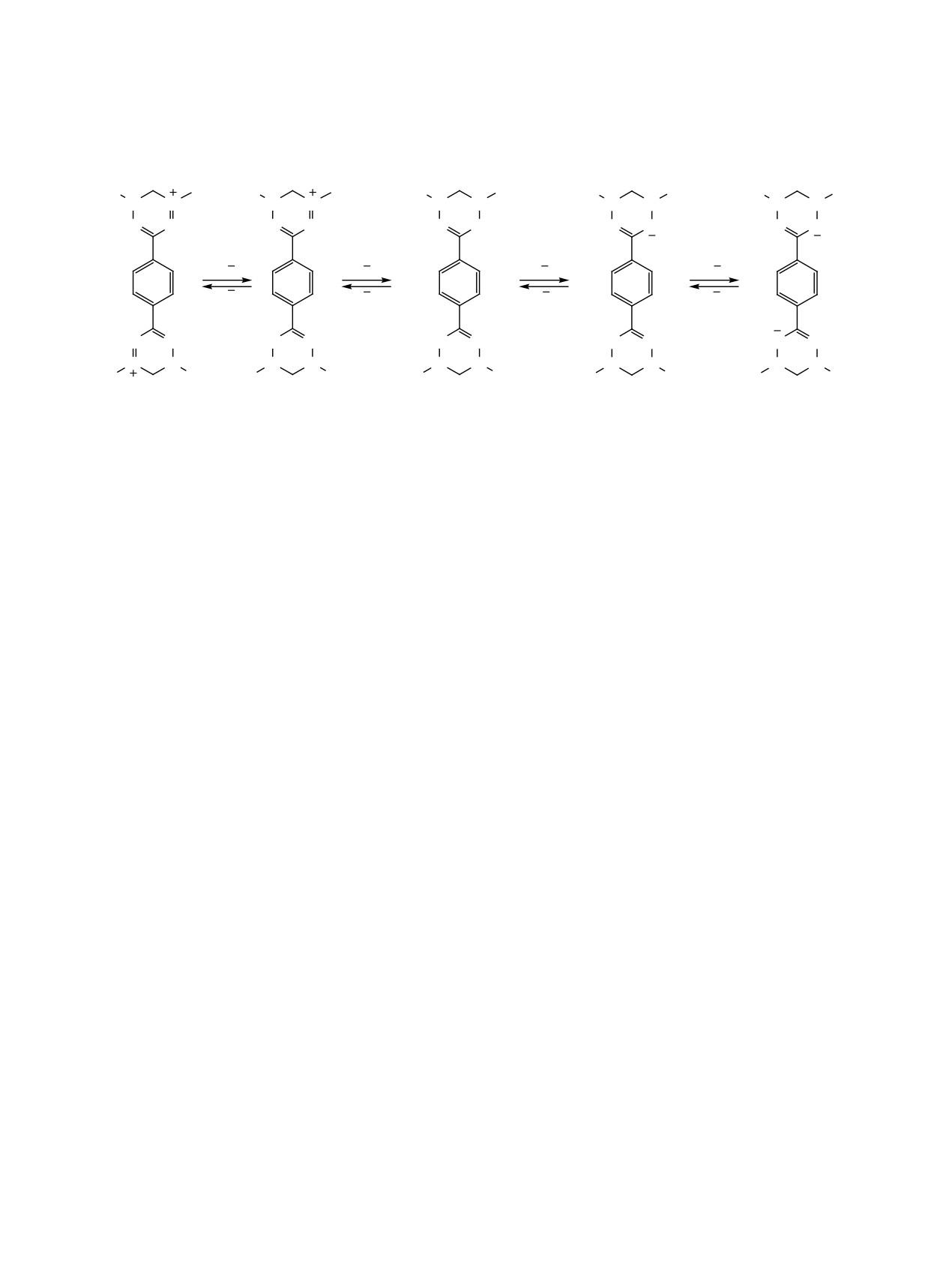
цикловольтамперограммы наблюдается появ-
ление обратимых волн как при окислении, так и
при восстановлении. В цикловольтамперограмме
бирадикалов 1а-д наблюдается образование четы-
рех обратимых волн, которые в анодной области
соответствуют последовательному их окислению
до катион-радикала К1 и далее до дикатиона К2,
в катодной области последовательному восстанов-
лению бирадикала до анион-радикала А1, а затем
до дианиона А2 (схема 4).
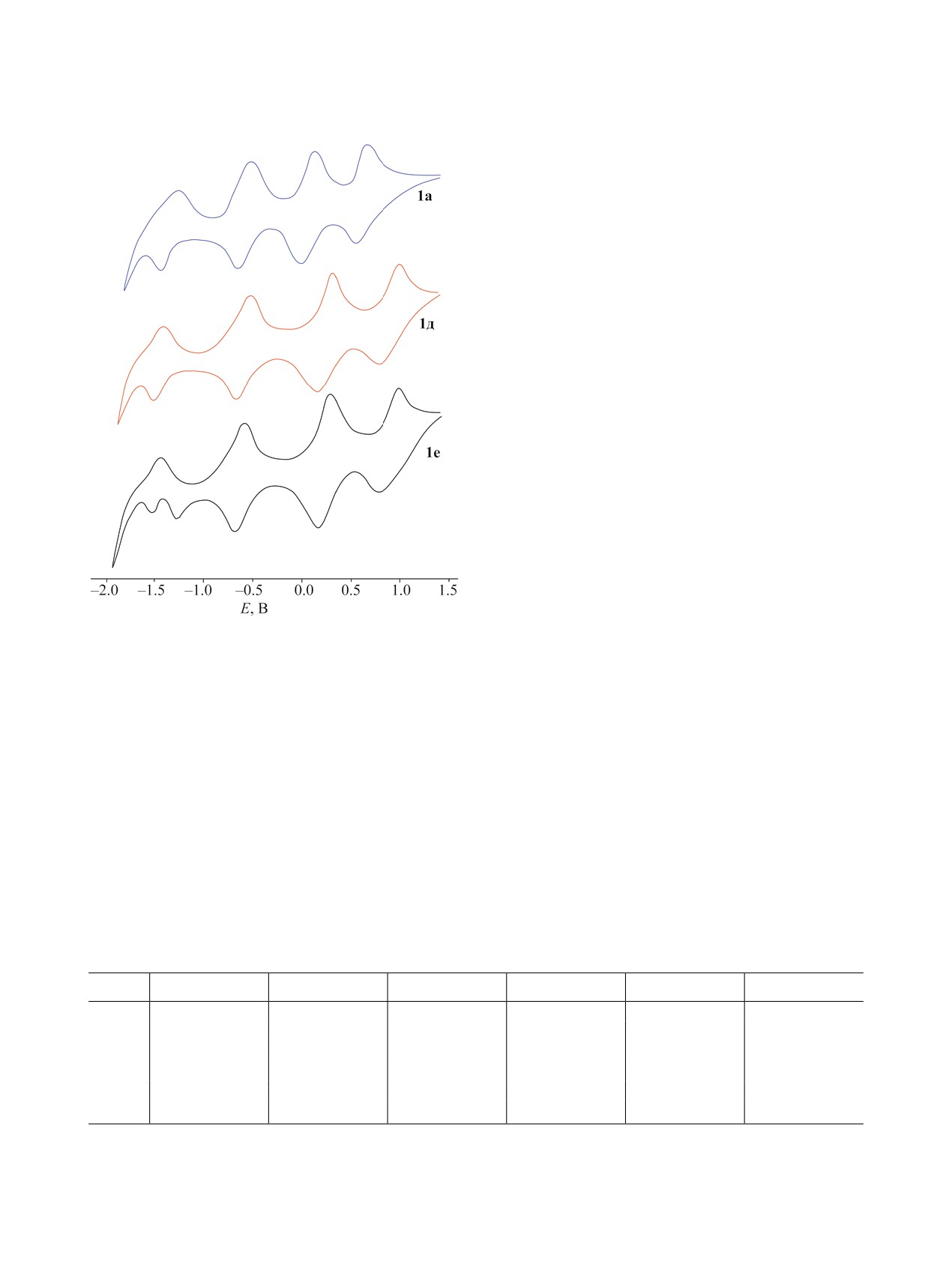
Значения первого потенциала окисления вер-
дазилов 1a-д находятся в диапазоне от 0.05 до
0.22 В, второго потенциала окисления - от 0.59 до
0.89 В (Ag|AgCl|KCl). Значения первого потенциа-
ла восстановления - от -0.50 до -0.59 В и второго
потенциала - от -1.08 до -1.51 В (Ag|AgCl|KCl)
(рис. 2).
Как видно из табл. 1, природа заместителя в па-
ра-положении ароматического кольца положения
2 сильнее влияет на процесс окисления и значи-
тельно меньше - на процесс восстановления. Так,
донорные заместители практически не влияют на
процесс окисления, так как имеет место увели-
Рис. 2. Циклические вольтамперограммы соединений
чение Eox11/2 для соединения 1б (Me) на 0.04 В и
1е и 1д. Вольтамперограммы сняты в растворе CH3CN
для соединения 1г (OМе) на 0.08 В по сравнению
в присутствии фонового электролита 0.1 М. Bu4NBF4
со скоростью сканирования 200 мВ/с (вольтамперо-
с вердазилом 1а. Электроноакцепторные замести-
граммы изображены со смещением относительно оси у).
тели значительно затрудняют процесс окисления,
смещая Eox11/2 в катодную область для соединений
1д (CN) и 1e (NO2) на 0.16 и 0.17 В соответствен-
но по сравнению с вердазилом 1а. На значение
стве фонового электролита Bu4NBF4. В качестве
первого потенциала восстановления Ered11/2 элек-
рабочего использовался платиновый электрод,
тронодонорные и электроноакцепторные замести-
вспомогательным электродом выступала - плати-
тели практически не влияют, однако наблюдается
на, а электродом сравнения - стандартный хлорид-
более значительное и дифференцированное влия-
серебряный. В случае всех радикалов, за исклю-
ние на значение второго потенциала восстановле-
чением нитропроизводного 1e, при регистрации
ния: электронодонорные заместители (Ме, MeO)
Таблица 1. Электрохимические параметры вердазильных радикалов 1a-е
№
R
Eox11/2, В
Eox21/2, В
Ered11/2, В
Ered21/2, В
Eщели, В
1а
H
0.05
0.61
-0.51
-1.25
0.56
1б
Me
0.09
0.60
-0.50
-1.12
0.59
1в
Cl
0.16
0.59
-0.59
-1.31
0.75
1г
MeO
0.13
0.58
-0.55
-1.08
0.68
1д
CN
0.21
0.84
-0.55
-1.48
0.76
1е
NO2
0.22
0.89
-0.56
-1.51
0.78
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 93 № 4 2023
512
КОСТРЮКОВ и др.
Схема 4.
Ph
Ar
Ph
Ar
Ph
Ar
Ph
Ar
Ph
Ar
N
N
N
N
N
N
N
N
N
N
N
N
N
N
N
N
N
N
N
N
•
+e
+e
+e
+e
-e
−e
-e
-e
•
•
•
N
N
N
N
N
N
N
N
N
N
N
N
N
N
N
N
N
N
N
N
Ar
Ph
Ar
Ph
Ar
Ph
Ar
Ph
Ar
Ph
K2
K1
A1
A2
смещают потенциал Ered21/2 в катодную область, а
двулучевом УФ-ВИД спектрофотометре UV-2600
электроноакцепторные (Сl, CN, NO2) - в анодную.
(Shimadzu) в ацетонитриле. Спектры ЭПР реги-
В рассмотренном ряду бирадикалов 1б-е величина
стрировали для бензольных растворов радикалов
электрохимической щели (Ещели = |Eox11/2. - Ered11/2|)
с концентрацией ~10-4 М. на ЭПР-спектрометре
незначительно увеличивается по сравнению с ра-
PS 100.X (Advanced Analytical Instruments) при
дикалом 1а.
комнатной температуре в кварцевых ампулах на
частоте 9.3 ГГц. Настройки ЭПР спектрометра:
Таким образом, синтезированы тетразиниль-
мощность СВЧ 2.0-2.6 мВт, частота модуляции
ные бирадикалы, содержащие в своем составе
100 кГц, амплитуда модуляции 0.1 мТл, время раз-
п-фениленовый фрагмент и 4-R-замещенные ари-
вертки 20 с, количество точек 4096, количество
лы. Полученные радикалы исследованы с помо-
сканирований 1. Элементный анализ выполнен
щью методов спектроскопии ЭПР и циклической
на СHNS-анализаторе Vario MICRO (Elementar,
вольтамперометрии, данные которых подтвержда-
Германия). Условия аналитической ТСХ: адсор-
ют их бирадикальную природу и способность об-
бент - Sorbfil, элюент - гексан-этилацетат (3:1),
ратимо окисляться или восстанавливаться.
проявление в иодной камере или УФ светом.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Флеш-хроматографию проводили на колонке с
силикагелем Merck 60 (0.040-0.063 мм-1) c ис-
В работе использовали коммерчески доступ-
пользованием градиентных систем растворителей
ные реагенты: терефталевый альдегид (99%, CAS
гексан-этилацетат (10:0 → 10:3). Температуры
623-27-8), анилин (99%, CAS 62-53-3), п-толуидин
плавления соединений определяли в запаянных
(99%, CAS 106-49-0), 4-хлоранилин (99%, CAS
стеклянных капиллярах с использованием ана-
106-47-8), 4-метоксианилин (99%, CAS 104-94-9),
лизатора точки плавления МР-50 (Mettler-Toledo,
4-нитроанилин (99%, CAS 100-01-6), гидрохлорид
Швейцария).
фенилгидразина (99%, CAS 59-88-1) и 70%-ный
Перхлораты
3,3′-(1,4-фенилен)бис(1-4-R-
раствор хлорной кислоты (CAS 7601-90-3, Sigma-
фенил-5-фенил-5,6-дигидро-1,2,4,5-тетразиния)
Aldrich), а также водные растворы формальдегида
1a-е получали по методике, аналогичной приве-
(35%) и гидроксида аммония (25%) (АО «Вектон»).
денной в работе [22]. Температуры плавления и
Диоксан, ДМФА, этилацетат, бензол предвари-
спектральные характеристики совпадают с лите-
тельно очищали перегонкой.
ратурными данными.
ИК спектры получены в таблетках KBr на
Общая методика синтеза вердазилов 1а-е. К
Фурье-спектрометре ИнфраЛЮМ ФТ-08 (ООО
перемешиваемому раствору 0.001 моля одной из
«Люмэкс», Россия). УФ спектры получены на
тетразиниевой соли 2a-е в 40 мл этилацетата при
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 93 № 4 2023
СИНТЕЗ ТЕТР
АЗИНИЛЬНЫХ БИРАДИКАЛОВ
513
перемешивании и охлаждении ледяной водой до-
1153, 1046, 937. УФ спектр, λmax, нм: 350, 710.
бавляли одной порцией раствор 1.8 г (0.01 моль)
Спектр ЭПР: g 2.0034, aN-1 5.65 Г, aN-2 5.78 Г, aN-4
D-глюкозы в 40 мл H2O и сразу после этого 6 мл
6.10 Г, aN-5 6.25 Г. Найдено, %: C 71.15; H, 5.19; N
25%-ного раствора аммиака. Постепенно реак-
18.52. C36H32N8O2. Вычислено, %: C 71.04; H 5.30;
ционная смесь изменяла цвет на темно-зеленый
N 18.41.
(1а-г) или коричнево-зеленый (1д, е). Переме-
6,6′-(1,4-Фенилен)бис[4-фенил-2-(4-циано-
шивание продолжали от 15 мин до 1 ч, контро-
фенил)-3,4-дигидро-1,2,4,5-тетразин-1-2H-ил]
лируя по ТСХ исчезновение перхлоратов 5,6-ди-
(1д). Выход 0.27 г (43%), т. пл. 232-233°C (разл.)
гидро-1,2,4,5-тетразиния
2a-г. По окончании
(гексан-этилацетат). ИК спектр (KBr), ν, cм-1:
реакции органический слой отделяли, промывали
3096, 2256 (CN), 1599 (С=N), 1513 (N=N), 1285,
ледяной водой (3×20 мл) и сушили над безводным
843. УФ спектр, λmax, нм: 395, 721. Спектр ЭПР: g
Na2SO4. После удаления растворителя, получен-
2.0034, aN-1 5.61 Г, aN-2 5.79 Г, aN-4 6.19 Г, aN-5 6.30
ный остаток очищали с помощью флеш-хромато-
Г. Найдено, %: C 64.13; H 3.97; N 21.75. C36H26N10.
графии на силикагеле.
Вычислено, %: C 63.94; H 4.10; N 21.93.
6,6′-(1,4-Фенилен)бис(2,4-дифенил-3,4-диги-
6,6′-(1,4-Фенилен)бис[2-(4-нитрофенил)4-
дро-1,2,4,5-тетразин-1-2H-ил) (1a). Выход 0.29 г
фенил-3,4-дигидро-1,2,4,5-тетразин-1-2H-ил]
(53%), т. пл. 193-194°C (разл.) (гексан-этилаце-
(1e). Выход 0.26 г (44%), т. пл. 198-199°C (разл.)
тат). ИК спектр (KBr), ν, cм-1: 3094, 2864, 1653
(гексан-этилацетат). ИК спектр (KBr), ν, cм-1:
(C=C), 1575 (С=N), 1499 (N=N), 1256, 1105, 752.
3097, 1605 (C=N), 1559 (NO2), 1507 (N=N), 1349
УФ спектр, λmax, нм: 376, 731. Спектр ЭПР: g
(NO2), 1312, 1234, 841. УФ спектр, λmax, нм: 410,
2.0034, aN-1 5.80 Г, aN-2 5.80 Г, aN-4 6.00 Г, aN-5
735. Спектр ЭПР: g 2.0034, aN-1 5.50 Г, aN-2 5.81 Г,
6.00 Г. Найдено, %: C 74.55; H 4.88; N 20.56.
a
6.22 Г, aN-5 6.34 Г. Найдено, %: C 72.13; H 4.27;
C34H28N8. Вычислено, %: C 74.43; H 5.14; N 20.42.
N-4
N 23.61. C34H26N10O4. Вычислено, %: C 72.23; H
6,6′-(1,4-Фенилен)бис[2-(п-толил)-4-фе-
4.38; N 23.40.
нил-3,4-дигидро-1,2,4,5-тетразин-1-2H-ил]
(1б). Выход 0.31 г (54%), т. пл. 165-166°C (разл.)
ИНФОРМАЦИЯ ОБ АВТОРАХ
(гексан-этилацетат). ИК спектр (KBr), ν, cм-1:
3097, 2954 (CH3), 1601 (С=N), 1495 (N=N), 1277,
Кострюков Сергей Геннадьевич, ORCID: https://
1175, 799. УФ спектр, λmax, нм: 381, 728. Спектр
orcid.org/0000-0002-1774-0836
ЭПР: g 2.0033, aN-1 5.55 Г, aN-2 5.70 Г, aN-4 6.06 Г,
Буртасов Алексей Анатольевич, ORCID: https://
aN-5 6.16 Г. Найдено, %: C 75.99; H 5.39; N 19.52.
orcid.org/0000-0003-2889-7369
C36H32N8. Вычислено, %: C 74.98; H 5.59; N 19.43.
Долганов Александр Викторович, ORCID:
6,6′-(1,4-Фенилен)бис[4-фенил-2-(4-хлор-
фенил)-3,4-дигидро-1,2,4,5-тетразин-1-2H-ил]
(1в). Выход 0.41 г (58%), т. пл. 202-203°C (разл.)
org/0000-0001-6245-2414
(гексан-этилацетат). ИК спектр (KBr), ν, cм-1:
Конушкин Иван Александрович, ORCID:
3097, 1601 (С=N), 1498 (N=N), 1259, 1139, 1078,
930, 795, 588 (C-Сl). УФ спектр, λmax, нм: 391, 742.
Спектр ЭПР: g 2.0035, aN-1 5.40 Г, aN-2 5.79 Г, aN-4
ФИНАНСОВАЯ ПОДДЕРЖКА
6.14 Г, aN-5 6.24 Г. Найдено, %: C 57.86; H 3.58; N
14.99. C34H26Cl2N8. Вычислено, %: C 57.81; H 3.71;
Работа выполнена при финансовой поддерж-
N 14.86.
ке Министерства науки и высшего образования
6,6′-(1,4-Фенилен)бис[2-(4-метоксифенил)-
Российской Федерации (тема № 121111000064-5)
4-фенил-3,4-дигидро-1,2,4,5-тетразин-1-2H-ил]
в рамках государственного задания Мордовского
(1г). Выход 0.36 г (59%), т. пл. 156-157°C (разл.)
национального исследовательского университета
(гексан-этилацетат). ИК спектр (KBr), ν, cм-1:
им Н.П. Огарева (создание новых молодежных ла-
3093, 2865, 1605 (С=N), 1495 (N=N), 1273, 1245,
бораторий).
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 93 № 4 2023
514
КОСТРЮКОВ и др.
КОНФЛИКТ ИНТЕРЕСОВ
12.
Hu G., Xie S., Wang C., Timm C. // Beilstein J.
Nanotechnol. 2017. Vol. 8. P. 1919. doi 10.3762/
Авторы заявляют об отсутствии конфликта
bjnano.8.192
интересов.
13.
Sugisaki K., Nakazawa S.; Toyota K., Sato K., Shiomi D.,
Takui T. // ACS Cent. Sci. 2019. Vol. 5. N 1. P. 167. doi
СПИСОК ЛИТЕРАТУРЫ
10.1021/acscentsci.8b00788
1.
Kuhn R., Trischman H. // Monatsh. Chem. 1964.
14.
Kuhn R., Neugebauer F.A., Trischmann H. // Monatsh.
Vol. 95. N 2. P. 457. doi 10.1007/BF00901311
Chem. 1966. Vol. 97. P. 525. doi 10.1007/BF00905273
2.
Липунова Г.Н., Федорченко Т.Г., Чупахин О.Н. //
15.
Fischer P.H.H. // Tetrahedron. 1967. Vol. 23. N 4.
Усп. хим. 2013. Т. 82. № 8. C. 701; Lipunova G.N.,
P. 1939. doi 10.1016/S0040-4020(01)82597-7
Fedorchenko T.G., Chupakhin O.N. // Russ. Chem.
16.
Chung G., Lee D. // Chem. Phys. Lett. 2001. Vol. 350.
Rev. 2013. Vol. 82. N 8. P. 701. doi 10.1070/
N 3-4. P. 339. doi 10.1016/S0009-2614(01)01296-9
RC2013v082n08ABEH004341
17.
Bhattacharya D., Shil S., Panda A., Misra A. // J. Phys.
3.
Липунова Г.Н., Федорченко Т.Г., Цмокалюк А.Н.,
Chem. (A). 2010. Vol. 114. N 43. P. 11833. doi 10.1021/
Чупахин О.Н. // Изв. АН. Сер. Хим. 2020. № 7.
jp1072507
С. 1203; Lipunova G.N., Fedorchenko T.G., Tsmoka-
18.
Azuma N., Ishizu K., Mukai K. // J. Chem. Phys. 1974.
lyuk A.N., Chupakhin O.N. // Russ. Chem. Bull. 2020.
Vol. 61. P. 2294. doi 10.1063/1.1682306
Vol. 69. N 7. P. 1203. doi 10.1007/s11172-020-2892-6
4.
Brook D.J.R. // Comments Inorg. Chem. 2015. Vol. 35.
19.
Kopf P., Morokuma K., Kreilick R. // J. Chem. Phys.
N 1. P. 1. doi 10.1080/02603594.2014.974805
1971. Vol. 54. P. 105. doi 10.1063/1.1674577
5.
Липунова Г.Н., Федорченко Т.Г., Чупахин О.Н. //
20.
Meier P., Blume A., Ohmes E., Neugebauer F.A.,
Коорд. хим. 2022. T. 48. № 7. С. 389; Lipunova G.N.,
Kothe G. // Biochemistry. 1982. Vol. 21. N 3. P. 526. doi
Fedorchenko T.G., Chupakhin O.N. // Russ. J.
10.1021/bi00532a018
Coord. Chem. Vol. 48. N 7. P. 397. doi 10.1134/
21.
Кострюков С.Г., Баландина А.В., Козлов А.Ш.,
S1070328422070065
Крайнов Е.В., Пряничникова М.К., Черняева О.Ю.,
6.
Miyamoto S., Iwasaki Y., Uemoto N., Hosokoshi Y.,
Ахматова А.А., Люкшина Ю.И. // ЖОХ. 2020.
Fujiwara H., Shimono S., Yamaguchi H. // Phys. Rev.
Т. 90. № 3. С. 353; Kostryukov S.G., Balandina A.V.,
Mat. 2019. Vol. 3. N 6. Article 064410. doi 10.1103/
Kozlov A.S., Kraynov E.V., Pryanichnikova M.K.,
PhysRevMaterials.3.064410.
Chernyaeva O.Y., Akhmatova A.A., Lukshina Y.I. // Russ.
7.
Novitchi G., Shova S., Train C. // Inorg. Chem.
J. Gen. Chem. 2020. Vol. 90. N 3. P. 341. doi 10.1134/
2022. Vol. 61. N 43. P. 17037. doi 10.1021/acs.
S1070363220030044
inorgchem.2c01742
8.
Tretyakov E.V., Zhivetyeva S.I., Petunin P.V., Gorbu-
22.
Wilcox D.A., Agarkar V., Mukherjee S., Boudouris B.W. //
nov D.E., Gritsan N.P., Bagryanskaya I.Yu.,
Annu. Rev. Chem. Biomol. Eng. 2018. Vol. 9. P. 83. doi
Bogomyakov A.S., Postnikov P.S., Kazantsev M.S.,
10.1146/annurev-chembioeng-060817-083945.
Trusova M.E., Shundrina I.K., Zaytseva E.V.,
23.
Кострюков С.Г., Козлов А.Ш., Конушкин И.А.,
Parkhomenko D.A., Bagryanskaya E.G., Ovcharen-
Краснов Д.А., Янцен Н.В. // ЖОрХ. 2022. Т. 58.
ko V.I. // Angew. Chem. Int. Ed. 2020. Vol. 59. N 46.
№ 10. С. 1080; Kostryukov S.G., Kozlov A.S.,
P. 20704. doi 10.1002/anie.202010041
Konushkin I.A., Krasnov D.A., Yantsen N.V. // Russ. J.
9.
Tretyakov E.V., Petunin P.V., Zhivetyeva S.I., Gorbu-
Org. Chem. 2022. Vol. 58. N 10. P. 1416. doi 10.1134/
nov D.E., Gritsan N.P., Fedin M.V., Stass D.V.,
S1070428022100050
Samoilova R.I., Bagryanskaya I.Y., Shundrina I.K.,
24.
Кострюков С.Г., Козлов А.Ш., Краснов Д.А.,
Bogomyakov A.S., Kazantsev M.S., Postnikov P.S.,
Буртасов А.А., Петров П.С., Тезикова В.С.,
Trusova M.E., Ovcharenko V.I. // J. Am. Chem. Soc.
Асфандеев А.Ю., Идрис Т.Д. // ЖОХ. 2021. Т. 91.
2021. Vol. 143. N 21. P. 8164. doi 10.1021/jacs.1c02938
№ 4. С. 531; Kostryukov S.G, Kozlov A.S., Krasnov D.A.,
10.
Abe M. // Chem. Rev. 2013. Vol. 113. N 9. P. 7011. doi
10.1021/cr400056a
Burtasov A.A., Petrov P.S., Tezikova V.S., Asfande-
11.
Sanvito S. // Chem. Soc. Rev. 2011. Vol. 40. P. 3336. doi
ev A.Yu., Idris T.D. // Russ. J. Gen. Chem. 2021. Vol. 91.
10.1039/C1CS15047B
N 4. P. 614. doi 10.1134/S107036322104006X
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 93 № 4 2023
СИНТЕЗ ТЕТР
АЗИНИЛЬНЫХ БИРАДИКАЛОВ
515
Synthesis of Tetrazinyl Biradicals
Containing a p-Phenylene Fragment
S. G. Kostryukova,*, А. А. Burtasova, A. V. Dolganova, A. Sh. Kozlova, I. A. Konushkina,
N. A. Malova, D. A. Krasnova, and A. Yu. Asfandeeva
a National Research Ogarev Mordovia State University, Saransk, 430005 Russia
*e -mail: kostryukov_sg@mail.ru
Received December 21, 2022; revised February 25, 2023; accepted March 1, 2023
3,3′-(1,4-Phenylene)bis[1-(4-R-phenyl)-5-phenyl-5,6-dihydro-1,2,4,5-tetrazinium] perchlorates were trans-
formed into stable tetrazinyl biradicals by the action of D-glucose in slightly alkaline medium (NH4OH) in the
presence of air oxygen. The tetrazinyl biradicals were isolated in individual state and characterized by cyclic
voltammetry, elemental analysis, IR, UV, EPR spectroscopy methods.
Keywords: 5,6-dihydro-1,2,4,5-tetrazinium perchlorate, 1,2,3,4-tetrahydro-1,2,4,5-tetrazinyl, verdazyl radical,
cyclic voltammetry, EPR spectroscopy
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 93 № 4 2023