ЖУРНАЛ ОБЩЕЙ ХИМИИ, 2023, том 93, № 5, с. 801-812
УДК 544.344.3
СУПРАМОЛЕКУЛЯРНЫЕ СИСТЕМЫ НА ОСНОВЕ
АЛЬГИНАТА НАТРИЯ И ВИОЛОГЕНОВОГО
КАЛИКС[4]РЕЗОРЦИНА ДЛЯ ИНКАПСУЛЯЦИИ
ГИДРОФОБНЫХ СОЕДИНЕНИЙ
© 2023 г. Р. Р. Кашапов1,*, Ю. С. Разуваева1, А. Ю. Зиганшина1, А. С. Сапунова1,
А. Д. Волошина1, В. В. Сальников2, Л. Я. Захарова1
1 Институт органической и физической химии имени А. Е. Арбузова, Федеральный исследовательский центр
«Казанский научный центр Российской академии наук», ул. Академика Арбузова 8, Казань, 420088 Россия
2 Казанский институт биохимии и биофизики, Федеральный исследовательский центр
«Казанский научный центр Российской академии наук», Казань, 420111 Россия
*e-mail: kashapov@iopc.ru
Поступило в редакцию 14 апреля 2023 г.
После доработки 14 апреля 2023 г.
Принято к печати 17 апреля 2023 г.
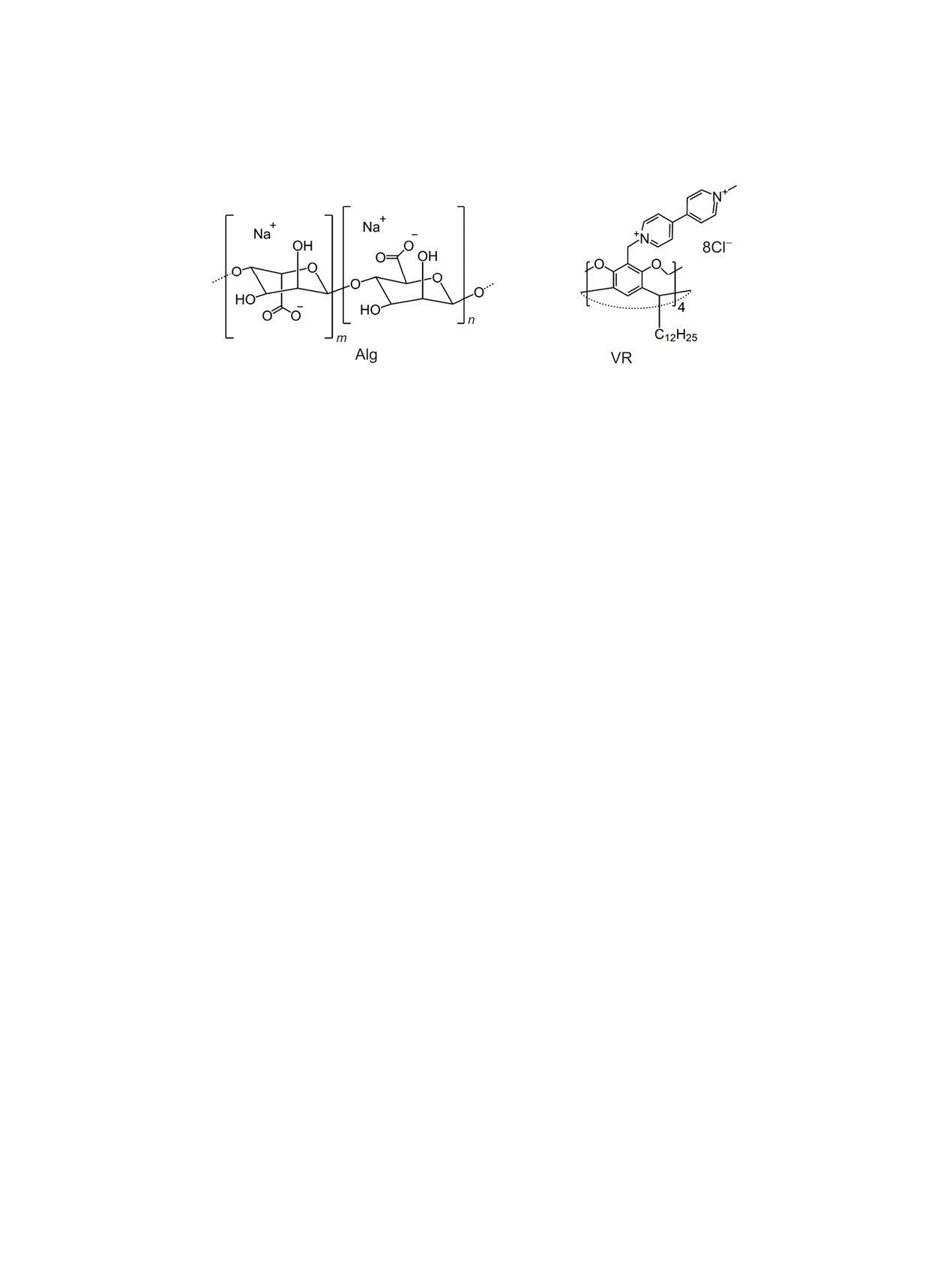
Работа посвящена исследованию супрамолекулярной системы на основе виологенового каликс[4]-
резорцина и альгината натрия в водной среде с привлечением набора физико-химических методов.
Установлено, что альгинат натрия и виологеновый каликс[4]резорцин в диапазоне концентрационных
соотношений макроцикл:полимер от 1:2 до 1:10 образуют стабильные наночастицы, способные ин-
капсулировать гидрофобные биологически активные вещества. Исследование цитотоксических свойств
данных наночастиц в присутствии инкапсулированных субстратов показало увеличение селективности
действия кверцетина и олеиновой кислоты по отношению к опухолевым клеткам M-HeLa в 2.47 и
1.14 раза соответственно.
Ключевые слова: каликсарен, полимер, самосборка, комплексообразование, солюбилизация, цитоток-
сичность
DOI: 10.31857/S0044460X23050153, EDN: DDCGOC
В настоящее время активно исследуются супра-
кой температуры, органический растворителей)
молекулярные системы на основе полиэлектроли-
получать нетоксичные функциональные системы
тов и противоположно заряженных ионных ПАВ,
с высокой эффективностью загрузки субстратов и
интерес к которым возрос в последние несколь-
стимул-чувствительными свойствами, что являет-
ко лет ввиду создания широкого спектра новых
ся актуальным для современной фундаментальной
функциональных систем для решения различных
науки и фармацевтической химии.
прикладных задач [1-4]. Способность к совмест-
Биополимер альгинат натрия, получаемый из
ной самоорганизации этих молекулярных блоков
морских водорослей, представляет собой линей-
с образованием функциональных наноразмерных
ный гетерополимер, содержащий 1,4-связанные
частиц лежит в основе супрамолекулярного под-
α-L-глюкуроновую кислоту и β-D-маннуроновую
хода к разработке новых многоцелевых агентов.
кислоту (схема 1) [5]. Он находит множество при-
Такой подход позволяет без применения специ-
менений в различных современных технологиях в
альных условий (синтетических процедур, высо-
области пищевой и биомедицинской промышлен-
801
802
КАШАПОВ и др.
Схема 1.
ности. Одним из основных преимуществ альги-
[24]. Кроме формирования супрамолекулярных
ната является простота приготовления гидрогеля
систем с противоположно заряженными полиме-
путем сшивания ионами многовалентных метал-
рами и наночастицами, молекулы ПАВ широко
лов без использования токсичных химических ве-
используются при создании полимер-коллоидных
ществ и жестких условий [6, 7]. В качестве сши-
комплексов [25,26], которые находят применение в
вающего агента применяется двухвалентный ион
медицине [3, 27], косметологии [28, 29], нефтяной
Ca2+ [8, 9], а в недавних публикациях ион Zn2+
[30, 31] и пищевой промышленности [32, 33]. Для
также использовали для приготовления гелей, ми-
получения альгинатных наночастиц также могут
кро- и наночастиц [10, 11]. Альгинатные гидроге-
быть использованы противоположно заряженные
ли широко изучаются именно с перспективой при-
ПАВ. Миртич и соавторы сравнили комплексо-
менения для доставки лекарств [7, 9, 12]. Капсулы
образование альгината с катионами металлов, по-
альгината стабильны в кислой среде желудка, но
лимерами и ПАВ [34]. Было показано, что исполь-
набухают в основной среде кишечника и высвобо-
зование ПАВ приводит к формированию самых
ждают инкапсулированное лекарство [13], поэто-
маленьких частиц с наименьшей полидисперсно-
му представляют собой идеальный полисахарид
стью и с самым низким дзета-потенциалом среди
для доставки лекарств в толстую кишку. Кроме
исследованных сшивающих агентов. Янг и соавто-
этого, комплексы альгинатов с металлами важны
ры [35] показали, что во взаимодействиях между
для медицинской практики, поскольку они спо-
альгинатом и ПАВ преобладающую роль играет
собны укреплять иммунную систему [14] и пре-
электростатическое притяжение, а при понижении
дотвращать развитие онкологических [15], сердеч-
рН межмолекулярные взаимодействия дополни-
но-сосудистых [16] и почечных заболеваний [17].
тельно стабилизировались гидрофобным эффек-
Помимо использования катионов металлов, воз-
том. В литературе также представлен ряд работ,
можно применение органических противоионов
посвященных исследованию агрегации катионных
для супрамолекулярных взаимодействий с про-
ПАВ в присутствии альгината. Взаимодействие
изводными альгината. Смешанные наночастицы
альгината с ПАВ индуцирует образование мицелл
можно получать в результате электростатических
при концентрациях ПАВ ниже их критической
взаимодействий между альгинатом и катионным
концентрации агрегации (ККА) [36-38]. Помимо
полимером, например, хитозаном [18, 19]. Данным
традиционных открытоцепных ПАВ макроцикли-
способом можно модифицировать поверхности на-
ческий амфифил, а именно катионный каликс[4]-
норазмерных частиц различной природы, а имен-
резорцин, может также электростатически вза-
но липосом [20], металлических [21] и полимер-
имодействовать с альгинатным полиэлектроли-
ных наночастиц [22, 23]. Полимерная оболочка в
том [39]. Как и в случае с традиционными амфи-
виде альгината способствует повышению стабиль-
филами, в присутствии полимера значение ККА
ности частиц [20, 23], улучшенному проникнове-
амфифила снижается, а в растворе формируются
нию в клетки и регулированию иммунного ответа
стабильные частицы, размер которых зависит от
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 93 № 5 2023
СУПР
АМОЛЕКУЛЯРНЫЕ СИСТЕМЫ
803
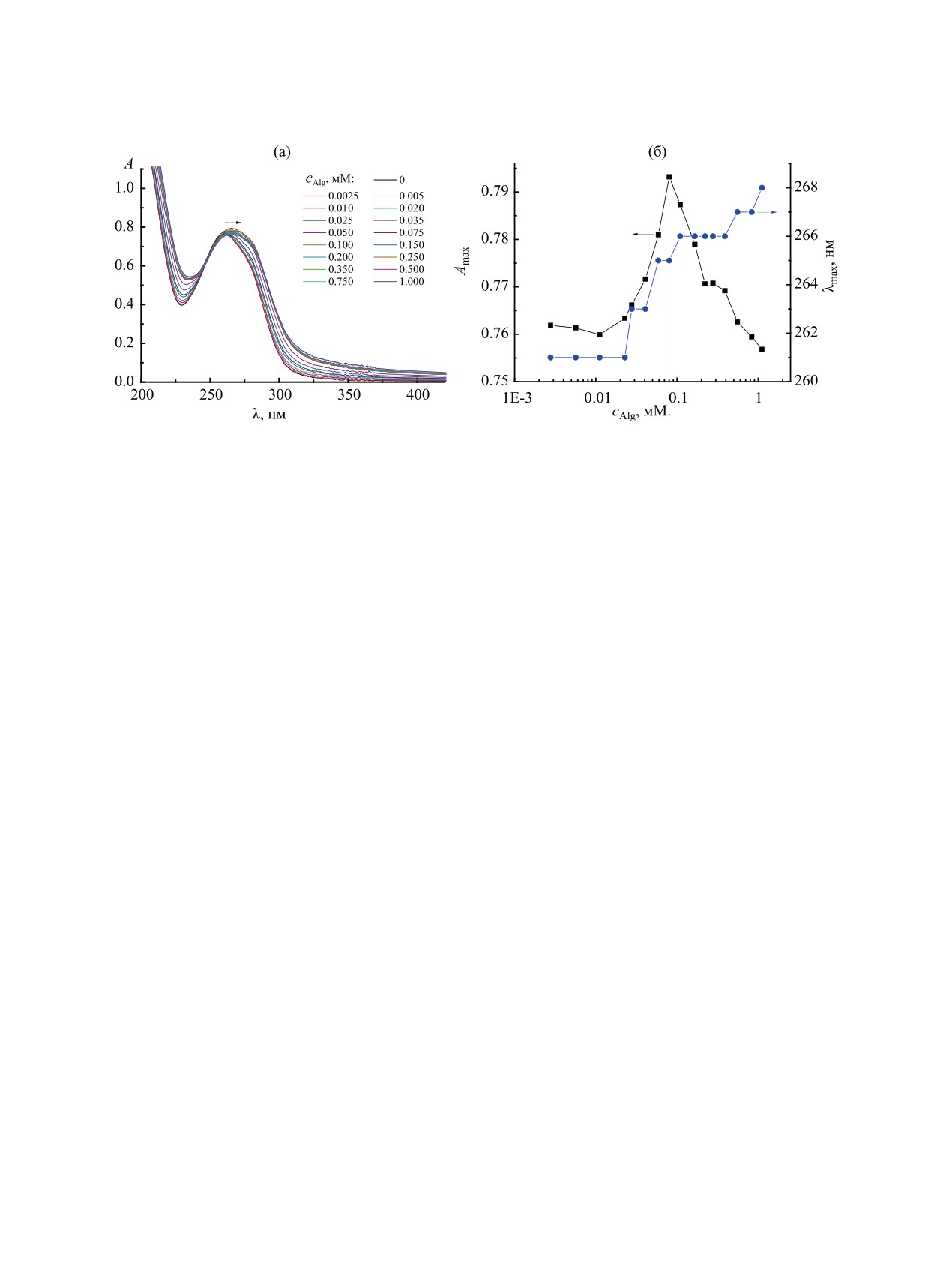
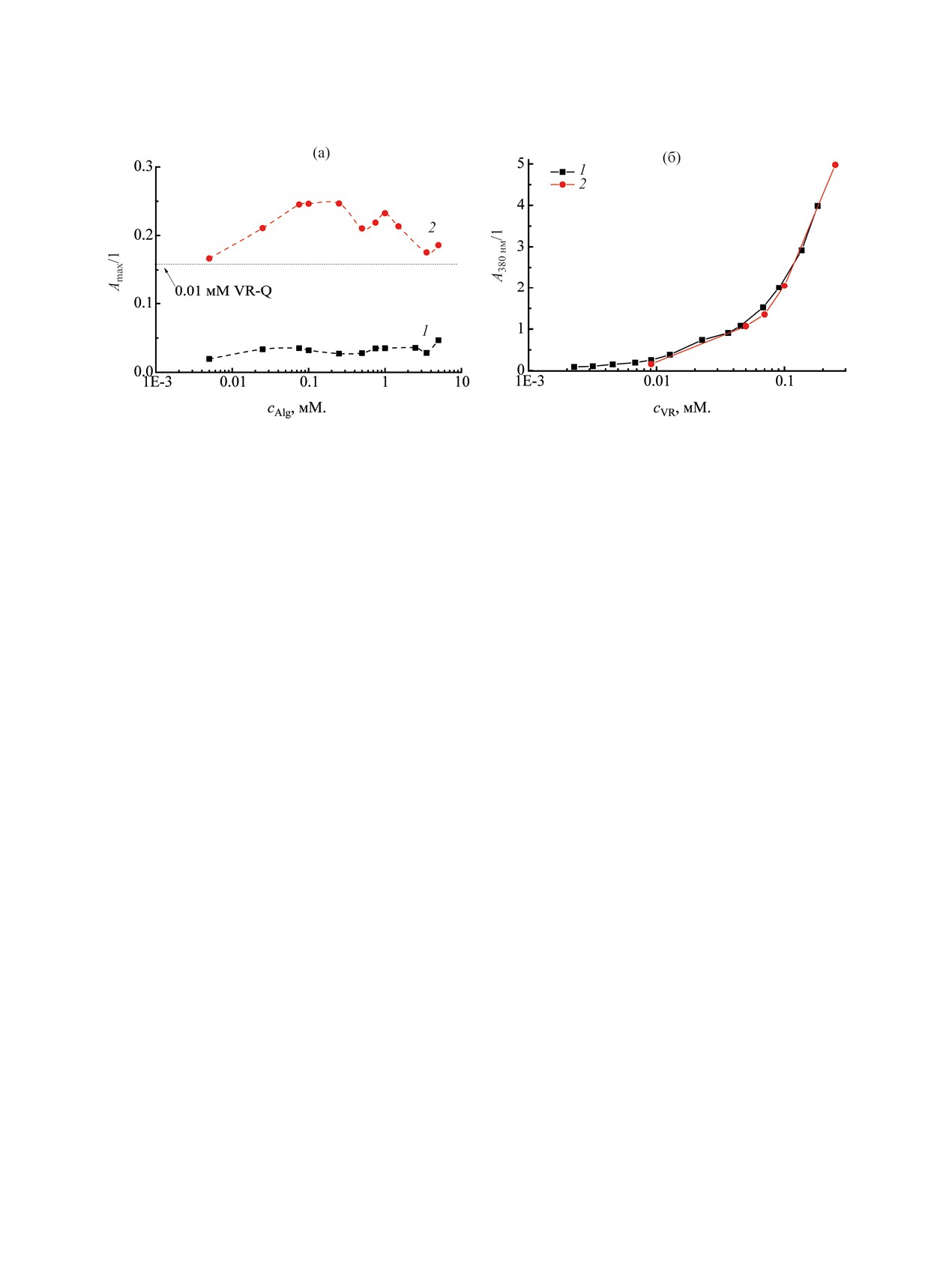
Рис. 1. УФ спектры водных растворов 0.01 мМ. VR в отсутствие и в присутствии различной доли Alg (оптический путь -
1 см) (а) и соответствующая им зависимость максимального поглощения (шкала слева) и длины волны этого поглощения
(шкала справа) от концентрации Alg (б).
длины гидрофобных заместителей и природы го-
способность образовывать смешанные агрегаты с
ловной группы макроцикла. Для сшивки альгина-
анионными ПАВ [49]. В данной работе набором
та можно использовать мицеллы цетилпиридиний
физико-химических методов была исследована
хлорида [40], которые проявляют антибактериаль-
агрегация в бинарной системе VR-Alg с образова-
ные свойства [40] и могут выступать в качестве
нием наночастиц, определены размеры агрегатов и
наноконтейнера для липофильного лекарства ибу-
оценены их биологические свойства. Полученные
профена [27]. Наночастицы на основе композиции
агрегаты были исследованы в качестве нанокон-
альгинат-Твин 80-геминальное катионное ПАВ
тейнеров для липофильных биологически актив-
использовали для связывания капсаицина [41].
ных веществ, а именно флавоноида кверцетина и
Как видно из представленных выше литературных
олеиновой кислоты.
данных, агрегация в смешанных системах альги-
На первом этапе исследований было изучено
ната и ПАВ широко изучена, однако применение
взаимодействие Alg с виологеновым каликс[4]-
этих композиций в качестве систем доставки ле-
резорцином при помощи спектрофотометрии.
карств недостаточно исследовано.
Виологеновый каликс[4]резорцин имеет характе-
Данная работа посвящена изучению надмоле-
ристическую полосу поглощения при 261 нм, в то
кулярных агрегатов, образующихся в растворах
же время поглощение Alg в этой области спектра
полианиона альгината натрия (Alg) и катионного
незначительно. Титрование водного раствора ви-
кавитанда, а именно виологенового каликс[4]-
ологенового каликс[4]резорцина с концентрацией
резорцина, содержащего н-додецильные заме-
0.01 мМ. показало, что с увеличением содержа-
стители на нижнем ободе (VR) (схема 1). Выбор
ния Alg наблюдается возрастание интенсивности
макроцикла обусловлен нацеленностью виологе-
поглощения с батохромным сдвигом его максиму-
новых групп на митохондрии клеток [42], кото-
ма, а затем снижение интенсивности поглощения
рые рассматриваются в качестве мишени в рамках
(рис. 1а). Если построить зависимость максиму-
новых перспективных методов лечения рака [43],
ма поглощения от молярной концентрации Alg,
сердечной недостаточности [44], резистентности
рассчитанной относительно мономерного звена
к инсулину [45] и нарушений в работе мозга [46].
Alg, то максимальное значение интенсивности
В предыдущих работах мы показали низкую ток-
на данной зависимости наблюдалось в смеси с
сичность виологенового макроцикла [47,48] и его
8-кратным избытком Alg (рис.
1б). Максимум
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 93 № 5 2023
804
КАШАПОВ и др.
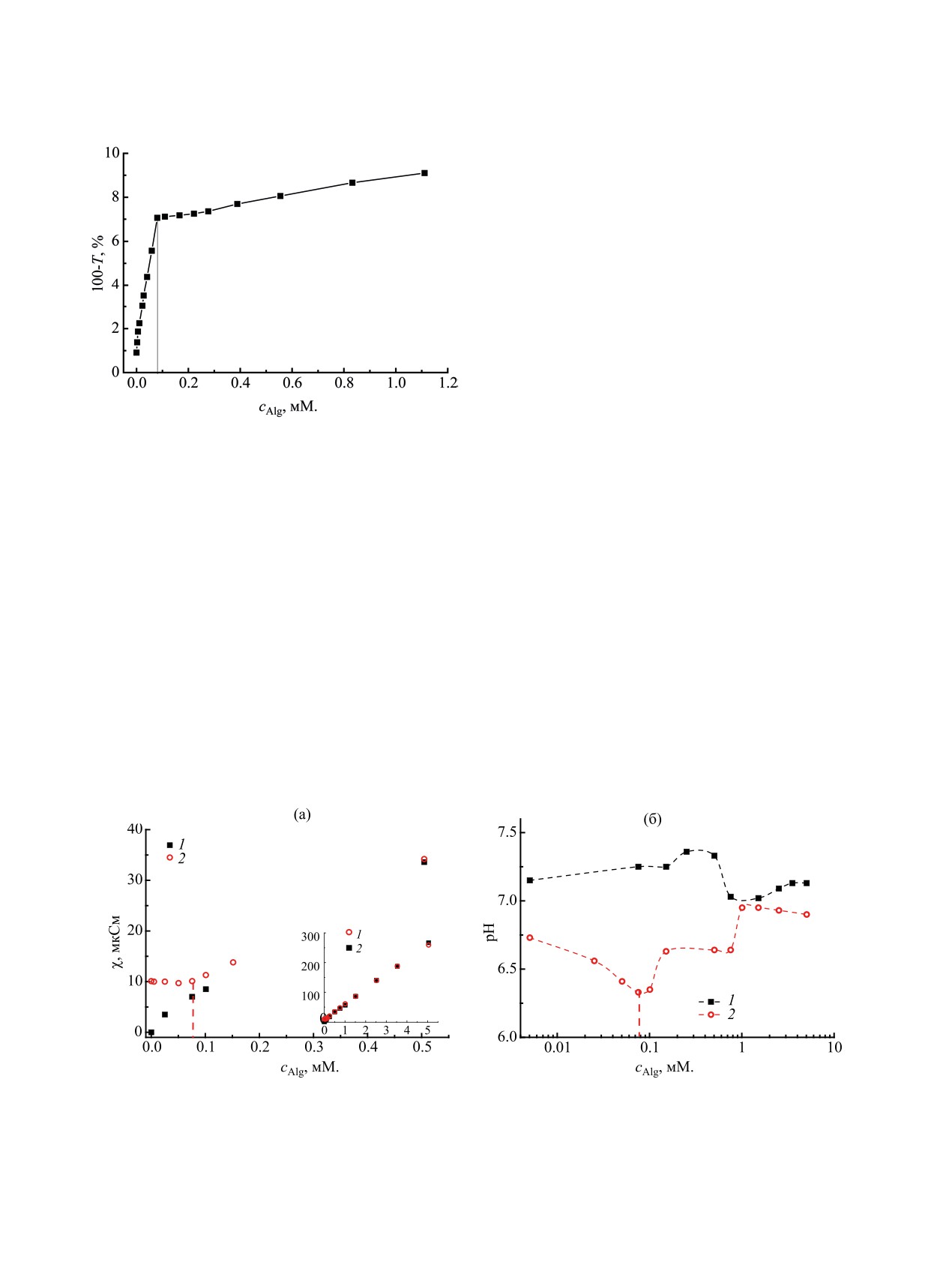
нента к другому приводит к резкому возрастанию
мутности до достижения соотношения VR:Alg =
1:8 (рис. 2). При дальнейшем увеличении концен-
трации Alg эти агрегаты не разрушаются и мут-
ность не снижается, что отражается на отсутствии
снижения оптической плотности после достиже-
ния 8-кратного избытка полимера. Таким образом,
каждая молекула VR при связывании с Alg ориен-
тирует вокруг себя восемь мономерных звеньев
полимерной молекулы, что указывает на электро-
статическую природу взаимодействия между VR и
Alg.
Значение удельной электропроводности в во-
дных растворах индивидуального Alg линейно
Рис. 2. Зависимость мутности смешанной системы
VR-Alg от концентрации Alg при фиксированной
возрастает в диапазоне концентраций до 0.5 мМ.
концентрации VR 0.01 мМ. в воде (λ 450 нм, l 10 мм,
(рис. 3а). В присутствии VR при увеличении со-
25°С).
держания Alg в растворе до 8-кратного избыт-
ка значение электропроводности не меняется
и остается на уровне свободного макроцикла
поглощения при титровании смещается вправо с
(рис. 3а), что подтверждает формирование наноча-
261 до 268 нм, что говорит об изменении микро-
стиц за счет электростатического взаимодействии
окружения молекул VR в присутствии Alg. Стоит
макроцикла с полимером и взаимной компенсации
отметить, что соотношение VR:Alg = 1:8 является
заряда виологеновых групп макроцикла и ацетат-
эквизарядным, поскольку на одну молекулу макро-
ных групп полимера при соотношении VR:Alg =
цикла приходится восемь положительных зарядов
1:8. При последующем добавлении Alg электро-
четырех виологеновых групп, а каждое мономер-
проводность смешанных растворов идентична
ное звено Alg содержит по одной ацетатной группе
электропроводности растворам индивидуального
(схема 1). Метод турбидиметрического титрова-
полимера, что указывает на появлении свободных
ния также показал, что добавление одного компо-
молекул полимера, не участвующих во взаимо-
Рис. 3. Зависимость удельной электропроводности (а) и рН (б) от концентрации Alg для смешанной системы VR-Alg (1) и
индивидуального раствора Alg (2) при фиксированной концентрации VR (0.01 мМ.) при 25°С.
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 93 № 5 2023
СУПР
АМОЛЕКУЛЯРНЫЕ СИСТЕМЫ
805
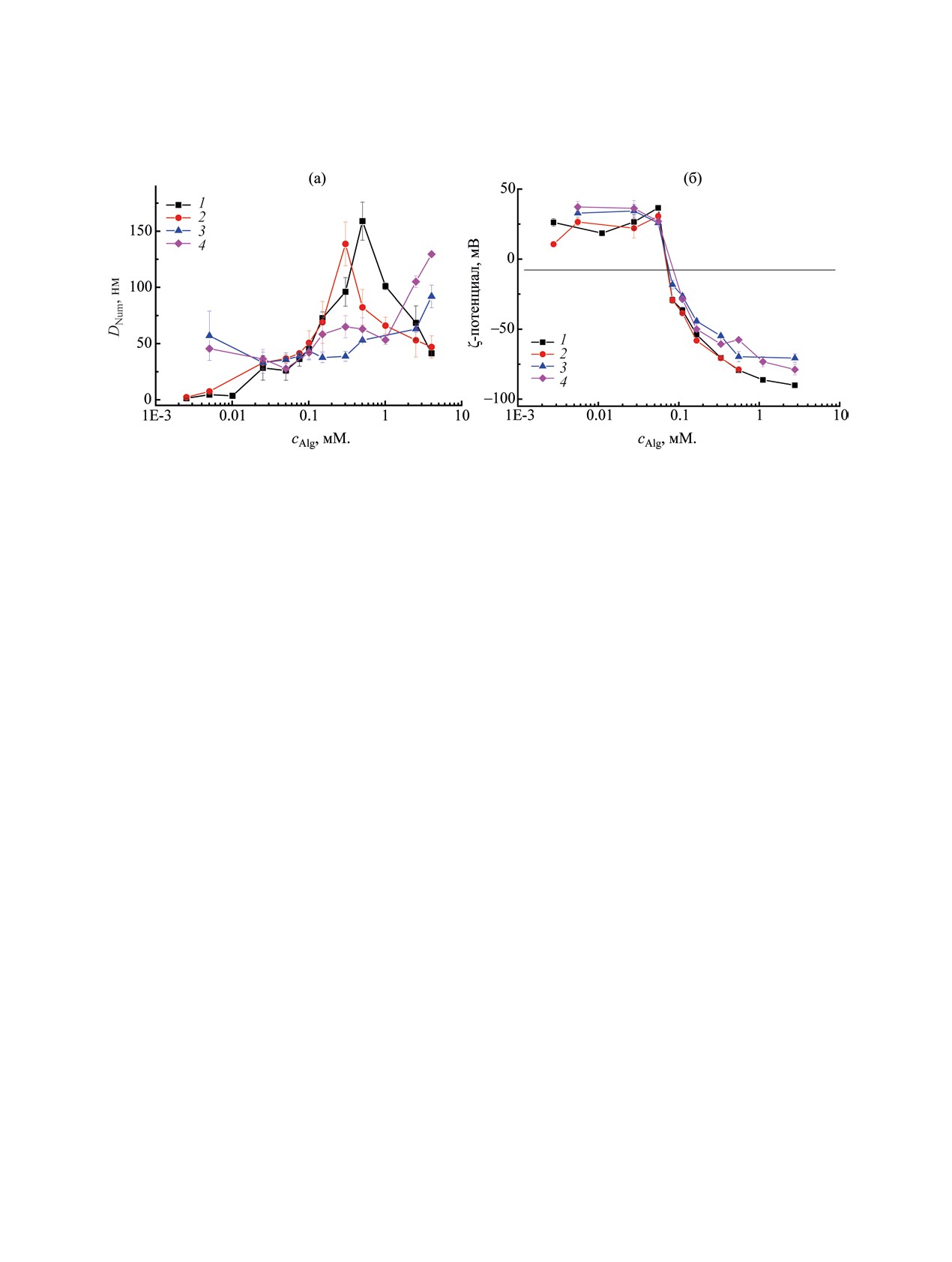
Рис. 4. Зависимость размера (а) и дзета-потенциала (б) частиц в смешанной системе VR-Alg от концентрации Alg при
фиксированной концентрации VR 0.01 мМ. при 25°С. 1 - свежеприготовленный образец, 2 - через 1 сут, 3 - через 7 сут,
4 - через 14 сут.
действии с виологеновым каликс[4]резорцином в
35 нм. Однако максимум значений гидродинамиче-
растворе.
ского диаметра наблюдается не при соотношении
VR:Alg = 1:8, которое соответствует перезарядке
Индивидуальный раствор 0.01 мМ. VR обла-
системы (рис. 4б), а при 50-80-кратном избытке
дает рН 6.77, а индивидуальный раствор Alg име-
полимера, что коррелирует с возрастанием мутно-
ет рН в нейтральной области, но добавление по-
сти в этом концентрационном диапазоне (рис. 2).
лимера к 0.01 мМ. VR приводит к снижению рН
Размер агрегатов в этих смешанных растворах в
с минимумом, наблюдаемым при соотношении
основном составляет 100-150 нм, но в то же вре-
VR:Alg = 1:8 (рис. 3б). Предполагаемой причиной
мя присутствует небольшая доля более крупных
снижения рН в этом концентрационном диапазоне
частиц с гидродинамическим диаметром 300-600
является то, что равновесное состояние нейтраль-
нм (рис. S1, см. Дополнительные материалы). Воз-
ной и анионной форм слабых α-L-глюкуроновой
можной причиной образования последних являет-
и β-D-маннуроновой кислот при взаимодействии
ся то, что вновь добавляемый полимер «склеивает»
с виологеновым каликс[4]резорцином сдвигается
агрегаты, образовавшиеся ранее, в более крупные
в сторону образования анионов. При дальнейшем
структуры. За одни сутки хранения при комнат-
увеличении избытка полимера значение рН воз-
ной температуре размер частиц, формируемых в
растает и приближается к нейтральному значению
растворах до достижения соотношения VR:Alg =
рН индивидуального полимера.
1:16, практически не изменяются, а в растворах
Формирование агрегатов в смешанном раство-
с 20-80-кратным избытком Alg происходит не-
ре было исследовано методом динамического рас-
монотонное изменение размеров. За две недели
сеяния света (ДРС) (рис. 4, S1, см. Дополнитель-
хранения наиболее стабильные частицы, сохра-
ные материалы). В индивидуальном растворе VR
няющие значения гидродинамического диаметра,
с концентрацией
0.01 мМ. наблюдаются только
наблюдались в растворах с избытком полимера в
неагрегированные молекулы, а образование агре-
диапазоне соотношений VR-Alg от 1:2 до 1:10. В
гатов начинается, когда концентрация Alg в сме-
течение этого срока значения дзета-потенциала
си превышает 0.01 мМ. (рис. 4а). При 8-кратном
данных растворов претерпевали незначительные
избытке Alg размер агрегатов составляет около
изменения.
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 93 № 5 2023
806
КАШАПОВ и др.
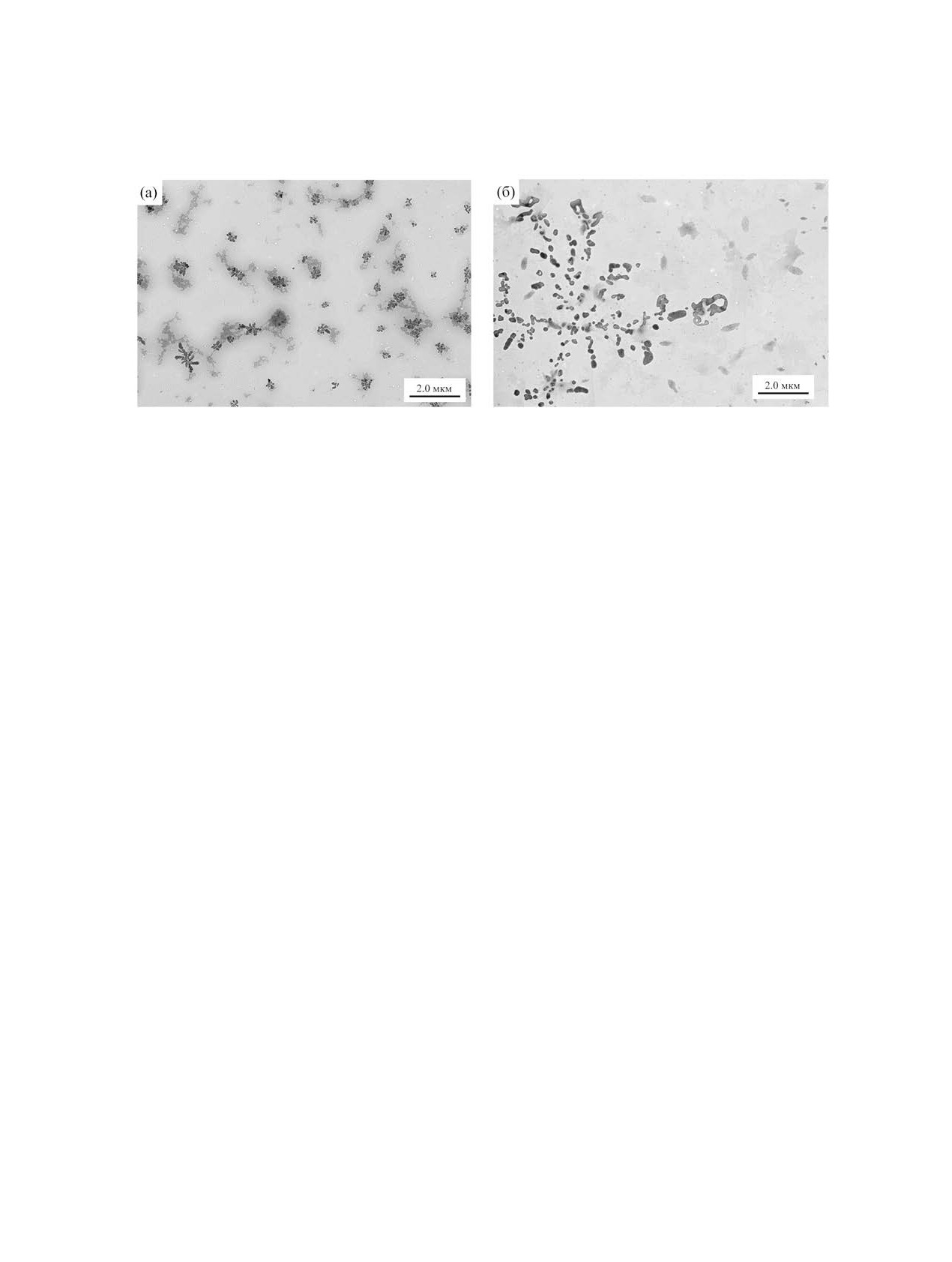
Рис. 5. Изображение ПЭМ для агрегатов, образованных в водной среде VR:Alg = 1:1 (а) и VR:Alg = 1:20 (б).
Убедившись с помощью ДРС в том, что добав-
блюдается как для индивидуального амфифильно-
ление VR в водный раствор Alg приводит к фор-
го раствора виологена [51], так и для смешанных
мированию совместных агрегатов, для смешан-
агрегатов с сульфокаликс[4]ареном [52].
ных систем с соотношением VR:Alg = 1:1 (рис.
Измерение дзета-потенциала частиц в раство-
5а) и 1:20 (рис. 5б) были получены микрофотогра-
рах VR-Alg проводили методом электрофоре-
фии просвечивающей электронной микроскопии
тического рассеяния света. В смеси с избытком
(ПЭМ). На данных фотографиях видно наличие
VR наблюдается положительное значение дзе-
несферических агрегатов, размер которых воз-
та-потенциала, обусловленное присутствием ви-
растает при увеличении доли полимера, что со-
ологеновых групп макроцикла. Добавление пер-
относится с данными ДРС. Несферическая форма
вых порций Alg к постоянному количеству VR
агрегатов может свидетельствовать об образова-
(0.01 мМ.) до достижения соотношения 1:7 незна-
нии супрамолекулярных полимеров как в случае
чительно влияет на положительное значение дзе-
формирования комплексов каликс[4]арена с солью
та-потенциала агрегатов (рис. 4б) несмотря на то,
виологена [50]. Однако метод ДРС выявил нали-
что в этом диапазоне соотношений уже наблюда-
чие одномодального распределения частиц для эк-
ется формирование агрегатов и появление мутно-
вимолярной смеси и бимодального распределения
сти (рис. 1а). Затем с увеличением доли Alg наблю-
для смеси с избытком Alg с хорошими корреляци-
дается резкая перезарядка смешанной системы, и
онными функциями и низкими значениями индек-
при соотношении VR:Alg = 1:8 дзета-потенциал
са полидисперсности, что свидетельствует о нали-
частиц составляет уже -29 мВ. При последующем
чии в растворе однородных сферических частиц.
увеличении концентрации полимера значение дзе-
На полученных микрофотографиях также иденти-
та-потенциала постепенно снижается в сторону
фицируется небольшое количество сферических
отрицательных значений, что обусловлено избыт-
частиц, поэтому не стоить исключать их образо-
ком отрицательно заряженных ацетатных групп
вание в растворе. Преобладание удлиненных агре-
Alg. Таким образом, комплексом физико-химиче-
гатов на изображениях ПЭМ обусловлено тем, что
ских методов показано то, что в супрамолекуляр-
удаление растворителя во время пробоподготовки
ных системах на основе VR и Alg формируются
изменяет реальные концентрации компонентов.
наночастицы за счет межмолекулярных электро-
статических взаимодействий.
Уменьшение содержания воды в образце сопрово-
ждается дегидратацией полярных групп молекул и
Наночастицы на основе VR-Alg были проте-
сближением агрегатов. Аналогичный эффект на-
стированы в качестве солюбилизаторов биологи-
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 93 № 5 2023
СУПР
АМОЛЕКУЛЯРНЫЕ СИСТЕМЫ
807
Рис. 6. Солюбилизация кверцетина в растворах Alg (1) и 0.01 мМ. VR-Alg (2, а), VR (1) и 0.1 мМ. Alg-VR (2, б) при 25°С.
чески активных субстратов. В качестве одного из
В отличие от кверцетина другой липофильный
них был использован гидрофобный антиоксидант
субстрат, олеиновая кислота, не имеет характери-
кверцетин. Кверцетин может связываться с инди-
стических полос поглощения и не флуоресцирует,
видуальным макроциклом в водной среде даже
поэтому было исследовано влияние олеиновой
при концентрациях макроцикла ниже ККА не
кислоты на интенсивность полосы поглощения
только за счет солюбилизации в гидрофобной об-
при 264 нм, относящейся к вVR в составе смеси с
ласти агрегатов VR, но также благодаря взаимо-
Alg при различных соотношениях VR-Alg. Добав-
действию с виологеновыми группами [47]. В ряде
ление олеиновой кислоты к макроциклу снижает
опубликованных работ было показано, что квер-
интенсивность его поглощения при 264 нм. Были
цетин может инкапсулироваться в наночастицы
исследованы три смешанных системы VR-Alg с
на основе Alg за счет водородных связей [53, 54].
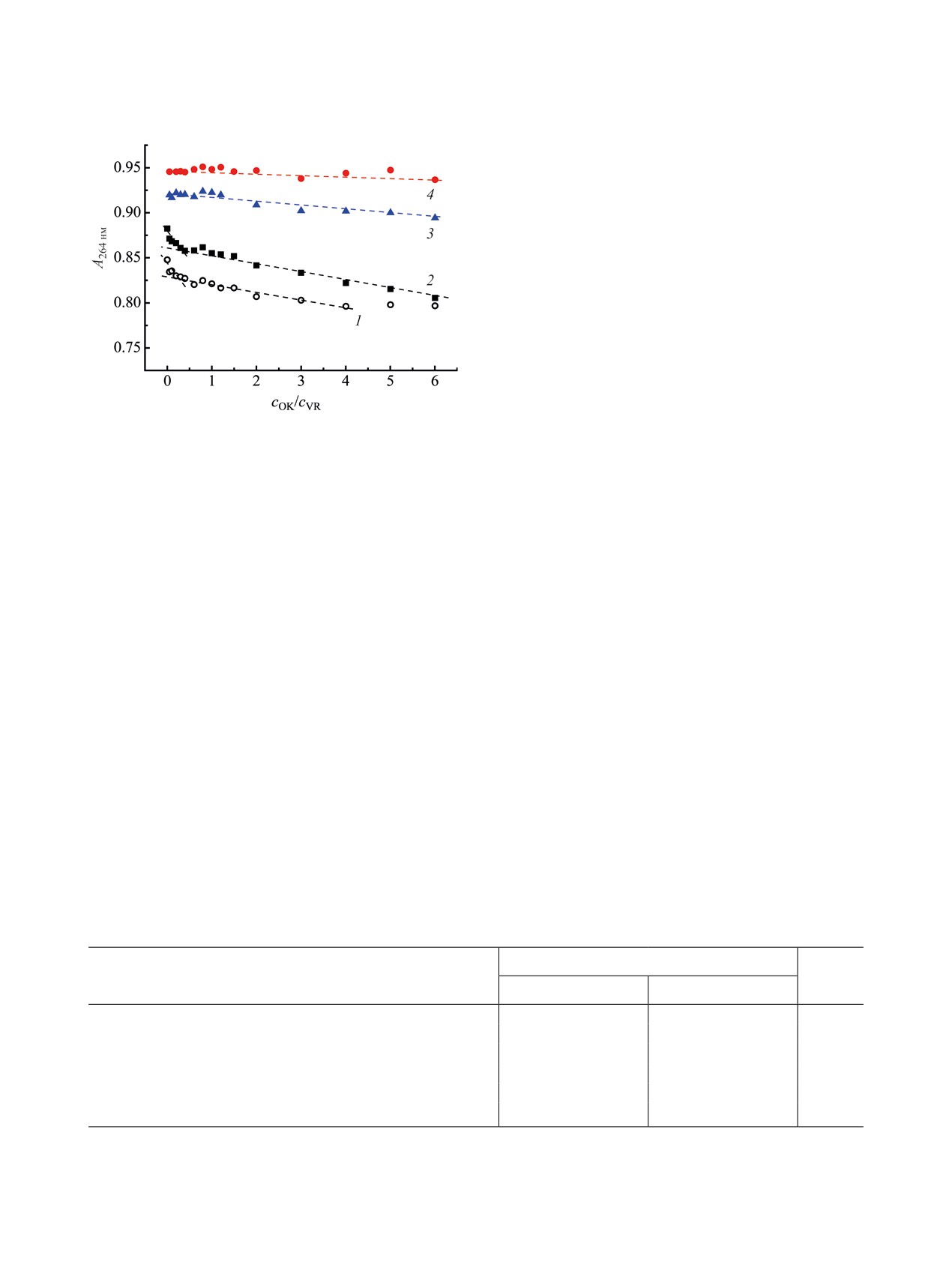
соотношением компонентов 1:1, 1:8 и 1:50 (рис. 7,
Тем не менее проведенный нами эксперимент по-
S3, см. Дополнительные материалы). Для систем
казал, что количество субстрата, связываемого ин-
с избытком Alg влияние олеиновой кислоты на
дивидуальным Alg, очень мало, что указывает на
интенсивность полосы поглощения макроцикла
отсутствие гидрофобных доменов в структуре по-
очень слабое, и наибольшее влияние олеиновой
лимера вследствие его малой концентрации (рис.
кислоты наблюдается на эквимолярную смесь,
6а, S2, см. Дополнительные материалы). Было по-
причем поглощение снижается при добавлении
казано, что присутствие Alg в смеси 0.01 мМ. VR-
олеиновой кислоты так же, как и в случае инди-
Alg приводит к увеличению солюбилизационней
видуального VR. Вероятно, основным фактором,
емкости (рис. 6а), что свидетельствует об увели-
обусловливающим возможность взаимодействия
ченном объеме гидрофобного домена смешанных
олеиновой кислоты и VR в составе комплекса c
систем по сравнению с агрегатами на основе ин-
Alg, являются положительный дзета-потенциал
дивидуального макроцикла. При сравнении солю-
совместных агрегатов, способствующий взаимо-
билизационной емкости индивидуального VR и
действию с карбоксильной группой олеиновой
смеси с постоянной долей Alg (0.1 мМ.) наблюда-
кислоты, и наличие гидрофобных доменов, фор-
мируемых н-додецильными группами VR (рис. 5а).
ется незначительное увеличение количества рас-
творенного кверцетина в смеси, но после дости-
После проведения исследования супрамолеку-
жения эквимолярного соотношения компонентов
лярной системы на основе VR и Alg обширным ком-
солюбилизация флавоноида в этой смеси иден-
плексом физико-химических методов были подго-
тична наблюдаемой в индивидуальном растворе
товлены образцы для скрининга биологических
(рис. 6б).
свойств. Водные растворы индивидуальных квер-
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 93 № 5 2023
808
КАШАПОВ и др.
нове эквимолярного комплекса не оказывает
существенного влияния на проявление цитотокси-
ческого действия, за исключением случая инкапсу-
лированной олеиновой кислоты по отношению к
Chang liver. Небольшое усиление клеточной ток-
сичности в данном случае, согласно литературным
данным, может быть обусловлено способностью
олеиновой кислоты увеличивать продукцию АТФ
и одновременно расширять митохондрии [55].
Таким образом, изучена агрегация Alg в сме-
шанной системе VR-Alg в водной среде. Благодаря
электростатическим взаимодействиям между вио-
логеновыми группами VR и ацетатными группами
Alg самопроизвольно формируются функциональ-
Рис. 7. Зависимость поглощения при 264 нм в водных
ные наночастицы без использования органических
растворах индивидуального раствора VR и смесей
растворителей, температурного и ультразвукового
VR-Alg с различными соотношениями компонентов
от концентрации олеиновой кислоты (l 10 мм, 25°С).
воздействия. Размер и свойства данных частиц
1 - 0.01 мМ. VR-OK, 2 - 0.01 мМ. VR-0.01 мМ.
зависят от соотношения компонентов в системе,
Alg-OK, 3 - 0.01 мМ. VR-0.08 мМ. Alg-OK, 4 -
прежде всего, от соотношения их зарядов. Полу-
0.01 мМ. VR-0.50 мМ. Alg-OK.
ченные наночастицы способны инкапсулировать
липофильные биологически активные вещества и
значительно улучшать их растворимость в воде и,
цетина и олеиновой кислоты были приготовлены
как следствие, биодоступность. Возможность ре-
с использованием 2%-ного этанола и обладали по-
гулировать физико-химические свойства агрегатов
ниженным индексом селективности, которое рас-
на основе VR-Alg, контролируя соотношение ком-
считывается как отношение значения концентра-
понентов, предлагает путь к рациональному полу-
ции, вызывающей гибель 50% нормальных клеток
чению биосовместимых композиций, способных
Chang liver (IC50), к значению IC50 для опухолевых
повысить растворимость липофильных биологи-
клеток М-HeLa. Индивидуальный Alg не цитоток-
чески активных веществ в водных растворах.
сичен, а его эквимолярный комплекс с VR проявля-
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
ет цитотоксическое действие c небольшой селек-
тивностью по отношению к опухолевым клеткам
Подробности синтеза VR описаны в работе
(табл. 1). Наличие гидрофобных субстратов (квер-
[47]. Альгинат натрия (Acros Organics), кверцетин
цетина и олеиновой кислоты) в агрегатах на ос-
(95%, Acros Organics) и олеиновую кислоту (99%,
Таблица 1. Цитотоксичность индивидуальных растворов Alg, кверцетина и олеиновой кислоты, эквимолярной
системы VR-Alg в отсутствие и в присутствии солюбилизированных субстратов кверцетина и ОК, а также значения
индекса селективности (ИС)
IC50(Alg), мМ.
Композиция
ИС
M-HeLa
Chang liver
Alg
>0.05
>0.05
-
Кверцетин
0.07±0.006
0.03±0.001
0.42
Oлеиновая кислота
0.33±0.2
0.22±0.1
0.66
VR-Alg
0.046±0.004
0.051±0.004
1.11
VR-Alg-кверцетин
0.048±0.003
0.05±0.004
1.04
VR-Alg-олеиновая кислота
0.048±0.003
0.036±0.002
0.75
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 93 № 5 2023
СУПР
АМОЛЕКУЛЯРНЫЕ СИСТЕМЫ
809
Alfa Aesar) использовали без дополнительной
точной пролиферации - МТТ-теста [56]. Клетки
очистки. Растворы готовили в деионизированной
высевали на 96-луночный планшет фирмы Nunc
воде (18.2 MΩ), полученной на системе очистки
в концентрации 5×103 клеток на лунку в объеме
воды Millipore Direct-Q 5 UV (Molsheim, Фран-
100 мкл среды и культивировали в СО2-инкубато-
ция). Растворы полимера и макроцикла готовили
ре при 37°С до образования монослоя. Затем пи-
путем растворения твердой навески вещества в
тательную среду удаляли, и в лунки вносили по
определенном объеме воды при перемешивании
100 мкл растворов испытуемых образцов в за-
на магнитной мешалке в течение 30 мин. Сме-
данных разведениях, которые готовили непо-
шанные растворы VR-Alg готовили простым сме-
средственно в питательной среде. Через 24 ч ин-
шиванием различных объемов исходных водных
кубации клеток с тестируемыми соединениями
растворов полимера и макроцикла в определенном
питательную среду удаляли с планшетов, добавляли
соотношении.
100 мкл питательной среды без сыворотки с МТТ
Для определения электропроводности исполь-
в концентрации 0.5 мг/мл и инкубировали 4 ч при
зовался кондуктометр InoLab Cond 720 (WTW
37°С. Затем в каждую лунку к кристаллам фор-
GmbH, Германия), оснащенный графитовым элек-
мазана добавляли по 100 мкл ДМСО. Оптиче-
тродом. Для измерения рН растворов использовали
скую плотность регистрировали при длине волны
рН-метр HI 2110 (Hanna Instruments, США). Все из-
540 нм на планшетном-ридере Invitrologic (Рос-
мерения проводили при 25°C, повторяли не менее
сия). Значения IC50 были рассчитаны с использо-
трех раз и определяли среднее значение. Размеры
ванием онлайн-калькулятора MLA - Quest Graph™
частиц и их дзета-потенциал измеряли на анали-
IC50 Calculator AAT Bioquest, Inc. (AAT Bioquest
заторе частиц Zetasizer Nano (Malvern Instruments,
Великобритания). Спектры поглощения измеряли
aatbio.com/tools/ic50-calculator).
Эксперименты
в кварцевых кюветах толщиной 1 и 10 мм с помо-
были повторены трижды, и результаты представ-
щью спектрофотометра Specord 250 Plus (Analytic
лены как среднее значение ± стандартное отклоне-
Jena, Германия) при 25 °C. Изображения ПЭМ по-
ние. Эксперименты с животными не проводились.
лучали с помощью просвечивающего электронно-
ИНФОРМАЦИЯ ОБ АВТОРАХ
го микроскопа Hitachi HT7800 (Hitachi, Япония).
Микроскоп работал при ускоряющем напряжении
Кашапов Руслан Равилевич, ORCID: https://
80 кВ. Перед съемкой 5 мкл раствора помещали на
orcid.org/0000-0002-8019-353X
покрытую формваром медную сетку диаметром
Разуваева Юлия Сергеевна, ORCID: https://
3 мм, после чего высушивали при комнатной тем-
orcid.org/0000-0003-1417-7416
пературе в течение 24 ч.
Зиганшина Альбина Юлдузовна, ORCID:
Для экспериментов по цитотоксичности ис-
пользовали культуру опухолевых клеток М-HeLa
Сапунова Анастасия Сергеевна, ORCID: https://
клон 11 (эпителиоидный рак шейки матки, субли-
orcid.org/0000-0002-4355-1430
ния HeLa, клон М-HeLa из коллекции Института
Волошина Александра Дмитриевна, ORCID:
цитологии РАН (Санкт-Петербург) и линию кле-
ток печени человека (Chang liver) из коллекции На-
учно-исследовательском институте вирусологии
Сальников Вадим Владимирович, ORCID:
РАМН (Москва). Клетки культивировали на стан-
дартной питательной среде Игла, изготовленной в
Захарова Люция Ярулловна, ORCID: https://
Институте полиомиелита и вирусных энцефали-
orcid.org/0000-0002-2981-445X
тов им. М.П. Чумакова РАН (компания «ПанЭко»),
ФИНАНСОВАЯ ПОДДЕРЖКА
с добавлением 10% эмбриональной телячьей сы-
воротки и 1% незаменимых аминокислот.
Работа выполнена при финансовой поддерж-
Цитотоксическое действие на клетки опреде-
ке Российского научного фонда (грант № 22-73-
ляли с помощью колориметрического метода кле-
10050).
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 93 № 5 2023
810
КАШАПОВ и др.
КОНФЛИКТ ИНТЕРЕСОВ
Wong M. // Biomater. Sci. 2017. Vol. 5. P. 1756. doi
10.1039/c7bm00341b
Л.Я. Захарова является членом редколлегии
15.
Dang W., Wang Y., Chen W.C., Ju E., Mintz R.L., Teng Y.,
Журнала общей химии. Остальные авторы заявля-
Zhu L., Wang K., Lv S., Chan H.F., Tao Y., Li M. // ACS
ют об отсутствии конфликта интересов
Appl. Mater. Interfaces. 2023. Vol. 15. P. 4911. doi
10.1021/acsami.2c18494
ДОПОЛНИТЕЛЬНЫЕ МАТЕРИАЛЫ
16.
Biopolymer Membranes and Films / Eds M.A. de
Moraes, C.F. da Silva, R.S. Vieira. New York: Elsevier,
Дополнительные материалы для этой статьи
2020. P. 273.
доступны по doi
10.31857/S0044460X23050153
17.
Eroǧlu M., Kurşaklioǧlu H., Misirli Y., Iyisoy A., Acar A.,
для авторизованных пользователей.
Işin Doǧan A., Denkba E.B. // J. Microencapsul. 2006.
Vol. 23. P. 367. doi 10.1080/02652040500286318
СПИСОК ЛИТЕРАТУРЫ
18.
Lawrie G., Keen I., Drew B., Chandler-Temple A.,
Rintoul L., Fredericks P., Grøndahl L.
/ /
1.
Kashapov R., Gaynanova G., Gabdrakhmanov D.,
Biomacromolecules. 2007. Vol. 8. P. 2533. doi 10.1021/
Kuznetsov D., Pavlov R., Petrov K., Zakharova L.,
bm070014y
Sinyashin O. // Int. J. Mol. Sci. 2020. Vol. 21. P. 6961.
19.
Yoncheva K., Tzankov B., Yordanov Y., Spassova I.,
doi 10.3390/ijms21186961
2.
Polymer-Surfactant Systems / Ed. J.C.T. Kwak. New
Kovacheva D., Frosini M., Valoti M., Tzankova V. // J.
York: CRC Press, 2020. 500 p.
Drug. Deliv. Sci. Technol. 2020. Vol. 59. P. 101870. doi
10.1016/j.jddst.2020.101870
3.
Chavanpatil M.D., Khdair A., Panyam J. // Pharm. Res.
2007. Vol. 24. P. 803. doi 10.1007/s11095-006-9203-2
20.
Azumah J., Smistad G., Hiorth M. // Colloids Surf.
4.
Khan N., Brettmann, B. // Polymers. 2019. Vol. 11.
(A). 2022. Vol. 653. P. 129924. doi 10.1016/j.
P. 51. doi 10.3390/polym11010051
colsurfa.2022.129924
5.
Lee K.Y., Mooney D.J. // Prog. Polym. Sci. 2012.
21.
Prabha G., Raj V. // Mater. Sci. Eng. (C). 2017. Vol. 79.
Vol. 37. P. 106. doi 10.1016/j.progpolymsci.2011.06.003
P. 410. doi 10.1016/j.msec.2017.04.075
6.
Gurikov P., Smirnova I. // Gels. 2018. Vol. 4. P. 14. doi
22.
Maity S., Mukhopadhyay P., Kundu P.P., Chakra-
10.3390/gels4010014
borti A.S. // Carbohydr. Polym. 2017. Vol. 170. P.124.
7.
Uyen N.T.T., Hamid Z.A.A., Tram N.X.T., Ahmad N. //
doi 10.1016/j.carbpol.2017.04.066
Int. J. Biol. Macromol. 2020. Vol. 153. P. 1035. doi
23.
Khan M.A., Yue C., Fang Z., Hu S., Cheng H.,
10.1016/j.ijbiomac.2019.10.233
Bakry A.M., Liang L. // J. Food Eng. 2019. Vol. 258.
8.
Massana Roquero D., Bollella P., Katz E., Melman A. //
P. 45. doi 10.1016/j.jfoodeng.2019.04.010
ACS Appl. Polym. Mater. 2021. Vol. 3. P. 1499. doi
24.
Ayaz F., Alas M.O., Genc R. // Inflammation. 2020.
10.1021/acsapm.0c01358
Vol. 43. P. 777. doi 10.1007/s10753-019-01165-0
9.
Abasalizadeh F., Moghaddam S.V., Alizadeh E.,
25.
Guzmán E., Llamas S., Maestro A., Fernández-
Akbari E., Kashani E., Fazljou S.M.B., Torbati M.,
Peña L., Akanno A., Miller R., Ortega F., Rubio R.G. //
Akbarzadeh A. // J. Biol. Eng. 2020. Vol. 14. P. 17. doi
Adv. Colloid. Interface Sci. 2016. Vol. 233. P. 38. doi:
10.1186/s13036-020-00239-0
10.1016/j.cis.2015.11.001
10.
Sabater I Serra R., Molina-Mateo J., Torregrosa-
26.
Holmberg K., Jönsson B., Kronberg B., Lindman B.
Cabanilles C., Andrio-Balado A., Dueñas J.M.M.,
Surfactants and Polymers in Aqueous Solutions.
Serrano-Aroca Á. // Polymers. 2020. Vol. 12. P. 702.
Chichester: Wiley, 2002. 545 p.
doi 10.3390/polym12030702
27.
Mirtič J., Paudel A., Laggner P., Hudoklin S.,
11.
Straccia M.C., D’Ayala G.G., Romano I., Laurienzo P. //
Kreft M.E., Kristl J. // Int. J. Pharm. 2020. Vol. 580.
Carbohydr. Polym. 2015. Vol. 125. P. 103. doi 10.1016/j.
P. 119199. doi 10.1016/j.ijpharm.2020.119199
carbpol.2015.03.010
28.
Somasundaran P., Chakraborty S., Qiang Q., Deo P.,
12.
Li S., Wang X., Chen J., Guo J., Yuan M., Wan G., Yan C.,
Wang J., Zhang R. // Int. J. Cosmet. Sci. 2005. Vol. 27.
Li W., Machens H.G., Rinkevich Y., Yang X., Song H.,
P. 135. doi 10.1111/j.1467-2494.2005.00257_2.x
Chen Z. // Int. J. Biol. Macromol. 2022. Vol. 202.P. 657.
29.
Llamas S., Guzmán E., Ortega F., Baghdadli N.,
doi 10.1016/j.ijbiomac.2022.01.080
Cazeneuve C., Rubio R.G., Luengo G.S. // Adv. Colloid.
13.
Pasparakis G., Bouropoulos N. // Int. J. Pharm. 2006
Interface Sci. 2015. Vol. 222. P. 461.
Vol. 323. P. 34. doi 10.1016/j.ijpharm.2006.05.054
30.
Zhao L., Wang J., Zhang X., Guo X., Chen L., Zhang
14.
Kerschenmeyer A., Arlov Ø., Malheiro V., Steinwachs M.,
A., Cao K., Li J. // J. Pet. Explor. Prod. Technol. 2022.
Rottmar M., Maniura-Weber K., Palazzolo G., Zenobi-
Vol. 13. P. 853. doi 10.1007/s13202-022-01564-4
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 93 № 5 2023
СУПР
АМОЛЕКУЛЯРНЫЕ СИСТЕМЫ
811
31.
Wu Q., Ding L., Zhang L., Ge J., Rahman M.A.,
45.
Carvalho C., Moreira P.I. // Curr. Opin. Neurobiol. 2023.
Economou I.G., Guérillot D. // Energy. 2023. Vol. 264.
Vol. 79. P. 102694. doi 10.1016/j.conb.2023.102694
P. 126256. doi 10.1016/j.energy.2022.126256
46.
Hazra R., Novelli E.M., Hu X. // CNS Neurosci. Ther.
32.
Kralova I., Sjöblom J. // J. Dispers. Sci. Technol. 2009.
2023. Vol. 29. P. 783. doi 10.1111/cns.14068
Vol. 30. P. 1363. doi 10.1080/01932690902735561
47.
Kashapov R., Razuvayeva Y., Ziganshina A., Sapunova A.,
33.
Handbook of Nutraceuticals and Natural Products:
Lyubina A., Amerhanova S., Kulik N., Voloshina A.,
Biological, Medicinal, and Nutritional Properties and
Nizameev I., Salnikov V., Zakharova L. // J. Mol.
Applications / Eds P. Balakrishnan, S. Gopi. Hoboken:
Liq. 2022. Vol. 345. P. 117801. doi 10.1016/j.
Wiley, 2022. P. 363.
molliq.2021.117801
34.
Mirtič J., Ilaš J., Kristl J. // Carbohydr. Polym. 2018.
48.
Kashapova N.E., Kashapov R.R., Ziganshina A.Y.,
Vol. 181. P. 93. doi 10.1016/j.carbpol.2017.10.040
Nikitin D.O., Semina I.I., Salnikov V.V., Khutoryan-
35.
Yang J., Chen S., Fang Y. // Carbohydr. Polym. 2009.
skiy V. V., Moustafine R.I., Zakharova L.Y. //
Vol. 75. P. 333. doi 10.1016/j.carbpol.2008.07.037
Pharmaceutics. 2023. Vol. 15. P. 921. doi 10.3390/
36.
Degen P., Paulus M., Zwar E., Jakobi V., Dogan S.,
pharmaceutics15030921
Tolan M., Rehage H. // Surf. Interface. Anal. 2019.
49.
Kashapov R., Razuvayeva Y., Ziganshina A., Lyubina A.,
Vol. 51. P. 1051. doi 10.1002/sia.6691
Amerhanova S., Sapunova A., Voloshina A.,
37.
Neumann M.G., Schmitt C.C., Iamazaki E.T. //
Carbohydr. Res. 2003. Vol. 338. P. 1109. doi 10.1016/
Nizameev I., Salnikov V., Zakharova L. // Colloids
S0008-6215(03)00051-X
Surf. (A). 2022. Vol. 648. P. 129330. doi 10.1016/j.
38.
Hoque M.A., Mahbub S., Khan M.A., Eldesoky G.E.
colsurfa.2022.129330
// J. Dispers. Sci. Technol. 2022. Vol. 43. P. 1039. doi
50.
Pescatori L., Arduini A., Pochini A., Secchi A.,
10.1080/01932691.2020.1847661
Massera C., Ugozzoli F. // Org. Biomol. Chem. 2009.
39.
Morozova J.E., Myaldzina C.R., Voloshina A.D.,
Vol. 7. P. 3698. doi 10.1039/B906409E
Lyubina A.P., Amerhanova S.K., Syakaev V.V.,
51.
Lv Z.-P., Chen B., Wang H.-Y., Wu Y., Zuo J.-L. // Small.
Ziganshina A.Yu., Antipin I.S. // Colloids Surf. (A). 2022.
2015. Vol. 11. P. 3597. doi 10.1002/smll.201500090
Vol. 642. P. 128622. doi 10.1016/j.colsurfa.2022.128622
52.
Wang K., Guo D.-S., Wang X., Liu Y. // ACS Nano. 2011.
40.
Mirtič J., Kogej K., Baumgartner S., Smistad G.,
Vol. 5. P. 2880. doi 10.1021/nn1034873
Kristl J., Hiorth M. // Int. J. Pharm. 2016. Vol. 511.
53.
Chen Y.-B., Zhang Y.-B., Wang Y.-L., Kaur P.,
P. 774. doi 10.1016/j.ijpharm.2016.07.065
Yang B.-G., Zhu Y., Ye L., Cui Y.L. // J. Nanobiotechnol.
41.
Ahmady A.R., Solouk A., Saber-Samandari S.,
2022. Vol. 20. P. 272. doi 10.1186/s12951-022-01452-3
Akbari S., Ghanbari H., Brycki B.E. // J. Colloid.
54.
Qi Y., Jiang M., Cui Y.L., Zhao L., Zhou X. // Nanoscale
Interface. Sci. 2023. Vol, 638. P. 616. doi 10.1016/j.
Res. Lett. 2015. Vol. 10. P. 408. doi 10.1186/s11671-
jcis.2023.01.139
015-1117-7
42.
Zhao G., Cao K., Xu C., Sun A., Lu W., Zheng Y., Li H.,
55.
Park E.-J., Lee A.Y., Chang S.-H., Yu K.-N., Kim J.-H.,
Hong G.L., Wu B., Qiu Q.M., Lu Z. // Int. J. Biol. Sci.
Cho M.-H. // Toxicol. Lett. 2014. Vol. 224. P. 114. doi
2017. Vol. 13, P. 888. doi 10.7150/ijbs.18468
10.1016/j.toxlet.2013.09.018
43.
Liu A.-R., Lv Z., Yan Z.-W., Wu X.-Y., Yan L.-R.,
Sun L.-P., Yuan Y., Xu Q. // J. Transl. Med. 2023.
56.
Smolobochkin A.V., Gazizov A.S., Yakhshilikova
Vol. 21. P. 27. doi 10.1186/s12967-023-03878-1
L.J., Bekrenev D.D., Burilov A.R., Pudovik M.A.,
44.
Yu X., Yang Y., Chen T., Wang Y., Guo T., Liu Y., Li H.,
Lyubina A.P., Amerhanova S. K., Voloshina A.D. //
Yang L. // Front. Cell. Dev. Biol. 2023. Vol. 11.
Chem. Biodiversity. 2022. Vol. 19. P. e202100970. doi
P. 1075917. doi 10.3389/fcell.2023.1075917
10.1002/cbdv.202100970
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 93 № 5 2023
812
КАШАПОВ и др.
Supramolecular Systems Based on Sodium Alginate
and Viologen Calyx[4]resorcinol for Encapsulation
of Hydrophobic Compounds
R. R. Kashapova,*, Yu. S. Razuvaevaa, A. Yu. Ziganshinaa, A. S. Sapunovaa,
A. D. Voloshinaa, V. V. Salnikovb, and L. Ya. Zakharovaa
a A.E. Arbuzov Institute of Organic and Physical Chemistry, Federal Research Center
“Kazan Scientific Center of the Russian Academy of Sciences”, Kazan, 420088 Russia
b Kazan Institute of Biochemistry and Biophysics, Federal Research Center
“Kazan Scientific Center of the Russian Academy of Sciences”, Kazan, 420111 Russia
*e-mail: kashapov@iopc.ru
Received April 14, 2023; revised April 14, 2023; accepted April 17, 2023
The work is devoted to the study of a supramolecular system based on viologen calix[4]resorcinol and sodium
alginate in an aqueous medium using a set of physicochemical methods. It was established that sodium alginate
and viologen calix[4]resorcinol form stable nanoparticles capable of encapsulating hydrophobic biologically
active substances in the range of macrocycle:polymer concentration ratios from 1:2 to 1:10. The study of the
cytotoxic properties of these nanoparticles in the presence of encapsulated substrates showed an increase in
the selectivity of the action of quercetin and oleic acid against M-HeLa tumor cells by 2.47 and 1.14 times,
respectively.
Keywords: calixarene, polymer, self-assembly, complexation, solubilization, cytotoxicity
ЖУРНАЛ ОБЩЕЙ ХИМИИ том 93 № 5 2023