ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ, 2023, том 59, № 7, с. 956-960
КРАТКИЕ СООБЩЕНИЯ
УДК 547.38; 547.333.1
пара-ЗАМЕЩЕННЫЕ АНИЛИНЫ В РЕАКЦИЯХ
С СОЛЯМИ ТРОПИЛИЯ И ДИБЕНЗОСУБЕРЕНОЛОМ
© 2023 г. Т. А. Акентьева*, С. Н. Жакова
ФГБОУ ВО «Пермский государственный аграрно-технологический университет им. академика Д.Н. Прянишникова»,
Россия, 614990 Пермь, ул. Петропавловская, 23
*e-mail: akentjeva-perm@yandex.ru
Поступила в редакцию 30.05.2022 г.
После доработки 11.06.2022 г.
Принята к публикации 12.06.2022 г.
Изучены особенности взаимодействия пара-замещенных анилинов с солями тропилия и дибензо-
суберенолом. Взаимодействием пара-замещенных анилинов с солями тропилия (перхлоратом или
тетрафторборатом) в среде этанола или тетрагидрофурана вместо ожидаемых орто-тропилирован-
ных анилинов были получены соответствующие азометины. Цикл тропилидена (1,3,5-циклогепта-
риеновый цикл) подвергся бензилиденовому сужению по причине повышения температуры в ходе
химической реакции. Структурно-родственный цикл тропилидена - дибензосуберен - можно ввести
в орто-положение пара-замещенных анилинов с образованием устойчивых орто-продуктов. Дибен-
зосуберенол в кислой среде способен взаимодействовать с этанолом с образованием простого эфира.
Ключевые слова: соли тропилия, тетрафторборат тропилия, перхлорат тропилия, пара-замещенные
анилины, бензилиденовое сужение 1,3,5-циклогептариенового цикла, дибензосуберенол, имидазол
DOI: 10.31857/S0514749223070108, EDN: HTSEXS
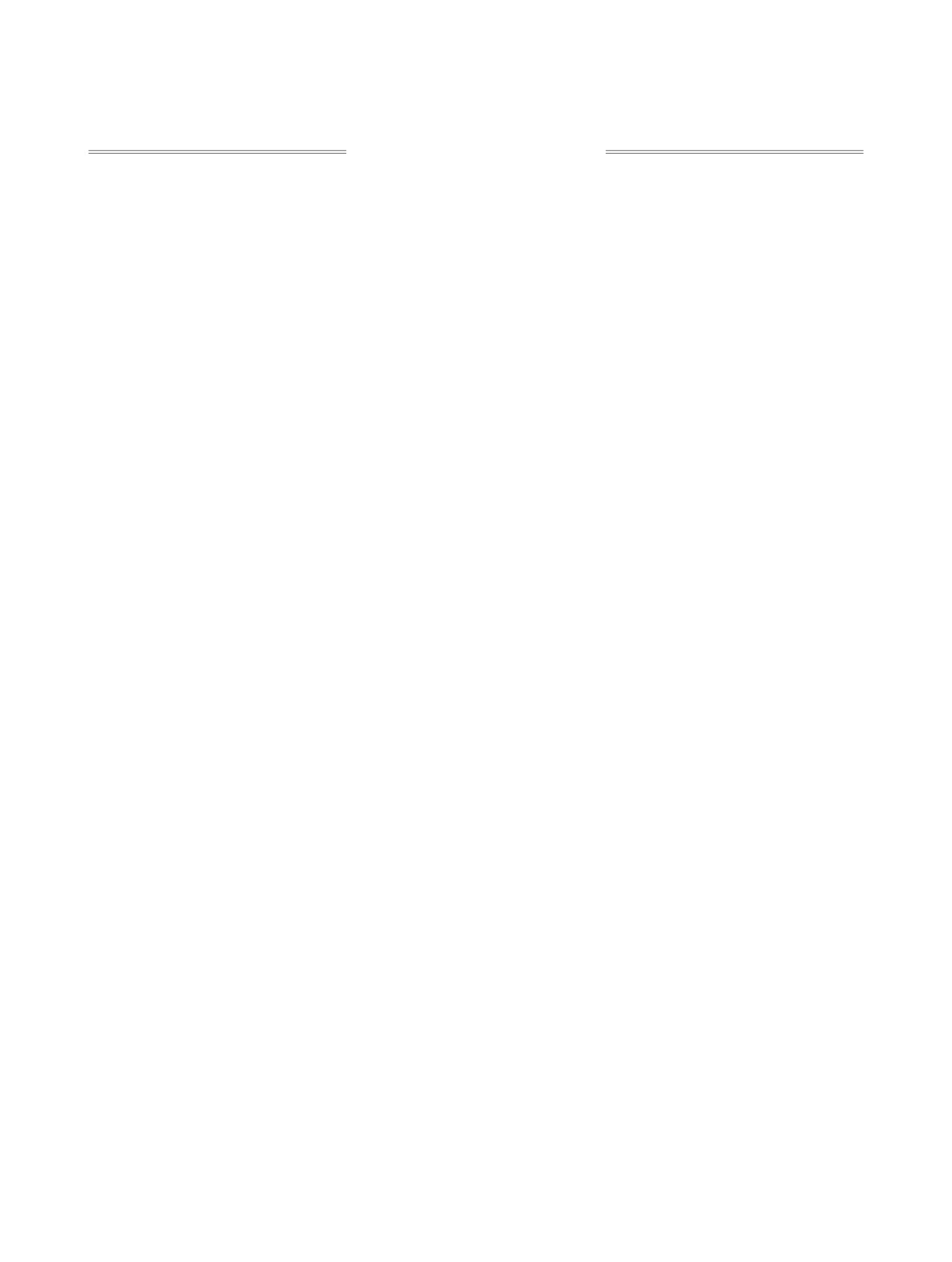
В проведенных ранее исследованиях
[1-6]
ходе дистилляции подвергается изомеризации до
показано, что структурные аналоги 1,3,5-цикло-
соединения 10 (схема 1).
гептатриен (тропилиден) и 5Н-дибензо[a,d]цикло-
Целью работы было изучение взаимодей-
гептен (дибензосуберен) способны образовывать
ствия пара-замещенных анилинов с солями тро-
однотипные структуры 1-6 с анилином, вторич-
пилия и дибензосуберенолом, а также получение
ными ароматическими аминами и азометинами
орто-тропилированных анилинов.
(см. рисунок), однако с пара-замещенными анили-
Взаимодействие катиона тропилия с пара-за-
нами синтезировать ряд орто-продуктов не уда-
мещенными анилинами сопровождается бензи-
лось.
лиденовым сужением
1,3,5-циклогептатриено-
Возможность получения орто-замещенного
вого цикла и образованием азометинов вместо
продукта ранее была показана при взаимодей-
ожидаемых орто-тропилированных продуктов.
ствии пара-броманилина с дибензосубуренолом
Исследовали влияние донорных (OCH3, CH3) или
[6], при этом введение цикла тропилидена сопро-
акцепторных (Br, NO2) заместителей в анилинах,
вождается образованием изомеров. Так, был опи-
противоиона в соли тропилия и растворителя. Ни
сан синтез орто-тропилированного анилина 9 [7]
в одном из изученных случаев не были получены
при взаимодействии пара-толуидина 7а с этокси-
ожидаемые орто-продукты. Так, при взаимодей-
тропилиденом 8, который в процессе выделения в
ствии тетрафторбората тропилия 11а с пара-за-
956
пара-ЗАМЕЩЕННЫЕ АНИЛИНЫ В РЕАКЦИЯХ С СОЛЯМИ ТРОПИЛИЯ
957
H2N
H2N
1
CH
N
2
R
3
CH
N
R
CH2 NH
R
5
4
CH2 NH
R
6
3-6, R = CH3 (a), Br (b), NO2 (c), OCH3 (d).
ɐɢɤɥɨɝɟɩɬɚ
ɬɪɢɟɧɢɥ ɚɧɢɥɢɧ ɬɪɨɩɢɥɢɪɨɜɚɧɧɵɣ ɚɧɢɥɢɧ
ɇ Ⱦɢɛɟɧɡɨ>a,d@ɰɢɤɥɨɝɟɩɬɟɧ ɢɥ ɚɧɢɥɢɧ
1
3. N Ⱥɪɢɥɦɟɬɢɥɟɧ
ɰɢɤɥɨɝɟɩɬɚ
ɬɪɢɟɧɢɥ ɚɧɢɥɢɧɵ
1
4. N Ⱥɪɢɥɦɟɬɢɥɟɧ
ɇ ɞɢɛɟɧɡɨ>ɚ,d@ɰɢɤɥɨɝɟɩɬɟɧ ɢɥ ɚɧɢɥɢɧɵ
1
N Ⱥɪɢɥɦɟɬɢɥ
ɰɢɤɥɨɝɟɩɬɚ
ɬɪɢɟɧɢɥ ɚɧɢɥɢɧɵ
1
6. N Ⱥɪɢɥɦɟɬɢɥ
ɇ ɞɢɛɟɧɡɨ>ɚ,d@ɰɢɤɥɨɝɟɩɬɟɧ ɢɥ ɚɧɢɥɢɧɵ
Амины и азометины с фрагментами тропилидена и дибензосуберена
мещенными ариламинами 7а-d при соотноше-
4-нитроанилин
(12c), N-бензилиден-4-метокси-
нии исходных реагентов амин-тетрафторборат
анилин (12d) с высоким выходом от 70-89%
(схема 2).
тропилия 1:1 были выделены соответствующие
азометины - N-бензилиден-4-метиланилин (12a),
Попытка использовать имидазол в качестве
N-бензилиден-4-броманилин (12b), N-бензилиден-
«перевозчика» (схема 3) для получения целевых
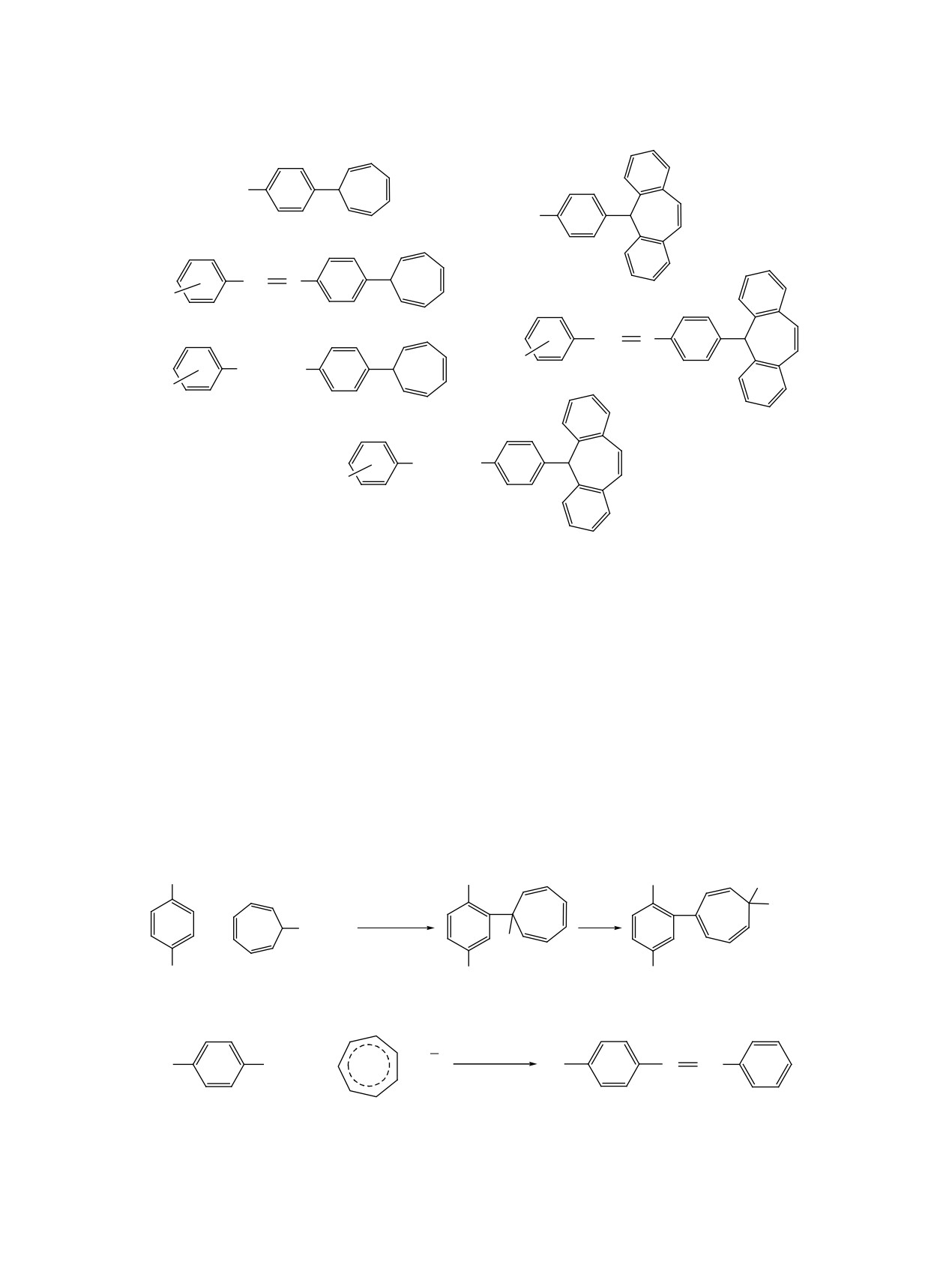
Схема 1
NH2
NH2
NH2
H
H
C2H5OH
+
OC2H
5
HClO4
H
CH3
CH3
CH3
7a
8
9
10
Схема 2
C2H5OH
R
NH2
+
BF4
R
N
CH
+
7a-d
11a
12a-d
R = CH3 (a), Br (b), NO2 (c), OCH3 (d).
ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ том 59 № 7 2023
958
АКЕНТЬЕВА, ЖАКОВА
Схема 3
H
N
ɌȽɎ
R
NH2
+
+
ClO4
+
R
N
CH
N
7a, b, d
11b
13
12a, b, d
R = CH3 (a), Br (b), OCH3 (d).
орто-продуктов оказалась безуспешной. Так, при
замещенных анилинов (схема 4), однако препара-
взаимодействии перхлората тропилия 11b с арил-
тивное выделение целевых продуктов усложняет-
аминами 7a, b, d в среде ТГФ в присутствии акти-
ся процессом диспропорционирования дибензо-
ватора имидазола 13 при использовании исходных
суберенола 14. По данным хроматомасс-спектро-
скопии процесс диспропорционирования сопро-
реагентов амин-перхлорат тропилия-имидазол в
вождается образованием дибензосуберенона
16
соотношении 1:1:0,5 выделены с высоким выхо-
и дибензосуберена 17, что затрудняет выделение
дом азометины 12а, b, d (от 70 до 87%) (схема 3).
соединений 15а, с, d.
Можно предположить, что бензилиденовое су-
Диспропорционирование дибензосуберенола
жение цикла тропилидена происходит в резуль-
удалось существенно снизить при использовании
тате повышения температуры в ходе химической
смешанного растворителя - смеси уксусной кис-
реакции, факт сужения цикла тропилидена под-
лоты и этанола в соотношении 1:1.5. Установлено,
тверждается рядом исследований [8-13].
что при взаимодействии аминов 7a-d образуют-
В отличие от цикла тропилидена, фрагмент ди-
ся преимущественно 2 вещества - ожидаемый
бензосуберена удается ввести в орто-положение
орто-продукт 15а-d и простой эфир 18 (схема 5).
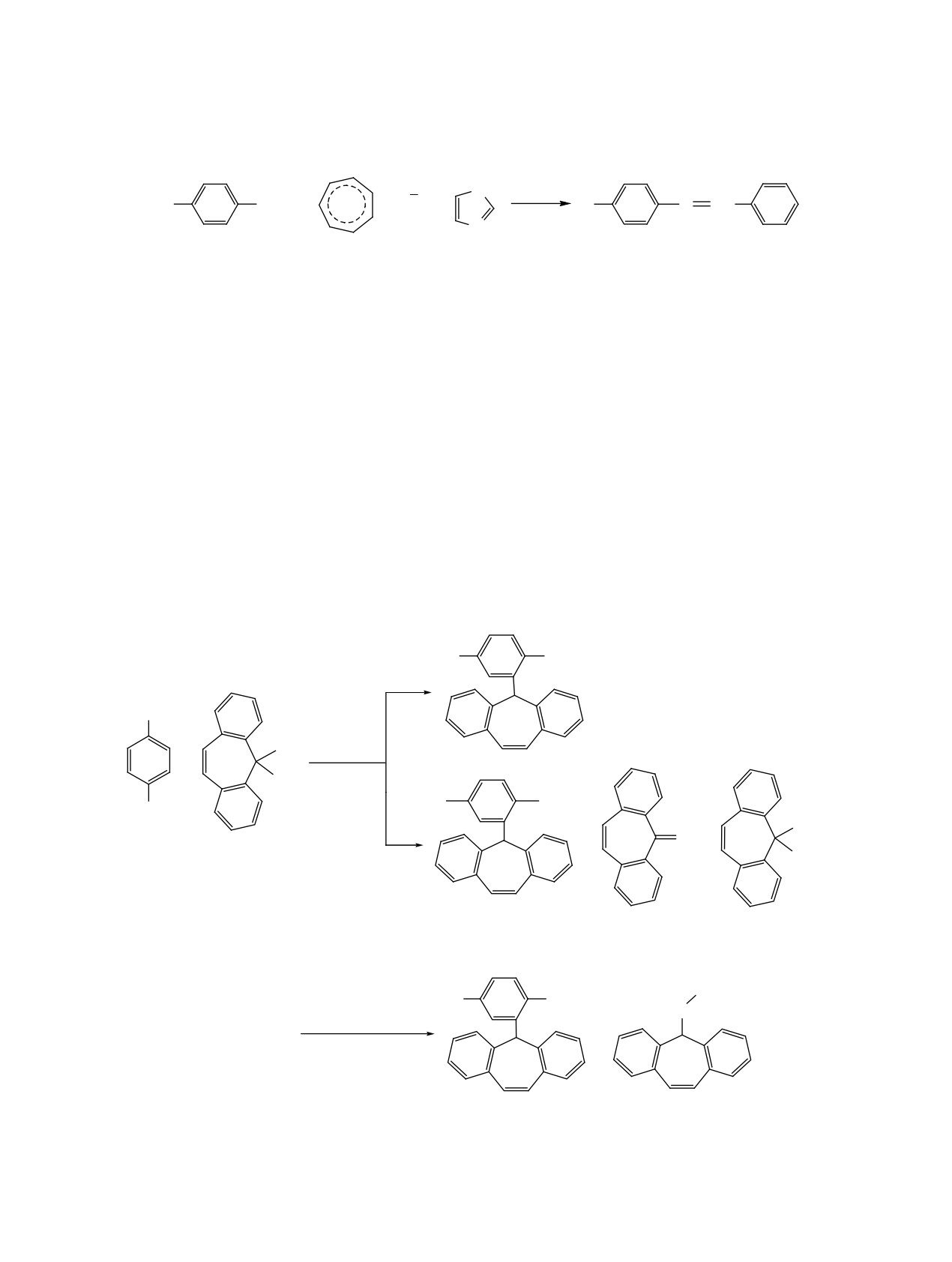
Схема 4
Br
NH2
R
OHCH3COOH
+
15b
H
R
NH2
NH2
H
O
7a-d
14
+
+
H
15a, c, d
16
17
R = CH3 (a), Br (b), NO2 (c), OCH3 (d).
Схема 5
C5H5
R
NH2
O
CH3COOH:C2H5OH
7a-d
+
14
+
15a-d
18
R = CH3 (a), Br (b), NO2 (c), OCH3 (d).
ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ том 59 № 7 2023
пара-ЗАМЕЩЕННЫЕ АНИЛИНЫ В РЕАКЦИЯХ С СОЛЯМИ ТРОПИЛИЯ
959
Препаративно выделить с высоким выходом
пара-анилинов при комнатной температуре не за-
80% удалось только 4-бром-2-(5Н-дибензо[a,d]-
висит от таких факторов как эффект заместителя,
циклогептен-5-ил)анилин 15b. Вещества 15а, c, d
наличие противоиона в соли тропилия или нали-
были определены только в реакционной массе по
чие активатора. Cужение цикла тропилидена в ис-
данным хроматомасс-спектров (соединение 15a -
следуемых условиях происходит в результате по-
12%, соединение 15c - 10%, соединение 15d -
вышения температуры в ходе химической реакции.
36%).
Установлено, что взаимодействие дибензосубере-
нола с пара-замещенными анилинами в уксусной
Соединение 18 также получено в результате
кислоте сопровождается образованием продуктов
«холостого опыта» при кратковременном нагреве
диспропорционирования дибензосуберенола, что
дибензосуберенола 14 в смешанном растворителе
мешает препаративному выделению орто-продук-
(уксусная кислота - этанол, 1:1.5), выход составил
тов
-
4-арил-2-(5Н-дибензо[a,d]циклогептен-5-
83%.
ил)анилинов. Реакция дибензосуберенола с арила-
5-Этокси-4-(5Н-дибензо[a,d]циклогептен)
минами зависит от растворителя. При использова-
(18). К 0.42 г (2 ммоль) дибензосуберенола при-
нии смешанного растворителя (уксусная кислота-
бавляли 3 мл ледяной уксусной кислоты и 4.5 мл
этанол), наряду с орто-продуктом, образуется про-
95%-ного этанола, смесь перемешивали, нагрева-
стой эфир 5-этокси-5Н-дибензо[a,d]циклогептен.
ли в течение 5 минут, охлаждали, разбавляли во-
дой, нейтрализовали 25%-ным аммиаком до рН
БЛАГОДАРНОСТИ
7.0. Выпавшие кристаллы отделяли и перекри-
Авторы выражают благодарность за оказание
сталлизовывали из гексана. Выход 0.40 г (83%).
консультационной помощи профессору кафедры
Белые кристаллы, т.пл. 96-97°С. Спектр ЯМР 1Н
общей химии ФГБОУ ВО «Пермский государ-
(CDCl3), δ, м.д.: 1.34 с (3H, CH3), 3.61 с (2Н, ОСH2),
ственный аграрно-технологический универси-
7.12-7.35 м (11Н, С15Н11). Масс-спектр, m/z (Iотн,
тет имени академика Д.Н. Прянишникова» д.х.н.
%): 236 (40) [М]+, 207 (6), 191 (100). Найдено, %:
Л.П. Юнниковой.
C 86.28; H 6.58. C17H16О. Вычислено, %: C 86.41;
H 6.82.
ФОНДОВАЯ ПОДДЕРЖКА
Физические константы и спектры соединений
Работа выполнена в рамках технологиче-
12a-d и 15b соответствуют приведенным в лите-
ского проекта Пермского НОЦ мирового уров-
ратуре [6, 10, 14, 15].
ня
«Рациональное недропользование»
«Инно-
вационные химические, медицинские и фармацев-
Спектры ЯМР 1Н зарегистрированы на прибо-
тические технологии».
ре Mercury 300 (300 МГц) (фирма Varian, США),
внутренний стандарт ГМДС. Хроматомасс-
ИНФОРМАЦИЯ ОБ АВТОРАХ
спектры получены на приборе Agilent Technologies
6890N/5975В, колонка НР-5ms
(30×0.25 мм,
orcid.org/0009-0004-5768-9336
0.25 мкм, газ носитель - гелий, ионизация элек-
тронным ударом 70 эВ, температура термостата
КОНФЛИКТ ИНТЕРЕСОВ
колонки 100°С). Температура испарителя - 290°С.
Авторы заявляют об отсутствии конфликта ин-
Дибензосуберенол брали в готовом виде (98%, ком-
тересов.
пания, Mikromol, Великобритания). Элементный
СПИСОК ЛИТЕРАТУРЫ
анализ проведен на анализаторе углерода, водо-
рода, азота и серы CHNS-932 (LECO Corporation,
1. Юнникова Л.П., Лихарева Ю.Е., Эсенбаева В.В.
США).
ЖОХ. 2019, 89, 1462-1466. [Yunnikova L.P., Likhare-
va Y.E., Esenbaeva V.V. Russ. J. Gen. Chem. 2019, 89,
ЗАКЛЮЧЕНИЕ
1927-1930.] doi 10.1134/S0044460X1909021X
В ходе тропилирования пара-анилинов солями
2. Юнникова Л.П., Лихарева Ю.Е., Баландина С.Ю.
тропилия установлено бензилиденовое сужение
Изв. Вузов. Сер. Хим. и хим. технол. 2019, 62, 79-84.
цикла тропилидена. Результат тропилирования
[Yunnikova L.P., Likhareva Y.E., Balandina S.Yu. Izv.
ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ том 59 № 7 2023
960
АКЕНТЬЕВА, ЖАКОВА
Vuzov, Ser. Khim. i Khim. Tekhnol. 2019, 62, 79-84.]
7. Takase K., Asao T., Hirata N.A. Bull. Chem. Soc. Jpn.
doi 10.6060/ivkkt.20196202.5751
1968, 41, 3027.
3. Эсенбаева В.В., Юнникова Л.П., Кудаярова Т.В.,
8. Föhlisch B., Haug E. Chem. Ber. 1971, 104, 2324-
Данилова Е.А. ЖОХ. 2018, 88, 2087-2090. [Esenbae-
2337.
va V.V., Yunnikova L.P., Kudayarova T.V., Danilo-
9. Harrison A.G., Honnen L.R., Dauben H.J. Jr., Loss-
va E.A. Russ. J. Gen. Chem. 2018, 88, 2691-2694.] doi
ing F.P. J. Am. Chem. Soc. 1960, 82, 5593-5598. doi
10.1134/S0044460X18120235
10.1021/ja01506a008
4. Юнникова Л.П., Эсенбаева В.В. ЖОрХ. 2018, 54,
10. Katsumi Е., Etsurou S. Bull. Chem. Soc. Jpn. 1969, 42,
1015-1018. [Yunnikova L.P., Esenbaeva V.V. Russ.
2693-2694. doi 10.1246/bcsj.42.2693
J. Org. Chem. 2018, 54, 1018-1022]. doi 10.1134/
11. Blair J.A., Tate C.J. J. Chem. Soc. (C). 1971, 1592-
S1070428018070084
1596.
5. Yunnikova L.P., Esenbaeva V.V., Shklyaeva E.V. Izv.
12. Johnson B.F.G., Lewis J., McArdle P., Randall G.L.P.
Vuzov, Khim. i Khim. Tekhnol. 2018, 61, 48-52. doi
J. Chem. Soc., Dalton Trans. 1972, 4, 456-462. doi
10.6060/ivkkt.20186108.5817
10.1039/DT9720000456
13. Woods W.G. J. Org. Chem. 1958, 23, 110-112. doi
6. Юнникова Л.П., Акентьева Т.А., Александрова Г.А.,
10.1021/jo01095a617
Михайлова Л.А., Елисеев С.Л. Хим.-фарм. ж.
2014, 48, 26-29. [Yunnikova L.P., Akent’eva T.A.,
14. Billman J.H., Diesing A.C. J. Org. Chem. 1957, 22,
Aleksandrova G.A., Mikhailova L.A., Eliseev S.L.
1068-1070. doi 10.1021/jo01360a019
Pharm. Chem. J. 2014, 48, 22-25.] doi 10.1007/
15. Nozomu E. Bull. Chem. Soc. Jpn. 1961, 34, 1151-1158.
s11094-014-1038-2
doi 10.1246/bcsj.34.1151
para-Substituted Anilines in Reactions
with Tropyl Salts and Dibenzosuberenol
T. A. Akent’eva* and S. N. Zhakova
Perm State Agro-Technological University Named after Academician D.N. Pryanishnikov
ul. Petropavlovskaya, 23, Perm, 614000 Russia
*e-mail: akentjeva-perm@yandex.ru
Received May 30, 2022; revised June 11, 2022; accepted June 12, 2022
The features of the interaction of para-substituted anilines with tropyl salts and dibenzosuberenol have been
studied. By the interaction of para-substituted anilines with tropyl salts (perchlorate or tetrafluoroborate) in
an ethanol or tetrahydrofuran medium, the corresponding azomethines were obtained instead of the expected
ortho-tropylated anilines. The tropilidene cycle (1,3,5-cycloheptariene cycle) underwent benzilidene narrowing
due to an increase in temperature during a chemical reaction. The structurally related tropilidene - dibenzosu-
berene cycle can be introduced into the ortho position of para-substituted anilines to form stable ortho products.
Dibenzosuberenol in an acidic environment is able to interact with ethanol to form an ether.
Keywords: tropylium salts, tropylium tetrafluoroborate, tropylium perchlorate, para-substituted anilines, ben-
zylidene contraction of the 1,3,5-cycloheptariene ring, dibenzosuberenol, imidazole
ЖУРНАЛ ОРГАНИЧЕСКОЙ ХИМИИ том 59 № 7 2023