Журнал прикладной химии. 2019. Т. 92. Вып. 11
СОРБЦИОННЫЕ И ИОНООБМЕННЫЕ ПРОЦЕССЫ
УДК 678.675:66.067.38
ВЛИЯНИЕ ПРИРОДЫ ИММОБИЛИЗОВАННЫХ КОМПОНЕНТОВ
НА АДСОРБЦИОННЫЕ И МАССООБМЕННЫЕ СВОЙСТВА
УЛЬТРАФИЛЬТРАЦИОННЫХ МЕМБРАН
НА ОСНОВЕ СУЛЬФОНАТСОДЕРЖАЩЕГО СОПОЛИАМИДА
© Н. Н. Смирнова1, И. В. Красильников2
1 Владимирский государственный университет
им. Александра Григорьевича и Николая Григорьевича Столетовых,
600000, г. Владимир, ул. Горького, д. 87
2 Ивановский государственный политехнический университет,
153000, г. Иваново, Шереметевский пр., д. 21
E-mail: smirnovann@list.ru
Поступила в Редакцию 30 мая 2019 г.
После доработки 25 июля 2019 г.
Принята к публикации 20 августа 2019 г.
Получены ультрафильтрационные мембраны на основе ароматического сополиамида, включающего
10% звеньев с сульфонатными группами. Показана возможность их использования в качестве ма-
трицы для иммобилизации применяемых в аффинной хроматографии лигандов: катионов металлов,
аминокислот, красителей. Компонентами иммобилизации являлись ионы меди(II), гистидин, лизин и
3,6-диамино-10-метилакридин хлорид. Установлено, что иммобилизация в основном происходит за
счет электростатического взаимодействия соответствующих функциональных групп компонента
и сополиамида и не сопровождается снижением удельной производительности мембран по воде.
Выполнены исследования адсорбционных (в статических условиях и условиях ультрафильтрации
растворов белков) и массообменных свойств модифицированных мембран. Выявлен характер влияния
модификации на массообменные характеристики полученных материалов. Для немодифицированной
мембраны оптимальное сочетание селективности и удельной производительности реализуется при
pH белкового раствора выше его изоэлектрической точки. В зависимости от природы иммобилизо-
ванного компонента селективности 0.96-0.99 можно достичь при значениях рН ниже или равных
изоэлектрической точке белка.
Ключевые слова: ультрафильтрационные мембраны; иммобилизация компонентов; адсорбционные
свойства; массообменные свойства
DOI: 10.1134/S0044461819110148
Последние годы характеризуются впечатляющим
биотехнологии до водоподготовки и водоочистки.
ростом промышленного внедрения мембранных
Ежегодный рост некоторых сегментов рынка достига-
технологий. Анализ развития рынка мембранных
ет 10-15%. Для целого ряда процессов синтетические
модулей и установок свидетельствует о разнообра-
мембраны не имеют конкурентов по эффективно-
зии реализуемых направлений — от медицины и
сти, производительности, стоимости и легкости кор-
1476
Влияние природы иммобилизованных компонентов на адсорбционные и массообменные свойства...
1477
ректировки исходных разделительных параметров.
емые или выделяемые вещества рассмотрены в ряде
Однако стремление к достижению характеристик,
работ [2-8]. Что касается аффинной фильтрации, то
присущих биологическим мембранам, определяет
многие теоретические подходы и их эксперименталь-
направления текущих и перспективных исследований
ное воплощение при разработке мембран пришли в
в области мембранной науки и технологии. Среди
эту область мембранной технологии из аффинной
наиболее важных могут быть выделены следующие
хроматографии. Высокоспецифические взаимодей-
[1]: синтез новых поли- и сополимеров с заданной
ствия в аффинных мембранах преимущественно обе-
структурой, способной обеспечить хорошие «ба-
спечивают иммобилизованные за счет ковалентных
рьерные» свойства; функционализация поверхности
или нековалентных связей макро- и микролиганды
мембран для реализации «индивидуальных» взаи-
[9-16], в последнем случае речь идет, как правило,
модействий с компонентами разделяемых систем;
об электростатическом взаимодействии мембрана/
получение «смешанных» или «составных» мембран,
активный компонент. В качестве матрицы используют
сочетающих свойства различных используемых ма-
мембраны на основе целлюлозы и ее производных [3,
териалов.
4, 17-19], полибутилентерефталата [20], полиэтилена
Необходимость решения задач концентрирования,
[21], полиэфирсульфона [2, 8].
фракционирования и очистки в пищевой, фармацев-
В настоящей работе рассмотрена возможность
тической и других отраслях промышленности опре-
получения ультрафильтрационной мембраны с на-
деляет в ближайшие годы значительный потенциал
правленно регулируемыми адсорбционными и мас-
роста ультрафильтрации. Высокие регулируемые мас-
сообменными свойствами путем иммобилизации
сообменные характеристики ультрафильтрационных
компонентов на матрице на основе сульфонатсодер-
мембран могут быть реализованы за счет обеспечения
жащего ароматического сополиамида. Компоненты
селективных взаимодействий компонентов фильтруе-
для иммобилизации были выбраны из трех групп
мых систем с поверхностью мембраны, т. е. речь идет
известных в аффинной хроматографии лигандов:
о молекулярно-селективном механизме фильтрации.
катионы металлов, аминокислоты, красители.
Такая селективность может определяться электропо-
верхностными свойствами мембраны и сродством ее
Экспериментальная часть
материала или иммобилизованных на поверхности
веществ к молекулам определенного вида. При этом
Ароматический сополиамид. Статистический со-
для сохранения проницаемости необходимо миними-
полимер на основе дихлорангидрида изофталевой
зировать нежелательные взаимодействия мембраны и
кислоты и замещенных и незамещенных диаминов:
компонентов фильтруемых растворов, т. е. речь идет о
натриевой соли 4,4′-диаминодифиниламин-2-суль-
необходимости контроля адсорбционных процессов.
фокислоты и 1,4-фенилендиамина [ПА(-)] — синте-
Вопросы реализации и эффективности заряд-селек-
зирован в ОАО «Полимерсинтез» под руководством
тивных взаимодействий пористая мембрана/разделя-
Ю. А. Федотова [22]:
где m = 10, n = 90 мол%.
ли в статическом режиме и режиме фильтрации.
Для получения мембран использовали сополимер
Концентрация компонентов в фильтруемых растворах
молекулярной массы 40 кДа, Mw/Mn = 1.5.
составляла 0.1%.
Получение и модификация мембран. Мембраны
Концентрацию ионов меди в растворе определяли
изготавливали фазоинверсионным методом мокрого
методом ААС (КВАНТ-Z.ЭТА). Для измерения кон-
формования. Для проведения исследований были
центрации аминокислот и красителя использовали
получены образцы на подложке из нетканого матери-
спектрофотометр СФ-2000, оптическую плотность
ала с номинально отсекаемой молекулярной массой
растворов контролировали при длине волны λ, равной
~30 кДа. В качестве компонентов иммобилизации ис-
210 и 448 нм соответственно.
пользовали ионы меди(II), гистидин (His), лизин (Lys)
ИК-спектры воздушно-сухих образцов регистри-
(табл. 1) и 3,6-диамино-10-метилакридин хло-
ровали на ИК-спектрометре ФСМ 1202 с Фурье-
рид (Acr). Обработку образцов мембран проводи-
преобразованием.
1478
Смирнова Н. Н., Красильников И. В.
Таблица 1
Характеристика аминокислот [23]
Кислотно-основные свойства
функциональных групп
Компонент
Структура
рI
рKа (-СООН)
рKа (-NH3+)
Гистидин
1.8
9.2
7.7
6.0
(имидазольная
группа)
Лизин
2.2
9.0
9.8
10.5
(-NH3+ в радикале)
Содержание натрия в материалах определяли по-
разцами исследовали в статическом и динамическом
сле сжигания навески массой 0.5-1.0 г в муфельной
(ультрафильтрация) режимах. Для эксперимента в
печи при температуре 800°С. Образующийся сухой
статических условиях использовали образцы пло-
остаток растворяли в бидистиллированной воде, кон-
щадью 2 см2. Объем раствора белка составлял 5 см3.
центрацию ионов натрия в растворе определяли ме-
Для приготовления растворов применяли универсаль-
тодом ААС (спектрометр КВАНТ-Z.ЭТА).
ный буфер (ионная сила раствора 0.02 моль∙дм-3).
Адсорбционные и массообменные свойства мем-
Адсорбционные свойства мембран оценивали по из-
бран. Адсорбцию белков (табл. 2) мембранными об- менению содержания белка в растворах после выдер-
Таблица 2
Характеристика белков [24-26]
Стоксовский радиус
Белок
Молекулярная масса, кДа
pI
Размеры, Å
молекулы rs, Å
Бычий сывороточный альбу-
67.0
4.9
150 × 40 × 45
34.0
мин (BSA) (Sigma)
Миоглобин (Myo) (Sigma)
16.8
7.0
44 × 44 × 25
16.0
Таблица 3
Изотермы адсорбции
Модель
Уравнение*
Константы и параметры
Qmbc
Изотерма Ленгмюра
Qm — расчетное значение максимальной
Q =
1 + bc
адсорбции, мг∙см-2;
b — константа, характеризующая сродство в
системе адсорбат/адсорбент, дм3∙мг-1
Изотерма Ленгмюра-Фрейнд-
KLF — константа, дм3∙мг-1; n — безразмер-
(KLFc)1/n
Q = Qm
лиха
ный параметр
1 + (KLFc)1/n
Q — адсорбционная емкость мембраны, мг∙см-2; c — равновесная концентрация белка в растворе, мг∙дм-3.
Влияние природы иммобилизованных компонентов на адсорбционные и массообменные свойства...
1479
живания в них образцов до установления равновесия.
адсорбционной емкости мембран в процессе филь-
Адсорбционную емкость мембран Q рассчитывали
трации рассчитывали значение QUF.
как отношение массы адсорбированного вещества к
Селективность и удельную производительность
площади образца. Количество параллельных опытов
образцов определяли по формулам
составляло не менее пяти. Результаты, описывающие
c0 - cf
экспериментальные данные, обрабатывали по теории
R =
,
c0
ошибок. Доверительный интервал определяли для
уровня значимости 0.05.
где сf и с0 — концентрация белка в фильтрате и исход-
Для математической обработки эксперименталь-
ном фильтруемом растворе соответственно (г∙дм-3);
ных данных применяли двухпараметрическую мо-
V
I =
,
дель адсорбции Ленгмюра и трехпараметрическую
St
модель Ленгмюра-Фрейндлиха [27-30] (табл. 3). Для
оценки степени соответствия экспериментальных
где V — объем фильтрата (см3), t — время экспери-
данных выбранным математическим моделям исполь-
мента (мин), S — площадь мембраны (см2).
зовали значения R2 [28].
Концентрацию белка фиксировали с помощью
Адсорбцию белков в динамическом режиме
спектрофотометра СФ-2000 по оптической плотно-
оценивали с помощью тупиковой разделительной
сти при длине волны 278 и 408 нм (для BSA и Myo
ячейки с рабочей поверхностью мембраны 9.62 см2.
соответственно).
Исследования проводили при комнатной температуре
и давлении 0.1 МПа, концентрация белка в буферном
Обсуждение результатов
растворе при соответствующем значении рН состав-
ляла 0.1 г∙дм-3. Давление в системе поддерживали
Наличие в макромолекулярной цепи сополиамида
с помощью сжатого азота. Общий объем фильтру-
сульфонатных групп позволяет предполагать, что
емого раствора 40 см3. До начала разделительного
иммобилизация катионов меди(II) и органических
эксперимента мембраны промывали раствором KCl
компонентов с выраженными основными свойствами
концентрацией 0.01 моль∙дм-3 и дистиллированной
происходит прежде всего за счет кулоновских сил.
водой. Для измерения оптической плотности отби-
В случае лизина схема иммобилизации может
рали пробы фильтрата и концентрата. Для оценки быть представлена следующим образом:
•
О справедливости подобного предположения
онами различной природы [31]. Полосы поглощения
свидетельствует характер изменений в ИК-спектрах
Амид I и Амид II (1654 и 1541 см-1) претерпевают ме-
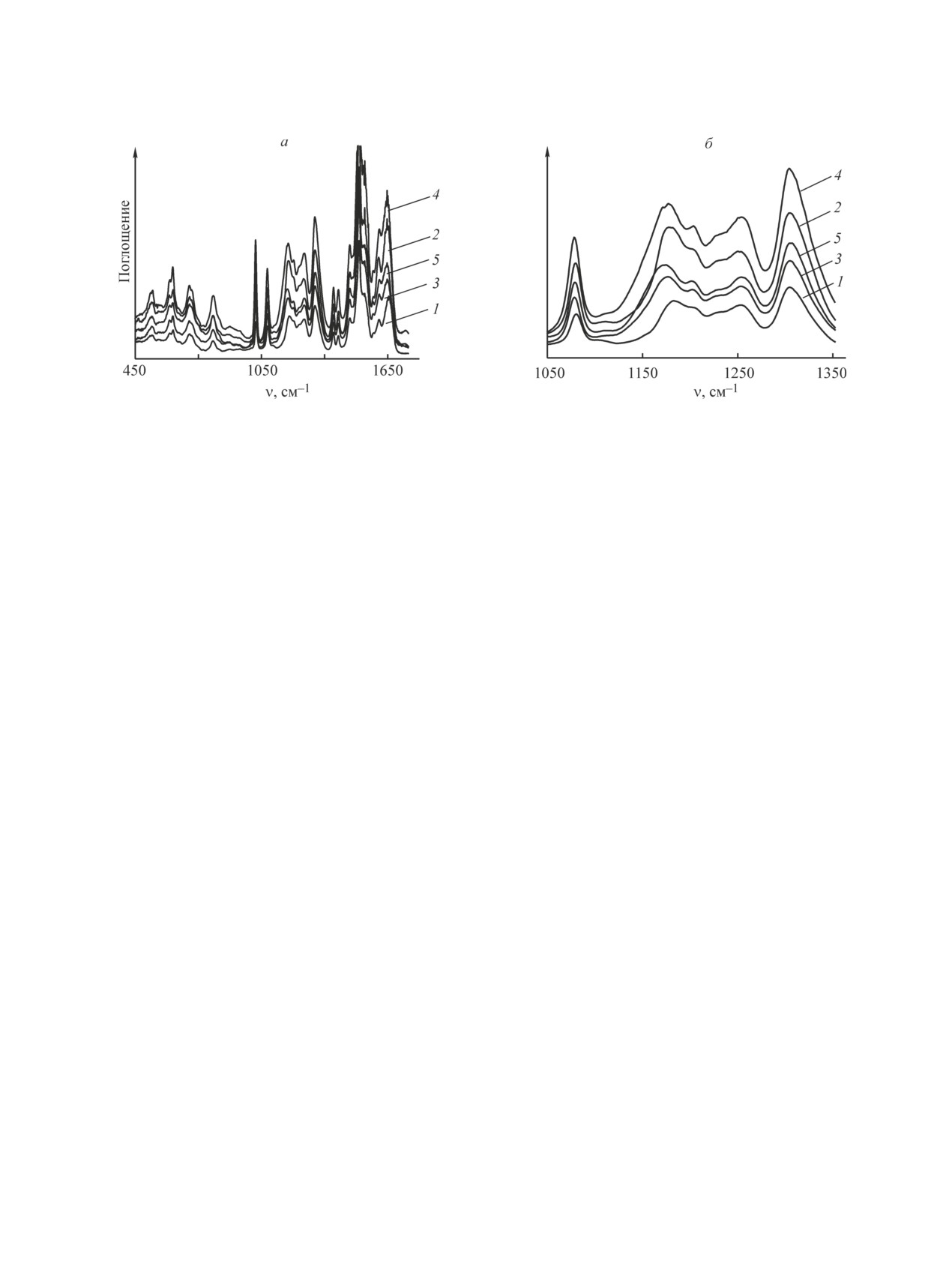
материалов (рис. 1). Для всех модифицированных
нее существенные изменения, в наибольшей степени
образцов наблюдается коротковолновое смещение в
выраженные для ПА(His): коротковолновое смещение
области полосы, соответствующей асимметричным
полосы Амид I до 1646 см-1 и изменение контура по-
валентным колебаниям SO2 в сульфонатной группе,
лосы Амид II, что, по-видимому, обусловлено интен-
с 1185 [ПА(-)] до 1178 [ПА(Acr)], 1177 [ПА(Lys)],
сивными водородными связями в рассматриваемой
1176 [ПА(His)] и 1171 см-1 [ПА(Cu)]. Проведенные
системе.
ранее подробные исследования показали, что харак-
Адсорбционная емкость образцов по катионам
тер смещения этой полосы следует рассматривать
меди(II), акрифлавину, гистидину и лизину равна
как относительную меру силы взаимодействия суль-
0.87, 1.07, 1.79 и 1.30 мкмоль∙см-2 соответственно.
фонатсодержащих полимерных электролитов с кати-
Для оценки полноты замещения ионов натрия в сопо-
1480
Смирнова Н. Н., Красильников И. В.
Рис. 1. ИК-спектры поглощения ПА(-) (1), ПА(Acr) (2), ПА(Lys) (3), ПА(His) (4), ПА(Cu) (5).
лиамиде использовали элементный анализ. В случае
мембраной наряду с кулоновскими силами опреде-
Cu(II) замещение было практически полным (более
ляют ван-дер-ваальсовые, гидрофобные, гидрофиль-
90%), для Acr, Lys и His — составило 30-35%, что
ные и стерические взаимодействия [33]. Согласно
может быть обусловлено различной доступностью
опубликованным данным, вклад в величину свобод-
сульфонатных групп мембраны для существенно раз-
ной энергии адсорбции белка кулоновских сил со-
личающихся по размерам ионов меди и органических
ставляет ~10-20 кДж∙моль-1, ван-дер-ваальсовых
молекул. Однако высокие значения адсорбционной
взаимодействий — ~10 кДж∙моль-1, гидрофобных
емкости мембраны по органическим компонентам
сил — ~10 кДж∙моль-1, водородных взаимодей-
свидетельствуют о возможности их иммобилизации
ствий — 4-9 кДж∙моль-1 [34]. Роль различных вза-
как за счет электростатических взаимодействий, так
имодействий белок/мембрана в процессе адсорбции
и за счет сил неэлектростатической природы.
будет изменяться в зависимости от природы иммо-
На рис. 2 показаны экспериментальные изотер-
билизованного компонента. Таким образом, природа
мы адсорбции BSA мембранами ПА(-), ПА(Acr),
лигандов становится инструментом, позволяющим
ПА(Lys), ПА(His), ПА(Cu) в статических условиях
изменять адсорбционную емкость мембраны.
при значениях рН 3.3, 4.9 и 8.0. Результаты мате-
В частности, иммобилизация на поверхности со-
матической обработки экспериментальных данных
держащего конденсированные ароматические коль-
представлены в табл. 4. Сравнительный анализ полу-
ца 3,6-диамино-10-метилакридин хлорида прежде
ченных результатов показывает, что общий характер
всего должна приводить к возрастанию интенсивно-
зависимостей адсорбции немодифицированной и
сти гидрофобных взаимодействий белок/мембрана.
модифицированных мембран, свидетельствующий
Кроме того, в кислой среде молекула этого лиган-
о доминирующем вкладе электростатического вза-
да содержит две протонированные аминогруппы.
имодействия белок/мембрана, сохраняется для всех
Следствием суммарного влияния этих факторов
исследованных систем [32]. Это может быть обу-
является снижение адсорбции модифицированных
словлено отличным от единицы значением степени
образцов при рН 3.3 и ее увеличение при рН 4.9 и
превращения реакции сульфонатных групп сополи-
8.0. Способность катионов тяжелых металлов к об-
амида и противоположно заряженных лигандов на
разованию комплексов с макромолекулами белков
поверхности мембраны. Следствием этого является
является причиной значительного роста адсорбции
присутствие на поверхности свободных сульфонат-
BSA на мембране с иммобилизованными ионами
ных групп, которые и определяют наиболее высокие
меди(II) прежде всего при рН 4.9, т. е. в том случае,
значения адсорбции в том диапазоне рН, когда белок
когда положительные и отрицательные заряды ма-
заряжен положительно.
кромолекулы белка скомпенсированы и вклад элек-
Максимальные экспериментальные значения ад-
тростатических взаимодействий белок/мембрана в
сорбции при рН 3.3 для ПА(-), ПА(Acr), ПА(Lys),
адсорбцию минимален.
ПА(His) и ПА(Cu) составили 0.23, 0.13, 0.18, 0.16 и
Для рассматриваемых аминокислот уравнения
0.15 мг∙см-2 соответственно. Наблюдаемые разли-
ионизации могут быть представлены следующими
чия обусловлены тем, что взаимодействие белка с
схемами:
Влияние природы иммобилизованных компонентов на адсорбционные и массообменные свойства...
1481
COOH
COO-
COO-
COO-
-H+
-H+
-H+
CH—N+H3
CH—N+H3
CH—NH2
CH—NH2
+H+
+H+
+H+
(CH2)4—N+H3
(CH2)4—N+H3
(CH2)4—N+H3
(CH2)4—NH2
pKa1 2.2
pKa2 9.0
pKa3 10.5
COOH
COO-
COO-
COO-
HC—N+H3
HC—N+H3
HC—N+H3
HC—NH2
H2C
H2C
H2C
H2C
H
H
H
H
C—N
-H+
C—N
-H+
C—N
-H+
C—N
CH
CH
CH
CH
+H+
+H+
HC—N+
HC—N+
HC—N
+H+ HC—N
H
H
pKa1 1.8
pKa2 6.0
pKa3 9.2
При рН 3.3, 4.9 и 8.0 молекулы лизина представ-
карбоксильные группы лиганда) заряженные группы.
ляют собой катионы, включающие две протониро-
Это приводит к снижению адсорбционной емкости
ванные аминогруппы, т. е. на поверхности матери-
мембраны при рН 3.3 и увеличению при рН 8.0. У мо-
ала ПА(Lys) присутствуют как положительно, так
лекул гистидина при рН выше 6.0 протонированной
и отрицательно (сульфонатные группы матрицы и
является только α-аминогруппа, т. е. на поверхности
Таблица 4
Параметры изотерм адсорбции BSA мембранами ПА(-), ПА(Acr), ПА(Lys), ПА(His), ПА(Cu)
Изотерма Ленгмюра
Изотерма Ленгмюра-Фрейндлиха
Мембрана
рН
Qm
b∙103
R2
Qm
KLF∙103
1/n
R2
ПА(-)
3.3
0.338
1.31
0.983
0.490
0.62
0.96
0.988
4.9
0.134
1.11
0.981
0.257
0.42
0.99
0.999
8.0
0.028
1.01
0.984
0.042
0.55
0.98
0.995
ПА(Acr)
3.3
0.219
1.05
0.927
0.212
2.45
0.45
0.987
4.9
0.171
1.46
0.964
0.161
0.92
0.19
0.977
8.0
0.140
1.01
0.896
0.148
0.23
0.55
0.989
ПА(Lys)
3.3
0.251
1.67
0.747
0.182
3.13
0.36
0.973
4.9
0.135
1.24
0.938
0.134
1.27
0.99
0.972
8.0
0.033
1.74
0.984
0.057
0.44
0.44
0.991
ПА(His)
3.3
0.221
1.52
0.776
0.256
3.29
0.27
0.985
4.9
0.156
1.02
0.917
0.150
0.25
0.53
0.979
8.0
0.015
1.08
0.972
0.014
0.82
0.98
0.996
ПА(Cu)
3.3
0.217
1.92
0.988
0.220
3.98
0.58
0.997
4.9
0.359
1.57
0.992
0.434
0.69
0.89
0.998
8.0
0.037
1.05
0.983
0.063
0.84
0.98
0.989
1482
Смирнова Н. Н., Красильников И. В.
Рис. 2. Изотермы адсорбции BSA ПА(-) (а), ПА(Acr) (б), ПА(Lys) (в), ПА(His) (г), ПА(Cu) (д) при рН 3.3 (1), 4.9 (2),
8.0
(3).
мембраны ПА(His) в этом диапазоне рН присутству-
производительности (а) и селективности (б) получен-
ют отрицательно заряженные сульфонатные и карбок-
ных мембран в процессе фильтрации.
сильные группы (матрицы и лиганда соответственно).
Следует отметить, что иммобилизация лизина,
Известно, что адсорбция оказывает значительное
гистидина, акрифлавина и ионов меди(II) на по-
влияние на массообменные характеристики мембран.
верхности ультрафильтрационных мембран, с од-
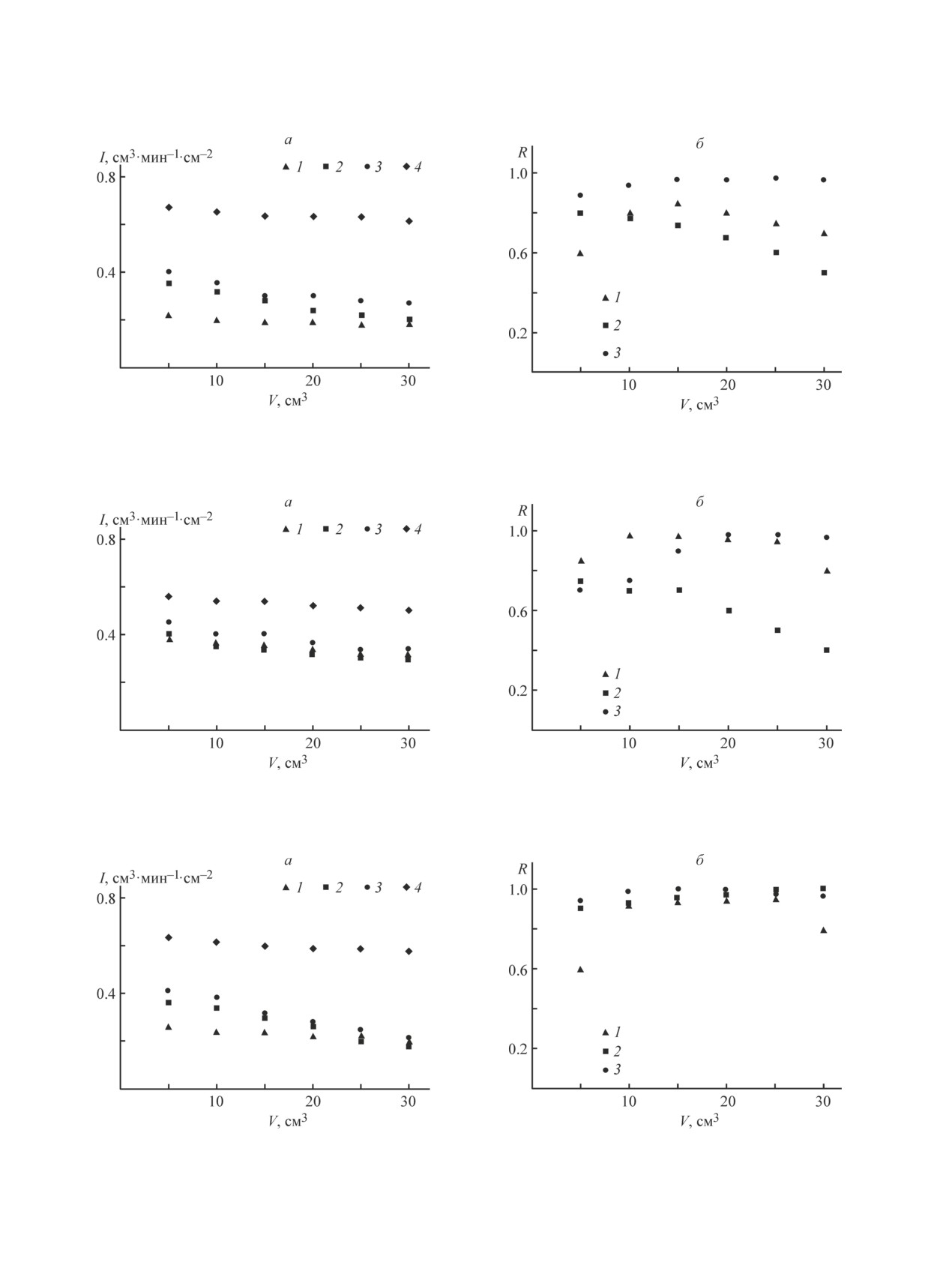
На рис. 3-7 показан характер изменения удельной
ной стороны, не оказывает существенного влия-
Влияние природы иммобилизованных компонентов на адсорбционные и массообменные свойства...
1483
Рис. 3. Изменение удельной производительности (а) и селективности (б) мембраны ПА(-) при фильтрации раствора
BSA при рН 3.3 (1), 4.9 (2), 8.0 (3) и воды (4).
Рис. 4. Изменение удельной производительности (а) и селективности (б) мембраны ПА(Acr) при фильтрации рас-
твора BSA при рН 3.3 (1), 4.9 (2), 8.0 (3) и воды (4).
Рис. 5. Изменение удельной производительности (а) и селективности (б) мембраны ПА(Lys) при фильтрации рас-
твора BSA при рН 3.3 (1), 4.9 (2), 8.0 (3) и воды (4).
1484
Смирнова Н. Н., Красильников И. В.
ния на их удельную производительность по воде,
адсорбционных экспериментов. Однако модифика-
а с другой — ощутимо изменяет засорение мем-
ция мембраны в значительной степени определяет
бран в процессе фильтрации белка. Минимальная
характер изменения ее задерживающей способности.
адсорбционная емкость (QUF) при рН 3.3 наблюда-
В зависимости от природы взаимодействия белок/
ется для ПА(Acr) (6.8 мкг·см-2), при рН 4.9 — для
мембрана в рассмотренном временном диапазоне
ПА(Lys) (4.3 мкг·см-2), при рН 8.0 — для ПА(-)
селективность образцов либо монотонно снижается,
(1.9 мкг·см-2). Максимальной адсорбционной способ-
либо проходит через максимум, либо колеблется в до-
ностью при рН 3.3 обладает ПА(-) (54.8 мкг·см-2),
статочно узком диапазоне. При фильтрации раствора
при рН 4.9 — ПА(Cu) (59.8 мкг·см-2), при рН 8.0 —
BSA через немодифицированные мембраны на осно-
ПА(Lys) (15.1 мкг·см-2). В целом значения Q исследо-
ве сульфонатсодержащего ароматического сополиа-
ванных образцов достаточно высоки, что может быть
мида максимальные массообменные характеристики
обусловлено способностью составляющих основу
(R = 0.97, I = 0.29 см3∙мин-1∙см-2) достигаются при
мембранного материала ароматических полиамидов
pH белкового раствора выше его изоэлектрической
к интенсивным гидрофобным взаимодействиям и
точки, т. е. в условиях, когда мембрана и белок одно-
образованию водородных связей [35, 36].
именно заряжены. Для ПА(Acr) селективности выше
Данные динамических исследований не противо-
0.96 удается достичь при рН ниже 4.9. Для мембран
речат результатам, полученным в ходе статических ПА(Lys), ПА(His), ПА(Cu) значения R превышают
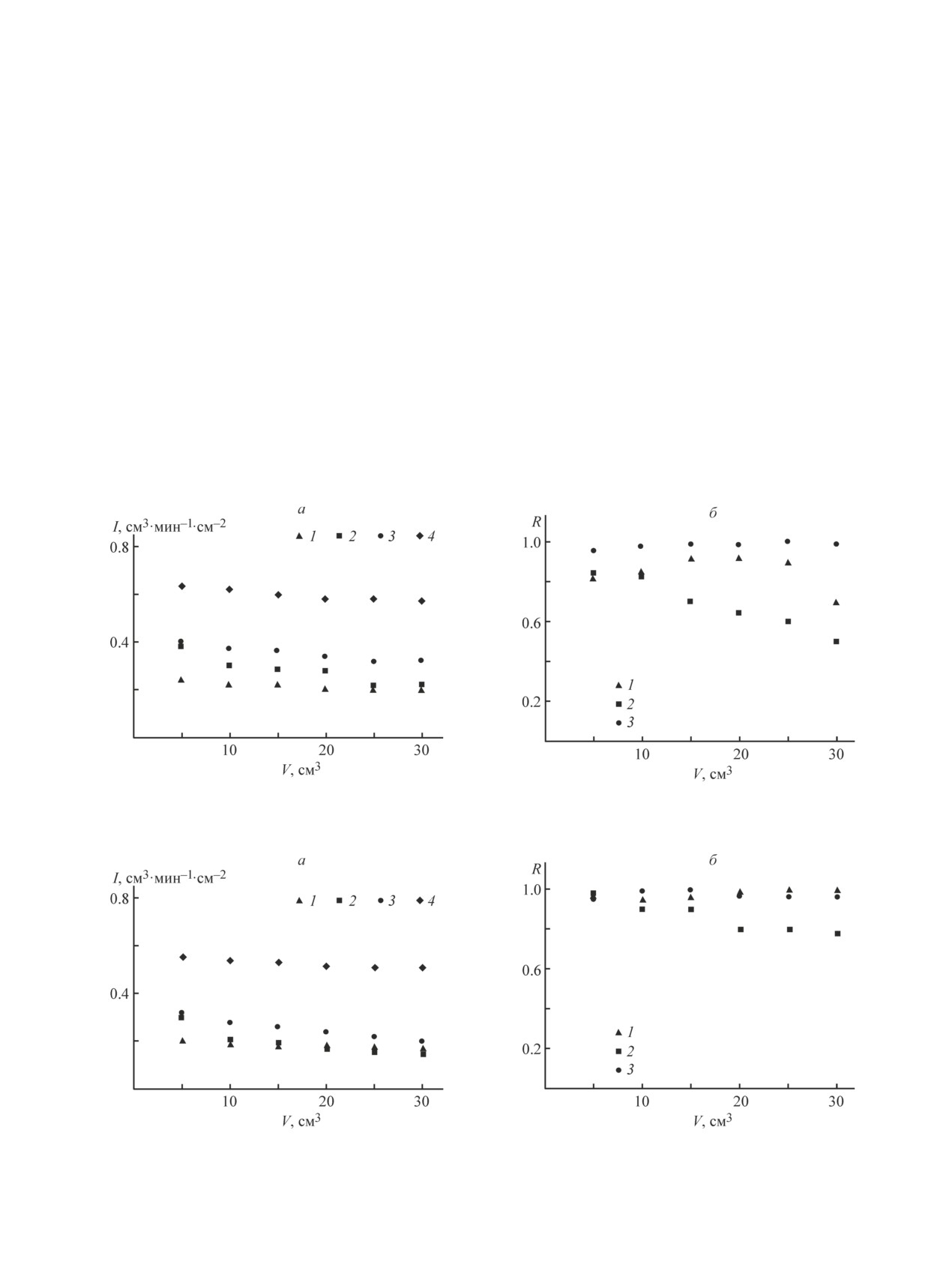
Рис. 6. Изменение удельной производительности (а) и селективности (б) мембраны ПА(His) при фильтрации рас-
твора BSA при рН 3.3 (1), 4.9 (2), 8.0 (3) и воды (4).
Рис. 7. Изменение удельной производительности (а) и селективности (б) мембраны ПА(Cu) при фильтрации рас-
твора BSA при рН 3.3 (1), 4.9 (2), 8.0 (3) и воды (4).
Влияние природы иммобилизованных компонентов на адсорбционные и массообменные свойства...
1485
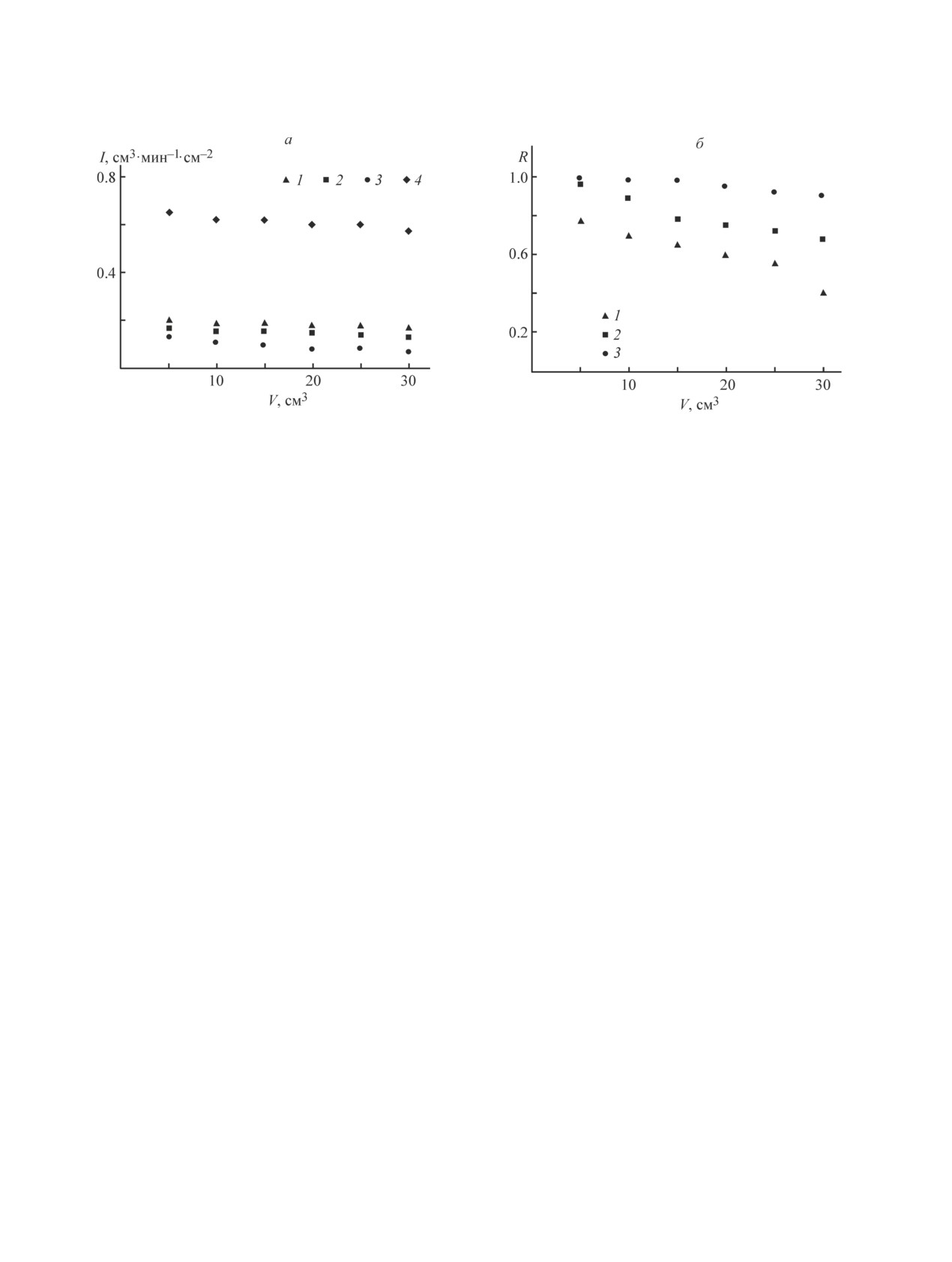
Рис. 8. Изменение удельной производительности (а) и селективности (б) мембраны при фильтрации раствора Myo
при рН 7.0 (1-3) и воды (4): ПА(-) (1, 4), ПА(Lys) (2), ПА(Cu) (3).
0.95 при рН выше и ниже изоэлектрической точки
основе в качестве матриц для иммобилизации актив-
белка. Из всех рассмотренных систем для образцов
ных компонентов прежде всего за счет электроста-
ПА(Lys) и ПА(Cu) были получены значения селектив-
тического взаимодействия соответствующих функ-
ности 0.98-0.99 при рН 4.9. Однако в случае ПА(Cu)
циональных групп. Использование для получения
высокая адсорбционная емкость приводит к суще-
мембран сополимеров обеспечивает равномерное
ственному снижению удельной производительности
распределение заряженных групп по разделительной
мембраны.
поверхности. Следствием иммобилизации является
На рис. 8 показан характер изменения удельной
направленная функционализация поверхности мате-
производительности (а) и селективности (б) для мем-
риала за счет регулирования природы взаимодействия
бран ПА(-), ПА(Lys) и ПА(Cu) при фильтрации рас-
белок/мембрана. Одновременно иммобилизация
твора миоглобина при рН = рIMyo.
компонентов сопровождается изменением размера
Полученные данные дают представление о влия-
пор материала. Вклад последней составляющей в
нии модификации на задерживающую способность
основном будет зависеть от молекулярной массы
мембран при фильтрации белка, стоксовский радиус
иммобилизованных веществ. Совместное действие
молекул которого более чем в 2 раза меньше, чем
вышеобозначенных факторов приводит к изменению
BSA, при величине рН, равной его изоэлектрической
массообменных характеристик образцов мембран.
точке.
При фильтрации раствора BSA через немодифици-
Для немодифицированного образца cелектив-
рованные мембраны ПА(-) оптимального сочета-
ность на начальном этапе фильтрации составляет
ния селективности и удельной производительности
0.77. В случае ПА(Lys) значение R увеличивается до
(R = 0.97, I = 0.29 см3∙мин-1∙см-2) достигают при pH
0.97. Однако модификация не оказывает влияния на
раствора выше изоэлектрической точки BSA, т. е. в
характер изменения селективности. В рассматривае-
условиях, когда мембрана и белок одноименно заря-
мом временном диапазоне R снижается для немоди-
жены. Для ПА(Acr) селективность выше 0.96 удается
фицированной мембраны до 0.37, а для ПА(Lys) — до
получить в ходе разделительного эксперимента при
0.65. Для ПА(Cu) селективность выше 0.95 удается
рН ниже 4.9. Для мембран ПА(Lys), ПА(His), ПА(Cu)
сохранить на более значительном временном про-
значения R превышают 0.95 при рН выше и ниже
межутке, но удельная производительность образцов
изоэлектрической точки белка. Для образцов ПА(Lys)
составляет около 0.07 см3∙мин-1∙см-2.
и ПА(Cu) при рН 4.9 были получены значения селек-
тивности 0.98-0.99 при фильтрации раствора BSA и
0.96-0.99 — раствора Myo. Таким образом, можно
Выводы
говорить об одном из дополнительных преимуществ
Наличие ионных групп в сульфонатсодержащих
пористых мембран на основе полимерных электро-
ароматических сополиамидах предоставляет воз-
литов (наряду с улучшенными массообменными ха-
можность использования пористых мембран на их
рактеристиками, определяемыми присутствием за-
1486
Смирнова Н. Н., Красильников И. В.
ряженных групп): наличие ионных групп открывает
and separation performance of polyethersulfone
возможности использования такого инструмента, как
ultrafiltration membranes through poly(ethylenimine)
иммобилизация различных компонентов, для направ-
grafting // J. Membr. Sci. 2018. V. 554. P. 125-133.
ленного регулирования их свойств.
[8] Emin C., Kurnia E., Katalia I., Ulbricht M. Polyaryl-
sulfone-based blend ultrafiltration membranes
Конфликт интересов
with combined size and charge selectivity for
protein separation // Separ. Purif. Technol. 2018.
Авторы заявляют об отсутствии конфликта инте-
ресов, требующего раскрытия в данной статье.
seppur.2017.11.008
[9] Romero J., Zydney A. pH and salt effects on chiral
separations using affinity ultrafiltration // Desalination.
Информация об авторах
Смирнова Наталья Николаевна, д.х.н., до-
S0011-9164(02)00671-9
цент, директор Института биологии и экологии
[10]
Serpa G., Augusto E., Tamashiro W., Ribeiro M.,
Владимирского государственного университета,
Miranda E., Bueno S. Evaluation of immobilized metal
membrane affinity chromatography for purification
of an immunoglobulin G1 monoclonal antibody // J.
Красильников Игорь Викторович, к.т.н., дирек-
Chromatography. B. 2005. V. 816. P. 259-268. https://
тор Института развития компетенций Ивановского
doi.org/10.1016/j.jchromb.2004.11.043
государственного политехнического университета,
[11]
Rao S., Zydney A. High resolution protein separations
using affinity ultrafiltration with small charged ligands
org/10.1016/j.memsci.2006.02.035
Список литературы
[12]
Aquino L., Sousa H., Miranda E., Vilela L., Bueno S.
[1] Ulbricht M. Advanced functional polymer membranes
Evaluation of IDA-PEVA hollow fiber membrane
metal ion affinity chromatography for purification of
org/10.1016/j.polymer.2006.01.084
a histidine-tagged human proinsulin // J. Chromato-
[2] Kuma M., Ulbricht M. Novel antifouling positively
charged hybrid ultrafiltration membranes for protein
org/10.1016/j.jchromb.2006.02.015
separation based on blends of carboxylated carbon
[13]
Ribeiro M., Vijayalakshmi M., Todorova-Balvay D.,
nanotubes and aminated poly(arylene ether sulfone)
Bueno S. Effect of IDA and TREN chelating agents
and buffer systems on the purification of human IgG
org/10.1016/j.memsci.2013.07.055
with immobilized nickel affinity membranes // J.
[3] Valino V., Román F., Ibanez R., Ortiz I. Improved
Chromatography. B. 2008. V. 861. P. 64-73. https://
separation of bovine serum albumin and lactoferrin
doi.org/10.1016/j.jchromb.2007.11.018
mixtures using charged ultrafiltration membranes //
[14]
Edwie F., Chung T.-S. Exploration of regeneration
Separ. Purif. Technol. 2014. V. 125. P. 163-169. https://
and reusability of human serum albumin as a
doi.org/10.1016/j.seppur.2014.01.023
stereoselective ligand for chiral separation in affinity
[4] Chen X., Zhao Y., Moutinho J., Shao J., Zydney A. L.,
ultrafiltration // J. Membr. Sci. 2010. V. 362. P. 501-
He Y. Recovery of small dye molecules from aqueous
solutions using charged ultrafiltration membranes //
[15]
Ferraris M., Barrera G., Padilla A., Rodriguez J.
Affinity adsorption of lysozyme on a macroligand
org/10.1016/j.jhazmat.2014.10.031
prepared with Cibacron Blue 3GA attached to yeast
[5] Lin X., Wang K., Feng Y., Liu J.Z., Fang X., Xu T.,
cells // J. Chromatography. B. 2011. V. 879. P. 2741-
Wang H. Composite ultrafiltration membranes from
polymer and its quaternary phosphonium-functionalized
[16]
Muthukuma S., Rathore A. High throughput process
derivative with enhanced water flux // J. Membr. Sci.
development (HTPD) platform for membrane
chromatography// J. Membr. Sci. 2013. V. 442. P. 245-
memsci.2015.02.017
[6] Arunkumar A., Etzel M. R. Negatively charged tangential
[17]
Zhang L., Zhao Y.-H., Bai R. Development of a
flow ultrafiltration membranes for whey protein
multifunctional membrane for chromatic warning
concentration // J. Membr. Sci. 2015. V. 475. P. 340-
and enhanced adsorptive removal of heavy metal
ions: Application to cadmium // J. Membr. Sci.
[7] Lin Zh., Hu Ch., Wu X., Zhong W., Chen M., Zhang Q.,
Zhu A., Liu Q. Towards improved antifouling ability
memsci.2011.05.044
Влияние природы иммобилизованных компонентов на адсорбционные и массообменные свойства...
1487
[18]
Rohani M., Zydney A. Protein transport through
zwitterionic ultrafiltration membranes // J. Membr. Sci.
cej.2009.09.013
[29] Quiroga E., Ramirez-Pastor A. J. Statistical thermo-
memsci.2011.12.021
dynamics of molecules with multiple adsorption states:
[19]
Kosior A., Antošová M., Faber R., Villain L.,
Application to protein adsorption // Chem. Phys. Lett.
Polakovič M. Single-component adsorption of
proteins on a cellulose membrane with the phenyl
cplett.2012.11.019
ligand for hydrophobic interaction chromatography //
[30] Smirnova N. N., Nebukina I. A. Effect of the mem-
brane/protein interaction nature on adsorptive
org/10.1016/j.memsci.2013.04.013
properties of UF-membranes based on aromatic poly-
[20]
Liu H., Zheng Y., Gurgel P., Carbonell R. Affinity
and copolyamides // Сорбцион. и хроматогр. процес-
membrane development from PBT nonwoven by
сы. 2018. Т. 18. № 3. С. 352-364.
photo-induced graft polymerization, hydrophilization
[31] Цундель Г. Гидратация и межмолекулярное взаи-
and ligand attachment // J. Membr. Sci. 2013.
модействие. М.: Мир, 1972. С. 49-62 [Zundel G.
Hydration and intermolecular interaction. Infrared
memsci.2012.09.047
investigations with polyelectrolyte membranes. New
[21]
Zhu J., Yang J., Sun G. Cibacron Blue F3GA
York: Academic: 1969. 430 p.].
functionalized poly(vinyl alcohol-co-ethylene) (PVA-
[32] Смирнова Н. Н. Ультрафильтрационные мем-
co-PE) nanofibrous membranes as high efficient
браны на основе интерполиэлектролитных ком-
affinity adsorption materials // J. Membr. Sci. 2011.
плексов: адсорбционные и массообменные
свойства // ЖПХ. 2017. Т. 90. № 6. С. 770-777
memsci.2011.10.001
[Smirnova N. N. Ultrafiltration membranes based
[22]
Федотов Ю. А., Смирнова Н. Н. Ароматические
on interpolyelectrolyte complexes: adsorption and
полиамиды с ионогенными группами: синтез,
mass-exchange properties // Russ. J. Appl. Chem.
свойства, области применения // Пласт. массы.
2017. V. 90. N 6. P. 923-930. DOI: 10.1134/
2008. № 8. С. 18-21.
S1070427217060131].
[23]
White J. S., White D. Ch. Proteins, peptides and amino
[33] Molek J., Ruanjaikaen K., Zydney A. Effect of
acids. Source book. Humana Press, 2002. Р. 715-939.
electrostatic interactions on transmission of PEGylated
[24]
White A., Handler Ph., Smit E. Principles of
proteins through charged ultrafiltration membranes //
biochemistry. N.Y. V. 1. 1978. Р. 125.
[25]
Jakubke H.-D., Jeschkeit H. Aminosӓuren, Peptide,
org/10.1016/j.memsci.2010.02.031
Proteine. Berlin: Akademie-Verlag, 1982. Р. 412-415.
[34] Norde W., Luklema J. Why proteins prefer interfaces
[26]
Tristram G. R. Proteine. N.Y. V. 1. 1953. Р. 244.
// J. Biomater. Sci. Polym. Ed. 1991. V. 2. P. 183-202.
[27]
Dabrowski A. Adsorption — from theory to practice
[35] Цветков В. Н. Жесткоцепные полимерные молеку-
// Adv. Colloid and Interface Sci. 2001. V. 93. P. 135-
лы. Л.: Наука, 1986. С. 161-176.
[36] Михайлин Ю. А. Термоустойчивые полимеры и
[28]
Foo K. Y., Hameed B. H. Insights into the modeling
полимерные материалы. СПб: Профессия, 2006.
of adsorption isotherm systems // Chem. Eng. J.
С. 348-462.