Журнал прикладной химии. 2019. Т. 92. Вып. 4
НЕОРГАНИЧЕСКИЙ СИНТЕЗ И ТЕХНОЛОГИЯ НЕОРГАНИЧЕСКИХ ПРОИЗВОДСТВ
УДК 546.281:543.544
ИССЛЕДОВАНИЕ СТАБИЛЬНОСТИ РЯДА МОЛЕКУЛЯРНЫХ ПРИМЕСЕЙ
В МОНОСИЛАНЕ
© A. Ю. Созин1, В. А. Крылов2, О. Ю. Чернова1, Т. Г. Сорочкина1,
А. Д. Буланов1,2, О. Ю. Трошин1,2, А. П. Котков1,3, Н. Д. Гришнова1,3,
А. И. Скосырев1,3, М. Н. Матвеева2
1 Институт химии высокочистых веществ им. Г. Г. Девятых РАН, Нижний Новгород
2 Нижегородский государственный университет им. Н. И. Лобачевского
3 ОА НПП Салют, Нижний Новгород
E-mail: sozin@ihps.nnov.ru
Поступила в Редакцию 25 сентября 2018 г.
После доработки 30 января 2019 г.
Принята к публикации 4 февраля 2019 г.
Методом хроматомасс-спектрометрии проведено исследование стабильности примесей углеводоро-
дов С1-С7, фтор-, хлорпроизводных углеводородов, алкилпроизводных силана, гомологов моносилана,
силоксанов в моносилане при его хранении в ампулах из молибденового стекла и баллонах из нержаве-
ющей стали. Установлено, что при хранении в стеклянных ампулах происходит уменьшение концен-
трации примесей этилена и тетрафторэтилена и увеличение концентрации этилсилана и дисилана.
При хранении моносилана в баллоне из нержавеющей стали установлено изменение концентрации
присутствующей в нем примеси ацетилена.
Ключевые слова: моносилан; примеси; концентрация; хроматомасс-спектрометрия
DOI: 10.1134/S0044461819040029
Моносилан является исходным веществом для
химической устойчивости примесей на разных ста-
получения высокочистого изотопно-обогащенного
диях получения высокочистого моносилана, в том
кремния, который является перспективным материа-
числе и при его хранении. Изменение примесного
лом для создания физически обоснованного эталона
состава моносилана может существенно влиять на
единицы массы и уточнения значения числа Авогадро
результаты его аттестации и на качество получаемых
[1-3], создания квантового компьютера, элементов
из него материалов.
интегральных схем, спиновой наноэлектроники,
Согласно литературным данным, в образцах изо-
новых полупроводниковых структур, радиационно
топно-обогащенного 28SiH4, полученного по реакции
стойких детекторов ионизирующих излучений [4-6].
28SiF4 c CaH2, обнаружены примеси предельных и
Для получения кремния, в том числе изотопно-обога-
непредельных углеводородов С1-С9, некоторых их
щенного, используется моносилан, который должен
фтор- и хлорпроизводных, алкилсиланов, силокса-
обладать высокой химической чистотой. Поэтому
нов, гомологов моносилана Si2H6-Si5H12, моногер-
при разработке методик его глубокой очистки важ-
мана [7-9]. Их концентрации находятся на уровне
ной является информация о присутствующих в нем
n·10-1-n·10-6 мол%. Следует отметить возможность
примесях. Также представляют интерес сведения о
взаимодействия ряда примесных соединений с моно-
436
Исследование стабильности ряда молекулярных примесей в моносилане
437
силаном, что приводит к изменению качественного и
Примесный состав 28SiH4
количественного состава примесей [10-16]. По дан-
ным [10] моносилан способен вступать в реакции с
Концентрация, мол%
предельными углеводородами с заметной скоростью
Примесь
очищенный
после синтеза
при температуре 600°С с образованием алкилсиланов.
образец
В работах [11-13] изучено взаимодействие моно-
силана с непредельными углеводородами, главным
N2
(9.8 ± 0.9)·10-4
(4.0 ± 0.5)·10-5
образом — этилена. Эта примесь является одной из
Ar
(1.0 ± 0.1)·10-4
(9 ± 2)·10-7
наиболее трудноудаляемых при ректификационной
CO
(6 ± 1)·10-5
<3·10-5
очистке моносилана [2], поэтому изучение ее пове-
CH4
(3.2 ± 0.3)·10-3
<5·10-6
дения является актуальным. Конверсия этилена в
С2H2
(9 ± 2)·10-6
<2·10-6
другие формы примесей позволяет повысить эффек-
C2H4
(1.7 ± 0.2)·10-4
<2·10-6
тивность глубокой очистки моносилана. При его вза-
имодействии с этиленом при 460-510°С и давлении
C2H6
(5.6 ± 0.6)·10-5
<2·10-6
760 мм рт. ст. основными продуктами реакции явля-
C3H6
(2.1 ± 0.2)·10-5
<2·10-6
ются моно- и диалкилсиланы [11]. При повышенном
C3H8
(9.3 ± 0.9)·10-6
<1·10-6
давлении указанная реакция протекает при 100°С.
i-C4H10
(1.4 ± 0.2)·10-5
<2·10-6
В обычных условиях взаимодействие SiH4 с C2H4
возможно при облучении ультрафиолетовым светом,
n-C4H10
(6 ± 1)·10-6
<2·10-6
основным продуктом фотохимической реакции явля-
C4H8 1-пропен-2-ме-
(7 ± 2)·10-6
<2·10-6
ется винилсилан [12]. Этилен также взаимодействует
тил
с моносиланом в присутствии оксидов некоторых
C4H8 1-бутен
(4 ± 1)·10-6
<2·10-6
металлов (ZrO2, MgO, Al2O3) при температуре 500-
C4H8 2-бутен
(3 ± 1)·10-6
<2·10-6
600°С [13], а также при пропускании через молеку-
n-C5H12
(3 ± 1)·10-6
<2·10-6
лярные сита 4А [14]. Продуктами данных реакций
n-C7H16
(4 ± 2)·10-6
<2·10-6
являются этилсилан и диэтилсилан. По данным [10]
при температуре 200-800°С в присутствии MgO обра-
C6H6
(4.8 ± 0.5)·10-4
<2·10-7
зуется этинилсилан и этинилдивинилсилан. Из работ
GeH4
(1.2 ± 0.1)·10-5
<3·10-6
[15, 16] известно, что в результате неполного терми-
C2F4
(4.0 ± 0.5)·10-3
<3·10-7
ческого разложения силана происходит образование
1,1-C2H2F2
(1.1 ± 0.3)·10-6
<3·10-7
из него дисилана, трисилана и водорода.
С2НF3
(4 ± 1)·10-4
<3·10-7
Изменение качественного и количественного со-
става примесей моносилана может оказаться весьма
CHF3
(4 ± 1)·10-5
<5·10-6
существенным при повышенной температуре, высо-
транс-1,2-C2H2F2
(4 ± 1)·10-4
<5·10-7
ком давлении, длительном времени контакта реаген-
цис-1,2-С2Н2F2
(4 ± 1)·10-5
<4·10-7
тов. Следует отметить, что ряд указанных факторов
СH3Cl
(7 ± 2)·10-6
<5·10-7
реализуется при хранении моносилана в сжатом со-
СF3Cl
(3 ± 1)·10-4
<5·10-7
стоянии. Исследований качественного и количествен-
ного примесного состава моносилана в условиях его
Si2H6O
(6 ± 2)·10-1
(7 ± 2)·10-6
хранения при комнатной температуре нами в литера-
Si3H8O2
(6 ± 2)·10-2
(1.4 ± 0.5)·10-6
туре не найдено.
i-Si4O3H10
(1.1 ± 0.3)·10-2
(1.3 ± 0.3)·10-6
Целью работы являлось исследование стабиль-
n-Si4O3H10
(2.0 ± 0.7)·10-3
<2·10-7
ности молекулярных форм присутствующих в моно-
Si2OH4F2
(6 ± 2)·10-6
<7·10-7
силане примесей при его хранении в металлических
баллонах и стеклянных ампулах при комнатной тем-
Si2OH5F
(7 ± 2)·10-5
<6·10-7
пературе.
Si3O2H6F2
(2.0 ± 0.7)·10-6
<3·10-7
Si3O2H7F
(4 ± 1)·10-5
<4·10-7
Экспериментальная часть
Si2H6
(1.2 ± 0.3)·10-1
(4 ± 1)·10-5
В работе исследовали поведение примесей в изо-
Si3H8
(1.9 ± 0.6)·10-2
(8 ± 1)·10-7
топно-обогащенном моносилане 28SiH4, полученном
i-Si4H10
(3 ± 1)·10-3
(6 ± 2)·10
-7
по реакции взаимодействия изотопно-обогащенного
438
Созин А. Ю. и др.
колонку осуществляли с помощью системы про-
Продолжение таблицы
боотбора, выполненной из металлических трубок
Концентрация, мол%
(нержавеющая сталь 12Х18Н10). Ввод пробы осу-
Примесь
ществляли автоматическим краном-дозатором Valco
очищенный
после синтеза
образец
EH2C6WEZPH-CER5, функционировавшим в защит-
ной атмосфере гелия марки Б (ТУ 51-940-80). Объем
n-Si4H10
(1.4 ± 0.4)·10-3
(3 ± 1)·10-7
пробы составлял 50 мкл при давлении 0.1-1.0 атм.
i-Si5H12
(6 ± 2)·10-4
<3·10-6
Подробное описание применяемой системы про-
n-Si5H12
(8 ± 2)·10-5
<3·10-6
боотбора приводится в работе [7]. Для хроматогра-
CH3SiH3
(2.7 ± 0.9)·10-3
<1·10-6
фического разделения примесей, имеющих невы-
сокие относительно силана температуры кипения,
C2H5SiH3
(3 ± 1)·10-5
<1·10-6
использовали капиллярную адсорбционную колонку
(SiH3)2CH2
(4 ± 1)·10-4
<3·10-7
GS-GasPro 60 м × 0.32 мм (Agilent Techologies), со-
(CH3)2SiH2
(1.2 ± 0.3)·10-5
<4·10-7
держащую в качестве сорбента модифицированный
Si2H5CH3
(8 ± 2)·10-5
<1·10-6
силикагель. Для определения примесей с более вы-
SiC3H10
(4 ± 1)·10-6
<8·10-7
сокими температурами кипения использовали ка-
пиллярную адсорбционную колонку с сорбентом по-
SO2F2
(3 ± 1)·10-6
<9·10-7
литриметилсилилпропином 25 м × 0.26 мм [19]. При
использовании колонки GS-GasPro начальная темпе-
тетрафторида кремния 28SiF4 с гидридом кальция
ратура анализа составляла 30°С. Затем через 8 мин
[17, 18]. В таблице приведен примесный состав ис-
ее повышали до 100°С со скоростью 10 град·мин-1.
следуемых образцов моносилана: после синтеза и
Выдерживали при этой температуре 5 мин и далее
очистки методом низкотемпературной ректификации.
повышали до 130°С со скоростью 10 град·мин-1. При
Определение концентрации примесей проводили по
использовании колонки c политриметилсилилпропи-
методикам, приведенным в работах [7-9].
ном начальная температура анализа составляла 30°С.
Изучали поведение примесей в моносилане при
Через 8 мин ее повышали со скоростью 10 град·мин-1
хранении его в ампулах из молибденового стекла, не
до 130°С и выдерживали при этой температуре до
защищенных от света, и в металлическом баллоне для
окончания анализа. В качестве газа-носителя при-
работы с особо чистыми веществами класса 6N, изго-
меняли гелий марки 70 (ТУ 0271-001-45905715-02).
товленном из нержавеющей стали марки 12Х18Н10Т.
Его средняя линейная скорость в колонках составляла
Начальное давление моносилана в них составляло
30 см·с-1. Во время выхода из колонки максималь-
3 абс. атм.
ной концентрации основного компонента отключали
При хранении моносилана в ампулах контроли-
напряжение на ионном источнике для исключения
ровали поведение следующих примесных веществ:
перегорания катода. При использовании колонки GS-
этилена, дисилана, об изменении концентрации ко-
GasPro время отключения составляло 4.2-5.3 мин, а
торых в нем сообщается в литературных источниках,
для колонки с политриметилсилилпропином напря-
а также тетрафторэтилена, являющегося, как и эти-
жение включали через 1.9 мин после начала анализа.
лен, непредельным соединением. Для этого готовили
Масс-спектры примесей регистрировали в режи-
смесь указанных веществ и очищенного моносилана
ме ионизации электронами (энергия ионизирующих
(см. таблицу), в котором концентрации этих веществ
электронов 70 эВ) в интервале сканирования масс
и вероятных продуктов реакции были ниже пределов
12-350 а. е. м. Напряжение на электронном умножи-
обнаружения. Для ее приготовления использовали
теле, выставленное при автоматической настройке
C2H4 (ГОСТ 25070-87) и C2F4 (СТП 044-39-200).
электронной оптики, составляло 1435 В. Температура
Концентрация этих веществ в смеси составляла
источника ионов была 150°С, квадрупольного филь-
(1.6 ± 0.2)·10-3 и (4.0 ± 0.5)·10-3 мол% соответствен-
тра масс — 106°С, интерфейса — 200°С.
но. Дисилан в смесь не вводили, так как он уже при-
Идентификацию примесей проводили сравнени-
сутствовал в моносилане на уровне (4 ± 1)·10-5 мол%.
ем их экспериментальных масс-спектров с библи-
Исследуемые образцы моносилана храни-
отечными из базы данных NIST 2005, входящей в
ли при комнатной температуре 18-25°С в течение
состав программного обеспечения хроматомасс-спек-
370 дней. Анализ образцов проводили с использова-
трометра. Для большинства веществ коэффициенты
нием хроматомасс-спектрометра Agilent 6890/MSD
подобия их масс-спектров с библиотечными состав-
5973N. Дозирование проб в хроматографическую
ляли высокие значения — 0.85-0.95, что свидетель-
Исследование стабильности ряда молекулярных примесей в моносилане
439
ствовало о высокой надежности их идентификации.
В ходе наблюдений отмечено образование продук-
Примеси германа, силоксанов, фторсилоксанов, го-
та реакции этилена с моносиланом — этилсилана.
мологов силана отсутствуют в этой библиотеке. Их
В начале исследований концентрация этой примеси
идентифицировали с использованием масс-спектров,
находилась ниже предела обнаружения, составля-
приведенных работах [8, 20].
ющего 1·10-6 мол%. Часть кривой, относящейся к
Количественное определение примесей проводи-
изменению его концентрации на графике с 0-го по
ли методом абсолютной градуировки по площадям
21-й день, обозначена штриховой линией, так как
хроматографических пиков и с использованием за-
начальная концентрация этилсилана неизвестна. По
висимости чувствительности детектирования от ве-
мере протекания реакции, как видно из графика, кон-
личин их полных сечений ионизации [8, 21] согласно
центрация этилсилана к 309-му дню наблюдений
методикам [7-9].
достигла (1.6 ± 0.5)·10-3 мол%, что коррелирует с
начальной концентрацией этилена.
На рис. 2 приведены результаты исследования
Обсуждение результатов
изменения концентрации тетрафторэтилена в силане
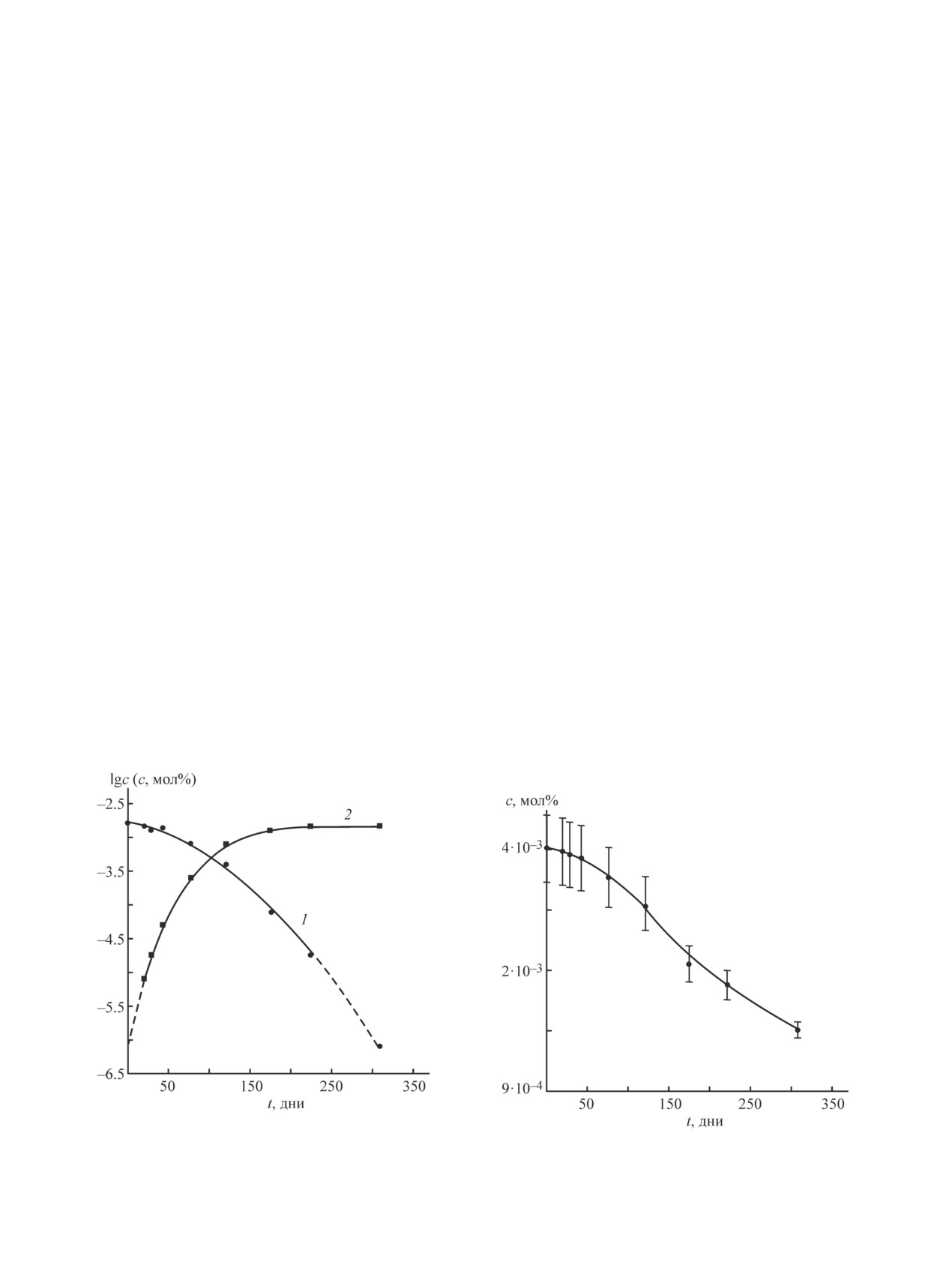
На рис. 1 приведена кинетическая кривая, описы-
при хранении в стеклянной ампуле. Видно, что изме-
вающая изменение концентрации примеси этилена в
нения его концентрации произошли в меньшей степе-
моносилане при его хранении в стеклянной ампуле.
ни. Так, за время 309 дней его концентрация умень-
Из полученных результатов видно, что в течение
шилась с (4.0 ± 0.5)·10-3 до (1.0 ± 0.2)·10-3 мол%.
225 дней наблюдений произошло изменение кон-
Возможные продукты реакции тетрафторэтилена
центрации этилена с (1.6 ± 0.2)·10-3 до (2.0 ± 0.2)×
с силаном (фторалкилпроизводные силана) установ-
×10-5 мол%. Часть кривой, отображающей изменение
лены не были. Вероятной причиной этого может
его концентрации с 225-го по 309-й день, отмече-
быть специфическое взаимодействие этих веществ
на штриховой линией. Данный участок представ-
с сорбентами в хроматографических колонках, в ре-
ляет собой аппроксимацию зависимости изменения
зультате которых не происходит их элюирования.
концентрации этой примеси. Концентрация этилена
В работах, посвященных исследованию примесного
на 309-й день наблюдений была ниже предела об-
состава силана, получаемого из тетрафторида крем-
наружения, составляющего 2·10-6 мол%. Согласно
ния [7-9], также, несмотря на присутствие в силане
аппроксимации его концентрация при сохранении на-
большого разнообразия фторсодержащих углеводоро-
блюдаемой динамики изменений может уменьшиться
дов, не было отмечено присутствие в нем примесей
до 8·10-7 мол% в течение указанного времени хранения.
фторированных алкилпроизводных силана.
Возможными причинами различной реакционной
способности примесей C2H4 и C2F4 в SiH4 является
Рис. 1. Изменение концентрации C2H4 (1) и Si2H5CH3
(2) в моносилане во времени при хранении его в сте-
Рис. 2. Изменение концентрации C2F4 в моносилане во
клянной ампуле.
времени при хранении его в стеклянной ампуле.
440
Созин А. Ю. и др.
При исследовании поведения примесей в моноси-
лане после синтеза при хранении в баллоне наблю-
дение за изменением их концентраций проводили в
течение 370 дней. Из всех присутствующих приме-
сей, включая этилен, дисилан, тетрафторэтилен, было
отмечено изменение только концентрации ацетилена
(рис. 4). Из полученных данных видно, что за время
хранения его концентрация уменьшилась с (9 ± 2)·10-6
до (3 ± 1)·10-6 мол%. Возможные продукты реакции
[10] — винилсилан и этинилдивинилсилан обнару-
жены не были. Во многом это может быть связано с
низкой исходной концентрацией примеси ацетилена
и образующихся продуктов. Изменения концентраций
остальных примесей в течение данного времени но-
сят случайный характер и не превышают 20% от их
первоначального значения.
Таким образом, установлено, что при хранении
силана в ампуле из молибденового стекла происходит
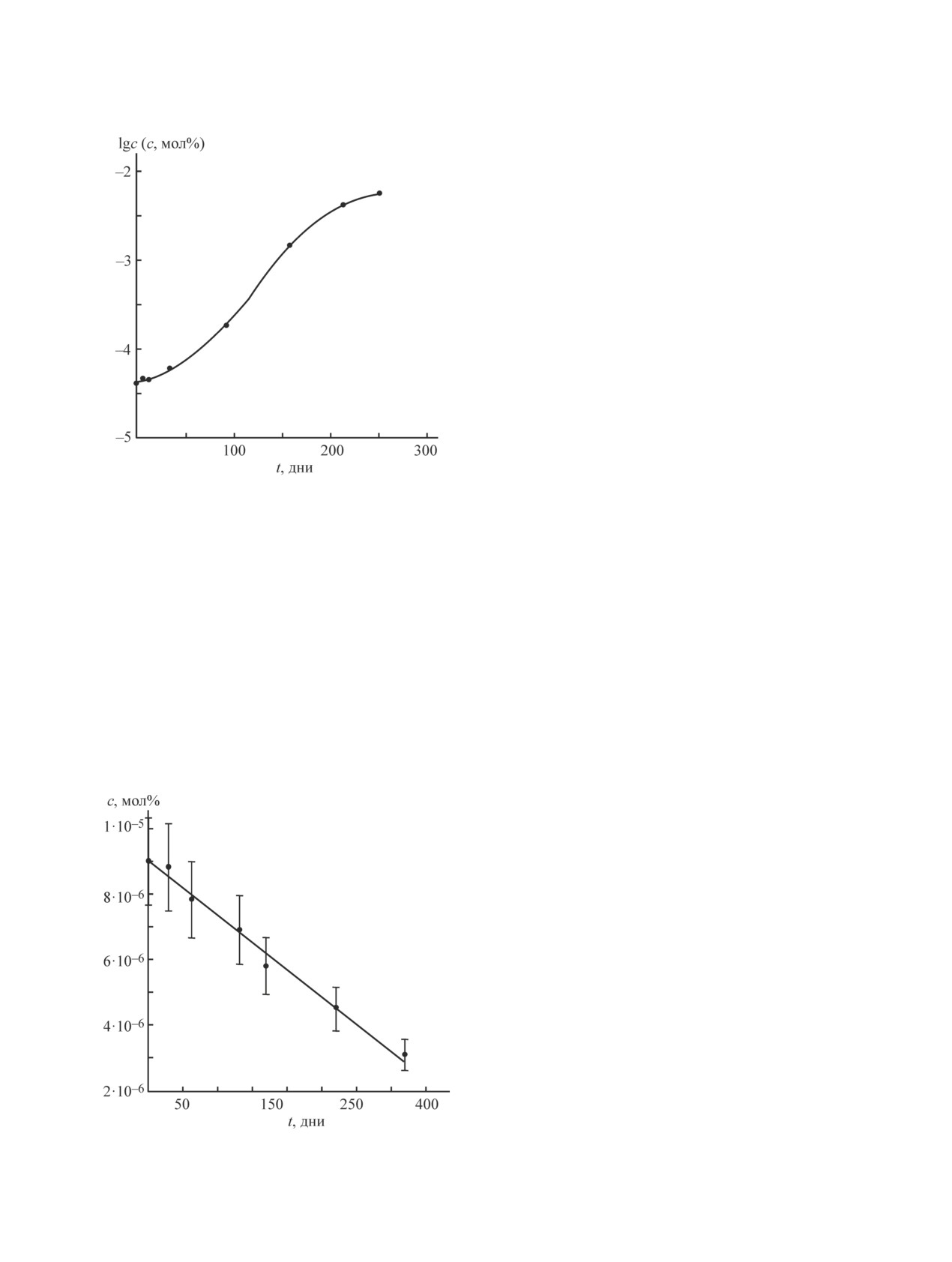
Рис. 3. Изменение концентрации Si2H6
во времени при уменьшение концентрации присутствующих в нем
хранении моносилана в ампуле.
примесей этилена и тетрафторэтилена, а концентра-
ция дисилана увеличивается. Возможной причиной
сложность образования промежуточного соединения
этого является протекание фотохимических реакций
тетрафторэтилена с силаном из-за пониженной элек-
C2H4 и С2F4 с основным компонентом, а увеличение
тронной плотности на атомах углерода по причине
концентрации дисилана связано с разложением мо-
отрицательного индукционного эффекта, оказываемо-
носилана. О подобной возможности взаимодействия
го атомами фтора, а также из-за экранирования ими
примесей под действием ультрафиолетового света
атомов углерода [22].
сообщается в работе [12]. Протекание таких реакций
Результаты изучения стабильности примеси ди-
под действием света также подтверждается тем, что
силана при хранении моносилана в ампуле показы-
при хранении в металлическом баллоне изменения
вают, что за 250 дней произошло изменение концен-
концентраций этих веществ отмечено не было.
трации дисилана с (4 ± 1)·10-5 до (6 ± 2)·10-3 мол%
(рис. 3).
Выводы
1. Для исследования стабильности примесей в
моносилане проведено сопоставление данных по
концентрации ряда молекулярных примесей в моно-
силане. Установлено, что в моносилане при хранении
в течение 309 сут содержание этилена снижается
с (1.6 ± 0.2)·10-3 до уровня менее 2·10-6 мол%, со-
держание этилсилана увеличивается с уровня менее
1·10-6 до (1.6±0.5)·10-3 мол%. Изменение концен-
трации этилсилана коррелирует с изменением со-
держания этилена в моносилане и свидетельствует о
взаимодействии моносилана с этиленом.
2. Установлено снижение концентрации те-
трафторэтилена в моносилане с (4.0 ± 0.5)·10-3 до
(1.0 ± 0.2)·10-3 мол% и увеличение концентрации
дисилана с (4 ± 1)·10-5 до (6 ± 2)·10-3 мол% при хра-
нении в стеклянной ампуле в течение 309 сут.
3. При хранении моносилана в металлическом
Рис. 4. Изменение концентрации примеси C2H2 во вре-
баллоне для работы с особо чистыми веществами
мени при хранении моносилана в баллоне.
класса 6N из нержавеющей стали 12Х18Н10Т уста-
Исследование стабильности ряда молекулярных примесей в моносилане
441
новлено уменьшение концентрации ацетилена с
[Devyatykh G. G., Bulanov A.D., Gusev A.V. Kova-
(9 ± 2)·10-6 до (3 ± 1)·10-6 мол%. Изменение кон-
lev I. D., Krylov V. A., Potapov A. M., Sennikov P. G.,
центрации других веществ, в том числе этилена и
Adamchik S. A., Gavva V. A., Kotkov A. P., Churba-
nov M. F., Dianov E. M., Kaliteevskii A. K., Godisov O. N.,
этилсилана, в пределах погрешности не наблюдается.
Pohl H.-J., Becker P., Riemann H., Abrosimov N. V. //
Russ. Reports Acad. Sci. 2008. V. 421. N 1. P. 61-64].
Финансирование работы
[4] Чурбанов М. Ф., Гусев А. В., Буланов А. Д., Пота-
Работа выполнена в соответствии с Программой
пов А. М. // Изв. АН. Сер. хим. 2013. № 2. С. 275-280
фундаментальных научных исследований госу-
[Churbanov M. F., Gusev A. V., Bulanov A. D., Pota-
pov A. M. // Russ. Chem. Bull. 2013. N 2. P. 275-280].
дарственных академий наук на 2019-2021 годы,
[5] Takyu K., Itoh K. M., Oka K., Saito N., Ozhogin V. I. //
№ темы 0095-2019-0001 и 0095-2019-0008.
Jpn. J. Appl. Phys. 1999. V. 38. P. 1493-1495.
[6] Инюшкин А. В. // Неорган. материалы. 2002. Т. 38.
Конфликт интересов
№ 5. С. 527-534 [Inyushkin A. V. // Inorg. Mater.
Авторы заявляют об отсутствии конфликта инте-
2002. V. 38. N 5. P. 527-534].
ресов, требующего раскрытия в данной статье.
[7] Крылов В. А., Чернова О. Ю., Созин А. Ю. // Масс-
спектрометрия. 2007. Т. 4. № 2. С. 125-130.
[8] Крылов В. А., Созин А. Ю., Зорин В. А., Берез-
Информация об авторах
кин В. Г., Крылов А. В. // Масс-спектрометрия.
Созин Андрей Юрьевич, к.х.н., ORCID: https://
2008. Т. 6. № 4. С. 225-233.
orcid.org/0000-0002-0237-6998
[9] Крылов В. А., Чернова О. Ю., Созин А. Ю. //
Крылов Валентин Алексеевич, д.х.н., ORCID:
Аналитика и контроль. 2011. Т. 5. № 4. С. 421-428.
[10] White G., Rochow E. G. // J. Am. Chem. Soc. 1954.
V. 76. P. 3897-3902.
org/0000-0002-1028-4946
[11] Pat. US 2537763 (publ. 1951). Preparation of organo-
silanes.
Сорочкина Татьяна Геннадьевна, к.х.н., ORCID:
[12] Pat. US 2786862 (publ. 1957). Preparation of dialkyl-
silanes.
Буланов Андрей Дмитриевич, д.х.н., ORCID:
[13] Itoh M., Iwata K., Mitsuzuka M. // Appl. Catal. A:
General. 2001. V. 217. P. 185-189.
[14] Pat. US 4554141 (publ. 1992). Removal of ethylene
org/0000-0001-6996-1561
from silane using a distillation step after separation
Котков Анатолий Павлович, к.х.н., ORCID: https://
using a zeolite molecular sieve.
orcid.org/0000-0001-7476-5936
[15] Вотинцев В. Н., Михеев В. С., Смирнов В. Н. //
Гришнова Наталья Дмитриевна, к.х.н., ORCID:
Высокочистые вещества. 1988. № 12. C. 17-28.
[16] Neudorfi P., Jodhan A., Strausz O. P. // J. Phys. Chem.
1980. V. 84. N 3. P. 338-339.
org/0000-0003-3372-0904
[17] Скорынин Г. М., Пульников И. И., Шарин Г. А.,
Зырянов С. М. // Изв. Том. политех. ун-та. 2004.
Матвеева Марина Николаевна, ORCID: https://
Т. 307. № 7. С. 88-90.
orcid.org/0000-0002-7660-6960
[18] Девятых Г. Г., Дианов Е. М., Буланов А. Д., Тро-
шин О. Ю., Балабанов В.В., Пряхин Д. А. // ДАН.
Список литературы
2003. Т. 391. № 5. С. 638-639 [Devyatykh G. G.,
[1] Becker P., Schiel D., Pohl H.-J., Kaliteevski A. K.,
Dianov E. M., Bulanov A. D. Troshin O. Yu., Balaba-
Godisov O. N., Churbanov M. F., Dianov E. M. // Meas.
nov V. V., Priakhin D. A. // Russ. Reports Acad. Sci.
Sci. Technol. 2006. V. 17. P. 1854-1860.
2003. V. 391. N 5. P. 638-639].
[2] Becker P., Bettin H., De Bievre Holm С., Kutgens U.,
[19] Березкин В. Г., Королев А. А., Хотимский В. С. //
Spieweck F., Stumpel J., Valkiers S., Zulehner W. // IEEE
ДАН. 2000. Т. 370. № 2. С. 200-204 [Berezkin V. G.,
Transactions on instrumentation and measurement.
Korolev A. A., Khotimsky V. S. // Russ. Reports Acad.
1995. V. 45. P. 522-525.
Sci. 2000. V. 370. N 2. P. 200-204].
[3] Девятых Г. Г., Буланов А. Д., Гусев А. В., Кова-
[20] Агафонов И. Л., Девятых Г. Г. Масс-спектрометри-
лев И. Д., Крылов В. А., Потапов А. М., Сенни-
ческий анализ газов и паров особой чистоты. М.:
ков П. Г., Адамчик С. А., Гавва В. А., Котков А. П.,
Наука, 1980. 336 с.
Чурбанов М. Ф., Дианов Е. М., Калитеевский А. К.,
[21] Fitch W. L. // Anal. Chem. 1983. V. 55. N 6. P. 832-835.
Годисов О. Н., Поль Х.-Й., Беккер П., Риман Х.,
[22] Матье Ж., Панико Р. Курс теоретических основ
Абросимов Н. В. // ДАН. 2008. Т. 421. № 1. С. 61-64
органической химии. М.: Мир, 1975. 556 с.