Журнал прикладной химии. 2019. Т. 92. Вып. 4
ВЫСОКОМОЛЕКУЛЯРНЫЕ СОЕДИНЕНИЯ И МАТЕРИАЛЫ НА ИХ ОСНОВЕ
УДК 541.64:539.2:537.5
ВЛИЯНИЕ ДОБАВКИ КОМПЛЕКСА ЖЕЛЕЗА(III)
С ТЕТРАФЕНИЛПОРФИРИНОМ НА СТРУКТУРУ ВОЛОКОН
ПОЛИ(3-ГИДРОКСИБУТИРАТА), ПОЛУЧЕННЫХ ЭЛЕКТРОФОРМОВАНИЕМ
© А. А. Ольхов1,2,3, А. В. Лобанов1,2, С. Г. Карпова3, А. В. Бычкова3,
А. А. Артюх3, А. Н. Голощапов3, А. Л. Иорданский1
1 Институт химической физики им. Н. Н. Семенова РАН, Москва
2 Российский экономический университет им. Г. В. Плеханова, Москва
3 Институт биохимической физики им. Н. М. Эмануэля РАН, Москва
E-mail: aolkhov72@yandex.ru
Поступила в Редакцию 1 октября 2018 г.
После доработки 26 ноября 2018 г.
Принята к публикации 20 декабря 2018 г.
Методом электроформования получены ультратонкие волокна на основе биополимера поли(3-гидрок-
сибутирата), содержащие 1-5 мас% комплекса железа(III) с тетрафенилпорфирином. Межмолеку-
лярное взаимодействие компонентов волокон изучено методом УФ-спектроскопии. С помощью метода
магнитного резонанса определено наличие парамагнитных реакционных центров в смесях. Структура
кристаллических и аморфных областей волокон изучена методами дифференциальной сканирующей
калориметрии, рентгеноструктурного анализа, методом ЭПР спиновых зондов, сканирующей элек-
тронной микроскопии. Показано, что при добавлении комплекса в волокна поли(3-гидроксибутирата)
наблюдается увеличение размера кристаллитов и значительный рост степени кристалличности,
замедляется молекулярная подвижность в аморфных областях полимера. Температурный отжиг
при 140°С приводит к резкому росту кристалличности и снижению молекулярной подвижности в
аморфных областях поли(3-гидроксибутирата). Озонолиз изучаемых волокон при небольшом времени
воздействия (до 5 ч) обусловливает резкое замедление молекулярной подвижности, при более длитель-
ном озонировании волокон наблюдается рост подвижности. Полученные волокнистые материалы
обладают бактерицидными свойствами и могут найти приложение при создании терапевтических
систем антибактериального и противоопухолевого действия.
Ключевые слова: комплекс железа(III) с тетрафенилпорфирином, ультратонкие волокна, поли(3-ги-
дроксибутират), электроформование, озонолиз, кристаллическая структура, аморфная фаза, бак-
терицидные свойства.
DOI: 10.1134/S0044461819040066
В схемах лечения многих инфекционных и онколо-
систем используется наиболее распространенный
гических заболеваний часто применяются трансдер-
представитель нового класса природных полиэфи-
мальные системы на основе твердых полимерных
ров — поли(3-гидроксибутират) (ПГБ).
матриц или гелей, содержащих функциональные ве-
Одним из перспективных видов матриц с анти-
щества с антисептическими (бактерицидными) свой-
септическими свойствами являются нано- и микрово-
ствами [1, 2]. Для создания таких терапевтических
локнистые нетканые материалы, получаемые методом
465
466
Ольхов А. А. и др.
электроформования. Метод основан на ориентации
ют другие — атом металла (реакции диссоциации и
полимерного раствора в виде тонкой вязкой струи в
металлообмена [14]) и связи металл-экстралиганд
поле действия механических и электростатических
для МР со сложной координационной сферой ком-
сил с последующим формированием волокна диаме-
плекса. Некоторые РЦ в молекулах Н2Р и МР всту-
тром в диапазоне от десятков до тысяч нанометров [3].
пают в реакции синхронно или почти синхронно,
Получение полимерных модификаций биологи-
как, например, третичные атомы азота и NH-связи
чески активных соединений является в настоящее
в реакциях комплексообразования [13], атомы ме-
время активно развивающейся областью химиче-
талла металлопорфиринов и π-макроциклический
ской технологии и направлено на синтез полимерных
хромофор в процессах образования молекулярных
материалов со значимыми биомедицинскими свой-
комплексов или формирования супрамолекулярных
ствами. Фундаментальный и прикладной интерес
систем [15].
к порфиринсодержащим полимерам связан с широ-
Наиболее перспективными носителями для функ-
кими возможностями синтеза молекулярных струк-
циональных низкомолекулярных веществ (частиц)
тур, обладающих специфическими свойствами, легко
являются полимерные волокна наноразмерного ди-
контролируемыми и изменяемыми в соответствии с
апазона.
областью их использования [4]. Установлено также
Настоящая работа рассматривает влияние желе-
лечебное действие различных порфиринов и их ме-
зо(III)хлортетрафенилпорфирина (FeClТФП) на гео-
таллокомплексов при лучевом поражении организма.
метрию, кристаллическую структуру и молекулярную
При этом показано, что эффективность радиозащит-
динамику в межкристаллитном пространстве (амор-
ного и пострадиационного воздействия порфиринов
фной фазе) ультратонких волокон поли(3-гидрокси-
существенно зависит от наличия в молекуле того или
бутирата). Исследуемый структурно-динамический
иного металла и полимерного окружения [5].
комплекс свойств волокнистых материалов является
Комплексы железа с порфиринами являются
основой для конструирования полимерных терапев-
гомогенными катализаторами автоокисления ряда
тических систем, обеспечивающих антибактериаль-
биогенных веществ. В этом процессе происходит
ные свойства.
промежуточное образование активных форм кислоро-
да — супероксидного анион-радикала, пероксидного
Экспериментальная часть
и гидроксильного радикалов, пероксида водорода,
цитостатическая активность которых хорошо извест-
Для получения волокон ПГБ использовали при-
на. Эти радикальные и ион-радикальные частицы
родный биоразлагаемый полимер полигидроксибу-
вызывают окислительные деструктивные реакции
тират серии 16F, полученный методом микробиоло-
в клетках, обусловливая бактерицидный эффект
гического синтеза компанией BIOMER® (Германия).
[6]. Порфирины принадлежат к числу соединений
Средневязкостная молекулярная масса ПГБ составля-
с большим количеством тесно взаимодействующих
ла 2.06·105, степень кристалличности ~59%.
реакционных центров (РЦ). Эта взаимосвязь РЦ во
В качестве модифицирующего вещества для соз-
многом и обусловливает специфику свойств молекул.
дания волокнистых матриксов с антисептическими
У простейших лигандов Н2Р имеется но крайней мере
свойствами использовали комплекс железа(III) с те-
четыре реакционных центра. Это пиррольные (-NH)
трафенилпорфирином (FeClТФП). Для получения во-
и пирролениновые (-N=) атомы азота, участвующие
локон готовили формовочные растворы ПГБ и ПГБ с
в процессах кислотно-основного взаимодействия [7],
FeClТФП в хлороформе. Концентрация ПГБ в раство-
комплексообразования [8] и нуклеофильного замеще-
ре составляла 7 мас%. Содержание FeClТФП в фор-
ния [9, 10], а также СβСβ-π-связи пиррольных колец,
мовочном растворе составляло 1, 3 и 5 мас% отно-
подверженные раскрытию или замещению водорода у
сительно массы ПГБ. Формовочные растворы ПГБ с
Сβ углеродного атома [9, 11, 12], и собственно макро-
FeClТФП готовили при температуре 60°С, используя
циклическая π-система, вступающая в реакции элек-
автоматическую магнитную мешалку. Волокна полу-
трофильного и нуклеофильного замещения Н-атома
чали методом электроформования (ЭФ) с помощью
в мезо-положении [11, 12], в процессы π-π-комплек-
однокапиллярной лабораторной установки с диаме-
сообразования, окисления-восстановления [13] и
тром капилляра 0.1 мм, напряжением электрического
т. д. При переходе к металлопорфиринам (МР) в ре-
тока 12 кВ, расстоянием между электродами 18 см,
зультате выравнивания электронной плотности на
электропроводимостью раствора 10 мкСм·см-1 [16].
атомах азота в молекуле исчезает РЦ, связанный с
ЭПР-спектры (Х-диапазона) регистрировали на
реакциями диссоциации NH-связи, однако возника-
автоматизированном ЭПР-спектрометре ЭПР-В
Влияние добавки комплекса железа(III) с тетрафенилпорфирином на структуру волокон...
467
(ИХФ РАН). Значение микроволновой мощности в
картины рассеяния высокого разрешения были полу-
резонаторе, чтобы избежать эффектов насыщения,
чены при помощи системы мало- и широкоуглового
не превышало 7 мВт. При записи спектров ампли-
рассеяния рентгеновского излучения S3-Micropix,
туда модуляции всегда была существенно мень-
изготовленной фирмой Hecus (CuKα-излучение,
ше ширины резонансной линии и не превышала
λ = 1.542 Å). Использовались детектор Pilatus 100K,
0.5 Гс. В качестве зонда использовали стабильный
а также линейный детектор PSD 50M в токе Ar/Me
нитроксильный радикал 2,2,6,6-тетраметилпипери-
8 бар, высокое напряжение на источнике Xenocs
дин-1-оксил (ТЕМПО). Радикал вводили в волокна
Genix трубке и ток составляли 50 кВ и 1 мА соответ-
из газовой фазы при температуре 40°С. Концентрация
ственно. Для формирования рентгеновского пучка
радикала в полимере не превышала 10-3 моль·л-1.
использовалась рентгеновская оптика Fox 3D, диаме-
Экспериментальные спектры спинового зонда в обла-
тры формирующих щелей в коллиматоре Кратки: 0.1
сти медленных движений (τ > 10-10 с) анализировали
и 0.2 мм соответственно. Интервал измерения углов
в рамках модели изотропного броуновского вращения
дифракции 0.003-1.9 A-1. Для устранения рассеяния
с помощью программы, описанной в работе [17]. При
рентгеновских лучей на воздухе блок рентгеновских
моделировании спектров были использованы следую-
зеркал и камера находились в вакуумной системе
щие главные значения g-тензора и тензора сверхтон-
(давление ≈ (2-3)·10-2 мм рт. ст.). Время накопления
кого взаимодействия (СТВ) радикала: gxx = 2.0096,
варьировали в интервале 600-5000 с.
gyy = 2.0066, gzz = 2.0025, Ахх = 7.0 Гc, Ayy = 5.0 Гc,
Геометрию волокнистых материалов исследовали
Azz = 35.0 Гc. Величина Аzz была определена экс-
с помощью сканирующего электронного микроскопа
периментально из ЭПР-спектров нитроксильного
Hitachi TM-3000 (Япония) при ускоряющем напряже-
радикала в полимере при -216°С, она незначитель-
нии 20 кВ. На поверхность образца нетканого волок-
но отличается от значения, приведенного в работе
нистого материала напыляли слой золота толщиной
[18]. Значения времени корреляции вращения зонда
100-200 Å.
τ в области быстрых вращений (5·10-11 < τ < 10-9 с)
Электронные спектры поглощения (УФ-спектры)
определяли из спектров ЭПР по формуле
растворов ПГБ-FeClТФП получены на спектрофо-
тометре Hitachi UV-2001 с использованием кварце-
τ = ∆Н+[(I+/I-)0.5 - 1]·6.65·10-10,
вых кювет с длиной оптического пути 1 см. Био-
логические исследования материалов проводили по
где ∆Н+ — ширина компоненты спектра, располо-
следующей методике. В качестве тест-культур были
женной в слабом поле; I+/I- — отношение интенсив-
использованы S.aureus р 209 (Золотистый стафило-
ностей компонент в слабом и сильном поле соответ-
кокк), S. typhimurium (Сальмонелла тифимуриум),
ственно.
E. coli 1257 (Эшерихиа коли). Контролем служили
Ошибка определения τ составляла ±5. Спектры
образцы необработанного волокнистого материа-
магнитного резонанса волокон без введения зонда
ла. Культуры тест-микроорганизмов пересевали на
регистрировали по методике, описанной в работе
скошенный мясо-пептонный агар и инкубировали в
[19] при разных настройках мощности: 0.1, 1, 10 мВт.
течение 17-18 ч при 37°С. Затем готовили в физиоло-
В образцы помещали стеклянную ампулу с этало-
гическом растворе суспензию каждого микроорганиз-
ном — Mn2+ (1 мг).
ма и устанавливали концентрацию микробных клеток
Исследование образцов методом дифференци-
по стандарту мутности 10 4 м.к./мл. В стерильные
альной сканирующей калориметрии (ДСК) было
чашки Петри помещали образцы волокнистого мате-
проведено на приборе DSC 204 F1 фирмы Netzsch
риала (контрольные и опытные) размером 10 × 10 см.
в среде аргона cо скоростью нагрева 10 град·мин-1.
По поверхности ткани распределяли 1 мл суспензии
Среднестатистическая ошибка измерения тепловых
тест-культуры и выдерживали при комнатной тем-
эффектов составляла ±3%. Энтальпия плавления бы-
пературе в течение 30 мин. Затем в чашку наливали
ла рассчитана по программе Netzsch Proteus [19].
9 мл стерильного физиологического раствора и вы-
Разделение пиков осуществлялось с помощью про-
держивали в течение 10-15 мин для элюирования
граммного обеспечения Netzsch Peak Separation 2006.01.
тест-культуры с волокнистого материала. По исте-
Вычисления проводили комбинированным методом
чении экспозиции материал из чашек в количестве
Гаусса-Ньютона, в котором метод Marquardt скомби-
100 мкл (0.1 мл) высевали на поверхность мясо-пеп-
нирован с оптимизацией длины шага итерации [20].
тонного агара, разлитого предварительно в чашки
Рентгеноструктурный анализ образцов проводили
Петри. Посевы инкубировали в течение 14-48 ч при
с использованием съемок на просвет. Двумерные
37°С. Параллельно производили высев используемых
468
Ольхов А. А. и др.
в опыте суспензий тест-культур для контроля кон-
Обсуждение результатов
центрации жизнеспособных микроорганизмов. Затем
В основе получения комплексов металлов с тетра-
проводили подсчет выросших на поверхности агара
фенилпорфирином лежат реакция комплексообразо-
колоний жизнеспособных микроорганизмов.
вания:
H2Р(Solv)p + MXm(Solv)n-m = МР(Solv)q + mHX(Solv)r,
где Н2Р — порфирин, МХm — соль металла, МР — ме-
с максимумом при 415-420 нм и малоинтенсивные
таллопорфирин, n — максимальное координационное
Q-полосы в области длин волн 550-650 нм. Полоса
число катиона металла в данном растворителе, m —
Соре, характерная для макроциклических структур,
число монодентатных однозарядных ацидолигандов.
обусловлена переходом π q π* типа, связанного с
Хлориды большинства двух- и трехзарядных ка-
переносом заряда с участием порфиринового лиганда
тионов металлов хорошо образуют с порфиринами
и атома металла.
комплексы в различных органических растворителях.
Молекулярный механизм заключается в том, что
На вставке рис. 1 приведена структурная формула
центральный атом металла, вытесняя из порфирино-
FeClТФП. Данное соединение обладает высокой ка-
вого лиганда два протона, оказывается практически в
талитической активностью перехода молекулярного
симметричном электростатическом поле четырех ато-
кислорода в активные формы, обусловливающие его
мов азота, с которыми он образует четыре эквивалент-
повышенные бактерицидные свойства.
ные координационные связи донорно-акцепторного
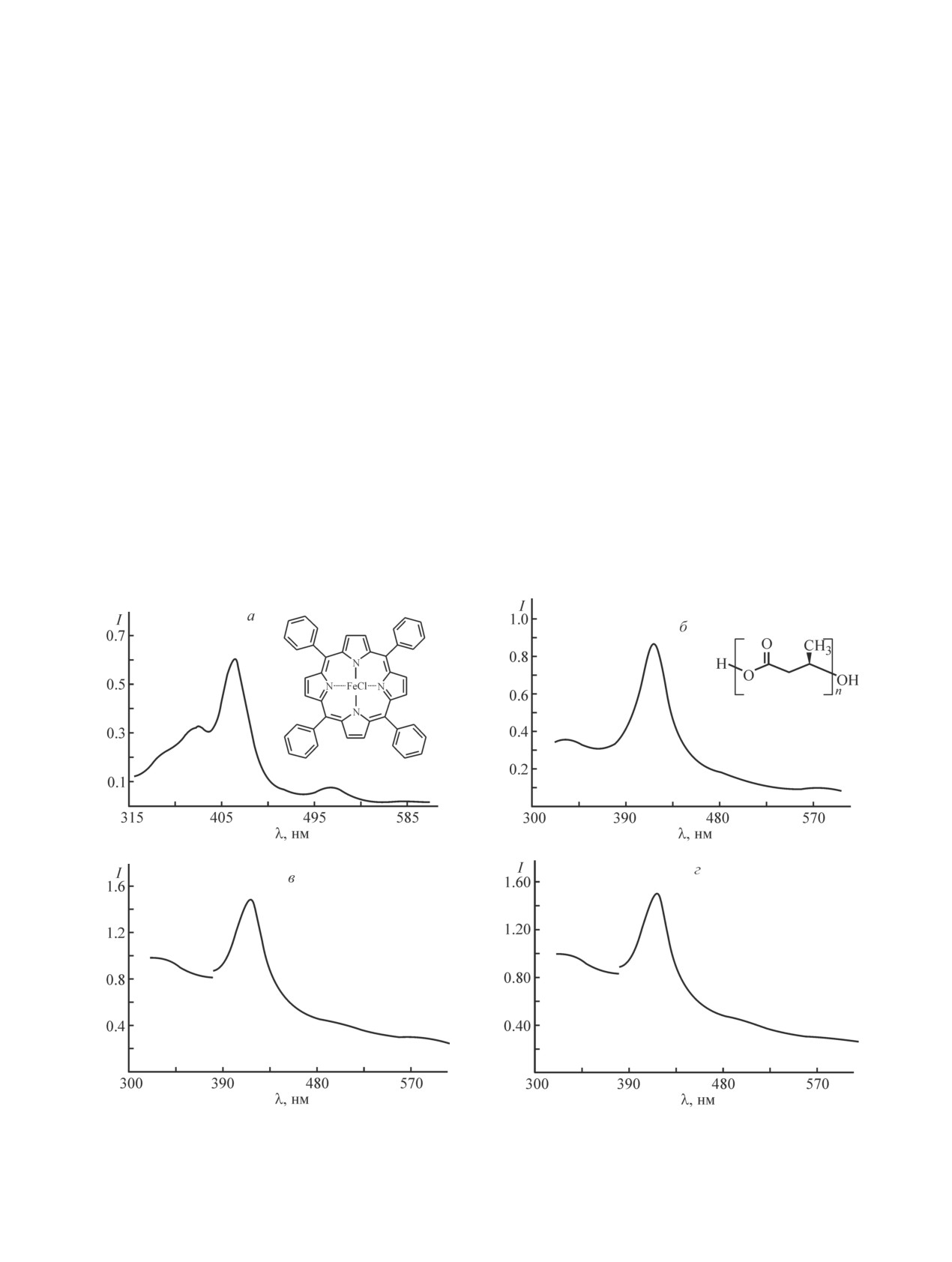
Электронные спектры поглощения (рис. 1) содер-
типа. Если взаимодействие металла с анионом порфи-
жат интенсивную характеристическую полосу Соре рина ограничивается преимущественно электростати-
Рис. 1. Электронные спектры (зависимость интенсивности от длины волны) FeClТФП в хлороформе (а) и смесей
ПГБ-FeClТФП в хлороформе с содержанием порфирина 1 (б), 3 (в) и 5% (г).
На вставках: а — структурная формула FeClТФП, б — структурная формула ПГБ.
Влияние добавки комплекса железа(III) с тетрафенилпорфирином на структуру волокон...
469
ческим взаимодействием, то образуются лабильные
комплексы ионного типа. Если же электростатическое
взаимодействие сопровождается заполнением вакант-
ных орбиталей центрального атома металла электро-
нами донорных N-атомов лиганда, то образуются ста-
бильные комплексы порфиринов преимущественно
ковалентного типа. Тот или иной тип взаимодействия
определяется как пространственной структурой пор-
фириновых лигандов (тетрадентатностью и относи-
тельной жесткостью планарного макрогетероцикла),
так и внешними факторами окружения (тип раство-
рителя, наличие в растворе полярных низкомоле-
кулярных или высокомолекулярных веществ и др.).
Из анализа рис. 1 следует, что положение полосы
Соре в растворах FeClТФП и ПГБ-FeClТФП не из-
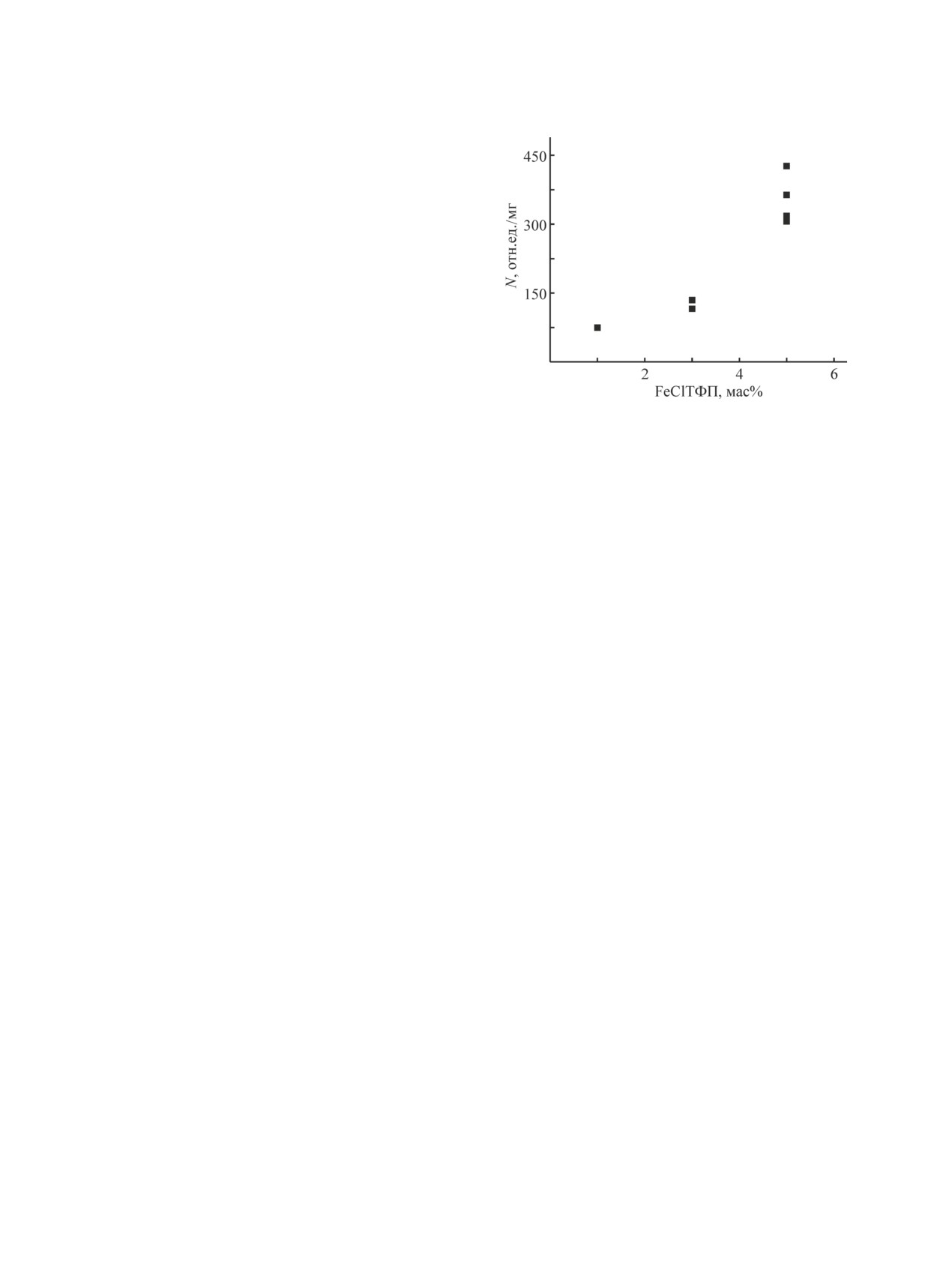
Рис. 2. Зависимость количества парамагнитных центров
меняется, что свидетельствует об отсутствии хими-
в волокнах ПГБ-FeClТФП, приведенных к 1 мг, от кон-
центрации FeClТФП.
ческого связывания комплексов с функциональными
группами ПГБ, а также водородных связей между
компонентами формовочного раствора. При этом
возрастает, что свидетельствует о парамагнитных
наблюдается некоторый рост интенсивности и уши-
свойствах комплексов как в формовочном растворе,
рения пиков растворов ПГБ-FeClТФП относительно
так и в волокне. По площадям спектральных кривых
раствора FeClТФП, что может свидетельствовать
образцов были рассчитаны относительные количе-
об адсорбционном взаимодействии компонентов по
ства парамагнитных центров (рис. 2).
механизму Ван-дер-Ваальса. При этом может проис-
Количество парамагнитных центров в образцах
ходить иммобилизация на полярных функциональных
находится практически в линейной зависимости от
группах ПГБ молекул порфириновых комплексов.
концентрации порфирина. Разброс показателя мо-
Иммобилизация FeClТФП на ПГБ предотвращает
жет быть связан с агломерацией части комплексов в
нежелательную ассоциацию комплексов, что может
матрице ПГБ, а также с межмолекулярным взаимо-
повышать устойчивость системы к агрессивным сре-
действием полимера с комплексами. На данные ЭМР
дам. Связанные полимером молекулы комплексов
может влиять остаточный статический электрический
порфиринов придают модифицированному полимеру
заряд, образующийся на поверхности ПГБ-волокон
значимые свойства: каталитическую, биологическую
при электростатическом формовании. Поскольку ПГБ
активность, фотофизические и фармакологические
и FeClТФП хорошо растворимы в хлороформе, мож-
свойства и др.
но ожидать равномерного распределения комплексов
Иммобилизованные макромолекулями ПГБ в рас-
в объеме волокна. При взаимном влиянии компо-
творах хлороформа супрамолекулярные комплексы
нентов возможно изменение морфологии волокон в
FeClТФП, по всей видимости, должны оставаться в
зависимости от концентрации FeClТФП. Методом
стабильном состоянии и при формировании твердого
сканирующей электронной микроскопии (СЭМ) были
ультратонкого волокна.
получены изображения участков волокнистых мате-
Каждая молекула супрамолекулярного комплекса
риалов, представленных на рис. 3.
FeClТФП имеет свой реакционный центр. Эти реак-
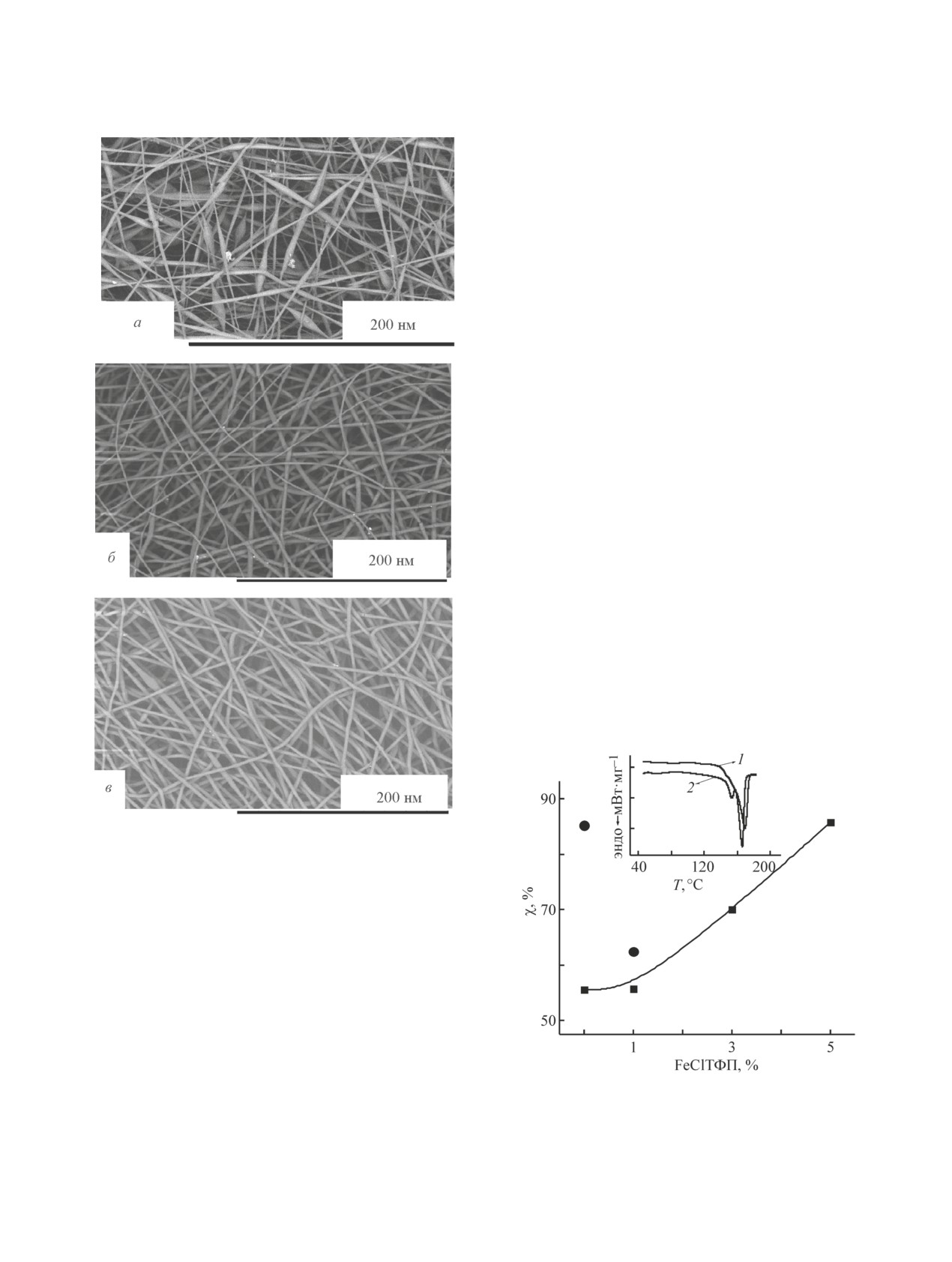
Как показано на рис. 3, добавление в раствор ПГБ
ционные центры в супрамолекулярных комплексах
комплекса FeClТФП приводит к существенному из-
FeClТФП вследствие наличия координационно свя-
менению морфологии волокна. У исходного волок-
занных ионов железа, обладающих ярко выраженны-
на ПГБ (рис. 3, а) наблюдается чередование цилин-
ми парамагнитными свойствами, можно достаточно
дрических и веретенообразных участков. Наличие
уверенно регистрировать методом электронного маг-
утолщений в структуре волокна может объясняться
нитного резонанса (ЭМР). По числу парамагнитных
низкими значениями электропроводимости и поверх-
центров можно судить о сравнительном количестве
ностного натяжения полимерного формовочного рас-
супрамолекулярных комплексов и степени их локаль-
твора [21]. Средний диаметр цилиндрических участ-
ной агломерации в образцах.
ков волокна составляет 1-6 мкм, а веретеноподобные
С ростом содержания комплексов FeClТФП в во-
элементы имеют максимальный диаметр ~10 мкм и
локнах ПГБ интенсивность и площадь спектров ЭПР
протяженность 20-30 мкм.
470
Ольхов А. А. и др.
мости вытягивание капли раствора в поле действия
электростатической силы происходит более интен-
сивно, что влечет за собой выравнивание волокон по
толщине.
Наряду с изменением геометрии ультратонких
волокон ПГБ при введении FeClТФП следует ожидать
и изменения структурно-динамических параметров
кристаллической и аморфной фаз. При добавлении
в раствор слабополярного ПГБ полярных молекул
FeClТФП может происходить взаимодействие между
ними за счет сил молекулярного притяжения [22-24].
При этом в процессе формирования волокна изменят-
ся скорости процессов кристаллизации, ориентации и
релаксации полимерных макроцепей [25].
Следует отметить, что концентрация порфирина
в аморфных областях полимера будет значительно
выше, чем исходно заданные значения 1, 3 и 5%, так
как этот расчет проводили на всю массу образца, а
комплексы FeClТФП находятся только в аморфной
фазе.
На рис. 4 представлены данные по изменению сте-
пени кристалличности в образцах с ростом концен-
трации FeClТФП. Видно, что доля кристаллической
фазы ПГБ резко возрастает с ростом концентрации
FeClТФП. Из полученных данных можно заключить,
что порфирин в композитах выступает в роли струк-
турного пластификатора, обеспечивающего рост сво-
бодного межмолекулярного объема в ПГБ. Это оказы-
Рис. 3. Изображения морфологии волокнистых матери-
алов ПГБ-FeClТФП.
а — ПГБ, б — ПГБ + 1% FeClТФП, в — ПГБ + 5%
FeClТФП.
При добавлении в раствор 1-5% FeClТФП вере-
теноподобные элементы в структуре волокна про-
падают полностью (рис. 3, б, в). При добавлении
1% комплекса в волокнистом материале появляются
волокна со средним диаметром 1.5, 3, 5 мкм. При
увеличении концентрации FeClТФП формируются
волокна со средним диаметром 3 мкм, а волокна с
диаметрами 1.5 и 6 мкм практически полностью ис-
Рис. 4. Зависимость степени кристалличности (ДСК) от
чезают. Исчезновение веретеноподобных структур
концентрации порфирина в волокнах ПГБ.
можно объяснить увеличением электропроводимости
Точки на рисунке — после отжига при 140°С.
формовочных растворов при введении полярных ком-
На вставке: термограммы плавления ПГБ с 3% порфирина:
плексов FeClТФП. При увеличении электропроводи-
1 — исходный образец, 2 — после отжига при 140°С.
Влияние добавки комплекса железа(III) с тетрафенилпорфирином на структуру волокон...
471
вает влияние на кристаллизацию макромолекул ПГБ
в процессе электроформования волокна.
Полимерные пленки и волокна ПГБ имеют не-
равновесную структуру, что приводит к незавершен-
ности процесса кристаллизации. Для приведения
системы в термодинамическое равновесие исполь-
зуют метод термического отжига при температурах
на 20-30° ниже температуры плавления, поэтому
мы подвергали образцы отжигу при 140°С в тече-
ние 2 ч (рис. 2, а, кривая 2) и быстро их охлаждали.
Степень кристалличности ПГБ при этом увеличи-
лась в 1.6 раза, в ПГБ с 1% порфирина в 1.1 раза, в
то время как в образцах ПГБ с 3 и 5% FeClТФП эта
величина заметно уменьшилась.
Объяснением полученных закономерностей, по
нашему мнению, может являться сильное межмолеку-
лярное взаимодействие молекул FeClТФП с концевы-
ми гидроксильными и карбонильными группами ос-
новной цепи ПГБ. При 140°С происходит частичное
плавление кристаллитов ПГБ, и частицы FeClТФП
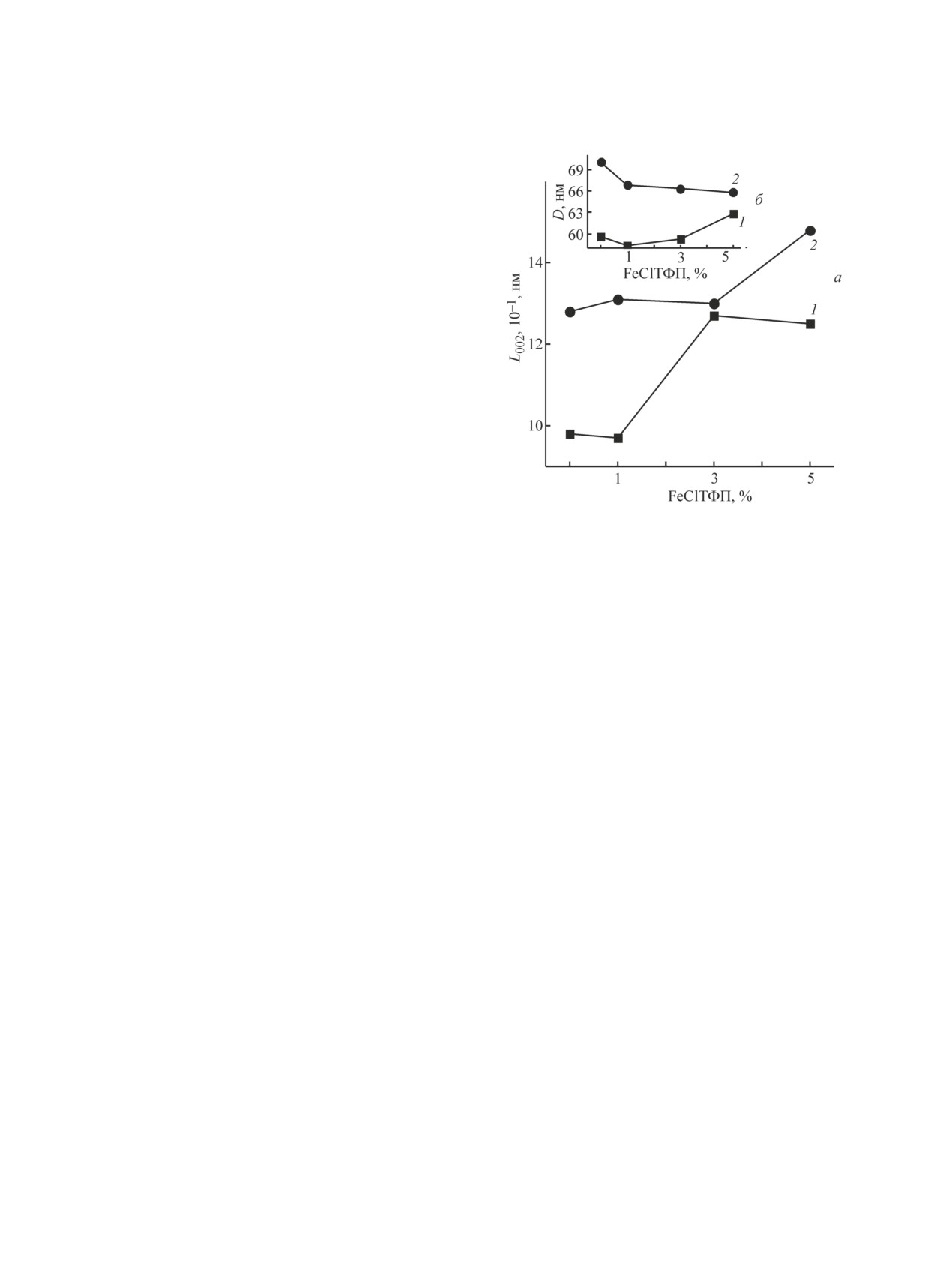
Рис. 5. Зависимость продольного размера кристаллитов
проникают в эти области. При быстром охлаждении
ПГБ (а) в волокнах от концентрации FeClТФП.
образца вследствие межмолекулярного взаимодей-
На вставке: б — зависимость большого периода в волокнах
ствия ПГБ с FeClТФП молекулы последнего остаются
ПГБ от концентрации FeClТФП: 1 — исходный образец,
2 — после отжига при 140°С.
в этих областях полимера, что препятствует процессу
кристаллизации. Степень кристалличности снижает-
ся (табл. 1). Чем выше концентрация FeClТФП, тем в
ности и размера кристаллитов после температурного
большей степени протекают процессы аморфизации
отжига при 140°С свидетельствует о неравновесном
кристаллических областей. Однако при добавлении
состоянии надмолекулярной структуры волокон. При
5% FeClTФП наблюдается повышение кристаллично-
температурном воздействии происходит достройка
сти (относительно образца ПГБ с 3% FeClТФП). По
кристаллитов [26].
нашему мнению, такие изменения обусловлены более
Кристаллиты и аморфные области в ориентиро-
низкой долей деформированных лекарственным пре-
ванном полимере в общем случае не отвечают ми-
паратом кристаллических областей по сравнению с
нимуму свободной энергии. Стремление аморф-
образцами, содержащими 3% FeClТФП (так как доля
но-кристаллической системы к минимуму свободной
аморфных областей в волокне с 5% препарата более
энергии облегчается при отжиге полимера ниже тем-
низкая, чем в волокне с 3%, и вследствие термоди-
пературы плавления, когда макромолекулы получают
намического равновесия количество FeClТФП также
достаточную подвижность. При этом аморфные обла-
характеризуется более низкими значениями).
сти стремятся релаксировать к состоянию переохлаж-
Методом рентгеновской дифракции в больших и
денного расплава, а кристаллические области стре-
малых углах проведено исследование волокон ПГБ и
мятся к минимуму свободной энергии посредством
ПГБ с FeClТФП разного состава, исходных и отож-
изменения размеров и в первую очередь продольных
женных при 140°С (рис. 5). Результаты, полученные
размеров кристаллитов. Абсолютному минимуму сво-
рентгеноструктурным анализом, свидетельствуют о
бодной энергии соответствует бесконечно большой
росте размера кристаллитов L002 при добавлении в
продольный размер кристаллита. По этой причине
волокна ПГБ порфирина. Важно отметить, что если
кристаллиты стремятся увеличить продольный раз-
степень кристалличности, определенная методом
мер и тем самым понизить свою свободную энергию.
рентгеноструктурного анализа, для ПГБ составля-
Поэтому следует ожидать увеличения периода скла-
ет 57% и возрастает с повыщением концентрации
дывания всякий раз, когда макромолекулы получают
порфирина до 67%, то по данным ДСК эта величина
достаточную подвижность, в частности, при темпера-
возрастает от 56 до 86%. Представленные данные
турном воздействии, и, как правило, кристаллический
свидетельствуют о наличии в волокнах паракристал-
полимер рекристаллизуется. Экспериментальное изу-
лических структур. Увеличение степени кристаллич-
чение роста размеров складчатых кристаллитов при
472
Ольхов А. А. и др.
Таблица 1
Термофизические параметры* волокнистых материалов ПГБ-FeClТФП
Нагрев
Охлаждение
FeClTФП, %
χ
пл,%
Тпл, °С (±1°)
χпл,%
Тпл, °С (±1°)
0
65
175
68
94
1
66
170
45
68
3
68
169
59
89
5
85
169
58
76
* χ — степень кристалличности, Тпл — температура плавления.
постоянной температуре отжига [27] показало, что
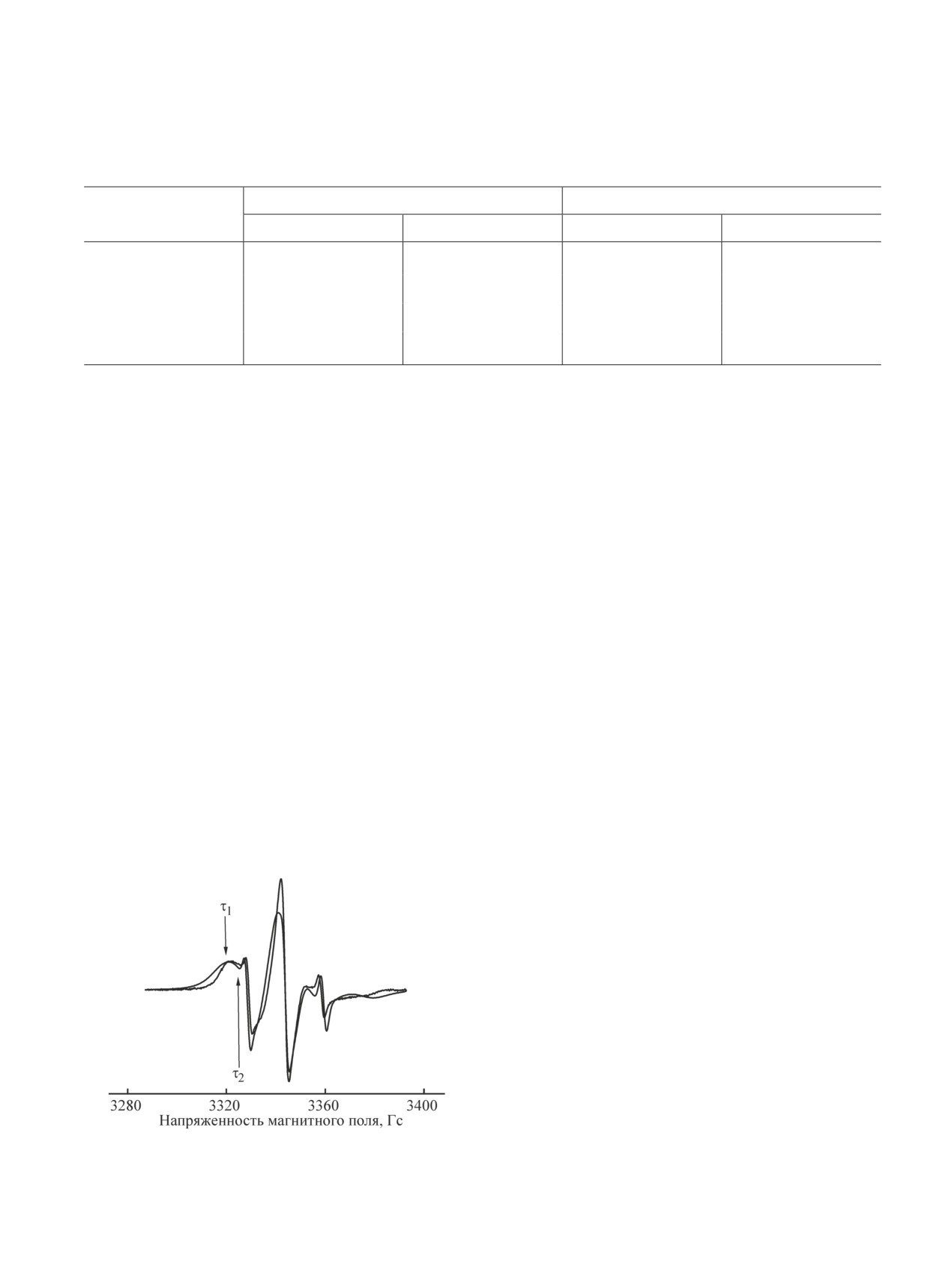
личающимися временами корреляции τ1 и τ2, где τ2
продольный размер кристаллитов L002 зависит от
характеризует молекулярную подвижность в менее
времени отжига по закону L002 = А + Вlgt, где В —
плотных, а τ1 — в более плотных аморфных областях
скорость роста размеров кристаллитов. В данной
(рис. 6).
работе образцы отжигали при 140°С в течение 2 ч.
Оценка соотношения концентраций различных по
Результаты исследований показали, что отжиг при-
плотности областей была проведена путем матема-
водит к значительному росту кристаллитов и степени
тической обработки спектров с помощью програм-
кристалличности. При отжиге происходит самопроиз-
мы NLSL (в программном пакете Bruker WinEPR
вольное распрямление и доориентация части цепей.
для спектра ЭПР) аналогично процедуре, описанной
Структура аморфных областей в значительной
ранее в работе [19]. Соответствующие расчеты по-
степени определяется долей кристаллических обра-
казали, что доля плотных областей в аморфной фазе
зований. Вследствие этого при добавлении малых
ПГБ существенно превосходит долю менее плотных,
концентраций FeClТФП растет степень кристаллич-
и с ростом концентрации FeClТФП в образце доля
ности ПГБ, изменяются размеры кристаллитов, что
плотных областей увеличивается (табл. 2). Возрастает
приводит к изменению структурного и динамическо-
и время корреляции радикала, а следовательно, мо-
го состояния аморфных областей.
лекулярная подвижность в плотных областях поли-
Молекулярную динамику этих областей наибо-
мера замедляется, в то время как в рыхлых областях
лее удобно исследовать методом ЭПР с использо-
аморфной фазы подвижность радикала практически
ванием стабильных радикалов. ЭПР-спектры ради-
не изменяется.
кала ТЕМПО в матрице ПГБ имеют сложный вид и
При использовании биомедицинских материалов
представляют собой суперпозицию двух спектров,
одновременно с механическим и температурным воз-
соответствующих двум популяциям радикалов с раз-
действием на их структуру и сегментальную подвиж-
ность оказывает влияние озон. Здесь следует указать
два источника его появления в атмосфере. Во-первых,
озон образуется при работе мощных электрических
приборов, обеспечивающих жизнедеятельность па-
циентов как в процессе хирургических операций,
так и при терапии или мониторинге в стационаре.
Во-вторых, озон в некоторых частных случаях про-
должает использоваться при стерилизации медицин-
ских изделий. Несмотря на повседневный контакт
данного агрессивного соединения с полимерами, его
влияние на их морфологические и динамические ха-
рактеристики остается малоисследованной областью
полимерного материаловедения. Ко всему прочему
воздействие озона можно использовать как струк-
Рис. 6. Спектры ЭПР нитроксильного радикала ТЕМПО
турно чувствительный метод для оценки стойкости
образца ПГБ с 3% FeClТФП.
полимерной системы к окислению.
Влияние добавки комплекса железа(III) с тетрафенилпорфирином на структуру волокон...
473
Таблица 2
Структурные характеристики аморфной фазы волокон ПГБ в зависимости от концентрации FeClТФП
Доля плотных и рыхлых областей
Время корреляции τ, 10-10 ± 5%, с
в аморфной фазе α,%
FeClТФП, %
плотная
рыхлая
плотная
рыхлая
0
70
4.0
44
66
1
73
4.3
68
32
3
104
4.3
60
40
5
110
4.3
81
19
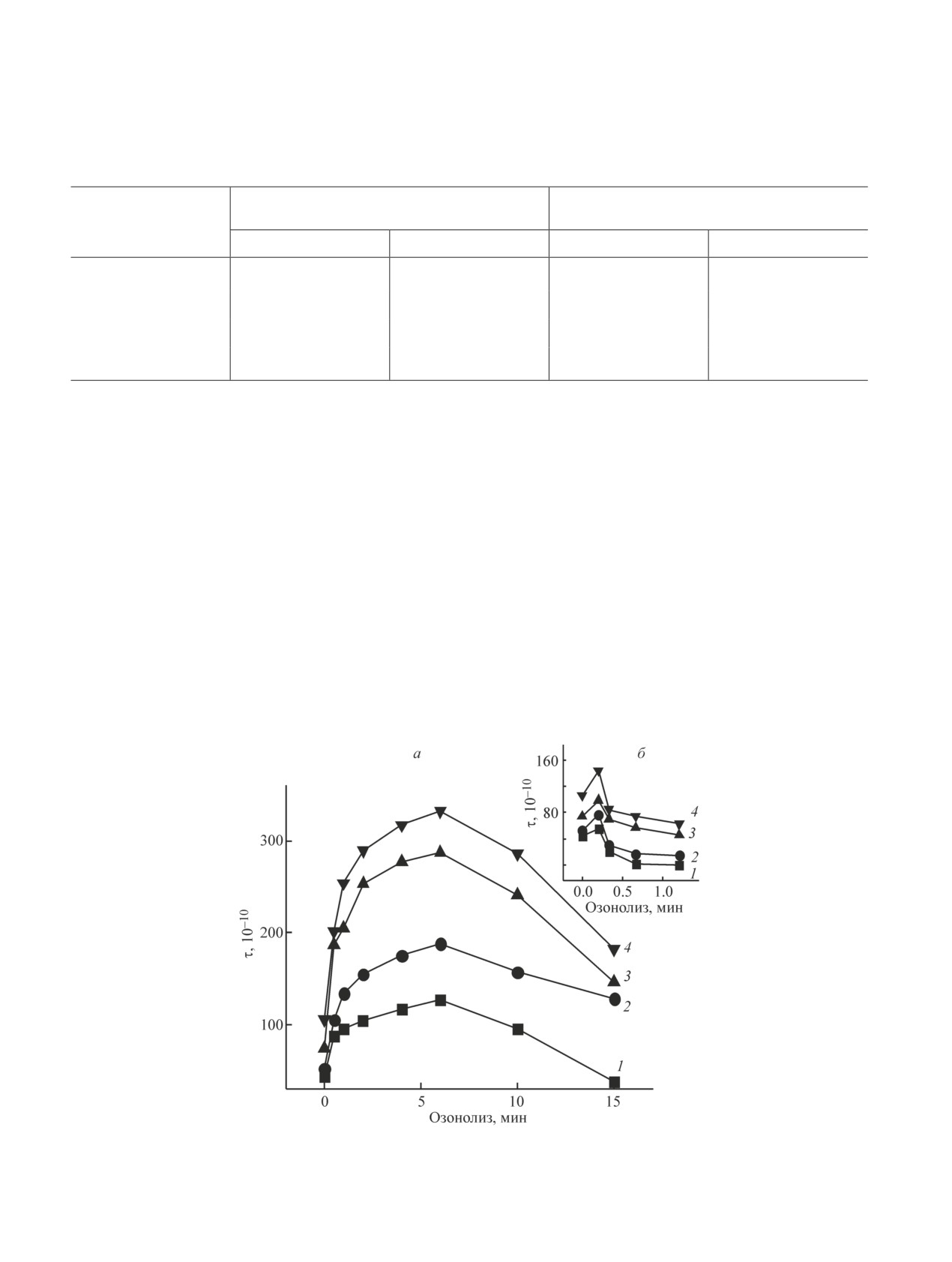
В работе изучали влияния озонного воздействия
наиболее высокой скоростью окисляются петли ма-
на смесевые композиции при двух температурах — 22
кромолекул на границе кристаллит-аморфная фаза,
и 40°С (рис. 7). Озонолиз сложным образом влияет на
так как на этих участках концентрируются наибо-
структуру полимера. С одной стороны, как показали
лее высокие напряжения и, следовательно, наиболее
результаты ранних работ [27, 28], рост жесткости
высокая скорость окисления. Разрыв этих петель
аморфных областей при небольших степенях окис-
сопровождается распрямлением сегментов, что за-
ления происходит как вследствие самопроизволь-
медляет молекулярную подвижность в этих обла-
ной доориентации цепей, а с другой — в результате
стях. Образование кислородсодержащих групп в бо-
усиления межмолекулярного взаимодействия из-за
ковых цепях макромолекул приводит к усилению
накопления полярных кислородсодержащих групп.
межмолекулярного взаимодействия, как результат,
Самопроизвольная доориентация части цепей при
молекулярная подвижность цепей также замедляет-
озонолизе ПГБ происходит по причине разрывов
ся. Поэтому, как видно из рис. 7, а, б, на начальном
перенапряженных участков цепей в местах узлов
этапе окисления замедляется подвижность зонда, а
и зацеплений макромолекул и их распрямления. С
следовательно, и молекулярная подвижность цепей.
Рис. 7. Зависимость времени корреляции от времени озонолиза волокон ПГБ-FeClТФП при 22 (а) и 40°С (б).
Концентрация FeClТФП (%): 1 — 0, 2 — 1, 3 — 3, 4 — 5.
474
Ольхов А. А. и др.
Таблица 3
Влияние содержания комплекса железо(III)порфирина на жизнеспособность культур микроорганизмов
на волокнистом материале ПГБ с FeClТФП
Количество жизнеспособных микроорганизмов, КОЕ/мл
Тест-культура
исходная тест-культура
опытный образец
контрольный образец
S. aureus р 209
2·104
1.8·103
4·103
E. coli 1257
1.6·104
менее 1·102
9·103
S. typhimurium
2.2·104
1.0·103
6·103
Чем выше степень кристалличности, тем более высо-
действия изученных нетканых волокнистых матери-
кая дисперсность кристаллитов и тем больше петель
алов ПГБ-FeClТФП при содержании комплекса 1%.
участвуют в процессе окисления, что и наблюдается
В данной работе исследования проводили на клетках
экспериментально. Одновременно происходит так-
золотистого стафилококка (Staphylococcus aureus),
же деструкция цепей в рыхлых аморфных областях,
кишечной палочки (Escherichia coli) и грибковой
что приводит к росту молекулярной подвижности и
культуры Salmonella typhimurium (S. typhimurium)
как следствие к уменьшению времени корреляции.
как наиболее распространенных микроорганизмов.
Поэтому при более длительном времени окисления
Стафилококк (Staphylococcus) распространен повсю-
(свыше 6 ч) преобладают именно такие процессы.
ду и часто входит в состав нормальной микрофло-
Аналогичные результаты были получены при озоно-
ры человека, обычно колонизирует носовые ходы,
лизе полиэтилена, полипропилена и ПГБ с полиуре-
брюшную полость и подмышечные участки. При
таном [27, 28].
повреждениях кожи и слизистых оболочек стафи-
Зависимость изменения подвижности от времени
лококки проникают в глубь организма и способ-
озонного окисления при 40°С имеет отличный от пре-
ны поражать практически любые ткани и органы.
дыдущего случая характер (рис. 7, б). Рост времени
E. coli — представитель нормальной микрофлоры
корреляции наблюдается только до 0.2 ч. Дальнейшее
кишечника человека, однако некоторые ее варианты
воздействие озона приводит к снижению молекуляр-
способны в определенных условиях вызывать много-
ной подвижности. Объяснением может служить более
численные заболевания. Дрожжеподобные грибы ви-
высокая скорость озонного окисления и деструкции во-
да S. typhimurium — одноклеточные микроорганизмы
локна. В общем случае энергетическое состояние кри-
овальной или круглой формы широко распростране-
сталлических и аморфных областей не характеризует-
ны в окружающей среде. Некоторые из них обитают
ся минимумом свободной энергии. Аморфные области
на кожных покровах и слизистых оболочках человека,
стремятся релаксировать к состоянию переохлажден-
формируя вместе с бактериями нормальные биоце-
ного расплава, а кристаллиты стремятся к минимуму
нозы. Однако при определенных неблагоприятных
свободной энергии посредством изменения размеров, и
условиях они могут вызвать у человека клинически
в первую очередь продольных размеров. Абсолютному
выраженные заболевания.
минимуму свободной энергии соответствует беско-
Результаты биологических испытаний образцов
нечно большой продольный размер кристаллитов, и
волокнистых материалов ПГБ с FeClТФП приведены
следует ожидать увеличения периода складывания
в табл. 3.
всякий раз, когда молекулы получают достаточную
Мы полагаем, что антибактериальные свойства
подвижность, в частности, при температуре отжига.
полученных комплексов FeClТФП в волокнистой
Поэтому возникающие дополнительные напряжения
матрице ПГБ связаны в первую очередь с их воздей-
на выпрямленных участках молекул при повышенных
ствием на клеточные стенки микроорганизмов путем
температурах, в частности при 40°С, обусловлива-
изменения заряда бактериальной клетки. Как след-
ют более высокую скорость окисления. В результате
ствие этого комплексы способны подавлять функ-
процессы деструкции преобладают над процесса-
цию адгезии и колонизации болезнетворных микро-
ми сшивок уже на более ранних стадиях окисления.
организмов. По-видимому, комплексы FeClТФП в
В заключительной части исследований была сде-
составе микрофибриллярных матриц ПГБ способны
лана проверка эффективности антибактериального
нарушать ионный баланс живой клетки.
Влияние добавки комплекса железа(III) с тетрафенилпорфирином на структуру волокон...
475
Порфириновые молекулы проявляют биологи-
содержащих групп. При более глубоком окислении
ческие и каталитические функции только в составе
подвижность радикала возрастает, что объясняется
металлокомплексов. Эти функции определяются ко-
их интенсивной деструкцией.
ординационными (донорно-акцепторными, комплек-
Взаимное влияние кристаллических и аморфных
сообразующими) свойствами молекулы порфирина
областей в биоразлагаемых высококристаллических
и соли металла. Поскольку между тетрапиррольным
полимерах и их композициях остается достаточно
макрогетероциклом и ионом металла в молекуле ме-
сложной, малоизученной проблемой современного
таллопорфирина (см. вставку на рис. 1, а) существует
полимерного материаловедения. Исследования состо-
сильное взаимодействие, можно говорить о коорди-
яния полимерной матрицы и роль металлокомплексов
национных свойствах FeClТФП [29].
порфиринов впервые позволили интерпретировать на
Из данных, приведенных в табл. 3, видно, что в
молекулярном уровне воздействие ряда агрессивных
эксперименте на волокнистом материале, импрегни-
факторов (таких как температура и озон) на струк-
рованном FeClТФП, количество жизнеспособных ми-
турно-динамические характеристики волокон смесей
кробных клеток после экспозиции 30 мин снизилось
поли(3-гидроксибутирата)-порфирин.
для золотистого стафилококка в 2.2 раза, E. coli не
Полученные данные свидетельствуют о перспек-
менее чем в 90 раз, для S. typhimurium в 6 раз.
тивности использования импрегнированных желе-
Полученные данные свидетельствуют о перспек-
зо(III)порфирином нетканых материалов в санитар-
тивности использования импрегнированных желе-
но-гигиенических целях и при лечении различных
зо(III)порфирином нетканых материалов в санитар-
ран и ожогов.
но-гигиенических целях и при лечении различных
ран и ожогов.
Благодарности
В работе использовали приборы Центра коллек-
Выводы
тивного пользования Института биохимической фи-
В настоящем исследовании на основе струк-
зики РАН «Новые материалы и технологии». Авторы
турно-динамического подхода, сочетая методы
выражают благодарность проф. U. J. Haenggi (Bio-
СЭМ, ЭМР (в том числе ЭПР спиновых зондов),
mer®, Krailling, Germany) за предоставленный по-
УФ-спектроскопии, ДСК и рентгеноструктурный ана-
ли(3-гидроксибутират). Авторы благодарят сотрудни-
лиз, мы представили результаты влияния комплексов
ков Института химической физики им. Н. Н. Семенова
FeClТФП на кристаллическую фазу и сегментальную
за проведение спектральных измерений (тема
подвижность молекул поли(3-гидроксибутирата) в
№ АААА-А18-118020890097-1) и калориметрических
аморфных областях ультратонких волокон. Введение
исследований (тема № АААА-А17-117040610309-0).
малых концентраций порфирина (1-5%) приводит к
значительному увеличению размера кристаллитов
Конфликт интересов
и степени кристалличности поли(3-гидроксибути-
рата). Как отклик на изменение кристаллической
Авторы заявляют об отсутствии конфликта инте-
фазы было зарегистрировано изменение динамики
ресов, требующего раскрытия в данной статье.
вращения зонда в аморфных областях. Причиной
этого является межмолекулярное взаимодействие
Информация об авторах
компонентов, обусловленное силами Ван-дер-Ваальса
либо водородными связями между молекулами ком-
Голощапов Александр Николаевич, к.б.н., помощ-
плексов и функциональными группами поли(3-
гидроксибутирата). Отжиг волокон приводит к рез-
org/0000-0003-1751-0034
кому увеличению кристаллической фазы в волокнах
Артюх Анастасия Александровна, с.н.с. ИБХФ
поли(3-гидроксибутирата), что свидетельствует о
неравновесном состоянии надмолекулярной струк-
Бычкова Анна Владимировна, к.х.н., науч. сотр.,
туры волокон.
Озонное воздействие на начальном этапе (до 6 ч)
SPIN-код: 2180-2705, ID: 603454; WoS Researcher ID:
на волокна изучаемой смеси показало резкий рост
K-1231-2015; Scopus ID: 35096067800
времени корреляции, что объясняется ростом доли
Ольхов Анатолий Александрович, к.т.н., в.н.с. РЭУ
выпрямленных цепей и усилением межмолекулярно-
им. Г. В. Плеханова, с.н.с. ИХФ РАН, ORCID: https://
го взаимодействия вследствие накопления кислород-
orcid.org/ 0000-0003-0615-6914
476
Ольхов А. А. и др.
Иорданский Алексей Леонидович, д.х.н., г.н.с. ИХФ
[14]
Митасова Ю. В., Кузнецов Р. Е., Баланцева Е. В.,
Агеева Т. А., Койфман О. И. // Изв. вузов. Химия и
Лобанов Антон Валерьевич, д.х.н., зав. лаб. ИХФ
хим. технология. 2008. Т. 51. Вып. 1. С. 74-77.
[15]
Valkova, L., Borovkov N., Koifman O., Kutepov A.,
Berzina T., Fontana M., Rella R., Valli L. // Biosensors
Карпова Светлана Геннадьевна, к.ф.-м.н., с.н.с.
and Bioelectronics. 2004. V. 20. P. 1177-1184.
[16]
Yео L. Y., Friend J. R. // J. Experimental Nanosci.
5843; Scopus ID: 16218970000
2006. V. 1. N 2. Р. 177-209.
[17]
Тимофеев В. П., Мишарин А. Ю., Ткачев Я. В. //
Биофизика. 2011. Т. 56. № 3. С. 420-432 [Timofe-
Список литературы
ev V. P., Tkachev Y. V., Misharin A. Y. // Biophysics.
[1] Бойко А. В., Олтаржевская Н. Д., Щвец В. И.,
2011. V. 56. N 3. P. 407-417].
Демидова Л. В., Дунаева Е. А., Дубовецкая О. Б.,
[18]
Карпова С. Г., Ольхов А. А., Шилкина Н. Г., По-
Мельникова В. Ю., Ерастова Е. И., Кожевнико-
пов А. А., Филатова А. Г., Кучеренко Е. Л.,
ва С. А. // Патологическая физиология и эксперим.
Иорданский А. Л. // Высокомолекуляр. соединения.
терапия. 2018. Т. 62. № 3. С. 120-127.
2017. T. 59А. № 1. C. 53-62 [Karpova S. G., Po-
[2] Корытова Л. И., Сокуренко В. П., Маслюкова Е. А.,
pov A. A., Ol′khov A. A., Shilkina N. G., Filatova A. G.,
Мешечкин А. В., Олтаржевская Н. Д., Корови-
Kucherenko E. L., Iordanskii A. L. // Polym. Sci.
на М. А., Гусев И. В., Кузнецов А. Д., Красни-
Ser. A. 2017. V. 59. N 1. P. 58-66].
кова В. Г., Обухов Е. М. // Рос. биотерапевт. журн.
[19]
Бычкова А. В., Иорданский А. Л., Коварский А. Л.,
2015. Т. 14. № 4. С. 99-103.
Сорокина О. Н., Косенко Р. Ю., Маркин В. С., Фи-
[3] Прокопчук Н. Р., Шашок Ж. С., Прищепенко Д. В. //
латова А. Г., Гумаргалиева К. З., Роговина С. З.,
Полимер. материалы и технологии. 2015. Т. 1. № 2.
Берлин А. А. // Рос. нанотехнологии. 2015. Т. 10.
С. 36-56.
№ 3-4. С. 132-139.
[4] Голубчиков О. А., Пуховская С. Г., Кувшинова Е. М.
[20]
Чегерев М. Г., Пискунов А. В., Старикова А. А.
// Успехи химии. 2005. Вып. 3. С. 268-284.
// ЖОХ. 2017. Т. 87. № 11. С. 1841-1848 [Chege-
[5] Никитина Н. И., Потапов Г. П. // Химия раст. сы-
rev M. G., Piskunov A. V., Starikova A. A. // Russ. J.
рья. 2002. № 2. С. 79-84.
Gen. Chem. 2017. V. 87. N 11. P. 2582-2588].
[6] Лобанов А. В., Неврова О. В., Илатовский В. А.,
[21]
Ramakrishna S, Fujihara K., Teo W., Lim T.-C., Ma Z.
Синько Г. В., Комиссаров Г. Г. // Макрогетероциклы.
An Introduction to Electrospinning and Nanofibers.
2011. Т. 4. № 2. С. 132-134.
Singapoor: World Scientific Publ. Co. Pte. Ltd, 2005.
[7] Курмаз С. В., Перепелицина Е. О. // Изв. АН. Сер.
396 p.
хим. 2006. № 5. С. 807-816.
[22]
Карпова С. Г., Ольхов А. А., Иорданский А. Л.,
[8] Помогайло Д. А., Уфлянд И. Е. Макромолекулярные
Ломакин С. М., Шилкина Н. С., Попов А. А., Гумар-
металлохелаты. М.: Химия, 1991. 304 с.
галиева К. З., Берлин А. А. // Высокомолекуляр. сое-
[9] Титов В. А., Кривых Е. С., Агеева Т. А., Шико-
динения. 2016. Т. 58A. № 1. С. 61-72 [Karpova S. G.,
ва Т. Г., Соловьева А. Б., Тимофеева В. А., Вер-
Ol′khov A. A., Iordanskii A. L., Lomakin S. M., Shilki-
шинина И. А., Рыбкин В. В., Choi H. S. // Высоко-
na N. G., Popov A. A., Gumargalieva K. Z., Ber-
молекуляр. соединения. 2008. Т. 50А. № 8.
lin A. A. // Polym. Sci. Ser. A. 2016. V. 58. N 1. P. 76-
С. 1454-1462 [Titov V. A., Ageeva T. A., Shikova T. G.,
86].
Rybkin V. V., Krivykh E. S., Vershinina I. A.,
[23]
Ольхов А. А., Маркин В. С., Косенко Р. Ю., Гольд-
Solov′eva A. B., Timofeeva V. A., Choi H. S. // Polym.
штрах М. А., Иорданский А. Л. // ЖПХ. 2015. Т. 88.
Sci. Ser. A. 2008. V. 50. N 8. P. 841-847].
№ 2. С. 307-312 [Olkhov A. A., Markin V. S., Kosen-
[10] Исламова Р. М., Насретдинова Р. Н., Агеева Т. А.
ko R.Yu., Gol′dshtrakh M. A., Iordanskii A. L. // Russ.
Успехи химии порфиринов. СПб: Изд-во НИИ
J. Appl. Chem. 2015. V. 88. N 2. P. 308-313].
Химии, 2007. Т. 5. 323 c.
[24]
Wang Z., Sun B., Zhang M. // J. Bioactive Compat.
[11] Гришин Д. Ф., Семенычева Л. Л., Колякина Е. В. //
Polym. 2013. V. 28. P. 154-166.
ЖПХ. 2001. Т. 74. № 3. С. 483-486.
[25]
Ol′khov A. A., Iordanskii A. L, Staroverova O. V.,
[12] Помогайло Д. А. Полимерные иммобилизованные
Gumargalieva K. Z., Sklyanchuk E. D., Gur′ev V. V.,
металлокомплексные катализаторы. М.: Наука,
Abbasov T. A., Ishchenko A. A., Rogovina S. Z., Ber-
1988. 303 с.
lin A. A. // Fibre Chem. 2016. V. 47. N 5. Р. 348-361.
[13] Мамардашвили Г. М., Симонова О. Р., Чижо-
[26]
Иорданский А. Л., Ольхов А. А., Карпова С. Г.,
ва Н. В., Мамардашвили Н. Ж. // ЖОХ. 2018. Т. 88.
Кучеренко Е. Л., Косенко Р. Ю., Роговина С. З.,
№ 6. С. 974-983 [Mamardashvili G. M., Simono-
Чалых А. Е., Берлин А. А. // Высокомолекуляр.
va O. R., Chizhova N. V., Mamardashvili N. Z. // Russ.
соединения. 2017. T. 59А. № 3. C. 273-284
J. Gen. Chem. 2018. V. 88. N 6. P. 1154-1163].
[Iordanskii A. L., Ol′khov A. A., Karpova S. G.,
Влияние добавки комплекса железа(III) с тетрафенилпорфирином на структуру волокон...
477
Kucherenko E. L., Kosenko R. Yu., Rogovina S. Z.,
лун С. Н., Берлин А. А. // Хим. физика. 2012. Т. 31.
Chalykh A. E., Berlin A. A. // Polym. Sci. Ser. A. 2017.
№ 1. С. 79-87 [Karpova S. G., Popov A. A., Shilki-
V. 59. N 3. Р. 343-353].
na N. G., Lomakin S. M., Iordanskii A. L., Berlin A. A.,
[27] Карпова С. Г., Попов А. А., Заиков Г. Е. //
Chvalun S. N., Shcherbin M. A. // Russ. J. Phys. Chem.
Высокомолекуляр. соединения. 1991. Т. 33. № 5.
B. 2012. V. 6. N 1. P. 72-80].
С. 931-949.
[29] Березин Б. Д. Координационные соединения
[28] Карпова С. Г., Иорданский А. Л., Попов А. А., Шил-
порфиринов и фталоцианина. М.: Наука, 1978.
кина Н. Г., Ломакин С. М., Щербин М. А., Чва-
280 с.