Каталитическая активность полифункциональных ионных жидкостей в окислении модельных сульфидов
531
Журнал прикладной химии. 2019. Т. 92. Вып. 4
УДК 542.943.6
КАТАЛИТИЧЕСКАЯ АКТИВНОСТЬ ПОЛИФУНКЦИОНАЛЬНЫХ
ИОННЫХ ЖИДКОСТЕЙ В ОКИСЛЕНИИ МОДЕЛЬНЫХ СУЛЬФИДОВ
© А. В. Акопян, Е. А. Есева, П. Д. Поликарпова,
Т. М. Байгильдиев, И. А. Родин, А. В. Анисимов
Московский государственный университет им. М. В. Ломоносова
E-mail: arvchem@yandex.ru
Поступила в Редакцию 8 октября 2018 г.
После доработки 14 декабря 2018 г.
Принята к публикации 28 января 2019 г.
Синтезированы ионные жидкости на основе 1-метилимидазола, содержащие бренстедовские
кислотные центры в катионе, а также атом переходного металла в анионе. Синтезированные
полифункциональные ионные жидкости являются эффективными катализаторами процесса окис-
лительного обессеривания. Подобраны условия для достижения 100%-ной конверсии метилфенил-
сульфида в мягких условиях в присутствии полученных катализаторов — ионных жидкостей [ионная
жидкость — 3-(карбоксиметил)-1-метил-1Н-имидазол-3-ий молибдат, S:Мо = 24:1 (мол.), 2 ч, 40°С,
Н2О2:S = 12:1 (мол.)].
Ключевые слова: ионные жидкости; окислительное обессеривание; 1-метилимидазол; пероксоком-
плексы; молибден; пероксид водорода
DOI: 10.1134/S0044461819040145
В связи с введением жестких экологических тре-
водорода как экологически безопасного растворителя,
бований к топливам увеличивается потребность в
продуктом его восстановления является вода.
поиске новых решений по очистке нефтяных фракций
Наиболее распространенные каталитические си-
от сернистых соединений [1, 2]. Наиболее распро-
стемы для окислительного обессеривания содержат в
страненный метод обессеривания — гидроочистка
своем составе соединения переходных металлов, та-
требует высоких капитальных и энергетических за-
ких как молибден, вольфрам или ванадий, способных
трат при его внедрении, а рост содержания серы в
образовывать пероксокомплексы в присутствии пе-
углеводородном сырье ведет к ужесточению условий
роксида водорода или алкилпероксидов [4-9]. Однако
проведения этого процесса, что требует совершен-
использование таких систем сопряжено с фазовыми
ствования имеющихся катализаторов и увеличения
ограничениями, поскольку сернистые соединения
размеров реакторов [3]. В связи с удорожанием про-
находятся в органической фазе, а катализатор и окис-
цесса гидроочистки все более широкое распростране-
литель — в водной. Уменьшить это ограничение по-
ние получают безводородные методы обессеривания,
зволяет использование ионных жидкостей (ИЖ), ко-
наиболее перспективным из которых является окис-
торые могут выступать как межфазные переносчики
лительное обессеривание [4, 5]. Метод основан на
в процессе окисления [10-12].
окислении сераорганических соединений с последу-
В литературе широко описано применение
ющим их извлечением полярным растворителем или
бренстедовских кислот в качестве катализаторов
адсорбентом из углеводородной среды [6]. Одно из
окисления сернистых соединений (неорганиче-
основных преимуществ окислительного обессерива-
ские — серная, фосфорная кислоты, органические —
ния — мягкие условия проведения окисления (темпе-
муравьиная, уксусная, трифторуксусная и т. д.)
ратуры до 80°С и атмосферное давление). В качестве
[13-15]. Известны примеры использования ионных
окислителя перспективно использование пероксида
жидкостей с бренстедовскими кислотными центра-
532
Акопян А. В. и др.
ми в качестве катализаторов окисления сернистых
воде и ацетонитрил. Образец вводили при помощи
соединений [16-18], однако такие системы уступают
автосемплера через соединитель нулевого объема
по эффективности катализаторам на основе солей
напрямую в масс-спектрометр. Скорость потока под-
молибдена или вольфрама [19-21]. В данной работе
вижной фазы 0.3 мл·мин-1. Масс-спектрометрическое
были использованы полифункциональные ионные
детектирование проводили в режиме сканирования в
жидкости, состоящие из катиона имидазолия с кар-
интервале m/z 80-500 Да. Масс-спектры ионов-про-
боксильной группой и аниона, содержащего молиб-
дуктов получали в интервале 50-143 Да. Пробы го-
ден, вольфрам или ванадий. Важным преимуществом
товили в деионизированной воде, массовая доля ве-
такого подхода является сочетание в одном катализа-
щества 2%.
торе высокой каталитической активности, присущей
Исследование элементного состава проводили
соединениям переходных металлов и кислотам, с
методом рентгеноспектрального флуоресцентного
функциями межфазного переносчика.
анализа (РСФА) с использованием рентгенофлуо-
ресцентного волнового спектрометра ARL Perform′X
(Thermo Fisher Scientific, New Wave).
Экспериментальная часть
Пробоподготовку проводили по следующей ме-
Для синтеза ионных жидкостей использовали
тодике: порошкообразные пробы прессовали в та-
хлоруксусную кислоту (97.6%, РусХим), этиловый
блетки на подложке из борной кислоты и накрывали
спирт (96%), 1-метилимидазол (99%, Lanster), серную
лавсановой пленкой, которую прижимали оправой
кислоту (95%, Компонент-Реактив), соляную кислоту
в виде кольца к кювете. Жидкие пробы помещали в
(37%, Сигма-Тэк).
кювету, накрывали лавсановой пленкой и прижимали
Модельная смесь состояла из метилфенилсуль-
ее оправой.
фида (MeSPh, 99%, Acros Organics), растворенного в
Состав продуктов реакции и контроль чистоты
додекане (99%, Sigma-Aldrich). Исходное содержание
исходных веществ осуществляли методом газовой
общей серы в смеси — 1000 ppm. Аналогично гото-
хроматографии на хроматографе Кристалл-2000М с
вили смеси дибензилсульфида (Bn2S, 98%, Sigma-
пламенно-ионизационным детектором, колонка —
Aldrich), бензотиофена (БТ, 98%, Sigma-Aldrich) и
Zebron, L = 30 м, d = 0.32 мм, жидкая фаза ZB-1, при
дибензотиофена (ДБТ, 98%, Sigma-Aldrich).
программировании температуры от 100 до 250°С.
Для синтеза окислительно-каталитических сме-
Хроматограммы записывали и анализировали на
сей использовали: молибдат натрия (Na2MoO4·2H2O,
компьютере с использованием программы Хроматэк
99%, Sigma-Aldrich), вольфрамат натрия (Na2WO4×
Аналитик 1.5.
×2H2O, 99%, Sigma-Aldrich), ванадат натрия (NaVO3,
Условия проведения анализа реакционной смеси
99%, Sigma-Aldrich), пероксид водорода (Н2О2, 50%,
до и после окисления:
Prime Chemicals Group), трет-бутилгидропероксид
— газ-носитель — азот (p = 200 кПа), объемная
(t-BuOOH, 70%, ABCR), три(пентафтороэтил)трифто-
скорость потока 30 мл·мин-1;
рофосфат 1-бутил-3-метилимидазолия (99%, Merck).
— начальная температура колонки 100°С;
Спектры ЯМР 1Н регистрировали на спектро-
— температура инжектора 150°С;
метре Varian-ХR-400 с рабочей частотой 400 МГц.
— температура детектора 250°С;
Использовали 2%-ные растворы образцов в дей-
— скорость нагрева колонки 20 град·мин-1.
терированной воде или дейтерированном диме-
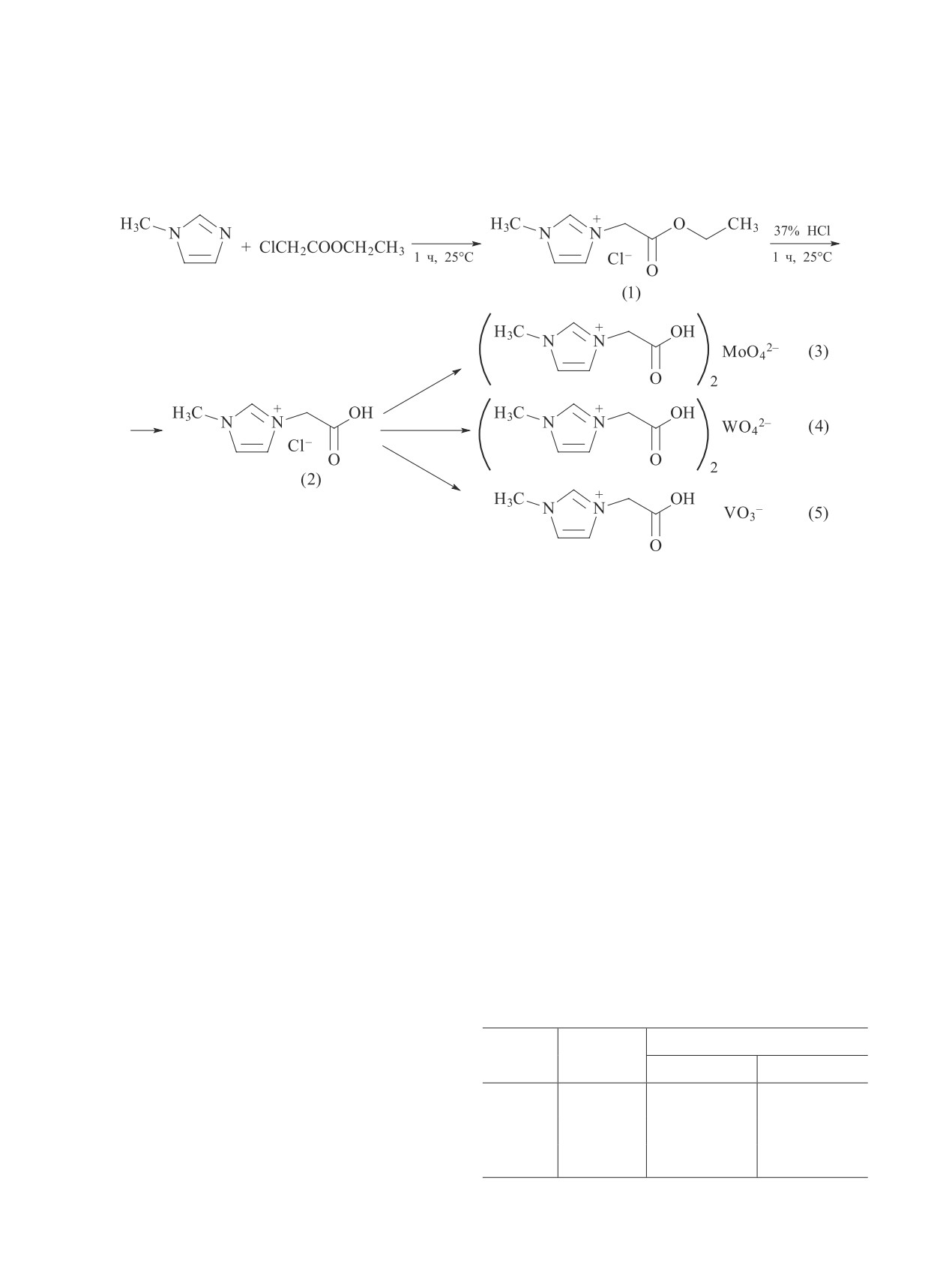
Синтез ионных жидкостей. Ионные жидкости
тилсульфоксиде. Химические сдвиги приведены в
(3)-(5), используемые в данной работе в качестве ка-
миллионных долях по шкале относительно гексаме-
тализаторов окисления сернистых соединений, были
тилдисилоксана как внутреннего стандарта.
синтезированы на схеме 1.
Строение полученных соединений подтверждали
Синтез 3-(2-этокси-2-оксоэтил)-1-метил-1Н-ими-
методами спектроскопии ЯМР 1Н, масс-спектроме-
дазол-3-ий хлорида (ИЖ-1). Реакцию кватернизации
трии ESI-MS, а также методом элементного анализа.
проводили по методике [22]. Продукт анализировали
Спектры ESI-МS были зарегистрированы на жидкост-
методами ЯМР и ESI-MS. Спектр ЯМР 1Н (DMSO,
ном хроматографе Dionex Ultimate 3000 c тандемным
400 МГц), δ: 1.20-1.23 м (3Н), 3.85-3.92 с (3Н), 4.15-
квадрупольным масс-спектрометрометрическим де-
4.20 м (2Н), 5.38 с (2Н), 7.82-7.84 м (2Н), 9.41 с (1Н).
тектором AB Sciex 3200 Qtrap при ионизации пробы
ESI-MS: m/z = 169.
электрораспылением (ЕSI) в режиме регистрации
Синтез 3-(карбоксиметил)-1-метил-1Н-имида-
положительных ионов. В качестве подвижной фа-
зол-3-ий хлорида (ИЖ-2). Продукт реакции кватерни-
зы использовали смесь 0.1% муравьиной кислоты в
зации подвергали гидролизу в присутствии избытка
Каталитическая активность полифункциональных ионных жидкостей в окислении модельных сульфидов
533
Схема 1
Схема синтеза ионных жидкостей, содержащих бренстедовские кислотные центры в катионе и атом
переходного металла в анионе
37%-ного водного раствора соляной кислоты [22].
продолжали в течение 5 мин до полного растворения
Продукт анализировали методами ЯМР и ESI-MS.
ионной жидкости.
Спектр ЯМР 1Н (DMSO, 400 МГц); δ: 3.90 с (3Н),
Окисление модельных смесей сераорганических
5.16 с (2Н), 7.74-7.76 д (2Н), 9.26 с (1Н). ESI-MS:
соединений. Реакцию окисления модельных смесей
m/z = 141.
(схема 2) проводили следующим образом: к 5 мл
Реакции обмена 3-(карбоксиметил)-1-метил-
раствора сераорганического соединения, содержа-
1Н-имидазол-3-ий хлорида (ИЖ-2) с солями пере-
щего 1000 ppm общей серы, добавляли 0.02-0.08 мл
ходных металлов с получением ИЖ-3-ИЖ-5. ИЖ-2
каталитической окислительной смеси, состоящей
(0.5 г) растворяли в 5 мл дистиллированной воды,
из пероксида водорода или трет-бутилгидроперок-
полученный раствор добавляли по каплям к 10 мл
сида и ионной жидкости (ИЖ-2-ИЖ-5) в мольном
водного раствора молибдата натрия (количество мо-
соотношении металл:пероксид водорода от 1:600
либдата натрия рассчитывали исходя из мольного
до 1:48. Реакцию проводили при постоянном пере-
соотношения ИЖ-2:молибдат натрия, равного 2:1).
мешивании при 20-80°С в течение 0.5-6 ч. Состав
Образовавшийся осадок белого цвета отделяли, про-
реакционной смеси по окончании реакции анализи-
мывали водой до полного удаления хлорида натрия,
ровали методом газовой хроматографии. Продуктами
наличие которого проверяли качественной реакцией
окисления в каждом случае являются соответствую-
на хлорид-ионы с использованием нитрата серебра, и
щие сульфоны.
сушили при комнатной температуре в течение 1 сут.
Аналогично проводили анионный обмен с вольфра-
матом и ванадатом натрия (в случае с ванадатом на-
Содержание металлов в синтезированных
трия мольное соотношение ИЖ-2:ванадат натрия
ионных жидкостях по данным элементного анализа
было равно 1:1). Синтезированные соединения ана-
Количество металла, мас%
лизировали методами РСФА (см. таблицу ) и ESI-MS.
Ионная
Металл
жидкость
По данным ESI-MS: m/z = 141.
рассчитанное
фактическое
Приготовление каталитической окислительной
ИЖ-3
Молибден
21.4
20.5
смеси. К 0.2-0.8 мл 50%-ного раствора пероксида
водорода или трет-бутилгидропероксида добавля-
ИЖ-4
Вольфрам
34.1
34.7
ли при постоянном перемешивании 0.015-0.035 г
ИЖ-5
Ванадий
13.0
12.6
ионной жидкости (ИЖ-2-ИЖ-5). Перемешивание
534
Акопян А. В. и др.
Схема 2
Реакции окисления серосодержащих соединений
Обсуждение результатов
важно отметить, что ИЖ, содержащая кислотную
функциональную группу, но в состав которой не вхо-
Для сравнения эффективности полученных ката-
дит металл, проявляет каталитическую активность,
лизаторов в идентичных условиях были проведены
обусловленную образованием надкислоты в условиях
реакции в присутствии каталитической системы, со-
окисления, что характерно для пероксидного окис-
держащей молибдат натрия и модельную ионную
ления серосодержащих соединений в присутствии
жидкость — три(пентафтороэтил)трифторофосфат
кислот [1].
1-бутил-3-метилимидазолия (IL), а также полученных
Изучение влияния температуры окисления на
ионных жидкостей с различными анионами (ИЖ-2-
конверсию метилфенилсульфида проводили в при-
ИЖ-5, схема 1). Смесь молибдата натрия и модельной
сутствии ИЖ-3, содержащей в анионе атом мо-
ионной жидкости использовали для оценки влияния
бренстедовских кислотных центров, содержащихся
в синтезированных катализаторах (ИЖ-2-ИЖ-5), на
конверсию метилфенилсульфида (MeSPh).
Как видно из рис. 1, наиболее эффективным ката-
лизатором является синтезированная в данной работе
ионная жидкость, содержащая в составе аниона атом
молибдена (ИЖ-3). Ионные жидкости с молибденом
и вольфрамом проявляют высокую активность, по-
скольку данные металлы образуют в присутствии
пероксида водорода или алкилпероксидов активные
пероксокомплексы. Из полученных данных можно
сделать вывод, что синтезированные катализаторы яв-
ляются более эффективными по сравнению с чистым
молибдатом натрия и смесью молибдата натрия с ион-
ной жидкостью (IL), что свидетельствует об участии
катионной части, содержащей карбоксильную группу,
в процессе окисления.
Таким образом, полученные результаты свидетель-
ствуют об эффективности использования полифунк-
циональных ионных жидкостей, содержащих в своем
Рис. 1. Влияние катализатора на конверсию метилфенил-
составе как кислотный центр, так и атом переходного
сульфида [Н2О2:S = 6:1 (мол.), S:металл = 24:1 (мол.),
металла. Такой подход позволяет улучшить результа-
2 ч, 40°С].
ты по сравнению с использованием ИЖ, не содержа-
IL — три(пентафтороэтил)трифторофосфат 1-бутил-3-ме-
щих бренстедовских кислотных центров. При этом
тилимидазолия.
Каталитическая активность полифункциональных ионных жидкостей в окислении модельных сульфидов
535
Рис. 2. Влияние температуры на конверсию метилфе-
нилсульфида [окислитель:общая сера = 6:1 (мол.), ката-
Рис. 4. Влияние количества катализатора на конверсию
метилфенилсульфида [Н2О2:S = 6:1 (мол.), катализа-
лизатор — ИЖ-3, S:Мо = 24:1 (мол.), 2 ч, 40°С].
тор — ИЖ-3, 2 ч, 40°С].
либдена (рис. 2). В качестве окислителей были
сти ИЖ-3 (рис. 3) при 40°С. В этих условиях полное
выбраны пероксид водорода и трет-бутилгидропе-
окисление достигается за 8 ч.
роксид в мольном соотношении окислитель:общая
Варьирование соотношения сера:молибден (и как
сера 6:1. Как видно из рис. 2, пероксид водорода
следствие соотношения сера:катализатор) показывает
является более эффективным окислителем по срав-
(рис. 4), что увеличение количества добавленного
нению с трет-бутилгидропероксидом, оптимальная
катализатора приводит к росту конверсии метил-
температура окисления составляет 60°С для перок-
фенилсульфида. Достичь мольного соотношения се-
сида водорода и 80°С — для трет-бутилгидропе-
ра:молибден ˂ 12:1 не удается в связи с ограниченной
роксида.
растворимостью катализатора в растворе пероксида
Исследование влияния продолжительности окис-
водорода.
ления на конверсию метилфенилсульфида проводили
Изучение влияния количества пероксида водорода
в присутствии пероксида водорода и ионной жидко-
на конверсию метилфенилсульфида при мольном из-
Рис. 3. Влияние времени окисления на конверсию ме-
Рис. 5. Влияние количества пероксида водорода на кон-
тилфенилсульфида [Н2О2:S = 6:1 (мол.), катализатор —
версию метилфенилсульфида [катализатор — ИЖ-3,
ИЖ-3, S:Мо = 24:1 (мол.), 40°С].
S:Мо = 24:1 (мол.), 2 ч, 40°С].
536
Акопян А. В. и др.
зол-3-ий молибдат, мольное соотношение пероксид
водорода:сера = 12:1, мольное соотношение сера:-
молибден = 24:1, 2 ч, 40°С]. Показана более высокая
эффективность использования полифункциональных
катализаторов на основе ионных жидкостей, содержа-
щих в катионе бренстедовский кислотный центр, для
окисления сераорганических соединений по сравне-
нию с использованием простой смеси ионной жидко-
сти с солью переходного металла.
Финансирование работы
Исследование выполнено за счет гранта Россий-
ского научного фонда (проект № 18-79-00116).
Конфликт интересов
Авторы заявляют об отсутствии конфликта инте-
Рис. 6. Окисление различных сераорганических со-
ресов, требующего раскрытия в данной статье.
единений [Н2О2:S = 6:1 (мол.), катализатор — ИЖ-3,
S:Мо = 24:1 (мол.), Н2О2:S = 6:1 (мол.), 2 ч, 60°С].
Информация об авторах
бытке пероксида водорода по отношению к сульфиду
от 2 до 12 (рис. 5) показало, что 12-кратный избыток
org/0000-0001-6386-0006
пероксида водорода позволяет полностью окислить
метилфенилсульфид до соответствующего сульфона.
org/0000-0001-7538-9012
Было проведено сравнительное исследование
Поликарпова Полина Димитровна, ORCID: https://
окисления серосодержащих соединений в присут-
orcid.org/0000-0002-0456-8248
ствии ИЖ-3 (рис. 6). Как видно из представленных
Байгильдиев Тимур Муратович, ORCID: https://
данных, метилфенилсульфид и дибензилсульфид
orcid.org/0000-0003-2351-8403
окисляются практически полностью, а дибензотио-
фен в данных условиях — на 30%, хуже всего окисля-
org/0000-0002-0588-6870
ется бензотиофен, что коррелирует с литературными
Анисимов Александр Владимирович, ORCID:
данными по снижению активности сернистых соеди-
нений в ряду сульфид > дибензотиофен > тиофен [23].
Список литературы
Выводы
[1] Акопян А. В., Федоров Р. А., Андреев Б. В., Тара-
Синтезированы ионные жидкости, имеющие кис-
канова А. В., Анисимов А. В., Караханов Э. А. //
лотные центры в катионе имидазолия, а также содер-
ЖПХ. 2018. Т. 91. № 4. С. 457-471 [Akopyan A. V.,
жащие в анионе атомы молибдена, вольфрама или ва-
Fedorov R. A., Andreev B. V., Tarakanova A. V., Ani-
надия, и исследована их каталитическая активность в
simov A. V., Karakhanov E. A. // Russ. J. Appl. Chem.
2018. V. 91. N 4. P. 529-542].
окислении сераорганических соединений. Показано,
[2] Ma X., Sun L., Song C. // Catal. Today. 2002. V. 77.
что наибольшую каталитическую активность про-
N 1-2. P. 107-116.
являет ионная жидкость, содержащая в своем со-
[3] Bhutto A. W., Abro R., Gao S. R., Abbas T., Chen X. C.,
ставе атом молибдена. Изучено влияние продолжи-
Yu G. R. // J. Taiwan Institute Chem. Eng. 2016. V. 62.
тельности реакции, количества ионной жидкости
P. 84-97.
и окислителя на конверсию метилфенилсульфида.
[4] Ismagilov Z., Yashnik S., Kerzhentsev M., Parmon V.,
Подобраны условия для достижения 100%-ной кон-
Bourane A. // Catal. Rev. — Sci. Eng. 2011. V. 53. N 3.
версии метилфенилсульфида в мягких условиях в
P. 199-255.
присутствии полученных ионных жидкостей [ионная
[5] Акопян А. В., Григорьев Д. А., Поликарпова П. Д.,
жидкость — 3-(карбоксиметил)-1-метил-1Н-имида-
Есева Е. А., Литвинова В. В., Анисимов А. В. //
Каталитическая активность полифункциональных ионных жидкостей в окислении модельных сульфидов
537
Нефтехимия. 2017. Т. 57. № 5. С. 582-585 [Ako-
Tarakanova A. V., Rakhmanov E. V., Polyakova O. V.,
pyan A. V., Grigoriev D. A., Polikarpova P. D.,
Anisimov A. V., Vinokurov V. A., Karakhanov E. A. //
Eseva E. A., Litvinova V. V., Rakhmanov E. V.,
Petrol. Chem. 2015. V. 55. N 7. Р. 571-574].
Anisimov A. V. // Petrol. Chem. 2017. V. 57. N 10.
[14] Shang H., Zhang H. // J. Ind. Eng. Chem. 2013. V. 19.
P. 904-907].
N 5. P. 1426-1432.
[6] Babich I. V., Moulijn J. A. // Fuel. 2003. V. 82. Р. 607-
[15] Muhammad Y., Shoukat A., Rahman A. U., Ra-
631.
shid H. U., Ahmad W. // Chinese J. Chem. Eng. 2018.
[7] Rafiee E., Rezaei S. // J. Taiwan Institute Chem. Eng.
V. 26. N 3. P. 593-600.
2016. V. 61. P. 174-180.
[16] Gui J., Liu D., Sun Z., Liu D., Min D., Song B., Peng X.
[8] Conte V., Bortolini O. // J. Inorg. Biochem. 2005.
// J. Mol. Catal. A: Chemical. 2010. V. 331. P. 64-
V. 99. P. 1549-1557.
70.
[9] Kadijani J. A., Narimani E. // Petroleum & Coal. 2014.
[17] Liu D., Gui J., Song L., Zhang X., Sun Z. // Petrol. Sci.
V. 56. N 1. P. 116-123.
Technol. 2008. V. 26. P. 973-982.
[10] Li H. M., He L. N., Lu J. D., Zhu W. S., Jiang X.,
[18] Zhao D., Sun Z., Li F., Shan H. // Fuel Chem. Technol.
Wang Y., Yan Y. S. // Energy & Fuels. 2009. V. 23.
2009. V. 37. N 2. P. 194-198.
P. 1354-1357.
[19] Kulkarni P., Afonso C. // Green Chem. 2010. V. 12.
[11] Lü H., Deng C., Ren W., Yang X. // Fuel Processing
P. 1139-1149.
Technol. 2014. V. 119. P. 87-91.
[20] Zhu W., Li H., Jiang X., Yan Y., Lu J., He L., Xia J. //
[12] Xun S., Zhu W., Zheng D., Li H., Jiang W., Zhang M.,
Green Chem. 2008. V. 10. P. 641-646.
Qin Y., Zhao Z., Li H. // RSC Advances. 2015. V. 5.
[21] Zhang J., Wanga A., Li X., Ma X. // J. Catal. 2011.
P. 43528-43536.
V. 279. N 2. P. 269-275.
[13] Акопян А. В., Иванов Е. В., Поликарпова П. Д.,
[22] Fei Z., Zhao D., Geldbach T., Scopelliti R., Dyson P.
Тараканова А. В., Рахманов Э. В., Полякова О. В.,
// Chem. Eur. J. 2004. V. 10. N 19. P. 4886-4893.
Анисимов А. В., Винокуров В. А., Караханов Э. А.
[23] Polikarpova P., Akopyan A., Shigapova A., Glotov A.,
// Нефтехимия. 2015. Т. 55. № 5. С. 426-429
Anisimov A., Karakhanov E. // Energy & Fuels. 2018.
[Akopyan A. V., Ivanov E. V., Polikarpova P. D.,
V. 32. P. 10898-10903.