Пиролиз метана на резистивном ZrO2/SiC катализаторе
1179
Журнал прикладной химии. 2019. Т. 92. Вып. 9
УДК 546.26, 542.97, 547.21, 546.72.
ПИРОЛИЗ МЕТАНА НА РЕЗИСТИВНОМ ZrO2/SiC КАТАЛИЗАТОРЕ
© С. С. Сигаева, Д. А. Шляпин, В. Л. Темерев, П. Г. Цырульников
Центр новых химических технологий Института катализа им. Г. К. Борескова СО РАН,
644040, г. Омск, ул. Нефтезаводская, д. 54
E_mail: s_in_cube@mail.ru
Поступила в Редакцию 11 сентября 2018 г.
После доработки 27 мая 2019 г.
Принята к публикации 26 июня 2019 г.
Изучена динамика пиролиза метана на резистивном катализаторе ZrO2/SiC при различных темпе-
ратурах. При температуре 1300°С конверсия метана проходит через максимум (55%) на 60-й ми-
нуте, при этом селективность по ацетилену монотонно нарастает в течение всего эксперимента.
Методом сканирующей микроскопии с EDAX-анализом показано, что в первые 10 мин эксперимента
происходит почти полное зауглероживание образца ZrO2/SiC при температуре 1300°С, а также за-
фиксировано образование углеродного покрытия слоистой структуры на поверхности катализатора в
процессе эксперимента, при этом в продуктах пиролиза по-прежнему присутствуют С2-углеводороды.
Показано, что углеродные отложения, образующиеся на поверхности катализатора, являются ка-
талитически активными в процессе образования ацетилена. Регенерация катализатора не приводит
к полному восстановлению его каталитических свойств.
Ключевые слова: пиролиз; метан; резистивный катализатор; углерод; динамика превращения
DOI: 10.1134/S0044461819090111
Природный газ является исходным сырьем для
метан, продуктов реакции. В качестве резистивных
получения многих ценных химических продуктов,
катализаторов могут быть использованы различные
однако доля газа, используемого в России в качестве
металлы и сплавы, активные в реакции превращения
химического сырья, крайне низка и не превышает
метана. Основным недостатком этих катализаторов
1.5% от добываемого объема [1, 2]. Поиск путей эф-
является их зауглероживание и разрушение за счет
фективной переработки метана, являющегося ос-
протекания углеродной коррозии c образованием кар-
новным компонентом природного и попутного не-
бидов металлов [15, 16].
фтяного газа, в ценные продукты является одной
Карборунд — синтетический материал со-
из основных проблем катализа. Из прямых методов
става SiC — представляет собой широкозонный
переработки метана в ценное углеводородное сырье
полупроводник с высокими рабочими температурами,
можно выделить окислительный и плазмохимиче-
электрической прочностью и хорошей теплопрово-
ский пиролиз с получением ацетилена и окислитель-
дностью. В связи с тем что карборунд (SiC) является
ную конденсацию с образованием этана и этилена
карбидом, он не подвергается углеродной коррозии,
[3-11]. Новым направлением переработки метана в
но SiC, как было установлено ранее [17], малоакти-
С2-углеводороды является пиролиз на резистивных
вен в реакции пиролиза метана. Нанесение на по-
катализаторах [12-14]. Данный способ предполагает
верхность данного материала оксидов ZrO2, MgO,
нагревание катализатора пропусканием через него
Al2O3 или SiO2 позволяет значительно увеличить
электрического тока до температур 700-1500°С с по-
активность и селективность катализатора в реакции
дачей на катализатор холодной газовой смеси. Часть
пиролиза метана [17].
холодной смеси проходит через реакционный объем,
Целью данной работы было исследование ди-
не контактируя с катализатором, что способствует
намики активности и селективности резистивного
закаливанию образующихся, менее стабильных, чем
катализатора ZrO2/SiС в реакции пиролиза метана
1180
Сигаева С. С. и др.
и изменения его фазового и химического состава во
32 мм, скорость подачи газовой смеси составляла
времени при выбранных температурах.
100 мл·мин-1.
Пробу смеси после реактора анализировали
хроматографическим методом, который проводи-
Экспериментальная часть
ли с использованием хроматографа Цвет-500М.
Синтез нанесенного на SiC катализатора ZrO2/
Содержание остаточного метана, а также образу-
SiC. В качестве предшественника оксидного ком-
ющихся этана, этилена и ацетилена определяли с
понента ZrO2 использовали ZrО(NO3)2·2H2O.
помощью детектора ионизации в пламени [условия
Поскольку поверхность карборунда гидрофобна,
хроматографирования: капиллярная колонка с непод-
стержни из SiC предварительно нагревали в муфеле
вижной фазой SiO2 длиной 30 м, давление газа-носи-
до 200°С и затем опускали в раствор ZrО(NO3)2·2H2O
теля (азот) 1 кгс·см-2, расход воздуха 300 мл·мин-1,
с концентрацией, рассчитанной на оксид циркония,
расход водорода 30 мл·мин-1, температура колонки
50 мг·мл-1. Образующиеся оксиды и оксинитраты
50°С]. Содержание азота и образующегося Н2 ана-
циркония осаждались на поверхности карборунда.
лизировали с помощью детектора теплопроводности
После этого образцы сушили, прокаливали на воз-
[условия хроматографирования: насадочная колонка
духе в муфельной печи при 500°С в течение 30 мин
с цеолитом СаА длиной 1.5 м, скорость газа-носителя
и охлаждали до комнатной температуры. Повторные
(аргон) 50 мл·мин-1, ток детектора 164 мA, темпера-
пропитки и термообработки проводили до тех пор,
тура колонки 50°С].
пока суммарное количество нанесенного оксида ZrO2
По результатам анализа реакционной смеси рас-
не составило 10 мас%. После нанесения необходимо-
считывали конверсию метана и селективность по
го количества образцы прокаливали на воздухе при
продуктам реакции.
температуре 1000°С в течение 4 ч.
Образцы зауглероженных катализаторов исследо-
Исследование каталитической активности.
вали методом электронной сканирующей микроско-
Реакцию пиролиза метана на резистивных катали-
пии (СЭМ), микроснимки поверхности были получе-
заторах исследовали с использованием проточной
ны на растровом электронном микроскопе JSM-6460
установки, снабженной электрическими вводами для
LV фирмы Jeol, Япония.
нагрева катализатора [13, 17]. Нагрев катализатора
до температур 700-1400°С и более осуществляли
Обсуждение результатов
переменным электрическим током. Температуру за-
меряли бесконтактным методом с использованием
На рис. 1 представлены микроснимки поверхности
оптического пирометра (ПД-10, ОАО НПП «Эталон»,
носителя и исходного катализатора.
г. Омск) с лазерным наведением на катализатор. На
Морфологически поверхность карборунда пред-
разогретый электрическим током катализатор подава-
ставлена частицами размером ~50 мкм. Проведенное
ли исходный реакционный газ, содержащий 15% ме-
картирование показало, что Si, C и O распределены
тана в азоте. Для исследования катализаторов на ос-
по поверхности достаточно равномерно. Методом
нове карборундовых стержней (длина 30 мм, диаметр
ЕDAX определен состав карборунда, основным
8 мм), расположенных перпендикулярно газовому
компонентом которого является кремний в форме
потоку, использовали кварцевый реактор диаметром
карбида (табл. 1). Наличие небольшого количества
Рис. 1. Микрофотография поверхности носителя SiC (а) и катализатора до реакции пиролиза метана ZrO2/SiC (б).
Пиролиз метана на резистивном ZrO2/SiC катализаторе
1181
Таблица 1
ры для катализатора 10 мас% ZrO2/SiC. Температуру
EDAX-Анализ поверхности SiC и ZrO2/SiC
поднимали ступенчато с шагом 50° и выдерживанием
на каждой ступени в течение 30 мин.
Содержание в катализаторе, мас%
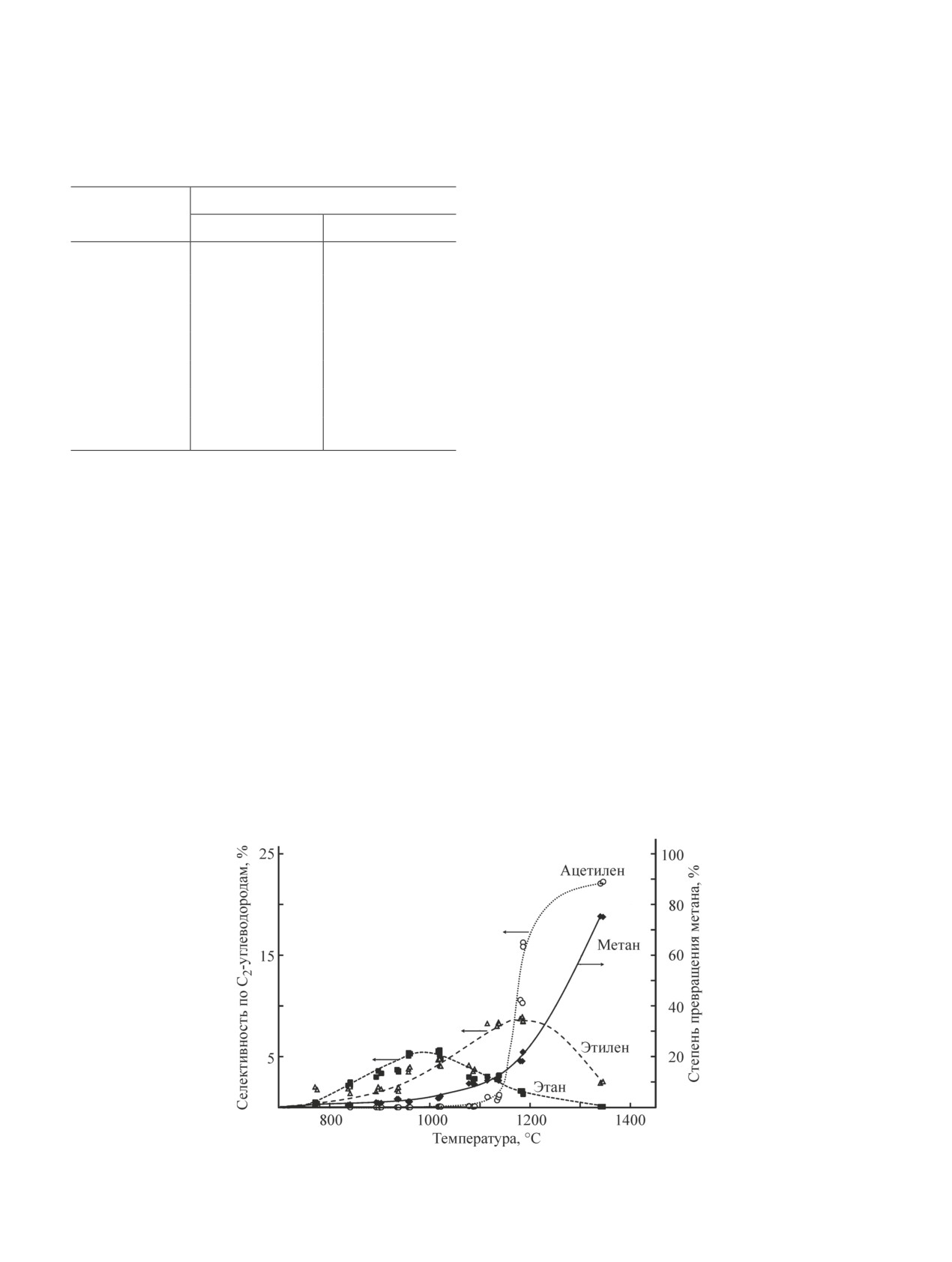
Превращение метана на катализаторе начинается
Элемент
SiC
ZrO2/SiC
с 700°С. В температурном интервале 700-1200°С при
низкой конверсии метана, не достигающей 10%, ос-
С
28.7
5.63
новными продуктами превращения метана являются
этан (S = 5%) и этилен (S = 9%), максимумы селектив-
Si
66.2
1.99
ности по которым достигаются в области температур
O
3.9
25.75
950 и 1180°С соответственно. Ацетилен на карборун-
Al
0.4
—
де начинает образовываться при температуре 1120°С,
и с повышением температуры выход его возрастает.
Na
0.3
—
Полученные результаты свидетельствуют о последо-
Fe
0.5
—
вательном дегидрировании этан → этилен → ацети-
лен с повышением температуры. Максимальная се-
Zr
—
66.63
лективность по ацетилену при конверсии метана 75%
и температуре 1350°С составляет 22%. Для оценки
кислорода в составе доказывает присутствие на по-
стабильности катализатора была исследована дина-
верхности и окисленного кремния. Основными при-
мика его каталитических характеристик при разных
месями в карборунде являются алюминий, натрий и
температурах в течение 120 мин эксперимента. Для
железо (до 0.5 мас%). Необходимо отметить, что Al
этого на нагретый до выбранной температуры ката-
на поверхности присутствует в виде редких агломе-
лизатор подавали метансодержащую смесь и следили
ратов частиц оксида размером 2-4 нм.
за изменением конверсии метана и селективности по
Оксид циркония, нанесенный на карборунд, об-
С2-продуктам во времени. Катализатор испытывали
разует пленку, образованную мелкими плоскими
при температурах 950, 1100, 1250 (начало появле-
частицами и практически полностью закрываю-
ния ацетилена и высокая селективность по этилену),
щую поверхность носителя. Тем не менее согласно
1300°С (высокая селективность по ацетилену).
результатам картирования и EDAX на поверхно-
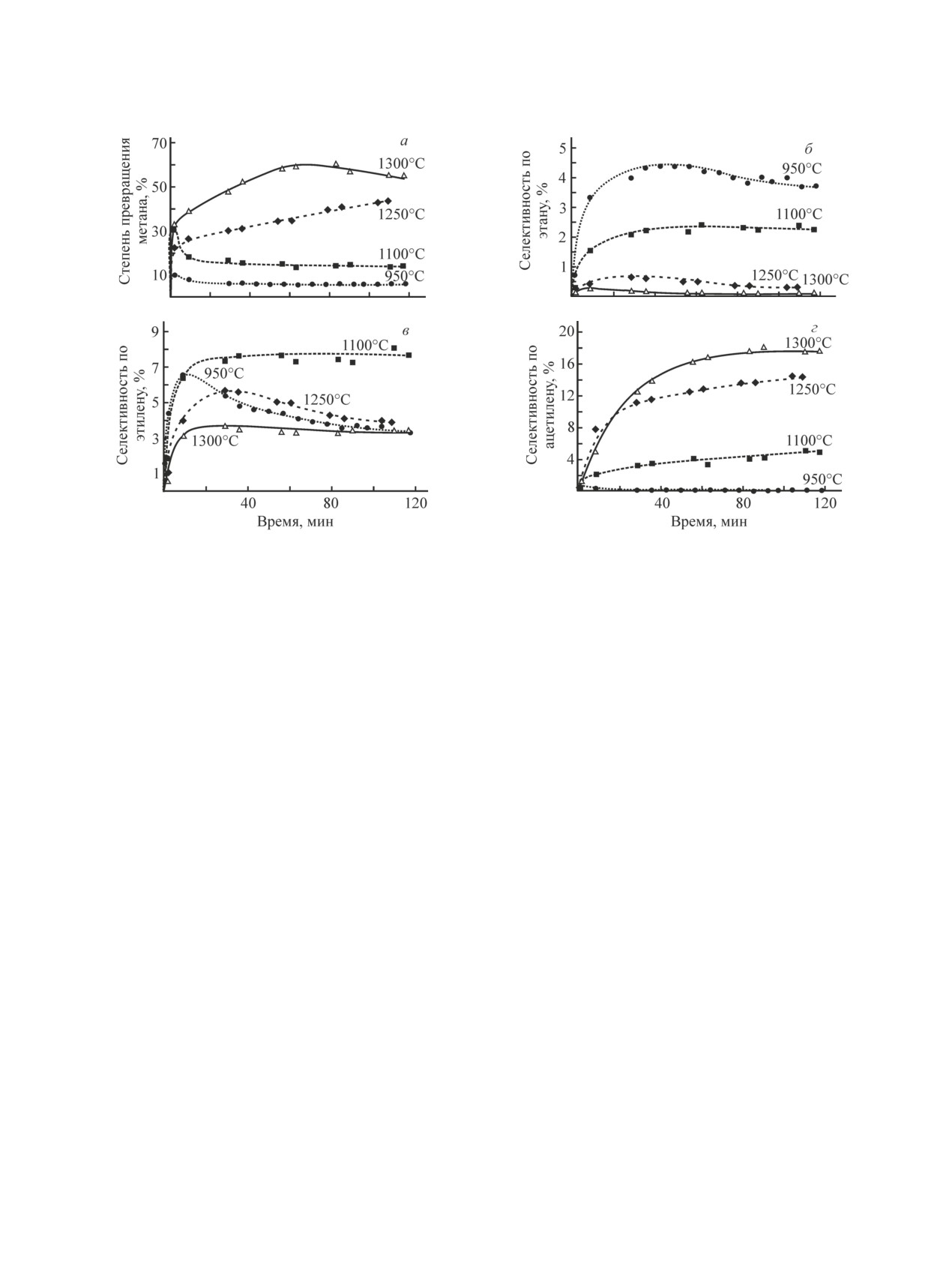
Из приведенных на рис. 3, а данных видно, что
сти данного катализатора наблюдаются небольшие
при температурах 950-1100°С степень превращения
участки не покрытого пленкой ZrO2 карбида кремния
метана уменьшается в первые 10 мин эксперимента
(табл. 1).
от 10 (950°С) и 30 (1100°С) до постоянного значения,
На рис. 2 представлена зависимость конверсии ме-
равного 7 и 18% соответственно. При температу-
тана и селективности по С2-продуктам от температу-
ре 1250°С конверсия метана монотонно нарастает
Рис. 2. Зависимость конверсии метана и селективностей по С2-продуктам от температуры.
1182
Сигаева С. С. и др.
Рис. 3. Динамика конверсии метана катализатора и селективности по С2-углеводородам при различных темпера-
турах.
с 22 до 42% за 2 ч эксперимента, а при выдержива-
нии эксперимента (120 мин) до величины 14%, при
нии катализатора при температуре 1300°С степень
1300°С — выходит на постоянное значение 17.5%
превращения сначала монотонно нарастает с 32 до
на 80-й мин эксперимента и сохраняется в течение
58% за 1 ч, затем начинает снижаться. При времени
еще 120 мин. Для температуры 950°С наблюдаются
выдерживания 200 мин конверсия метана уменьша-
исчезающе малые количества ацетилена в реакци-
ется до 48%.
онной смеси (рис. 3, г). Таким образом, наблюдает-
Отметим, что при отсутствии кислорода большая
ся экстремальная зависимость конверсии метана от
часть метана разлагается на катализаторе до углерода.
времени испытания катализатора при сохранении
Так, при температуре 950°С в углерод превращается
селективности по ацетилену при температуре ката-
93% прореагировавшего метана, при 1100°С в виде
лизатора 1300°С.
углерода на катализаторе отлагается более 85% ме-
В соответствии с результатами динамических экс-
тана, при 1250°С — более 80%, а при температуре
периментов были выбраны значения времени после
1300°С в углерод переходит не менее 75% метана.
начала эксперимента, при достижении которых бы-
Таким образом, увеличение температуры приводит к
ли взяты пробы для электронно-микроскопического
увеличению селективности по С2-углеводородам, в
исследования поверхности катализаторов: 10, 60 и
частности ацетилену.
240 мин. Так, после 10 мин эксперимента согласно
Селективность по этану при температуре 950°С
СЭМ катализатор ZrO2/SiC полностью покрыт угле-
(рис. 3, б) достигает лишь 4.3%, при повышении тем-
родом (рис. 4, табл. 2). Небольшие количества Zr
пературы она снижается. При 950°С селективность
можно отметить на краях отработанного катализатора
по этилену в первые 10 мин эксперимента достигает
(рис. 4, область 1) по сравнению с центральной обла-
6.5%, но затем значительно быстрее, чем селектив-
стью карборундового стержня (область 2), что может
ность по этану, снижается вплоть до 3.5% (рис. 3, в).
быть связано с более низкой температурой за счет
Максимальная селективность по этилену, близкая к
теплоотдачи металлическим контактам.
8%, достигается при температуре 1100°С и сохра-
Морфология поверхности катализатора после
няется на протяжении 2 ч. При температуре 1250 и
10 мин работы в реакции пиролиза метана также
1300°С селективность по этилену значительно ниже
представлена на рис. 4. Катализатор однородно по-
и близка к 3.5%. При этом селективность по ацети-
крыт углеродом, редко на поверхности катализатора
лену при 1250°С медленно нарастает на протяже-
наблюдаются волокна диаметром 10 мкм и высотой
Пиролиз метана на резистивном ZrO2/SiC катализаторе
1183
Рис. 4. Микроснимки поверхности отработавшего в реакции пиролиза метана образца ZrO2/SiC в разном масштабе:
1:35 (а), 1:270 (б), 1:1000 (в, г).
Температура реакции 1300°С, время работы катализатора 10 мин, концентрация метана 15%,
скорость потока 100 мл·мин-1.
около 50 мкм. Таким образом, основная реакция,
углеродной шубы можно наблюдать зародыши бу-
протекающая на поверхности катализатора, это его
дущих углеродных волокон. Образование слоистого
восстановление и карбидизация (согласно данным
углеродного покрытия сопровождается увеличением
РФА) с дальнейшим покрытием образованного кар-
конверсии метана при одновременном увеличении
бида циркония углеродной корочкой.
селективности по ацетилену.
Увеличение времени контакта катализатора с ме-
После 4 ч работы катализатор полностью покрыт
тансодержащей смесью до 60 мин приводит к обра-
углеродом в виде волокон диаметром около 100 мкм
зованию на поверхности катализатора углеродной
и высотой до 500 мкм (рис. 6).
«шубы» слоистой структуры (рис. 5).
Несмотря на увеличение поверхности образца за
EDAX-Анализ поверхности катализатора в ме-
счет образовавшихся волокон, конверсия метана зна-
стах, не покрытых слоистым углеродом, показал, что
чительно снижается: до 48% на 200-й минуте экспе-
на них катализатор зауглерожен, но есть участки, со-
римента от достигнутых на 60-й минуте 58%. Можно
держащие большие количества Zr и Si в окисленном
предположить, что это связано с появлением гради-
состоянии (рис. 6, картирование). На поверхности
ента температуры поверхности за счет изменения ее
Рис. 5. Микроснимок поверхности отработавшего в реакции пиролиза метана образца ZrO2/SiC в разных масштабах:
1:55 (а), 1:450 (б), 1:5000 (в) — и результаты EDAX-анализа на углерод (г), цирконий (д), кремний (е).
Температура реакции 1300°С, время работы катализатора 1 ч, концентрация метана 15%, скорость потока 100 мл·мин-1.
1184
Сигаева С. С. и др.
Рис. 6. Микроснимок поверхности отработавшего в реакции пиролиза метана образца ZrO2/SiC в разном масштабе:
1:30 (а), 1:100 (б), 1:1000 (в).
Температура реакции 1300°С, время работы катализатора 4 ч, концентрация метана 15%, скорость потока 100 мл·мин-1.
морфологии (рис. 6). Тем не менее селективность по
ацетилену сохраняется постоянной (17.5%) с 80-й
минуты эксперимента.
Отработанный катализатор ZrO2/SiC исследовали
методом рентгенофазового анализа. Было показано,
что после 4 ч эксперимента фазовый состав катали-
затора представлен только графитоподобным угле-
родом.
Наблюдается большое различие в химическом
составе поверхности и морфологии углеродных отло-
жений для образца после пиролиза при температуре
1100°C и катализатора, испытанного в течение 4 ч
при 1300°С (рис. 7). Поверхность образца однород-
но представлена углеродом и цирконием в отличие
от образца, испытанного при 1300°С, покрытого
Рис. 7. Микроснимок поверхности отработавшего в
углеродными волокнами. Концентрации кислорода
реакции пиролиза метана образца ZrO2/SiC, масштаб
1:500.
и циркония на поверхности резко снижаются после
4 ч работы, а содержание углерода увеличивается до
Температура реакции 1100°С, время работы катали-
затора 4 ч, концентрация метана 15%, скорость потока
85.5% (табл. 3). Это согласуется с данными элемент-
100 мл·мин-1.
ного картирования, отражающими сходное распреде-
Таблица 2
Локальный химический состав поверхности
катализатора
Таблица 3
Химический состав поверхности катализатора
Состав, мас%
Содержание
C
O
Si
Zr
Состав, мас%
Время работы
C
O
Si
Zr
примеси
Суммарное
96.4
1.2
0.2
2.2
Область 1 (рис. 4)
89
0.8
0.9
9.3
10 мин
9.8
23.7
0.6
65.3
0.6
Область 2 (рис. 4)
97.8
1.4
—
0.8
4 ч
85.5
2.7
0.4
10.9
0.5
Пиролиз метана на резистивном ZrO2/SiC катализаторе
1185
Рис. 8. Динамика конверсии метана и селективности по ацетилену катализатора ZrO2/SiC до и после регенерации
(Т = 1000°С, воздух, 4 ч).
Температура реакции 1250°С, концентрация метана 15%, скорость потока 100 мл·мин-1.
ление циркония и углерода в поверхностном слое, и с
температуры важны химические свойства носителя.
данными рентгенофазового анализа об образовании
Так, в [17] показано, что на поверхности чистого
карбида циркония. При этом образец, испытанный
карборунда необходимый каталитический слой не
при 1300°С, после 4 ч эксперимента покрыт углеро-
образуется.
дом на 99.9%.
Гравиметрический анализ исследуемого образ-
Образец ZrO2/SiC, испытанный в реакции пиро-
ца показал, что после окислительной обработки
лиза метана при температуре 1250°С в течение 2 ч,
отработанного катализатора масса его значитель-
затем регенерировали в муфеле на воздухе в течение
но снизилась по сравнению с массой катализатора
4 ч и снова испытывали в реакции пиролиза метана
до испытания в реакции пиролиза метана (табл. 4).
при 1250°С (рис. 8).
Возможно, это связано с разрушением оксидного
Конверсия метана нарастала со временем в гораз-
слоя, нанесенного на карборунд в процессе пиролиза,
до меньшей степени, чем на исходном катализаторе,
за счет его восстановления и образования углерода и
снижалась и селективность по ацетилену. Согласно
удалением его в процессе регенерации с поверхности
ранее проведенным исследованиям [17] и результатам
катализатора.
данных исследований можно предположить, что для
формирования каталитически активного слоя угле-
Выводы
рода на поверхности резистивного носителя кроме
Пиролиз метана на резистивном катализаторе при
температуре 950-1300°С приводит к формированию
на поверхности катализатора слоя углеродных отложе-
Таблица 4
ний. Слой углеродных отложений формируется очень
Изменение массы исследуемого образца в ходе
быстро, в первые 10 мин эксперимента, и покрывает
эксперимента
практически всю поверхность катализатора, однако
образец остается активным в превращении метана в
Проведенная операция
Масса, г
ацетилен и практически не изменяет значение селек-
Нанесение активного компонента
3.4420
тивности, что говорит о формировании на поверхности
слоя углеродных отложений каталитически активных
Каталитический эксперимент
3.5477
центров. Согласно данным сканирующей электронной
Регенерация
3.4301
микроскопии, слой углеродных отложений образуется
из отдельных волокон, формирующих в итоге угле-
Регенерация и каталитический эксперимент
3.4442
родную «шубу» слоистой структуры. Выдерживание
1186
Сигаева С. С. и др.
на воздухе катализатора при температуре 1000°С
selective synthesis of acetylene // Fuel Processing
приводит к удалению с поверхности катализатора слоя
углеродных отложений, однако при этом изменяется и
org/10.1016/j.fuproc.2017.12.025
[6] Moldoveanu S. C. Pyrolysis of Organic Molecules.
его поверхность, что приводит к снижению скорости
формирования углеродной «шубы» при повторном
org/10.1016/B978-0-444-64000-0.00002-0
эксперименте.
[7] Bidgoli A.M., Ghorbanzadeh A., Lotfalipour R., Ehsan
Roustaei, Zakavi M. Gliding spark plasma: physical
Финансирование работы
principles and performance in direct pyrolysis of
methane // Energy. 2017. V. 125. P. 705-715. https://
Работа выполнена в рамках государственно-
doi.org/10.1016/j.energy.2017.02.144
го задания Центра новых химических техноло-
[8] Hidaka Y., Sato K., Henmi Y., Tanaka H., Inami K.
гий Института катализа СО РАН в соответствии с
Shock-tube and modeling study of methane pyrolysis
Программой фундаментальных научных исследо-
and oxidation // Combustion and Flame. 1999.
ваний государственных академий наук на 2013-
2020 годы по направлению V. 46, проект V.46.2.5
2180(99)00010-3
(номер госрегистрации в системе ЕГИСУ НИОКТР
[9] Zherlitsyn A. G., Shiyan V. P., Demchenko P. V.
Microwave plasma torch for processing hydrocarbon
AAAA-A17-117021450096-8).
gases // Resource-Efficient Technol. 2016. V. 2. P. 11-
[10]
Fincke J. R., Anderson R. P., Hyde T., Detering B. A.,
Конфликт интересов
Wright R., Bewley R. L., Haggard D. C.,
Авторы заявляют об отсутствии конфликта инте-
Swank W. D. Plasma thermal conversion of metha-
ресов, требующего раскрытия в данной статье.
ne to acetylene // Plasma Chem. and Plasma Proces-
org/10.1023/A:1012944615974
Информация об авторах
[11]
Rokstad O. A., Olsvik O., Holmen A. Thermal coupling
of methane // Studies in Surface Sci. and Catal. 1991.
org/0000-0001-5307-6517
2991(08)60120-2
[12]
Sun Qi., Tang Yo., Gavalas G. R. Methane pyrolysis in
org/0000-0001-6280-9292
a hot filament reactor // Energy & Fuels. 2000. N 14.
org/0000-0002-4524-4178
[13]
Сигаева С. С., Лихолобов В. А., Цырульников П. Г.
Павел Григорьевич Цырульников, ORCID: http://
Пиролиз метана на термообработанной фехрале-
orcid.org/0000-0001-5244-3530
вой спирали, нагреваемой электрическим током //
Кинетика и катализ. 2013. Т. 54. № 2. С. 208-215
[Sigaeva S. S., Likholobov V. A., Tsyrul′nikov P. G. //
Список литературы
Kinet. and Catal. 2013. V. 54. N 2. P. 199-206. https://
[1] Сайфуллин И. Ш., Сайфуллин Р. И. Состояние и
doi.org/10.1134/S0023158413010126].
перспективы реализации технологий переработки
[14]
Порсин А. В., Куликов А. В., Амосов Ю. И.,
газа в синтетические жидкие топлива // Проблемы
Рогожников В. Н., Носков А. С. Синтез ацетиле-
машиностроения и автоматизации. 2018. С. 136-144.
на при пиролизе метана на вольфрамовой нити
[2] Арутюнов В. С., Лапидус A. Л., Сайфуллин И. Ш.,
// Тeорет. основы хим. технологии. 2014. Т. 48.
Резуненко B. И. XXI век — век газохимии // Газ.
С. 426-433 [Porsin A. V., Kulikov A. V., Amosov Yu. I.,
пром-сть. 2003. № 3. С. 76-80.
Rogozhnikov V. N., Noskov A. S. Acetylene synthesis
[3] Chukeaw T., Sringam S., Chareonpanich M., Seubsai A.
by methane pyrolysis on a tungsten wire // Theoret.
Screening of single and binary catalysts for oxidative
Foundations Chem. Eng. 2014. V. 48. P. 397-403.
coupling of methane to value-added chemicals // Mol.
[15]
Сигаева С. С., Цырульников П. Г., Темерев В. Л.,
mcat.2019.03.021
Борисов В. А. Пиролиз метана на фехралевом ре-
[4] Holmen A. Direct conversion of methane to fuels and
зистивном катализаторе при добавлении водорода
chemicals // Catal. Today. 2009.V. 142. P. 2-8. https://
или кислорода в реакционную смесь // Катализ в
doi.org/10.1016/j.cattod.2009.01.004
пром-сти. 2015. № 2. С. 6-9 [Sigaeva S. S., Temerev
[5] An H., Cheng Y., Li T., Li Y., Cheng Y. Numerical
V. L., Borisov V. A., Tsyrul′nikov P. G. Pyrolysis of
analysis of methane pyrolysis in thermal plasma for
methane on fechral resistive catalyst with additions of
Пиролиз метана на резистивном ZrO2/SiC катализаторе
1187
hydrogen or oxygen to the reaction mixture // Catal.
kov M. Yu. Carbon deposits on a resistive FeCrAl
catalyst for the suboxidative pyrolysis of methane //
org/10.1134/S2070050415030101].
Kinet. and Catal. 2014. V. 55. N 3. P. 319-326. https://
[16] Борисов В. А., Сигаева С. С., Цырульников П. Г.,
doi.org/10.1134/S002315841403001X].
Тренихин М. В., Леонтьева Н. Н., Слептерев А. А.,
[17] Сигаева С. С., Темерев В. Л., Кузнецова Н. В.,
Кан В. Е., Бирюков М. Ю. Углеродные отложе-
Цырульников П. Г. // Катализ в пром-сти. 2017.
ния на резистивном фехралевом катализаторе суб-
№ 2. С. 94-101 [Sigaeva S. S., Temerev V. L., Kuzne-
окислительного пиролиза метана // Кинетика и
tsova N. V., Tsyrul′nikov P. G. // Catal. in Industry.
катализ. 2014. Т. 55. № 3. С. 334-341 [Borisov V. A.,
Sigaeva S. S., Tsyrul′nikov P. G., Trenikhin M. V.,
S2070050417030114].
Leont′eva N. N., Slepterev A. A., Kan V. E., Biryu-