282
Вахрушев А. Ю. и др.
Журнал прикладной химии. 2020. Т. 93. Вып. 2
УДК 546.824-31:546.57
ФОТОКАТАЛИТИЧЕСКИЕ СВОЙСТВА МАТЕРИАЛОВ
НА ОСНОВЕ ОКСИДА ТИТАНА(IV) И НАНОЧАСТИЦ СЕРЕБРА
© А. Ю. Вахрушев1, Д. С. Крайнов2, Т. Б. Бойцова2, В. В. Горбунова2, В. Н. Пак2
1 Высшая школа технологии и энергетики СПбГУПТД,
198095, г. Санкт-Петербург, ул. Ивана Черных, д. 4
2 Российский государственный педагогический университет им. А. И. Герцена,
191186, г. Санкт-Петербург, наб. р. Мойки, д. 48
Е-mail: nanochimiste@gmail.com
Поступила в Редакцию 17 апреля 2019 г.
После доработки 16 октября 2019 г.
Принята к публикации 14 декабря 2019 г.
Исследовано влияние фазового состава, присутствия наночастиц серебра и рН среды на каталитиче-
скую активность гетерофазных материалов на основе оксида титана(IV) в реакциях фотодеградации
метилового оранжевого и метиленового синего. Установлено, что наибольшая степень фотодеграда-
ции красителей достигается, когда соотношение фаз анатаз/рутил в фотокатализаторе находится
в диапазоне от 60/40 до 50/50 (мас%), образцы фотокатализатора модифицированы частицами
серебра, а значения рН растворов красителей составляют менее 5. Обоснование выявленных зако-
номерностей основано на использовании данных энергетических характеристик фаз TiO2 и серебра.
Ключевые слова: оксид титана(IV); наночастицы серебра; фотокатализ
DOI: 10.31857/S0044461820020176
Оксид титана(IV) является одним из самых рас-
частицами переходных металлов. В работе [15] было
пространенных фотокатализаторов. Многообразие
показано, что полученные материалы обладают ката-
методов синтеза TiO2 (золь-гель [1], гидротермаль-
литической активностью в реакции фотодеградации
ный [2], электрохимический [3]) позволяют варьи-
метилового оранжевого.
ровать состав и структуру получаемого материала.
Целью данной работы являлось установление кор-
Гетерофазные анатаз/рутил (модификации TiO2)
реляций между составом и строением TiO2 и TiO2/Ag
системы обладают более высокой фотокаталитиче-
материалов и их каталитическими свойствами в ре-
ской активностью, чем чистые анатаз или рутил [4-6].
акции фотодеградации метилового оранжевого и ме-
Причина данного явления заключается в простран-
тиленового синего.
ственном разделении фотогенерированных носителей
заряда, однако единого мнения о направлении пере-
Экспериментальная часть
носа заряда нет. В литературе имеются сведения как
о перемещении фотогенерированных электронов из
Получение образцов оксида титана(IV) и модифи-
фазы рутила к анатазу [7, 8], так и в обратном направ-
кацию их наночастицами серебра осуществляли тем-
лении [9, 10]. Снижению рекомбинации носителей
платным способом по описанной ранее методике [16].
заряда и повышению фотокаталитической активности
В качестве темплата для формирования оксида тита-
также способствует модификация TiO2 наночастица-
на(IV) использовали беленую сульфатную целлюлозу
ми металлов [11], оксидов [12], сульфидов [13] и т. п.
(Илим, Санкт-Петербург). Образцы целлюлозы без
Ранее мы сообщали о темплатном методе синтеза
предварительной обработки пропитывали 2.5%-ным
[14], который позволяет получать оксид титана(IV) с
раствором тетра-н-бутоксида титана(IV) в пропано-
высокой удельной поверхностью и контролируемым
ле-2, после чего сушили на воздухе при температу-
фазовым составом, а также модифицировать его нано-
ре 100°С. Отжиг темплата проводился в фарфоро-
Фотокаталитические свойства материалов на основе оксида титана(IV) и наночастиц серебра
283
вых тиглях в муфельной печи Wise Therm в течение
Для подщелачивания раствора до рН 10 исполь-
20 мин при температуре 500-950°С на воздухе. Оксид
зовался кристаллический карбонат натрия (х.ч.,
титана(IV), модифицированный наночастицами се-
ЗАО «Вектон»). Эксперименты при рН 3.6 и 4.6 про-
ребра, получали по двустадийной методике. Образец
водили в среде цитратного буфера. Соотношение
целлюлозы пропитывали 5.0∙10-3 моль∙л-1 раствором
массы катализатора и объема раствора красителей
нитрата серебра в пропаноле-2, при этом предполага-
составляло 3 мг на 10 мл. Облучение растворов про-
лось, что после высушивания масса нитрата серебра
изводилось при интенсивном перемешивании моно-
в образце соответствовала навеске, используемой
хроматическим УФ-светом лампы Philips TUV 4W/
для приготовления раствора. После высушивания на
G4 T5 с длиной волны 254 нм и интенсивностью
воздухе при температуре 100°С образец помещали
3.0·1016 квант·см-2·с-1; толщина слоя облучаемого
в 2.5%-ный раствор тетра-н-бутоксида титана(IV) в
раствора — 15 мм. Перед началом экспонирования
пропаноле-2. Дальнейшие операции были аналогич-
образцы выдерживали в течение 30 мин в темноте
ны описанным выше для синтеза немодифицирован-
в растворе метилового оранжевого или метиленово-
ного оксида титана(IV).
го синего для установления равновесия процессов
Площадь удельной поверхности TiO2 и TiO2/Ag
адсорбции-десорбции в системе краситель-TiO2.
определяли, используя метод адсорбции паров во-
Каталитическую активность образцов оценивали
ды. Количество адсорбированной воды определя-
спектрофотометрически по спаду характерного для
ли при комнатной температуре весовым способом,
метилового оранжевого и метиленового синего погло-
задавая относительное давление пара в интервале
щения. Оценка относительной скорости разложения
p/p0 = 0.10-0.99 с помощью растворов серной кисло-
соединений производилась по тангенсу угла наклона
ты соответствующих концентраций.
кинетической кривой, отражающей зависимость изме-
Структуру образцов, немодифицированных и мо-
нения оптической плотности от времени облучения.
дифицированных серебром, анализировали с помо-
щью сканирующего электронного микроскопа (СЭМ)
Обсуждение результатов
JEOL JSM 7600F, снабженного энергодисперсионным
анализатором EDS SDD Oxford.
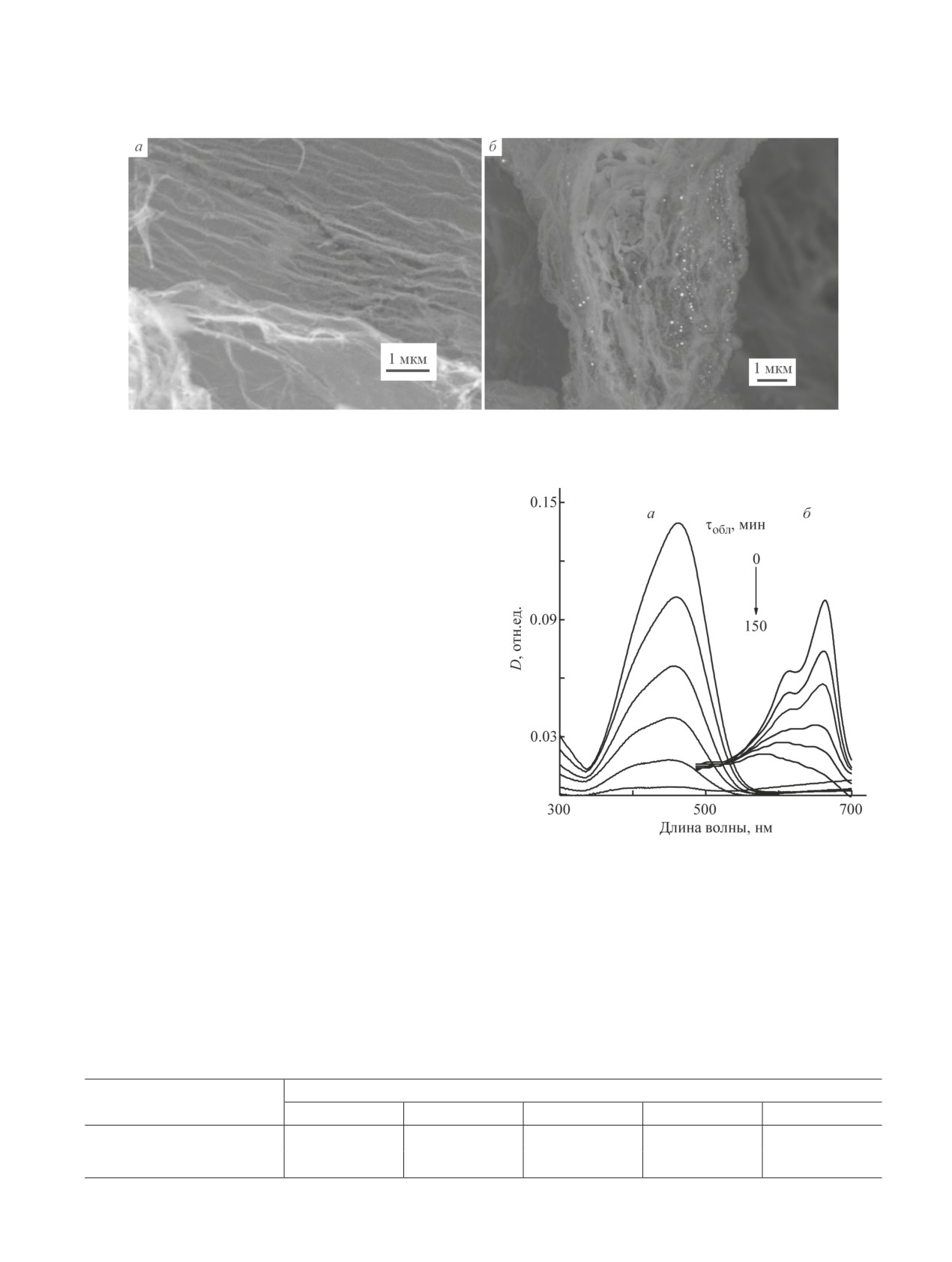
Типичные образцы фотокатализатора представ-
Фазовый состав образцов устанавливали методом
ляют собой волокнистый материал, повторяющий
рентгенофазового анализа на рентгеновском диф-
форму исходных волокон целлюлозы, с пористыми
рактометре ДРОН-7. Для анализа использовалось
стенками (рис. 1), сформированными за счет выде-
характеристическое излучение медного анода CuKα
ляющихся при горении органического темплата и
с длиной волны 0.154 нм. Оценка размеров кристал-
тетра-н-бутоксида титана(IV) дымовых газов. Размер
литов D оксида титана(IV) и частиц серебра была
пор варьируется от 50 до 200 нм для чистого TiO2 и
проведена по формуле Селякова-Шерера [17].
от 70 до 230 нм — для модифицированного серебром.
Соотношение фаз анатаз/рутил в образцах рассчи-
Больший размер пор в случае модифицированных
тывали по формуле [18]
образцов объясняется дополнительным выделени-
ем газов (NO2 и O2) при термическом разложении
xр = 1∙100/ (1 + kIа/Iр),
нитрата серебра. Удельная поверхность получен-
где xр — содержание рутила в смеси (%); Ia и Iр —
ных темплатным методом образцов TiO2 состав-
интегральные интенсивности соответственно (101)
ляет 55-60 м2·г-1, TiO2/Ag — 80-85 м2·г-1 и, как
и (110) рефлекса анатаза и рутила; k — коэффициент,
и размер пор, не зависит от температуры отжига.
равный тангенсу угла наклона калибровочной кривой,
Фазовый состав TiO2 и TiO2/Ag фотокатализаторов
представляющей собой зависимость отношения ин-
определяется температурой отжига целлюлозного
тенсивностей Iа/Iр стандартов как функцию отноше-
темплата. Повышение температуры отжига TiO2 и
ния их масс ma/mр, в условиях эксперимента k =0.794.
TiO2/Ag от 500 до 950°С приводит к первоначаль-
Регистрация спектров поглощения осущест-
ному формированию фазы анатаза, индексируемой
влялась с помощью спектрофотометра Shimadzu
по дифракционным пикам при 2θ, равном 24.9 (101),
UV-2550.
38.3 (004), 48.2° (200) (PDF N 00-001-0562), а за-
Фотокаталитические свойства структурированных
тем ее постепенной трансформации в рутил с ха-
образцов исследовали в реакции разложения метило-
рактерными пиками при 26.9 (110), 35.6 (101), 40.7
вого оранжевого (Sigma-Aldrich, 85%) и метиленового
(111), 43.7 (210) и 53.8° (211) (PDF N 00-001-1292).
синего (Sigma-Aldrich, ≥82%), концентрация водных
При 950°С образцы преимущественно состоят из
растворов которых составляла 2.5·10-5 моль·л-1.
рутила (табл. 1). В дифрактограммах TiO2/Ag при-
284
Вахрушев А. Ю. и др.
Рис. 1. Изображения оксида титана(IV) (а) и оксида титана(IV), модифицированного наночастицами серебра (б),
после отжига при 650°С в течение 20 мин, полученные с помощью сканирующего электронного микроскопа.
сутствуют пики, соответствующие рефлексам сере-
бра при 2θ, равном 38.1 (111), 44.5 (200), 64.4 (220)
и 78.0° (311), относящиеся к кубической кристал-
лической структуре металла (PDF N 00-004-0783).
Содержание серебра в образцах составляет 2.50-
2.55 ат% и не зависит от температуры отжига.
Для исследования каталитической активности об-
разцов были выбраны водные растворы метилового
оранжевого и метиленового синего, что обусловлено
их высокой устойчивостью к действию УФ-света
в отсутствие TiO2 и наличием полос поглощения в
видимой области спектра.
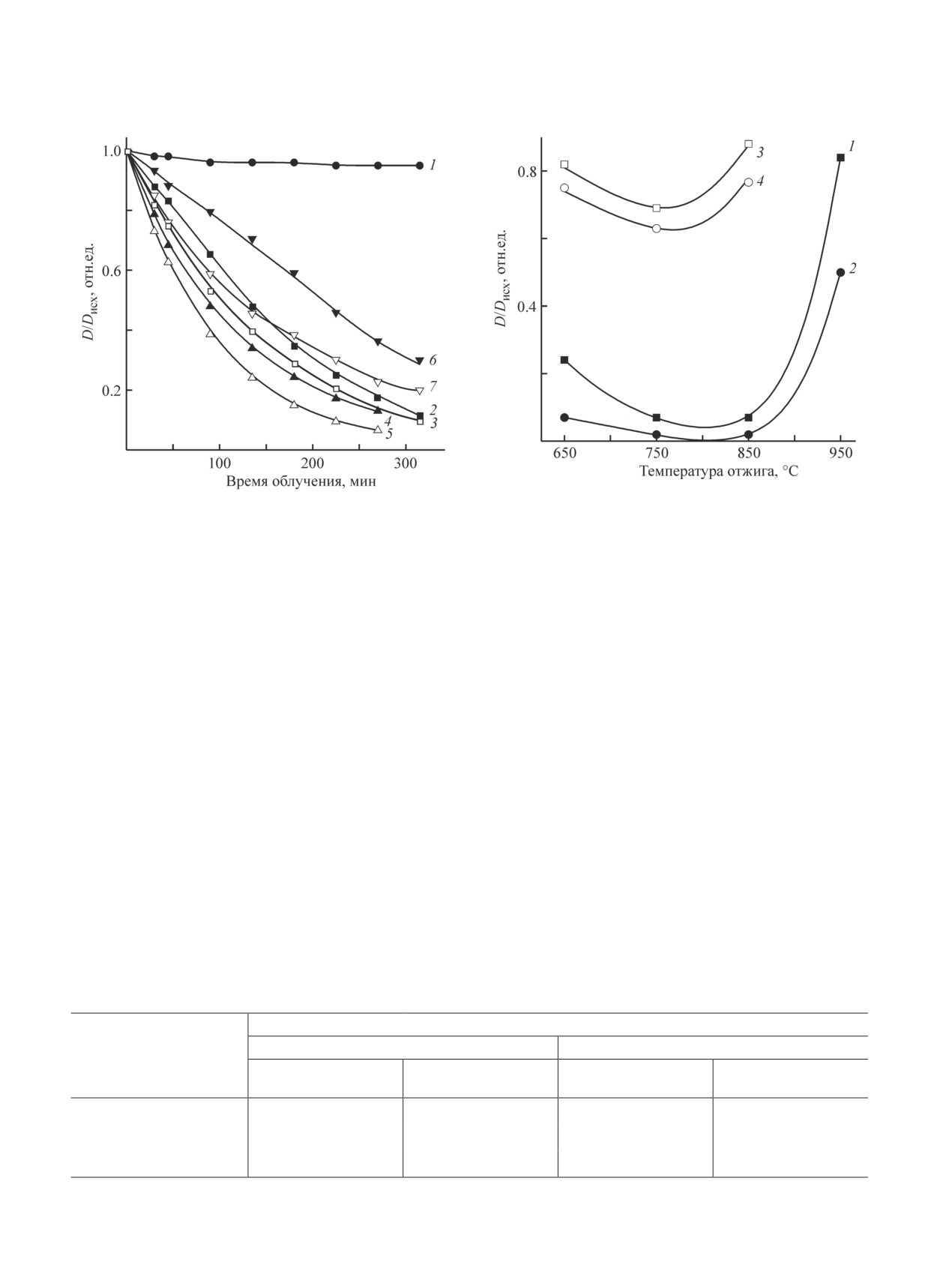
Облучение УФ-светом водных растворов краси-
телей приводит к снижению интенсивности полосы
поглощения метилового оранжевого при 465 нм и
характеристических полос димерной (612 нм) и моно-
мерной (668 нм) форм метиленового синего (рис. 2),
что свидетельствует об изменениях в структуре этих
соединений. Установлено, что скорость фотодеграда-
Рис. 2. Эволюция спектров поглощения водных раство-
ции красителей зависит от соотношения кристалли-
ров метилового оранжевого (а) и метиленового синего
ческих фаз TiO2, наличия частиц серебра в образцах
(б) при облучении УФ-светом в присутствии TiO2 ката-
лизатора.
фотокатализатора и рН растворов метилового оран-
жевого и метиленового синего.
На рис. 3 представлены типичные кинетические
оранжевого рассмотрены в статье [15]. Вид кине-
кривые фотокаталитического разложения метиле-
тических кривых (рис. 3) и значения относитель-
нового синего, аналогичные кривые для метилового
ной скорости деградации метилового оранжевого
Таблица 1
Содержание рутила в образцах катализаторов в зависимости от температуры отжига целлюлозного темплата
Содержание рутила, %, при температуре, °С
Образец
500
650
750
850
950
TiO2
0
16.5
38.5
91.0
97.5
TiO2/Ag
10.6
25.0
38.0
92.5
98.0
Фотокаталитические свойства материалов на основе оксида титана(IV) и наночастиц серебра
285
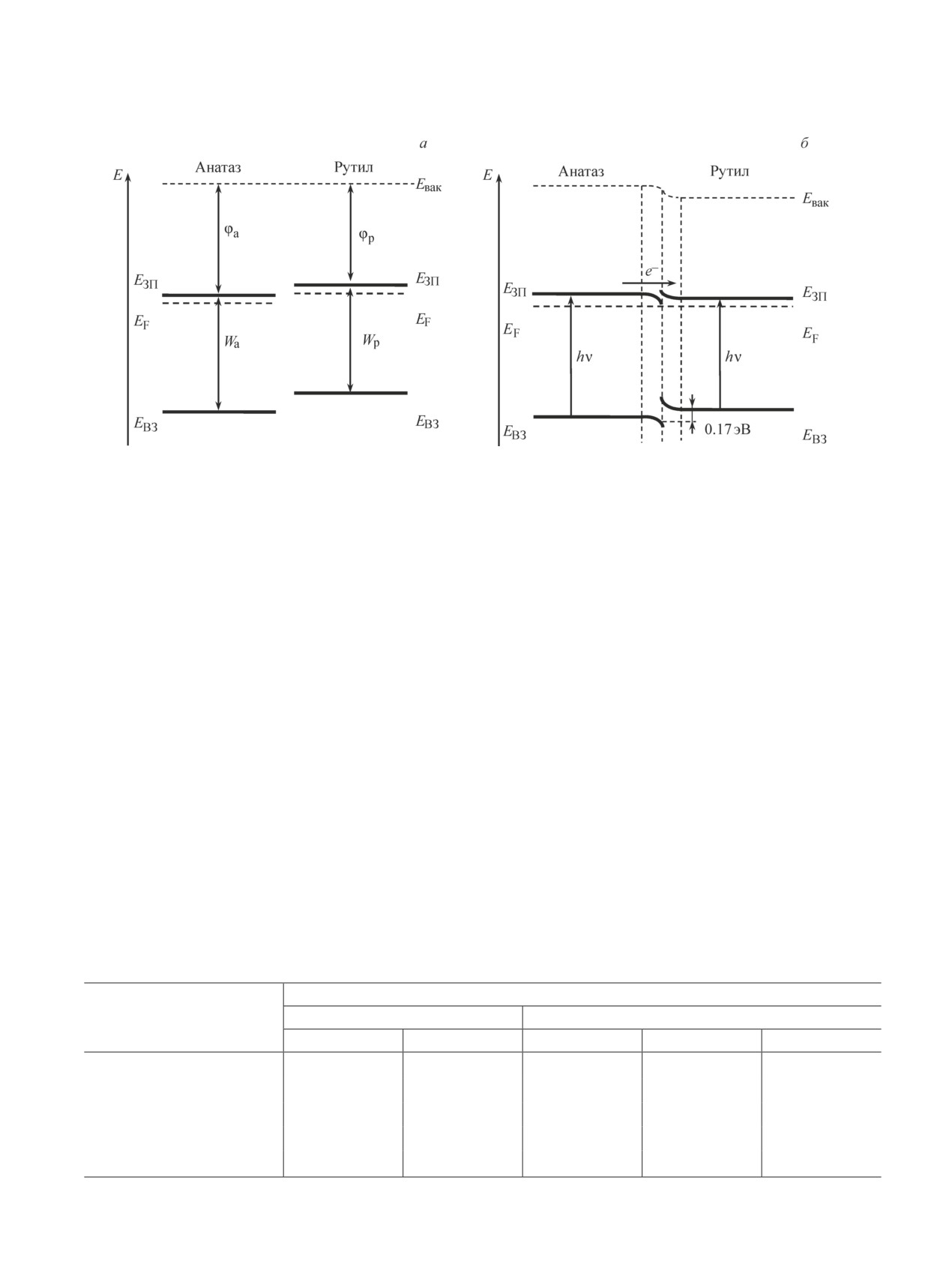
Рис. 4. Зависимость значений максимума оптической
Рис. 3. Кривые фотокаталитического разложения вод-
плотности растворов метилового оранжевого (D465) и
ных растворов метиленового синего в присутствии TiO2
метиленового синего (D668) при УФ-облучении в тече-
(2, 4, 6) и TiO2/Ag (3, 5, 7), полученных при температуре
ние 45 мин от температуры отжига TiO2 (1, 3) и TiO2/Ag
отжига 650 (2, 3), 750 (4, 5), 850°С (6, 7) и без катали-
(2, 4) катализаторов.
затора (1).
рН растворов красителей 4.6.
и метиленового синего (табл. 2) свидетельствуют о
тализатора варьируется от 60/40 до 50/50. Схожесть
большей каталитической активности гетерофазных
полученных значений соотношений фаз, а также бли-
TiO2/Ag образцов. Анализ данных табл. 2 и сопо-
зость размеров частиц анатаза и рутила (табл. 3) в
ставление значений оптической плотности, дости-
TiO2 и TiO2/Ag материалах позволяет утверждать,
гаемых за одинаковый интервал облучения (рис. 3),
что повышение каталитической активности образ-
позволили определить оптимальный фазовый состав
цов TiO2/Ag в реакции фоторазложения метилового
катализаторов, который вызывает наиболее полное
оранжевого и метиленового синего вызвано главным
обесцвечивание растворов метилового оранжевого и
образом влиянием частиц серебра.
метиленового синего. Наилучший результат для обо-
Полученные результаты проясняют данные зон-
их видов красителей наблюдается при температуре
ных диаграмм TiO2 (рис. 5). Как известно, анатаз
отжига целлюлозного темплата 750-800°С (рис. 4).
и рутил являются полупроводниками n-типа [10],
Соотнесение этих температур с динамикой изменения
ширина их запрещенных зон (W) составляет 3.20 и
фазового состава (табл. 1) показало, что оптимальное
3.03 эВ соответственно. Различие в термодинами-
соотношение анатаз/рутил (мас%) в образцах фотока-
ческих работах выхода (φ) анатаза (5.1 эВ) и рутила
Таблица 2
Зависимость относительной скорости фотокаталитического разложения метилового оранжевого и метиленового
синего (рН 7) от температуры отжига образцов TiO2 и TiO2/Ag
Относительная скорость фоторазложения
TiO2
TiO2/Ag
Температура отжига, °С
метиловый
метиловый
метиленовый синий
метиленовый синий
оранжевый
оранжевый
650
0.007
0.07
0.005
0.03
750
0.01
0.10
0.008
0.07
850
0.005
0.08
0.002
0.04
286
Вахрушев А. Ю. и др.
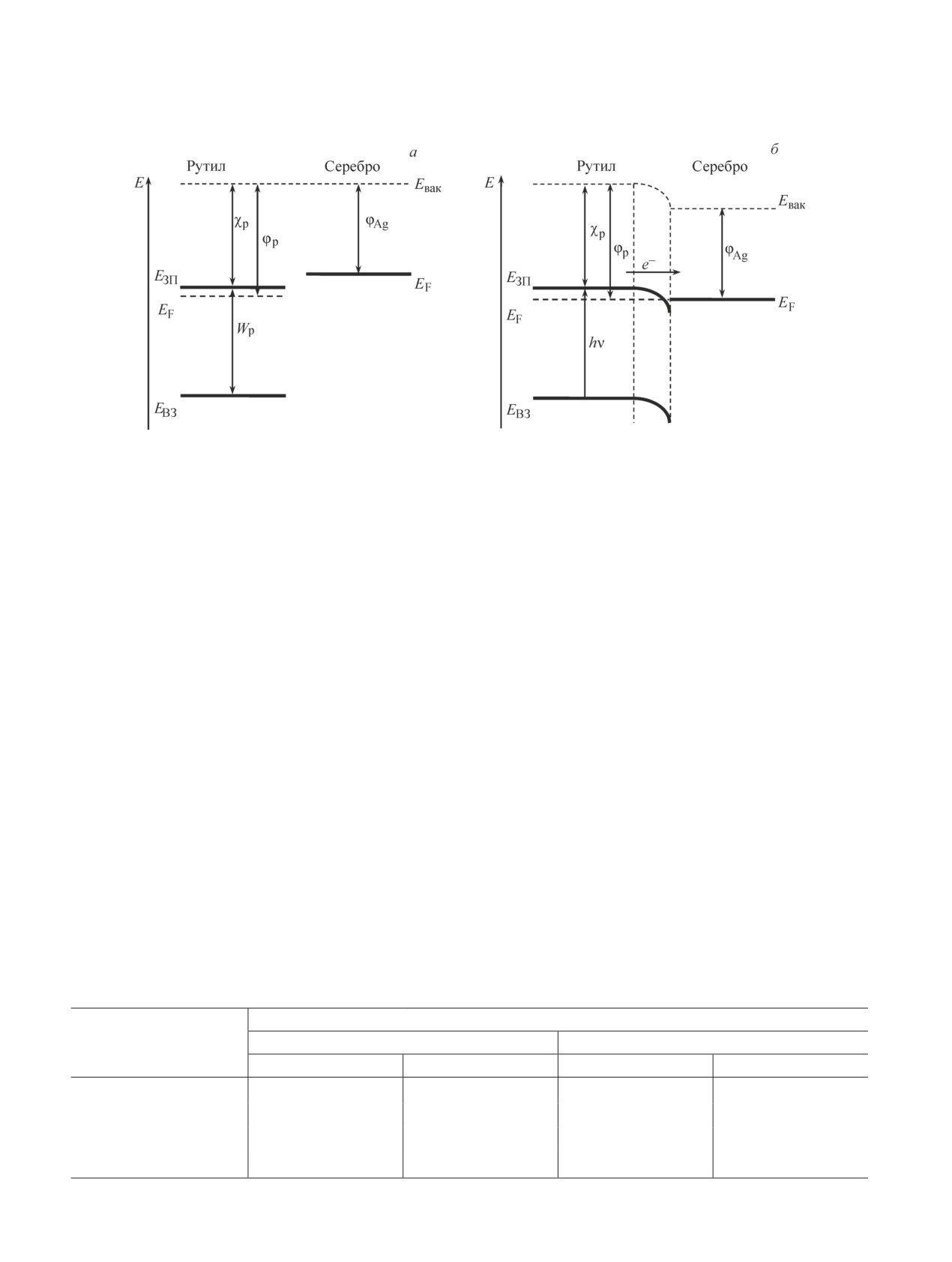
Рис. 5. Схема энергетических уровней фаз анатаз/рутил до (а) и после (б) соприкосновения и установления термо-
динамического равновесия.
(4.8 эВ) [19] и близость энергий Ферми к краю зоны
установлении термодинамического равновесия часть
проводимости [20] определяют положение зоны про-
электронов из серебра переходит в рутил (работа
водимости анатаза на 0.3 эВ глубже, чем у рутила.
выхода серебра составляет 4.26 эВ [19]). Результатом
В результате контакта частиц разных фаз происходит
процесса является повышение потенциального барь-
выравнивание уровней Ферми (рис. 5, б) и возник-
ера до ~0.54 эВ, который должна преодолеть дыр-
новение потенциального барьера в ~0.17 эВ, кото-
ка, переходя из металла в рутил. В этом случае на-
рый должна преодолеть дырка, переходя из рутила
ряду с переносом заряда в оксиде титана(IV) при
в анатаз. Вследствие этого становится возможным
УФ-возбуждении следует допустить возможность
разделение зарядов и повышение каталитической
«перетекания» электронов через межграничную по-
активности гетерофазных композитов по сравнению
верхность на серебро. Следует ожидать, что в случае
с чистыми анатазом и рутилом. Действительно, в
композитов TiO2(анатаз)/Ag потенциальный барьер
условиях описанного эксперимента при температу-
будет выше (~0.84 эВ). Однако наличие ионов серебра
рах отжига ниже 750°С в образцах преобладает фаза
промотирует рутилизацию [16], в результате которой
анатаза, а выше 800°С — рутила (табл. 1), демонстри-
окружение частиц серебра составляет рутил.
рующая меньшую каталитическую активность.
Немаловажным фактором, влияющим на фотока-
Близкая по смыслу схема может быть предложена
талитические свойства, является размер наночастиц
для объяснения активности системы TiO2/Ag (рис. 6).
серебра. Сопоставление данных табл. 3 и рис. 3 по-
В результате контакта частиц серебра и рутила при
зволило установить оптимальный размер частиц,
Таблица 3
Средний размер частиц анатаза, рутила и серебра в немодифицированном и модифицированном серебром оксиде
титана(IV)
Средний размер частиц, нм
Температура отжига, °С
TiO2
TiO2/Ag
анатаз
рутил
анатаз
рутил
серебро
500
16.0
—
15.4
19.8
11.5
650
18.7
22.3
16.1
19.7
16.5
750
19.7
23.0
17.6
20.0
19.2
850
21.5
30.2
22.2
23.0
22.0
950
18.0
38.0
18.5
29.5
22.5
Фотокаталитические свойства материалов на основе оксида титана(IV) и наночастиц серебра
287
Рис. 6. Схема энергетических уровней фаз рутил/серебро до (а) и после (б) соприкосновения и установления тер-
модинамического равновесия.
который в условиях эксперимента составил 19 ± 3 нм
— при рН > 5 скорость фотодеградации метило-
(отжиг при 650-950°С). Частицы меньшего размера
вого оранжевого в присутствии TiO2 выше в 1.5-2.0,
(11.5 ± 2 нм, отжиг при 500°С) влияют на каталити-
а метиленового синего — в 1.25 раза.
ческие свойства в меньшей степени, что может быть
Подобные экспериментальные наблюдения можно
обусловлено меньшей длиной пробега захватываемых
объяснить с точки зрения возможности сдвига уров-
частицей электронов и последующей рекомбинацией
ня Ферми в TiO2 при варьировании рН. Повышение
зарядов.
концентрации протонов в системе приводит к пони-
Установлено, что фотокаталитическая активность
жению энергии уровня Ферми анатаза и (или) рутила.
образцов TiO2 и TiO2/Ag зависит от pH растворов
В случае контакта фаз анатаз/рутил (рис. 5) подобный
красителей. При этом выявлены следующие законо-
сдвиг EF наблюдается в обеих фазах, поэтому величи-
мерности (табл. 4):
на потенциального барьера изменяется незначитель-
— с ростом рН скорость обесцвечивания раство-
но. При межфазном контакте рутил/серебро (рис. 6)
ров метилового оранжевого и метиленового синего
возникающее контактное электрическое поле вызы-
уменьшается при использовании как модифициро-
вает усиление изгиба краев зоны проводимости и
ванных серебром, так и чистых TiO2 катализаторов;
валентной зоны рутила по сравнению с наблюдаемой
— при рН < 5 активность TiO2/Ag превышает в
в нейтральной среде. Результатом процесса являет-
1.5-2.0 раза таковую для TiO2 при фотодеградации
ся повышение потенциального барьера (>0.54 эВ),
метилового оранжевого и в 2.0-2.5 раза в случае ме-
величина которого будет определяться характерным
тиленового синего;
для данного рН значением работы выхода рутила
Таблица 4
Зависимость относительной скорости фоторазложения метилового оранжевого и метиленового синего
от рН среды
Температура отжига образцов TiO2 и TiO2/Ag 650°С
Относительная скорость фоторазложения
рН
метиловый оранжевый
метиленовый синий
TiO2
TiO2/Ag
TiO2
TiO2/Ag
3.6
8.70
16.8
0.012
0.025
4.6
1.40
3.00
—
—
7
0.07
0.03
0.007
0.005
10
0.01
0.004
—
—
288
Вахрушев А. Ю. и др.
(∆ = φр - φAg) и увеличиваться при снижении рН.
Бойцова Татьяна Борисовна, д.х.н., проф., ORCID:
Таким образом, низкие значения рН способствуют бо-
лее полному разделению заряда в композитах TiO2/Ag
Горбунова Валентина Васильевна, к.т.н., доц.,
и как следствие повышению каталитических свойств
материалов по сравнению с чистыми TiO2 образцами.
Пак Вячеслав Николаевич, д.х.н., проф., ORCID:
При увеличении рН растворов красителей происхо-
дит сдвиг EF в область положительных значений.
В результате контакта частиц рутила и серебра элек-
Список литературы
троны перемещаются из рутила в серебро. При этом
металл заряжается отрицательно, а полупроводник —
[1] Ishikawa Y., Honda H., Sugahara Y. Preparation of
положительно. Для миграции фотогенерированных
titania from tetrakis (diethylamino)titanium via
hydrolysis // J. Sol-gel Sci. Technol. 2000. V. 19. N 1.
в TiO2 электронов из зоны проводимости в серебро
требуется преодолеть потенциальный барьер, вели-
[2] Jämting A. K., Bell J. M., Swain M. V., Wielunski L. S.,
чина которого будет увеличиваться с повышением
Clissold R. Measurement of the micro mechanical
рН. Наличие барьера в свою очередь способствует
properties of sol-gel TiO2 films // Thin Solid Films.
рекомбинации зарядов в фазе TiO2 и снижению фо-
1998. V. 332. N 1. P. 189-194.
токаталитической активности TiO2/Ag композитов.
[3] Natarajan C., Nogami G. Cathodic electrodeposition
of nanocrystalline titanium dioxide thin films // J.
Выводы
Electrochem. Soc. 1996. V. 143. N 5. P. 1547-1550.
Таким образом, фотокаталитическая активность
[4] Li G., Dimitrijevic N. M., Chen L., Nichols J. M.,
TiO2 материалов определяется совокупностью фак-
Rajh T., Gray K. A. The important role of tetrahedral
торов: соотношением кристаллических фаз, присут-
Ti4+ sites in the phase transformation and photocatalytic
ствием наночастиц серебра и рН среды поллютан-
activity of TiO2 nanocomposites // J. Am. Chem. Soc.
та. Применение диаграмм положения границ зон в
2008. V. 130. N 16. P. 5402-5403.
полупроводниках и металлах позволило объяснить
наблюдаемые эффекты и использовать полученные
[5] Baiju K. V., Zachariah A., Shukla S., Biju S.,
представления для прогнозирования каталитической
Reddy M. L. P., Warrier K. G. K. Correlating
активности и конструирования гетерофазных ката-
photoluminescence and photocatalytic activity of
лизаторов.
mixed-phase nanocrystalline titania // Catal. Lett. 2009.
V. 130. N 1-2. P. 130-136.
Благодарности
[6] Lv K., Yu J., Deng K., Li X., Li M. Effect of phase
Работа выполнена при финансовой поддержке
structures on the formation rate of hydroxyl radicals
on the surface of TiO2 // J. Phys. Chem. Solids. 2010.
конкурса грантов для студентов вузов, расположен-
V. 71. N 4. P 519-522.
ных на территории Санкт-Петербурга, аспирантов
вузов, отраслевых и академических институтов, рас-
[7] Ohno T., Tokieda K., Higashida S., Matsumura M.
положенных на территории Санкт-Петербурга (ПСП
Synergism between rutile and anatase TiO2 particles in
№ 18505).
photocatalytic oxidation of naphthalene // Appl. Catal.
A. 2003. V. 244. N 2. P. 383-391.
Конфликт интересов
[8] Scanlon D. O., Dunnill C. W. Buckeridge J.,
Авторы заявляют об отсутствии конфликта инте-
Shevlin S. A., Logsdail A. J., Woodley S. M.,
ресов, требующего раскрытия в данной статье.
Catlow C. R. A., Powell M. J., Palgrave R. G.,
Parkin I. P., Watson G. W., Keal T. W., Sherwood P.,
Walsh A., Sokol A. A. Band alignment of rutile and
Информация об авторах
anatase TiO2 // Nature Mater. 2013. V. 12. N 9. P.798-
Вахрушев Александр Юрьевич, ORCID: https://
[9] Kawahara T., Konishi Y., Tada H., Tohge N., Nishii J.,
orcid.org/0000-0001-7758-0216
Ito S. A patterned TiO2(Anatase)/TiO2(Rutile) bilayer-
Крайнов Дмитрий Сергеевич, ORCID: https://
type photocatalyst: Effect of the anatase/rutile junction
orcid.org/0000-0002-8420-6641
on the photocatalytic activity // Angew. Chem. Int.
Фотокаталитические свойства материалов на основе оксида титана(IV) и наночастиц серебра
289
Ed. 2002. V. 41. N 15. P. 2811-2813. https://
на(IV) и наночастиц серебра // ЖОХ. 2016. Т. 86.
doi.org/10.1002/1521-3757(20020802)114:15<
№ 4. С. 603-608 [Vakhrushev A. Y., Gorbunova V. V.,
2935::AID-ANGE2935>3.0.CO;2-6
Boitsova T. B., Stozharov V. M. Structure and
[10]
Liu S., Yan Y., Guan W., Li M., Jiang R. Role of n-n
photocatalytic properties of materials based on
anatase-rutile heterojunction in the photocatalysis of
titanium dioxide and silver nanoparticles // Russ. J.
mixed-phase titania // Asian J. Chem. 2013. V. 25. N 3.
Gen. Chem. 2016. V. 86. N 4. P. 792-797.
P. 1307-1310.
[16] Вахрушев А. Ю., Бойцова Т. Б., Горбунова В. В.,
[11]
Jakob M., Levanon H., Kamat P. V. Charge distribution
Стожаров В. М. Влияние добавок серебра на
between UV-irradiated TiO2 and gold nanoparticles:
структурно-фазовые свойства композитов TiO2/
Determination of shift in the Fermi level // Nano Lett.
Ag // Неорган. материалы. 2017. Т. 53. № 2. С. 156-
2003. V. 3. N 3. P. 353-358.
[Vakhrushev A. Y., Boitsova T. B., Gorbunova V. V.,
[12]
Binas V., Venieri D., Kotzias D., Kiriakidis G. Modified
Stozharov V. M. Effect of silver additions on the
TiO2 based photocatalysts for improved air and health
structural properties and phase composition of TiO2/
quality // J. Materiomics. 2017. V. 3. N 1. P. 3-16.
Ag composites // Inorg. Mater. 2017. V. 53. N 2.
P. 171-175.
[13]
Yu Z., Meng J., Xiao J., Li Y., Li Y. Cobalt sulfide
quantum dots modified TiO2 nanoparticles for efficient
[17] Langford J. I., Wilson A. J. C. Scherrer after
photocatalytic hydrogen evolution // Int. J. Hydrogen
sixty years: A survey and some new results in the
Energy. 2014. V. 39. N 28. P. 15387-15393. https://
determination of crystallite size // J. Appl. Cryst.
doi.org/10.1016/j.ijhydene.2014.07.165.
1978. V. 11. N 2. P. 102-113.
[14]
Вахрушев А. Ю., Горбунова В. В., Бойцова Т. Б.,
Стожаров В. М., Луканина Т. Л. Синтез мезо-
[18] Spurr R. A., Myers H. Quantitative analysis of anatase-
структурированного материала на основе TiO2 и
rutile mixtures with an X-ray diffractometer // Anal.
его функционализация наночастицами серебра //
Chem. 1957. V. 29. N 5. P. 760-762.
Неорган. материалы. 2013. Т. 49. № 12. С. 1311-
[19] Tsukamoto D., Shiro A., Shiraishi Y., Sugano Y.,
[Vakhrushev A. Y., Gorbunova V. V., Boitsova T. B.,
Ichikawa S., Tanaka S., Hirai T. Photocatalytic H2O2
Stozharov V. M., Lukanina T. L. Synthesis of
production from ethanol/O2 system using TiO2 loaded
mesostructured TiO2-based material and its
with Au-Ag bimetallic alloy nanoparticles //ACS
functionalization with silver nanoparticles // Inorg.
Catal. 2012. V. 2. N 4. P. 599-603.
Mater. V. 49. N 12. P. 1209-1212.
[20] Mi Y., Weng Y. Band alignment and controllable
[15]
Вахрушев А. Ю., Горбунова В. В., Бойцова Т. Б.,
electron migration between rutile and anatase TiO2
Стожаров В. М. Структура и фотокаталитиче-
// Sci. Reports. 2015. V. 5. Article N 11482. https://
ские свойства материалов на основе оксида тита-
doi.org/10.1038/srep11482