446
Билера И. В. и др.
Журнал прикладной химии. 2020. Т. 93. Вып. 3
УДК 544.45; 665.723; 661.961.622-977
ВЛИЯНИЕ ДОБАВКИ ВОДОРОДА
НА НЕКАТАЛИТИЧЕСКОЕ ПАРЦИАЛЬНОЕ ОКИСЛЕНИЕ КИСЛОРОДОМ
ПРИРОДНОГО ГАЗА В ПРОТОЧНОМ РЕАКТОРЕ
С ПОВЫШЕННОЙ ТЕПЛОНАПРЯЖЕННОСТЬЮ
© И. В. Билера*, Н. Н. Буравцев**, И. В. Россихин
Институт нефтехимического синтеза им. А. В. Топчиева РАН,
119991, г. Москва, Ленинский пр., д. 29
E-mail: *bilera@ips.ac.ru; **buravtsev@ips.ac.ru
Поступила в Редакцию 1 июля 2019 г.
После доработки 26 августа 2019 г..
Принята к публикации 14 декабря 2019 г.
В проточном реакторе с повышенной теплонапряженностью проведено исследование влияния добав-
ки водорода на парциальное окисление смеси природный газ/О2. Установлено, что добавка водорода
CH4/H2 = 3 к богатой смеси природный газ/О2 с коэффициентом избытка окислителя α = 0.34 при-
водит к увеличению выходов Н2, СО и отношения H2/CO, к снижению выходов СО2, Н2О, С2Н4, С2Н2
и величины ∆С. Показано, что добавка водорода CH4/H2 = 3 оказывает положительное влияние на
производство водорода при парциальном окислении смесей природный газ/О2.
Ключевые слова: турбулентное горение; природный газ; метан; водород; парциальное окисление;
синтез-газ; ацетилен; проточный реактор; теплонапряженность; сажеобразование; моделирование
DOI: 10.31857/S0044461820030172
Некаталитическое парциальное окисление угле-
ские трудности при их переработке [5]. Несомненное
водородного сырья, в том числе природного газа —
достоинство метода некаталитического парциального
один из промышленных способов получения син-
окисления состоит в принципиальной возможности
тез-газа, являющегося ключевым полупродуктом при
превращения природных газов и попутных нефтяных
химической переработке метансодержащих газов
газов в синтез-газ в одну стадию без предварительно-
природного происхождения [1-3]. Несмотря на боль-
го метанирования или выделения гомологов метана
шие усилия, предпринятые для развития химической
[6, 7]. Преимуществами технологии парциального
переработки углеводородных газов, существующие
окисления также являются энергетическая автоном-
технологии получения синтез-газа энерго- и ресур-
ность, отсутствие катализаторов, малое содержание
созатратны, металлоемки и экономически оправданы
СО2 и остаточного метана, снижение расходов на
только при очень больших масштабах производства
сжатие синтез-газа вследствие высокого давления в
[4, 5]. Поэтому актуальной задачей является иссле-
реакторе его получения, а недостатками — потреб-
дование новых вариантов получения синтез-газа с
ность в кислороде, высокая температура процесса,
целью поиска решений для создания более дешевой
недостаточное для ряда приложений отношение
технологии его производства. Особое значение имеет
Н2/СО и образование сажи [2, 8].
создание экономически эффективных малотоннаж-
Добавление водорода к метано-кислородным сме-
ных технологий конверсии углеводородного газового
сям может быть одним из вариантов интенсификации
сырья в жидкие химические продукты [5].
некаталитического парциального окисления и прео-
Углеводородная часть природных газов представ-
доления или по крайней мере смягчения отмеченных
лена метаном и его гомологами — алканами С2+, все
выше недостатков. Добавки водорода существенно
они обладают низкой, но различной реакционной спо-
улучшают характеристики воспламенения и горе-
собностью, что создает дополнительные технологиче-
ния углеводородов [9, 10]. В метано-воздушных [11,
Влияние добавки водорода на некаталитическое парциальное окисление кислородом природного газа...
447
12], метано-кислородных [13, 14] смесях и смесях
бутин-1, а также моноциклических ароматических
СН4/О2/газ-разбавитель [15] при различных значе-
углеводородов, таких как бензол и толуол.
ниях коэффициента избытка окислителя α добавки
При парциальном окислении метансодержащих
водорода расширяют пределы воспламенения, умень-
газов естественным следствием добавления водо-
шают время задержки воспламенения и увеличивают
рода к реагентам будет увеличение отношения
скорость горения. Для модельных смесей природного
Н2/СО в синтез-газе, что благоприятно для дальней-
газа добавки водорода также способствуют воспла-
ших каталитических синтезов, например, метанола.
менению и горению [16, 17], при этом в метановых
Более того, анализ экспериментальных данных ра-
смесях с высоким содержанием гомологов метана
боты [25] показывает, что при малых добавках Н2
(более 10%) добавки водорода незначительно снижа-
(CH4/H2 = 5) приращение Н2, образовавшегося при
ют время задержки воспламенения [18].
парциальном окислении метана, с учетом добавлен-
В ИХФ РАН было установлено, что в богатых сме-
ного Н2 может быть больше, чем без таких добавок.
сях углеводород-окислитель реакционная способ-
При дальнейшем увеличении водорода, добавляемого
ность смесей с водородом не всегда выше, чем в его
к реагентам (при CH4/H2 ≤ 2.5), этот эффект пропа-
отсутствие. Для модельных смесей СН4/С3Н8/Н2 =
дает.
= 80/20/5 и СН4/С3Н8/Н2 = 60/40/5 при окислении
Несмотря на достаточно большое число работ
кислородом (α = 0.30) добавки водорода в зависи-
по воспламенению и горению метановых смесей с
мости от условий оказывают на химическую ре-
добавками водорода, исследованию парциального
акцию разнонаправленное действие: при высоких
окисления метансодержащих смесей с добавками
температурах они ускоряют химическую реакцию,
водорода уделено недостаточно внимания. Как было
а при низких температурах (≈760-780 K и ниже)
отмечено авторами [26], наблюдается недостаток дан-
и повышенных давлениях тормозят ее [19, 20].
ных для смесей природного газа и природный газ/Н2
Аналогичный эффект был получен при расчетах по
при низких значениях коэффициента избытка окисли-
кинетической модели для стехиометрических смесей
теля (α < 0.5), т. е. в области соотношений реагентов,
н-гептан/Н2/воздух: при температурах менее 1050 K
пригодных для парциального окисления. Шевчук
добавки водорода увеличивают задержку самовос-
изучил влияние добавок водорода на термоокисли-
пламенения [21].
тельную конверсию метана в проточном реакторе
Добавки водорода к богатым метано-кислородным
при температурах 1200-1600°С [27]. Было показано,
и метано-воздушным смесям снижают выход газовой
что для богатых метано-кислородных смесей (α ≤ 0.3)
сажи [6, 19, 22-24]. Борисов и др. [6, 19, 22] показали,
добавки водорода CH4/H2 = 0.6-3 уменьшают пре-
что добавки 5% Н2 к богатым метано-кислородным
вращение метана в оксиды углерода и увеличивают
смесям практически полностью подавляют саже-
превращение метана в ацетилен и сумму ацетилен +
образование. Детальный механизм влияния водорода
+ этилен. Ли (C. Li) и др. [25] в проточном реакторе,
на образование сажи при окислительной конверсии
обогреваемом сверхвысокочастотным индукционным
метана до сих пор надежно не установлен. Полагают,
нагревателем, исследовали парциальное окисление
что наличие водорода в исходной смеси увеличивает
богатых смесей CH4/O2/N2 и CH4/H2/O2/N2. В серии
концентрацию атомов Н, способствующих сокраще-
экспериментов при температуре ≈1670 K и постоян-
нию времени существования повышенной концен-
ном отношении реагентов CH4/О2 = 1.11 добавляли
трации ацетилена, что приводит к замедлению по-
водород при отношении H2/О2 = 0-1.11, при этом
верхностного роста частиц сажи, несмотря на более
коэффициент избытка окислителя α изменялся от
быстрое образование зародышей сажи [14, 22]. Лиу
0.45 до 0.36. Было установлено, что добавки водо-
(F. Liu) и др. [23] показали, что подавление образова-
рода не оказывают влияния на степень превращения
ния сажи добавками водорода менее эффективно, чем
метана, а влияние на степень превращения кислорода
добавками гелия, и по сравнению с гелием добавки
наблюдается только при малых добавках CH4/H2 = 5.
водорода приводят к некоторому повышению темпе-
С увеличением добавки Н2 селективность образо-
ратуры и оказывают промотирующее влияние на об-
вания СО падает, ацетилена — растет, а этилена и
разование сажи за счет более высоких концентраций
СО2 практически остается без изменений. Качмарек
пирена и ацетилена. Ахмед (A. M. Ahmed) и др. [24]
(D. Kaczmarek) и др. [26] исследовали парциальное
исследовали влияние добавок водорода на химиче-
окисление метансодержащих смесей в проточном
скую структуру метановых пламен при атмосферном
реакторе при давлении 6 атм в интервале темпера-
давлении, в том числе на образование ненасыщенных
тур 473-973 K при трех значениях коэффициента
углеводородов, таких как ацетилен, пропин, аллен,
избытка окислителя α = 0.5, 0.1 и 0.05. Согласно
448
Билера И. В. и др.
полученным результатам, малая добавка водорода
зажигания и отсечки подачи дополнительного кисло-
(CH4/H2 = 45) не оказывает заметного влияния на
рода реализуется переходный режим горения II, после
степень превращения исходных алканов и на состав
него при самовоспламенении подаваемых реагентов
продуктов. Сопоставление результатов расчетов по
устанавливается стационарный режим горения III.
модели проточного реактора идеального вытеснения
Стационарный режим горения при отборе газовых
[28], выполненных с использованием кинетического
проб из камер смешения и сгорания с небольшим
механизма [29], показало удовлетворительное со-
понижением давлений в них обозначен IV.
ответствие полученным экспериментальным дан-
В работе использовали горючее (природный газ и
ным. Ранее [30] было показано, что расчеты по этой
смесь природного газа и водорода) и окислитель —
модели с использованием кинетических механизмов
технический кислород с добавкой неона (≈4 об%).
GRI-Mech 3.0 (включает соединения С1-С3) [31] и
В ходе работы перед огневыми экспериментами про-
USC-II (С1-С6) [32] показывают удовлетворительное
водили холодные продувки реактора с измерением
совпадение температур воспламенения и выхода ос-
по газовым часам объемного расхода (GV, нл·с-1)
новных продуктов при горении богатых метановых
смеси горючего с окислителем при нормальных
смесей.
условиях. Мольный расход рассчитывали по фор-
В наших работах для проведения парциального
муле F0 = GV/22.4 моль·c-1, массовый расход —
окисления метана и метансодержащих газов был
Gисхm = F0МВисх, где МВисх — молекулярный вес
использован проточный реактор с повышенной те-
исходной смеси реагентов. Газовые пробы исходной
плонапряженностью (РХПТ). Экспериментально
смеси из камеры смешения и смеси продуктов парци-
показано, что при парциальном окислении метан-
ального окисления из камеры сгорания отбирали ав-
содержащих газов достигается высокий выход Н2
томатически в вакуумированные пробоотборники при
и СО при практически полной конверсии исходных
достижении стационарного режима горения. Составы
реагентов, а также минимизировано образование са-
исходной смеси и смеси продуктов анализировали
жи [33-36]. Состав продуктов парциального окисле-
методом газовой хроматографии, также при опреде-
ния существенно зависит от значений коэффициента
лении коэффициента избытка окислителя α исходной
избытка окислителя α [33] и состава газового сырья
смеси использовали газоанализатор на метан Кедр
[36], дополнительного источника турбулентности в
07-01, диапазон 0-100% (Химавтоматика, г. Москва).
проточной камере сгорания [35] и ее теплонапряжен-
Наличие внутреннего стандарта (неона) в газо-
ности (WКC) [34].
образных пробах исходных реагентов и продуктов
Целью настоящей работы являлось эксперимен-
парциального окисления дает возможность рассчи-
тальное и модельное исследование влияния водорода
тать массовый дисбаланс атомов углерода (∆С), кис-
на парциальное окисление богатых смесей природ-
лорода (∆О), водорода (∆Н) и по этим величинам
ный газ/О2 в проточном реакторе с повышенной те-
плонапряженностью. С учетом положительного вли-
яния на увеличение выхода водорода [25] и ацетилена
[14, 25], а также на снижение образования сажи [22]
величина добавки водорода была выбрана CH4/H2 = 3.
Экспериментальная часть
Эксперименты проводили в проточном реакторе
с повышенной теплонапряженностью конструкции
ИНХС РАН. Подробное описание конструкции ре-
актора и порядок проведения экспериментов при его
использовании описаны в работах [33-35], внешний
вид реактора на огневом стенде ИНХС РАН показан
в [36].
В начале огневого опыта при включенной свече
зажигания и при подаче в камеру сгорания дополни-
тельного кислорода устанавливается нестационар-
ный режим турбулентного горения, обозначенный на
Рис. 1. Изменение во времени давления в камерах сме-
рис. 1 римской цифрой I. После выключения свечи
шения (1) и сгорания (2).
Влияние добавки водорода на некаталитическое парциальное окисление кислородом природного газа...
449
оценить в смеси продуктов массовые доли воды и
тах, при этом находили адиабатическую температуру
углеродсодержащих продуктов, не определенных в
газа в камере сгорания, время задержки самовоспла-
хроматографическом анализе. Подробнее методика
менения (τз.в, мс) и пребывания в камере сгорания
хроматографического анализа описана в работах [34,
(τп, мс), теплонапряженность камеры сгорания (WКС,
35].
МВт·м-3), а также выход основных продуктов сгора-
ния (viпрод, мол%).
Кинетическое моделирование
Результаты экспериментов
Как было отмечено в работах [33, 34, 36], благо-
и модельных расчетов
даря подаче стационарного потока смеси горючего и
окислителя, предварительно перемешанных в камере
Были проведены три серии экспериментов по изу-
смешения, в камере сгорания после турбулизатора
чению влияния добавки водорода на парциальное
наблюдается изотропное стационарное течение ис-
окисление природного газа в проточном реакторе с
ходных реагентов с мелкомасштабной турбулент-
повышенной теплонапряженностью.
ностью. В этом потоке после некоторой временной
Первая серия экспериментов. В первой серии
задержки происходит самовоспламенение реагентов и
сравнили составы продуктов парциального окисления
образуется стационарная зона турбулентного горения,
природного газа с добавкой и без добавки водорода,
в каждом поперечном сечении которой практически
полученных в сопоставимых условиях, в том числе
отсутствуют градиенты средних скоростей газовых
при одинаковых значениях объема камеры сгорания
молекул, температуры и концентраций компонентов
VKC = 68 cм3 и давления в ней РКС = 0.5 МПа (см. таб-
химически реагирующей смеси. Поэтому градиенты
лицу). В эксперименте с добавкой водорода мольное
этих параметров можно считать одномерными и рас-
отношение CH4/H2 = 2.98, массовый расход смеси
пределенными в основном вдоль оси цилиндрическо-
Gисхm = 4.57 г·с-1, коэффициент избытка окислителя
го газового потока. При таких характеристиках для
α = 0.34, а без добавки — Gисхm = 4.48 г·с-1 и α = 0.35
расчета модельного состава продуктов парциального
соответственно. При расчетах по модели проточного
окисления представляется возможным использовать
реактора идеального вытеснения состав смеси исход-
простейшую математическую модель проточного
ных реагентов νiисх, мольный расход F0 и давление
реактора идеального вытеснения [28]. Для расчетов
PKC были заданы такими же, как в экспериментах.
использовали модуль Reaction Engineering Lab из па-
В обоих экспериментах — с добавкой Н2 и без
кета программ COMSOL Multiphysics 3.5a,* модель
нее при сравнении экспериментальных и расчетных
plug-flow и кинетический механизм GRI-Mech.3.0
значений наблюдается удовлетворительное совпа-
[31].
дение выхода основных продуктов парциального
Для запуска модели plug-flow задавали началь-
окисления — H2, CO и H2O и остаточного содержа-
ные условия: F0 — мольный расход смеси горючего
ния исходного О2 и существенные различия в выходе
и окислителя, который определяли при холодных
СО2, C2H2, C2H4 и в остаточном содержании исход-
продувках реактора; мольный состав в виде моль-
ного СН4 (см. таблицу). Рассчитанные по модели
ных долей νiисх i-тых компонентов исходной смеси;
значения выхода ацетилена в присутствии добавки
Т0 — температуру газовой смеси на входе в каме-
Н2 (2.24 мол%) и в ее отсутствие (6.49 мол%) выше
ру сгорания; РКС — постоянное давление в камере
экспериментальных значений в 1.5 и 3.2 раза соот-
сгорания на стационарном режиме горения. Из-за
ветственно. Экспериментальные значения выходов
технических трудностей и погрешностей измерения
этилена в присутствии добавки Н2 и в ее отсутствие
термопарами температуры T0 ее значение находили
выше рассчитанных по модели в 6.5 и 18.6 раза,
подбором при моделировании стационарного режи-
СО2 — выше в 1.6 и 1.7 раза, остаточного содержа-
ма горения с самовоспламенением, так, чтобы при
ния СН4 выше в 3.1 и 1.9 раза соответственно. Для
достижении объема, равного экспериментальному
ацетилена эти расхождения могут быть вызваны от-
объему камеры сгорания VКC, расчетный выход во-
сутствием в кинетическом механизме GRI-Mech.3.0
дорода был равен экспериментальному его значению:
реакций убыли ацетилена, приводящих к образова-
νH2модели = νH2эксп. Модельные расчеты выполняли с
нию зародышей сажи, для этилена — отсутствием
такими же начальными условиями, как в эксперимен-
в кинетическом механизме GRI-Mech.3.0 алканов
С4+ и реакций образования этилена при их распаде,
для СО2 и СН4 — недостаточным перемешиванием
ing-module
исходных компонентов.
450
Билера И. В. и др.
Добавка водорода к смеси природный газ/О2 не
смеси природный газ/O2: 0.231 - 0.0 = 0.231 г·с-1.
привела к изменению степени превращения О2 и СН4,
Этот результат находится в соответствии с литера-
но повлияла на распределение продуктов. Этот ре-
турными данными [25], где при добавке водорода
зультат соответствует экспериментальным результа-
CH4/H2 = 5.0 был получен аналогичный эффект.
там [25]. Согласно полученным экспериментальным
Выяснение условий, при которых добавка водоро-
данным, основные различия в составах смесей про-
да оказывает положительное влияние на получение
дуктов парциального окисления природный газ/Н2/О2
водорода, должно быть предметом дополнительных
и природный газ/О2 состоят в увеличении выхода Н2
исследований.
и СО и снижении выхода СО2, С2Н4, С2Н2, а также
Снижение выхода ацетилена при парциальном
рассчитанных по балансу значений выхода Н2О и ∆С.
окислении природного газа кислородом вследствие
Расчеты по модели подтверждают эти результаты, в
добавки водорода также соответствует литературным
том числе для Н2О.
данным [14, 22]. Отмеченное в работе [27] отсут-
При добавке в исходную смесь природный газ/
ствие влияния добавки водорода CH4/H2 = 3.13 на
О2 водорода в мольном отношении CH4/H2 = 2.98 в
выход ацетилена (8.0 об%) происходило при более
полученном синтез-газе мольное отношение H2/CO
низких коэффициентах избытка окислителя (α = 0.325
повышается от 1.83 до 2.05, а отношение СО/СО2
и α = 0.306 без добавки и с добавкой Н2 соответствен-
увеличивается с 5.0 до 8.6. Более того, как следует
но). Существенным представляется снижение дис-
из данных таблицы, прирост массового содержания
баланса по углероду ΔC с 4.44 до 0.0% в результате
водорода в смеси продуктов парциального окисления
добавки водорода (см. таблицу), что свидетельствует
природный газ/H2/O2 с учетом добавленного водорода
о пренебрежимо малом образовании высокомолеку-
0.346 - 0.072 = 0.275 г·с-1, что на 19% выше, чем в
лярных углеродсодержащих продуктов, в том числе
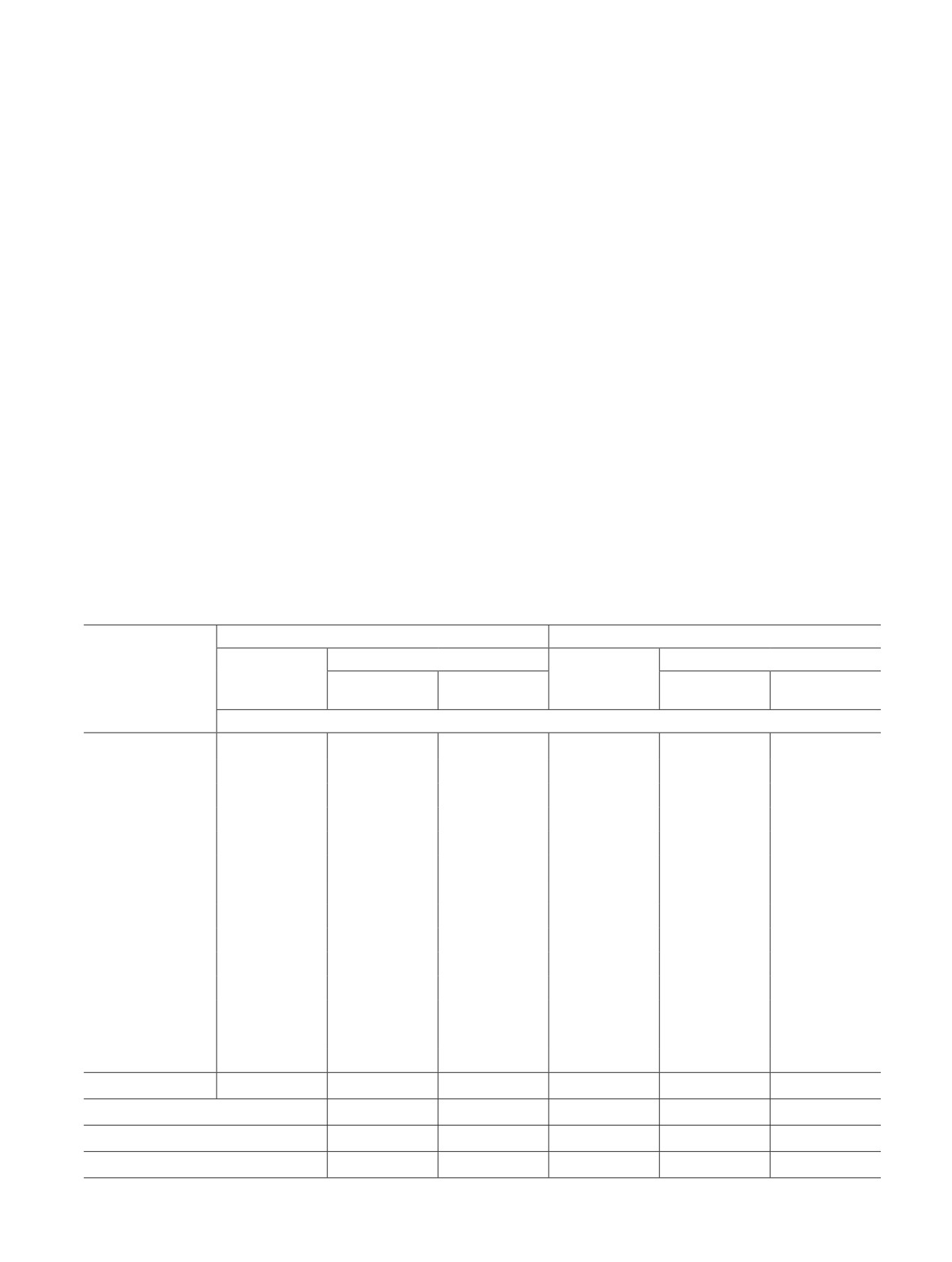
Выходы продуктов горения исходных смесей природный газ/О2 с добавкой Н2 и без нее
Природный газ/Н2/О2
Природный газ/О2
смесь продуктов
смесь продуктов
смесь исходных
смесь исходных
Компонент
реагентов
расчет
реагентов
расчет
эксперимент
эксперимент
по модели
по модели
мол%
Ne
1.08
0.72
0.72
1.11
0.74
0.74
H2
15.45
49.90
49.76
0.00
37.65
37.80
O2
35.87
0.05
0.00
41.27
0.00
0.00
CO
0.00
24.35
28.48
0.00
20.60
21.43
CO2
0.13
2.82
1.76
0.11
4.14
2.46
CH4
46.00
2.34
0.76
56.31
3.39
1.74
C2H6
1.02
0.01
0.00
0.78
0.03
0.00
C3H8
0.32
0.00
0.00
0.28
0.00
0.00
C2H4
0.00
0.26
0.04
0.01
0.93
0.05
C2H2
0.00
1.51
2.24
0.01
2.00
6.49
H2O
0.00
18.03
16.00
0.00
25.98
28.57
∆C
0.00
0.00
0.00
0.00
4.44
0.00
СН3
0.00
0.00
0.05
0.00
0.00
0.30
Н
0.00
0.00
0.16
0.00
0.00
0.37
Сумма
99.88
99.97
99.97
99.88
99.87
99.28
Мольное отношение Н2/СО
2.05
1.75
—
1.83
1.76
Мольное отношение СО/СО2
8.63
16.18
—
4.98
8.71
Конверсия YO2 и YСН4
0.998 и 0.924
1.00 и 0.975
—
1.00 и 0.909
1.00 и 0.953
Влияние добавки водорода на некаталитическое парциальное окисление кислородом природного газа...
451
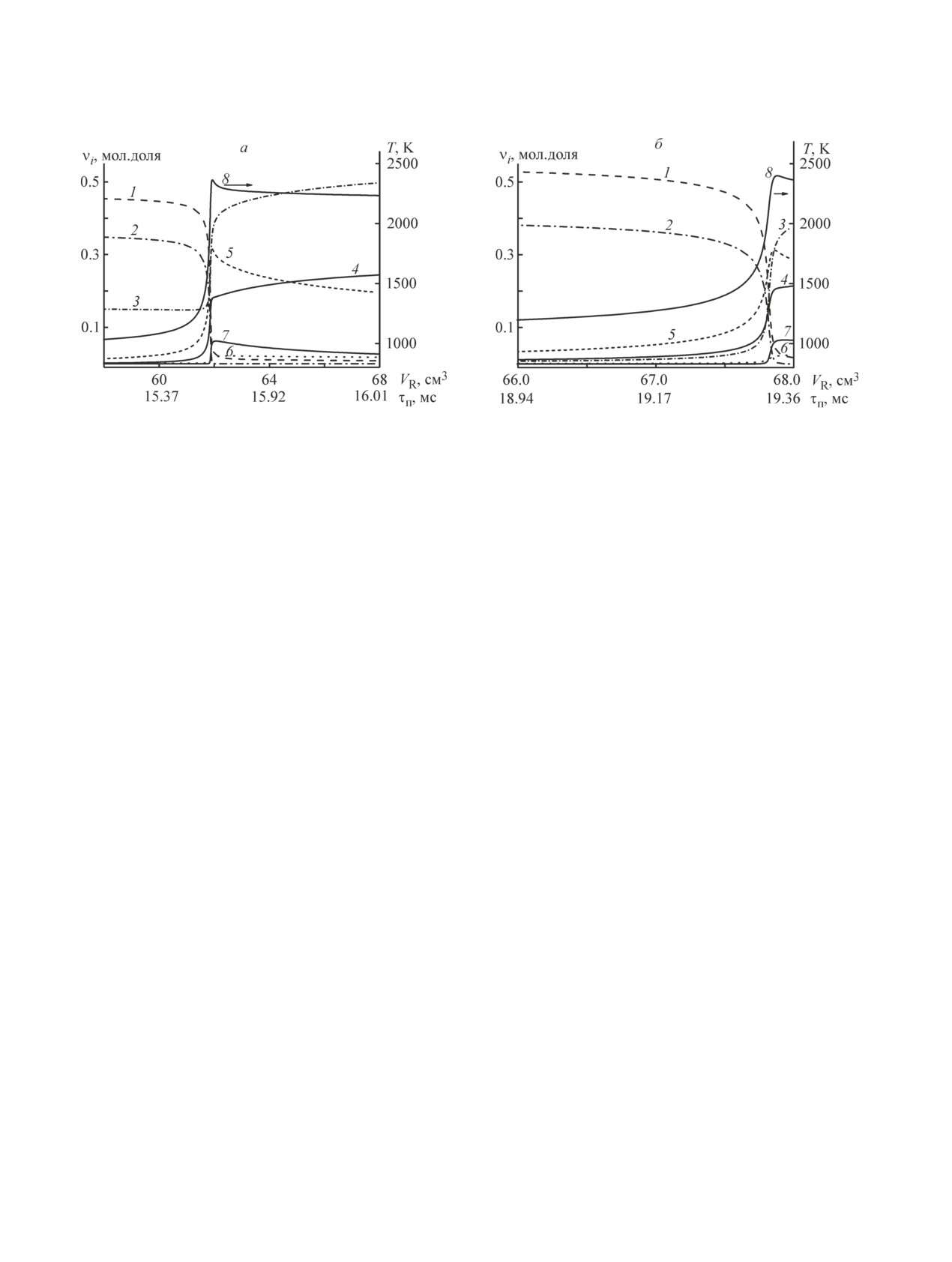
Рис. 2. Расчеты по математической модели проточного реактора идеального вытеснения в адиабатическом прибли-
жении: а — с добавкой Н2 (α = 0.34, CH4/H2 = 2.98, T0 = 963 K), б — без добавки Н2 (α = 0.35, T0 = 1062 K).
Компонент смеси: 1 — СН4, 2 — О2, 3 — Н2, 4 — СО, 5 — Н2О, 6 — СО2, 7 — С2Н2; 8 — температура потока Тпрод.
и сажи, при парциальном окислении богатых метано-
происходит резкое уменьшение содержания О2 до
водородных смесей. Этот результат также находится
практически нулевых значений, т. е. в самом начале
в соответствии с литературными данными [6, 19,
зоны пиролиза. В смеси без добавки Н2 выход аце-
22-24].
тилена остается без изменений до конца зоны пиро-
Согласно расчетам по модели реактора идеального
лиза (время пребывания в этой зоне всего 0.008 мс).
вытеснения, добавка водорода приводит к сокра-
В смеси с добавкой Н2 снижение содержания ацети-
щению времени задержки воспламенения богатой
лена начинается сразу по достижении максимального
смеси природный газ/О2 с τ = 19.3 (соответствует
значения и продолжается до конца зоны пиролиза,
VR = 67.86 см3, рис. 2, б), до τ = 15.8 мс (соответству-
что находится в соответствии с результатами кине-
ет VR = 61.8 см3, рис. 2, а). При этом температура
тических расчетов [14, 22]. Рассчитанные по модели
на входе в камеру сгорания Т0, при которой выпол-
проточного реактора идеального вытеснения значе-
няется равенство νH2модели = νH2эксп, для исходной
ния адиабатической температуры на выходе из каме-
смеси с добавкой Н2 на 92° меньше, чем без добавки,
ры сгорания в опыте с добавкой водорода (2233 K)
вследствие некоторого снижения относительного
ниже, чем без добавки водорода (2365 K), что мо-
содержания О2 в исходной смеси (α = 0.35 и 0.34 для
жет быть объяснено различиями в коэффициентах
смесей без добавки Н2 и с добавкой соответственно).
избытка окислителя исходных смесей (см. таблицу,
Резкое изменение содержания исходных компонен-
рис. 2).
тов и продуктов происходит в узкой области объема
Таким образом, экспериментальные данные
реактора, а следовательно, и за малый промежуток
и результаты расчета по модели показывают, что
времени. После этого содержание О2, согласно рас-
добавка водорода (CH4/H2 ≈ 3) в исходную смесь
четам, падает практически до нулевых значений, и
природный газ/О2 при его парциальном окислении
высокотемпературная конверсия протекает без уча-
приводит к уменьшению задержки воспламенения и
стия свободного кислорода, т. е. в режиме пиролиза.
повышению стабильности горения богатых смесей
Присутствие добавок водорода ускоряет воспламе-
метана, увеличивает выход Н2, СО при существен-
нение смеси и тем самым существенно расширяет
ном снижении образования высокомолекулярных
«зону пиролиза», от 0.14 (рис. 2, б) до примерно 6 см3
углеродсодержащих продуктов, в том числе сажи, и
(рис. 2, а).
повышает в получаемом синтез-газе мольное отно-
Согласно расчетам, в зоне пиролиза происходит
шение H2/CO до 2.05 и функционал f = (H2 - СО2)/
увеличение выхода Н2, СО и снижение выхода Н2О
(CO + СО2) до 1.73, что достаточно близко к значени-
при практически неизменном выходе СО2 (рис. 2).
ям этих величин, оптимальным для каталитического
Максимальный выход ацетилена как в случае до-
синтеза метанола [37].
бавки Н2, так и в ее отсутствие достигается в том
Вторая серия экспериментов. В промышленности
поперечном сечении проточного реактора, в котором
некаталитическое парциальное окисление метана в
452
Билера И. В. и др.
режиме горения используют с целью получения не
экспериментальный выход СО2 находится в интер-
только синтез-газа, но и ацетилена, при этом коэф-
вале 2.23-2.47 мол% (рис. 3, б, точки 5), оставаясь
фициент избытка окислителя α в исходной смеси
примерно на одну и ту же величину несколько выше
уменьшают до 0.28-0.29, максимальный выход аце-
рассчитанной по модели линии 5 (рис. 3, б).
тилена достигает 8-8.5 об% [38], см. также статью в
Экспериментальный выход С2Н2 (рис. 3, б, точ-
энциклопедии Ульмана.* Выше было показано, что
ки 6) при α = 0.30 имеет максимум, который не пре-
для метано-кислородных смесей с α = 0.34-0.35 до-
вышает 3.5 мол%, в то время как модельная кри-
бавка Н2 снижает выход ацетилена, а следовательно,
вая 6 выхода С2Н2 при α = 0.30 достигает значения
она будет изменять и значение коэффициента избытка
7.7 мол%. Как было отмечено выше, согласно рас-
окислителя α, при котором достигается максималь-
четам по модели, максимальный выход ацетилена в
ный выход ацетилена. В связи с этим была проведена
камере сгорания достигается в момент резкого сни-
вторая серия экспериментов и модельных расчетов,
жения содержания О2 до нулевых значений. В зоне
в которой исследовали влияние добавки водорода
пиролиза содержание ацетилена в смеси продуктов
на выход С2Н2 и целевых компонентов синтез-га-
остается без изменений по крайней мере в течение
за Н2 и СО, а также на величину ∆С в интервале
0.01 мс (рис. 2, б), а в дальнейшем оно снижается
значений α = 0.288-0.324 (рис. 3). Эксперименты и
(рис. 2, а). Поэтому при использовании добавок Н2
расчеты проводили при одинаковых значениях объ-
для получения максимального выхода С2Н2 при окис-
ема камеры сгорания V КC = 48 cм3 и давления в ней
лительном пиролизе в режиме горения представля-
РКС = 0.5 МПа, при одинаковых расходах природно-
ется целесообразным существенно сокращать зону
го газа, добавка водорода CH4/H2 = 2.98 моль/моль.
пиролиза, за которой необходимо осуществлять рез-
В этих опытах вследствие изменения расхода кис-
кое охлаждение смеси продуктов при закалке водой
лорода мольный расход исходной смеси горючего
или углеводородами, как в известных промышленных
с окислителем F0 изменялся в интервале значений
процессах получения ацетилена [38]. Кроме того,
0.218-0.227 моль·с-1.
необходимо оптимизировать величину добавки Н2
С увеличением α возрастает теплонапряженность
к смеси природный газ/О2. Следует отметить, что в
объема камеры сгорания (рис. 3, а, кривая 8), с ро-
наших экспериментах при окислительном пиролизе
стом которой должна уменьшаться масштабность
смесей природный газ/Н2/О2 при α = 0.34 значение
турбулентности в камере сгорания [35]. В результате
∆С = 0.0 (см. таблицу), но при уменьшении коэффи-
увеличивается выход Н2 и СО и уменьшается выход
циента избытка окислителя α от 0.324 до 0.288 вели-
Н2О. В этом интервале значений α в полученном
чина ∆С увеличилась от 3.0 до 7 мол% (рис. 3, б). При
синтез-газе значения мольного отношения Н2/СО
разборе реактора и камеры сгорания во внутреннем
увеличиваются до 2.49-2.65, а величины функциона-
канале был обнаружен тонкий матовый налет черно-
ла f — до 2.04-2.20, т. е. до значений, оптимальных
го цвета, который свидетельствует об образовании
для каталитического синтеза метанола [37]. При раз-
сажи при парциальном окислении смеси природный
личных значениях α также хорошее согласование экс-
газ/Н2/О2 в этом интервале коэффициентов избытка
периментальных выходов Н2, СO и остаточного СН4
окислителя α.
(точки) с рассчитанными по модели значениями (ли-
Третья серия экспериментов. В третьей серии
нии). Однако рассчитанные по модели значения вы-
экспериментов и модельных расчетов было проведе-
хода H2O превышают экспериментальные значения,
но исследование влияния одновременного изменения
это может быть связано с наличием систематической
времени пребывания реагентов и теплонапряженно-
погрешности при оценке H2O по эксперименталь-
сти камеры сгорания на выход основных продуктов
ному массовому дисбалансу ∆О. В исследованном
и величину ∆С при добавке водорода CH4/H2 = 2.98
интервале значений α адиабатические температу-
(рис. 4). Изменение значений теплонапряженности
ры продуктов Tпрод, рассчитанные по модели про-
в каждом опыте проводили при изменении объема
точного реактора идеального вытеснения (рис. 3,
камеры сгорания, для этого использовали вставки
б, кривая 9), увеличиваются от 1912 до 1997 K, а
различного объема.
С уменьшением объема камеры сгорания VКС воз-
* Pässler P., Hefner W., Buckl K., Meinass H., Meiswinkel
растают теплонапряженность WКC (рис. 4, а, кривая 8),
A., Wernicke H., Ebersberg G., Müller R., Bässler J., Behringer
хотя адиабатическая температура смеси продуктов
H., Mayer D. Acetylene // Ullmann′s Encyclopedia of Industrial
Тпрод (рис. 4, б, кривая 9) снижается. При изменении
Chemistry. Wiley-VCH Verlag GmbH & Co. KGaA, 2008.
объема камеры сгорания и экспериментальные, и
097.pub3
рассчитанные по модели значения выхода H2, СО,
Влияние добавки водорода на некаталитическое парциальное окисление кислородом природного газа...
453
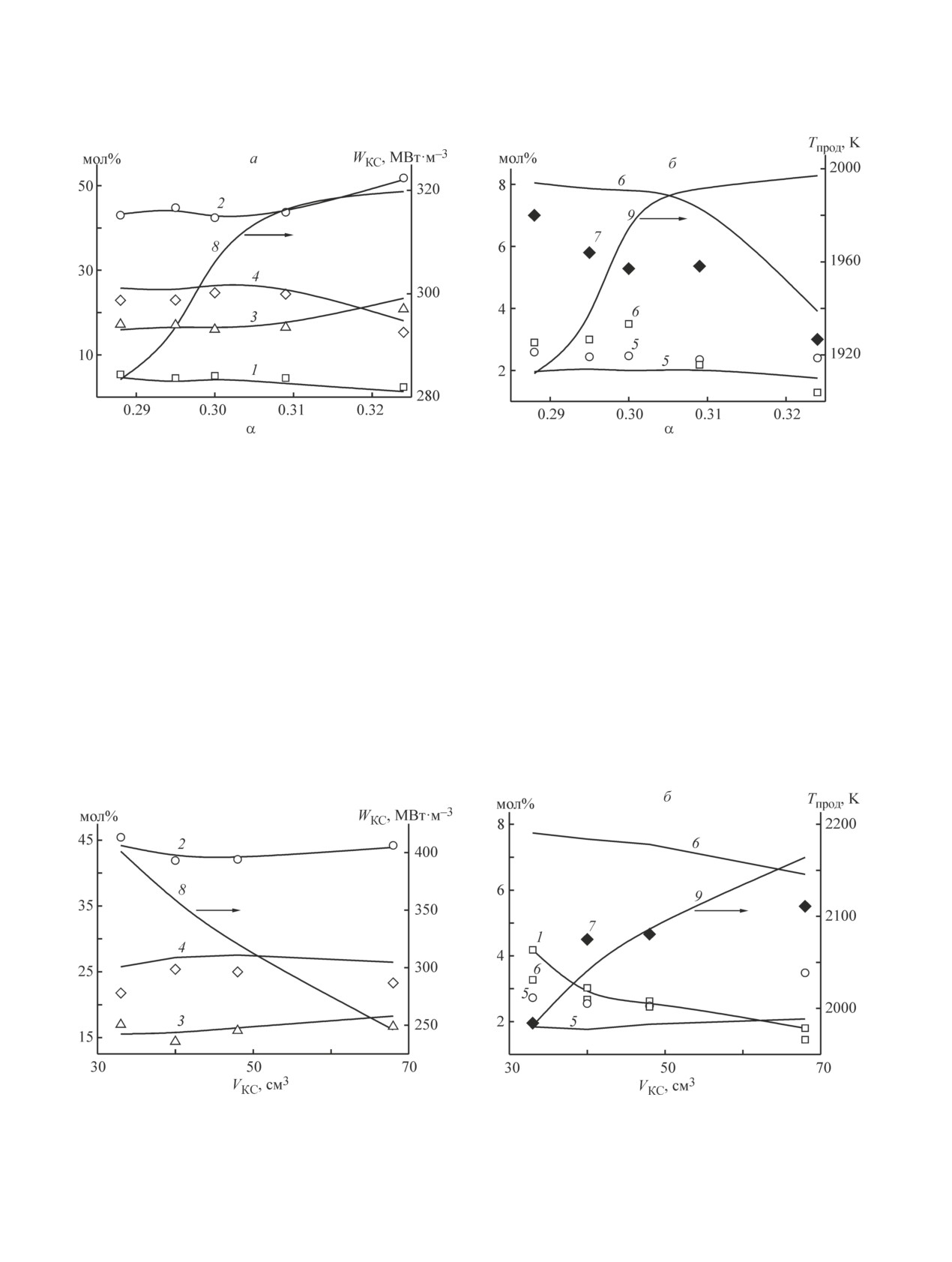
Рис. 3. Влияние коэффициента избытка окислителя α на парциальное окисление смеси природный газ/Н2/О2
(CH4/H2 = 2.98).
Компонент смеси (мол%): 1 — СН4, 2 — Н2, 3 — СО, 4 — Н2О, 5 — СО2, 6 — С2Н2; 7 — ∆С; 8 — теплонапряженность
камеры сгорания WКС; 9 — температура потока Тпрод.
Точки — эксперимент, линии — расчет по математической модели в адиабатическом приближении.
СО2, H2О практически не изменяются, при этом для
высокомолекулярных углеродсодержащих продук-
H2 и СО они удовлетворительно совпадают. Снижение
тов. С ростом теплонапряженности камеры сгорания
объема камеры сгорания приводит к увеличению
одновременно с увеличением выхода C2H2 снижа-
остаточного содержания СН4, а также к увеличению
ется массовый дисбаланс по углероду ∆С (рис. 4,
выхода C2H2. Наблюдается значительное расхождение
б, точки 7). Это свидетельствует о принципиальной
экспериментальных и рассчитанных по модели значе-
возможности заметного уменьшения превращения в
ний выхода C2H2, что может быть в первую очередь
высокомолекулярные углеродсодержащие продукты,
объяснено отсутствием закалки смеси продуктов при
в том числе сажу, при уменьшении объема камеры
проведении экспериментов, а также образованием
сгорания в процессе парциального окисления метана.
Рис. 4. Влияние объема камеры сгорания на парциальное окисление смеси природный газ/Н2/О2 (CH4/H2 = 2.98).
Компонент смеси (мол%): 1 — СН4, 2 — Н2, 3 — СО, 4 — Н2О, 5 — СО2, 6 — С2Н2; 7 — ∆С; 8 — теплонапряженность
камеры сгорания WКС; 9 — температура потока Тпрод.
Точки — эксперимент, линии — расчет по математической модели в адиабатическом приближении.
454
Билера И. В. и др.
Выводы
Nielsen J. R. Technologies for large-scale gas
conversion // Appl. Catal. A: General. 2001. V. 221.
При исследовании парциального окисления бога-
N 1-2. P. 379-387.
той метано-кислородной смеси в проточном реакторе
установлено, что добавка водорода CH4/H2 ≈ 3 при-
[2] Wilhelm D. J., Simbeck D. R., Karp A. D.,
водит к увеличению выхода Н2, СО и снижению вы-
Dickenson R. L. Syngas production for gas-to-liquids
хода СО2, Н2О, С2Н4, С2Н2, а также к существенному
applications: technologies, issues and outlook // Fuel
уменьшению выхода высокомолекулярных углеродсо-
Processing Technol. 2001. V. 71. N 1-3. P. 139-148.
держащих веществ, в том числе сажи. В результате в
получаемом синтез-газе возрастают значения мольно-
[3] Махлин В. А. Современные технологии получения
синтез-газа из природного и попутного газа // Хим.
го отношения H2/CO и функционала f = (H2 - СО2)/
пром-сть сегодня. 2010. № 3. С. 6-17.
(CO + СО2). При коэффициенте избытка окислителя
[4] Corke M. GTL technologies focus on lowering costs
α = 0.34 они принимают значения 2.05 и 1.73 соответ-
// Oil Gas J. 1998. V. 96. N 38. P. 71-77.
ственно, а в интервале значений α = 0.288-0.324 H2/
[5] Савченко В. И., Макарян И. А., Фокин И. Г., Се-
CO = 2.49-2.65 и f = 2.04-2.20, что оптимально для
дов И. В., Магомедов Р. Н., Липилин М. Г., Арутю-
каталитического синтеза метанола.
нов В. С. Малотоннажные GTL-процессы на базе
Экспериментально показано, что по сравнению с
прямого парциального окисления углеводород-
парциальным окислением богатой смеси природный
ных газов без стадии получения синтез-газа //
газ/О2 без добавки водорода добавка водорода CH4/
Нефтеперераб. и нефтехимия. 2013. № 8. С. 21-26.
H2 ≈ 3 в богатую смесь природный газ/О2 при α = 0.34
[6] Колбановский Ю. А., Билера И. В., Россихин И. В.,
приводит к приросту массового содержания водорода
Борисов А. А., Трошин К. Я. Одностадийная кон-
в смеси продуктов с учетом добавленного водорода.
версия попутного нефтяного и природного газа в
Уменьшение объема камеры сгорания и соот-
синтез-газ в процессах горения и самовоспламе-
ветственно увеличение ее теплонапряженности не
нения // Рос. хим. журн. 2010. Т. 54. № 5. С. 62-
69 [Kolbanovskii Yu. A., Bilera I. V., Rossikhin I. V.,
оказывает существенного влияния на выход Н2, СО,
Borisov A. A., Troshin K. Ya. Single-stage conversion
СО2, Н2О, приводит к увеличению остаточного со-
of associated petroleum gas and natural gas to syngas
держания CH4 и способствует увеличению выхода
in combustion and auto-ignition processes // Russ. J.
ацетилена при снижении выхода высокомолекуляр-
Gen. Chem. 2011. V. 81. N 12. P. 2594-2603.
ных углеродсодержащих веществ, в том числе сажи.
[7] Arutyunov V. S., Shmelev V. M., Sinev M. Yu.,
Финансирование работы
Shapovalova O. V. Syngas and hydrogen production
in a volumetric radiant burner // Chem. Eng. J. 2011.
Работа выполнена в рамках государственного за-
V. 176-177. P. 291-294.
дания Института нефтехимического синтеза РАН.
[8] Rostrup-Nielsen J. R. Catalysis and large-scale
Конфликт интересов
conversion of natural gas // Catal. Today. 1994. V. 21.
N 2-3. P. 257-267.
Авторы заявляют об отсутствии конфликта инте-
ресов, требующего раскрытия в данной статье.
[9] Tang C., Zhang Y., Huang Z. Progress in combustion
investigations of hydrogen enriched hydrocarbons //
Информация об авторах
Renew. Sustain. Energy Rev. 2014. V. 30. P. 195-216.
Билера Игорь Васильевич, к.х.н., ORCID: https://
[10] Emami S. D., Kasmani R. Md., Hamid M. D.,
orcid.org/0000-0001-6724-1907
Hassan C. R. C., Mokhtar K. M. Kinetic and
Буравцев Николай Николаевич, д.х.н., ORCID:
dynamic analysis of hydrogen-enrichment mixtures
in combustor systems — A review paper // Renew.
Россихин Игорь Владимирович, к.т.н., ORCID:
Sustain. Energy Rev. 2016. V. 62. P. 1072-1082.
[11] Yu G., Law C. K., Wu C. K. Laminar flame speeds of
hydrocarbon + air mixtures with hydrogen addition //
Список литературы
Combust. Flame. 1986. V. 63. N 3. P. 339-347. https://
[1] Aasberg-Petersen K., Bak Hansen J.-H. B.,
doi.org/10.1016/0010-2180(86)90003-9
Christensen T. S., Dybkjaer I., Christensen P. S.,
[12] Ilbas M., Crayford A. P., Yılmaz İ., Bowen P. J., Syred
Stub Nielsen C., Winter Madsen S. E. L., Rostrup-
N. Laminar-burning velocities of hydrogen-air and
Влияние добавки водорода на некаталитическое парциальное окисление кислородом природного газа...
455
hydrogen-methane-air mixtures: An experimental
сей попутных нефтяных газов с добавками водо-
study // Int. J. Hydrogen Energy. 2006. V. 31. N 12.
рода // Горение и взрыв. 2012. Т. 5. С. 33-39.
P. 1768-1779.
[20] Борисов А. А., Трошин К. Я., Скачков Г. И.,
Колбановский Ю. А., Билера И. В. Влияние добавок
[13]
Трошин К. Я., Борисов А. А., Рахметов А. Н.,
водорода на самовоспламенение богатых кисло-
Арутюнов В. С., Политенкова Г. Г. Скорость го-
родных метан-пропановых смесей // Хим. физика.
рения метанводородных смесей при повышенных
2014. Т. 33. № 12. С. 45-48.
давлениях и температурах // Хим. физика. 2013.
Т. 32. № 5. С. 76-87.
[Borisov A. A., Troshin K. Ya., Skachkov G. I.,
Kolbanovskii Yu. A., Bilera I. V. Effect of hydrogen
[Troshin K. Ya., Borisov A. A., Rakhmetov A. N.,
additives on the self-ignition of rich oxygen methane-
Arutyunov V. S., Politenkova G. G. Burning velocity
propane mixtures // Russ. J. Phys. Chem. B. 2014.
of methane-hydrogen mixtures at elevated pressures
V. 8. N 6. P. 866-869.
and temperatures // Russ. J. Phys. Chem. B. 2013. V. 7.
N 3. P. 290-301.
[21] Frolov S. M., Medvedev S. N., Basevich V. Ya.,
Frolov F. S. Self-ignition of hydrocarbon-hydrogen-
[14]
Борисов А. А., Борунова А. Б., Трошин К. Я.,
air mixtures // Int. J. Hydrogen Energy. 2013. V. 38.
Колбановский Ю. А., Билера И. В. Влияние доба-
N 10. P. 4177-4184.
вок водорода на кинетику образования и гибели
ацетилена при воспламенении и горении смесей
[22] Борисов А. А., Борунова А. Б., Трошин К. Я.,
метана с кислородом // Хим. физика. 2015. Т. 34.
Колбановский Ю. А., Билера И. В. О роли добавок
№ 4. С. 40-46.
водорода в формировании сажи при окислительной
конверсии метана // Горение и взрыв. 2014. Т. 7.
[Borisov A. A., Borunova A. B., Troshin K. Ya.,
С. 100-106.
Kolbanovskii Yu. A., Bilera I. V. Effect of hydrogen
[23] Liu F., Ai Y., Kong W. Effect of hydrogen and helium
additives on the kinetics of formation and destruction
addition to fuel on soot formation in an axisymmetric
of acetylene during the ignition and combustion of
coflow laminar methane/air diffusion flame // Int. J.
methane-oxygen mixtures // Russ. J. Phys. Chem. B.
Hydrogen Energy. 2014. V. 39. N 8. P. 3936-3946.
2015. V. 9. N 2. P. 261-267.
[24] Ahmed A. M., Mancarella S., Desgroux P., Gasnot L.,
[15]
Dagaut P., Nicolle A. Experimental and detailed
Pauwels J.-F., El Bakali A. Experimental and
kinetic modeling study of hydrogen-enriched natural
numerical study on rich methane/hydrogen/air laminar
gas blend oxidation over extended temperature and
premixed flames at atmospheric pressure: Effect of
equivalence ratio ranges // Proc. Combust. Inst. 2005.
hydrogen addition to fuel on soot gaseous precursors //
V. 30. N 2. P. 2631-2638.
Int. J. Hydrogen Energy. 2016. V. 41. N 16. P. 6929-
[16]
Herzler J., Naumann C. Shock-tube study of the
[25] Li C., Kuan B., Lee W. J., Burke N., Patel J. The
ignition of methane/ethane/hydrogen mixtures with
non-catalytic partial oxidation of methane in a flow
hydrogen contents from 0% to 100% at different
tube reactor using indirect induction heating — An
pressures // Proc. Combust. Inst. 2009. V. 32. N 1.
experimental and kinetic modelling study // Chem.
P. 213-220.
Eng. Sci. 2018. V. 187. P. 189-199.
[17]
Khan A. R., Ravi M.R., Ray A. Experimental and
[26] Kaczmarek D., Atakan B., Kasper T. Plug-flow reactor
chemical kinetic studies of the effect of H2 enrichment
study of the partial oxidation of methane and natural
on the laminar burning velocity and flame stability of
gas at ultra-rich conditions // Combust. Sci. Technol.
various multicomponent natural gas blends // Int. J.
2019. V. 191. N 9. P. 1571-1584.
Hydrogen Energy. 2019. V. 44. N 2. P. 1192-1212.
[27] Шевчук В. У. Окислительный пиролиз метана в
[18]
Cao S., Wang D., Wang T. Simulation of partial
присутствии водорода // Газовая пром-сть. 1957.
oxidation of natural gas with detailed chemistry:
№ 7. С. 32-37.
Influence of addition of H2, C2H6 and C3H8 // Chem.
[28] Harriott P. Chemical reactor design. New York; Basel:
Eng. Sci. 2010. V. 65. N 8. P. 2608-2618.
Marcel Dekker, 2003. P. 106-127.
[29] Burke U., Somers K. P., O′Toole P., Zinner C. M.,
[19]
Борисов А. А., Трошин К. Я., Колбановский Ю. А.,
Marquet N., Bourque G., Petersen E. L.,
Билера И. В. Самовоспламенение модельных сме-
Metcalfe W. K., Serinyel Z., Curran H. J. An ignition
456
Билера И. В. и др.
delay and kinetic modeling study of methane, dimethyl
при парциальном окислении метано-кислород-
ether, and their mixtures at high pressures // Combust.
ных смесей в режиме горения // ЖПХ. 2018. Т. 91.
Flame. 2015. V. 162. N 2. P. 315-330.
№ 10. С. 1404-1412.
[30] Köhler M., Oßwald P., Xu H., Kathrotia T., Hasse Ch.,
[Buravtsev N. N., Kolbanovskii Yu. A., Rossikhin I. V.,
Riedel U. Speciation data for fuel-rich methane oxy-
Bilera I. V. Effect of the calorific intensity of
combustion and reforming under prototypical partial
combustion chamber on production of synthesis gas
oxidation conditions // Chem. Eng. Sci. 2016. V. 139.
in partial oxidation of methane-oxygen mixtures in the
combustion mode // Russ. J. Appl. Chem. 2018. V. 91.
[31] Smith G. P., Golden D. M., Frenklach M., Mo-
N 10. P. 1588-1596.
riarty N. W., Eiteneer B., Goldenberg M., Bow-
man C. T., Hanson R. K., Song S., Gardiner Jr. W. C.,
[35]
Буравцев Н. Н., Колбановский Ю. А., Росси-
Lissianski V. V., Qin Z. W. GRI-Mech 3.0. URL:
хин И. В., Билера И. В. Влияние дополнительного
источника турбулентности в проточной камере сго-
щения: 05.07.2018).
рания на режим горения богатых метанокислород-
[32] Wang H., You X., Joshi A. V., Davis S. G., Laskin A.,
ных смесей // Хим. физика. 2019. Т. 38. № 3. С. 30-
Egolfopoulos F., Law C. K. USCMech Version II.
High-Temperature Combustion Reaction Model
[Buravtsev N. N., Kolbanovskii Yu. A., Rossikhin I. V.,
of H2/CO/C1-C4 Compounds. 2007. URL: http://
Bilera I. V. Effect of an additional turbulence source in
ignis.usc.edu/USC_Mech_II.htm (дата обращения:
a flow combustion chamber on the combustion mode
05.07.2018).
of rich methane-oxygen mixtures // Russ. J. Phys.
[33] Билера И. В., Буравцев Н. Н., Колбановский Ю. А.,
Chem. B. 2019. V. 13. N 2. P. 273-279.
Россихин И. В. Получение синтез-газа при горе-
нии метансодержащего сырья в проточном реак-
[36]
Колбановский Ю. А., Буравцев Н. Н., Билера И. В.,
торе с повышенной теплонапряженностью // Сб.
Россихин И. В., Борисов Ю. А. Конверсия биогаза
тр. «Технологическое горение» / Под общ. ред.
в синтез-газ в реакторе с высокой теплонапряжен-
С. М. Алдошина и М. И. Алымова. М.: РАН, 2018.
ностью // НефтеГазоХимия. 2015. № 1. С. 28-32.
Гл. 2. С. 35-61.
[37]
Караваев М. М., Леонов В. Е., Попов И. Г., Шепе-
лев Е. Т. // Технология синтетического метанола.
[34] Буравцев Н. Н., Колбановский Ю. А., Росси-
М.: Химия, 1984. С. 13.
хин И. В., Билера И. В. Влияние теплонапряжен-
[38]
Антонов В. Н., Лапидус А. С. // Производство аце-
ности камеры сгорания на получение синтез-газа
тилена. М.: Химия, 1970. С. 154-214.