Журнал прикладной химии. 2020. Т. 93. Вып. 4
КАТАЛИЗ
УДК 554.755.3.1.1.6.6.09.4.187.3
ОКИСЛИТЕЛЬНОЕ ДЕГИДРИРОВАНИЕ ЭТИЛБЕНЗОЛА В СТИРОЛ
НА ОТРАБОТАННОМ АЛЮМОХРОМОВОМ КАТАЛИЗАТОРЕ
© М. Т. Мамедова
Институт нефтехимических процессов им. Ю. Г. Мамедалиева НАН Азербайджана,
Az 1025, Азербайджан, г. Баку, пр. Ходжалы, д. 30
E-mail: memmedova-melahet@mail.ru
Поступила в Редакцию 21 июня 2019 г.
После доработки 5 ноября 2019 г.
Принята к публикации 14 декабря 2019 г.
Синтезированы катализаторы на основе отработанного промышленного алюмохромового катализа-
тора, используемого в дегидрировании углеводородов компанией SABIC, проведено модифицирование
этих катализаторов медью и карбонатом калия. Катализаторы испытаны в реакции окислительно-
го дегидрирования этилбензола в стирол. Установлено, что приготовленный и модифицированный
1 мас% Cu катализатор при превращении этилбензола в стирол в присутствии О2 проявляет актив-
ность 53% при селективности по стиролу 85%. Показано, что введение в реакционную зону диоксида
углерода приводит к возрастанию активности до 60-63%, а селективности до 89-91%. Изучена
стабильность функционирования промотированного медью катализатора и влияние на процесс
паров воды. Установлено, что в условиях, близких к промышленным, в пределах 100 ч наблюдается
стабильное превращение смеси (этилбензол:О2 = 9:1):Н2О = 4:1 с селективностью по стиролу не
ниже 90% при объемной скорости 2 ч-1 (по жидкому этилбензолу).
Ключевые слова: этилбензол; стирол; дегидрирование; окисление; кислород; медь
DOI: 10.31857/S0044461820040027
Каталитическое дегидрирование этилбензола в
две группы: высокотемпературные [2-5] и низко-
стирол является одним из важнейших промышлен-
температурные [6-8]. По-видимому, в первом случае
ных процессов. Однако высокая энергоемкость де-
превращение этилбензола в стирол на катализаторе
гидрирования этилбензола в стирол и как следствие
происходит за счет окисления водорода, образую-
низкая производительность промышленных устано-
щегося в результате дегидрирования этилбензола
вок, реализующих этот процесс, являются ограничи-
(окислительное дегидрирование), а во втором — не-
тельным фактором роста потребления стирола и сти-
посредственным окислением этилбензола в стирол с
мулируют поиск эффективных путей получения этого
выделением молекул воды (окисление).
продукта [1]. Одним из предполагаемых решений
Поиск подходящих окислителей также является
этой проблемы является замена обычного дегидри-
составной частью этих исследований. В качестве
рования этилбензола с получением стирола на окис-
окислителя были проверены в основном кислород
лительное. Особое внимание уделяется поиску более
воздуха [9] и диоксид углерода [10, 11].
активных и селективных катализаторов. В зависимо-
Принимая во внимание высокотемпературные
сти от механизма превращения этилбензола в стирол
условия функционирования установок дегидриро-
предполагаемые катализаторы можно разделить на
вания этилбензола в стирол, можно предположить,
483
484
Мамедова М. Т.
что подбором соответствующего полифункциональ-
этилбензола в стирол был использован отработанный
ного катализатора, обладающего дегидрирующими и
промышленный алюмохромовый катализатор, ис-
окислительными свойствами, можно интенсифици-
пользуемый в дегидрировании углеводородов фирмой
ровать процесс получения целевого продукта за счет
SABIC.
отмеченного выше окислительного дегидрирования
Предварительные исследования показали прак-
этилбензола в стирол. В связи с этим представляет
тическую неактивность этого отработанного катали-
интерес изучить воздействие кислорода воздуха, СО2
затора в целевом процессе. С целью удаления угле-
и их смеси на этот процесс в условиях, близких к
родистых отложений катализатор предварительно
функционированию отмеченных установок, в первую
подвергали окислительной обработке в токе воздуха
очередь с использованием известных промышленных
при 650-700°С (3 ч), затем температуру снижали
катализаторов.
до комнатной. Полученный таким образом образец
Создание подобного каталитического процесса
измельчали в агатовой ступке и при тщательном пе-
тесным образом связано с такими параметрами ка-
ремешивании обрабатывали концентрированным
тализатора, как продолжительность реакционного
раствором гидроксида калия (48 ч). В результате
функционирования и воспроизводимость активности
гранулы образца размягчались и осадок приобретал
и селективности катализатора после определенных
пастообразную консистенцию. Осадок фильтровали,
регенерационных обработок. Перевод получения
декантировали дистиллированной водой, оставляли
стирола из обычного высокоэнергоемкого процесса
обезвоживаться на воздухе (24 ч), а затем формовали
дегидрирования этилбензола на более высокопро-
продавливанием через фильеру диаметром 3 мм, су-
изводительное и малоэнергоемкое окислительное
шили на воздухе под электрической лампой накали-
дегидрирование делает вопросы стабильности и ре-
вания (24 ч), измельчали в цилиндрические гранулы
генеративности особенно актуальными. Превращение
высотой 5-6 мм, помещали в чашку и подвергали
этилбензола в стирол с участием воздуха, СО2 или их
сушке при 80°С (3 ч), 120°С (3 ч) и, ступенчато под-
смеси протекает с участием паров воды и предполага-
нимая температуру (100°С/1.5 ч), прокаливали при
ет образование Н2О, СО2 или их смеси в зависимости
700°С в течение 3 ч. Приготовленную таким образом
от используемого окислителя.
массу алюмохромового образца делили на три равные
Известно, что применяемые в промышленности
части. 1/3 часть образца обрабатывали раствором
алюмохромовые катализаторы обладают высокой
карбоната калия. Раствор после 24 ч выдержки выпа-
дегидрирующей и окислительной способностью.
ривали, а затем подвергали по описанной выше мето-
Введение в такую систему меди (Cu) может позво-
дике сушке и прокалке. Содержание K2СО3 в готовом
лить также активировать процесс паровой конверсии
катализаторе составляло 15% (катализатор К-1).
монооксида углерода.
Оставшиеся 2/3 части образца помещали в фар-
Цель работы — изучение окислительного дегидри-
форовые чашки и заливали раствором нитрата ме-
рования этилбензола в стирол в присутствии воздуха,
ди с заранее заданной различной концентрацией.
СО2 и их смеси на алюмохромовых катализаторах.
Образцы выдерживали в растворах в течение 48 ч,
а затем выпаривали. Высушенные образцы обра-
батывали насыщенным раствором гидрокарбоната
Экспериментальная часть
натрия, декантировали дистиллированной водой, су-
В качестве исходного материала для приготовле-
шили при 80°С (3 ч) и 120°С (3 ч). Далее образцы
ния катализатора окислительного дегидрирования
помещали в реактор и подвергали восстановлению в
Таблица 1
Состав* и текстурные характеристики синтезированных и использованных в окислительном дегидрировании
этилбензола в стирол алюмохромовых катализаторов
Атомное соотношение
K2O (промотор),
Cu (модификатор),
Удельная поверхность,
Объем пор,
Образец
Al:Cr
мас%
мас%
м2·г-1
см3·г-1
К-1
2:1
9.78
—
69
0.27
К-2
2:1
9.78
1.0
65
0.26
К-3
2:1
9.78
1.5
63
0.24
* Содержание железа в составе катализаторов не превышает 0.02 мас%.
Окислительное дегидрирование этилбензола в стирол на отработанном алюмохромовом катализаторе
485
токе водорода при 185°С. Линейная скорость подачи
лительной обработкой катализатора. Перед проведе-
водорода в реактор составляла 20 см3·мин-1. Процесс
нием опытов установку продували инертным газом
восстановления продолжали до полного прекраще-
(Не) 1 ч, затем катализатор обрабатывали воздухом
ния выделения паров воды в ловушке, помещенной
со скоростью подачи 4 л·ч-1 при 500°С. Количества
на выходе из реактора. Модифицированные медью
выделившихся Н2О и СО2 определяли как гравиме-
образцы обрабатывали K2CO3 по вышеуказанной
трически (путем их поглощения ангидроном и аска-
методике. Содержание меди в модифицированных
ридом, помещенными в соответствующие капсулы, c
образцах составляло 1 и 1.5 мас% от массы исходных
последующим взвешиванием этих ампул), так и непо-
катализаторов (катализаторы К-2 и К-3 соответствен-
средственно, анализом образовавшихся углеродистых
но), содержание промотора K2СО3 в обоих катализа-
отложений с применением элементного анализатора
торах — 15 мас% (табл. 1).
фирмы TruSpec Micro. Во избежание ошибок воздух,
Удельную поверхность и объем пор определяли
входящий в реактор, также пропускали через трубки,
по адсорбции бензола и рассчитывали по уравнению
заполненные ангидроном и аскаридом.
Брунауэра-Эммета-Теллера.
Окислительное дегидрирование этилбензола изу-
Обсуждение результатов
чали в каталитической установке проточного типа,
снабженной кварцевым адиабатическим реактором с
Как уже отмечалось выше, отработанный алю-
загрузкой катализатора 3-10 см3.
мохромовый катализатор неактивен в превращении
Перед проведением экспериментов катализаторы
этилбензола в стирол. Последующие окислительные
подвергали стандартной обработке в токе воздуха
и восстановительные обработки этого катализатора
(20 см3·мм-1) с увеличением температуры реактора
также не оказали на него активирующего воздей-
до 650°С. При этой температуре образцы выдержи-
ствия.
вали в течение 1 ч. Далее температуру снижали до
Отработанный катализатор приобрел активность
600°С, затем в реактор подавали этилбензол с объ-
в изучаемой реакции лишь после проведения опи-
емной скоростью 2 ч-1 (по жидкости) и воздух со
санного выше синтеза. В присутствии азота катали-
скоростью 25 cм3·мин-1. Дозирование этилбензола
заторы К-1, К-2 и К-3 обладают примерно близкими
осуществляли через испаритель-смеситель, в кото-
значениями активности и селективности по целе-
рый поступал также воздух и происходило смешение
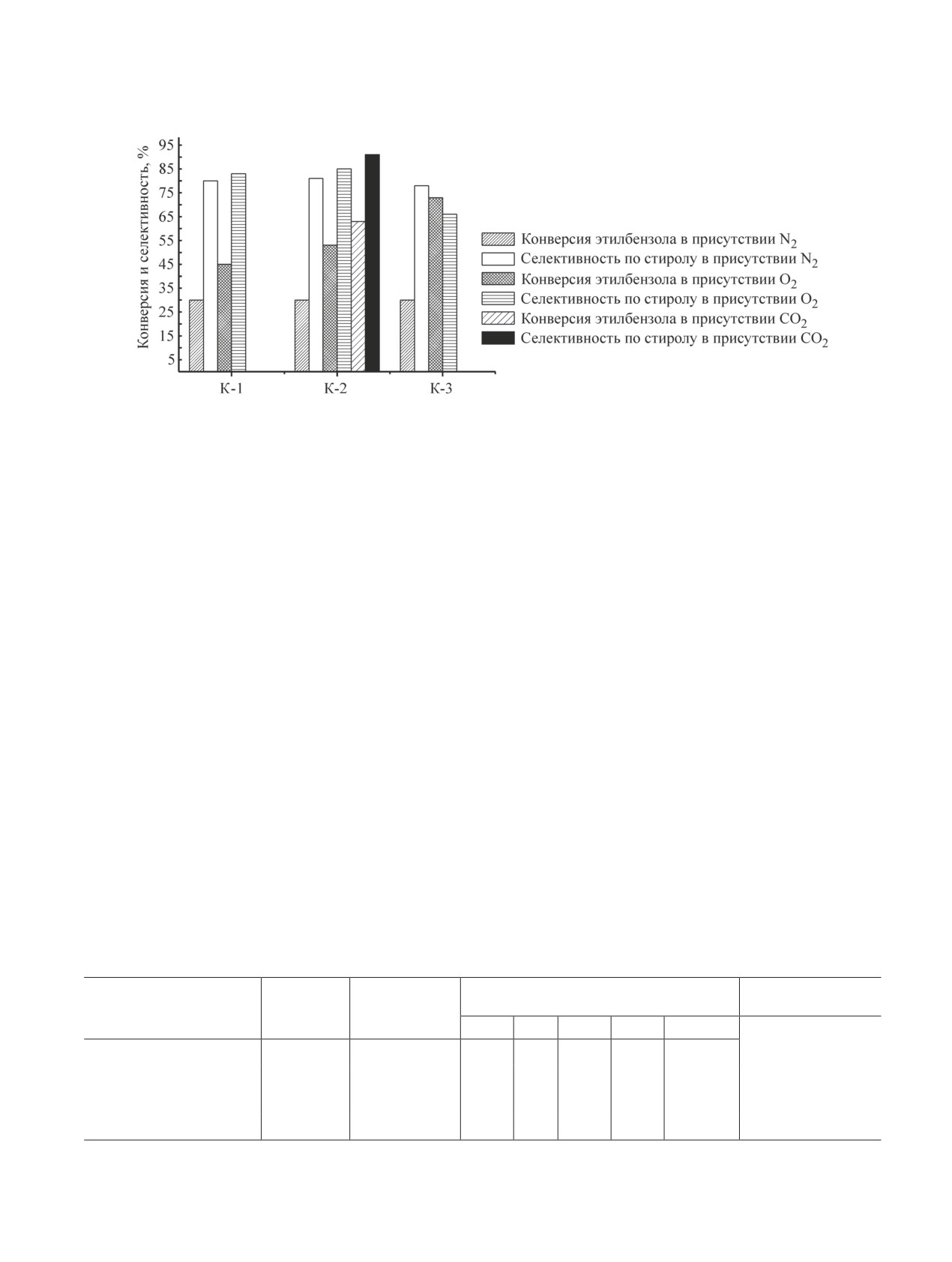
вому продукту (рис. 1). В присутствии кислорода
реактантов. Следует отметить, что испаритель-смеси-
воздуха конверсия этилбензола на К-1 повышается
тель выполнял также функции подогревателя, пройдя
на 15%, достигая 45% при селективности по сти-
через который, реактанты поступали в реактор с тем-
ролу 83%. Конверсия этилбензола на К-2 повыша-
пературой 475-500°С.
ется до 53% при селективности 85%. Более высо-
Воздух, используемый в процессе реакции,
кая конверсия этилбензола (73%) наблюдается на
предварительно увлажнялся барботированием при
катализаторе К-3, но в этом случае селективность
температуре 70°С. В экспериментах по изучению
снижается на 17%, достигая 66%. Таким образом,
влияния диоксида углерода на окислительное де-
К-2 является оптимальным катализатором для этого
гидрирование этилбензола в стирол подачу CO2 в
процесса.
реактор осуществляли из газометра путем его вытес-
Введение диоксида углерода в процесс окис-
нения с определенной скоростью, регулируемой по-
лительного дегидрирования этилбензола в стирол
дачей раствора из мерной емкости (20-40 мл·мин-1).
оказывает существенное влияние на выход целево-
Диоксид углерода также поступал в испаритель-сме-
го продукта. Под воздействием CO2 активность ка-
ситель и далее в составе смеси поступал в реактор.
тализатора К-2 возрастает почти на 10% (рис. 1).
Соотношение этилбензол:CO2 регулировали в преде-
Важно отметить, что такое повышение активности
лах 2:4 (мольное).
сопровождается повышением селективности выхода
Стабильность функционирования катализатора
стирола до 89-91%. Изменение каталитической ак-
К-2 выясняли на примере превращения смеси (этил-
тивности и селективности может являться следствием
бензол:О2 = 9:1):Н2О = 4:1 (мольное) при атмосфер-
разбавления реактанта инертным разбавителем, т. е.
ном давлении, температуре 590-600°С и объемной
понижения парциального давления реактанта. Но
скорости подачи жидкости 2 ч-1. Продукты реакции
роль СО2 в этом процессе нельзя лимитировать толь-
анализировали хроматографическим методом.
ко этим фактором, так как снижение соотношения
Определение количеств углеродистых отложений,
этилбензол:CO2 от 2:1 до 4:1 (при постоянстве парци-
накапливающихся на катализаторах, проводили окис-
ального давления этилбензола) приводит к снижению
486
Мамедова М. Т.
Рис. 1. Влияние окислителей на превращение этилбензола на алюмохромовых катализаторах.
активности катализатора с 62-60 до 59-57%. В этом
версии этилбензола (на 6%) связано со снижением
случае селективность также снижается. Такое сниже-
парциального давления СО2, взаимодействующе-
ние параметров каталитического процесса, очевидно,
го с выделяющимся водородом (CO2 + H2
CO +
не может быть объяснено воздействием СО2 на про-
+ H2O). Вместе с тем высокая селективность по сти-
цесс в качестве разбавителя, а скорее всего свиде-
ролу, возможно, является результатом взаимодействия
тельствует о его окислительной роли в превращении
кислорода с образующимися молекулами монооксида
этилбензола в стирол [12]. Сравнительные данные
углерода.
(табл. 2) являются дополнительным подтверждени-
Окислительное дегидрирование этилбензола в
ем этому предположению. Дополнительный анализ
стирол сопровождается образованием молекул воды,
контактного газа указывает на обогащение послед-
поэтому представляет интерес рассмотреть влияние
него монооксидом углерода, концентрация которого
паров воды на активность и селективность синте-
примерно соответствует повышению концентрации
зированного катализатора конверсии этилбензола в
стирола при замене N2 на СО2.
стирол.
Нами показано, что в присутствии воздуха актив-
С ростом концентрации паров воды от нуля до
ность катализатора выше, чем в присутствии СО2, но
20% наблюдается повышение активности катали-
во втором случае селективность по целевому продук-
затора в конверсии этилбензола и выхода стирола,
ту выше на 22% (табл. 2). Сопоставление данных по
дальнейшее повышение содержания паров воды прак-
превращению этилбензола в стирол с использованием
тически не оказывает влияния на активность катали-
окислительной смеси СО2:воздух с аналогичными
затора в окислительном дегидрировании этилбензола
данными, полученными при использовании только
в стирол (табл. 3).
СО2 или только воздуха, показывает, что активность
Результаты исследования стабильности работы
катализатора снижается. Отмеченное снижение кон- К-2 в процессе окислительного дегидрирования этил-
Таблица 2
Влияние СО2, кислорода (воздуха) и их смеси на превращение этилбензола в стирол на катализаторе К-3
Конверсия
Углеродистые
Селективность
Углеводородный состав продуктов, мас%
Окислитель
этилбен-
отложения,* мас%
по стиролу, %
зола, %
СН4
С2
С6Н6
С7Н8
СО2-СО
Азот
28
80
0.9
2.0
5.0
3.5
0
СО2
46
88
0.3
0.7
2.2
2.9
1.96
0.84
Воздух
73
66
5.2
3.1
19.0
2.6
—
СО2:воздух = 8:15 (об.)
40
90
0.3
0.3
2.1
2.9
0.39
* Накопления углеродистых отложений в процессе выхода катализатора на стабильный режим работы (максимальная
активность).
Окислительное дегидрирование этилбензола в стирол на отработанном алюмохромовом катализаторе
487
Таблица 3
Влияние паров воды на конверсию этилбензола в стирол на катализаторе К-2
Мольное соотношение этилбензол:О2 = 5:1
Содержание Н2О, об%
Конверсия этилбензола, %
Выход стирола, мас%
0
24
17
10
46
40
20
57
49
30
59
50
бензола в стирол в присутствии паров воды представ-
(рис. 2) не способствует стабильной работе катализа-
лены на рис. 2 и 3. Наличие паров воды оказывает
тора и соответственно характеризуется невысокими
значительное влияние на стабильность катализатора.
выходами стирола.
Низкое содержание паров воды в реактанте (10%)
Учитывая, что в современных установках деги-
дрирования этилбензола в стирол реактант подается в
реактор в смеси с 20-30% парами воды, исследование
стабильности катализатора К-2 проводили с реакци-
онной смесью, содержащей 20% воды. Полученные
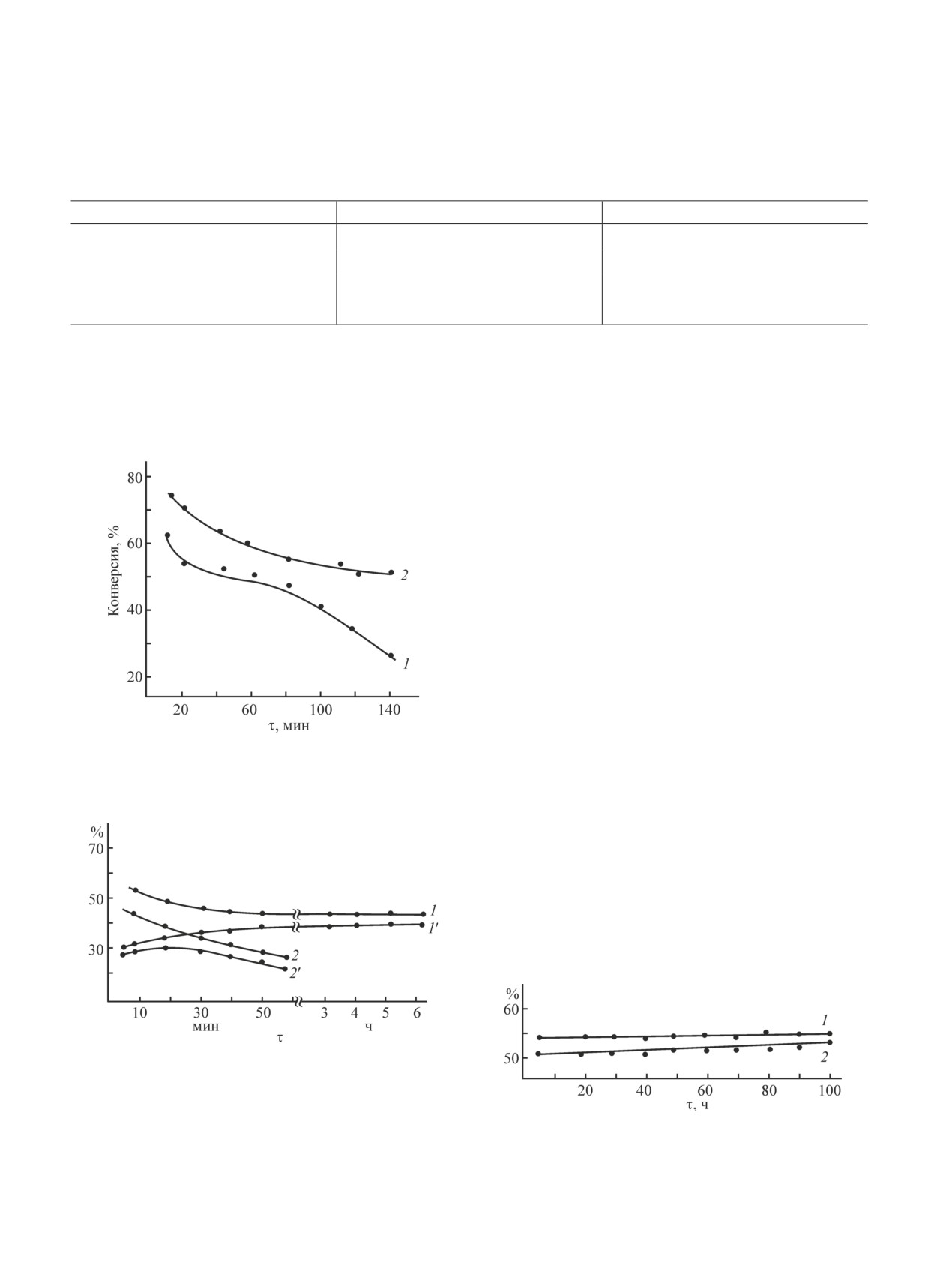
данные (рис. 3) показывают, что с 5-й до 50-й минуты
эксперимента катализатор характеризуется ростом
активности, но относительно низкой селективностью
по стиролу. В дальнейшем активность катализато-
ра стабилизируется на уровне 55%, а выход стиро-
ла — на 50-51%, что соответствует селективности
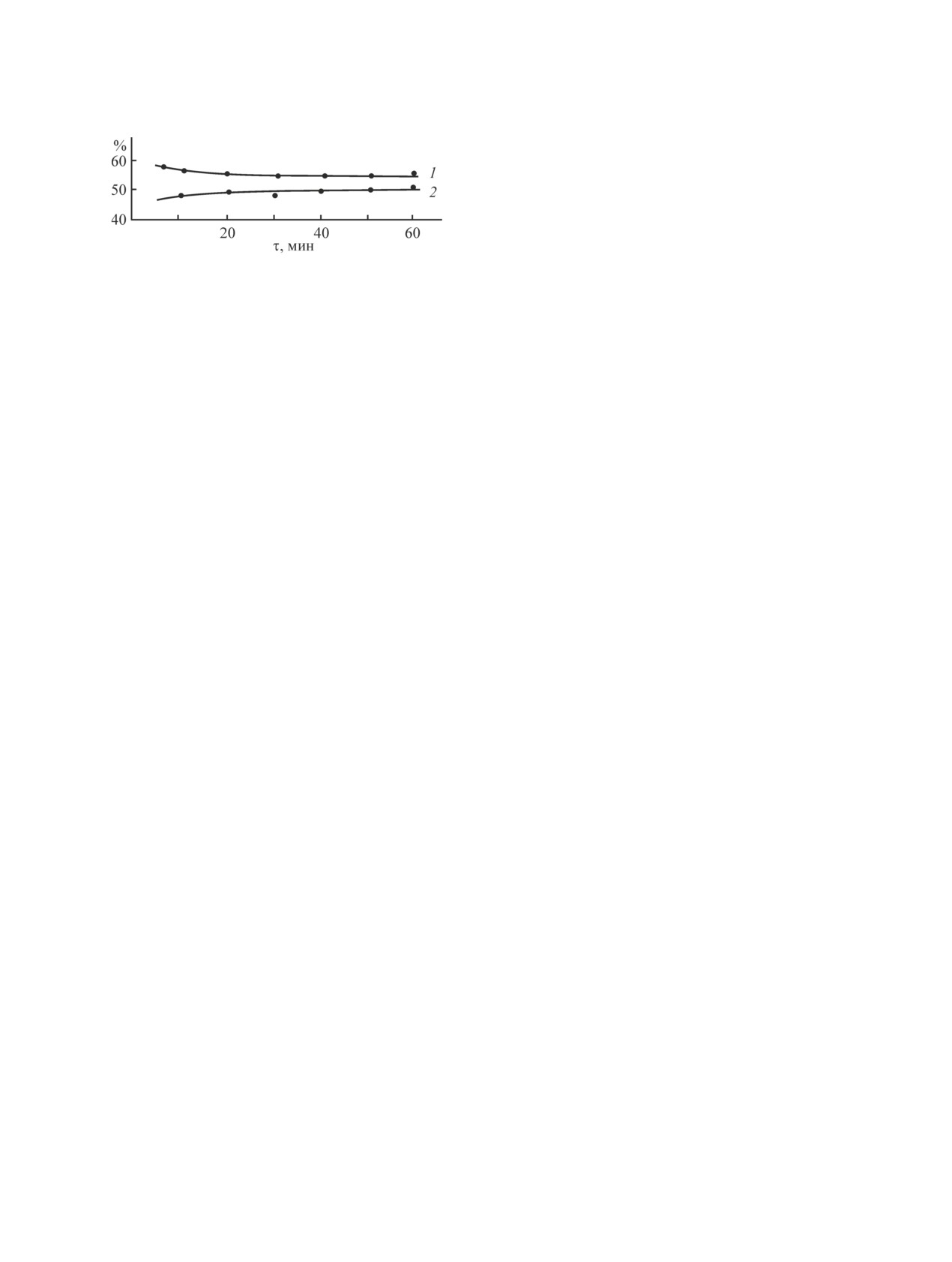
92-93%. Эти параметры процесса сохраняются на
протяжении 100 ч, причем в этом случае заметно
также возрастание селективности по целевому про-
дукту (рис. 4).
Таким образом, возрастание выхода стирола при
разбавлении исходного этилбензола парами воды
Рис. 2. Влияние продолжительности опыта на кон-
связано как со снижением парциального давления
версию этилбензола (1) селективность по стиролу (2)
паров реактанта, так и возможным предотвраще-
на катализаторе К-2.
нием нежелательного блокирования поверхности
катализатора прочно сорбирующимися продуктами
олигомеризации стирола.
Результаты многочисленных регенерационных об-
работок катализатора показывают полную воспроиз-
водимость данных (рис. 3) и подтверждают высокую
регенеративную устойчивость катализатора К-2.
Рис. 3. Влияние продолжительности эксперимента на
окислительное дегидрирование этилбензола в стирол
на катализаторе К-2.
1, 1′ — конверсия этилбензола и выход стирола при пре-
Рис. 4. Стабильность функционирования катализатора
вращении смеси (этилбензол:О2 = 5:1):Н2О = 4:1; 2, 2′ —
К-2 в дегидрировании этилбензола в стирол.
конверсия этилбензола и выход стирола при превращении
смеси этилбензол:О2 = 5:1.
1 — конверсия этилбензола, 2 — выход стирола.
488
Мамедова М. Т.
Благодарности
Благодарю д.х.н., проф., зав. лаб. «Гетерогенный
катализ» С. И. Абасова за ценные советы при подго-
товке этой статьи.
Конфликт интересов
Рис. 5. Влияние повторных запусков установки на ста-
бильность функционирования катализатора окисли-
Автор заявляет об отсутствии конфликта интере-
тельного дегидрирования этилбензола в стирол К-2
сов, требующего раскрытия в данной статье.
(этилбензол:О2 = 5:1):Н2О = 4:1.
1 — конверсия этилбензола, 2 — выход стирола.
Информация об авторах
Мамедова Малахат Таги кызы, к.х.н., доцент,
Эксперименты проводили в течение 5 ч, после
чего реактор охлаждался в токе азота. Повышение
температуры перед продолжением дальнейших экс-
Список литературы
периментов также проводилось в атмосфере азота.
[1] Cavani F., Trifiro F. Alternative processes for the
В результате подобных перерывов и повторных за-
production of styrene // Appl. Catal. A: General. 1995.
пусков реакции наблюдается незначительное повы-
V. 133. P.219-239.
шение общей конверсии этилбензола и снижение
выхода стирола в первые 20 мин работы катализатора
[2] Samuel P. D. M., Anderson L. P., Tiago P. B.,
(рис. 5), что может быть объяснено примесями кисло-
Antoninho V., Josue M. F., Alcineia C. O. Nanocasted
рода в используемом азоте. Вместе с тем эти данные
oxides for oxidative dehydrogenation of ethylbenzene
свидетельствуют об устойчивости каталитической
utilizing CO2 as soft oxidant // J. Mol. Catal. A:
системы К-2 в условиях окислительного дегидри-
Chemical. 2011. V. 348. P. 1-13.
рования этилбензола в стирол, которое по условиям
реализации близко к условиям реализации обычного
[3] Venkata R. B. G., Siva S. E., Suresh M., Ramudu P.,
дегидрирования. Следовательно, при прочих равных
Said P., David R. B., Seetha R. R. K. The advantage of
условиях применение К-2 и окислительное дегидри-
ceria loading over V2O5/Al2O3 catalyst for vapor phase
рование этилбензола в стирол позволяют поднять
oxidative dehydrogenation of ethylbenzene to styrene
производительность промышленных установок по-
using CO2 as a soft oxidant // Appl. Petrochem. Res.
2016. V. 6. P. 427-437.
лучения стирола из этилбензола почти в 4 раза бла-
годаря увеличению объемной скорости реализации
[4] Itika K., Gurram V. R. B., Jayesh T. B., Kamaraju S. R. R.,
процесса от 0.5 до 2.0 ч-1 при значительном сниже-
Bhari M. N. Development of stable MoO3/TiO2-
нии энергозатрат.
Al2O3 catalyst for oxidative dehydrogenation of
ethylbenzene to styrene using CO2 as soft oxidant //
J. CO2 Utilization. 2017. V. 18. P. 309-317. https://
Выводы
doi.org/10.1021/acscatal.5b01519
На основе промышленного отработанного алю-
[5] Benjaram M. R., Dae-Soo H., Nanzhe J., Park S. E.
мохромового катализатора можно синтезировать ка-
Dehydrogenation of ethylbenzene to styrene with
carbon dioxide over ZrO2-based composite oxide
тализатор с высокими показателями в реакции окис-
catalysts // Catal. Surv. Asia. 2008. V. 12. P. 56-69.
лительного дегидрирования этилбензола в стирол.
Модифицирование 1 мас% меди этого катализатора
[6] Badstube T., Papp H., Dziembaj R., Kustrowski P.
приводит к высокой селективности — 83-85% при
Screening of catalysts in the oxidative dehydrogenation
активности 53-50% в присутствии кислорода возду-
of ethylbenzene with carbon dioxide // Appl. Catal. A.
ха. Введение в реакционную смесь диоксида углерода
General. 2000. V. 204. P. 153-165.
повышает активность до 62-60%, а селективность —
до 89-91%. Наличие паров воды оказывает стабили-
[7] Nederlof Ch., Zarubina V., Ignacio V. M. C.,
зирующее воздействие на процесс окислительного
Erik H. J. H., Talebi H., Kapteijn F., Makkee M.
дегидрирования этилбензола в стирол с участием
Application of staged O2 feeding in the oxidative
катализатора К-2 благодаря эффективному выносу
dehydrogenation of ethylbenzene to styrene over Al2O3
продукта из реакционной зоны.
and P2O5/SiO2 catalysts // Appl. Catal. A: General.
Окислительное дегидрирование этилбензола в стирол на отработанном алюмохромовом катализаторе
489
presence of carbon dioxide over supported Fe2O3-
uuid:83b1d146-55e1-4b7b-8993-6cc88791f5bf
Cr2O3 mixed oxides catalysts // Asian J. Chem. 2014.
[8] Zarubina V., Talebi H., Nederlof Ch., Kapteijn F.,
V. 26. N 2. P. 504-508.
Makkee M., Cabrera I. M. On the stability of
conventional and nano-structured carbon-based
[11] Antonio J. R. Castro, Joao M. Soares, Josue M. Filho,
catalysts in the oxidative dehydrogenation of
Alcineia C. Oliveira, Adriana Campos, Edwin R. C.
ethylbenzene under industrially relevant conditions //
Milet. Oxidative dehydrogenation of ethylbenzene
Carbon. 2014. V. 77. P. 329-340.
with CO2 for styrene production over porous iron-
based catalysts // Fuel. 2013. V. 108. P. 740-748.
[9] Jie X., Lun-Cun W., Yong-Mei L., Yong C., He-
Yong H., Kang-Nian F. Mesostructured CeO2 as an
[12] Park M. S., Vislovskiy V. P., Chang J. S., Shul Y. G.,
effective catalyst for sturene synthesis by oxidative
Yoo J. S., Park S. E. Catalytic dehydrogenation of
dehydrogenation of ethylbenzene // Catal. Lett. 2009.
ethylbenzene with carbon dioxide: Promotional effect
V. 133. P. 307-313.
of antimony in supported vanadium-antimony oxide
catalyst // Catal. Today. 2003. V. 87 (1-4). P. 205-212.
[10] Ahmed A., Hoceine B., Zeid A., Al-Othman M.,
Rafiq H. S. Dehydrogenation of ehylbenzene in