Журнал прикладной химии. 2020. Т. 93. Вып. 5
НЕОРГАНИЧЕСКИЙ СИНТЕЗ И ТЕХНОЛОГИЯ НЕОРГАНИЧЕСКИХ ПРОИЗВОДСТВ
УДК 542; 546.06
ФОРМИРОВАНИЕ АНИЗОМЕТРИЧНЫХ ЧАСТИЦ ГИДРОКСИАПАТИТА
В ГИДРОТЕРМАЛЬНЫХ УСЛОВИЯХ
© Т. П. Масленникова1*, И. П. Добровольская2,3**, Э. Н. Гатина1,
Д. А. Кириленко4, В. Л. Уголков1, В. Е. Юдин2,3
1 Институт химии силикатов им. И. В. Гребенщикова РАН,
199034, г. Санкт-Петербург, наб. Макарова, д. 2
2 Санкт-Петербургский политехнический университет Петра Великого,
195251, г. Санкт-Петербург, ул. Политехническая, д. 29
3 Институт высокомолекулярных соединений РАН,
199004, г. Санкт-Петербург, Большой пр. В.О., д. 31
4 Физико-технический институт им А. Ф. Иоффе,
194021, г. Санкт-Петербург, Политехническая ул., д. 26
E-mail: *maslennikova.tp@iscras.ru; **zair2@mail.ru
Поступила в Редакцию 12 сентября 2019 г.
После доработки 23 сентября 2019 г.
Принята к публикации 14 декабря 2019 г.
Методами рентгенофазового анализа, просвечивающей электронной микроскопии, а также комплекс-
ного термического анализа показано, что в результате синтеза из водных растворов гидрофосфата
аммония и нитрата кальция образуются кристаллы брушита. Гидротермальная обработка брушита
приводит к формированию квазиодномерных наночастиц гидроксиапатита, продольный размер кото-
рых составляет около 400 нм, а поперечный — 40 нм. Показано, что наночастицы гидроксиапатита
могут быть использованы в качестве наполнителей композиционных матриц для тканевой инженерии,
в частности, в трансплантологии костной ткани.
Ключевые слова: гидроксиапатит; брушит; гидротермальная обработка; наночастицы; кристал-
лическая структура
DOI: 10.31857/S0044461820050023
Гидроксиапатит является одним из основных ком-
связанные с клетками и фибриллярным коллагеном.
понентов костной ткани животных и человека, его со-
Целью тканевой инженерии является разработка ма-
держание составляет 50-70%. Костная ткань состоит
териалов, которые после имплантирования их в жи-
из клеток (остеобластов, остеоцитов, остеокластов),
вой организм под воздействием биологической актив-
коллагена и нерастворимых фосфатов кальция в виде
ной среды инициируют процесс образования новой
гидроксиапатита Ca10(PO4)6(OH)2 и карбонатапатита
ткани, идентичной ткани реципиента [1], поэтому в
Ca10(PO4)6СО3. Гидроксиапатит в тканях представля-
последние годы резко возрос интерес к разработке
ет собой наноразмерные частицы различной формы,
способа получения наночастиц гидроксиапатита.
620
Формирование анизометричных частиц гидроксиапатита в гидротермальных условиях
621
Наночастицы синтетического гидроксиапатита
щью магнитной мешалки, pH суспензии составлял
различной морфологии получают с помощью твер-
5.0-5.1. Суспензию переносили в тефлоновый тигель
дофазных реакций, эмульсионных и золь-гель тех-
объемом 100 мл и проводили гидротермальную обра-
нологий, а также гидротермального метода [2-5].
ботку при Т = 200°C, давлении 10 МПа в течение 20 ч.
Наиболее полно способы получения и свойства нано-
Полученный порошок промывали дистиллированной
частиц синтетического гидроксиапатита для исполь-
водой до достижения нейтральной реакции и сушили
зования их в биологии и медицине описаны в работах
при Т = 50°C в атмосфере воздуха. Для исследования
[6-8]. Особое внимание уделено изучению формы од-
состава и структуры частиц, полученных в результате
но-, двух- и трехмерных частиц. Результаты исследо-
синтеза и не подвергнутых гидротермальной обработ-
вания влияния термической обработки на структуру и
ке, суспензию выдерживали до формирования осадка,
свойства наночастиц синтетического и биологическо-
который отделяли и промывали дистиллированной
го гидроксиапатита приведены в статье [9]. Методами
водой.
рентгеновской дифракции, электронной просвечива-
Кристаллическую структуру порошков иссле-
ющей микроскопии показано, что гидроксиапатит,
довали с помощью метода рентгенофазового ана-
полученный методом осаждения, представляет собой
лиза (РФА) на дифрактометре ДРОН-3М (НПО
порошок, состоящий из анизометричных частиц, про-
«Буревестник»). Измерения проводили в режиме на
дольный размер которых составляет 70-100 нм, а по-
отражение (геометрия Брэгга-Брентано) с исполь-
перечный — 7-9 нм. Синтетический гидроксиапатит
зованием CuKα-излучения (λ = 1.54 Å, никелевый
характеризуется меньшей термической устойчиво-
β-фильтр). Регистрацию вели в пошаговом режиме в
стью по сравнению с гидроксиапатитом биологиче-
интервале углов 2θ = 10-70° с шагом 0.02° при экс-
ского происхождения.
позиции в точке 1 с. Обработку полученных данных
Основным требованием к материалам для кле-
и идентификацию пиков проводили с использовани-
точных технологий является их биосовместимость,
ем пакета программы DFWin и базы данных ICDD
отсутствие негативного влияния на клетки как са-
PDF-2.
мих материалов, так и продуктов их биорезорбции,
Размеры кристаллитов определяли методом
поэтому наиболее перспективным представляется
Шеррера, использовали рефлексы гидроксиапатита
метод синтеза кристаллов гидроксиапатита из водных
(100), 2θ = 10.80° и (002), 2θ = 26.12°.
растворов солей кальция. Такой метод не предпола-
Форму и размеры наночастиц определяли с по-
гает использования каких-либо реагентов, способных
мощью просвечивающей электронной микроскопии
повлиять на пролиферативную активность клеток.
(ПЭМ) на электронном микроскопе высокого раз-
Несмотря на большое число работ, посвященных
решения JEM 2100-F с Uуск до 200 кВ с приставкой
синтезу гидроксиапатита, крайне мало исследований
Oxford Instruments INCA для энергодисперсионного
по изучению влияния условий формования на мор-
микрорентгеноспектрального анализа.
фологию наночастиц гидроксиапатита. Вместе с тем
Комплексный термический анализ проводили
известно, что такие параметры структуры твердых
на анализаторе STA 429 CD Netzsch с использова-
тел, как пористость, величина удельной поверхности,
нием платинородиевого держателя образцов типа
размеры и дефектность кристаллитов, существенно
TG + DSC в интервале температур 50-1000°С при
влияют на реакционную способность материала, его
нагревании со скоростью 20 град·мин-1, в потоке
поведение в жидких активных средах [10].
воздуха 10 + 40 см3·мин-1. При анализе регистриро-
Целью работы являлось изучение процесса фор-
вали изменения массы образца с точностью ±0.005 мг
мирования структуры наночастиц синтетического
[кривые термогравиметрии (ТГ), % от исходной мас-
гидроксиапатита, полученных из водных растворов
сы] и изменения энтальпии материала [кривые диф-
гидрофосфата аммония и нитрата кальция.
ференциально-сканирующей калориметрии (ДСК),
мВт·мг-1], направления экзотермических эффектов
вниз, так как для исследуемой системы (таблетки
Экспериментальная часть
материала) выделение тепла (экзотермия) имеет от-
Синтез гидроксиапатита проводили из водных рас-
рицательное значение.
творов (NH4)2HPO4 х.ч. и Ca(NO3)2·4H2O «чистый» в
Исследование структуры полученных порошков
дистиллированной воде, растворы солей были взяты в
проводили методом ИК-спектроскопии при исполь-
молярном отношении Ca/P = 1.67. Раствор гидрофос-
зовании Фурье-спектрометра ФСМ-1201. Диапазон
фата аммония медленно добавляли к раствору нитра-
волновых чисел составлял 450-4000 см-1, измерения
та кальция при постоянном перемешивании с помо-
проводили на воздухе в режиме пропускания, разре-
622
Масленникова Т. П. и др.
шение составляло 4 см-1. Обработку спектров осу-
ществляли с использованием базового программного
обеспечения Fspec, реализующего автоматическое из-
мерение спектров, имеющего средства графического
отображения спектров и их фрагментов. Полученные
с помощью программы Excel цифровые данные ис-
пользовали для построения спектра пропускания.
Для определения удельной поверхности образцов
использовался метод низкотемпературной адсорбции
азота (метод Брунауэра-Эммета-Теллера, газовый
анализатор Quantochrome, Nova-1200e).
Обсуждение результатов
Кристаллическую структуру образцов исследо-
Рис. 1. Рентгеновские дифрактограммы образцов, по-
вали методом рентгенофазового анализа. По дан-
лученных в результате осаждения (1) и после гидротер-
ным РФА установлено, что в результате осаждения
мальной обработки осажденного порошка (2).
из водных растворов (NH4)2HPO4 и Ca(NO3)2·4H2O
1 — СаHPO4·2H2O — брушит (JCPDC 11-293), 2 —
начинает формироваться кристаллогидрат гидрофос-
Ca10(PO4)6(OH)2 — гидроксиапатит (JCPDC 9-432).
фата кальция (СаHPO4·2H2O) — аналога минерала
брушита (рис. 1, кривая 1). После гидротермальной
обработки суспензии в течение 20 ч в водной среде
ностью измерения. Это позволяет предположить,
происходит перекристаллизация брушита в гидрок-
что размеры кристаллитов брушита больше 100 нм.
сиапатит. На рентгеновских дифрактограммах (рис. 1,
Данные ИК-спектроскопии образцов достаточно
кривая 2) были зафиксированы пики, относящиеся
хорошо согласуются с данными рентгенофазового
только к фазе гидроксиапатита.
анализа (рис. 2). В ИК-спектре осажденного образца
Рассчитанный методом Шеррера поперечный
присутствуют все полосы, характерные для брушита.
размер кристаллита гидроксиапатита составляет
Группы полос поглощения можно отнести к деформа-
29 ± 1 нм, продольный — 40 ± 1 нм. Корректно опре-
ционным δ(PO43-) — 525, 576, 662 см-1 и валентным
делить размеры кристаллитов брушита не представля-
ν(PO43-) — 987, 1057, 1135 см-1 колебаниям связей
ется возможным ввиду малых значений полуширины
O-P-O в группах HPO42- [11]. Наличие в структуре
рефлексов, менее 0.01°, что сопоставимо с погреш-
брушита кристаллизационной воды подтверждается
Рис. 2. ИК-спектры синтезированных образцов до (1) и после (2) гидротермальной обработки.
Формирование анизометричных частиц гидроксиапатита в гидротермальных условиях
623
валентными [791 см-1 — ν(H2O)] и деформационны-
методом ПЭМ (рис. 3). Преимущественная морфо-
ми [1219 см-1 δ(H2O)] колебаниями O-H-О.
логия частиц — стержнеобразная. Размеры частиц:
В ИК-спектре образца, полученного после ги-
длина от 300 нм до нескольких микрометров, ширина
дротермальной обработки, присутствуют валентные
от 90 до 300 нм (рис. 3, а, б). В образце присутствуют
(471, 575, 601 см-1) и деформационные (963, 1040,
частицы микрометрового размера с морфологией,
1090 см-1) колебания связей O-P-O. Полоса погло-
близкой к гексагональной и сферической. Размеры
щения при 642 см-1 соответствует деформационным
таких частиц составляют от 500 до 900 мкм.
колебаниям OH-групп, валентные колебания сорби-
Анализ данных ПЭМ образца, полученного после
рованной и кристаллизационной воды представлены
гидротермальной обработки, показал, что частицы
в спектре фоном в области 3350-3500 см-1. На де-
гидроксиапатита имеют четко выраженную анизо-
формационные колебания H-O-H указывают поло-
метричную форму, продольные размеры частиц со-
сы 1670-1675 см-1. Перечисленные спектральные
ставляют 200-400 нм, поперечные — около 40 нм
особенности характерны для кристаллов гидрокси-
(рис. 3, в). На микрофотографии высокого разрешения
апатита.
(рис. 3, г) наблюдается практически идеальная гек-
После синтеза до гидротермальной обработки в
сагональная кристаллическая структура гидрокси-
суспензии формируются частицы различной морфо-
апатита.
логии, с большим разбросом значений по размерам,
Методом низкотемпературной адсорбции азота
что следует из результатов исследования образцов были определены значения удельной поверхности
Рис. 3. Просвечивающая электронная микроскопия синтезированных образцов до (а, б) и после (в, г)
гидротермальной обработки.
624
Масленникова Т. П. и др.
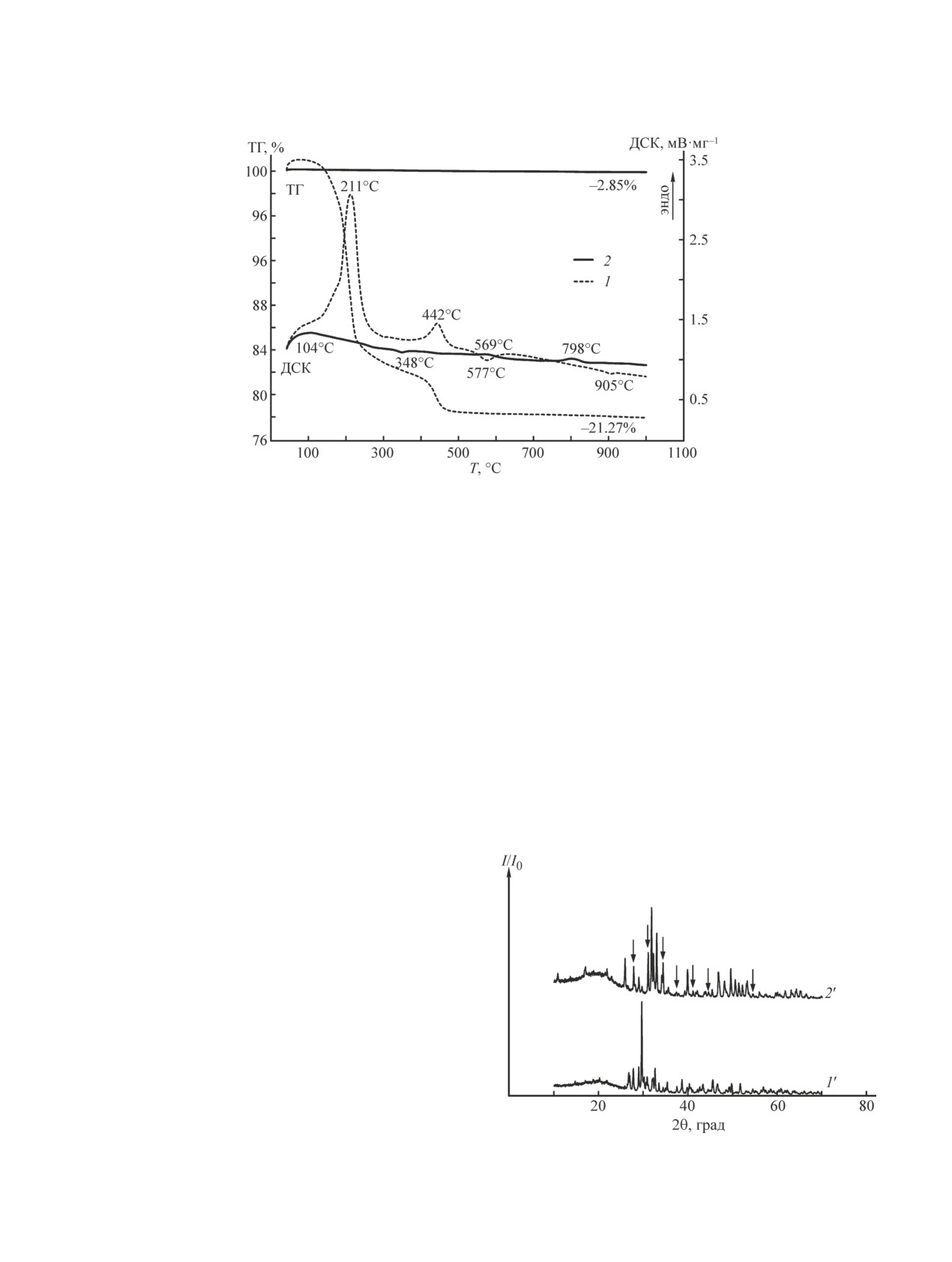
Рис. 4. Кривые дифференциально-сканирующей калориметрии и термогравиметрии образцов до (1) и после (2)
гидротермальной обработки.
образцов синтетического брушита и гидроксиапатита.
Т = 1000°С, составила менее 3% (рис. 4, кривая 2),
Для брушита эта величина составила 34 м2·г-1, для
что, вероятно, свидетельствует о высокой степени его
наночастиц гидроксиапатита — 40 м2·г-1.
кристалличности. В интервале температур 50-200°С
Результаты исследования термических свойств
происходит удаление несвязанной и сорбированной
кристаллов брушита и гидроксиапатита приведены на
воды, при Т = 348°С зафиксирован экзоэффект, ко-
рис. 4. Для кривой ДСК образца брушита (кривая 1)
торый может быть отнесен к разложению нитрата
характерно наличие двух эндотермических максиму-
аммония, входящего в состав гидроксиапатита. При
мов Т1 = 211°С и Т2 = 442°С. Первый эндоэффект свя-
температурах Т = 569 и 798°С наблюдаются еще два
зан с удалением сорбированной (несвязанной воды)
эндоэффекта, которые могут быть отнесены к уда-
из брушита, второй — с удалением кристаллизацион-
лению углекислого газа и остатков воды одновре-
ной воды и образованием гидрофосфата кальция —
менно с частичным переходом гидроксиапатита в
СаHPO4, аналога минерала монетита. По данным
β-Ca3(PO4)2.
термогравиметрического анализа в интервале тем-
ператур 200-450°С наблюдается интенсивная потеря
массы образца, не подвергнутого гидротермальной
обработке. По данным исследований, проведенных
методом ДСК, при Т = 569°С был зафиксирован эк-
зоэффект, который связан с переходом монетита в пи-
рофосфат кальция (Ca2P2O7). Этот эффект также свя-
зан с удалением остатков оксидов азота. Последний
небольшой экзоэффект при Т = 905°С, по всей
вероятности, связан с совершенствованием и ростом
кристаллов пирофосфата кальция. Данный экзотер-
мический эффект сопровождается потерей массы об-
разца менее 1%. На протяжении всего температурного
интервала исследования Т = 50-1000°С, как следует
из результатов термогравиметрического анализа,
потеря массы образца составила 21.27%
Потеря массы образца гидроксиапатита, под-
Рис. 5. Дифрактограммы образцов брушита (1′) и ги-
вергнутого высокотемпературной обработке до
дроксиапатита (2′) после обработки при Т = 1000ºС.
Формирование анизометричных частиц гидроксиапатита в гидротермальных условиях
625
Данные термического анализа хорошо согласу-
Кириленко Демид Александрович, к.ф.-м.н.,
ются с данными РФА образцов, полученных после
термообработки до Т = 1000°С. Из анализа пред-
Уголков Валерий Леонидович, к.т.н.,
ставленных на рис. 5 (кривые 1′ и 2′) дифрактограмм
образцов синтетического брушита и гидроксиапатита,
Юдин Владимир Евгеньевич, д.ф.-м.н.,
термообработанных в динамическом режиме нагрева
со скоростью 20 град·мин-1 до 1000°С, следует, что
в образцах присутствуют фазы, относящиеся к про-
Список литературы
дуктам разложения и термических преобразований
брушита и гидроксиапатита.
[1] Добровольская И. П., Юдин В. Е., Попрядухин П. В.,
На кривой 1′ зафиксированы только пики, при-
Иванькова Е. М. Полимерные матрицы для ткане-
надлежащие фазе пирофосфата кальция (Ca2P2O7)
вой инженерии. СПб: Изд.-полиграф. ассоциация
(JCPDC 9-346). На кривой 2′ наблюдаются пики ор-
ун-тов России, 2016. С. 41-55 [Dobrovolskaya I. P.,
тофосфата кальция Ca3(PO4)2 (JCPDC 9-169). Данная
Yudin V. E., Popryadukhin P. V., Ivan′kova E. M.
Polymer scaffolds for tissue engineering. St. Petersburg:
фаза отмечена стрелками. Все остальные неотмечен-
Mediapapir, 2018. P. 37-49].
ные пики на кривой 2′ относятся к фазе гидроксиапа-
[2] Paz A., Guadarrama D., López M., González J. E.,
тита Ca10(PO4)6(OH)2 (JCPDC 9-432).
Brizuela N., Aragón J. A comparative study of
hydroxyapatite nanoparticles synthesized by different
routes // Quimica Nova. 2012. V. 35. N 9. P. 1724-1727.
Выводы
В результате взаимодействия водных растворов ги-
[3] de Caprariis B., Di Rita M., Stoller M., Verdone N.,
Chianese A. Reaction-precipitation by a spinning disc
дрофосфата аммония и нитрата кальция формируют-
reactor: Influence of hydrodynamics on nanoparticles
ся кристаллы брушита. Установлено, что в результате
production // Chem. Eng. Sci. 2012. V. 76. P. 73-80.
гидротермальной обработки осажденной суспензии
формируются монофазные анизометричные наноча-
[4] Landi E., Logroscino G., Proietti L., Tampieri A.,
стицы гидроксиапатита с продольными размерами
Sandri M., Sipro S. Biomimetic Mg-substituted
200-400 нм и поперечными около 40 нм.
hydroxyapatite: From synthesis to in vivo behavior //
Анализ свойств и структуры синтезированных на-
J. Mater. Sci. Mater. Medicine. 2008. V. 19. N 1.
ночастиц гидроксиапатита позволяет рекомендовать
их в качестве наполнителя композиционных матриц
[5] Liu C., Huang Y., Shen W., Cui J. Kinetics of
для тканевой инженерии, а также для применения в
hydroxyapatite precipitation at pH 10 to 11 //
клеточных технологиях.
Biomaterials. 2001. V. 22. N 4. P. 301-306. https://
doi.org/10.1016/S0142-9612(00)00166-6
[6] Dorozhkin S. V. Calcium orthophosphate deposits:
Финансирование работы
Preparation, properties and biomedical applications //
Mater. Sci. Eng. C. 2015. V. 55. P. 272-326. https://
Работа выполнена при поддержке Российского
doi.org/10.1016/j.msec.2015.05.033
научного фонда, проект № 19-73-30003.
[7] Karpikhin A. E., Fedotov A. Yu., Komlev V. S.,
Barinov S. M., Sirotinkin V. P., Gordeev A. S.,
Shamrai V. F. Structure of hydroxyapatite powders
Конфликт интересов
prepared through dicalcium phosphate dihydrate
Авторы заявляют об отсутствии конфликта инте-
hydrolysis // Inorg. Mater. 2016. V. 52. N 2. P. 170-175.
ресов, требующего раскрытия в данной статье.
[8] Šupová M. Isolation and preparation of nanoscale
bioapatites from natural sources: A review // J. Nanosci.
Информация об авторах
Nanotechnol. 2014. V. 14. N 1. P. 546-563. https://
doi.org/10.1166/jnn.2014.8895
Масленникова Татьяна Петровна, к.х.н.,
[9] Добровольская И. П., Царев Н. С., Осмолов-
ская О. М., Касаткин И. А., Иванькова Е. М.,
Добровольская Ирина Петровна, д.ф.-м.н.,
Попова Е. Н., Панкова Г. А., Юдин В. Е. Влияние
термической обработки на структуру и свой-
Гатина Эльмира Надыревна,
ства гидроксиапатита // ЖПХ. 2018. Т. 91. № 3.
С. 328-334 [Dobrovol′skaya I. P., Tsarev N. S.,
626
Масленникова Т. П. и др.
Osmolovskaya O. M., Kasatkin I. A., Ivan′kova E. M.,
[Regel′ V. R., Slutsker A. I., Tomashevskii E. E. The
Popova E. N., Pankova G. A., Yudin V. E. Effect of
kinetic nature of the strength of solids // Soviet
thermal treatment on the structure and properties of
Physics Uspekhi. 1972 V. 15. N 1. P. 45-65. http://
hydroxyapatite // Russ. J. Appl. Chem. 2018. V. 91.
dx.doi.org/10.1070/PU1972v015n01ABEH004945].
N 3. P. 368-374.
[11] Mandel S., Tas A. C. Brushite (CaHPO4·2H2O) to
octacalcium phosphate (Ca8(HPO4)2(PO4)4·5H2O)
[10] Регель В. Р., Слуцкер А. И., Томашевский Э. Е.
transformation in DMEM solutions at 36.5°C // Mater.
Кинетическая природа прочности твердых тел //
Sci. Eng. C. 2010. V. 30. N 2. P. 245-254. https://
Успехи физ. наук. 1972. Т. 106. № 2. С. 193-228
doi.org/10.1016/j.msec.2009.10.009