Журнал прикладной химии. 2020. Т. 93. Вып. 6
УДК 544.4.032.7
УГЛЕКИСЛОТНАЯ КОНВЕРСИЯ МЕТАНА (обзор)
© В. В. Недоливко1, Г. О. Засыпалов1, А. В. Вутолкина1,3, П. А. Гущин1,2,
В. А. Винокуров1,2, Л. А. Куликов3, С. В. Егазарьянц1,3, Э. А. Караханов3,
А. Л. Максимов3,4, А. П. Глотов1,2*
1 Российский государственный университет нефти и газа (НИУ) им. И. М. Губкина,
119991, г. Москва, Ленинский пр., д. 65
2 НП «Технопарк Губкинского университета»,
119296, г. Москва, Ленинский пр., д.63/2, к. 1
3 Московский государственный университет им. М. В. Ломоносова,
119991, г. Москва, Ленинские горы, д. 1, стр. 3
4 Институт нефтехимического синтеза им. А. В. Топчиева РАН,
119991, г. Москва, Ленинский пр., д. 29, стр. 2
* E-mail: glotov.a@gubkin.ru
Поступила в Редакцию 13 мая 2020 г.
После доработки 13 мая 2020 г.
Принята к публикации 19 мая 2020 г.
В обзоре рассмотрены термодинамические и кинетические аспекты углекислотной конверсии мета-
на, систематизированы данные о типах используемых каталитических систем и об особенностях
промышленной реализации данного процесса. Оптимальные значения технологических параметров
процесса углекислотной конверсии метана лежат в интервале 700-900°С для температуры и
2-4 МПа для давления. На основании детального анализа литературных данных об активности и
стабильности катализаторов сухого риформинга установлено, что ключевым фактором, определя-
ющим активность катализаторов и их устойчивость к коксообразованию, является баланс между
свойствами носителя и составом активной металлической фазы. Так, например, кислотно-основные
свойства носителя определяют силу связывания металла с поверхностью, что может влиять как на
активность катализатора, так и его стабильность за счет предотвращения спекания частиц актив-
ного компонента. В качестве носителей наиболее широко применяются оксиды кремния, алюминия,
цирконий- и титан-силикаты, а контроль над их кислотностью осуществляется путем введения ле-
гирующих добавок, в частности, оксидов церия, кальция и магния. Активной фазой могут выступать
как переходные (Ni и Co), так и благородные (Rh, Ru, Pd, Pt и Ir) металлы, а также биметаллические
системы, содержащие центры двух типов. Основной проблемой, ограничивающей внедрение и мас-
штабирование процесса углекислотной конверсии метана, остается дезактивация катализатора
вследствие коксования носителя и спекания частиц активного компонента.
Ключевые слова: углекислотная конверсия; паровая конверсия; сухой риформинг; синтез-газ; водяной
газ; коксообразование
DOI: 10.31857/S0044461820060018
763
764
Недоливко В. В. и др.
Введение
тов (метанола или диметилового эфира), что в сово-
купности с энергозатратами делает данную техноло-
В последние несколько десятков лет наблюда-
гию экономически невыгодной [9]. Перспективной
ется рост выбросов в атмосферу диоксида углеро-
является комбинация процессов парового и сухого
да антропогенного происхождения, образующегося
риформинга метана, когда дефицит водорода в си-
при сжигании ископаемых топлив (нефтяной уголь,
стеме компенсируется подачей водяного пара, что
природный газ, биомасса), являющихся основным
позволяет регулировать мольное отношение H2/CO
энергоресурсом [1]. Многими странами были заклю-
за счет протекания реакции водяного газа. Данный
чены соглашения о сокращении выбросов диоксида
подход может быть применим для получения газовой
углерода.* В связи с этим возникает необходимость
смеси с соотношением H2/CO = 2:1 для процесса
разработки технологий накопления и улавливания
Фишера-Тропша, направленного на производство
CO2, в том числе с целью его дальнейшей перера-
компонентов моторных топлив, а также для получе-
ботки, направленной на производство продуктов с
ния метанола [10].
высокой добавленной стоимостью: синтетического
Углекислотная конверсия метана — эндотермиче-
топлива или сырья и полупродуктов нефтехимии
ский процесс, что предполагает его проведение при
[2, 3].
высоких температурах (700-1000°C) для достижения
С открытием крупных месторождений сланце-
желаемых уровней конверсии сырья. Для смещения
вого газа в мире и совершенствованием технологий
равновесия в сторону образования продуктов ре-
фракционирования газов одним из наиболее предпоч-
акцию также целесообразно проводить при низком
тительных энергоресурсов стал метан [4]. Помимо
давлении водорода (2-4 атм). С целью преодоления
сланцевого газа источником метана является попут-
термодинамических ограничений и энергетического
ный газ, образующийся при добыче нефти, а также
барьера реакции диссоциации чрезвычайно стабиль-
газ анаэробного происхождения, которые, вместе с
ных молекул диоксида углерода и метана применя-
тем, содержат и углекислый газ [5]. В определен-
ют катализаторы на основе металлов VIII группы,
ных условиях углекислый газ и метан могут взаи-
что также позволяет снизить температуру процесса
модействовать с образованием синтез-газа (мольное
до 500-550°C. Однако даже при пониженной тем-
соотношение H2/CO = 1:1) — одного из основных
пературе основной проблемой остается дезактива-
источников длинноцепочечных углеводородов [6].
ция катализатора вследствие коксования носителя
Данный процесс получил название «сухой рифор-
и спекания частиц активного компонента, что огра-
минг метана», или «углекислотная конверсия метана»
ничивает внедрение и масштабирование процесса
(УКМ). Кроме того, образующийся синтез-газ может
углекислотной конверсии метана и требует поиска
быть использован для получения кислородсодержа-
новых технологических решений и каталитических
щих соединений, таких как уксусная кислота, диме-
систем [11, 12].
тиловый эфир, альдегиды, спирты и др. [7]. Основное
Исследования в области создания высокоактив-
количество водорода, получаемого углекислотной
ных и стабильных катализаторов сухого риформинга
конверсией метана, расходуется на получение ам-
метана могут лечь в основу работ, направленных на
миака либо используется в различных процессах ги-
создание технологии получения синтез-газа с задан-
дрирования в нефтеперерабатывающей и пищевой
ным мольным отношением H2/CO для процессов
промышленности.
Фишера-Тропша, гидроформилирования, получения
Для промышленного получения синтез-газа ис-
углеводородов, оксигенатов (метанола, формальдеги-
пользуют паровую конверсию метана. Однако дан-
да, диметилового эфира и др.).
ный высокотемпературный процесс (700-900°С для
Вышесказанное в большей мере относится к стра-
традиционных никелевых катализаторов) имеет ряд
нам с высокими показателями нефте- и газодобычи,
существенных недостатков, таких как необходимость
в числе которых одно из лидирующих положений
обеспечения невысоких объемных скоростей подачи
занимает Россия. Для России данная тема актуальна
газов и наличие узла отделения избытка водорода [8].
еще и тем, что основные регионы добычи природных
Кроме того, капитальные затраты на получение син-
ресурсов все в большей степени перемещаются на
тез-газа путем паровой конверсии метана составляют
север, а это неизбежно приводит к удорожанию не
примерно две трети от стоимости конечных продук-
только нефти и газа, но продуктов на их основе, в
связи с чем разработка перспективных с техноло-
* United Nations Framework Convention on Climate
гической и экономической точек зрения процессов
Change (UNFCCC). Adoption of the Paris Agreement.
FCCC/CP/2015/L.9/Rev.1. 2015.
нефтехимического синтеза очень важна.
Углекислотная конверсия метана (обзор)
765
Цель данной работы — изучение результатов ис-
Термодинамика реакции
следований в области термодинамики и кинетики
углекислотной конверсии метана
процесса углекислотной конверсии метана, система-
Реакция взаимодействия метана и углекислого
тизация данных об особенностях реализации данного
газа [уравнение (1)], как и паровая конверсия метана
процесса на различных типах каталитических систем
[уравнение (2)] или автотермический риформинг,
и оценка влияния металлов, носителей и промоторов
носит эндотермический характер, в связи с чем для
на активность и стабильность используемых катали-
преодоления термодинамических ограничений про-
заторов.
цесс проводится при высоких температурах [13].
CH4 + CO2
2CO + 2H2, ΔH°298K = 248 кДж·моль-1,
(1)
CH4 + H2O CO + 3H2, ΔH°298K = 206 кДж·моль-1.
(2)
В ходе углекислотной конверсии метана на актив-
— реакция конверсии водяного газа [уравнение
ных центрах катализатора параллельно могут проте-
(3)]. Протекание данной реакции выгодно в случае
кать побочные реакции, как влияющие на термодина-
необходимости получения синтез-газа с мольным
мическое равновесие процесса, так и определяющие
отношением H2/CO = 1 или менее 1 [14-16]:
мольное отношение H2:CO в реакционной смеси:
CO2 + H2 CO + H2O, ΔH°298K = 41.2 кДж·моль-1;
(3)
— реакции диспропорционирования. Помимо ре-
зованию кокса, осаждающегося в порах носителя и
акции водяного газа в ходе углекислотной конверсии
блокирующего активные центры катализатора, что
метана может протекать реакция высокотемпера-
в большинстве случаев приводит к его обратимой
турного разложения метана [(уравнение (4)] и (или)
дезактивации [17]. Вероятность протекания данных
диспропорционирования монооксида углерода [ре-
реакций определяется составом газовой смеси и тем-
акция Будуара, уравнение (5)], приводящие к обра-
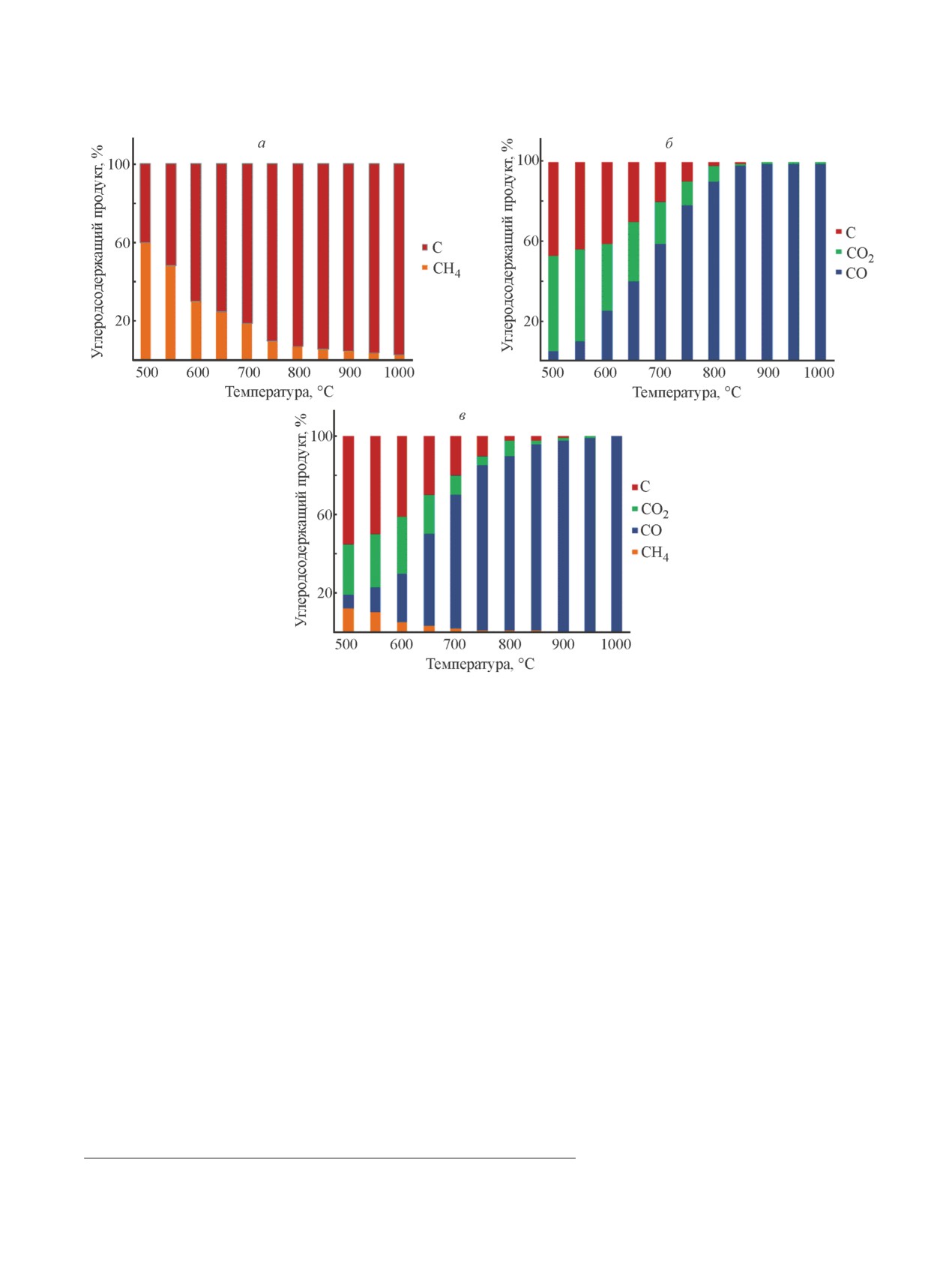
пературой процесса (рис. 1):
CH4 q C + H2, ΔH°298K = 75 кДж·моль-1;
(4)
2CO q C + CO2, ΔH°298K = 172 кДж·моль-1.
(5)
Разложению CH4 [уравнение (4)] благоприятству-
температур даже в присутствии избытка окислителя,
ют высокие температуры, в то время как реакция
однако в области высоких температур окислитель
Будуара [уравнение (5)] протекает преимуществен-
способен подавлять образование кокса.
но при низких температурах и практически не идет
Несмотря на то что часть осажденного углерода
при температурах выше 900°С (рис. 1). Образование
удаляется в ходе его неполного [до СО, уравнения (6),
кокса обусловлено протеканием именно этих реак-
(7)] или полного [до СО2, уравнение (8)] окисления,
ций, каждая из которых вносит свой вклад только в
основное его количество остается в реакционной
определенном интервале температур. Таким образом,
смеси:
нельзя избежать образования кокса в области низких
C + H2O CO + H2, ΔH°298K = -131.2 кДж·моль-1,
(6)
C + 1/2O2 CO, ΔH°298K = 110.5 кДж·моль-1,
(7)
C + O2 CO2, ΔH°298K = -393.4 кДж·моль-1;
(8)
— реакция метанирования СО [18]:
CO + 3H2 CH4 + H2O, ΔH°298K = -205.8 кДж·моль-1.
(9)
Степень протекания каждой из вышеуказанных ре- метров процесса: температура и давление в реакторе,
акций, как основной, так и побочных, зависит от пара- исходное мольное отношение CO2/CH4 и состав обра-
766
Недоливко В. В. и др.
Рис. 1. Зависимость выхода кокса на катализаторе от температуры при разложении метана (а),
монооксида углерода (б) и в ходе протекания процесса углекислотной конверсии метана (в) [17].*
зующейся газовой смеси, состав активной фазы ката-
М. Нико и Н. Амин [18] на основании термоди-
лизаторов, текстурные характеристики и кислотность
намических расчетов оценили вероятность протека-
носителя. Рассмотрим подробнее каждый из них.
ния различных реакций в условиях углекислотной
Большое число исследований посвящено модели-
конверсии метана (табл. 1). Согласно термодинами-
рованию термодинамики углекислотной конверсии
ческим расчетам, конверсия метана с мольным соот-
метана при различных температурах, мольном от-
ношением CO2:CH4 = 2:3 должна достигать практиче-
ношении CO2/CH4, давлении, наличии/отсутствии
ски количественных значений (97%) при температуре
окислителя с целью изучения влияния указанных
800°C. При температуре выше 1000°C и стехиометри-
параметров на протекание побочных реакций с об-
ческом (или меньше) отношении CO2:CH4 в исходной
разованием углерода [10, 17, 18]. На основании про-
смеси конверсия метана не превышает 42%.
веденных расчетов в ряде работ показано, что необ-
Я. Ли с соавт. [19] провели термодинамические
ходимым условием достижения высокой конверсии
расчеты по влиянию мольного отношения CO2:CH4
сырья и снижения выхода кокса является проведение
на протекание сухого риформинга метана. Авторы по-
углекислотной конверсии метана при высоких темпе-
казали, что конверсия метана при температуре 750°C
ратурах (выше 850°C) и низких давлениях (1-3 атм).
возрастает с увеличением содержания диоксида угле-
Следует отметить, что при проведении данных рас-
рода в составе газовой смеси, а мольное соотношение
четов был принят ряд допущений, в частности, не
CO2:CH4 должно превышать 5:1. Повышение темпе-
учитывалось влияние катализатора на состав про-
ратуры до 1000°C позволяет достигать высоких кон-
дуктов реакции.
версий CH4 (93%) при отношении CO2:CH4 меньше 1.
* Разрешение на публикацию от издательства Elsevier от 18.05.2020.
Углекислотная конверсия метана (обзор)
767
Таблица 1
Расчетные значения энтальпии побочных реакций, протекающих в ходе углекислотной конверсии метана
Реакция
Схема реакции
ΔH°298K, кДж·моль-1
Литературный источник
(10)
C + 2H2O CO2 + 2H2
-113.1
[14]
(11)
2CH4 + CO2 C2H6 + CO + H2O
106
(12)
2CH4 + 2CO2 C2H4 + 2CO + 2H2O
284
(13)
C2H6 C2H4 + H2
136
(14)
CO + 2H2 CH3OH
-90.6
(15)
CO2 + 3H2 CH3OH + H2O
-49.1
[18]
(16)
2CH3OH CH3OCH3 + H2O
-37
(17)
CH3OCH3 + CO2
3CO + 3H2
258.4
(18)
CH3OCH3 + H2O
2CO + 4H2
204.8
(19)
CH3OCH3 + 3H2O
2CO2 + 6H2
136
(20)
CO2 + 4H2 CH4 + 2H2O
-165
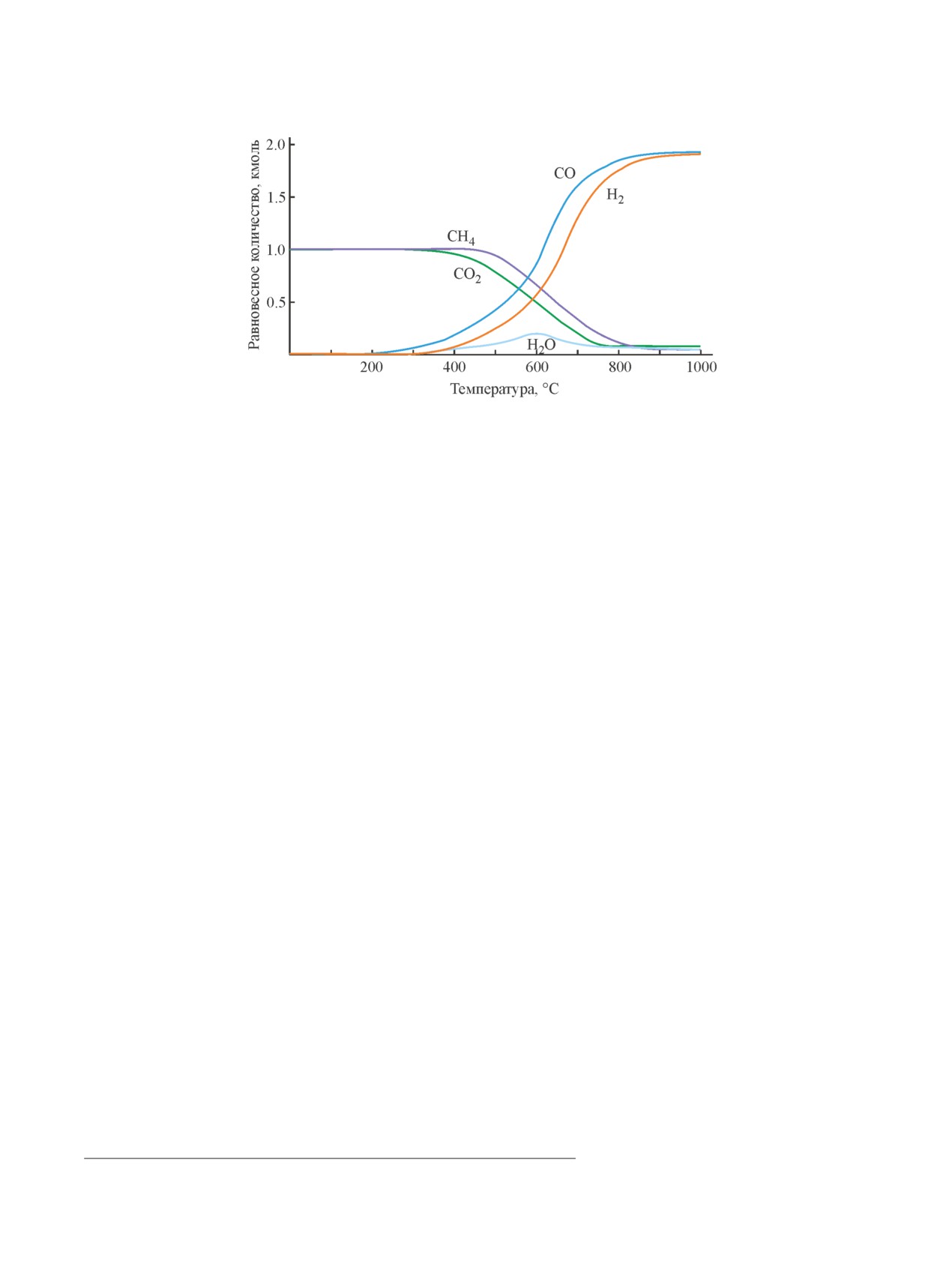
Помимо влияния температуры на протекание угле-
ции образования углерода не протекают, показывают,
кислотной конверсии метана авторами были иссле-
что мольное отношение H2:CO при температурах
дованы закономерности процесса в зависимости от
выше 300°C составляет 0.8-1, а образование H2O
давления водорода в реакционной среде. Согласно
по реакции водяного газа происходит в интервале
полученным данным, повышение давления приводит
температур 400-800°C, что согласуется с расчетами
к уменьшению конверсии метана и углекислого газа
свободной энергии процесса (рис. 2) [23].
в широком интервале температур (600-900°C). При
Однако, согласно этому же расчету, при допуще-
этом выход кокса возрастает [20]. При атмосферном
нии образования отдельной твердой фазы углерода
давлении и мольном отношении CO2:CH4 = 1 образо-
зависимость состава равновесной смеси от темпера-
вание углерода термодинамически возможно вплоть
туры кардинально изменяется. Мольное отношение
до 800°C. Лишь при более высоких температурах и
H2:CO существенно выше во всем интервале темпе-
атмосферном давлении выход синтез-газа близок к
ратур. Так, когда температура не превышает 900°С,
50%, а мольное отношение H2O:СО стремится к нулю
мольное отношение H2:CO превосходит 1, поскольку
[21], что также нашло подтверждение и в других ра-
с ростом выхода углерода уменьшается выход СО.
ботах [10, 11, 22].
Выше 900°С выход углерода невелик, в результате
Безусловно, сравнивать данные о конверсии мета-
чего мольное отношение H2:CO близко к 1. Данные
на и углекислого газа, полученные на основании тер-
расчета также свидетельствуют о том, что образова-
модинамических расчетов методом минимизации сво-
ние углерода является неизбежным при 900°С, что
бодной энергии Гиббса, с фактическими результатами
обусловлено термодинамическими особенностями
не совсем корректно, так как протекание процесса
реакции.
во многом зависит от используемого катализатора.
На основании вышесказанного можно сделать вы-
С. Ванг и соавт. [14] изучали влияние состава ката-
вод о том, что повышение температуры способствует
лизатора и типа используемого носителя на термо-
протеканию углекислотной конверсии метана и ин-
динамику реакции углекислотной конверсии метана
гибирует побочные реакции. Однако с точки зрения
в интервале температур 600-950°C. Как сообщают
энергетических затрат проведение процесса выше
авторы, разложение CH4 c образованием углерода
700°C экономически невыгодно и требует дополни-
происходит при температуре выше 557°C, а реакция
тельных технических и технологических решений.
Будуара — при температуре ниже 700°C. Они предпо-
Решением проблемы подвода и отвода тепла
ложили, что оптимальная температура при мольном
может стать разработка процесса, совмещающе-
соотношении CO2:CH4 = 1:1 для достижения высокой
го углекислотную и паровую конверсию метана
конверсии и минимального выхода кокса составляет
в присутствии кислорода, в котором без дополни-
от 870 до 1040°C.
тельного подвода тепла сочетаются реакции (1)-(3).
Расчеты, проведенные с учетом допущения, что в
Термодинамические параметры для такой комби-
ходе процесса углекислотной конверсии метана реак-
нированной термонейтральной (автотермической)
768
Недоливко В. В. и др.
Рис. 2. Зависимость равновесного количества продуктов реакции углекислотной конверсии метана от температуры
при общем давлении в реакционной смеси 1 атм и мольном отношении CO2:CH4 = 1 [23].*
конверсии рассчитаны в работе О. Крылова [21].
на поверхности с образованием частиц СНх и С и их
Варьируя исходное мольное отношение CH4/CO2,
последующее взаимодействие с адсорбированным
можно получить синтез-газ состава 1:1 при сохране-
атомом О [10, 23].
нии термонейтральности. Повышение температуры
Ключевым параметром при рассмотрении кине-
приводит к увеличению выхода монооксида углерода
тики и механизма процесса является энергия акти-
(38% при 900°С), а ее снижение — к увеличению
вации молекул метана и монооксида углерода, ко-
выхода водорода (36.4% при 700°С).
торая зависит главным образом от типа и структуры
К. Томишиг с соавт. [24] предлагают использовать
формирующегося на поверхности катализатора ак-
для данного процесса реакторы с псевдоожиженным
тивного центра. Значения энергии активации CH4 и
слоем катализатора, в которых метан частично или
CO2 для разных типов катализаторов углекислотной
полностью окисляется кислородом, а тепло, выделя-
конверсии метана лежат в интервале 25-355 и 30-
ющееся в ходе реакции, используется при проведе-
135 кДж·моль-1 соответственно [23]. Для каждого из
нии углекислотной конверсии метана. Комбинация
представленных катализаторов энергия диссоциации
горения и углекислотной конверсии метана делает
CH4 выше энергии диссоциации CO2, что согласует-
весь процесс термонейтральным, что позволяет пре-
ся с другими реакциями с участием CH4 и связано с
дотвратить протекание реакций, приводящих к чрез-
энергией, необходимой для активации относительно
мерному образованию углерода [25]. Использование
стабильной молекулы CH4. При этом энергия акти-
мембранных реакторов также может помочь в прео-
вации существенно зависит от основности носителя.
долении термодинамических ограничений реакции.
Механизм активации молекулы СН4. Важной ста-
Так, например, было показано, что Pd-Ag-мембраны
дией процесса углекислотной конверсии метана при
могут выступать в качестве катализаторов углекис-
отсутствии диффузионных ограничений является
лотной конверсии метана и, вместе с тем, селективно
адсорбция молекулы CH4 на активных центрах ка-
удалять водород из газовой смеси, смещая тем самым
тализатора и ее последующая активация. Чаще все-
равновесие в сторону образования водорода и CO
го в качестве активной фазы катализаторов сухого
[26].
риформинга метана выступают системы Ru, Rh, Pt,
Ni [15, 27]. Сорбируясь на металлических центрах,
метан диссоциирует с образованием промежуточных
Кинетические параметры и механизм реакции
соединений углерода, CHx- или формильной груп-
углекислотной конверсии метана
пы. Д. Биттер с соавт. [28] для серии катализаторов
Энергия активации молекул СН4 и CO2. В боль-
Pt/ZrO2 с разным содержанием платины наблюдали,
шинстве предлагаемых в литературе механизмов
что скорость реакции углекислотной конверсии мета-
углекислотной конверсии метана рассматривается
на возрастает с увеличением массового содержания
последовательная диссоциативная адсорбция СН4
металла лишь до определенного предела. Это гово-
* Разрешение на публикацию от издательства Royal Society of Chemistry от 19.05.2020.
Углекислотная конверсия метана (обзор)
769
рит о том, что в активации CH4 участвуют не только
температуре ниже 550°C, а диссоциация протекает
металлические центры, но и основные и кислотные
при существенно бóльших температурах [28].
центры носителя.
Д. Биттер и соавт. [28] предположили, что в ходе
Реакция углекислотной конверсии метана, как пра-
реакции CH4 активируется на металлических цен-
вило, имеет первый порядок по CH4 [29], в связи с
трах, в то время как активация CO2 происходит на
чем катализатор должен обеспечивать низкую энер-
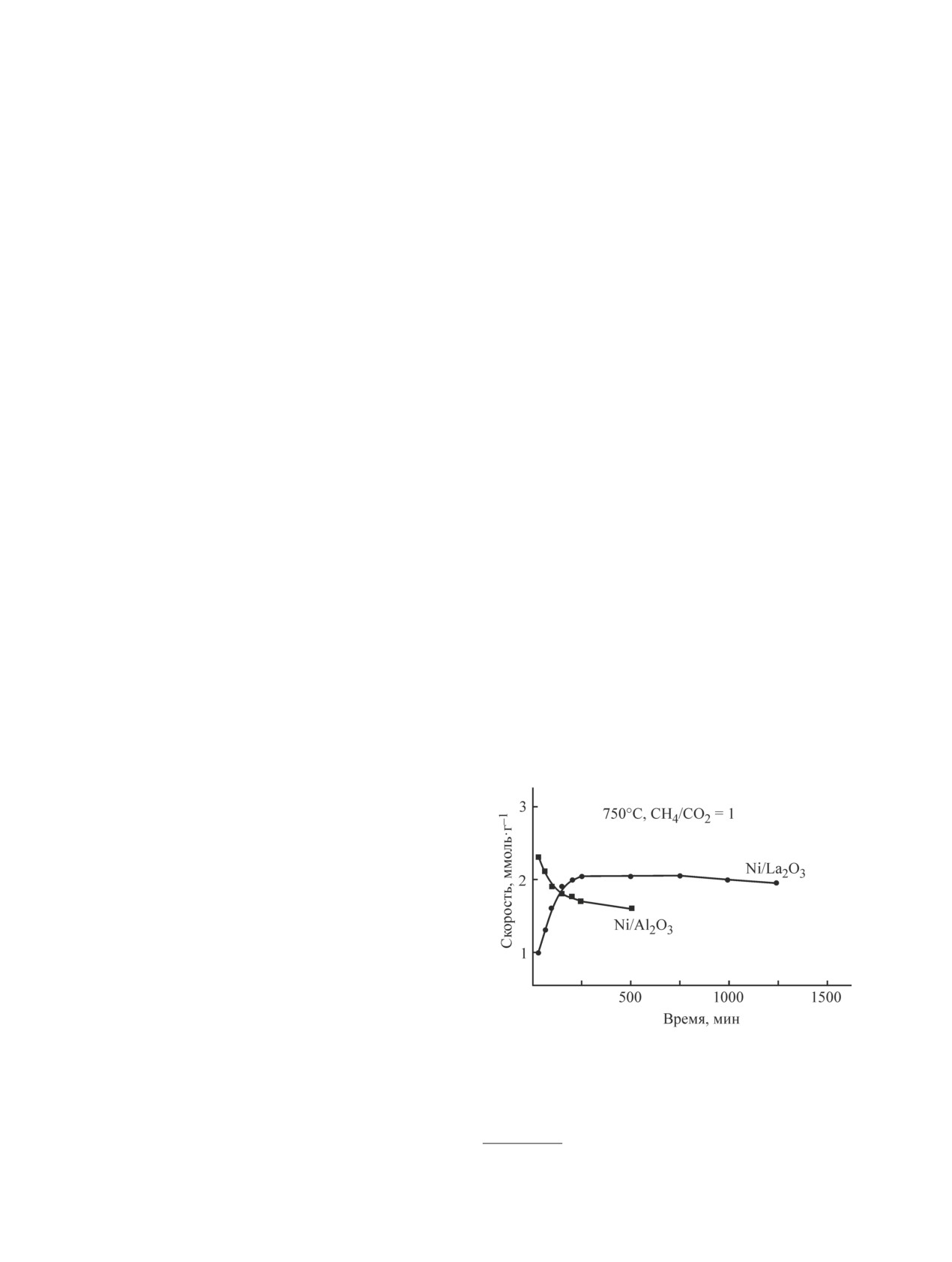
кислотных центрах носителя. З. Чанг с соавт. [36]
гию активации CH4 для протекания реакции диссо-
изучали влияние носителя на активность никелевых
циации. При этом для катализаторов на основе Rh,
катализаторов в углекислотном риформинге мета-
Ru и Pt энергия активации зависит от дисперсности
на. Было установлено, что в случае катализатора на
металла [30], которая определяет частоту оборотов
основе Al2O3 конверсия CH4 выше, чем при исполь-
реакции, что также продемонстрировано в работах
зовании La2O3 в качестве носителя (рис. 3). Авторы
[29, 31]. Д. Вей [29] показал, что реакция взаимо-
выдвинули предположение о том, что кислотные цен-
действия углекислого газа и метана на катализаторе
тры Al2O3 участвуют в активации CH4. Однако в этом
Rh/Al2O3 имеет первый порядок по CH4, к тому же
случае также наблюдается повышенное коксообра-
диссоциация CH4 на родиевых центрах начинает-
зование, приводящее к дезактивации катализатора.
ся уже при 150°C, в то время как для других типов
С течением времени реакции активность Ni/Al2O3
каталитических систем необходима более высокая
существенно снижается, что связано с отравлением
температура. В зависимости от типа носителя реак-
активных металлических центров катализатора и
ция углекислотной конверсии метана может иметь
блокировкой пор носителя образующимися углерод-
различный порядок по CO2: при использовании ок-
ными частицами. В случае же Ni/La2O3 рост скорости
сидов металлов (например, La2O3, SiO2, TiO2 и MgO)
реакции с увеличением времени обусловлен наличи-
реакция имеет первый порядок по CH4 и нулевой по
ем основных центров La2O3, на которых происходит
CO2, в то время как на La2O3 порядок реакции по CO2
активация CO2 и окисление поверхностного углерода,
равен 0.34 [32].
что и объясняет сохранение активности катализатора
Для того чтобы установить, какая стадия процес-
и его устойчивость к дезактивации.
са углекислотной конверсии метана является ско-
Л. Лизи с соавт. [37] обнаружили, что в случае
рость-лимитирующей, было проведено исследование
катализаторов на основе перовскита кислород в
активности катализатора Rh/Al2O3 в превращении
структуре кристаллической решетки участвует в
CD4 и CH4 [33]. Согласно полученным результатам,
активации молекулы CH4. Аналогичные результаты
конверсия CH4 была выше, чем конверсия CD4. Это
получены и в работах Д. Пакхаре с соавт. [23], кото-
свидетельствует о том, что скорость диссоциация свя-
зи С-Н определяет скорость реакции взаимодействия
метана и углекислого газа. Это позволило авторам
сделать вывод о протекании процесса преимуще-
ственно по пути диссоциации метана до монооксида
углерода, причем данная реакция необратима в ука-
занных условиях.
С применением квантово-химических расчетов
было установлено, что диссоциация молекулы CH4,
адсорбированной на активных металлических цен-
трах, может протекать по двум механизмам: прямая
диссоциация с образованием монооксида углерода
[34] и многоступенчатая диссоциация, предполагаю-
щая постадийный разрыв связи С-Н с образованием
CHx или формильной группы и, в конечном счете,
монооксида углерода [35]. Существенно, что оба
Рис. 3. Зависимость скорости реакции углекислотной
механизма реализуются только для катализаторов,
конверсии метана от времени для катализаторов
17 мас% Ni/La2O3 и 17 мас% Ni/Al2O3 при 750°C,
содержащих кислотные центры, или в присутствии
давлении 1 атм и мольном соотношении
окислителя, в качестве которого в данном случае
CH4:CO2 = 1:1 [36].*
может выступать диоксид углерода. При этом пред-
полагается, что активация молекулы CH4 с образо-
* Разрешение на публикацию от издательства Springer
ванием промежуточных соединений начинается при
Letters от 19.05.2020.
770
Недоливко В. В. и др.
рые подтвердили данное предположение с помощью
Rh-Ni/Al2O3. Однако стоит учитывать, что различия в
метода термопрограммируемого восстановления.
активности также могут быть связаны с особенностя-
В работе [38] сообщается, что для активации мо-
ми синтеза катализаторов и дисперсностью активной
лекулы CH4 необходим поверхностный кислород.
фазы на поверхности носителя. Авторы также пока-
В случае кислотных носителей источником кисло-
зали, что в отсутствие металла диссоциация CH4 не
рода могут выступать гидроксильные группы, а для
происходит. Это доказывает, что активация молеку-
основных — карбонатные. Адсорбционные свой-
лы метана происходит на активных металлических
ства кислородных центров, заключенных в структуре
центрах.
кристаллической решетки NiO/MgO, были детально
Новый подход к изучению механизма диссоциации
изучены с применением импульсной хемосорбции
метана был предложен Л. Кианом с соавт. С исполь-
при подаче 18CO2, 18O2, 13CO2 и 13CH4 с изотопной
зованием ядерно-магнитного резонанса 13C и 1H с
меткой [39]. Было установлено, что в адсорбции и
вращением под магическим углом они изучали про-
активации молекул участвуют два типа кислородных
текание реакции углекислотной конверсии метана с
центров, различающихся реакционной способностью
использованием катализатора 1 мас% Rh/SBA-15, а
по отношению к углероду. Для центров первого типа
также силу адсорбции 13CH4 на активных центрах
характерно быстрое взаимодействие с изотопным
катализатора [43]. По спектрам 1Н ЯМР было уста-
углеродом при низких температурах, в то время как
новлено, что около 3/4 1Н, образующегося в ходе
на центрах второго типа, отличающихся от центров
превращения 13СН4, не регистрируется, в результа-
первого типа координационным окружением, адсо-
те чего авторы пришли к выводу, что значительная
рбция протекает относительно медленно даже при
часть активированного СН4 существует в форме СН3.
высоких температурах.
Это означает, что при адсорбции CH4 не происходит
Влияние основных свойств носителя на актива-
диссоциации его молекулы. Данное утверждение
цию CH4 было подробно изучено М. Брэдфордом
справедливо при температурах ниже 550°С. Однако
с соавт. [40], которые использовали ИК-Фурье-
стоит отметить, что некоторое количество 13CH4 под-
спектроскопию для изучения структуры катализа-
вергается диссоциации с образованием продуктов
торов, нанесенных на TiO2, после восстановления
сгорания 13CO2 при температуре выше 300°С, что
водородом. Авторы установили, что появление полос
также соотносится с данными, полученными в работе
поглощения в области 3660 см-1 связано с восстанов-
[28]. При температуре выше 600°С реакция углекис-
лением гидроксильных частиц на поверхности TiO2.
лотной конверсии метана протекает с существенно
Полосы в диапазоне 910 и 960 см-1 свидетельствуют
большими скоростями с образованием 13CO. Также
о разрыве связи Ti-O, что подтверждает образова-
было установлено, что конверсия 13CO2 превышала
ние частиц TiOx на поверхности носителя. Наличие
конверсию 13CH4. Данный факт является доказатель-
частиц TiOx играет важную роль в активации CH4 с
ством того, что адсорбция CO2 протекает быстрее,
последующим образованием CHxO. Однако для Pd- и
чем адсорбция CH4.
Ni-катализаторов данное явление не наблюдалось.
Из вышесказанного следует, что активация моле-
А. Лукредио и соавт. [41] изучали влияние Rh
кулы CH4 является скорость-лимитирующей стадией
на дисперсность Ni-катализатора, нанесенного на
процесса углекислотной конверсии метана и в зависи-
Mg(Al)O (гидроталькит) и γ-Al2O3. Было показано,
мости от температуры может протекать по механизму,
что использование в качестве носителя гидроталькита
приводящему к образованию либо промежуточных
с добавлением Rh обеспечивает образование высоко-
соединений (при температурах ниже 600°C), либо
дисперсной никелевой фазы и вызывает агрегацию
единственного продукта — монооксида углерода при
частиц металла в случае γ-Al2O3. А. Эрдогели и соавт.
температурах выше 600°C. Кроме того, кинетика дис-
[42] обнаружили иной результат, когда изучали вли-
социации CH4 во многом зависит от дисперсности ак-
яние носителя, в качестве которого использовались
тивной фазы катализатора, так как протекает главным
Al2O3, TiO2, SiO2 и MgO, на активность родиевых
образом на металлических центрах, в то время как за
катализаторов в процессе диссоциации CH4. Авторы
активацию СО2 отвечает носитель, кислотно-основ-
наблюдали наибольшую конверсию (21.7%) газо-
ные свойства которого определяют скорость адсорб-
вой смеси на катализаторе Rh/Al2O3. Таким образом,
ции молекул диоксида углерода.
монометаллические родиевые катализаторы на ос-
Механизм активации молекулы CO2. В ходе про-
нове Al2O3 характеризуются существенно большей
цесса углекислотной конверсии метана CO2 активи-
активностью в реакции углекислотной конверсии
руется и восстанавливается до CO, что способствует
метана по сравнению с биметаллическими системами
окислению поверхностного углерода, образующегося
Углекислотная конверсия метана (обзор)
771
в результате активации CH4. Считается, что реакция
носителя существуют и другие факторы, которые
восстановления протекает через образование карбо-
способствуют активации CO2, например образование
натных предшественников в присутствии основных
водорода в результате активации CH4, сила взаимо-
каталитических центров. При этом активация CO2
действия носителя и металла, состав активной ме-
может происходить не только на активных металли-
таллической фазы катализаторов, благодаря которым
ческих центрах, но и на основных участках носителя
происходит восстановление СО2 до СО [50, 51].
или координационно-ненасыщенных центрах атомов
Механизм реакции углекислотной конверсии ме-
кислорода в его структуре (за исключением инерт-
тана. С кинетической точки зрения диссоциация
ных материалов, таких как SiO2) [28, 44]. Так, А. ван
CH4 ввиду относительно невысокой скорости про-
Куелен с соавт. [45] обнаружили, что количество ад-
текания, как правило, является наиболее значимой
сорбированных молекул СО2 на поверхности ката-
стадией процесса углекислотной конверсии метана
лизатора Pt/ZrO2 намного больше, чем количество
[29]. Однако было обнаружено, что при использова-
атомов Pt. Предполагая, что один активный центр Pt
нии некоторых носителей данная стадия не является
взаимодействует с одной молекулой СО2, они про-
скорость-лимитирующей. Б. Пант с соавт. [52] пред-
вели расчет, который показал, что в активации CO2
положили, что CH4 активируется на Pt-центрах с
также участвует носитель.
образованием углерода и водорода при диссоциации.
В работе [46] авторы исследовали природу
Этот углерод окисляется за счет наличия кислорода
углеродных частиц на поверхности катализаторов
в кристаллической решетке перовскита LaCoO3, в
Ni/La2O3 и Ni/Al2O3, чтобы понять, образуются они
результате чего на поверхности носителя образуются
из CH4 или из CO2. Материальный баланс по углеро-
вакансии кислорода. Этот же механизм диссоциации
ду показал, что в случае использования катализатора
CH4 на Pt-центрах и активация CO2 на кислотных
Ni/La2O3 количество CO, образовавшегося в ходе
центрах ZrO2 был описан С. Стаггом с соавт. [49] для
реакции, существенно выше количества израсходо-
катализатора 1.5 мас% Pt/ZrO2. Было обнаружено,
ванных CH4 или CO2. При использовании катализа-
что промотирование La и Ce не влияет на механизм
тора Ni/Al2O3 указанная разница в количестве обра-
процесса, однако приводит к росту скорости проте-
зовавшегося и потребленного углерода существенно
кания промежуточных стадий, в частности скорости
меньше. Авторы связывают это с более высокой ско-
окисления углерода.
ростью образования La2O2CO3 в ходе активации CO2
Зависимость процесса углекислотной конверсии
на La2O3, что приводит к снижению выхода кокса и
метана от температуры и давления в реакционной
увеличению выхода СО. Существенно, что содержа-
среде является причиной разногласий о механизме
ние обратимо адсорбированного CH4 было намного
протекания данной реакции. Для того чтобы разо-
выше, чем CO2. Это доказывает, что активация CO2
браться с влиянием температурного фактора, Я. Куи
на центрах La2O3 существенно выше по сравнению
и соавт. [53] провели исследование кинетики реакции
с CH4.
при постоянном парциальном давлении в интервале
Х. Ванг и соавт. [47] исследовали активность ро-
температур 350-750°С и установили, что скорость
диевых катализаторов, нанесенных на различные ок-
диссоциации CH4 была максимальна в интервале
сиды (CeO2, ZrO2, Nb2O5, Ta2O5, TiO2, La2O3, Al2O3,
температур 550-575°С, тогда как взаимодействие CHx
MgO, Y2O3, SiO2). По результатам испытаний ката-
с CO2 протекало с высокими скоростями в интервале
лизаторы Rh/La2O3 и Rh/MgO оказались наиболее
650-750°С.
стабильными. Авторы связывают это с тем, что ос-
В работе [54] предложен ступенчатый механизм
новные центры на поверхности носителя усиливают
протекания углекислотной конверсии метана на ка-
активацию CO2, ингибируя образование углерода.
тализаторе 0.5 мас% Pt/SrTiO3, предполагающий,
В то же время активация CO2 на кислотных носи-
что активация CH4 происходит на металлических
телях выражена слабее, чем на основных, и проис-
центрах, тогда как CO2 активируется на основных
ходит в основном за счет образования формиатов в
центрах носителя. При этом происходит диссоциация
результате взаимодействия CO2 с поверхностными
молекулы CH4 с образованием активного водорода
гидроксильными группами.
и углерода. Водород может либо десорбироваться,
Таким образом, активация CO2 является отно-
либо реагировать с адсорбированным CO2 с обра-
сительно быстрым процессом в сравнении с акти-
зованием CO и H2O по реакции конверсии водяного
вацией СН4 и происходит в основном на основных
газа. Механизм реакции с участием водорода опре-
центрах носителя или на границе контакта металла с
деляется при этом типом катализатора, температурой
носителем [48, 49]. Помимо основности/кислотности
и поверхностной концентрацией CO2. Вместе с тем
772
Недоливко В. В. и др.
может протекать диссоциация адсорбированного CO2
Данное уравнение скорости реакции учитывает
с образованием монооксида углерода и атомарного
диссоциативную адсорбцию CH4 и молекулярную
кислорода, который участвует в окислении поверх-
адсорбцию CO2. При этом скорость-лимитирующей
ностного углерода с образованием СО.
стадией является взаимодействие углерода, адсорби-
Таким образом, для большинства катализаторов
рованного на поверхности катализатора, с молекулой
углекислотной конверсии метана, за исключением
CO2. Авторы подчеркивают, что кинетическая модель
тех, которые имеют инертные носители в своем со-
реакции может изменяться в зависимости от типа
ставе, реализуются параллельные процессы актива-
используемого катализатора (на основе благородных
ции молекул метана и диоксида углерода на активных
или переходных металлов), диапазона температур и
центрах двух типов, а координация промежуточных
парциальных давлений, однако скорость-лимитирую-
соединений происходит в местах связывания металла
щая стадия при этом одинакова: диссоциация CH4 или
с носителем. В случае же инертного носителя все
окисление поверхностного углерода (в том случае,
процессы протекают на металлических центрах, од-
когда носитель катализатора не является инертным).
нако катализатор в этом случае более подвержен дез-
Были предложены кинетические модели и для
активации, вызванной образованием углерода или
совместного процесса паровой и углекислотной кон-
спеканием активной фазы.
версий метана [53]:
Кинетические модели, применяемые для расчета
CH4 + 2CO2 q H2 + H2O + 3CO.
(22)
скорости реакции углекислотной конверсии метана.
Во многих исследованиях для проведения кинетиче-
Теоретические расчеты проводились на основе экс-
ского анализа реакции углекислотной конверсии мета-
периментальных данных, полученных с использовани-
на применялись наиболее простые модели степенного
ем никелевых катализаторов, нанесенных на активный
закона [55, 56]. Эти модели в большинстве случаев
уголь, оксиды кремния, магния, титана. Уравнение
применялись для объяснения того, как присутствие
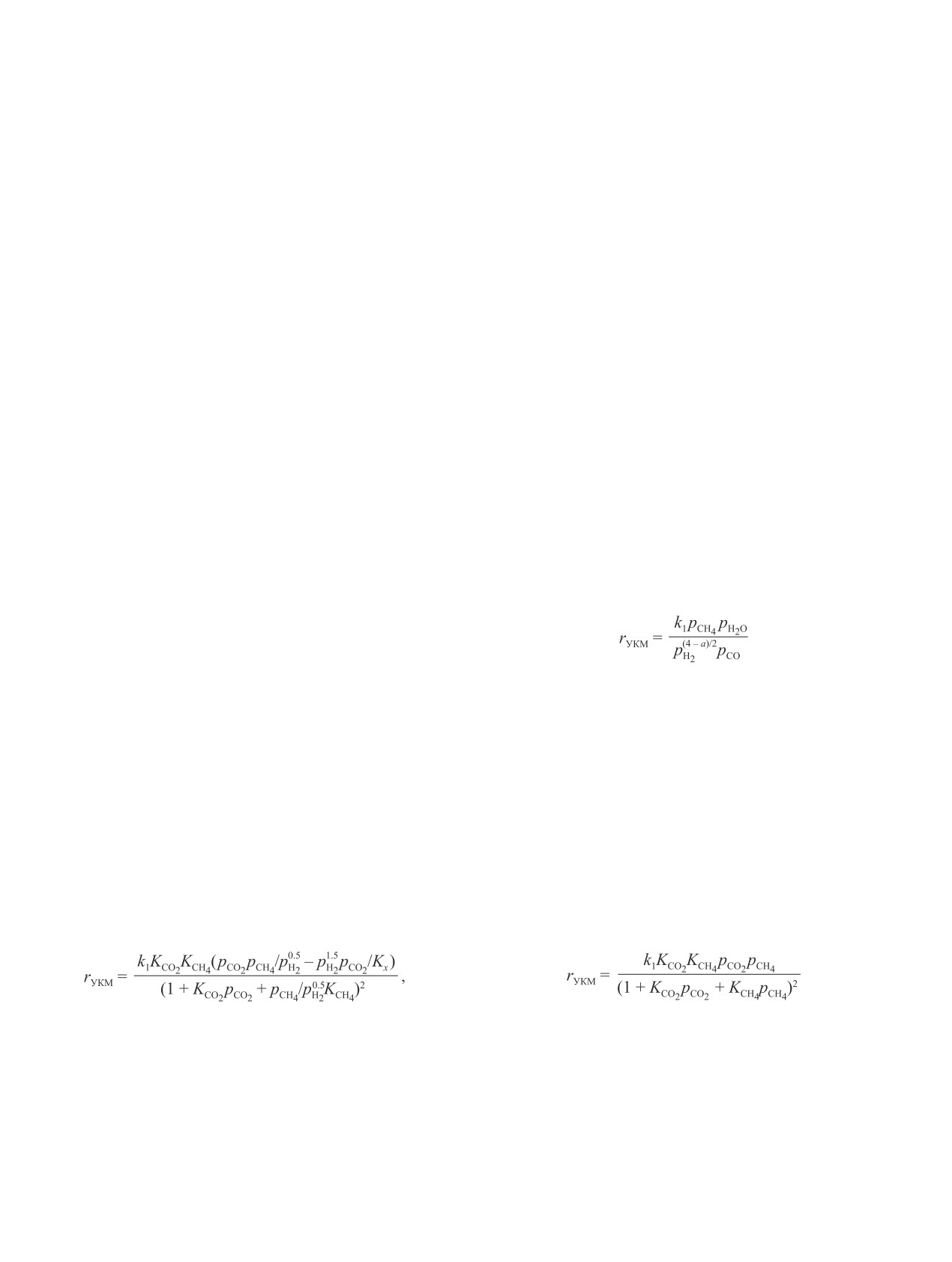
скорости реакции имеет следующий вид [53]:
благородных металлов в качестве промоторов помога-
ет уменьшить образование углерода на катализаторе
,
(23)
Ni/Al2O3. Так, при мольном соотношении Ni:Pt = 75:1
порядок реакции по CO2 равен 1.4, а при мольном
соотношении 33:1 — 0.87. Это говорит о том, что
где pH2O — парциальное давление Н2О; а — количе-
присутствие Pt повышает реакционную способность
ство атомов Н2, образовавшихся в ходе диссоциации
кислорода из CO2 и способствует дальнейшему
молекулы СН4.
его взаимодействию с осажденным углеродом. Pt
Предложены и другие кинетические модели реак-
также снижает ингибирующее влияние CO на про-
ции углекислотной конверсии метана [56, 60]. Так,
текание углекислотной конверсии метана [57, 58].
Д. Ричардсон с соавт. [56], допуская, что адсорбция
М. Куирога и соавт. [59] проводили расчеты ско-
CH4 и CO2 является скорость-лимитирующей ста-
рости реакции углекислотной конверсии метана на
дией, получили выражение для скорости реакции с
катализаторе Ni-Rh/Al2O3, на основании чего предпо-
применением уравнений Ленгмюра-Хиншелвуда-
ложили кинетику данного процесса. Авторы устано-
Хоугена-Уотсона. Авторы показали, что предложен-
вили, что кинетическая модель, которая наилучшим
ная ими теоретическая модель полностью согласуется
образом описывала полученные экспериментальные
с данными, полученными в ходе экспериментов на
данные для катализатора Ni-Rh/Al2O3, имела вид
катализаторе Rh/Al2O3:
(21)
(24)
где rУКМ — скорость реакции углекислотной кон-
М. Марк с соавт. [61], основываясь на экспери-
версии метана; k1 — константа скорости реакции
ментальных данных, предложили модель, соглас-
углекислотной конверсии метана; KCO2, KCH4 — кон-
но которой CH4 диссоциирует на углерод и водород
станты адсорбции СО2 и СН4 соответственно; Kx —
(скорость-лимитирующая стадия), в то время как
константа равновесия реакции сухого риформинга
окисление CHx в CO и диссоциация CO2 в CO проте-
метана при температуре реакции; pCO2, pCH4, pH2,
кает довольно быстро, что нашло подтверждение и в
pCO — парциальные давления СО2, СН4, Н2 и СО
работе [62]. В результате уравнение скорости реакции
соответственно.
с учетом данных допущений имеет вид
Углекислотная конверсия метана (обзор)
773
М. Соуза с соавт. [63] предложили схожую кинети-
ческую модель на основе механизма углекислотной
(25)
конверсии метана на катализаторе Pt/ZrO2. Механизм
включает такие лимитирующие стадии, как дис-
социация CH4 и реакция между адсорбированным
CHx и недиссоциированным адсорбированным CO2.
где KC-z — константа равновесия реакции, обратной
Скорость реакции описывается уравнением
реакции Будуара.
(26)
Таким образом, предложенные кинетические
углерода не всегда влечет за собой дезактивацию
модели основываются на различных допущениях и
катализатора. Б. Коубази с соавт. [67] при проведе-
описывают процесс в заданном диапазоне параме-
нии углекислотной конверсии метана на катализа-
тров (температуры и давления) с учетом природы
торах Ni-Rh/CeZr и Ni/CeZr наблюдали осаждение
активных центров носителя и металла. Однако все
углерода, но в отличие от Ni/CeZr биметаллический
они схожи в том, что скорость-лимитирующей ста-
катализатор, промотированный родием, практически
дией является диссоциативная адсорбция метана или
не подвергался дезактивации. Авторы связывают это
окисление поверхностного углерода (в том случае,
с образованием разного типа углерода (углеродных
когда носитель катализатора не является инертным).
нанотрубок на монометаллическом Ni-катализаторе
и аморфного углерода на биметаллическом Ni-Rh
катализаторе), каждый из которых по-разному влияет
Дезактивация катализатора
на активность катализатора. Так, М. Гарсия с соавт.
и способы ее минимизации
[68] писали, что Pt ингибирует образование углерод-
Факторы, влияющие на морфологию и реакцион-
ных нанотрубок и нитей на катализаторе PtNi/Al2O3.
ную способность частиц адсорбированного углерода.
Однако нанотрубчатый и нитевидный углерод при-
Основной причиной дезактивации катализатора яв-
сутствовал на катализаторе Ni/Al2O3, что являлось
ляется осаждение углерода на его поверхности [64].
основной причиной блокировки активных центров
Образование углерода происходит главным образом
катализатора. Авторы предположили, что образую-
при диссоциации CH4, поскольку CO отсутствует в
щийся в ходе реакции углерод в силу его структур-
исходной смеси. При более длительном протекании
ных особенностей не мог диффундировать в поры
процесса с повышением рабочего давления растет
биметаллического катализатора, как это происходило
содержание СО в потоке газовой смеси, что повы-
в случае монометаллического Ni/Al2O3 [69]. К анало-
шает выход кокса [65]. Баланс между образованием
гичному выводу пришли Д. Ву и соавт. [70], которые
углерода в результате диссоциации CH4 и (или) дис-
наблюдали менее значимое снижение активности
пропорционирования CO и окислением поверхност-
биметаллического катализатора Rh-Ni по сравнению
ного углерода [66] определяет скорость и степень
с монометаллическим Ni-катализатором на основе
осаждения углерода на поверхности катализатора.
нитрида бора.
Реакционная способность углерода, адсорбиро-
Способы снижения дезактивации катализатора.
ванного на поверхности катализатора, определяется
Высокая дисперсность активной металлической фазы
его локализацией по отношению к активным метал-
на поверхности носителя, как правило, снижает вы-
лическим центрам, т. е. зависит от степени их доступ-
ход кокса [71]. Варьируя характеристики носителя,
ности. Углерод, находящийся в непосредственном
тип металла, концентрацию металла и промотора,
контакте с металлом, более химически активен, чем
метод приготовления, можно получать катализато-
углерод, расположенный на большем расстоянии или
ры, характеризующиеся высокой дисперсностью ак-
в порах и (или) на поверхности носителя [49].
тивной фазы и, следовательно, более устойчивые к
Дезактивация катализатора в ходе углекислотной
дезактивации [41].
конверсии метана может происходить не только по
Влияние дисперсности металла на образование
причине осаждения углерода. Существуют и другие
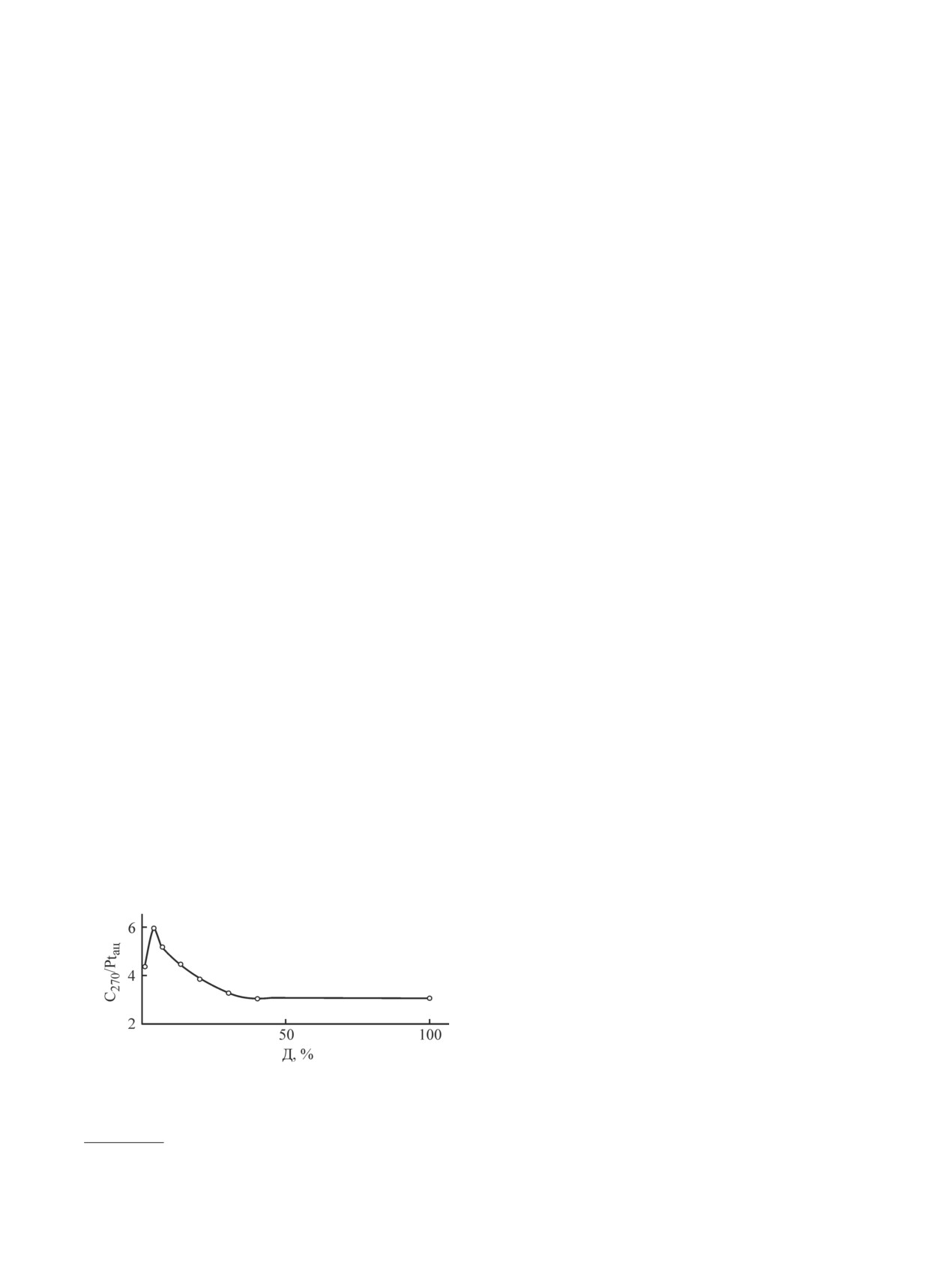
углерода для катализатора Pt/Al2O3 изучал Д. Барбиер
факторы, влияющие в той или иной степени на актив-
с соавт. [51]. На рис. 4 приведена взаимосвязь между
ность катализатора [39, 52]. Кроме того, образование
концентрацией углерода на поверхности катализатора
774
Недоливко В. В. и др.
и дисперсностью Pt, показывающая, что с увеличе-
в ходе экспериментов по термопрограммируемой
нием дисперсности металла содержание углеродных
десорбции O2 на LaCoO3 перовскитного типа на-
отложений существенно снижается.
блюдали максимум десорбированного O2 при 700°C,
Использование носителя с высокой удельной пло-
после чего предположили, что этот O2 участвует в
щадью поверхности (160-300 м2·гкат-1) позволяет
окислении поверхностного углерода во время реак-
улучшить дисперсность металлов [68, 72]. Однако
ции углекислотной конверсии метана на катализа-
в случае микропористых носителей могут возни-
торе Pt/LaCoO3. Известны примеры использования
кать диффузионные ограничения, затрудняющие до-
кислородпроводящих мембранных катализаторов,
ступ реагентов к активным центрам катализатора.
таких как La2NiO4, легированных Pt, которые также
Решением может стать применение носителей, обла-
обеспечивают газификацию поверхностного угле-
дающих бимодальным распределением пор (микро- и
рода, образующегося во время сухого риформинга
макропоры).
метана [77].
В литературе сообщается, что повышение основ-
Включение дополнительных окислителей, таких
ности катализаторов приводит к росту скорости ак-
как H2O или O2, в поток реагентов может также улуч-
тивации CO2, обладающего менее выраженными кис-
шить устойчивость катализатора к дезактивации [66].
лотными свойствами в сравнении с СН4, способствуя
На основании данных термодинамических расче-
тем самым окислению поверхностного углерода [30].
тов для процесса углекислотной конверсии метана
Адсорбированный на поверхности катализатора СО2
в присутствии O2 было установлено, что с ростом
препятствует образованию углерода, накапливающе-
мольного отношения O2:CH4 содержание углерода
гося при диссоциации СН4. В связи с этим добавле-
на поверхности катализатора снижается. М. Гарсия
ние основных промоторов, таких как CeO2, La2O3,
и др. [69] сообщают, что добавление небольших ко-
Nd2O3 и оксидов щелочноземельных металлов (MgO,
личеств перегретого водяного пара в смеси с CH4 и
CaO, SrO, BaO, KО), способствует активации CO2 с
CO2 благоприятствует газификации образующегося в
образованием реакционноспособных карбонатов [73],
ходе реакции углерода на катализаторе Rh-Ni/Al2O3.
в результате чего повышается концентрация атомов
Схожую стратегию проведения процесса углекис-
кислорода, участвующих в окислении углерода, и
лотной конверсии метана с использованием несколь-
тем самым уменьшается степень зауглероживания
ких окислителей описывали М. Сориа с соавт. [78].
катализатора [51, 74].
Они наблюдали, что увеличение концентрации пара
Эффективным методом борьбы с образованием
в потоке реагентов ингибирует реакцию водяного
углерода является включение активного металла в
газа и увеличивает селективность по H2, уменьшая
структуру носителя с высокой подвижностью кисло-
конверсию CO2. Изучая комбинированный процесс
рода [67]. Эта концепция была предложена авторами
углекислотной конверсии метана и парового окис-
работ [23, 75], которые сообщили о способности Ru-
ления CH4, авторы установили, что путем сочета-
и Pt-замещенных пирохлоров за счет содержания в
ния экзотермической реакции парового окисления
их кристаллической решетке реакционноспособного
метана и эндотермической реакции углекислотного
кислорода газифицировать углерод, образующийся
риформинга метана удается оптимизировать теплопе-
на поверхности катализатора. С. Стагг с соавт. [76]
ренос и минимизировать теплопотери и энергозатра-
ты. Несомненным преимуществом данного процесса
также является то, что, изменяя состав исходной га-
зовой смеси (O2 и CO2), можно получить синтез-газ
с заданным мольным отношением H2/CO в интервале
0.5-2.0 [78]. Это также сообщается в работе [79], где
показано, что добавление небольшого количества O2
к сырью значительно увеличивает конверсию CH4 и
уменьшает образование углерода.
Использование благородных металлов и основных
промоторов помогает поддерживать баланс между
Рис. 4. Зависимость содержания углерода на единицу
образованием и окислением углерода, что приводит
активного центра Ptaц (C270/Ptaц) от дисперсности ме-
к повышению срока службы катализатора. При этом
талла для катализатора Pt/Al2O3 [51].*
путем подбора отношения металл/промотор и усло-
* Разрешение на публикацию от издательства Elsevier
вий синтеза можно достичь высокой дисперсности
от 19.05.2020.
активной фазы, что также позволит повысить устой-
Углекислотная конверсия метана (обзор)
775
чивость катализатора к образующемуся углероду за
со 100 до 50% в случае проведения реакции при тем-
счет его высокой активности, коррелирующей с реак-
пературе 850°С и давлении 2 атм. Промотирование
ционной способностью углерода, адсорбированного
благородными металлами Rh, Pt, Pd приводит к
на поверхности.
уменьшению углеродных отложений, что позволяет
сохранить стабильность катализатора при высоких
температурах [85].
Катализаторы углекислотной конверсии метана
В работе [86] авторы продемонстрировали, что
Никелевые катализаторы углекислотной конвер-
увеличение концентрации никеля в катализаторе
сии метана. Традиционными катализаторами угле-
NiMgO до 20 мас% приводит к увеличению катали-
кислотной конверсии метана являются никелевые
тической активности и стабильности в сравнении с
системы на основе оксида алюминия. Существенным
системами Ni/SiO2 и Ni/Al2O3.
недостатком таких систем, ограничивающим их ши-
Использование основных оксидов в качестве но-
рокое применение, является чрезмерное образование
сителей приводит к росту активности катализато-
кокса на поверхности активной фазы. Более устойчи-
ров и их устойчивости к образованию кокса. Так,
выми к образованию кокса являются катализаторы на
при проведении сухого риформинга при темпера-
основе носителей основного характера. Эти матери-
туре 700-900°С наибольшую активность проявил
алы снижают общую кислотность катализатора, что
никелевый катализатор на основе CeO2-Al2O3 [87].
предотвращает протекание кислотно-катализируемых
Максимальные значения конверсий достигались в
реакций крекинга углеводородов. Кроме того, с ро-
случае содержания CeO2 5 мас%. Добавка оксида
стом основности катализатора скорость активации
церия (табл. 2) способствует росту дисперсности ни-
CO2 возрастает, что также замедляет коксообразо-
келя и благоприятствует его восстановлению. Также
вание за счет окисления поверхностного углерода,
благодаря основным свойствам CeO2 углерод на по-
образующегося в результате реакции разложения
верхности катализатора реагирует с СО2 по реакции
CH4. Так, при использовании в качестве носителя ос-
Будуара, что приводит к уменьшению выхода кокса.
новных оксидов TiO2, CaO, MgO содержание частиц
В работе [88] было изучено влияние промоторов
углерода на поверхности катализатора снижается за
Cr2O3 и La2O3 на активность катализатора Ni/MgO.
счет того, что адсорбированный СO2 вступает во вза-
Экспериментально установлено, что введение про-
имодействие с углеродом согласно реакции Будуара
моторов увеличивает устойчивость катализатора к
[80-83].
образованию отложений углерода. Во многом это
В работе
[84] каталитическая система
связано с тем, что промоторы увеличивают степень
Ni0.03Mg0.97O, состоящая из основных оксидов, про-
окисления никеля, что понижает вероятность разло-
являет бóльшую стабильность к образованию кокса,
жения метана до углерода.
чем традиционный катализатор Ni/Al2O3. При низких
Катализаторы на основе благородных металлов.
температурах (порядка 500°С) процесс образования
Металлы платиновой группы проявляют бóльшую
кокса не протекает вовсе, а при 700°С катализатор
каталитическую активность в сравнении с никелевы-
сохраняет активность в течение довольно длительно-
ми каталитическими системами и менее склонны к
го времени. При увеличении температуры до 900°С
коксообразованию, обеспечивая протекание целевой
содержание кокса невелико (менее 1 мас%), а весь ни-
кель восстанавливается до металлического состояния.
Таблица 2
Также авторы выдвигают гипотезу о том, что причи-
Текстурные характеристики каталитических систем
на дезактивации данных каталитических систем не
[87]*
только в осаждении углерода на активных центрах,
Катализатор
SBET, м2·г -1
DNi, нм
но и в окислении Ni0 до NiO, так как металлический
Ni восстанавливает CO2 до монооксида углерода.
Ni/Al2O3
145
13.5
Вместе с тем в восстановительной атмосфере за счет
Ni/1 мас% CeO2-Al2O3
155
10.8
образования водорода NiO может восстанавливаться
Ni/5 мас% CeO2-Al2O3
146
9.3
до Ni0, т. е. катализатор регенерируется.
Ni/10 мас% CeO2-Al2O3
130
6.9
С целью снижения образования кокса на поверх-
ности активной фазы катализатор Ni0.03Mg0.97O
Ni/CeO2
30
—
промотировали оксидами металлов второй группы.
Введение CaO ингибировало осаждение кокса на
* Разрешение на публикацию от издательства Elsevier
катализаторе, однако конверсия метана снижалась
от 19.05.2020.
776
Недоливко В. В. и др.
реакции уже при 450°С. Их существенным недостат-
поверхностью TiO2, что подтверждается данными
ком, ограничивающим применение в промышленно-
термопрограммируемого восстановления водородом.
сти, является высокая стоимость.
Схожие результаты были получены и для нанесенных
Среди нанесенных Ru- и Rh-катализаторов наи-
Ru-катализатоpов, активность которых убывает в
большую активность проявляют катализаторы на
ряду Ru/TiO2 > Ru/Al2O3 > Ru/C.
основе MgO, Al2O3, ZrO2. Промотирование катали-
Эффект сильного взаимодействия металл-носи-
затора Ni0.03Mg0.97O Pt, Pd или Ir (0.01 мас%) также
тель наблюдается также для металлов платиновой
приводит к существенному росту конверсии мета-
группы, нанесенных на TiO2 [28]. Согласно данным
на [89]. Катализаторы Rh/γ-Al2O3, Pt/ZrO2, Rh/ZrO2
ИК-Фурье-спектроскопии in situ, кислород, входящий
проявляют высокую каталитическую активность и
в структуру носителя, может участвовать в актива-
стабильность в углекислотной конверсии метана
ции как СН4, так и СО2. При взаимодействии СН4 с
при 550°С. Так, для катализатора Pt/ZrO2 при 700°С
M/TiO2 (М — металлы Ni, Fe, Cu, Pt, Ir, Rh ) при 500°С
скорость реакции углекислотной конверсии метана
на поверхности образуются частицы СНхО. Так, сре-
возрастает, а при 800°С и концентрации О2 14 мас%
ди систем на основе TiO2 максимальной активно-
практически не изменяется. При содержании О2 по-
стью обладает Pt-катализатор, а на основе M/SiO2 —
рядка 11 мас% конверсия не изменяется в течение
Rh-катализатор.
30 ч. В отсутствие кислорода конверсия снижается с
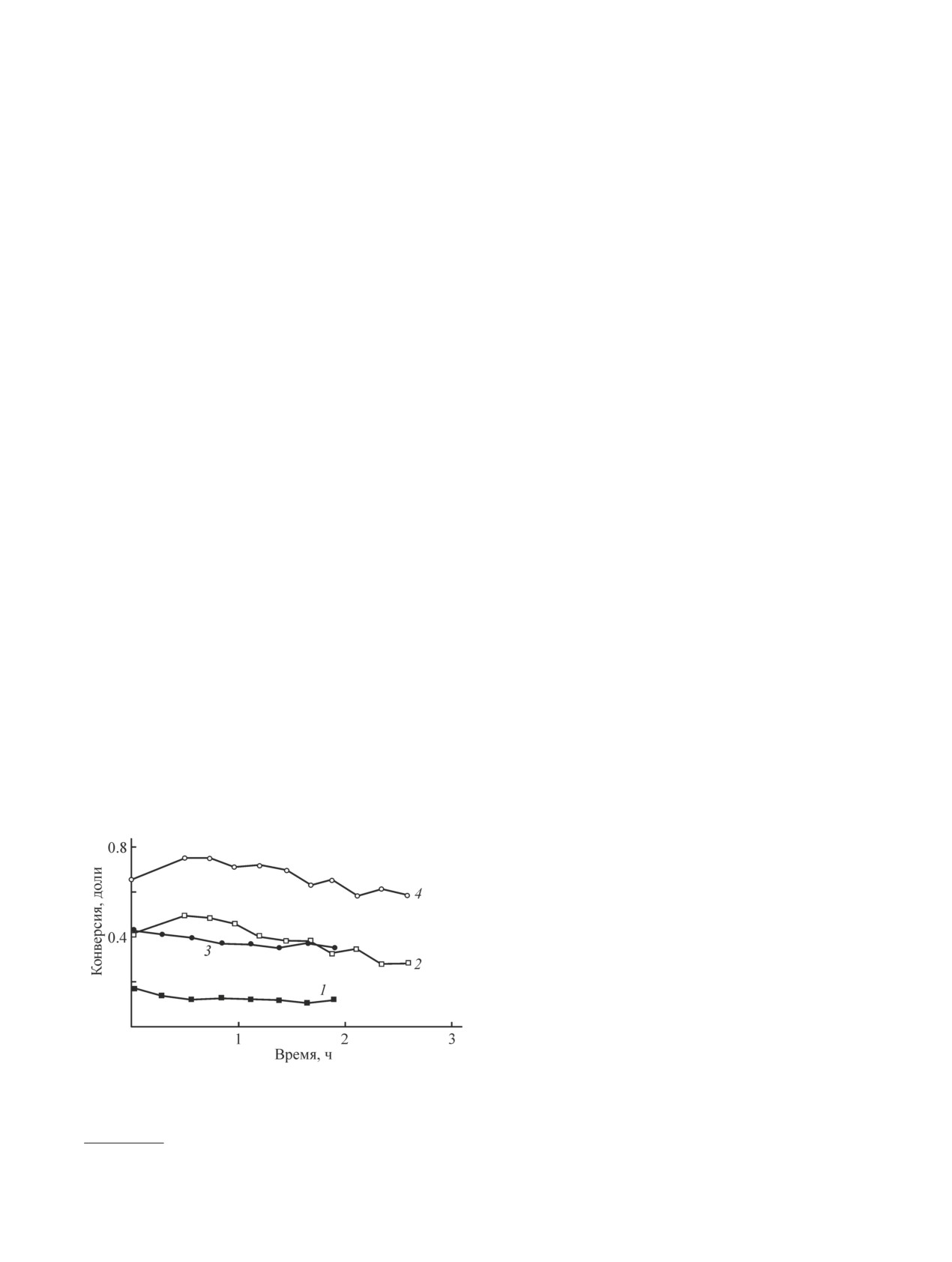
В работе [91] изучен эффект промотирования
75 до 70%. На основании экспериментальных данных
оловом катализаторов Pt/ZrO2 и Pt/SiO2. При про-
было выдвинуто предположение о том, что ZrO2 спо-
питке Pt/ZrO2 солями олова активность и стабиль-
собствует диссоциации СО2, участвующего в окисле-
ность этой системы снижаются (рис. 5), но при изо-
нии углерода, образующегося при диссоциации СН4.
морфном замещении атомов Pt атомами Sn удается
Ряд исследований посвящен возможности ис-
получить активные при 800°С и стабильные катали-
пользования наночастиц Pt в качестве активной фа-
заторы.
зы катализаторов углекислотной конверсии метана
Влияние носителя на активность катализатора и
[40, 90]. Установлено, что при 450°С катализаторы
его устойчивость к коксообразованию. Синтез высо-
Pt/SiO2 и Pt/Cr2O3 быстро дезактивируются, а
коактивных и стабильных катализаторов, устойчивых
Pt/ZrO2 и Pt/TiO2 сохраняют стабильность в течение
к дезактивации, очень важен с экономической точки
100 ч. По данным ИК-спектроскопии авторами статьи
зрения. В качестве активной фазы могут применять-
[40] установлено, что образование углерода на их
ся как переходные (Ni и Co), так и благородные (Rh,
поверхности в указанных условиях не происходит.
Ru, Pd, Pt и Ir) металлы. Катализаторы на основе
Для катализатора Pt/TiO2 характерно сильное вза-
благородных металлов проявляют высокую катали-
имодействие металл-носитель. При этом активные
тическую активность в реакции углекислотной кон-
центры расположены на участках связывания Pt с
версии метана и устойчивы к образованию углерода.
Катализаторы на основе Ni и Co более привлекатель-
ны в связи с их относительно низкой стоимостью.
При этом активность таких систем в ряде случаев
сравнима с катализаторами на основе благородных
металлов, однако они подвержены быстрой дезак-
тивации. С целью увеличения устойчивости к обра-
зованию кокса применяется промотирование систем
на основе Со и Ni благородными металлами, а также
используются основные носители. Роль носителя за-
ключается в обеспечении большой удельной площади
поверхности, а также дисперсности частиц металлов.
Кроме того, устойчивость носителя при высоких тем-
пературах обеспечивает стабильность катализатора
и предотвращает спекание активной фазы. Вместе с
Рис. 5. Зависимость конверсии CH4 (1, 2) и CO2 (3, 4)
тем носитель обеспечивает основность (CaO, La2O3 и
от времени для Pt-Sn/ZrO2 (1, 3) и Pt/ZrO2 (2, 4) при
MgO), наличие координационно-ненасыщенных кис-
800°С [91].*
лородных центров (CeO2, CeO2-ZrO2 и TiO2) и спо-
* Разрешение на публикацию от издательства Elsevier
собность к восстановлению металла (CeO2 и ZrO2),
от 19.05.2020.
подавляя тем самым коксообразование [21].
Углекислотная конверсия метана (обзор)
777
В работе [92] проведено систематическое иссле-
промоторов катализаторов углекислотной конверсии
дование влияния типа носителя, в качестве которо-
метана. Их введение снижает кислотность носителя
го использовались CeO2, Nb2O5, Ta2O5, TiO2, ZrO2,
и тем самым снижает долю реакций крекинга мета-
γ-Al2O3, La2O3, MgO, SiO2 и Y2O3, на активность
на, приводящих к образованию кокса. Повышение
родиевых катализаторов в углекислотной конверсии
основности катализатора также ускоряет активацию
метана. Наибольшей каталитической активностью
молекул CO2, вовлекая их в реакцию, обратную ре-
и стабильностью (табл. 3) обладают катализаторы
Rh/γ-Al2O3 и Rh/MgO. Это обусловлено сильным
Таблица 3
взаимодействием металл-носитель, приводящим к
образованию однородных твердых растворов типа
Активность каталитических систем в реакции сухого
риформинга метана [92]*
шпинелей, таких как MgRh2O4, образование кото-
рых было доказано методами термопрограммиру-
Конверсия,
Температура,
Катализатор
CO2/CH4
емого восстановления водородом и рентгеновской
%
°С
дифракции. В случае применения основных оксидов в
Ni/NaY
1:1
84
600
качестве носителей катализатор на основе Nb2O5 про-
Ni/Al2O3
1:1
36
600
являл низкую активность, а при использовании ZrO2
Ni/SiO2
1:1
14
600
и CeO2 необходима предварительная активация.
Детально влияние носителя на активность ката-
Pd/NaY
1:1
29
600
лизаторов углекислотной конверсии метана изучено
Pt/NaY
1:1
56
600
в работе [62]. Катализатор Ni/MgO-γ-Al2O3 в отличие
KNiCa/Al2O3
1:1
17
650
от Ni/γ-Al2O3 сохранял стабильность в течение 10 ч,
KNiCa/SiO2
1:1
21
650
после чего постепенно дезактивировался. В случае
KNiCa/ZSI
1:1
78
650
Ni/MgAl2O4 по истечении указанного времени актив-
ность сохранялась на прежнем уровне. Авторы связы-
Rh/TiO2
1:1
88
620
вают это с тем, что шпинель MgAl2O4 препятствовала
Rh/SiO2
1:1
5
620
переходу Ni или NiO в неактивную форму NiAl2O4 за
Rh/Al2O3
1:1
85
620
счет сильного взаимодействия Ni с MgAl2O4, что так-
Ni/Al2O3
1:1
85
777
же предотвратило дезактивацию катализатора ввиду
Pd/Al2O3
1:1
73
777
спекания активной фазы.
В работе [93] продемонстрирован синергический
Ru/Al2O3
1:1
65
777
эффект биметаллических катализаторов. Результаты
Rh/Al2O3
1:1
87
777
хемосорбции СО для моно- и биметаллических ката-
Ir/Al2O3
1:1
87
777
лизаторов на основе переходных металлов показали,
CoMgO/C
1:1
68
650
что в случае Ni-Co систем дисперсность металла по
Ni/CaO-MgO
1:1
80
850
данным просвечивающей электронной микроскопии
на 25% выше, чем для монометаллических Ni- или
Rh/Al2O3
1:1
85
800
Co-катализаторов.
Ru/Al2O3
1:1
83
800
Таким образом, варьируя состав металлической
Ru/Eu2O3
1:1
75
650
фазы и подбирая кислотность носителя, можно до-
Ir/Eu2O3
1:1
88
727
биться сильного связывания металл-носитель, обе-
Ru/MgO
1:1
90
690
спечивающего высокую дисперсность активной фазы
Rh/MgO
1:1
88
690
и, как следствие, высокой активности и устойчивости
катализатора к коксообразованию.
Pt/MgO
1:1
85
690
Роль основных центров катализаторов углекис-
Pd/MgO
1:1
84
690
лотной конверсии метана. Образование углерода
Ni/Al2O3
2.38:1
100
940
в результате разложения CH4 происходит преиму-
Ni/MgO-Al2O3
2.38:1
86
938
щественно на кислотных центрах катализатора.
Ni/CaO-Al2O3
2.01:1
88
938
Поддержание оптимального отношения кислотных/
основных центров является ключевым фактором уве-
Ni/CaO-TiO2-Al2O3
2.01:1
100
950
личения стабильности катализаторов углекислотной
конверсии метана. Оксиды щелочных и щелочнозе-
* Разрешение на публикацию от издательства American
мельных металлов широко используются в качестве
Chemical Society от 19.05.2020.
778
Недоливко В. В. и др.
акции Будуара, что обеспечивает окисление поверх-
катализатор было трудно активировать при темпера-
ностного углерода до СО и ингибирует тем самым
туре реакции 800°C. Было обнаружено, что добавле-
коксообразование [94].
ние небольшого количества Pt (0.1 мас%) позволяет
В работе [95] изучена активность никелевых
несколько снизить температуру предварительной об-
катализаторов на основе цеолита, промотирован-
работки H2 благодаря склонности Pt к восстановле-
ных щелочными и щелочноземельными металла-
нию. Pt-Содержащий катализатор Ni/Al2O3 проявил
ми. Добавление K2О и CaO в качестве промоторов
бóльшую активность в углекислотной конверсии ме-
позволило существенно увеличить стабильность
тана в сравнении с Pt/Al2O3 и Ni/Al2O3.
катализаторов. Так, наибольшую активность в угле-
Влияние текстурных характеристик на актив-
кислотной конверсии метана наряду с высокой ста-
ность катализаторов углекислотной конверсии ме-
бильностью показал образец Ni/Al2O3, промотиро-
тана. Упорядоченные мезопористые оксиды кремния
ванный MgO. Добавление небольших количеств CaO
используются в различных областях катализа бла-
также приводило к росту активности Ni/CaO/γ-Al2O3
годаря их высокой удельной площади поверхности.
катализаторов, и, как следствие, конверсия CO2 воз-
Однако их упорядоченная структура, обеспечиваю-
растала.
щая уникальные свойства носителей, разрушается
Авторы [96] исследовали промотированные CaO
при высоких температурах. В связи с этим активно
или MgO никелевые и кобальт-никелевые катализа-
разрабатываются методы, позволяющие увеличить
торы на основе оксида алюминия. Было установлено,
термическую и механическую прочность силикатных
что добавление основных оксидов улучшает сорбци-
мезоразмерных носителей.
онные свойства катализаторов по отношению к H2
В работе [99] изучали активность никелевых ката-
и CO2. Промотирование оксидом магния MgO при-
лизаторов на основе цеолита ZSM-5. Было установ-
водило к тому, что восстановление активной метал-
лено, что активность таких систем в реакции угле-
лической фазы происходило лишь при температурах
кислотной конверсии метана прямо пропорциональна
выше 600°С, что связано с сильным взаимодействием
содержанию доступных активных центров, количе-
MgO с Ni и Co и негативно сказывалось на конверсии
ство которых было оценено по данным импульсной
метана.
хемосорбции H2. Необходимо отметить, что данный
Особенности восстановления активной фазы
катализатор характеризуется большей стабильностью
катализаторов углекислотной конверсии метана.
по сравнению с Ni/SiO2.
Зачастую перед проведением реакции углекислот-
Авторы [100] синтезировали упорядоченные ме-
ной конверсии метана необходима стадия активации
зопористые трехкомпонентные оксиды NiO-CaO-
катализатора для восстановления исходных оксидов
Al2O3 и показали, что данные катализаторы обла-
до активной металлической фазы. При этом степень
дают высокой удельной площадью поверхности, а
восстановления определяет количество доступных
также термически стабильны. Активность никелевых
активных центров катализатора. В некоторых случаях
катализаторов на основе SANR-H, полученного из
слишком сильное взаимодействие между металлом и
природного галлуазита, была изучена в работе [101].
носителем обусловливает необходимость жестких ус-
Наиболее высокие конверсия и селективность по це-
ловий для проведения восстановления. В противном
левым продуктам были достигнуты при использова-
случае возможно образование неактивной фазы или
нии катализатора Ni/SANR-H, носитель для которого
недостаточного количества активных центров.
был получен путем прокаливания галлуазита при
В работе [97] изучено влияние ZrO2 на активность
1000°С, что обеспечило образование высокодисперс-
катализатора Ni/Al2O3. Было обнаружено, что степень
ной металлической фазы. Вместе с тем данный ката-
восстановления NiO, нанесенного на Al2O3-ZrO2,
лизатор оказался наиболее устойчивым к отложению
достигала 0.9, в то время как для NiO на основе Al2O3
углерода и спеканию частиц активного компонента,
она не превышала 0.7. Введение основного ZrO2 бла-
чем катализатор на основе традиционного оксида
гоприятствовало восстановлению активной металли-
алюминия, полученный путем пропитки носителя по
ческой фазы NiO до металлического Ni. Кроме того,
влагоемкости.
ZrO2 предотвращал образование неактивной шпинели
NiAl2O4, что является важным фактором, определя-
Промышленные технологии процесса
ющим степень образования кокса на поверхности
углекислотной конверсии метана
катализатора.
Авторы [98] протестировали катализатор NiO-
Для углекислотной конверсии метана применяют-
MgO в реакции риформинга и отметили, что данный
ся в основном никелевые катализаторы торговых ма-
Углекислотная конверсия метана (обзор)
779
рок ГИАП-3, ГИАП-8, КСП-2, ГИАП-16. Катализатор
полное восстановление оксидной фазы катализатора
ГИАП-16, активный при давлениях до 4 МПа, по-
и регенерация активных центров, так как идет по-
лучают путем механического смешения оксидов
стоянная рециркуляция частиц катализатора через
алюминия, бария и кальцийалюминатного цемента
реактор и зону восстановления.
(талюма) с последующей пропиткой раствором соли
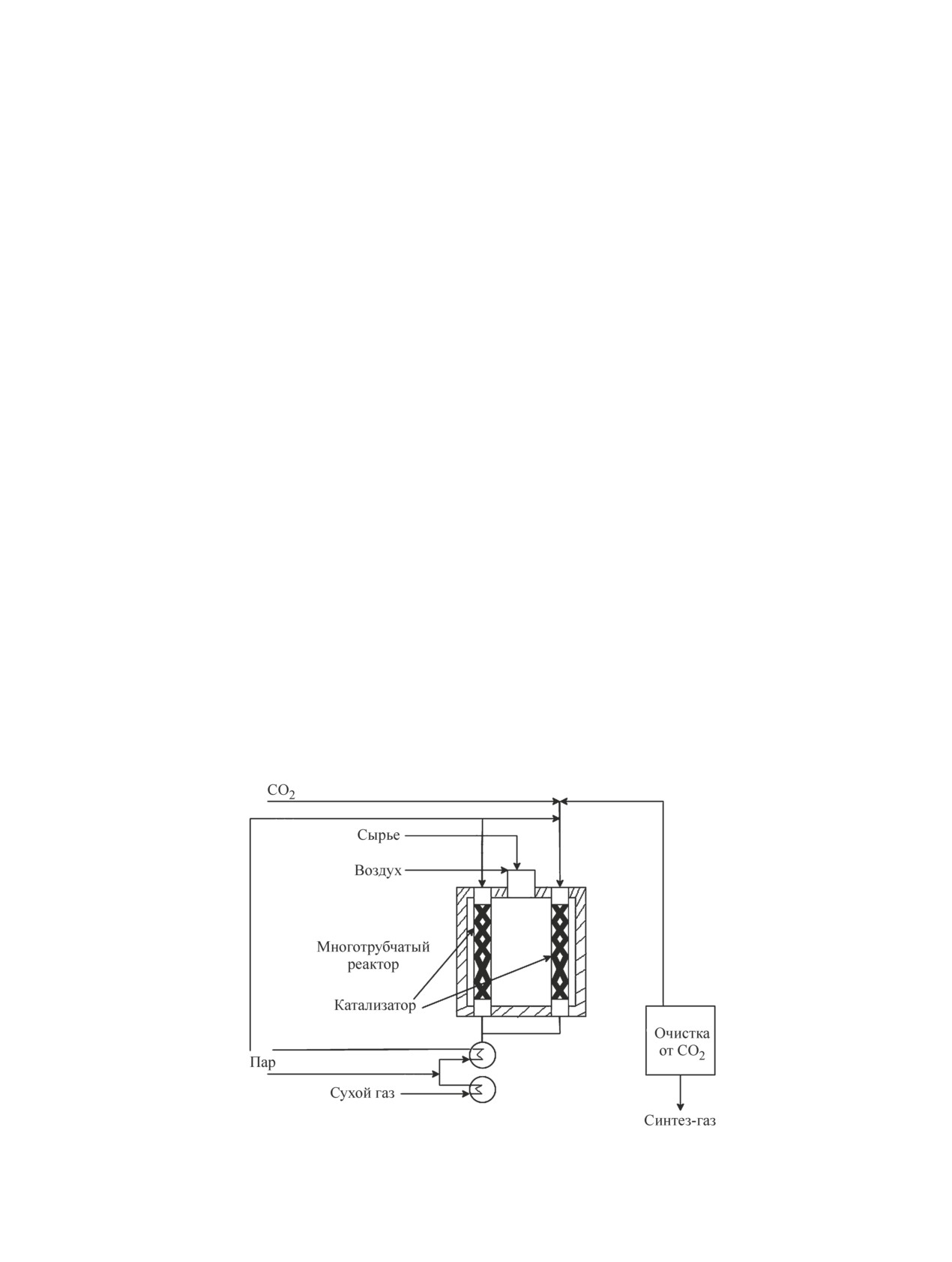
На настоящий момент наиболее перспективными
никеля. Затем следуют стадии полусухого таблетиро-
технологиями углекислотной конверсии метана яв-
вания, гидротермальной обработки и прокаливания
ляются процессы Calcor и SPARG (рис. 7), которые
при 380°С.
частично позволяют решить проблему чрезмерно-
В интервале давлений 2.0-2.5 МПа и объемной
го образования кокса на поверхности катализатора
скорости подачи до 1000 ч-1 применяют как сме-
[105, 106]. Первый проводится при низком давлении
шанный катализатор ГИАП-16, так и катализато-
и высокой температуре. Процесс оптимизируется с
ры повышенной активности ГИАП-8 (8 мас% NiO,
целью уменьшения содержания водорода в соста-
92 мас% Al2O3) и КСН-2 (15 мас% Ni, 83 мас% Al2O3,
ве газовой смеси. Реакция проводится в избытке
3 мас% CaO, 1 мас% MgO). Отметим, что в ката-
углекислого газа. При этом в реакционной смеси не
лизаторах зарубежных компаний содержатся те же
должно содержаться сероводорода. Ввиду сильной
компоненты, но в других количественных соотно-
эндотермичности реакции углекислотной конверсии
шениях. Катализатор RKS-2 (Haldor Topsoe, Дания):
метана часть природного газа используется в качестве
NiO — 8-10 мас%, Al2O3 — 62-64 мас%, MgO — 27-
топлива, которое нагнетается вместе с воздухом в
29 мас%; BC (BASF, Германия): NiO — 8-10 мас%,
инжекционную горелку. В результате смесь метана и
Al2O3 — 2-3 мас%, MgO — 84-88 мас%. Данные
диоксида углерода пропускают через нагретый труб-
катализаторы используют в шахтных реакторах.
чатый реактор, обогреваемый открытым пламенем.
Шахтный реактор углекислотной конверсии метана
Пламя образуется за счет горения топлива (метана)
представляет собой вертикальный аппарат, внутри
и остаточного газа от очистки СО. Синтез-газ затем
которого загружен катализатор. На вход реактора по-
может быть компримирован, а СО — очищен через
дается смесь из природного газа, диоксида углерода
мембраны. Мольный состав синтез-газа на выходе —
и кислорода. Такой тип аппаратов используется для
H2/CO = 0.42/1.
реализации одновременно экзо- и эндотермических
Процесс SPARG (опытно-промышленная уста-
процессов. Обе функции в шахтном реакторе обе-
новка находится в г. Хьюстон, США), разработанный
спечиваются за счет сжигания части сырья, вслед-
ствие чего выделившееся тепло используется для
углекислотной конверсии метана. Шахтный реактор
в промышленности чаще всего используется в па-
рокислородной или пароуглекислотной конверсии
метана. В трубчатых реакторах применяют RKS-1
(Haldor Topsoe, Дания): NiO — 16-18 мас%, Al2O3 —
57-59 мас%, MgO — 24-26 мас% [103].
Все лабораторные исследования процесса угле-
кислотной конверсии метана проводятся в реакторах
с неподвижным или псевдоожиженным слоем ката-
лизатора (рис. 6) [104].
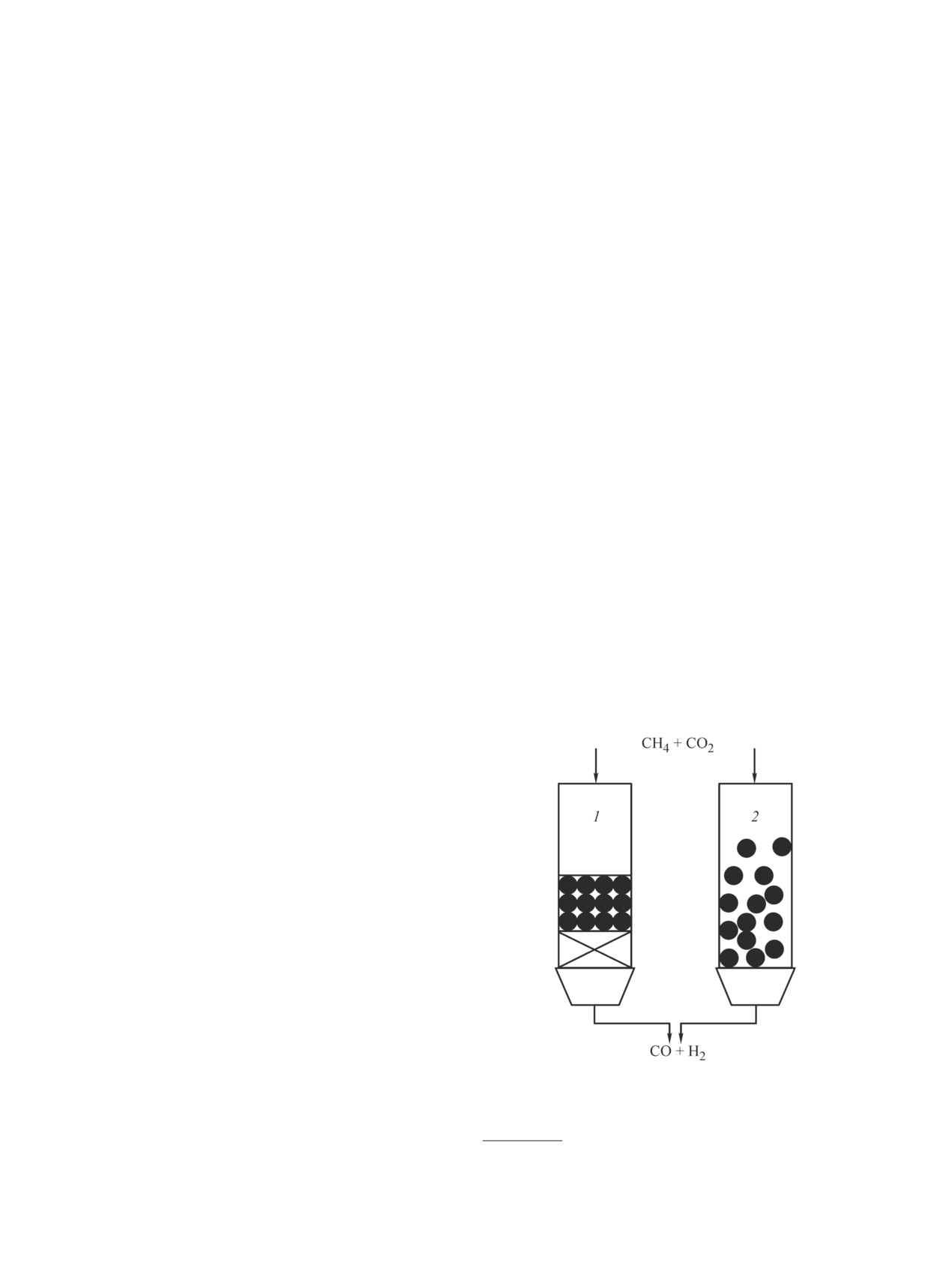
При реализации процесса сухого риформинга ме-
тана в реакторе с неподвижным слоем катализатора
возможна послойная загрузка катализатора. Так, в
работе [104] предлагается использовать в качестве
катализаторов верхнего слоя композиции NiAl2O4 и
NiO/Al2O3, обеспечивающие разложение метана, а в
нижем слое — катализатор, содержащий в качестве
Рис. 6. Варианты процесса углекислотной конверсии
активной фазы Ni0, обеспечивающий селективность
метана в реакторе с неподвижным (1) и псевдоожижен-
по целевым продуктам.
ным (2) слоем катализатора [102].*
Стабильность работы и высокая скорость массопе-
реноса достигается в реакторах с псевдоожиженным
* Разрешение на публикацию от издательства John
слоем катализатора. В таком реакторе происходит
Wiley and Sons от 19.05.2020.
780
Недоливко В. В. и др.
компанией Haldor Topsoe, основан на принципе «про-
К преимуществам данной технологии относятся:
мотирование путем отравления». Отложение углерода
высокая производительность за один проход, низкие
на Ni/Al2О3 подавляется путем пассивации H2S, кото-
эксплуатационные затраты, сниженный объем выбро-
рый подается вместе с потоком газовой смеси метана
сов, операционная готовность выше 99%, простота и
и диоксида углерода. Предполагается, что сера пре-
надежность эксплуатации.
пятствует образованию больших агломератов частиц
Технология SynCORTM позволяет добиться вы-
углерода и тем самым замедляет процесс образования
сокой степени превращения сырья за один проход.
кокса значительно более существенно, чем реакцию
Установки SynCORTM работают при мольном отно-
углекислотной конверсии метана. Согласно данной
шении пар/углерод порядка 0.6. Получаемый син-
технологии, поток нагревается при сгорании топлива
тез-газ находит применение в технологиях по произ-
и остаточного газа в смеси с воздухом. Параллельно
водству аммиака, метанола, жидких углеводородов
в реактор подается пар для контроля процесса отло-
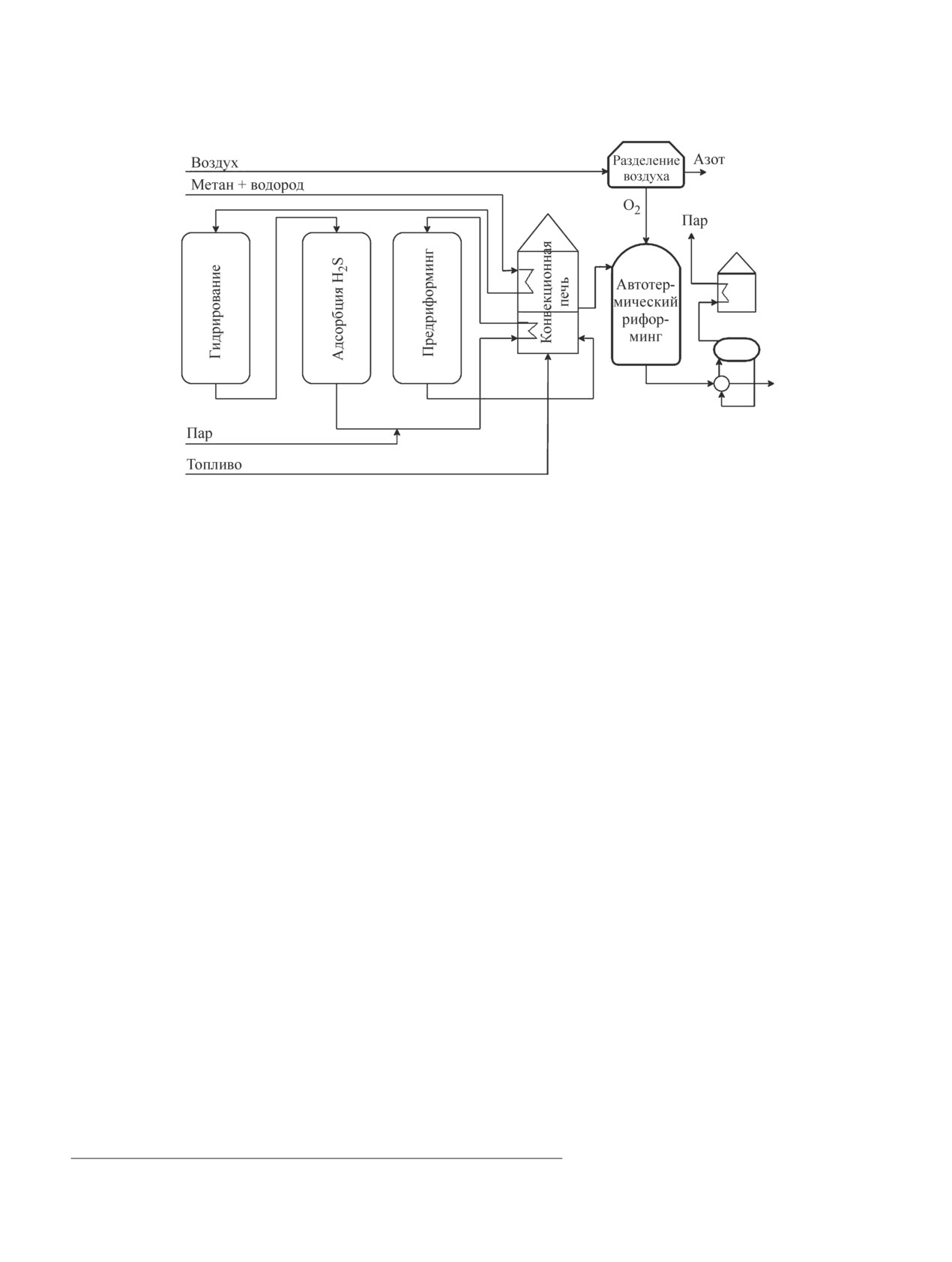
(рис. 8) (GTL).
жения кокса и мольного отношения H2/CO, которое
Согласно технологической схеме, природный газ
может варьироваться в интервале 0.7-1.9. Процесс
предварительно подогревается в конвекционной ка-
применяется для получения синтез-газа, обогащен-
мере печи за счет тепла отходящих газов и затем
ного СО, и восстановления железных руд.
направляется на очистку от сернистых соединений
Масштабной реализации процесса углекислотной
сначала в реактор гидрирования с целью превраще-
конверсии метана препятствует высокая энергоза-
ния всех S-содержащих соединений в сероводород,
тратность. С целью снижения энергозатрат многие
а затем в реактор с оксидом цинка, где поглощается
крупные компании (Haldor Topsoe, BASF, Air Liquids
весь H2S. Гидроочищенное углеводородное сырье
и др.) используют комбинации различных методов
смешивается с водяным паром и поступает в реак-
конверсии природного газа. Чаще всего это совме-
тор предриформинга. Затем полупрореагировавшее
щение процессов паровой и углекислотной конвер-
сырье проходит через радиантные трубы печи, где
сии метана или сухого риформинга с парциальным
нагревается до необходимой температуры процесса и
окислением метана.
поступает в реактор автотермической конверсии, куда
Компанией Haldor Topsoe (Дания) предложен ре-
также подается кислород. Как правило, автотермиче-
актор автотермического риформинга метана. Для
ский риформинг протекает в более жестких условиях,
многих современных крупнотоннажных процессов
чем традиционное парциальное окисление, поэтому
используют технологию автотермического рифор-
оборудование и катализаторы отличаются особой
минга SynCORTMТопсе (ранее известную как ATR).
термостойкостью. Современное оборудование Haldor
Рис. 7. Технологическая схема процесса углекислотной конверсии метана SPARG, Haldor Topsoe (рисунок адапти-
рован из работы [105]).
Углекислотная конверсия метана (обзор)
781
Рис. 8. Принципиальная технологическая схема получения синтез-газа путем автотермической конверсии метана
(Haldor Topsoe) (при создании рисунка использована информация электронных ресурсов компании Topsoe*).
Topsoe включает технологическую горелку, которая
торов, устойчивых к образованию кокса и спеканию
обеспечивает интенсивное горение без образования
под действием высоких температур. Разработка вы-
сажи, безопасность работы, равномерное смешивание
сокоактивных и стабильных катализаторов, устой-
и эффективную термическую конверсию.
чивых к дезактивации, является одной из наиболее
Таким образом, осуществление углекислотной
актуальных задач нефтехимии.
конверсии метана в традиционных реакторах с не-
Эффективность процесса (конверсия метана и
подвижным слоем катализатора сопряжено с рядом
диоксида углерода) зависит от совокупности факто-
проблем: используемые катализаторы склонны к
ров, среди которых особую роль играют температура,
образованию кокса на активной поверхности; для
давление, состав газовой смеси, объемная скорость
достижения высоких степеней превращения сырья
подачи сырьевой газовой смеси. Данные параметры
требуется большая масса катализатора; большие энер-
определяют механизм реакции, влияют на проте-
гозатраты, связанные с эндотермичностью реакции;
кание побочных процессов (реакция водяного газа,
низкая степень использования внутренней поверхно-
коксообразования), конверсию исходного сырья и
сти пор катализатора (для углекислотной конверсии
состав получаемой смеси H2/CO. Ввиду эндотермич-
метана она составляет порядка 6%).
ности реакции сухого риформинга метана процесс
целесообразно проводить при высоких температу-
рах. Оптимальный интервал составляет 700-900°С.
Заключение
Нижняя граница обусловлена стабильностью молекул
Разработка процесса углекислотной конверсии
метана и диоксида углерода, энергия активации кото-
метана имеет огромное значение как с экологической,
рых достаточно высока. При температуре выше 900°С
так и с экономической точек зрения. Вовлечение ди-
происходит чрезмерное образование кокса на поверх-
оксида углерода в технологический процесс позволит,
ности катализатора, которое можно предотвратить,
с одной стороны, существенно сократить его выбросы
варьируя состав газовой смеси. Так, увеличение доли
в атмосферу, а с другой — получать продукты нефте-
СО или О2 в реакционной смеси благоприятствует
химии с высокой добавленной стоимостью, а также
окислению кокса. Подача водяного пара в реактор в
компоненты товарных топлив. Одной из основных
смеси с CH4 и CO2 благоприятствует газификации
проблем, ограничивающих наращивание технологи-
углекислотной конверсии метана в присутствии O2.
ческих мощностей процесса углекислотной конвер-
Активность катализатора и его устойчивость к
сии метана, является отсутствие активных катализа- дезактивации определяются как составом активной
782
Недоливко В. В. и др.
фазы, так и свойствами носителя, отвечающими
алюмомагниевые, никель-лантановые шпинели. При
за активацию молекул метана и диоксида углеро-
этом возможно также использование смешанных ок-
да, определяющих протекание побочных реакций и
сидов NiO-MgO, Al2O3-La2O3, Al2O3-Ce2O2 и т. д.
коксообразование. Для большинства катализаторов
Перспективными носителями катализаторов являются
углекислотной конверсии метана, за исключением
композиты на основе оксидов кремния и алюминия.
тех, которые имеют инертные носители, реализуются
В качестве активной фазы могут применяться как
параллельные процессы активации молекул метана и
переходные (Ni и Co), так и благородные (Rh, Ru,
диоксида углерода на активных центрах носителя и
Pd, Pt и Ir) металлы. Катализаторы на основе благо-
металлической фазы, а координация промежуточных
родных металлов проявляют высокую каталитиче-
соединений происходит в местах связывания металла
скую активность в реакции углекислотной конвер-
с носителем. На металлических центрах носителя
сии метана и устойчивы к образованию углерода.
происходит диссоциация молекулы CH4 с образова-
Катализаторы на основе Ni и Co широко изучаются в
нием углерода и активного водорода, который может
связи с их относительно низкой стоимостью, причем
либо десорбироваться, либо реагировать с адсорбиро-
их активность в ряде случаев сравнима с катали-
ванными на основных центрах носителя молекулами
заторами на основе благородных металлов, однако
CO2 с образованием CO и H2O по реакции конверсии
они подвержены быстрой дезактивации. При этом
водяного газа. Поверхностный углерод может окис-
возможно использование катализаторов на основе
ляться до СО, что препятствует образованию кокса и
переходных металлов, промотированных Pt или Rh.
дезактивации катализатора. CO2 также может претер-
Такие каталитические системы, как правило, более
певать диссоциативную адсорбцию с образованием
активны и менее склонны к образованию кокса на
монооксида углерода и координационно-ненасыщен-
поверхности активной фазы.
ных кислородных вакансий, также благоприятству-
ющих окислению поверхностного углерода до СО.
Финансирование работы
Существенно, что в большинстве случаев активация
метана является лимитирующей стадией процесса.
Работы проведены при финансовой поддержке
Также роль носителя заключается в обеспечении
государства в лице Министерства науки и высшего
большой удельной площади поверхности, а также
образования РФ; уникальный идентификатор работ
дисперсности частиц металлов. Устойчивость носи-
(проекта) RFMEFI60719X0296.
теля при высоких температурах обеспечивает ста-
бильность катализатора и предотвращает спекание
Конфликт интересов
активной фазы.
Важной характеристикой носителя является не
А. Л. Максимов является главным редактором
только его удельная площадь поверхности, но и кис-
Журнала прикладной химии, в остальном авторы
лотность/основность. Поддержание оптимального
заявляют об отсутствии конфликта интересов, тре-
отношения кислотных/основных центров является
бующего раскрытия в данном обзоре.
ключевым фактором увеличения стабильности ката-
лизаторов углекислотной конверсии метана. От кис-
Информация об авторах
лотных и основных свойств носителя также зависит
сила связывания металла с поверхностью, а следова-
Недоливко Владимир Владимирович,
тельно, и дисперсность активной фазы, определяю-
щая активность катализатора. Кроме того, в случае
Засыпалов Глеб Олегович,
сильного взаимодействия металла с поверхностью
носителя предотвращается спекание активной фазы,
Вутолкина Анна Викторовна, к.х.н.,
что также обеспечивает стабильность катализатора.
Вместе с тем необходимо учитывать, что слишком
Гущин Павел Александрович, к.т.н.,
сильное взаимодействие металла с носителем может
вызывать сложности, связанные с восстановлени-
Винокуров Владимир Арнольдович, д.х.н., проф.,
ем оксидной фазы катализаторов до металлической,
или приводить к образованию неактивных частиц.
Куликов Леонид Андреевич, к.х.н.,
В качестве носителей катализаторов чаще всего при-
меняются оксиды кремния, алюминия, магния, це-
Егазарьянц Сергей Владимирович, д.х.н.,
рия, циркония, титана, лантана, алюмоникелевые,
Углекислотная конверсия метана (обзор)
783
Караханов Эдуард Аветисович, д.х.н., проф.,
[10] Aramouni N. A. K., Touma J. G., Tarboush B. A.,
Zeaiter J., Ahmad M. N. Catalyst design for dry
Максимов Антон Львович, д.х.н., чл.-корр. РАН,
reforming of methane: Analysis review // Renew.
Sustain. Energy Rev. 2018. V. 82. P. 2570-2585.
Глотов Александр Павлович, к.х.н.,
[11] Arora S., Prasad R. An overview on dry reforming
of methane: Strategies to reduce carbonaceous
deactivation of catalysts // RSC Adv. 2016. V. 6.
P. 108668-108688.
Список литературы
[1] Sokolov S., Kondratenko E. V., Pohl M. M.,
[12] Nagaoka K. Titania supported ruthenium as a coking-
Barkschat A., Rodemerck U. Stable low-temperature dry
resistant catalyst for high pressure dry reforming of
reforming of methane over mesoporous La2O3-ZrO2
methane // Catal. Commun. 2001. V. 2. P. 255-260.
supported Ni catalyst // Appl. Catal. B: Environmental.
2012. V. 113-114. P. 19-30.
[13] Brungs A. J., York A. P. E., Claridge J. B., Márquez-
Alvarez C., Green M. L. H. Dry reforming of methane
[2] Maestri M., Vlachos D. G., Beretta A., Groppi G.,
to synthesis gas over supported molybdenum carbide
Tronconi E. A C1 microkinetic model for methane
catalysts // Catal. Lett. 2000. V. 70. N 3-4. P. 117-122.
conversion to syngas on Rh/Al2O3 // AlChE J. 2009.
V. 55. N 4. P. 993-1008.
[14] Wang S., Lu G. Q., Millar G. J. Carbon dioxide
reforming of methane to produce synthesis gas over
[3] Naidja A., Krishna C. R., Butcher T., Mahajan D.
metal-supported catalysts: State of the art // Energy
Cool flame partial oxidation and its role in combustion
Fuels. 1996. V. 10. P. 896-904.
and reforming of fuels for fuel cell systems // Prog.
Energy Combust. Sci. 2003. V. 29. P. 155-191. https://
[15] Araujo G. C., de Lima S. M., de Assaf J. M.,
doi.org/10.1016/S0360-1285(03)00018-2
Peña M. A., Fierro, J. L. G., do Carmo Rangel M.
[4] Olah G. A., Goeppert A., Czaun M., Mathew T.,
Catalytic evaluation of perovskite-type oxide
May R. B., Prakash G. K. S. Single step bi-reforming
LaNi1-xRuxO3 in methane dry reforming // Catal.
and oxidative bi-reforming of methane with steam and
Today. 2008. V. 133. P. 129-135.
carbon dioxide to metgas for methanol synthesis // J.
Am. Chem. Soc. 2015. V. 137. P. 8720-8729. https://
[16] Kehres J., Jakobsen J. G., Andreasen J. W.,
doi.org/10.1021/jacs.5b02029
Wagner J. B., Liu H., Molenbroek A., Vegge T.
[5] Yu M., Zhu K., Liu Z., Xiao H., Deng W., Zhou X.
Dynamical properties of a Ru/MgAl2O4 catalyst
Carbon dioxide reforming of methane over promoted
during reduction and dry methane reforming // J. Phys.
NixMg1-xO (111) platelet catalyst derived from
Chem. C. 2012. V. 116. N 40. P. 21407-21415. https://
solvothermal synthesis // Appl. Catal. B: Environmental.
doi.org/10.1021/jp3069656
2014. V. 148. P. 177-190.
[17] Jang W. J., Jeong D. W., Shim J. O., Kim H. M., Roh
H. S., Son I. H., Lee S. J. Combined steam and carbon
[6] Yu M., Zhu Y.A., Lu Y., Tong G., Zhu K., Zhou X. The
dioxide reforming of methane and side reactions:
promoting role of Ag in Ni-CeO2 catalyzed CH4-CO2
Thermodynamic equilibrium analysis and experimental
dry reforming reaction // Appl. Catal. B: Environmental.
application // Appl. Eng. 2016. V. 173. P. 80-91.
2015. V. 165. P. 43-56.
[18] Nikoo M. K., Amin N. A. S. Thermodynamic analysis
[7] Gould T. D., Izar A., Weimer A. W., Falconer J. L.,
of carbon dioxide reforming of methane in view of
Medlin J. W. Stabilizing Ni catalysts by molecular layer
solid carbon formation // Fuel Process. Technol. 2011.
deposition fo harsh, dry reforming conditions // ACS
V. 92. N 3. P. 678-691.
Catal. 2014. V. 4. P. 2714-2717.
[19] Li Y., Wang Y., Zhang X., Mi Z. Thermodynamic
[8] Sternberg A., Jens C. M., Bardow A. Life cycle
analysis of auto-thermal steam and CO2 reforming of
assessment of CO2-based C1-chemicals // Green Chem.
methane // Int. J. Hydrogen Eng. 2008. V. 33. N 10.
2017. V. 19. P. 2244-2259.
P. 2507-2514.
[9] Ewbank J. L., Kovarik L., Kenvin C. C., Sievers C.
[20] Jang W. J., Shim J. O., Kim H. M., Yoo S. Y., Roh H. S.
Carbon dioxide reforming for synthesis gas and
A review on dry reforming of methane in aspect of
hydrogen products // Green Chem. 2014. V. 16. P. 885-
catalytic // Catal. Today. 2019. V. 324. P. 15-26.
784
Недоливко В. В. и др.
[21] Крылов О. В. Углекислотная конверсия метана
[32]
Munera J., Irusta S., Cornaglia L., Lombardo E.,
в синтез-газ // Рос. хим. журн. 2000. Т. 46. № 1.
Vargascesar D., Schmal M. Kinetics and reaction
С. 19-33.
pathway of the CO2 reforming of methane on Rh
[22] Aboonasr Shiraz M. H., Rezaei M., Meshkani F. Ni
supported on lanthanum-based solid // J. Catal. 2007.
catalysts supported on nano-crystalline aluminum
V. 245. P. 25-34.
oxide prepared by a microemulsion method for dry
reforming // Res. Chem. Intermed. 2016. V. 42. N 8.
[33]
Wang H. Y., Ruckenstein E. CH4/CD4 isotope effect
P. 6627-6642.
and the mechanism of partial oxidation of methane
to synthesis gas over Rh/γ-Al2O3 // J. Phys. Chem. B.
[23] Pakhare D., Spivey J. A review of dry (CO2) reforming
1999. V. 103. N 51. P. 11327-11331.
of methane over noble metal catalysts // Chem. Soc.
Rev. 2014. V. 43. N 22. P. 7813-7837.
[34]
Buyevskaya O. V., Wolf D., Baerns M. Rhodium-
catalyzed partial oxidation of methane to CO and H2.
[24] Tomishige K., Nurunnabi M., Maruyama K.,
Transient studies on its mechanism // Catal. Lett. 1994.
Kunimori K. Effect of oxygen addition to steam and
V. 29. N 1-2. P. 249-260.
dry reforming of methane on bed temperature profile
over Pt and Ni catalysts // Appl. Catal. A. 2004. V. 85.
[35]
Nielsen B.,
Luntz A. C., Holmblad P. M.,
Chorkendorff I. Activated dissociative chemisorption
[25] Izquierdo U., Barrio V. L., Requies J., Cambra J. F.,
of methane on Ni(100): A direct mechanism under
Güemez M. B., Arias P. L. Tri-reforming: A new biogas
thermal conditions? // Catal. Lett. 1995. V. 32. N 1-2.
process for synthesis gas and hydrogen production //
Int. J. Hydrogen Energy. 2013. V. 38. N 18. P. 7623-
[36]
Zhang Z., Verykios X. E. Mechanistic aspects of carbon
dioxide reforming of methane to synthesis gas over Ni
[26] Faroldi B., Bosko M. L., Múnera J., Lombardo E.,
catalysts // Catal. Lett. 1996. V. 38. N 3-4. P. 175-179.
Cornaglia L. Comparison of Ru/La2O2CO3
performance in two different membrane reactors for
[37]
Lisi L., Bagnasco G., Ciambelli P., De Rossi S.,
hydrogen production // Catal. Today. 2013. V. 213.
Porta P., Russo G., Turco M. Perovskite-type oxides
P. 135-144.
// J. Solid State Chem. 1999. V. 146. N 1. P. 176-183.
[27] Pakhare D., Shaw C., Haynes D., Shekhawat D.,
[38]
Ferreira-Aparicio P., Fernandez-Garcia M., Guerrero-
Spivey J. Effect of reaction temperature on activity
Ruiz A., Rodriguez-Ramos I. Evaluation of the role
of Pt- and Ru-substituted lanthanum zirconate
of the metal-support interfacial centers in the dry
pyrochlores (La2Zr2O7) for dry (CO2) reforming of
reforming of methane on alumina-supported rhodium
methane (DRM) // J. CO2 Util. 2013. V. 1. P. 37-42.
catalysts // J. Catal. 2000. V. 190. N 2. P. 296-308.
[28] Bitter J. H., Seshan K., Lercher J. A. On the
[39]
Ruckenstein E., Hu Y. H. Role of lattice oxygen
contribution of X-ray absorption spectroscopy to
during CO2 reforming of methane over NiO/MgO
explore structure and activity relations of Pt/ZrO2
solid solutions // Catal. Lett. 1998. V. 51. P. 183-185.
catalysts for CO2/CH4 reforming // Top. Catal. 2000.
V. 10. P. 295-305.
[40]
Bradford M. C., Albert Vannice M. The role of metal-
support interactions in CO2 reforming of CH4 //
[29] Wei J. Structural requirements and reaction pathways
Catal. Today. 1999. V. 50. N 1. P. 87-96. https://
in methane activation and chemical conversion
doi.org/10.1016/S0920-5861(98)00465-9
catalyzed by rhodium // J. Catal. 2004. V. 225. N 1.
[41]
Lucrédio A. F., Assaf J. M., Assaf E. M. Methane
conversion reactions on Ni catalysts promoted with
[30] Hou Z., Chen P., Fang H., Zheng X., Yashima T.
Rh: Influence of support // Appl. Catal. A: General.
Production of synthesis gas via methane reforming
2011. V. 400. N 1-2. P. 156-165.
with CO2 on noble metals and small amount of noble-
(Rh) promoted Ni catalysts // Int. J. Hydrogen Energy.
[42]
Erdohelyi A. Activation of CH4 and its reaction with
2006. V. 31. P. 555-561.
CO2 over supported Rh catalysts // J. Catal. 1993.
V. 141. N 1. P. 287-299.
[31] Yamaguchi A., Iglesia E. Catalytic activation and
reforming of methane on supported palladium
[43]
Qian L., Ren Y., Yu H., Wang Y., Yue B., He H.
clusters // J. Catal. 2010. V. 274. N 1. P. 52-63. https://
Controlled atmosphere 13C and 1H MAS NMR study
doi.org/10.1016/j.jcat.2010.06.001
of reforming route of methane with carbon dioxide
Углекислотная конверсия метана (обзор)
785
over Rh/SBA-15 // Appl. Catal. A: General. 2011.
[55] Erdöhelyi A., Cserényi J., Papp E., Solymosi F.
V. 401. N 1-2. P. 114-118.
Catalytic reaction of methane with carbon dioxide
over supported palladium // Appl. Catal. A: General.
[44]
Guo J., Lou H., Mo L., Zheng X. The reactivity of
1994. V. 108. N 2. P. 205-219.
surface active carbonaceous species with CO2 and its
role on hydrocarbon conversion reactions // J. Mol.
[56] Richardson J. T., Paripatyadar S. A. Carbon dioxide
Catal. A: Chemical. 2010. V. 316. N 1-2. P. 1-7.
reforming of methane with supported rhodium //
Appl. Catal. 1990. V. 61. N 1. P. 293-309. https://
[45]
Van Keulen A. N. J., Seshan K., Hoebink J. H. B. J.,
doi.org/10.1016/S0166-9834(00)82152-1
Ross J. R. H. TAP investigations of the CO2 reforming
[57] Özkara-Aydınoğlu S., Aksoylu A. E. CO2 reforming
of CH4 over Pt/ZrO2 // J. Catal. 1997. V. 166. N 2.
of methane over Pt-Ni/Al2O3 catalysts: Effects of
catalyst composition, and water and oxygen addition
[46]
Tsipouriari V. A., Verykios X. E. Kinetic study of the
to the feed // Int. J. Hydrogen Energy. 2011. V. 36. N 4.
catalytic reforming of methane with carbon dioxide to
P. 2950-2959.
synthesis gas over Ni/La2O3 catalyst // Catal. Today.
2001. V. 64. N 1-2. P. 83-90.
[58] Özkara-Aydınoğlu S., Erhan Aksoylu A. A comparative
study on the kinetics of carbon dioxide reforming of
[47]
Wang H., Ruckenstein E. Carbon dioxide reforming
methane over Pt-Ni/Al2O3 catalyst: Effect of Pt/Ni //
of methane to synthesis gas over supported rhodium
Chem. Eng. J. 2013. V. 215-216. P. 542-549. https://
catalysts: The effect of support // Appl. Catal. A:
doi.org/10.1016/j.cej.2012.11.034
General. 2000. V. 204. N 1. P. 143-152.
[59] Quiroga M. M., Castro Luna A. E. Kinetic analysis
of rate data for dry reforming // Ind. Eng. Chem. Res.
[48]
Ferreira-Aparicio P., Rodrıguez-Ramos I.,
2007. V. 46. P. 5265-5270.
Anderson J., Guerrero-Ruiz A. Mechanistic aspects
of the dry reforming of methane over ruthenium
[60] Luo J. Z., Yu Z. L., Ng C. F., Au C. T. CO2/CH4
catalysts // Appl. Catal. 2000. V. 202. P. 183-196.
reforming over Ni-La2O3/5A: An investigation on
carbon deposition and reaction // J. Catal. 2000.
[49]
Stagg-Williams S. M., Noronha F. B., Fendley G.,
V. 194. N 2. P. 198-210.
Resasco D. Reforming of CH4 over Pt/ZrO2 catalysts
promoted with La and Ce oxides // J. Catal. 2000.
[61] Mark M. F., Maier W. F., Mark F. Reaction kinetics of
V. 194. N 2. P. 240-249.
the CO2 reforming of methane // Chem. Eng. Technol.
1997. V. 20. N 6. P. 361-370.
[50]
Maestri M., Vlachos D., Beretta A., Groppi G.,
Tronconi E. Steam and dry reforming of methane on
[62] Guo J., Lou H., Zhao H., Chai D., Zheng X. Dry
Rh: Microkinetic analysis and hierarchy of kinetic
reforming of methane over nickel catalysts supported
models // J. Catal. 2008. V. 259. P. 211-222. https://
on magnesium aluminate spinels // Appl. Catal. A.
doi.org/10.1016/j.jcat.2008.08.008
2004. V. 273. P. 75-82.
[51]
Barbier J. Deactivation of reforming catalysts by
coking — a review // Appl. Catal. 1986. V. 23. N 2.
[63] Souza M. M. V., Aranda D. A., Schmal M. Reforming
P. 225-243.
of methane with carbon dioxide over Pt/ZrO2/Al2O3 //
J. Catal. 2001. V. 204. N 2. P. 498-511. https://
[52]
Pant B., Stagg-Williams S. M. Investigation of the
doi.org/10.1006/jcat.2001.3398
stability of Pt/LaCoO3 during high temperature
[64] Foo S. Y., Cheng C. K., Nguyen T. H., Adesina A. A.
reforming reactions // Catal. Commun. 2004. V. 5.
Oxidative CO2 reforming of methane on alumina-
P. 305-309.
supported Co-Ni catalyst // Ind. Eng. Chem. Res.
2010. V. 49. N 21. P. 10450-10458.
[53]
Cui Y., Zhang H., Xu H., Li W. Kinetic study of the
catalytic reforming of CH4 with CO2 to syngas over
[65] Kohn M. P., Castaldi M. J., Farrauto R. J. Auto-
Ni/Al2O3 catalyst: The effect of temperature on the
thermal and dry reforming of landfill gas over a
reforming mechanism // Appl. Catal. 2007. V. 318.
Rh/γ-Al2O3 monolith catalyst // Appl. Catal. B:
Environmental. 2010. V. 94. N 1-2. P. 125-133.
[54]
Topalidis A., Petrakis D. E., Ladavos A., Loukatzikou L.
A kinetic study of methane and carbon dioxide
[66] Chettapongsaphan C.,
Charojrochkul S.,
interconversion over 0.5%Pt/SrTiO3 catalysts //
Assabumrungrat S., Laosiripojana N. Catalytic H2O
Catal. Today. 2007. V. 127. N 1-4. P. 238-245. https://
and CO2 reforming of CH4 over perovskite-based
doi.org/10.1016/j.cattod.2007.04.015
La0.8Sr0.2Cr0.9Ni0.1O3: Effects of pre-treatment and
786
Недоливко В. В. и др.
co-reactant/CH4 on its reforming characteristics //
Mater. Sci. 2002. V. 6. N 3. P. 261-269. https://
Appl. Catal. A. 2010. V. 386. P. 194-200.
doi.org/10.1016/S1359-0286(02)00033-5
[78]
Soria M. A., Mateos-Pedrero C., Guerrero-Ruiz A.,
[67] Koubaissy B., Pietraszek A., Roger A. C.,
Rodríguez-Ramos I. Thermodynamic and experimental
Kiennemann A. CO2 reforming of methane over Ce-
study of combined dry and steam reforming
Zr-Ni-Me mixed catalysts // Catal. Today. 2010.
of methane on Ru/ZrO2-La2O3 catalyst at low
V. 157. N 1-4. P. 436-439.
temperature // Int. J. Hydrogen Energy. 2011. V. 36.
N 23. P. 15212-15220.
[68] García-Diéguez M., Pieta I. S., Herrera M. C.,
Larrubia M. A., Alemany L. J. Nanostructured Ni-
[79]
McGuire N. E., Sullivan N. P., Deutschmann O.,
based catalysts for CO2-reforming of // J. Catal. 2010.
Zhu H., Kee R. J. Dry reforming of methane in
V. 270. P. 136-145.
a stagnation-flow reactor using Rh supported on
strontium-substituted hexaluminate // Appl. Catal.
[69] Garcia-Dieguez M., Pieta I. S., Herrera M. S.,
A: General. 2011. V. 394. N 1-2. P. 257-265. https://
Larrubia M. A., Alemany L. J. Rh-Ni nanocatalysts
doi.org/10.1016/j.apcata.2011.01.009
for the CO2 and CO2 + H2O reforming of methane //
[80]
Yang Z. Fluorinated microporous organic polymers:
Catal. Today. 2011. V. 172. P. 136-142.
Design and applications in CO2 adsorption and
conversion // Chem. Commun. 2014. V. 50. P. 13910-
[70] Wu J. C. S., Chou H. C. Bimetallic Rh-Ni/BN catalyst
for methane reforming with // Chem. Eng. J. 2009.
[81]
Foo S. Oxidative CO2 reforming of methane on
V. 148. N 2-3. P. 539-545.
alumina-supported Co-Ni catalyst // Ind. Eng. Chem.
Res. 2010. V. 49. N 21. P. 10450-10458. https://
[71] Gallego G. S., Batiot-Dupeyrat C., Barrault J.,
doi.org/10.1021/ie100460g
Florez E., Mondragón F. Dry reforming of methane
[82]
Yamazaki O. Reduction of carbon dioxide by methane
over perovskites used as catalyst // Appl. Catal. A:
with Ni-on-MgO-CaO containg catalysts // Chem.
General. 2008. V. 334. N 1-2. P. 251-258. https://
Lett. 1992. V. 21. N 10. P. 1953-1954. https://
doi.org/10.1016/j.apcata.2007.10.010
doi.org/10.1246/cl.1992.1953
[72] Tao K., Zhang Y., Terao S., Tsubaki N. Development
[83]
Wang N. Synthesis, characterization and catalytic
of platinum-based bimodal pore catalyst for CO2
performances of Ce-SBA-15 supported nickel catalysts
reforming of CH4 // Catal. Today. 2010. V. 153. P. 150-
for methane dry reforming to hydrogen and syngas //
Int. J. Hydrogen Energy. 2012. V. 37. P. 19-30. https://
[73] Bhavani A. G., Kim W. Y., Kim J. Y., Lee J. S. Improved
doi.org/10.1016/j.ijhydene.2011.03.138
activity and coke resistance by promoters of nanosized
[84]
Yamazaki O. Development of highly stable nickel
trimetallic catalysts for auto-thermal carbon dioxide
catalyst for methane-steam reaction under low steam
reforming of methane // Appl. Catal. A: General. 2013.
to carbon ratio // Appl. Catal. A.: General. 1996.
V. 450. P. 63-72.
V. 136. P. 49-56.
[74] Ghelamallah M., Granger P. Impact of barium and
[85]
Chen Y. Promoting effect of Pt, Pd and Rh noble
lanthanum incorporation to supported Pt and Rh on
metals to the Ni0.03Mg0.97O solid solution catalysts
α-Al2O3 in the dry reforming of methane // Fuel. 2012.
for the reforming of CH4 with CO2 // Appl. Catal.
V. 97. P. 269-276.
A: General. 1997. V. 165. N 1-2. P. 335-347. https://
doi.org/10.1016/S0926-860X(97)00216-0
[75] Haynes D. J., Campos A., Berry D. A., Shekhawat D.,
[86]
Ruckenstein R. E. Combination of CO2 reforming
Roy A., Spivey J. J. Catalytic partial oxidation of
and partial oxidation of methane over NiO/MgO solid
a diesel surrogate fuel using an Ru-substituted
solution catalysts // Ind. Eng. Chem. Res. 1998. V. 37.
pyrochlore // Catal. Today. 2010. V. 155. P. 84-91.
[87]
Wang S., Lu C. Q. Role of CeO2 in Ni/CeO2-Al2O3
[76] Stagg-Williams S. M., Soares R., Romero E.,
catalysts for carbon dioxide reforming of methane //
Alvarez W. E. Metal-support interaction on Pt/ZrO2
Appl. Catal. 1998. V. B19. N 34. P. 267-277. https://
catalysts for the CO2 reforming of CH4 // Elsevier.
doi.org/10.1016/S0926-3373(98)00081-2
2000. V. 130. P. 3663-3668.
[88]
Chen P., Zhang H. B., Lin G. D., Tsai K. R.
Development of coking-resistant Ni-based catalyst
[77] Kharton V., Marques F. M. Mixed ionic-electronic
for partial oxidation and CO2-reforming of methane to
conductors: Effects of ceramic microstructure
syngas // Appl. Catal. 1998. V. A166 (12). P. 343-350.
on transport properties // Curr. Opin. Solid State
Углекислотная конверсия метана (обзор)
787
[89]
Erdöhelyi A. Reaction of CH4 with CO2 and H2O over
[98] Nakagawa Y. Development of Ni-Based catalysts
supported Ir catalyst // Stud. Surf. Sci. Catal. 1997.
for steam reforming of tar derived from biomass
V. 107. P. 525-530.
pyrolysis // Chin. J. Catal. 2012. V. 33. N 4-6. P. 583-
[90]
O′Connor A. M., Ross J. R. H. Dry reforming of methane
[99] Moradi G. Syngas production with dry reforming of
to syn-gas // Abstr. 5th Eur. workshop on methane
methane over Ni/ZSM-5 catalysts // J. Nat. Gas. Sci.
activation. Linerik, Ireland, 1997. V. 1. P. 46-47.
Eng. 2016. V. 33. P. 657-665.
[91]
Stagg S. Effect of promotion with Sn on supported Pt
catalysts for CO2 reforming of CH4 // J. Catal. 1998.
[100]
Xu L. One-pot synthesis of ordered mesoporous NiO-
V. 178. N 1. P. 137-145.
CaO-Al2O3 composite oxides for catalyzing CO2
reforming of CH4 // ACS Catal. 2012. V. 2. N 7.
[92]
Wang S. Carbon dioxide reforming of methane to
produce synthesis gas over metal-supported catalysts //
[101]
Zhao Z. Supported Ni catalyst on a natural halloysite
Appl. Catal. A: General. 1995. V. 133. N 1. P. 149-
derived silica-alumina composite oxide with
unexpected coke-resistant stability for steam-CO2
[93]
Dalai A. K. Effets of metal content on activity and
dual reforming of methane // RSC Adv. 2016. V. 6.
stability of Ni-Co bimetallic catalysts for CO2
N 55. P. 49487-49496.
reforming of CH4 // Appl. Catal. A: General. 2008.
V. 339. P. 121-129.
[102]
Fan M., Abdullah A. Z., Bhatia S. Catalytic
technology for carbon dioxide reforming of methane
[94]
Carrara C. Kinetic and stability studies of Ru/La2O3
to synthesis gas // ChemCatChem. 2009. V. 1. P. 192-
used in the dry reforming of methane // Top. Catal.
2008. V. 51. N 1-4. P. 98-106.
[103]
Лапидус А. Л., Голубева И. А., Жагфаров Ф. Г.
Газохимия. М.: РГУ нефти и газа им. И. М. Губ-
[95]
Dias J. Influence of calcium content in Ni/CaO/
кина, 2013. C. 328-330.
γ-Al2O3 catalysts for CO2-reforming of methane //
[104]
Ван дер Остеркамп П., Вагнер Э. Углекислотная
Catal. Today. 2003. V. 85. P. 59-68.
конверсия метана с использованием мембран-
ных катализаторов // Рос. хим. журн. 2000. Т. 44.
[96]
Sengupta S. Modifying alumina with CaO or MgO in
С. 34-35.
supported Ni and Ni-Co catalysts and its effect on dry
[105]
Teuner S. C., Neumann P., Von Linde F. CO
reforming of CH4 // J. CO2 Util. 2015. V.10. P. 67-77.
through CO2 reforming: The Calcor standard and
Calcor economy processes // Oil Gas Eur. Mag.
[97]
Li H. Study on CO2 reforming of methane to syngas
2001. V. 27. N 3. P. 44-46.
over Al2O3-ZrO2 supported Ni catalysts prepared via
[106]
Rostrup-Nielsen J. 40 years in catalysis // Catal.
a direct sol-gel process // Chem. Eng. Sci. 2004. V. 59.
Today. 2006. V. 111. Р. 4-11.
P. 4861-4867.