Журнал прикладной химии. 2020. Т. 93. Вып. 8
ОСОБЫЕ ТЕХНОЛОГИЧЕСКИЕ РЕШЕНИЯ
УДК 543.544.45
ПОЛУЧЕНИЕ ПОВЕРХНОСТНО-ПОРИСТЫХ СОРБЕНТОВ
НА ОСНОВЕ ДИОКСИДА КРЕМНИЯ
И ИЗУЧЕНИЕ ИХ АДСОРБЦИОННЫХ СВОЙСТВ
© Ж. В. Фаустова, Ю. Г. Слижов, Т. Н. Матвеева
Национальный исследовательский Томский государственный университет,
634050, г. Томск, пр. Ленина, д. 36
Поступила в Редакцию 30 ноября 2019 г.
После доработки 24 февраля 2020 г..
Принята к публикации 11 июня 2020 г.
Синтезированы сорбенты со слоем диоксида кремния на поверхности широкопористого носителя
Хроматон N-AW. Методом низкотемпературной адсорбции/десорбции азота изучена зависимость
текстурных характеристик (удельной площади поверхности и размера пор) полученных материалов
от количества тетраэтоксисилана, наносимого на Хроматон N-AW, и от pH-среды синтеза. Метода-
ми растровой электронной микроскопии, pH-метрии, термогравиметрического анализа, газовой хро-
матографии исследованы характеристики поверхности и адсорбционные свойства синтезированных
материалов. Установлено, что при синтезе сорбентов в кислой среде формируются образцы с разме-
рами пор 2-4, в щелочной — 13-16 нм. При увеличении количества тетраэтоксисилана наблюдается
уменьшение полярности сорбентов, специфической теплоты адсорбции по отношению к тестовым
соединениям и числа электронодонорных центров поверхности, при этом доля электроноакцепторных
центров поверхности существенно возрастает.
Ключевые слова: золь-гель синтез; диоксид кремния; адсорбция; газовая хроматография
DOI: 10.31857/S0044461820080137
Диоксид кремния является одним из наиболее
среды, мольного соотношения реагирующих компо-
востребованных соединений, применяемым в раз-
нентов и наличия темплатов. Варьирование условий
личных процессах химической технологии при
синтеза [1-5] позволяет получать силикагели линей-
концентрировании и разделении веществ. Широкое
ного или разветвленного строения, что оказывает
использование силикагелей обусловлено их меха-
влияние на пористость структуры и эксплуатацион-
нической прочностью, термической стабильностью,
ные характеристики.
радиационной устойчивостью, низкой каталитиче-
Материалы на основе диоксида кремния, приме-
ской активностью, а также возможностью создания
няемые в адсорбции и катализе, как правило, имеют
на их основе материалов с определенными морфоло-
широкое распределение пор по размерам и форме.
гическими характеристиками. Одним из основных
Упорядоченная структура мезопор способствует рав-
способов получения силикагелей является золь-гель
номерной диффузии молекул в сорбенте и катализа-
метод. Состав и строение силикагелей, полученных
торе, что существенно повышает перспективность
золь-гель методом, зависят главным образом от при-
использования данных материалов [6]. Кроме того,
роды применяемого прекурсора, pH реакционной
на однородных поверхностях наблюдается более рав-
1170
Получение поверхностно-пористых сорбентов на основе диоксида кремния и изучение их адсорбционных свойств
1171
номерное распределение модификаторов в процессе
путем формирования слоя SiO2 на поверхности ди-
модифицирования для получения материалов с тре-
атомитового носителя Хроматон N-AW с удельной
буемыми характеристиками.
площадью поверхности ~1 м2·г-1), со значением pH
Сорбционные материалы, полученные с исполь-
изоионного состояния (pHИИС) 7.8. Таким образом,
зованием темплатов, как правило, имеют большую
была получена серия образцов материалов, при син-
удельную площадь поверхности, поэтому чаще всего
тезе которых использовали различное количество
используются при разделении легколетучих соеди-
тетраэтоксисилана (0.0015, 0.003, 0.006, 0.02, 0.03,
нений и не находят широкого применения в газохро-
0.04 моль) в расчете на 1 г носителя. Синтез прово-
матографическом анализе высококипящих веществ
дили в присутствии соляной кислоты или водного
из-за значительного их удерживания, а в процессах
раствора аммиака.
сорбционного концентрирования — вследствие низ-
С использованием HCl в качестве катализатора
кой степени десорбции компонентов.
были получены сорбенты Хроматон N-AW + SiO2(HCl)
В связи с этим особый интерес представляет изуче-
при следующем мольном соотношении компонен-
ние закономерностей формирования поверхностно-по-
тов: 1.0 ТЭОС:0.3 С16-ЦТАБ:0.1 HСl:5.4 Н2О:20.0
ристых сорбентов с заданной толщиной активного
С2Н5ОН [9, 10]. При таком же соотношении реаген-
слоя диоксида кремния и текстурными характеристи-
тов были получены образцы SiO2(HCl) без диатомито-
ками, применение которых позволяет существенно
вого носителя Хроматон N-AW.
уменьшить диффузионные процессы массообмена
В спиртово-аммиачной среде сорбенты синте-
за счет увеличения скорости массопередачи между
зировали модифицированным методом Штобера
газовой и твердой фазами, сокращения времени диф-
(Хроматон N-AW + SiO2(NH4OH, метод Штобера)) [11]
фузии молекул адсорбата в пористом слое неподвиж-
при мольном соотношении реагентов 1.0 ТЭОС:0.015
ной фазы, повышает эффективность и экспрессность
С16-ЦТАБ:0.2 NH4OH:67.5 Н2О:15.0 С2Н5ОН [12].
разделения компонентов анализируемых смесей [7].
Определение удельной площади поверхности и
Целью работы — получение поверхностно-пори-
пористости сорбентов проводили с помощью автома-
стых сорбентов для газовой хроматографии на основе
тического газоадсорбционного анализатора TriStar II
диатомитового носителя Хроматон N-AW с заданной
с применением объемного варианта сорбционного
удельной площадью поверхности, толщиной актив-
метода. Удельную площадь поверхности рассчиты-
ного слоя, изучение их текстурных характеристик и
вали методом Брунауэра-Эммета-Теллера (БЭТ) в
адсорбционных свойств.
автоматическом режиме по изотерме низкотемпера-
турной сорбции паров азота после вакуумирования
при 200°С в течение 2 ч. Объем пор определяли при
Экспериментальная часть
относительном давлении p/p0 → 0.99. Размер пор
Для синтеза поверхностно-пористых сорбентов
рассчитывали по данным десорбционной ветви изо-
на основе диоксида кремния использовали диато-
термы методом Баррета-Джойнера-Халенды (BJH).
митовый носитель Хроматон N-AW (0.20-0.25 мм,
Относительная погрешность метода составляет 10%.
ООО «ХромЛаб» ), тетраэтоксисилан (ТЭОС) (ос.ч.
Морфологию поверхности изучали с помо-
14-5, ТУ 2637-187-44493179-2014, АО «ЭКОС-1»),
щью растрового электронного микроскопа Hitachi
цетилтриметиламмоний бромид (С16-ЦТАБ)
TM-3000 при ускоряющем напряжении 15 кВ в усло-
(≥99 мас%, AMRESCO), HCl (х.ч., ГОСТ 3118-77,
виях режима снятия заряда с образца (электронная
АО «ЭКОС-1»), спирт этиловый (ГОСТ 5962-2013,
пушка: 5·10-2 Па, камера для образца: 30-50 Па).
96.32 мас% «Люкс»), аммиак водный (ГОСТ 3760-79,
Толщину синтезированного слоя рассчитывали
≥25 мас%), бидистиллированную воду. Бидистиллят
по увеличению массы исходного носителя Хроматон
получали с помощью системы очистки воды Sartorius
N-AW после формирования слоя SiO2 и по величине
arium Pro UV (Германия).
удельной площади поверхности полученных мате-
Частицы диоксида кремния, синтезированные
риалов. Погрешность расчетов не превышает 10%.
золь-гель методом, как правило, имеют размер
Количество адсорбированной воды (nH2O) и сила-
5-100 нм [8], что ограничивает использование дан-
нольных групп (nOH) на поверхности синтезирован-
ного материала для заполнения насадочных колонок,
ных сорбентов определяли из данных термогравимет-
применяемых в газовой хроматографии, вследствие
рии по уравнению [13]
возникновения диффузионных затруднений процес-
сов массообмена и продолжительности анализа. В на-
(1)
шей работе сорбенты зернением 0.2-0.3 мм получали
1172
Фаустова Ж. В. и др.
где (WT0 - WTf in) - потеря массы (мас%) в интервале
Обсуждение результатов
температур Т0-Тf in, М(Н2О) — молекулярная масса
воды (г·моль-1).
Диоксид кремния, синтезированный золь-гель
Число молекул воды (NH2O) и ОН-групп (NOH) на
методом в кислой среде, имеет большую удельную
1 нм2 рассчитывали по уравнениям
площадь поверхности (~1000 м2·г-1) и полидис-
персность с преобладанием мелкой фракции раз-
мером менее 0.10 мм, что затрудняет его примене-
(2)
ние в качестве сорбента для газовой хроматографии.
Синтезированные образцы Хроматон N-AW + SiO2 в
условиях кислотного катализа обладают мезопори-
(3)
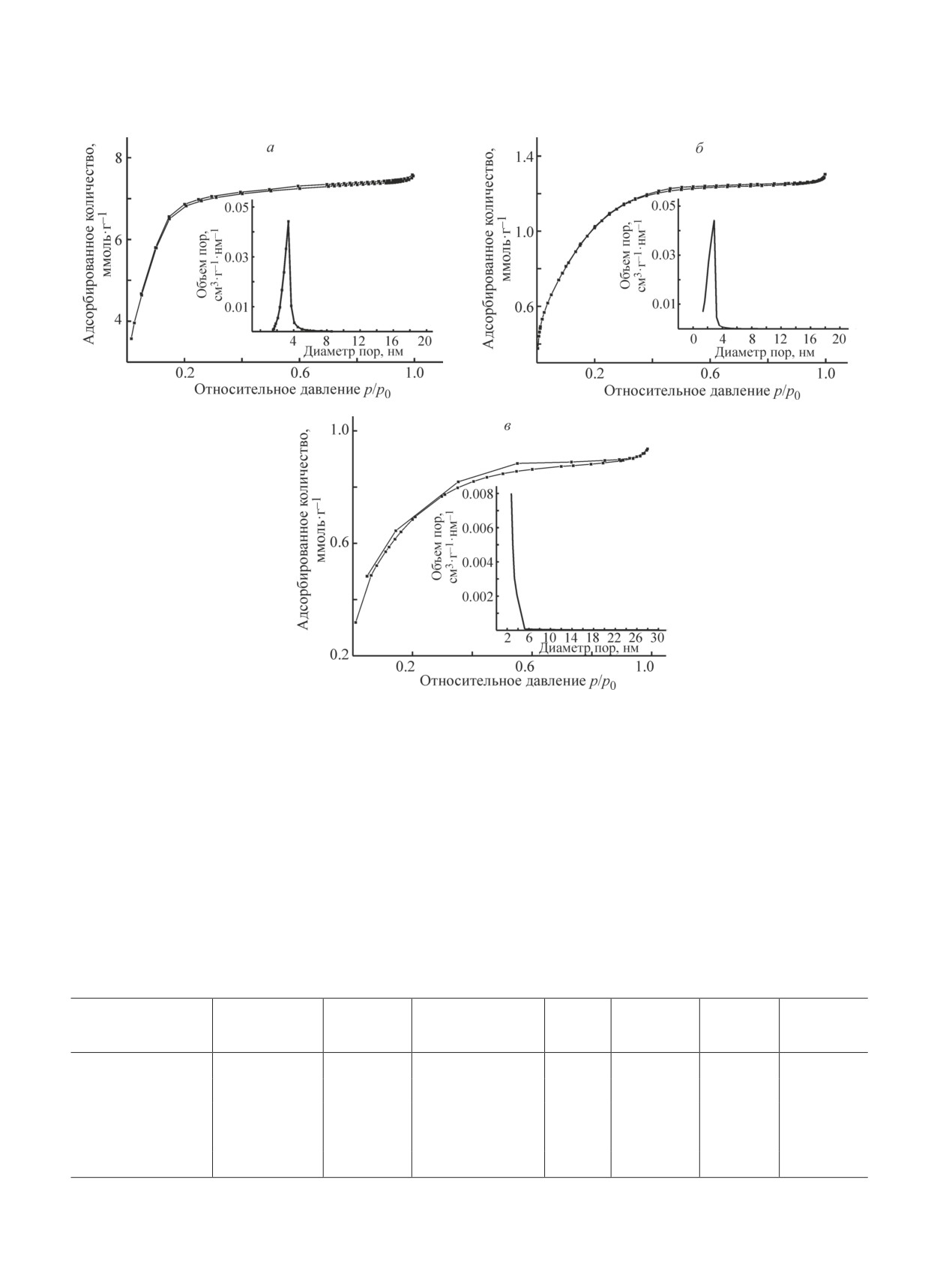
стой структурой с размером пор 2-4 нм. Изотермы
адсорбции, полученные на данных образцах, относят-
где n — число молей воды или OH-групп (ммоль·г-1),
ся к I типу по классификации IUPAC, имеют узкую
NА — число Авогадро (моль-1), Sуд — удельная пло-
петлю гистерезиса, свидетельствующую о наличии
щадь поверхности образца (м2·г-1).
мелких пор (рис. 1). Такие изотермы характерны для
мезопористых силикатных материалов со структурой
МСМ-41. Изотерма адсорбции на образце, получен-
проводили в одинаковых условиях: при постоянной
ном при количестве тетраэтоксисилана 0.0015 моль,
скорости нагревания — 10 град·мин-1, навеске образ-
имеет более широкую петлю гистерезиса, материал
ца 3 мг, в интервале температур 30-1000°С в воздуш-
содержит микро- и мезопоры.
ной атмосфере.
На основании текстурных характеристик со-
Кислотно-основные свойства поверхности иссле-
рбентов Хроматон N-AW + SiO2(HCl), полученных
дуемых сорбентов определяли методом pH-метрии по
золь-гель методом в условиях кислотного катализа
изменению значений pH водных суспензий образцов
(HCl) с различным количеством тетраэтоксисилана
во времени на pH-метре МУЛЬТИТЕСТ ИПЛ-111 с
(табл. 1), установлено, что при уменьшении количе-
комбинированным электродом ЭСК-10601/7 [14, 15].
ства тетраэтоксисилана происходит снижение удель-
Адсорбцию различных тестовых соединений на
ной площади поверхности и объема пор, при этом
полученных сорбентах изучали газохроматографи-
размер пор изменяется незначительно.
ческим методом с использованием газового хрома-
Образцы, синтезированные в условиях щелоч-
тографа МАЭСТРО 7820 (Agilent Technologies) с
ного катализа одновременным смешением компо-
пламенно-ионизационным детектором в изотерми-
нентов и добавлением тетраэтоксисилана порциями
ческом режиме. В работе использовали металличе-
через равные промежутки времени (метод Штобера),
ские наполненные колонки длиной 1 м и внутренним
имеют более крупные поры (13-15 нм) по сравне-
диаметром 3 мм. Расход газа-носителя (гелий) —
нию с образцами, синтезированными в кислой среде
30 см·мин-1.
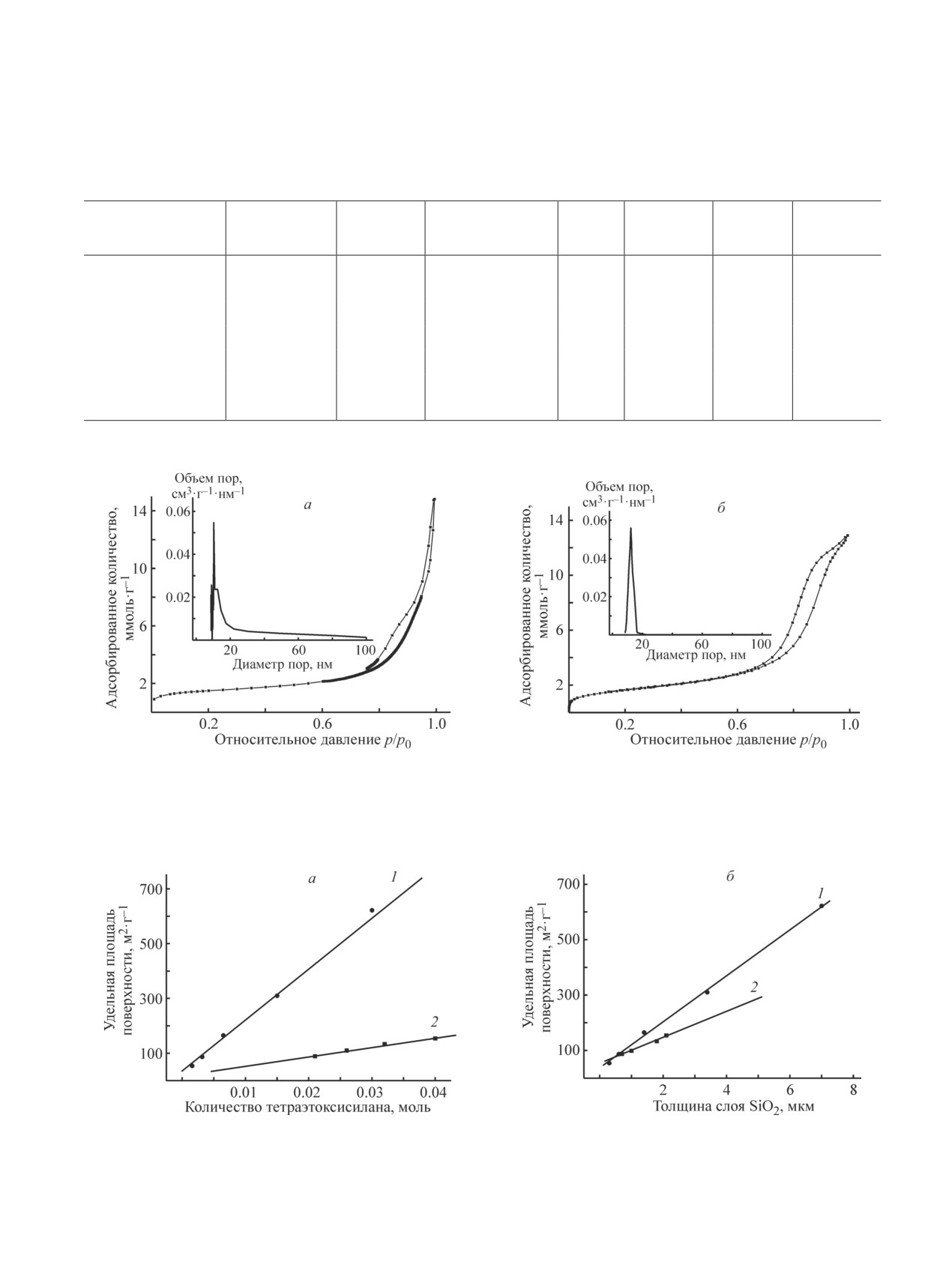
(табл. 2). Изотермы адсорбции, полученные на дан-
По хроматографическим данным рассчитывали
ных материалах (рис. 2), относятся к IV типу [17,
удельные объемы удерживания, отнесенные к еди-
18], петли гистерезиса не выходят на плато при от-
нице поверхности адсорбента, Vg,1, которые при
носительных давлениях, близких к давлению насы-
малых объемах вводимой пробы представляют со-
щенного пара, относятся к типу H3 и характерны для
бой константы Генри адсорбции K1,С (см3·м-2) [16].
материалов, состоящих из агрегатов со щелевидными
Изменения стандартной дифференциальной мольной
порами.
°
) и дифференциальной мольной те-
Установлена прямолинейная зависимость удель-
плоты адсорбции (qdif,1) определяли исходя из зави-
ной площади поверхности от количества тетраэток-
симости [16]
сисилана (рис. 3) при синтезе сорбентов на основе
диатомитового носителя Хроматон N-AW в кислой и
(4)
щелочной среде с использованием цетилтриметилам-
моний бромида в качестве темплата, что позволяет
где qdif,1 — дифференциальная мольная теплота ад-
получать материалы с требуемой удельной площадью
°
= ΔS
°
— изменение стандарт-
поверхности и пористостью.
ной дифференциальной мольной энтропии.
На снимках исходного носителя Хроматон N-AW,
Для всех тестовых соединений погрешность опре-
полученных с помощью растровой электронной ми-
° не превышала 10%.
кроскопии (рис. 4), отчетливо видны остатки диато-
Получение поверхностно-пористых сорбентов на основе диоксида кремния и изучение их адсорбционных свойств
1173
Рис. 1. Изотермы адсорбции-десорбции азота и распределение пор по размерам на образцах Хроматон N-AW + SiO2,
полученных в кислой среде с различным количеством тетраэтоксисилана: а — 0.04, б — 0.003, в — 0.0015 моль.
мий. После формирования слоя силикагеля четкие
пленкообразующий раствор в течение 24 ч, кото-
контуры диатомий пропадают, поверхность носителя
рый равномерно наносится на поверхность носителя
Хроматон N-AW покрывается слоем SiO2. При синте-
Хроматон N-AW.
зе SiO2 в щелочной среде частицы силикагеля обра-
Число силанольных (≡Si-OH) групп мезопористых
зуются уже через 20 мин после добавления раствора
сорбентов зависит от условий синтеза данных мате-
тетраэтоксисилана и адсорбируются на поверхности
риалов и по разным источникам [8, 17] изменяется
носителя. В кислой среде формируется прозрачный
в пределах 0.8-7.0 групп/нм2. Количество сорбиро-
Таблица 1
Текстурные характеристики сорбентов, синтезированных в кислой среде (pH 2), с различным количеством
тетраэтоксисилана
Количество
Толщина
Объем
Средний
Константа
Емкость
Удельная площадь
Образец
тетраэтоксиси-
слоя SiO2,
пор,
размер пор,
уравнения
монослоя,
поверхности, м2·г-1
лана, моль
мкм
см3·г-1
нм
БЭТ
ммоль·г-1
SiO2
—
1023
0.27
2.1
219
10.49
Хроматон N-AW +
0.03
7.0
622
0.17
2.5
201
6.38
+ SiO2
0.006
1.4
165
0.06
2.5
56
1.69
0.003
0.6
87
0.05
2.6
45
0.89
0.0015
0.3
54
0.03
2.5
93
0.56
1174
Фаустова Ж. В. и др.
Таблица 2
Текстурные характеристики сорбентов, синтезированных в щелочной среде (pH 10), с различным количеством
тетраэтоксисилана
Количество
Толщина
Объем
Средний
Константа
Емкость
Удельная площадь
-1Образец
тетраэтокси-
слоя SiO2,
пор,
размер пор,
уравнения
монослоя,
поверхности, м2·г-1
силана, моль
мкм
см3·г-1
нм
БЭТ
ммоль·г-1
SiO2 (метод
0.03
—
324
0.91
10.1
94
3.32
Штобера)
Хроматон
0.02
0.7
89
0.34
12.4
100
0.96
N-AW + SiO2
0.03
1.8
133
0.52
13.4
91
1.36
(метод Штобера)
0.04
2.1
154
0.52
12.6
84
1.58
Хроматон
0.03
1.1
110
0.51
15.5
126
1.13
N-AW + SiO2
Рис. 2. Изотермы адсорбции-десорбции азота и распределение пор по размерам на образцах Хроматон N-AW +
+ SiO2, полученных при 0.03 моль тетраэтоксисилана в щелочной среде одновременным смешением компонентов
(а), методом Штобера (б).
Рис. 3. Зависимость удельной площади поверхности от количества тетраэтоксисилана (а) и толщины слоя SiO2 (б)
при синтезе сорбентов на основе диатомитового носителя Хроматон N-AW в кислой среде (1), в щелочной среде
методом Штобера (2).
Получение поверхностно-пористых сорбентов на основе диоксида кремния и изучение их адсорбционных свойств
1175
Рис. 4. Результаты растровой электронной микроскопии поверхности исходного носителя Хроматон N-AW (а) и
сорбентов Хроматон N-AW + SiO2, полученных в щелочной среде методом Штобера с количеством тетраэтоксиси-
лана 0.03 моль (б), в кислой среде с количеством тетраэтоксисилана 0.0015 моль (в), в кислой среде с количеством
тетраэтоксисилана 0.006 моль (г).
ванной воды и поверхностных гидроксильных групп
удельной площадью поверхности, количество физи-
определяли методом ТГ/ДТА [19]. Полученные ре-
чески сорбированной воды уменьшается, что связано
зультаты (табл. 3) свидетельствуют о закономерном
с уменьшением числа кислотных центров адсорбции
увеличении числа OH-групп на образцах с большей
Льюиса на поверхности (рис. 5).
Таблица 3
Содержание гидроксильных групп на поверхности сорбентов Хроматон N-AW + SiO2,
синтезированных с различным количеством тетраэтоксисилана: а — 0.0015, б — 0.003, в — 0.006, г — 0.03 моль
— в кислой среде (1), в щелочной среде методом Штобера (2), по данным термогравиметрического анализа
Удельная
Содержание физически сорбированной воды
Содержание гидроксильных групп
площадь по-
количество
количество
число групп
Образец
потеря массы
число молекул
потеря массы
верхности,
адсорбированной
групп ОН,
ОН,
Н2О, %
воды, групп/нм2
ОН, %
м2·г-1
воды, ммоль·г-1
ммоль·г-1
групп/нм2
1а
54
0.30
0.17
1.86
0.25
0.28
3.10
1б
87
0.28
0.16
1.08
0.32
0.36
2.46
1в
165
0.23
0.13
0.47
0.52
0.58
2.11
2г
133
0.19
0.11
0.48
0.38
0.42
1.91
1176
Фаустова Ж. В. и др.
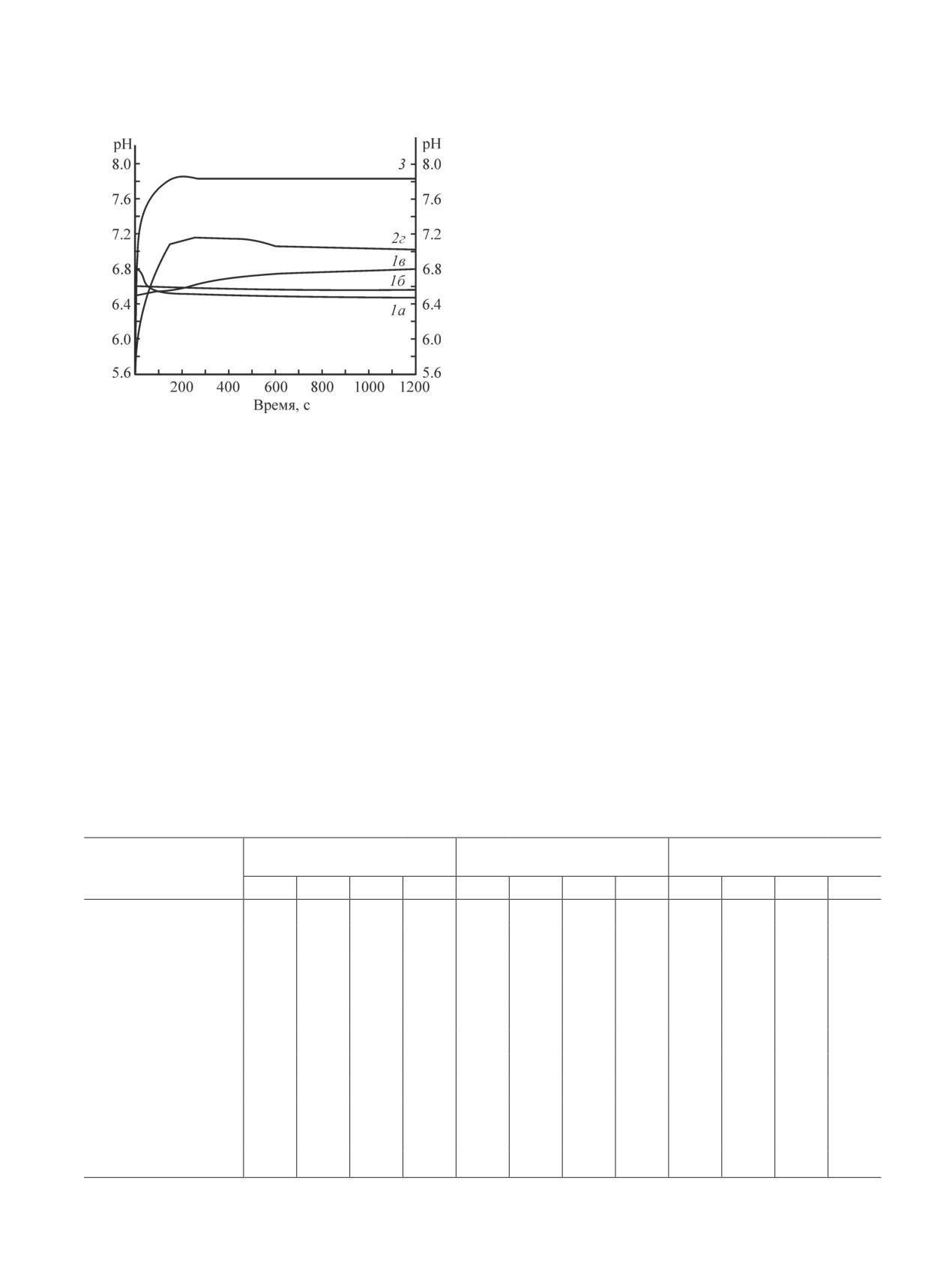
В начальный момент времени контакта образца
Хроматон N-AW + SiO2(NH4OH, 0.03, метод Штобера) с во-
дой значение pH водной суспензии увеличивается
(рис. 5, кривая 2г), что свидетельствует о преобла-
дании на поверхности данного сорбента центров ос-
новного типа, в качестве которых выступают атомы
кислорода силоксановых связей — основные центры
Льюиса. Значение рНИИС 7, что позволяет исполь-
зовать данный сорбент для разделения соединений,
имеющих кислотный, основный и нейтральный ха-
рактер, а при дальнейшем его модифицировании
способствует с большей точностью оценить вклады
модифицирующих добавок в процессы адсорбции и
разделения.
Результаты pH-метрических исследований об-
Рис. 5. Изменение рН водных суспензий во времени
разцов Хроматон N-AW + SiO2, синтезированных
исходного носителя Хроматон N-AW (3) и сорбентов
с использованием HCl (рис. 5, кривые 1а-1в), сви-
Хроматон N-AW + SiO2, синтезированных с различным
количеством тетраэтоксисилана: а — 0.0015, б — 0.003,
детельствуют о слабокислотном характере поверх-
в — 0.006, г — 0.03 моль — в кислой среде (1), в щелоч-
ности сорбентов. В начальный момент времени
ной среде методом Штобера (2).
контакта образца с водой значение pH водной су-
спензии Хроматон N-AW + SiO2(HCl, 0.0015) умень-
Результаты исследования кислотно-основных
шается (рис. 5, кривая 1а), что свидетельствует о
свойств поверхности исходного носителя Хроматон
преобладании на поверхности исследуемого сорбента
N-AW методом рН-метрии полностью совпадают с
кислотных центров Льюиса, в качестве которых вы-
литературными данными [17], в частности, кислот-
ступают атомы кремния, а также кислотных центров
ная обработка приводит к блокированию основных
Бренстеда — свободных гидроксильных групп. Для
центров твердого носителя и способствует форми-
образцов Хроматон N-AW + SiO2(HCl, 0.003) и Хроматон
рованию поверхности слабощелочного характера с
N-AW + SiO2(HCl, 0.006) (рис. 5, кривые 1б, 1в) не на-
рНИИС 7.8.
блюдается скачкообразных изменений pH среды, что
Таблица 4
Термодинамические характеристики адсорбции тестовых соединений на сорбентах Хроматон N-AW + SiO2,
синтезированных с различным количеством тетраэтоксисилана: а — 0.0015, б — 0.003, в — 0.006, г — 0.03 моль
— в кислой среде (1), в щелочной среде методом Штобера (2)
Удельный удерживаемый объем
Изменение энтропии адсорбции,
Теплота адсорбции, кДж·моль-1
при 150°C, мл·г-1
Дж·моль-1·K-1
Адсорбат
1а
1б
1в
2г
1а
1б
1в
2г
1а
1б
1в
2г
Гексан
7
7
31
4
63
52
42
38
175
156
122
128
Гептан
12
15
63
8
65
57
46
44
173
160
125
135
Нонан
27
68
222
26
60
64
49
53
153
164
120
147
Бензол
10
12
32
6
80
54
34
44
202
155
102
139
Толуол
18
28
80
12
81
67
37
50
206
180
102
147
Нитропропан-1
10
13
36
31
96
55
42
65
248
158
120
174
Метанол
7
8
21
8
87
74
46
36
231
205
127
117
Этанол
17
16
47
16
89
77
49
55
234
207
136
155
Ацетон
33
46
112
24
88
74
54
52
290
194
130
146
Бутанон-2
68
54
227
56
96
68
58
44
244
175
143
118
Гептен-1
12
18
59
13
92
53
38
43
237
151
106
130
Получение поверхностно-пористых сорбентов на основе диоксида кремния и изучение их адсорбционных свойств
1177
Таблица 5
Вклад дисперсионных и специфических взаимодействий в дифференциальную мольную теплоту адсорбции
на сорбентах Хроматон N-AW + SiO2, синтезированных с различным количеством тетраэтоксисилана:
а — 0.0015, б — 0.003, в — 0.006, г — 0.03 моль — в кислой среде (1), в щелочной среде методом Штобера (2)
Теплота дисперсионных взаимодействий,
Теплота специфических взаимодействий,
кДж·моль-1
кДж·моль-1
Сорбент
бензол
этанол
бутанон-2
нитропропан-1
бензол
этанол
бутанон-2
нитропропан-1
1а
48
48
39
52
32
41
57
44
1б
50
38
41
42
4
39
27
13
1в
34
28
31
32
0
21
27
10
2г
36
20
28
26
8
35
16
39
говорит о присутствии как основных, так и кислот-
адсорбции гексана на 24 кДж·моль-1, а на сорбенте
ных центров. Значения pHИИС для образцов, получен-
Хроматон N-AW + SiO2(HCl, 0.006) с толщиной слоя
ных с использованием HCl, изменяются в интервале
1.4 мкм теплоты адсорбции данных соединений име-
6.5-6.8 при увеличении количества тетраэтоксисила-
ют близкие значения — 42 и 46 кДж·моль-1, что сви-
на от 0.0015 до 0.006 моль [20, 21].
детельствует об уменьшении полярности сорбентов
Результаты расчетов термодинамических харак-
с увеличением толщины слоя SiO2 на поверхности
теристик адсорбции тестовых соединений на син-
носителя Хроматон N-AW.
тезированных сорбентах, полученных из графиче-
Вклад различных типов межмолекулярных взаимо-
ских зависимостей логарифмов констант Генри от
действий в общую теплоту адсорбции на полученных
обратной температуры (табл. 4), свидетельствуют
поверхностно-пористых материалах (табл. 5) оцени-
об уменьшении дифференциально-мольных теплот
вали методом Донга [22, 23]. Соотношение специфи-
адсорбции и энтропии адсорбции с увеличением тол-
ческих и неспецифических видов взаимодействий
щины слоя SiO2 на поверхности сорбентов Хроматон
сорбат-сорбент зависит не только от полярности и
N-AW + SiO2(HCl). При адсорбции соединений, об-
поляризуемости, но и от толщины поверхностного
ладающих электронодонорными свойствами, та-
слоя SiO2. Так, для насыщенных углеводородов (ал-
ких как кетоны, спирты, алкены, ароматические и
канов) определяющими являются дисперсионные
нитросоединения, максимальные значения теплот
межмолекулярные взаимодействия, энергия которых
адсорбции наблюдаются на сорбенте Хроматон
зависит прежде всего от поляризуемости сорбатов.
N-AW + SiO2(HCl, 0.0015), что согласуется с результата-
Более сильное по сравнению с алканами хроматогра-
ми pH-метрии, указывающими на преобладание кис-
фическое удерживание ароматических соединений,
лотных центров на его поверхности. Максимальные
спиртов, кетонов обусловлено дополнительными к
значения теплот адсорбции алканов на сорбенте
дисперсионным специфическими взаимодействиями.
Хроматон N-AW + SiO2(HCl, 0.0015) объясняются уве-
Разность теплот адсорбции тестового адсорбата и ал-
личением теплоты дисперсионных взаимодействий
кана с равным числом атомов углерода характеризует
при адсорбции в микропорах (рис. 1, в).
энергию специфических взаимодействий. Следует
Кроме центров адсорбции на разделение и удержи-
отметить, что в целом доля специфической теплоты
вание органических соединений существенное влия-
адсорбции с увеличением количества тетраэтокси-
ние оказывают диффузионные процессы, в частности,
силана (в расчете на 1 г носителя Хроматон N-AW
с увеличением толщины слоя силикагеля возрастает
при синтезе сорбентов) уменьшается. Данная зависи-
диффузия массообмена, что приводит к уменьшению
мость проявляется для всех использованных тестовых
изменения абсолютных величин энтропии тестовых
соединений, характеризующих π-взаимодействия
соединений.
(бензол), образование водородных связей с электро-
Величины теплот адсорбции соединений с близ-
нодонорными функциональными группами (этанол),
кими значениями температур кипения, например,
а также специфических межмолекулярных взаимо-
неполярного гексана и полярного метанола на сор-
действий за счет донорно-акцепторного комплексо-
бенте Хроматон N-AW + SiO2(HCl, 0.0015) с толщиной
образования (бутанон-2, нитрометан). Максимальный
слоя SiO2 0.3 мкм существенно различаются. Теплота
вклад специфических взаимодействий наблюдается на
адсорбции метанола превышает значение теплоты
сорбенте Хроматон N-AW + SiO2(HCl, 0.0015), что может
1178
Фаустова Ж. В. и др.
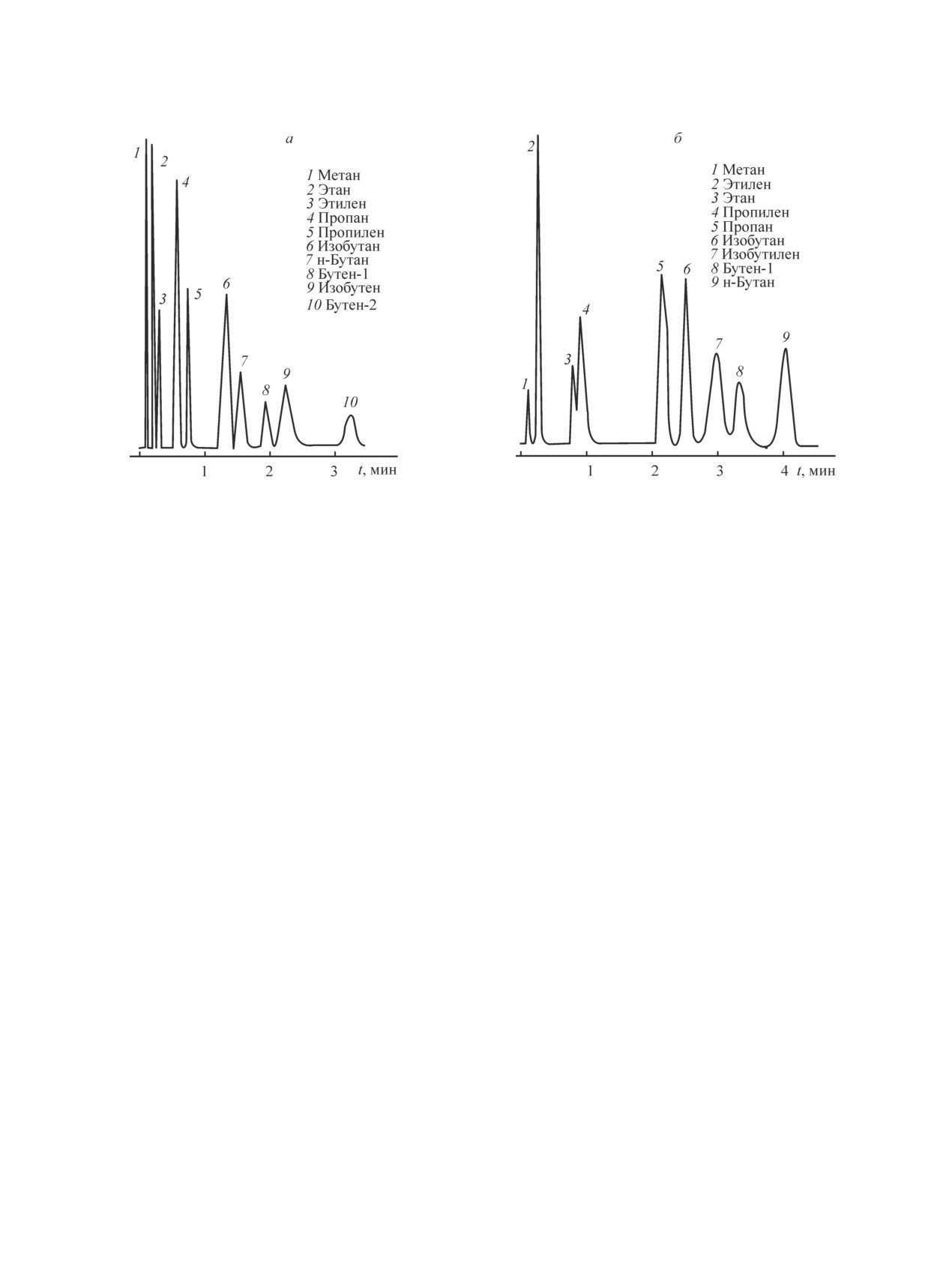
Рис. 6. Хроматограммы разделения смеси легких углеводородов на сорбентах Хроматон N-AW + SiO2, синтезирован-
ных с количеством тетраэтоксисилана 0.03 моль в кислой среде, режим программирования температуры 80-120°С,
скорость нагрева 5 град·мин-1 (а), в щелочной среде методом Штобера, режим программирования температуры
30-60°С, скорость нагрева 5 град·мин-1 (б).
быть обусловлено преобладанием кислотных центров
ваны образцы с размерами пор 2-4, в щелочной — 13-
Льюиса на его поверхности (рис. 5, кривая 1а). При
16 нм. С увеличением количества тетраэтоксисилана
этом больший вклад дисперсионных неспецифиче-
линейно возрастает толщина мезопористого слоя и
ских взаимодействий связан с увеличением адсорбции
удельная площадь поверхности полученных мате-
в микропорах (рис. 1, в), а также за счет межмолеку-
риалов, происходит уменьшение полярности син-
лярных взаимодействий на границе раздела фаз диок-
тезированных сорбентов и специфической теплоты
сида кремния и носителя Хроматон N-AW в процессе
адсорбции по отношению к тестовым соединениям.
газохроматографического разделения и адсорбции.
Проведенные исследования дают возможность
При разделении смеси легких углеводоро-
получать сорбенты с требуемой удельной площадью
дов на колонке с сорбентом Хроматон N-AW +
поверхности, толщиной активного слоя и с заданны-
+ SiO2(NH4OH, 0.03, метод Штобера) (рис. 6) компоненты
ми адсорбционными свойствами.
выходят в порядке увеличения их температур ки-
пения, а на колонке с сорбентом Хроматон N-AW +
Финансирование работы
+ SiO2(НCl, 0.03) молекулы алкенов удерживаются
сильнее соответствующих алканов, что согласуется
Работа выполнена в рамках государственного за-
с результатами исследования теплоты адсорбции и
дания Минобрнауки РФ по проекту № 721-2020-0037.
pH-метрии.
Полученные данные подтверждают, что с уве-
Конфликт интересов
личением количества тетраэтоксисилана от 0.0015
до 0.006 моль при синтезе сорбентов происходит
Авторы заявляют об отсутствии конфликта инте-
уменьшение количества электронодонорных центров
ресов, требующего раскрытия в данной статье.
адсорбции, в качестве которых выступают поверх-
ностные гидроксильные группы, при этом количество
Информация об авторах
электроноакцепторных центров возрастает.
Фаустова Жанна Владимировна,
Выводы
Матвеева Татьяна Николаевна, к.х.н.,
В результате формирования мезопористого слоя
SiO2 золь-гель методом на поверхности диатомитового
Слижов Юрий Геннадьевич, к.х.н.,
Получение поверхностно-пористых сорбентов на основе диоксида кремния и изучение их адсорбционных свойств
1179
Список литературы
pseudomorphically transformed derivative by gas and
liquid adsorption // Micropor. Mesopor. Mater. 2007.
[1]
Гуськов В. Ю., Сухарева Д. А., Салихова Г. Р.,
V. 102. N 1-3. P. 111-121.
Карпов С. И., Кудашева Ф. Х., Roessner F.,
[7]
Березкин В. Г., Никитина Н. С. Поверхностно-
слойные сорбенты в газовой хроматографии //
Успехи химии. 1971. № 5. С. 927-942.
2017. Т. 91. № 7. С. 1218-1222.
[8]
Шабанова Н. А., Саркисов П. Д. Основы золь-гель
технологии нанодисперсного кремнезема. М.: ИКЦ
Академкнига, 2004. С. 36-56.
[9]
Патрушев Ю. В., Сидельников В. Н., Ковалев М. К.,
Borodina E. V. Thermodynamic characteristics of the
Мельгунов М. С. Капиллярная газохроматографи-
ческая колонка с пористым слоем на основе ре-
гулярной структуры мезопористого материала //
Журн. физ. химии. 2008. Т. 82. № 7. С. 1355-1358
[2]
Парфенюк Е. В., Долинина Е. С., Романова Н. С.,
Melgunov M. S. A capillary gas chromatographic
[10]
[3]
Ноздрюхин Д. В., Беседина Н. А., Синдеева О. А.,
Chromatog. A. 2014. V. 1351. P. 103-109.
Ефимова О. И., Чернышев В. С., Бабёнышев А. В.,
Рудаковская П. Г., Горин Д. А., Ященок А. М.
[11]
Masalov V. M., Sukhinina N. S., Emelchenko G. A.
[12]
Zhang H., Wu J., Zhou L., Zhang D., Qi L. Facile
[4]
Земцова Е. Г., Арбенин А. Ю., Пономарева А. Н.,
synthesis of monodisperse microspheres and gigantic
hollow shells of mesoporous silica in mixed water-
ethanol solvents // Langmuir. 2007. V. 23. P. 1107-
[13]
Козлова С. А., Парфенов В. А., Тарасова Л. С.,
Smirnov V. M. Synthesis of magnetite nanoparticles in
С. 376-388.
[14]
Faustova Z., Matveeva T., Slizhov Y. Effect of carrier
properties on surface characteristics of sorbents
[5]
Синяева Л. А., Беланова Н. А., Карпов С. И.,
modified with acetylacetonates Ni (II), Cu (II) // AIP
of Students and Young Scientists. 2017. P. 020010-
[15]
Скворцова Л. Н., Чухломина Л. Н., Минакова Т. С.,
Шерстобоева М. В. Исследование кислотно-основ-
ных и сорбционных свойств поверхности металло-
керамических композитов // ЖПХ. 2017. Т. 90. № 8.
Minakova T. S., Sherstoboeva M. V. Investigation of
[6]
Iapichella J.,
Meneses J. M., Beurroies I.
Characterization of mesoporous silica and its
1180
Фаустова Ж. В. и др.
[16]
Ek S., Root A., Peussa M., Niinisto L. Determination
[21]
Тhommes M., Koehn R., Froeba M. Characterization
of the hydroxyl group content in silica by
of mesoporous solids: Pore condensation and sorption
thermogravimetry and a comparison with 1H MAS
hysteresis phenomena in mesoporous molecular sieves
NMR results // Thermochimiсa Acta. 2001. V. 379.
// Surf. Sci. Catal. 2002. V. 142. P. 1695-1701. https://
P. 201-212.
[22]
Белякова Л. Д., Буряк А. К., Ларионов О. Г.
[17]
Лисичкин Г. В. Химия привитых поверхностных
соединений. М.: Физматлит, 2003. С. 38-56.
[18]
Ланин С. Н., Банных А. А., Власенко Е. В.,
Виноградов А. Е., Ланина К. С., Легачев С. M.
2013. Т. 49. № 6. С. 551-574.
Адсорбционные свойства оксида алюминия, мо-
дифицированного наночастицами Co и CoO //
[Belyakova L. D., Buryak A. K., Larionov O. G.
Физикохимия поверхности и защита материалов.
2017. Т. 53. № 3. С. 247-254.
[23]
Сухарева Д. А., Гуськов В. Ю., Карпов С. И.,
Кудашева Ф. Х., Roessner F., Бородина Е. В.
[19]
Zhuravlev L. T. The surface chemistry of amorphous
silica. Zhuravlev model // Coll. Surf. A: Physicochem.
Eng. Asp. 2000. V. 173. P. 1-38.
[Sukhareva D. A., Gus′kov V. Yu., Karpov S. I.,
[20]
Ek S., Root A., Peussa M. Determination of the
hydroxyl group content in silica by thermogravimetry
and a comparison with 1H MAS NMR results //
Thermochim. Acta. 2001. V. 379. P. 201-212. https://