Журнал прикладной химии. 2021. Т. 94. Вып. 3
НЕОРГАНИЧЕСКИЙ СИНТЕЗ И ТЕХНОЛОГИЯ НЕОРГАНИЧЕСКИХ ПРОИЗВОДСТВ
УДК 541.183.1:546.98+546.924
ИЗВЛЕЧЕНИЕ ПАЛЛАДИЯ(II) И ПЛАТИНЫ(IV)
ГЕТЕРОЦЕПНЫМИ КОМПЛЕКСООБРАЗУЮЩИМИ СОРБЕНТАМИ
ИЗ МОДЕЛЬНЫХ РАСТВОРОВ ВЫЩЕЛАЧИВАНИЯ
ОТРАБОТАННЫХ ПРОМЫШЛЕННЫХ КАТАЛИЗАТОРОВ
И ОТРАБОТАННОГО РАСТВОРА АФФИНАЖНОГО ПРОИЗВОДСТВА
© Г. Р. Анпилогова, Ю. И. Муринов
Уфимский институт химии Уфимского федерального исследовательского центра РАН,
450054, г. Уфа, пр. Октября, д. 69
E-mail: hisam@anrb.ru
Поступила в Редакцию 28 мая 2020 г.
После доработки 29 декабря 2020 г.
Принята к публикации 15 января 2021 г.
В статических условиях изучена возможность селективного извлечения палладия(II) и платины(IV)
гетероцепными комплексообразующими сорбентами поликонденсационного типа из солянокислых
модельных растворов выщелачивания отработанных промышленных катализаторов и модельного
маточного раствора после осаждения гексахлороплатината аммония. Показано, что при темпера-
туре 19°C и времени контакта фаз 2 ч сорбент с 1-(2-аминоэтил)пиперазиновыми и диметиленсуль-
фидными функциональными группами извлекает более 99.9% палладия(II) из модельного раствора
выщелачивания катализатора АПК-2 (сорбционная емкость ЕPd = 501 мг·г-1) и 97-98% платины(IV)
из раствора выщелачивания платино-никелевого катализатора (EPt = 86 мг·г-1) с селективным от-
делением палладия(II) от Al(III) и платины(IV) от Al(III) и Ni(II). Полиметиленмоносульфид при 80°C
и времени контакта фаз 3 ч практически нацело извлекает палладий(II) (ЕPd = 34 мг·г-1) и 95% пла-
тины(IV) (EPt = 6 мг·г-1) из модельного маточного раствора с селективным отделением платиновых
металлов от сопутствующих элементов Cu(II), Zn(II), Fe(III) и Sn(IV).
Ключевые слова: полиметиленмоносульфид; полимерный аминотиоэфир; палладий(II); платина(IV);
сорбция
DOI: 10.31857/S0044461821030063
Потребление палладия и платины ежегодно воз-
катализаторы.*,** Растворы, получаемые при выще-
растает и в настоящее время превышает объем их
лачивании бедного сырья, характеризуются слож-
добычи из первичного сырья, в связи с чем в пере-
* Cowley A. Pgm Market Report February 2020. Johnson
работку вовлекаются бедные и упорные руды, раз-
Matthey PLC, 2020. P. 1-19.
нообразные промышленные и техногенные отходы.
** Информационно-технический справочник по наилуч-
Значимыми вторичными источниками Pd и Pt явля-
шим доступным технологиям ИТС 14-2016. Производство
ются отработанные промышленные и автомобильные
драгоценных металлов. М.: Бюро НДТ, 2016. С. 3-8, 29.
324
Извлечение палладия(II) и платины(IV) гетероцепными комплексообразующими сорбентами...
325
ным составом и низким содержанием благородных
представляют интерес для извлечения малых коли-
металлов. В аффинажном производстве существует
честв благородных металлов из сложных техноло-
проблема глубокого доизвлечения малых количеств
гических и отработанных растворов с получением
благородных металлов из больших объемов отрабо-
зольных концентратов [9].
танных растворов [1-3]. На отечественных и зару-
Цель работы — изучение возможности приме-
бежных предприятиях извлечение благородных ме-
нения полиметиленмоносульфида и полимерного
таллов из бедных растворов осуществляется обычно
аминотиоэфира, содержащего 1-(2-аминоэтил)пипе-
осаждением в виде труднорастворимых соединений
разиновые и диметиленсульфидные группы, для глу-
или цементацией [1, 3], при этом не всегда обеспе-
бокого селективного сорбционного извлечения пал-
чивается достаточно полное извлечение целевых
ладия(II) и платины(IV) из модельных солянокислых
металлов, растворы дополнительно загрязняются
растворов выщелачивания отработанных промыш-
реагентом-осадителем или ионами цементирующего
ленных катализаторов на основе оксида алюминия
металла, образуется значительное количество бедных
и модельного маточного раствора после осаждения
промпродуктов, требующих дальнейшей переработки
гексахлороплатината аммония.
или утилизации. Перспективным, более технологич-
ным и эффективным гидрометаллургическим мето-
Экспериментальная часть
дом селективного извлечения и концентрирования
малых количеств благородных металлов из сложных
В работе использовали гетероцепные комплексо-
растворов является сорбция [2-4].*
образующие сорбенты поликонденсационного типа
Сорбционная технология пока не находит широ-
полиметиленмоносульфид и полимерный аминотио-
кого применения в гидрометаллургии платиновых
эфир, представляющие собой мелкодисперсные по-
металлов, что, в частности, обусловлено высокой сто-
рошки белого цвета:
имостью селективных промышленных сорбентов и
трудностью подбора эффективных и технологически
подходящих элюентов. Однако высокая стоимость
драгоценных металлов, эффективность и стоимость
сорбента определяют целесообразность сжигания
сорбтива для получения зольного концентрата извле-
ченных металлов [2, 3, 5-7].
Высокоэффективные и селективные комплексо-
образующие гетероцепные S- и S,N-содержащие со-
рбенты поликонденсационного типа — полимерный
тиоэфир полиметиленмоносульфид и полимерные
Полиметиленмоносульфид синтезирован методом
аминотиоэфиры — используются для предваритель-
поликонденсации формальдегида с сероводородом в
ного концентрирования благородных металлов при
щелочной среде [11].
определении их содержания в разнообразных техно-
Найдено
(%): C 25.6, H 4.3, S 69.2.
логических и геологических объектах гибридными
CH2S. Вычислено (%): C 26.1, H 4.4, S 69.6.
методами анализа [8].** Сорбенты получают просты-
Размер частиц сорбента составлял 0.10-0.20 мм,
ми одностадийными методами синтеза с применени-
насыпная масса — 0.12 г∙см-3, содержание конце-
ем относительно недорогих и доступных реагентов
вых кислотных групп (СОЕ0.1 н NaOH, определен-
[9, 10], что определяет их существенно меньшую
ная в статических условиях сорбции стандартным
стоимость по сравнению с промышленными селек-
методом [12]) — 1.00 мг-экв∙г-1. Среднечисловая
тивными сорбентами, получаемыми сложными мно-
молекулярная масса сорбента, рассчитанная по
гостадийными методами. Гетероцепные сорбенты
концентрации концевых групп, составляла 2000.
Величина полной статической сорбционной емко-
* Информационно-технический справочник по наи-
сти по серебру ЕAg = 21.6 ммоль∙г-1 соответствовала
лучшим доступным технологиям ИТС 14-2016. Производ-
концентрации серосодержащих групп в сорбенте ЕS =
ство драгоценных металлов. М.: Бюро НДТ, 2016. С. 19-21,
= 21.7 мг-атом S/г.
49.
Полимерный аминотиоэфир получен взаимо-
** Золотов Ю. А., Цизин Г. И., Дмитриенко С. Г., Мо-
действием 1-(2-аминоэтил)пиперазина (99%, Acros,
росанова Е. И. Сорбционное концентрирование микро-
каталожный номер 40076) с формальдегидом (1:3)
элементов из растворов: применение в неорганическом
анализе. М.: Наука, 2007. С. 109-115.
и сероводородом в среде диметилформамида (х.ч.,
326
Анпилогова Г. Р. и др.
АО «ЭКОС-1») при пропускании тока H2S, темпе-
спектрофотометрическое определение платины(IV) в
ратуре 20°С и перемешивании в течение 3 ч [13].
таких растворах после сорбции палладия(II) и плати-
Элементный состав сорбента (%): C 36.7, H 6.2,
ны(IV). Низкие значения концентрации палладия(II)
N 11.1, S 46.8; средний размер частиц 0.056 мм; на-
(не более 0.5 мг∙л-1) в сложных растворах после со-
сыпная масса 0.50 г∙см-3.
вместной сорбции палладия(II) и платины(IV) бы-
В работе использовали водный раствор формаль-
ли подтверждены методом атомно-абсорбционной
дегида (37 мас%) — формалин технический высшего
спектроскопии (спектрофотометр Hitachi 508, пламя
сорта марки ФМ (ОАО «НЗСП»).
ацетилен-воздух, аналитическая длина волны опре-
Для приготовления водных растворов использо-
деления палладия 247.6 нм).
вали PdCl2 и H2PtCl6∙6H2O (ч., ОАО «Красцветмет»),
Концентрацию неблагородных металлов в инди-
AlCl3∙6Н2О (ч., Донецкий завод химреактивов),
видуальных растворах их солей определяли комплек-
FeCl3∙6H2O (ч., ООО «Компонент-Ректив»), ZnCl2
сонометрическими методами: Zn(II) — с индикато-
(ч.д.а., ОАО «Алмалыкский ГМК»), CuCl2∙2H2O
ром эриохром черный Т, Cu(II) и Ni(II) — мурексид
(ч.д.а., Донецкий завод химреактивов), AgNO3
[16], Fe(III) — сульфосалициловая кислота;** Al(III)
(ч.д.а., Уральский завод химреактивов), NiCl2∙6H2O
и Sn(IV) — с индикатором ксиленоловый оранжевый
(х.ч., Черкасский завод химреактивов), SnCl4
методами обратного титрования раствором ZnSO4 ***
(99.995%, Sigma-Aldrich 217913), NH4Cl (х.ч., ОАО
и [17] соответственно. Концентрацию Ag(I) в азотно-
«Лисичанская сода»), HNO3 (ч.д.а., АО НАК «Азот»)
кислых растворах определяли методом Фольгарда.****
и HCl (х.ч., АО «БСК»).
Сорбцию ионов металлов изучали статическим
В табл. 1 приведены литературные данные по со-
методом отдельных навесок при соотношении массы
ставу солянокислых растворов, принятых в качестве
сорбента (г) и объема раствора (см3) m:V = 1:200 при
модельных: усредненный состав отработанного рас-
перемешивании со скоростью 800 об·мин-1 (магнит-
твора аффинажного цеха одного из отечественных
ная мешалка типа ММ-2А) при комнатной (20 ± 1°С)
предприятий (маточный раствор после осаждения
или повышенной температуре. Сорбцию при повы-
гексахлороплатината аммония) и состав растворов,
шенной температуре проводили в термостатирован-
которые могут быть получены при выщелачивании
ных ячейках, температура поддерживалась с точно-
отработанных промышленных катализаторов на ос-
стью ±0.2°С (термостат типа UH 4). Сорбцию Zn(II),
нове оксида алюминия.
Cu(II), Ni(II), Fe(III), Al(III) и Sn(IV) из индивидуаль-
Концентрацию палладия(II) и платины(IV) в рас-
ных солянокислых растворов изучали при исходной
творах определяли спектрофотометрическими ме-
концентрации ионов металла 0.05 моль∙л-1. Полную
тодами с хлоридом олова(II)* на спектрофотометре
сорбционную емкость полиметиленмоносульфида
Specord M40. Определению платины(IV) в исходных
по Ag(I) определяли при исходной концентрации
сложных растворах, моделирующих состав отрабо-
0.95 моль∙л-1 AgNO3 в растворе 1 моль∙л-1 HNO3,
танного аффинажного раствора, мешало присутствие
при комнатной температуре, m:V = 1:100 и времени
палладия(II), концентрация которого девятикратно
контакта фаз 24 ч. Погрешность определения сорбци-
превышала концентрацию платины(IV) (табл. 1), по-
онной емкости по ионам металлов не превышала 5%.
этому исходную концентрацию платины(IV) рассчи-
тывали по концентрации стандартизованного раство-
Обсуждение результатов
ра платины(IV), используемого для приготовления
таких растворов. Присутствие платины(IV) не ме-
Зависимость сорбционной емкости гетероцеп-
шало анализу палладия(II) в растворах типа № 1 до и
ных сорбентов по платине(IV) и палладию(II) от
после сорбции палладия(II) и платины(IV) полимети-
исходной концентрации соляной кислоты в инди-
ленмоносульфидом, так как отсутствовало заметное
видуальных растворах соединений платиновых
поглощение окрашенных соединений платины с хло-
металлов (рис. 1) получена при времени контакта
ридом олова(II) при длине волны 635 нм. Следовые
концентрации палладия(II), не превышающие предел
** Марков В. К., Верный Е. А., Виноградов А. В., Ели-
его обнаружения (~1 мг∙л-1), не оказывали влияния на
сон С. В., Клыгин А. Е., Моисеев И. В. Уран. Методы его
определения. М.: Атомиздат, 1964. С. 360-361.
*** Тихонов В. Н. Аналитическая химия алюминия.
* Гинзбург С. И., Езерская Н. А., Прокофьева И. В.,
М.: Наука, 1971. С. 67-69.
Федоренко Н. В., Шленская В. И., Бельский Н. К.
**** Васильев В. П. Аналитическая химия. В 2 кн.
Аналитическая химия платиновых металлов. М.: Наука,
Кн. 1. Гравиметрический и титриметрический методы
1972. С. 321, 328.
анализа. М.: Высш. шк., 1989. С. 259.
Извлечение палладия(II) и платины(IV) гетероцепными комплексообразующими сорбентами...
327
Таблица 1
Состав модельного маточного раствора после осаждения гексахлороплатината аммония и модельных растворов
выщелачивания отработанных промышленных катализаторов на основе оксида алюминия
Литературный
№ раствора
Раствор
Состав, моль∙л-1
источник
1
Маточный раствор после осаждения гексахлоропла-
HCl 3
[2, 14]
тината аммония
NH4Cl 1
Pd(II) 0.0014
Pt(IV) 0.00015
Zn(II), Cu(II), Fe(III), Sn(IV) по 0.05
2
Раствор выщелачивания платино-никелевого ката-
HCl 3-5
[15]
лизатора изомеризации и гидрирования углеводо-
Pt(IV) 0.0015-0.0022
родов
Ni(II) 0.012-0.058
Al(III) 0.15-0.53
3
Раствор выщелачивания алюмопалладиевого катали-
HCl 3-4
[15]
затора АПК-2
Pd(II) 0.014-0.016
Al(III) 0.20-0.64
фаз 6 ч, достаточном для достижения равновесия
(Kd = 19-34 см3∙г-1). В представляющей интерес об-
сорбции палладия(II) из солянокислых растворов
ласти концентраций 3-5 моль∙л-1 HCl сорбционная
полимерным аминотиоэфиром [18] и полиметилен-
емкость данного сорбента по платине(IV) и палла-
моносульфидом (рис. 2) при комнатной температу-
дию(II) незначительно зависит от кислотности рас-
ре. В изученном диапазоне концентраций кислоты
твора. Полимерный аминотиоэфир существенно
(рис. 1) палладий(II) сорбируется полиметиленмо-
эффективнее извлекает платину(IV) и палладий(II),
носульфидом с более высокими коэффициентами
чем полиметиленмоносульфид. Сорбция платиновых
распределения (Kd = 74-225 см3∙г-1), чем платина(IV)
металлов этим сорбентом в изученном диапазоне
концентраций кислоты характеризуется высокой сте-
пенью извлечения (>99%) и высокими значениями
коэффициентов распределения (Kd ~ 104 см3∙г-1) дан-
ных металлов.
Полимерный аминотиоэфир с высокой эффек-
тивностью сорбирует медь(II) из растворов
1-5 моль∙л-1 HCl [18], что не позволяет использо-
вать его для селективного извлечения платиновых
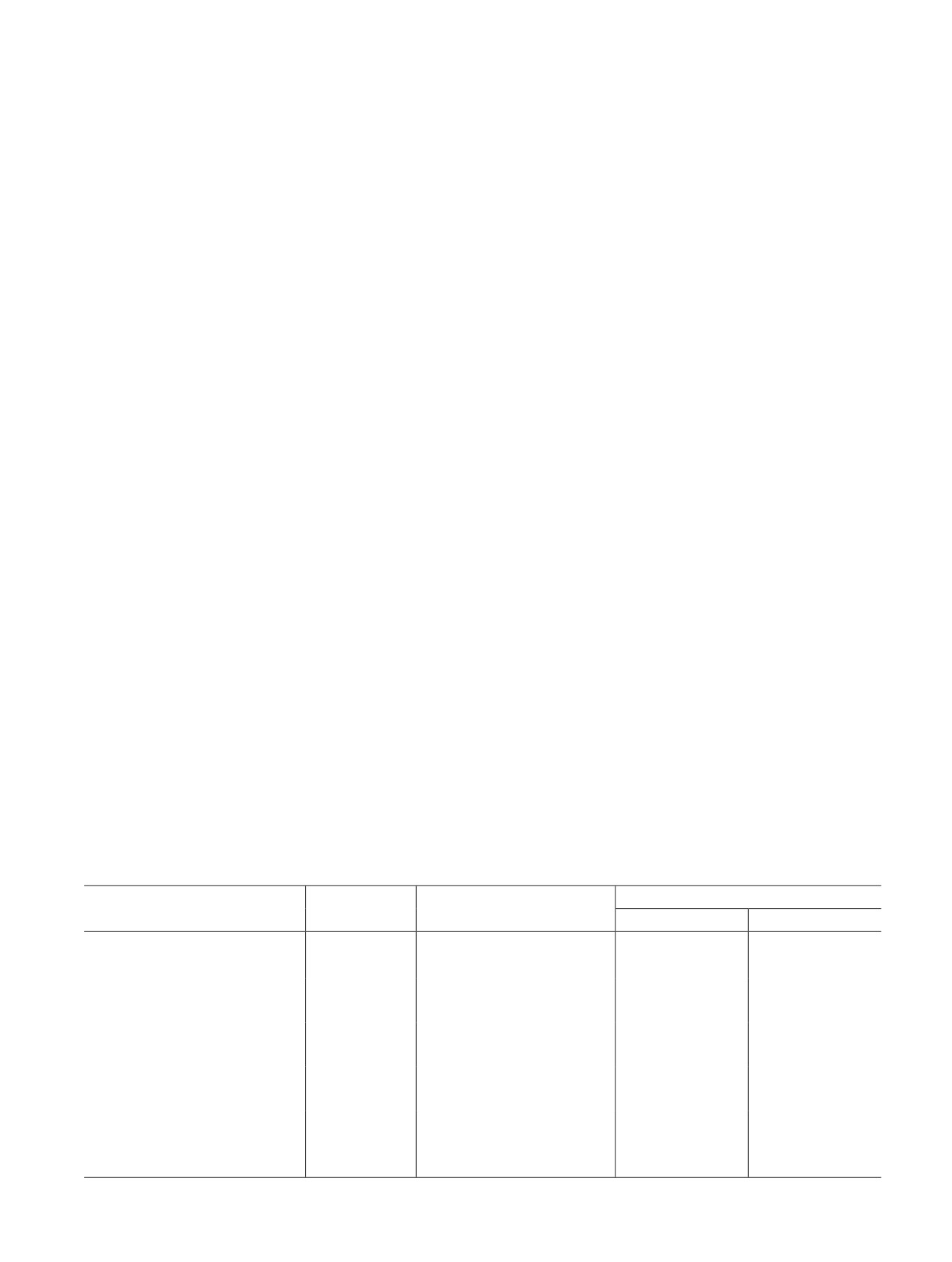
Рис. 1. Зависимость сорбционной емкости полимети-
ленмоносульфида (1, 2) и полимерного аминотиоэфира
(3, 4) по платине(IV) (1, 4) и палладию(II) (2, 3) от кон-
центрации соляной кислоты.
Рис. 2. Кинетическая кривая сорбции палладия(II) по-
Т = 20°С, время контакта фаз 6 ч.
лиметиленмоносульфидом из раствора 1 моль∙л-1 HCl.
1, 4 — сPt = 0.0056 моль∙л-1, 2 — сPd = 0.0056 моль∙л-1;
3 — сPd = 0.0051 моль∙л-1.
сPd = 0.0059 моль∙л-1, Т = 20°С.
328
Анпилогова Г. Р. и др.
металлов из отработанного аффинажного раствора
творе глубокое извлечение платины(IV) при данной
№ 1. Полиметиленмоносульфид является одним из
температуре не достигается даже при увеличении
наиболее селективных сорбентов платиновых метал-
времени контакта фаз до 6 ч (табл. 2). Повышение
лов. При температуре кипения раствора железо(III)
температуры до 80°С и времени контакта фаз до 3 ч
не извлекается сорбентом при кислотности водной
позволяет практически полностью извлечь плати-
фазы 1-10 моль∙л-1 HCl, а сорбция меди(II) из рас-
новые металлы при их совместном присутствии в
творов 3-10 моль∙л-1 HCl незначительна [19]. Данный
растворе (табл. 2). Установлено отсутствие сорбции
сорбент был выбран для изучения возможности глу-
Zn(II), Cu(II), Fe(III) и Sn(IV) из индивидуальных
бокого селективного извлечения платиновых метал-
растворов, содержащих 3 моль∙л-1 HCl и 1 моль∙л-1
лов из отработанного аффинажного раствора № 1.
NH4Cl, при температуре 20, 60 и 80°С и времени кон-
Установлено, что оба сорбента не извлекают Ni(II) и
такта фаз 2 ч (в пределах ошибки определения кон-
Al(III) из индивидуальных растворов ионов металлов,
центрации ионов металлов). Следовательно, данный
содержащих 3-5 моль∙л-1 HCl, при комнатной темпе-
сорбент позволяет селективно отделять платиновые
ратуре, а полиметиленмоносульфид — также и при
металлы от сопутствующих. В оптимальных усло-
60 и 80°С. Следовательно, они представляют инте-
виях сорбции из модельного раствора, содержащего
рес для изучения возможности селективной сорбции
сопутствующие элементы, полиметиленмоносульфи-
платиновых металлов из растворов выщелачивания
дом глубоко извлекаются палладий(II) (остаточная
отработанных катализаторов № 2, 3.
концентрация не более 1 мг∙л-1, ЕPd = 34.3 мг∙г-1)
Изучение сорбции платиновых металлов полиме-
и платина(IV) (остаточная концентрация 1.6 мг∙л-1,
тиленмоносульфидом из индивидуальных растворов,
ЕPt = 5.7 мг∙г-1) (табл. 2).
моделирующих состав раствора № 1 по содержанию
Изучение сорбции палладия(II) и платины(IV)
HCl (3 моль∙л-1) и NH4Cl (1 моль∙л-1) и содержащих
из модельных растворов выщелачивания промыш-
0.0014 моль∙л-1 палладия(II) или 0.00015 моль∙л-1
ленных катализаторов показало, что даже при повы-
платины(IV), показало, что степень извлечения пал-
шенных температурах полиметиленмоносульфид не
ладия(II) при времени контакта фаз 6 ч возрастает
обеспечивает полноты извлечения более высоких,
от 75.7 до >99% с увеличением температуры от 20
чем в растворе № 1, количеств платиновых металлов
до 60°С. Время контакта фаз, необходимое для прак-
(табл. 3). Достоинством полимерного аминотиоэфира
тически полного извлечения (>99%) палладия(II) и
является высокая скорость сорбции палладия(II) при
платины(IV) из их индивидуальных растворов при
кислотности водной фазы более 1 моль∙л-1 HCl [18].
60°С составляет 2 и 1.5 ч соответственно. Однако при
Установлено, что данный сорбент с высокой степе-
совместном присутствии платиновых металлов в рас-
нью извлечения сорбирует платину(IV) из раствора
Таблица 2
Влияние температуры и времени контакта фаз на степень извлечения палладия(II) и платины(IV)
полиметиленмоносульфидом из растворов, моделирующих состав отработанного аффинажного раствора № 1
Концентрация HCl — 3 и NH4Cl — 1 моль∙л-1
Степень извлечения, %
сМ, моль∙л-1
Т, °С
Время контакта фаз, ч
Pd(II)
Pt(IV)
Pd 0.00139
60
2
>99
66.9
Pt 0.00015
Pd 0.00139
60
6
>99
72.2
Pt 0.00015
Pd 0.00141
80
2
>99
90.9
Pt 0.00015
Pd 0.00141
80
3
>99
>99
Pt 0.00015
Pd 0.00161
80
3
>99
95.0
Pt 0.00015
Zn, Cu, Fe, Sn по 0.05
Извлечение палладия(II) и платины(IV) гетероцепными комплексообразующими сорбентами...
329
Таблица 3
Сорбция палладия(II) и платины(IV) гетероцепными сорбентами из модельных растворов выщелачивания
отработанных промышленных катализаторов
Время контакта
Степень извлечения, %
№ раствора
Состав, моль∙л-1
Сорбент
Т, °С
фаз, ч
Pd(II)
Pt(IV)
2
HCl 4,
Полиметиленмоносульфид
60
2
28.2
Pt(IV) 0.0023,
Ni(II) 0.058,
Al(III) 0.53
2
HCl 4,
Полиметиленмоносульфид
80
3
66.4
Pt(IV) 0.0023,
Ni(II) 0.058,
Al(III) 0.53
2
HCl 3-5,
Полимерный аминотиоэфир
20
2
97-98
Pt(IV) 0.0023,
Ni(II) 0.058,
Al(III) 0.17; 0.54
3
HCl 3.5,
Полиметиленмоносульфид
60
3
46.0
Pd(II) 0.015,
Al(III) 0.32
3
HCl 3-4,
Полимерный аминотиоэфир
19
1
>99.9
Pd(II) 0.015,
Al(III) 0.32; 0.64
№ 2 и практически полностью — палладий(II) из рас-
и концентрирования палладия(II) и платины(IV) из
твора № 3 при комнатной температуре и времени кон-
маточного раствора после осаждения гексахлоропла-
такта фаз 2 и 1 ч соответственно (табл. 3). При этом
тината аммония с селективным отделением платино-
сорбционная емкость полимерного аминотиоэфира
вых металлов от Zn(II), Cu(II), Fe(III) и Sn(IV) в оп-
по платине(IV) и палладию(II) составляет 85-88 и
тимальных условиях сорбции: m:V = 1:200, T = 80°С,
319 мг∙г-1 соответственно. Высокая эффективность
время контакта фаз — 3 ч. Гетероцепный сорбент
этого сорбента позволяет практически нацело из-
полимерный аминотиоэфир может быть предложен
влекать палладий(II) из раствора № 3, содержащего
для эффективного и селективного извлечения и кон-
HCl — 3.5, Al(III) — 0.32, Pd(II) — 0.016 моль∙л-1,
центрирования палладия(II) и платины(IV) из соля-
при m:V = 1:300 и времени контакта фаз 1 ч с высо-
нокислых растворов выщелачивания отработанных
ким значением ЕPd = 501 мг∙г-1 [остаточная концен-
промышленных катализаторов на основе оксида алю-
трация палладия(II) не более 1 мг∙л-1].
миния (АПК-2 и платино-никелевый катализатор) при
Поскольку сорбция палладия(II) и платины(IV)
комнатной температуре.
изученными гетероцепными сорбентами необрати-
ма [18, 20], сорбтивы платиновых металлов можно
Благодарности
перерабатывать сжиганием с получением зольных
концентратов, что целесообразно при относительно
Авторы благодарят Центр коллективного пользо-
небольшой стоимости сорбентов и высокой сорбци-
вания «Химия» УфИХ УФИЦ РАН и Региональный
онной емкости полимерного аминотиоэфира.
центр коллективного пользования «Агидель» УФИЦ
РАН за проведение элементного анализа сорбентов.
Выводы
Финансирование работы
Высокоселективный гетероцепный комплексо-
образующий сорбент полиметиленмоносульфид мо-
Работа выполнена по теме государственного зада-
жет быть рекомендован для глубокого доизвлечения ния № АААА-А20-120012090027-6.
330
Анпилогова Г. Р. и др.
Конфликт интересов
[Dalʹnova O. A., Baranovskaya V. B, Dalʹnova
Yu. S., Karpov Yu. A. New complexing polymer
Авторы заявляют об отсутствии конфликта инте-
aminothioether sorbents in the analytical control
ресов, требующего раскрытия в данной статье.
of recyclable metal-containing raw material of rare
and noble metals // J. Anal. Chem. 2018. V. 73. N 3.
P. 221-227.
Информация об авторах
Анпилогова Галина Рудольфовна, к.х.н.,
[9] Пат. РФ 2205237 (опубл. 2003). Способ извлечения
драгоценных и тяжелых металлов из растворов.
[10]
Семенов Д. Г., Афонин В. М., де Векки Д. А.,
Муринов Юрий Ильич, д.х.н., проф.,
Симанова С. А. Хемосорбция хлоридных комплек-
сов Rh(III) и Ir(III и IV) полиметиленсульфидом //
Изв. СПбГТИ (ТУ). 2019. № 50 (76). С. 3-15.
[11]
Рафиков С. Р., Алеев Р. С., Масагутов Р. М.,
Список литературы
Данилов В. Т., Дальнова Ю. С. Реакция формальде-
[1] Ильяшевич В. Д., Павлова Е. И., Жеребцова О. В.,
гида с сероводородом // Изв. АН СССР. Сер. хим.
Сиротина Д. Ю., Лукина К. В., Кривошеев Н. О.
1982. № 7. С. 1631-1633 [Rafikov S. R., Aleev R. S.,
Новый подход к обезблагораживанию производ-
Masagutov R. M., Danilov V. T., Dalʹnova Yu. S.
ственных растворов в Красцветмете // XXII Между-
Reaction of formaldehyde with hydrogen sulfide //
нар. Черняевская конф. по химии, аналитике и техно-
Russ. Chem. Bull. 1982. V. 31. P. 1452-1453.
логии платиновых металлов. Сб. тез. М., 2019. С. 85.
[2] Блохин А. А., Абовский Н. Д., Мурашкин Ю. В.,
[12]
Салдадзе К. И., Копылова-Валова В. Д. Комплексо-
Михайленко М. А. Сорбционное извлечение платины
образующие иониты (комплекситы). М.: Химия,
и палладия из отработанных аффинажных раство-
1980. С. 104-105.
ров с их низким содержанием // Цветные металлы
[13]
Анпилогова Г. Р. Сорбционные свойства S- и
Сибири-2009: Сб. докладов Первого междунар. кон-
N-содержащих гетероцепных сорбентов по отно-
гресса. Красноярск: ООО «Версо», 2009. С. 587-592.
шению к благородным металлам: Автореф. канд.
[3] Yahorava V., Kotze M. Ion exchange technology for the
дис. Уфа, 1997. 24 с.
efficient recovery of precious metals from waste and
[14]
Блохин А. А., Абовский Н. Д., Мурашкин Ю. В.
low-grade streams // J. S. Afr. Inst. Min. Metall. 2014.
Ионообменное извлечение палладия(II) из хло-
V. 114. N 2. Р. 173-181.
ридных растворов сложного состава // ЖПХ.
[4] Nikoloski A. N., Ang K.-L. Review of the application of
2007. Т. 80. № 7. С. 1089-1093 [Blokhin A. A.,
ion exchange resins for the recovery of platinum-group
Abovskii N. D., Murashkin Yu. V. Ion-exchange
metals from hydrochloric acid solutions // Mineral
recovery of palladium(II) from multicomponent
Processing and Extractive Metallurgy Rev. 2014. V. 35.
chloride solutions // Russ. J. Appl. Chem. 2007. V. 80.
N 6. P. 369-389.
N 7. P. 1058-1062.
[5] Ehrlich H. V., Buslaeva T. M., Maryutina T. A. Trends in
[15]
Анпилогова Г. Р., Хисамутдинов Р. А., Голубятни-
sorption of platinum metals: A critical survey // Russ. J.
кова Л. Г., Муринов Ю. И. Пропиконазол и пенкона-
Inorg. Chem. 2017. V. 62. N 14. P. 1797-1818. https://
зол — эффективные экстрагенты для селективного
doi.org/10.1134/S0036023617140030
извлечения и концентрирования платины(IV) и
[6] Tatarnikov A. V., Sokolskaya I., Shneerson Ya. M.,
палладия(II) из солянокислых растворов выще-
Lapin A. Yu., Goncharov P. M. Treatment of platinum
лачивания алюмоплатиновых и алюмопалла-
flotation products // Platinum Metals Rev. 2004. V. 48.
диевого отработанных катализаторов // ЖПХ.
N 3. P. 125-132.
2016. Т. 89. № 2. С. 195-201 [Anpilogova G. R.,
Khisamutdinov R. A., Golubyatnikova L. G.,
[7] Богданов В. И., Барабошкин В. Е., Гроховский С. В.
Murinov Yu. I. Propiconazole and penconazole as
Аффинажное производство // Драг. металлы. Драг.
effective extractants for selective recovery and
камни. 2005. № 8. С. 86-113.
concentration of platinum(IV) and palladium(II) from
[8] Дальнова О. А., Барановская В. Б., Дальнова Ю. С.,
hydrochloric acid solutions formed in leaching of spent
Карпов Ю. А. Новые комплексообразующие поли-
aluminoplatinum and aluminopalladium catalysts //
мерные аминотиоэфирные сорбенты в аналитиче-
Russ. J. Appl. Chem. 2016. V. 89. N 2. P. 206-211.
ском контроле возвратного металлсодержащего сы-
рья редких и благородных металлов // ЖАХ. 2018.
[16]
Калинина Л. С., Моторина М. А., Никитина Н. И.,
Т. 73. № 3. С. 181-188.
Хачапуридзе Н. А. Анализ конденсационных поли-
меров. М.: Химия, 1984. С. 86.
Извлечение палладия(II) и платины(IV) гетероцепными комплексообразующими сорбентами...
331
[17]
Мышляева Л. В., Максимова Т. Г. Комплексоно-
Petrukhin O. M., Shiryaeva O. A., Kolonina L. N.,
метрический метод в анализе элементокремний-
Marcheva E. V., Murinov Y. I., Bikbaeva G. G.,
органических и элементоорганических соединений
Nikitin Y. E., Zolotov Y. A. Sorption-x-ray fluorescence
// ЖАХ. 1968. Т. 23. № 10. С. 1584-1586.
determination of the platinum metals by means of
[18]
Анпилогова Г. Р., Алеев Р. С., Афзалетдинова Н. Г.,
a thioether polymer // J. Anal. Chem. USSR. 1981.
Хисамутдинов Р. А., Шишлов Н. С., Муринов Ю. И.
V. 36. N 9. P. 1250-1256].
Новый гетероцепный сероазотсодержащий ком-
[20] Петрухин О. М., Малофеева Г. И., Нефедов В. И.,
плексит для благородных металлов // ЖНХ. 1995.
Салынь Я. В., Марчева Е. В., Шестаков В. А.,
Т. 40. № 3. С. 466-471.
Ширяева О. А., Муринов Ю. И., Никитин Ю. Е.,
[19]
Шестаков В. А., Малофеева Г. И., Петру-
Золотов Ю. А. Сорбция платиновых металлов
хин О. М., Ширяева О. А., Колонина Л. Н., Мар-
полимерным тиоэфиром // ЖАХ. 1983. Т. 38.
чева Е. В., Муринов Ю. И., Бикбаева Г. Г.,
№ 2. С. 250-255 [Petrukhin O. M., Malofeeva G. I.,
Никитин Ю. Е., Золотов Ю. А. Сорбционно-
Nefedov V. I., Salyn Y. V., Marcheva E. V.,
рентгенофлуоресцентное определение пла-
Shestakov V. A., Shiryaeva O. A., Murinov Y. I.,
тиновых металлов с использованием поли-
Nikitin Y. E., Zolotov Y. A. Sorption of platinum metals
мерного тиоэфира // ЖАХ. 1981. Т. 36. № 9.
by a polymer thioether // J. Anal. Chem. USSR. 1983.
С. 1784-1792 [Shestakov V. A., Malofeeva G. I.,
V. 38. N 2. P. 196-201].