Агрохимия, 2020, № 1, стр. 50-57
ПРОДУКТИВНОСТЬ РАСТЕНИЙ ЯЧМЕНЯ И ВЗАИМОДЕЙСТВИЕ ЦИНКА, КАЛЬЦИЯ И МАГНИЯ В СИСТЕМЕ ПОЧВА–РАСТЕНИЕ ПРИ НЕЙТРАЛИЗАЦИИ ПОЧВЕННОЙ КИСЛОТНОСТИ ДОЛОМИТОВОЙ МУКОЙ
С. Е. Витковская 1, 2, *, К. Ф. Шаврина 1, О. Н. Яковлев 1
1 Российский государственный гидрометеорологический университет
192007 Санкт-Петербург, ул. Воронежская, 79, Россия
2 Агрофизический научно-исследовательский институт
195220 Санкт-Петербург, Гражданский просп., 14, Россия
* E-mail: s.vitkovskaya@mail.ru
Поступила в редакцию 21.03.2019
После доработки 15.04.2019
Принята к публикации 10.10.2019
Аннотация
В многолетнем микрополевом эксперименте установлено, что в интервале доз доломитовой муки 0–0.9 Нг урожайность зерна, соломы и половы ячменя линейно возрастала. Установлена тесная корреляционная связь между величинами дозы мелиоранта и соотношения зерно : солома (r = 0.925). Выявлено, что при известковании дерново-подзолистой почвы доломитовой мукой конкурентные взаимодействия Mg–Zn в системе почва–растение проявлялись интенсивнее, чем взаимодействия Ca–Zn. Содержание Zn в зерне, соломе и полове ячменя линейно снижалось с увеличением дозы мелиоранта, возрастанием рН и увеличением содержания обменных соединений Са2+, Mg2+ в почве. Содержание Mg в зерне, соломе и полове ячменя линейно возрастало в интервале доз доломитовой муки 0–1.5 Нг, а содержание Ca практически не зависело от дозы.
ВВЕДЕНИЕ
Интерес к взаимодействию макро- и микроэлементов-аналогов при переходе из почвы в растения направлен на решение экологических и методических задач, связанных с управлением качеством продукции растениеводства. Химическое сродство элементов-аналогов предопределяет сходство их биологического поведения в системе почва–растение: интенсивность сорбции почвой и растениями микро- и ультрамикроэлементов зависит от интенсивности сорбции макроэлемента-аналога [1, 2].
Цинк, кальций и магний, элементы II группы периодической системы химических элементов – неполные химические аналоги. Поглощение Zn растениями должно зависеть от концентрации и распределения Ca и Mg в среде. Так как Ca и Mg относятся к основным элементам питания растений, то его химические аналоги, относящиеся к жизненно важным элементам или/и представляющие опасность для здоровья человека, требуют особого внимания.
Цинк относится к числу эссенциальных (жизненно необходимых) химических элементов [3]. Среднее содержание Zn в поверхностных слоях различных почв изменяется в пределах 17–125 мг/кг. При дефиците Zn подавляется деление клеток, накапливаются редуцирующие сахара, уменьшается содержание сахарозы и крахмала, увеличивается накопление органических кислот, снижается содержание ауксина, нарушается синтез белка [4, 5]. Цинк поступает в растения как катион Zn2+ или в форме хелатных соединений через корни и листья. Признаком недостатка Zn у зерновых культур являются мелколистность и крайчатый хлороз [6].
Цинк – один из важнейших микроэлементов в организме человека. Он входит в состав более двухсот ферментов и гормонов, участвует в основных жизненных процессах: кроветворения, обмене углеводов, жиров и белков, энергетических и редокс-процессах. Этот элемент обнаружен в гипофизе и половых железах, т.е. участвует в процессах размножения, роста и развития. Как недостаток, так и избыток цинка в организме приводит к заболеваниям: анемии, сахарному диабету, нефриту, циррозу печени и другим. Содержание цинка в организме человека составляет 2–3 г, в том числе в крови 0.8–0.9 г, а также в железах внутренней секреции, в мышцах, в печени. Суточная потребность в цинке равна 15–20 мг [7]. Известкование кислых почв может приводить к дефициту Zn для растений, а также рассматривается как прием снижения поступления элемента в растения при повышенном содержании в почвах [8].
Существует взаимосвязь между содержанием Ca, Mg и Zn в растениях [9]. В полевом эксперименте установлено [10], что содержание Zn в зерне, полове и соломе озимой ржи линейно снижалось с увеличением содержания обменного кальция в почве. Выявлено, что конкурентные взаимодействия Mg–Zn в системе почва–растение проявлялись интенсивнее, чем взаимодействия Ca–Zn.
Цель работы – в многолетнем микрополевом эксперименте установить влияние возрастающих доз доломитовой муки (ДМ) на продуктивность растений ячменя и распределение Zn, Ca и Mg в системе почва–растение, выявить закономерности конкурентного взаимодействия указанных элементов-аналогов при переходе из почвы растения.
МЕТОДИКА ИССЛЕДОВАНИЯ
Влияние возрастающих доз ДМ на продуктивность растений ячменя (Hordeum L.) и взаимодействие цинка, кальция и магния в системе почва–растение изучали в условиях многолетнего микрополевого эксперимента, заложенного в мае 2012 г. в Меньковском филиале Агрофизического института в полиэтиленовых сосудах без дна (S = = 1 м2, глубина 25 см, ≈300 кг почвы/сосуд) на дерново-подзолистой легкосуглинистой почве [11, 12]. Перед закладкой опыта из каждой делянки (сосуда) была вынута почва на глубину пахотного слоя (25 см). По периметру делянок размещали полиэтиленовые сосуды без дна, которые наполняли кислой дерново-подзолистой почвой (≈300 кг почвы/сосуд): рНKCl 4.64 ± 0.04, Нг – 4.11 ± 0.08, Ca2+, Mg2+– 2.68 ± 0.14 и 0.36 ± ± 0.06 1/2 ммоль/100 г соответственно. Схема опыта, варианты: 1 – контроль, 2 – фон + ДМ 0.2 Нг, 3 – фон + ДМ 0.3 Нг, 4 – фон + ДМ 0.4 Нг, 5 – фон + ДМ 0.5 Нг, 6 – фон + ДМ 0.6 Нг, 7 – фон + + ДМ 0.7 Нг, 8 – фон + ДМ 0.8 Нг, 9 – фон + ДМ 0.9 Нг, 10 – фон + ДМ 1.5 Нг. Размещение делянок систематическое, 2-рядное, без повторностей. Фон – минеральные удобрения (АФК и Naa) – вносили ежегодно в каждый сосуд. Доза ДМ (СаСO3 – 50.4, MgCO3 – 48.9%) по 1 Нг составляла 5.54 т/га. Смешанные почвенные пробы отбирали 2 раза в год из каждого сосуда тростевым буром: 1-й отбор до внесения удобрений и мелиоранта – 22 мая 2012 г., далее – через 63, 359, 414, 713, 841 сут после закладки опыта. В период наблюдения в опыте выращивали следующие сельскохозяйственные культуры: викоовсяную смесь (2012 г.), рапс (2013 г.), овощные бобы (2014 г.).
В 2015 г. опытной культурой был ячмень сорта Ленинградский. Посев и внесение минеральных удобрений проводили 5 мая (500 семян/делянку или м2). Минеральные удобрения (нитроаммофоска (15:15:15) и аммиачная селитра) были внесены в дозе N120Р100К100. Суммарная за 2012–2015 гг. доза внесенных минеральных удобрений составила N330P250K250. Почвенные пробы отбирали до внесения удобрений 5 мая.
В процессе вегетации растений ячменя определяли динамику высоты растений – 10 замеров за вегетацию (через 15, 22, 28, 35, 42, 49, 56, 70, 77 и 84 сут после посева), объем выборки – 30 растений. Уборку урожая проводили в фазе восковой спелости, через 87 сут после посева. Проводили сплошной учет урожая с каждой делянки.
В почве определяли рНKCl – потенциометрическим методом, гидролитическую кислотность – по Каппену, содержание обменных Ca2+ и Mg2+ – согласно [13]. В почвенных и растительных пробах содержание Zn определяли атомно-абсорбционным методом. Содержание подвижных соединений Zn в почве определяли в вытяжке ААБ рН 4.8, содержание кислоторастворимых соединений устанавливали после химического разложения проб 5М HNO3. Повторность измерений трехкратная. Математическую обработку данных проводили в программе ORIGIN 7.5.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Полевые эксперименты, схемы которых включают широкий диапазон доз мелиоранта, позволяют установить зависимости доза–ответ, количественно характеризующие влияние мелиоранта на параметры плодородия почвы, продуктивность и элементный состав сельскохозяйственных культур. Влияние возрастающих доз ДМ на рост и развитие растений ячменя оценивали по следующим критериям: всхожесть (%), скорость увеличения высоты растений (см/сут), биомасса зерна, соломы и половы (т/га), соотношение массы зерно : солома. Всхожесть растений ячменя в вариантах опыта, установленная через 10 сут после посева, изменялась от 86 ± 5 до 94 ± 6% и не зависела от дозы мелиоранта. Коэффициенты вариации (v) данного показателя не превышали 2–10% (для расчета величины ${v}$ (%) использовали показатели всхожести в каждом рядке (10 рядков в варианте)).
Динамику высоты растений изучали в период от 0 до 81 сут с момента высева семян (10 замеров за вегетацию). Для описания указанного процесса хорошо логистическая (сигмоидная) модель [14, 15]:
где H1 – начальная высота, см (равна нулю), H2 – максимальная высота растений (см), t0 – точка перегиба, в момент которой H = 1/2(H1 + H2), dt – крутизна кривой (угол наклона) – постоянная величина для данной кривой. Скорость роста в высоту (см/сут) достигала максимума в момент t = t0. Отношение (H2 – H1)/4dt характеризовало скорость на момент времени t0 (максимальную), см/сут (Vmax) (табл. 1).Таблица 1.
Параметры логистической модели, характеризующие динамику высоты растений ячменя
| Вариант | r2 | H1, см | H2, см | t0, сут | dt | Vmax, см/сут |
|---|---|---|---|---|---|---|
| 1. Контроль | 0.98 | 0 | 94 ± 5 | 46 ± 2 | 9.2 ± 1.5 | 2.6 |
| 2. ДМ 0.2 Нг | 0.98 | 0 | 96 ± 5 | 46 ± 2 | 8.5 ± 1.4 | 2.8 |
| 3. ДМ 0.3 Нг | 0.98 | 0 | 96 ± 4 | 45 ± 2 | 8.6 ± 1.4 | 2.8 |
| 4. ДМ 0.4 Нг | 0.98 | 0 | 97 ± 4 | 44 ± 2 | 9.2 ± 1.3 | 2.6 |
| 5. ДМ 0.5 Нг | 0.98 | 0 | 99 ± 4 | 45 ± 2 | 8.7 ± 1.3 | 2.8 |
| 6. ДМ 0.6 Нг | 0.99 | 0 | 98 ± 4 | 45 ± 1 | 8.8 ± 1.2 | 2.8 |
| 7. ДМ 0.7 Нг | 0.99 | 0 | 98 ± 4 | 46 ± 2 | 8.8 ± 1.2 | 2.8 |
| 8. ДМ 0.8 Нг | 0.98 | 0 | 99 ± 5 | 45 ± 2 | 8.8 ± 1.4 | 2.8 |
| 9. ДМ 0.9 Нг | 0.98 | 0 | 100 ± 5 | 45 ± 2 | 8.9 ± 1.4 | 2.8 |
| 10. ДМ 1.5 Нг | 0.99 | 0 | 94 ± 4 | 45 ± 1 | 8.8 ± 1.2 | 2.7 |
Установлено, что величина Vmax, характеризующая рост растений ячменя в высоту, не зависела от дозы ДМ, варьировалась в пределах 2.6–2.8 см/сут. Полученные в ходе исследования величины Vmax практически совпадали с показателями для указанной сельскохозяйственной культуры, установленными ранее [15].
Влияние возрастающих доз ДМ на урожайность растений ячменя районированного сорта Ленинградский представлено в табл. 2. Максимальная урожайность зерна, отмеченная в интервале доз ДМ 0.5–0.9 Нг, варьировалась в пределах 4.5–4.9 т/га, что на 29–39% больше, чем в контрольном варианте. Известно [16], что максимальный урожай ячменя данного сорта (5.24 т/га), был получен в Ленинградской обл. в 2006 г.
Таблица 2.
Влияние возрастающих доз ДМ на урожайность растений ячменя, т/га [8]
| Вариант | Зерно | Солома | Полова | Зерно : солома |
|---|---|---|---|---|
| 1. Контроль | 3.49 | 3.97 | 0.71 | 0.88 |
| 2. ДМ 0.2 Нг | 4.37 | 4.55 | 0.83 | 0.96 |
| 3. ДМ 0.3 Нг | 4.29 | 4.69 | 0.82 | 0.91 |
| 4. ДМ 0.4 Нг | 4.19 | 4.26 | 0.79 | 0.98 |
| 5. ДМ 0.5 Нг | 4.70 | 4.63 | 0.85 | 1.01 |
| 6. ДМ 0.6 Нг | 4.87 | 4.84 | 0.86 | 1.00 |
| 7. ДМ 0.7 Нг | 4.52 | 4.44 | 0.81 | 1.01 |
| 8. ДМ 0.8 Нг | 4.74 | 4.75 | 0.93 | 1.00 |
| 9. ДМ 0.9 Нг | 4.76 | 4.62 | 0.86 | 1.03 |
| 10. ДМ 1.5 Нг | 3.86 | 3.51 | 0.67 | 1.10 |
Влияние ДМ в дозах 0.5–0.6 Нг на урожайность зерна ячменя было практически идентично влиянию доз 0.8–0.9 Нг. При внесении ДМ в дозе 1.5 Нг наблюдали снижение биомассы ячменя: прибавка урожая зерна по отношению к контролю не превысила 11% [8]. В интервале доз мелиоранта 0–0.9 Нг зависимости урожайности зерна, соломы и половы ячменя от дозы характеризовались коэффициентами корреляции (r) 0.830, 0.606 и 0.760, соответственно (критическая величина r на 5%-ном уровне значимости равна 0.666).
Установлена тесная корреляционная связь между дозой ДМ и соотношением массы зерно : солома в урожае ячменя (r = 0.925, при критической величине r на 5%-ном уровне значимости равной 0.632).
При известковании кислых почв доломитовой мукой изменение кислотно-основных свойств почвы, насыщение ППК кальцием и магнием приводит к усилению конкурентных взаимодействий в системе почва–растение между указанными химическими элементами и другими ионами, присутствующими в почвенном растворе. Влияние возрастающих доз ДМ на содержание Ca, Mg и Zn в растениях ячменя характеризуют экспериментальные данные, представленные в табл. 3. Содержание Zn в зерне, соломе и полове ячменя линейно снижалось с увеличением дозы ДМ (табл. 4). Внесение повышенной (1.5 Нг) дозы мелиоранта привело к снижению содержания Zn в зерне, соломе и полове ячменя по отношению к контрольному варианту в 6, 3 и 4 раза соответственно. Известно [4], что среднее содержание Zn в зерне ячменя в разных странах варьируется от 15 до 51 мг/кг, содержание элемента при его дефиците оценивается в 10–20 мг/кг сухой массы. Установлено, что при внесении ДМ в дозе 1.5 Нг содержание Zn в зерне ячменя снизилось до 7.0 мг/кг, в остальных вариантах опыта находилось в пределах нормы.
Таблица 3.
Влияние возрастающих доз доломитовой муки на содержание цинка (мг/кг), кальция и магния (%, а.с.в) в растениях ячменя
| Вариант | Ca | Mg | Zn | Ca | Mg | Zn |
|---|---|---|---|---|---|---|
| Зерно | Солома | |||||
| 1. Контроль | 0.08 ± 0.02 | 0.07 ± 0.01 | 42 ± 2 | 0.50 ± 0.03 | 0.04 ± 0.0 | 10 ± 0.3 |
| 2. ДМ 0.2 Нг | 0.08 ± 0.01 | 0.06 ± 0.01 | 32 ± 1 | 0.47 ± 0.03 | 0.06 ± 0.01 | 8.3 ± 0.3 |
| 3. ДМ 0.3 Нг | 0.06 ± 0.01 | 0.08 ± 0.01 | 29 ± 1 | 0.43 ± 0.01 | 0.06 ± 0.01 | 5.8 ± 0.4 |
| 4. ДМ 0.4 Нг | 0.06 ± 0.01 | 0.08 ± 0.01 | 29 ± 1 | 0.37 ± 0.02 | 0.06 ± 0.01 | 6.2 ± 0.1 |
| 5. ДМ 0.5 Нг | 0.07 ± 0.01 | 0.09 ± 0.01 | 28 ± 1 | 0.47 ± 0.01 | 0.07 ± 0.01 | 4.6 ± 0.5 |
| 6. ДМ 0.6 Нг | 0.08 ± 0.01 | 0.09 ± 0.01 | 25 ± 1 | 0.43 ± 0.02 | 0.14 ± 0.0 | 4.4 ± 0.3 |
| 7. ДМ 0.7 Нг | 0.09 ± 0.01 | 0.09 ± 0.01 | 23 ± 1 | 0.43 ± 0.01 | 0.10 ± 0.01 | 3.2 ± 0.1 |
| 8. ДМ 0.8 Нг | 0.09 ± 0.01 | 0.08 ± 0.01 | 24 ± 1 | 0.43 ± 0.01 | 0.07 ± 0.01 | 3.2 ± 0.1 |
| 9. ДМ 0.9 Нг | 0.08 ± 0.01 | 0.09 ± 0.01 | 23 ± 1 | 0.46 ± 0.02 | 0.08 ± 0.01 | 5.6 ± 0.5 |
| 10. ДМ 1.5 Нг | 0.08 ± 0.01 | 0.11 ± 0.01 | 7 ± 0.5 | 0.46 ± 0.02 | 0.11 ± 0.01 | 2.9 ± 0.1 |
| Полова | Корни | |||||
| 1. Контроль | 0.54 ± 0.02 | 0.22 ± 0.02 | 17 ± 2 | 0.19 ± 0.03 | 0.40 ± 0.02 | 14 ± 1 |
| 2. ДМ 0.2 Нг | 0.57 ± 0.03 | 0.22 ± 0.02 | 9.5 ± 0.5 | 0.39 ± 0.02 | 0.82 ± 0.01 | 13 ± 1 |
| 3. ДМ 0.3 Нг | 0.61 ± 0.02 | 0.29 ± 0.01 | 9.8 ± 0.5 | 0.36 ± 0.03 | 0.50 ± 0.03 | 11 ± 0.5 |
| 4. ДМ 0.4 Нг | 0.59 ± 0.04 | 0.26 ± 0.01 | 9.3 ± 0.4 | 0.39 ± 0.02 | 0.45 ± 0.03 | 13 ± 1 |
| 5. ДМ 0.5 Нг | 0.73 ± 0.04 | 0.32 ± 0.02 | 6.0 ± 0.5 | 0.45 ± 0.02 | 0.74 ± 0.04 | 11 ± 1 |
| 6. ДМ 0.6 Нг | 0.57 ± 0.05 | 0.30 ± 0.01 | 5.8 ± 0.2 | 0.46 ± 0.03 | 0.54 ± 0.02 | 12 ± 1.5 |
| 7. ДМ 0.7 Нг | 0.61 ± 0.03 | 0.32 ± 0.02 | 5.7 ± 0.4 | 0.41 ± 0.01 | 0.40 ± 0.01 | 12 ± 1 |
| 8. ДМ 0.8 Нг | 0.47 ± 0.03 | 0.28 ± 0.02 | 6.7 ± 0.5 | 0.55 ± 0.02 | 0.47 ± 0.01 | 13 ± 1 |
| 9. ДМ 0.9 Нг | 0.58 ± 0.04 | 0.30 ± 0.01 | 5.9 ± 0.5 | 0.42 ± 0.03 | 0.48 ± 0.02 | 9 ± 0.5 |
| 10. ДМ 1.5 Нг | 0.52 ± 0.02 | 0.43 ± 0.04 | 4.3 ± 0.2 | 0.49 ± 0.01 | 0.59 ± 0.02 | 12 ± 0.5 |
Таблица 4.
Коэффициенты корреляции, характеризующие зависимости содержания Zn, Ca и Mg в растениях ячменя от дозы доломитовой муки
| Зависимость | Зерно | Солома | Полова | Корни |
|---|---|---|---|---|
| Са(f) = Доза ДМ | 0.334 | –0.093 | –0.273 | 0.711 |
| Mg(f) = Доза ДМ | 0.887 | 0.604 | 0.903 | –0.036 |
| Zn(f) = Доза ДМ | –0.972 | –0.794 | –0.787 | –0.468 |
| Zn(f) = Ca | –0.236 | 0.394 | –0.127 | –0.402 |
| Zn(f) = Mg | –0.884 | –0.682 | –0.745 | –0.057 |
Содержание Mg в зерне, соломе и полове растений ячменя линейно возрастало в интервале доз ДМ 0–1.5 Нг, а содержание Ca практически не зависело от дозы мелиоранта. Коэффициент корреляции (r), характеризующий зависимость Ca(f) = = доза, в корнях растений составил 0.711 (табл. 4).
Взаимодействия Mg–Zn и Са–Zn в вегетативных и генеративных органах растений ячменя также аппроксимирует линейная модель. Содержание Zn в зерне, соломе и полове ячменя линейно снижалось с увеличением содержания Mg, и практически не зависело от содержания Ca.
Опыт показал, что при внесении ДМ увеличение содержания Mg в растениях оказывало значительно более существенное влияние на содержание Zn в растениях, чем увеличение содержания Ca, что, вероятно, связано с соотношением содержаний данных макроэлементов в почве. На момент закладки опыта содержание обменного Са2+ в почве составляло 2.7 ± 0.1, обменного Mg2+ – 0.36 ± 0.06 $\frac{1}{2}$ ммоль/100 г, что, согласно градации почв по содержанию элементов питания [17], соответствует низкому и очень низкому содержанию элементов соответственно. Известно [18], что обменного Mg2+ в почвах содержится в 2–8 раз меньше, чем обменного Са2+. Особенно бедны обменными основаниями кислые дерново-подзолистые почвы легкого гранулометрического состава. В почве опыта до внесения ДМ содержание Са2+ превышало содержание Mg2+ в 7.5 ± 1.4 раза [11]. То есть, при внесении мелиоранта в почву увеличение содержания Mg2+ было гораздо более существенным для растений, чем увеличение содержания Са2+.
Влияние возрастающих доз ДМ на содержание обменных соединений Са2+, Mg2+ и подвижных соединений Zn в почве на момент уборки растений (1211-е сут взаимодействия мелиоранта с почвой) представлено в табл. 5.
Таблица 5.
Влияние возрастающих доз доломитовой муки на содержание обменных Са2 и Mg2+ (1/2 ммоль/100 г) и подвижных соединений Zn (мг/кг) в почве*
| Вариант | Са2+ | Mg2+ | Zn |
|---|---|---|---|
| 1. Контроль | 3.4 ± 0.3 | 1.2 ± 0.02 | 0.66 ± 0.05 |
| 2. ДМ 0.2 Нг | 3.4 ± 0.2 | 1.6 ± 0.05 | 0.67 ± 0.04 |
| 3. ДМ 0.3 Нг | 3.4 ± 0.2 | 2.4 ± 0.1 | 0.47 ± 0.04 |
| 4. ДМ 0.4 Нг | 3.7 ± 0.3 | 2.7 ± 0.1 | 0.57 ± 0.02 |
| 5. ДМ 0.5 Нг | 3.8 ± 0.1 | 3.1 ± 0.2 | 0.31 ± 0.01 |
| 6. ДМ 0.6 Нг | 4.0 ± 0.2 | 3.0 ± 0.2 | 0.39 ± 0.01 |
| 7. ДМ 0.7 Нг | 4.1 ± 0.1 | 3.3 ± 0.3 | 0.32 ± 0.01 |
| 8. ДМ 0.8 Нг | 4.0 ± 0.1 | 3.3 ± 0.3 | 0.36 ± 0.02 |
| 9. ДМ 0.9 Нг | 4.8 ± 0.1 | 3.4 ± 0.2 | 0.34 ± 0.01 |
| 10. ДМ 1.5 Нг | 4.7 ± 0.1 | 3.5 ± 0.1 | 0.29 ± 0.01 |
Известно [19], что растворимость и доступность растениям соединений цинка возрастает с подкислением среды. Минимальную растворимость соединений Zn отмечают при рН 5.5–6.9, дальнейшее повышение рН ведет к увеличению растворимости, т.к. Zn как амфотерный элемент образует в щелочной среде цинкаты типа Zn(ONa)2 (или Na2ZnО2). Однако в присутствии достаточных количеств Са подвижность соединений Zn и в слабощелочной среде мала ввиду малой растворимости цинкатов кальция. Имеется информация [4], что растворимость и доступность Zn в почвах обнаруживают отрицательную корреляционную связь со степенью насыщенности кальцием. Низкое содержание доступного для растений Zn наблюдается в карбонатных почвах, особенно легкого гранулометрического состава [20].
Установлено, что в интервале доз ДМ 0–1.5 Нг на момент уборки урожая (1211-е сут взаимодействия ДМ с почвой) содержание подвижных соединений Zn линейно зависело от содержаний обменных Са2+, Mg2+ в почве: зависимости Zn(f) = Ca и Zn(f) = Mg характеризовались коэффициентами корреляции (r) –0.736 и –0.928 соответственно.
Содержание Zn в зерне, соломе, полове и корнях растений ячменя линейно снижалось с увеличением содержания обменных соединений Са2+, Mg2+ в почве (табл. 6), (рис. 1).
Таблица 6.
Коэффициенты корреляции (r)*, характеризующие взаимодействие цинка, кальция и магния в системе почва–растение
| Зависимость | Зерно | Солома | Полова | Корни |
|---|---|---|---|---|
| Са(почва)–Са(растения) | 0.487 | 0.257 | –0.214 | 0.550 |
| Са(почва)–Mg(растения) | 0.712 | 0.572 | 0.731 | –0.150 |
| Са(почва)–Zn(растения) | –0.814 | –0.623 | –0.709 | –0.612 |
| Mg(почва)–Са(растения) | 0.207 | –0.384 | – | 0.823 |
| Mg(почва)–Mg(растения) | 0.806 | 0.667 | 0.777 | –0.117 |
| Mg(почва)–Zn(растения) | –0.825 | –0.936 | –0.914 | –0.668 |
| Zn(почва)–Zn(растения) | 0.770 | 0.905 | 0.836 | 0.673 |
Рис. 1.
Зависимость содержания цинка в растениях ячменя от содержания: (а) – обменного магния и (б) – обменного кальция в почве.

Общепринято [21], что реакция почвы оказывает наибольшее влияние на содержание цинка в растениях: в почвах с рН$_{{{{{\text{Н}}}_{{\text{2}}}}{\text{О}}}}$ 6.0 бóльшая часть цинка находится в недоступной для растений форме, с увеличением кислотности почвы доступность Zn резко возрастает. Экспериментально установлено [22], что поглощение Zn растениями (Zea mays L.) значительно возросло, когда рН почвы снизился с 7.4 до 6.3.
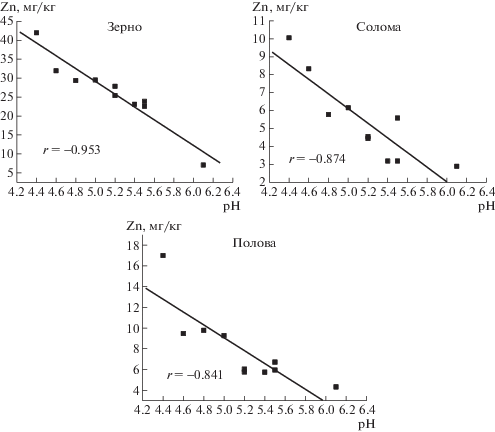
Опыт показал, что с увеличением рНKCl почвы линейно снижалось содержание Zn в зерне, соломе и полове ячменя. Наиболее тесной корреляционной связью (r = –0.953) характеризовалась зависимость Zn(зерно)–рН(почва) (рис. 2). Коэффициент корреляции, характеризующий зависимость Zn(корни)–рН(почва) не превысил –0.496 (критическая величина r на 5%-ном уровне значимости равна –0.632).
ВЫВОДЫ
1. Для описания динамики высоты растений ячменя хорошо подходит логистическая (сигмоидная) модель. Величины максимальной скорости роста растений ячменя в высоту (Vmax) не зависели от дозы доломитовой муки, варьировались в пределах 2.6–2.8 см/сут.
2. В интервале доз доломитовой муки (ДМ) 0–0.9 Нг урожайность зерна, соломы и половы ячменя линейно возрастали (коэффициенты корреляции (r) были равны 0.830, 0.606 и 0.760 соответственно). Максимальная урожайность зерна ячменя установлена в интервале доз ДМ 0.5–0.9 Нг (4.5–4.9 т/га, что на 29–39% больше, чем в контрольном варианте).
3. При известковании кислых почв доломитовой мукой изменение кислотно-основных свойств почвы, насыщение ППК кальцием и магнием приводили к усилению конкурентных взаимодействий в системе почва–растение между ионами Са, Mg, Zn, присутствующими в почвенном растворе.
4. Содержание Zn в зерне, соломе и полове ячменя линейно снижалось с увеличением дозы ДМ, возрастанием рН почвенного раствора и увеличением содержания обменных соединений Са2+и Mg2+ в почве. Внесение повышенной (1.5 Нг) дозы мелиоранта привело к снижению содержания Zn в зерне, соломе и полове ячменя по отношению к контрольному варианту в 6, 3 и 4 раза соответственно.
5. Содержание Mg в зерне, соломе и полове растений ячменя линейно возрастало в интервале доз ДМ 0–1.5 Нг, содержание Ca практически не зависело от дозы мелиоранта.
6. Увеличение содержания Mg в почве и растениях при внесении ДМ оказывало более существенное влияние на содержание Zn в растениях, чем увеличение содержания Ca.
Список литературы
Дричко В.Ф., Цветкова В.В. Сорбционная модель поступления радионуклидов из почвы в растения // Почвоведение. 1990. № 10. С. 35–40.
Витковская С.Е. Взаимодействие фосфора и радиосурьмы в системе почва–растение: Дис. … канд. биол. наук, Обнинск, 1996. 171 с.
Исидоров В.А. Введение в химическую экотоксикологию: Уч. пособ. СПб.: Химиздат, 1999. 144 с.
Кабата-Пендиас А., Пендиас Х. Микроэлементы в почвах и растениях. М.: Мир, 1989. 439 с.
Mousavi S.R., Galavi M., Rezaei M. The interaction of zinc with other elements in plants: a review // Inter. J. Agr. Crop Sci. 2012. V. 4(24). P. 1881–1884.
Вильдфлуш И.Р. Эффективность применения микроудобрений и регуляторов роста при возделывании сельскохозяйственных культур. Минск: Бел. наука, 2011. 293 с.
Ткаченко А.В., Маковкина Д.В., Дробышева О.М. Элемент здоровья – цинк и его определение в различных компонентах // Здоровье и образование в XXI веке. 2017. Т. 19. № 10. С. 264–266.
Шаврина К.Ф., Витковская С.Е. Влияние возрастающих доз доломитовой муки на распределение цинка в растениях ячменя // Мат-лы Всерос. научн. конф. с международ. участием “Агроэкосистемы в естественных и регулируемых условиях: от теоретической модели к практике прецизионного управления” (с семинаром “Полуэктовские чтения – 2016”), 21–23 сентября 2016 г. СПб.: АФИ, 2016. С. 382–386.
Тихомирова В.Я., Сорокина О.Ю. Взаимодействие магния, кальция и калия при поступлении в молодые растения льна-долгунца // Агрохимия. 2007. № 3. С. 28–33.
Витковская С.Е., Шаврина К.Ф. Влияние различных доз органических и минеральных удобрений на накопление цинка растениями озимой ржи // Агрофизика. 2017. № 3. С. 4–12.
Витковская С.Е., Яковлев О.Н., Шаврина К.Ф. Влияние возрастающих доз доломитовой муки на кислотно-основные свойства дерново-подзолистой почвы // Агрохимия. 2016. № 7. С. 3–11.
Витковская С.Е., Яковлев О.Н. Влияние возрастающих доз доломитовой муки на распределение марганца и железа в системе почва–растение // Агрохимия. 2017. № 11. С. 44–51.
ГОСТ 26487-85. Определение обменного кальция и обменного (подвижного) магния методами ЦИНАО. Введ. 26.03.85 // Сб. гос. стандартов. М.: Изд-во стандартов, 1985. С. 21–33.
Витковская С.Е., Дричко В.Ф., Хофман О.В. Оценка скорости нарастания биомассы сельскохозяйственных культур // Докл. РАСХН. 2014. № 1. С. 50–53.
Витковская С.Е. Закономерности формирования биомассы и элементного состава растений ячменя в полевом опыте // Агрохимия. 2015. № 1. С. 63–72.
ФГБНУ “Ленинградский НИИСХ Белогорка”. http://lniish.ru/sorts/grain/leningradskiy.html
Методические указания по проведению комплексного мониторинга плодородия почв земель сельскохозяйственного назначения. М., 2003. 195 с.
Воеводина Л.А., Воеводин О.В. Магний для почвы и растений // Научн. журн. Рос. НИИ проблем мелиорации. 2015. № 2(18). С. 70–81.
Возбуцкая А.Е. Химия почвы. М.: Высш. шк., 1968. 429 с.
Ефимов В.Н., Калиниченко В.Г., Горлова М.Л. Применение микроэлементов при выращивании сельскохозяйственных культур (овощные, кормовые корнеплоды, многолетние травы) на почвах Северо-Запада Нечерноземной зоны РСФСР: Уч. пособ. Л.: ЛГАУ, 1991. 36 с.
Химия тяжелых металлов, мышьяка и молибдена в почвах / Под ред. Зырина Н.Г. и Садовниковой Л.К. М.: Изд-во МГУ, 1985 208 с.
Amrani M., Westfall D.G., Petersen G.A. Zinc plant availability as influenced by zinc fertilizer sources and zinc water-solubility // Technic. Bul. TB97-4, Agricult. Exp. Station, Department of soil and crop sciences. September. 1997. 17 p.
Дополнительные материалы отсутствуют.