Журнал аналитической химии, 2019, T. 74, № 10, стр. 761-773
Новые электродные материалы и технологии измерений в вольтамперометрии, амперометрии и кулонометрии
С. С. Ермаков a, *, Д. В. Наволоцкая a, Е. А. Семенова a
a Санкт-Петербургский государственный университет, Институт химии
198504 Санкт-Петербург, Петергоф, Университетский просп., 26, Россия
* E-mail: s.ermakov@spbu.ru
Поступила в редакцию 27.11.2018
После доработки 20.03.2019
Принята к публикации 29.04.2019
Аннотация
Электрохимические методы анализа традиционно характеризуются высокой чувствительностью, простотой автоматизации, широким спектром определяемых аналитов и анализируемых объектов. Развитие электрохимических методов анализа на современном этапе во многом определяется созданием новых наноструктурированных электродных материалов, обладающих электрокаталитическими свойствами. Использование таких материалов во многих случаях позволяет повысить чувствительность и селективность определения целого ряда аналитов. Другим традиционным способом снижения предела обнаружения электрохимически активных веществ является разработка новых способов измерений, позволяющих улучшить соотношение сигнал/шум в неравновесных электрохимических методах анализа. Рассмотрению некоторых новых электродных материалов и способов электрохимических измерений посвящена настоящая статья.
НОВЫЕ СПОСОБЫ ПОЛУЧЕНИЯ РАБОЧИХ ЭЛЕКТРОДОВ ДЛЯ ВОЛЬТАМПЕРОМЕТРИИ
Одним из современных направлений развития электрохимических методов является миниатюризация анализа за счет создания электрохимических сенсоров. Ключевым компонентом амперометрического или вольтамперометрического сенсора, определяющим его эффективность, является рабочий электрод. Использование наноструктурированных материалов позволяет создавать электроды с высокоразвитой рабочей поверхностью и высокой электрохимической активностью и за счет этого существенно повысить чувствительность измерений [1–5]. Ниже рассмотрено несколько новых подходов к синтезу наноструктурированных материалов, которые были использованы на кафедре аналитической химии Института химии СПбГУ для создания вольтамперометрических сенсоров.
Метод ионного наслаивания. Аналитические возможности электродов, модифицированных наночастицами оксидов металлов. Один из методов, успешно применяемых для модификации поверхности электродов, − метод ионного наслаивания (ИН, SILD – successive ionic layer deposition). Считается, что первые работы, посвященные послойному синтезу с использованием растворов солей металлов были проведены Николау [6] и Толстым [7]. Принцип метода иллюстрирует рис. 1 [8].
Рис. 1.
Схематическое изображение последовательности обработок подложки реагентами при послойном синтезе.

В настоящее время метод послойного синтеза успешно применяется для синтеза наночастиц металлов, их оксидов и солей непосредственно на поверхности электродов. Количество слоев на поверхности электрода можно регулировать числом циклов в одном синтезе.
Модифицированные электроды, полученные методом ионного наслаивания, получили широкое распространение в химических и биологических сенсорах. Это связано с тем, что выбор компонентов для ионного наслаивания позволяет формировать модифицирующие слои для сенсоров практически на все классы соединений: неорганические и органические вещества, биологически активные вещества и глюкозу. Методом “слой-за-слоем” можно включать в поверхностный слой все необходимые компоненты: медиаторы, ферменты и другие вещества, ответственные за получение аналитического сигнала [8].
Одним из наиболее распространенных наноразмерных модификаторов являются наночастицы золота, которые также успешно синтезируются послойным синтезом. Пример послойного синтеза наночастиц золота на поверхности электрода из оксида индия−олова, приведен в работе [9]. Методом циклической вольтамперометрии показано, что модификация поверхности приводит к существенному увеличению истинной поверхности электрода и чувствительности при определении пероксида водорода.
Другие успешно синтезируемые методом ИН наноструктуры – наночастицы оксидов металлов. Они удобны для электрокатализа по нескольким причинам. Во-первых, оксиды металлов существенно более устойчивы к окислению кислородом, что позволяет использовать для электрокатализа не только благородные, но и более активные металлы после их электрохимического восстановления из оксидов. Во-вторых, многие оксиды (Co, Fe, Ni, Mn и др.) за счет изменения степени окисления в ходе электрохимической реакции могут служить медиаторами электронного переноса. В ряде случаев использование оксидов металлов позволяет существенно снизить предел обнаружения биологически важных аналитов, таких как, например, пероксид водорода. Использование электродов на основе смешанного оксида Fe0.5MnOx, полученного методом ионного наслаивания, позволяет снизить предел обнаружения Н2О2 до 10–8 М [10]. Подробно возможности сенсоров на основе электродов, модифицированных методом ИН, рассмотрены в обзоре [8].
Лазерное осаждение металлов и сплавов из раствора (ЛОМР) для создания бесферментных сенсоров. Новейшим методом получения микроэлектродов из металлов, сплавов и металл-оксидных материалов является ЛОМР − лазерно-индуцированное осаждение из раствора [11]. Принцип метода состоит в осаждении лучом лазера из раствора, содержащего соли металлов и восстановитель, металла или сплава на поверхности диэлектрической подложки. Принципиальная схема установки приведена на рис. 2а. На схеме изображена геометрия облучения диэлектрика “со стороны раствора”, используемая для прозрачных и слабо поглощающих излучение лазера материалов. В соответствии со схемой луч твердотельного лазера (1) попадает в систему коллимирующих зеркал (2), затем – в светоделительный куб (3), далее через прозрачное кварцевое стекло рабочей кюветы (5) и рабочий раствор (6) на диэлектрическую подложку (7), где фокусируется в пятно (d = = 5−10 мкм) с помощью 8-кратного объектива (4) на поверхности раздела диэлектрик−раствор. Отражаемый от подложки (7) свет проходит в обратном порядке через раствор (6), кварцевую стенку кюветы (5), объектив (4) и на светоделительном кубе (3) делится таким образом, что часть излучения через систему фокусировки (9) попадает на web-камеру (10), используемую для наблюдения процессов осаждения металла in situ и фокусировки исходного луча на подложке (7) на экране монитора. Диэлектрик и раствор электролита помещены на моторизованную подвижку (8), управляемую контроллером (12). Для подачи управляющих команд с ПК (11) используется программное обеспечение Standa Ltd. На монитор компьютера (11) также поступает информация от web-камеры (10), с помощью которой процесс фиксируется в режиме реального времени.
Рис. 2.
Схема экспериментальной установки для лазерно-индуцированного осаждения металлов из раствора (а). Электронно-микроскопическая (б) и оптическая (в) микрофотографии медного осадка из раствора, содержащего формалин в качестве восстановителя.

Полученные таким образом осадки металла содержат также оксиды, поскольку восстановление происходит при сильном разогреве приповерхностного слоя. Полученные осадки достаточно миниатюрны и, как правило, обладают достаточно развитой поверхностью (рис. 2б, 2в).
Изучению сенсорных свойств меди и сплавов меди с Co, Fe, Zn, Ni, Au (без использования биоселекторов), полученных методом ЛОМР, посвящены работы [12–16]. В качестве аналитов традиционно использовали пероксид водорода и глюкозу. Установлено, что наиболее высокой чувствительностью к этим аналитам обладает медь и ее сплавы с кобальтом и золотом. Использование сплава меди с золотом в качестве материала рабочего электрода позволяет достичь предела обнаружения (ПО) на уровне 0.025 мкМ. Показана высокая селективность полученных сенсорных материалов по отношению к основным метаболитам крови [15]. Сплавы меди с кобальтом характеризуются ПО 2.2 мкМ при верхней границе линейного диапазона до 30 мкМ [16]. Таким образом, ЛОМР является перспективным методом получения сенсорных материалов.
Прямое электрохимическое осаждение металлов и сплавов из раствора. Аналитические характеристики полученных наноструктурированных материалов на примере определения биологически значимых аналитов. Другой экспрессный метод получения наноструктур на основе металлов и их сплавов, предложенный недавно Оцтурком с соавт. [17] – прямое электрохимическое осаждение из раствора (directed electrochemical nanowire assembly, DENA). Принцип метода иллюстрирует рис. 3.
Рис. 3.
Схематическое изображение наложения сигнала при электроосаждении (а) и схема установки для направленного электрохимического синтеза наноструктурированных ультрамикроэлектродов (б).

В работах [18, 19] получены наноструктурированные ультрамикроэлектроды (УМЭ) диаметром 50−800 нм из золота, палладия и сплава палладий–золото. В работе [18] показано, что чувствительность и ПО при определении глюкозы составили 3.7 × 10−4 A/(М м2) и 33 мкМ соответственно, линейный диапазон – 0.1–5 мМ. В работе [19] методом DENA синтезированы УМЭ из сплава палладий–золото, найдены аналитические характеристики этих электродов при определении пероксида водорода: линейный диапазон 10−6–10−3 М, ПО 3 × 10−7 М и чувствительность – 18 мкA/M. Отмечена очень малая величина приложенного потенциала при амперометрическом определении пероксида водорода: 0.05 В против хлоридсеребряного электрода (Ag/AgCl, 3 M KCl), что делает этот материал биосовместимым. Последнее обстоятельство позволило применить его для изучения оксидативного стресса раковых клеток HL-1 [19]. В работе [20] отмечена перспективность электродов, полученных методом DENA, для мультисенсорных систем.
НОВЫЕ СПОСОБЫ ПРОБОПОДГОТОВКИ И ОБРАБОТКИ ПОВЕРХНОСТИ ЭЛЕКТРОДОВ
Важную роль в анализе играет подготовка пробы и, в частности, выделение аналита. Один из новых вариантов выделения аналита − первапорация [21], позволяющая упростить и автоматизировать подготовку пробы. В работе [21] первапорацию использовали для выделения этанола из биотоплива для последующего вольтамперометрического определения.
Другой важной стадией вольтамперометрических измерений является подготовка поверхности электрода. Эта стадия играет особенно важную роль при измерениях на твердых металлических электродах. Использование нового подхода к обновлению поверхности твердых металлических электродов, основанного на отказе от традиционного механического полирования и применение электрохимического полирования для золотого [22] и никелевого электродов [23], позволили существенно повысить чувствительность вольтамперометрических измерений.
НОВЫЕ ПОДХОДЫ К АМПЕРОМЕТРИЧЕСКИМ И ВОЛЬТАМПЕРОМЕТРИЧЕСКИМ ИЗМЕРЕНИЯМ
Каждый электрохимический метод анализа может быть описан с помощью двух характеристик – формы фактора возбуждения и соответствующей структуры аналитического сигнала. Именно эти две взаимосвязанные характеристики лежат в основе классификации электроаналитических методов, рекомендованной ИЮПАК [24], и определяют “технологию” электрохимических измерений. Изменение формы фактора возбуждения приводит к изменениям в структуре аналитического сигнала и, соответственно, к изменению чувствительности измерений.
Чувствительность электрохимических измерений определяется соотношением сигнал/шум. В амперометрии и вольтамперометрии под полезным сигналом принято понимать фарадеевский ток (в частности – диффузионный), зависящий от концентрации аналита. Помехой или “шумом” является остаточный ток, основной частью которого является ток заряжения двойного электрического слоя. Существует множество подходов к повышению соотношения сигнал/шум в амперометрии и вольтамперометрии. Их можно условно разделить на две группы – математические и инструментальные.
К математическим подходам можно отнести дифференцирование сигнала [25–28], Фурье- [29–32] и вейвлет-преобразования [33–36], которые эффективно устраняют “шумы”, при этом улучшая чувствительность и разрешение измерений. Однако эти методы заключаются в математической обработке уже полученных экспериментальных данных, но не улучшают аналитический сигнал физически. Более того, в некоторых случаях математическая обработка может привести к потере части полезного сигнала.
Большинство инструментальных подходов к повышению чувствительности измерений основано на временнóй и фазовой селекциях сигнала, которые позволяют разделять емкостной и фарадеевский токи. Временнáя селекция сигнала реализована в импульсной [37–39], дифференциально-импульсной [40, 41] и квадратно-волновой вольтамперометрии [42–44]. Фазовая селекция сигнала используется в переменнотоковой вольтамперометрии [45–48] и, в частности, в синусоидальной вольтамперометрии [49–53]. Различные инверсионные методы также являются мощными инструментами для повышения чувствительности измерений, так как фарадеевский ток увеличивается за счет предварительного концентрирования аналита или его производных на электроде [54–57].
Ниже рассмотрены два новых подхода к амперометрическим измерениям, существенно повышающим их чувствительность, разработанные на кафедре аналитической химии Института химии СПбГУ.
Переменнотоковая амперометрия. Один из способов повышения чувствительности и селективности вольтамперометрических измерений – дифференцирование тока по потенциалу как в постояннотоковом, так и в импульсном и переменнотоковом вариантах. В случае амперометрии дифференцирование предельного диффузионного тока по потенциалу приводит практически к нулевому значению. Классический вариант повышения чувствительности амперометрии, основанный на временнóй селекции сигнала – нормальный импульсный способ измерений, приводящий к увеличению чувствительности в 6−7 раз, но не повышающий селективность. В связи с этим амперометрия в классическом варианте находит применение в качестве способа детектирования в электрохимических сенсорах, хроматографии и в проточном инжекционном анализе, где селективность обеспечивается за счет предварительного разделения аналитов или использования химических реакций.
Другой вариант – использование импульсно-переменнотокового способа измерения [58, 59]. Сущность метода состоит в том, что на рабочий электрод налагают импульс определенной высоты, на фронт которого подают переменнотоковую, синусоидальную или прямоугольную развертку напряжения. В результате происходит селекция тока. Ток электрохимической реакции регистрируется в области потенциалов полуволны определяемого компонента. Форма налагаемого импульса представлена на рис. 4.
Рис. 4.
Форма импульса, налагаемого на рабочий электрод при измерениях в импульсном переменно-токовом режиме, где ΔE – высота импульса; ΔEf – амплитуда переменного напряжения; Δt – продолжительность импульса, связанная со скоростью развертки переменного напряжения Vр соотношением: ∆t = |Eнач − Eкон|/Vp, (1), где Eнач и Eкон – потенциалы начала и конца развертки переменного тока соответственно.

Импульс на систему накладывается многократно, потенциал каждый раз возвращается к своему первоначальному значению. Такой способ измерений включает достоинства переменнотоковых (чувствительность) и импульсных методов (возврат к начальному значению напряжений после цикла измерений) и меньше подвержен влиянию адсорбции аналитов или продуктов электрохимической реакции.
На примере хинона проведены сравнительные измерения с использованием постояннотокового, нормального импульсного и импульсного переменнотокового режимов. Чувствительность импульсного переменного режима в 40 раз выше постояннотокого режима и в 6 раз выше нормального импульсного [58, 59]. Кроме того, описанный вариант амперометрических измерений обладает селективностью переменнотоковых методов.
Коммутационная амперометрия, ее прямой и косвенный варианты, применение в сенсорах. Третий способ – использование коммутационного режима [60]. Повышение чувствительности связанно с таким способом формирования сигнала, при котором ток заряжения, так же как и фарадеевский, зависит от концентрации аналита. Сущность этого метода заключается в том, что в электрическую схему включают коммутатор, который периодически замыкает контур тока на небольшие промежутки времени (порядка 100 мкс) и размыкает контур тока на относительно большие (порядка 100 мс). Благодаря этому возникающий ток в основном содержит емкостную составляющую, существенно превосходящую ток электрохимической реакции, но прямо пропорционально зависящую от концентрации аналита [61]:
(2)
${{I}_{{{\text{к о м }}}}} = \frac{{{{T}_{{\text{к }}}}}}{{{{t}_{{\text{з }}}}}}\left( {{{I}_{{{\text{Э Р }}}}} + {{I}_{i}}} \right),$Отношение периода коммутации ко времени замыкания выполняет функцию коэффициента усиления. Чем больше соотношение времен замыкания и размыкания, тем больше коэффициент усиления тока электрохимической реакции. Следовательно, регулируя отношение времен замыкания и размыкания, можно управлять чувствительностью электрохимических измерений. Форму фактора возбуждения в методе коммутационной амперометрии иллюстрирует рис. 5.
Аналитические возможности метода исследованы на примере определения ионов Cd(II), Pb(II), Fe(III) [62], а также фенола и гидрохинона [63] в водных модельных растворах. Полученные аналитические характеристики коммутационной амперометрии представлены в табл. 1.
Таблица 1.
Аналитические характеристики коммутационной амперометрии на примере определения некоторых аналитов
| Аналит | Электрод | Предел обнаружения, нМ | Линейный диапазон, нМ | Чувствительность, нА/мкМ |
|---|---|---|---|---|
| Кадмий(II) | ВРК | 0.26 | 1–200 | 1.0 × 103 |
| Свинец(II) | 0.79 | 5–200 | 2.0 × 103 | |
| Железо(III) | ГЭ | 3.00 | 20–380 | 1.2 × 103 |
| ЗЭ | 200.00 | 2 × 103–18 × 103 | 0.81 | |
| Фенол | КЭ | 8.80 | 500–3 × 103 | 76 |
| Гидрохинон | 31.00 | 100–5 × 103 | 75 |
Данным способом определено содержание ионов железа(III) в воде в ходе первого мониторинга финско-эстонско-российской части Финского залива. Содержание ионов железа(III) также определяли референтным методом атомно-абсорбционной спектроскопии с электротермической атомизацией (ЭТААС). Результаты, полученные обоими методами, хорошо согласуются между собой [62].
Исследованы аналитические возможности косвенной коммутационной амперометрии, коммутационного амперометрического титрования. Аналитические характеристики коммутационного амперометрического титрования изучены на классической системе: соль Мора–дихромат калия. Исследования показали, что с помощью коммутационного амперометрического титрования можно понизить пределы обнаружения на порядок, до 10–7 М. Классическое амперометрическое титрование позволяет определять концентрации порядка 10–5 М, в редких случаях даже 10–6 М [64].
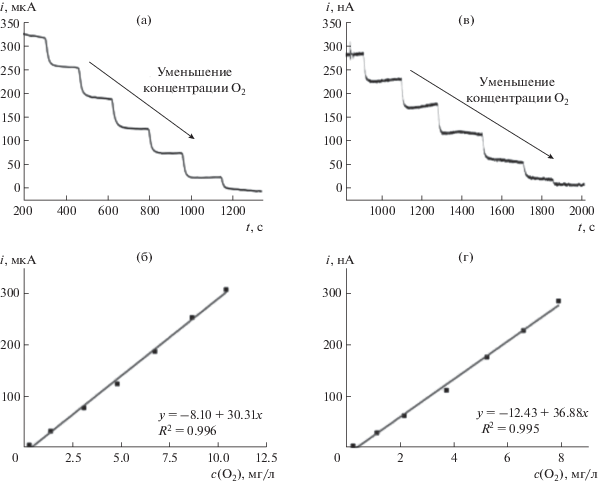
Коммутационную амперометрию также применяли в качестве способа детектирования растворенного в воде кислорода с помощью электрохимического сенсора [65]. На рис. 6 представлены зависимости, полученные в коммутационном и постояннотоковом режимах с помощью сенсора Кларка. Обнаружено, что использование коммутационного режима для определения кислорода обеспечивает значительное повышение чувствительности: предлагаемый метод примерно в тысячу раз чувствительнее, чем традиционный.
Рис. 6.
Сравнение коммутационного и постояннотокового режимов измерения тока при определении растворенного в воде кислорода сенсором Кларка: (а) – амперограмма, полученная в коммутационном режиме; (б) – градуировочный график для коммутационного режима; (в) – амперограмма, полученная в постояннотоковом режиме; (г) – радуировочный график в постояннотоковом режиме.
НОВЫЕ ПОДХОДЫ К КУЛОНОМЕТРИЧЕСКИМ ИЗМЕРЕНИЯМ
Инверсионная кулонометрия. В кулонометрическом методе анализа аналитическим сигналом является количество электричества, необходимое для количественного протекания электродного процесса с участием аналита [66]. Несомненными достоинствами метода являются отсутствие необходимости концентрационной градуировки и высокая точность, а существенными недостатками – длительность анализа и низкая чувствительность. Попытки преодолеть указанные недостатки привели к появлению нового варианта метода – инверсионной кулонометрии (ИКМ) [67], которая сочетает принципы кулонометрии при контролируемом потенциале (КПП) и инверсионной вольтамперометрии (ИВА). Схема анализа методом ИКМ включает те же этапы, что и в случае ИВА. Ключевыми стадиями измерений являются предэлектролиз, т.е. электролитическое концентрирование аналита на электроде, и последующее растворение накопленного вещества при развертке потенциала. Аналитическим сигналом в ИКМ, как и в методе КПП, служит количество электричества (Q∞), необходимое для полного выделения определяемого вещества из раствора. Предложено два подхода к нахождению значения Q∞: расчет по формуле Мейтса и использование кулонометрической константы. В любом случае после определения значения Q∞ количество аналита рассчитывают по закону Фарадея.
Мейтс [68] показал, что для нахождения полного количества электричества Q∞, необходимого для электрохимического выделения веществ, не обязательно их полностью выделять из раствора. Достаточно найти количество электричества, необходимое для выделения вещества за определенные промежутки времени:
(3)
${{Q}_{\infty }} = \frac{{Q_{2}^{2} - {{Q}_{1}}{{Q}_{3}}}}{{2{{Q}_{2}} - ({{Q}_{1}} + {{Q}_{3}})}},$Рис. 7.
Схема изменения потенциала электрода во времени в инверсионной кулонометрии с расчетом количества электричества по Мейтсу.

Работоспособность предложенного метода ИКМ проверяли на примере определения экологически значимых элементов, традиционно определяемых методом ИВА, − Hg [69, 70], Pb [70–72], Cu [70, 72], Cd [70, 72], а также Zn [73].
Вариант ИКМ с расчетом полного количества электричества по Мейтсу требует проведения трех последовательных измерений, что существенно увеличивает продолжительность анализа. Преодолеть эти ограничения позволяет другой вариант метода ИКМ – с интегрированием количества электричества по величине кулонометрической константы. Значение Q∞ в этом случае рассчитывают по следующей формуле:
где Qt – это количество электричества, затраченное на превращение данного вещества за время предэлектролиза t, а k – это кулонометрическая константа, зависящая от коэффициента диффузии определяемого иона (D), толщины диффузионного слоя (δ), объема раствора в измерительной ячейке (V) и площади рабочего электрода (S):Использование уравнения (4) для нахождения Q∞ позволяет упростить схему проведения измерений, поскольку в этом случае достаточно однократного определения количества электричества Qt, соответствующего времени накопления t, но для ее практического применения необходимо предварительное экспериментальное определение кулонометрической константы k. Схема измерений и нахождения Qt в данном варианте метода приведены на рис. 8.
Рис. 8.
Схема измерений и нахождения количества электричества при расчете Q∞ по величине кулонометрической константы.

Описанный экспрессный вариант ИКМ использован для количественного определения в водных растворах Hg [74, 75], As [76], Pb [77] и Cd [75].
Во всех перечисленных выше работах рабочим электродом являлся классический вращающийся дисковый электрод. При этом минимальный объем раствора в электрохимической ячейке составлял 1 мл. В целях миниатюризации и повышения экспрессности ИКМ-анализа предложено использовать печатные электроды (ПЭ) – планарные устройства, изготовленные методом трафаретной печати. Такие электроды позволяют работать с малыми объемами раствора при значительной площади рабочего электрода, что приводит к увеличению скорости изменения концентрации аналита при проведении электролиза в ячейках с ПЭ (см. уравнение (5)) и, соответственно, к сокращению продолжительности анализа. Кроме того, уменьшение объемов используемых реактивов и миниатюрность электрохимических ячеек в случае использования ПЭ делают метод ИКМ особенно привлекательным для автоматического и полевого анализа, а также снижают нагрузку на окружающую среду при массовых анализах.
Методом ИКМ в электрохимических ячейках на основе ПЭ успешно определены Hg, Pb, Cd и Cu [57, 78]. При этом достигнуты пределы обнаружения указанных металлов на уровне нМ при времени накопления 70 с и объеме раствора в ячейке 100 мкл. Следует отметить, что в любом из вариантов ИКМ, так же, как и в ИВА, чувствительность анализа возрастает при увеличении времени накопления аналита. Оптимальным временем накопления можно считать время, близкое ко времени полупревращения, так как в этом случае относительная погрешность измерения минимальна.
Кулонометрический сенсор для определения кислорода. Подавляющее число использующихся в настоящее время анализаторов растворенного кислорода основано на амперометрическом принципе детектирования. В таких анализаторах в качестве чувствительного элемента используют сенсор Кларка, в котором измерительная электродная система отделена от анализируемой среды кислород-проницаемой мембраной. Несмотря на широкое использование амперометрических анализаторов растворенного кислорода и продолжение работ по их техническому совершенствованию, не прекращается поиск альтернативных методов определения растворенного в воде кислорода. Одним из них является прямая потенциостатическая кулонометрия, применение которой в кислородном сенсоре описано в работах [79–81]. Преимуществом таких сенсоров являются отсутствие необходимости концентрационной градуировки и способность работать длительное время в автоматическом режиме.
Список литературы
Rajaji U., Arumugam R., Chen S.-M., Chen T.-W., Tseng T.-W., Chinnapaiyan S., Lee S.-Y., Chang W.-H. Graphene nanoribbons in electrochemical sensors and biosensors: A review // Int. J. Electrochem. Sci. 2018. V. 13. № 7. P. 6643.
El Rhazi M., Majid S., Elbasri M., Salih F.E., Oularbi L., Lafdi K. Recent progress in nanocomposites based on conducting polymer: Application as electrochemical sensors // Int. Nano Lett. 2018. V. 8. № 2. P. 79.
George J.M., Antony A., Mathew B. Metal oxide nanoparticles in electrochemical sensing and biosensing: A review // Microchim. Acta. 2018. V. 185. № 7. P. 358.
Baig N., Saleh T.A. Electrodes modified with 3D graphene composites: A review on methods for preparation, properties and sensing applications // Microchim. Acta. 2018. V. 185. № 6. P. 283.
Andre R.S., Sanfelice R.C., Pavinatto A., Mattoso L.H.C., Correa D.S. Hybrid nanomaterials designed for volatile organic compounds sensors: A review // Mater. Des. 2018. V. 156. P. 154.
Nicolau Y.F. Method and filing device on a substrate with a thin layer of a compound having at least one cationic component and at least one anionic component. Patent. FR2569427B1. Application FR2569427A1 dated 28.02.1986. Published on 14.11.1986.
Толстой В.П., Богданова Л.П., Митюкова Г.В. Способ синтеза двуокиси маргнца. Патент SU 1386600 A1. Заявка 4010248/31-33 от 07.01.1986. Опубл. 07.04.1988.
Ermakov S.S., Nikolaev K.G., Tolstoy V.P. Novel electrochemical sensors with electrodes based on multilayers fabricated by layer-by-layer synthesis and their analytical potential // Russ. Chem. Rev. 2016. V. 85. № 8. P. 880.
Gulina L.B., Pchelkina A.A., Nikolaev K.G., Navolotskaya D. V., Ermakov S.S., Tolstoy V.P. A brief review on immobilization of gold nanoparticles on inorganic surfaces and successive ionic layer deposition // Rev. Adv. Mater. Sci. 2016. V. 44. № 1. P. 46.
Кукло Л.И., Белянинова С.И., Ермаков С.С., Толстой В.П. Нанослои Fe0.5MnOx · nH2O, синтезируемые методом ионоого наслаивания и их применение при вольтамперометрическом безэнзимном определении перексиси водорода // Российские нанотехнологии. 2016. Т. 11. № 3–4. С. 21. (Kuklo L.I., Belyaninova S.I., Ermakov S.S., Tolstoy V.P. Fe0.5MnOx · ⋅ nH2O nanolayers synthesized via successive ionic layer deposition and their use in voltammetric nonenzymatic determination of hydrogen peroxide // Russ. Nanotechnol. 2016. V. 11. № 3–4. P. 137.)
Kochemirovsky V.A., Skripkin M.Y., Tveryanovich Y.S., Mereshchenko A.S., Gorbunov A.O., Panov M.S., Tumkin I.I., Safonov S.V. Laser-induced copper deposition from aqueous and aqueous‒organic solutions: state of the art and prospects of research // Russ. Chem. Rev. 2015. V. 84. № 10. P. 1059.
Panov M.S., Tumkin I.I., Mironov V.S., Khairullina E.M., Smikhovskaia A. V., Ermakov S.S., Kochemirovsky V.A. Sensory properties of copper microstructures deposited from water-based solution upon laser irradiation at 532 nm // Opt. Quantum Electron. 2016. V. 48. № 11. P. 1.
Khairullina E.M., Smikhovskaia A.V., Safonov S.V., Panov M.S., Logunov L.S., Ermakov S.S., Kochemirovsky V.A. / 17th Int. Conf. “Laser Optics 2016". Saint-Peterburg. 27 June−01 July 2016. P. S243.
Tumkin I.I., Panov M.S., Khairullina E., Gordeychuk D., Ermakov S.S., Kochemirovsky V.A. / SPIE/COS Photonics Asia. Beijing, 2016. V. 10018. Advanced Laser Processing and Manufacturing. P. 100180E-1.
Panov M.S., Vereshchagina O.A., Ermakov S.S., Tumkin I.I., Khairullina E.M., Skripkin M.Y., Mereshchenko A.S., Ryazantsev M.N., Kochemirovsky V.A. Non-enzymatic sensors based on in situ laser-induced synthesis of copper-gold and gold nano-sized microstructures // Talanta. 2017. V. 167. № 15. 2017. P. 201.
Smikhovskaia A.V., Panov M.S., Tumkin I.I., Khairullina E.M., Ermakov S.S., Balova I.A., Ryazantsev M.N., Kochemirovsky V.A. In situ laser-induced codeposition of copper and different metals for fabrication of microcomposite sensor-active materials // Anal. Chim. Acta. 2018. V. 1044. P. 138.
Talukdar I., Ozturk B., Flanders B.N., Mishima T.D. Directed growth of single-crystal indium wires // Appl. Phys. Lett. 2006. V. 88. № 22. P. 86.
Николаев К.Г., Ермаков С.С., Offenhäusser A., Mourzina Y.G. Бесферментное определение глюкозы на электродах, полученных методом прямого электрохимического синтеза // Журн. аналит. химии. 2017. Т. 72. № 4. С. 314. (Nikolaev K.G., Ermakov S.S., Offenhäusser A., Mourzina Y.G. Nonenzymatic determination of glucose on electrodes prepared by directed electrochemical nanowire assembly (DENA) // J. Anal-yt. Chem. 2017. V. 72. № 4. P. 371.)
Nikolaev K.G., Maybeck V., Neumann E., Ermakov S.S., Ermolenko Y.E., Offenhäusser A., Mourzina Y.G. Bimetallic nanowire sensors for extracellular electrochemical hydrogen peroxide detection in HL-1 cell culture // J. Solid State Electrochem. 2018. V. 22. № 4. P. 1023.
Nikolaev K.G., Ermolenko Y.E., Offenhäusser A., Ermakov S.S., Mourzina Y.G. Multisensor systems by electrochemical nanowire assembly for the analysis of aqueous solutions // Front. Chem. 2018. V. 6. P. 256.
Shishov A., Penkova A., Zabrodin A., Nikolaev K., Dmitrenko M., Ermakov S., Bulatov A. Vapor permeation-stepwise injection simultaneous determination of methanol and ethanol in biodiesel with voltammetric detection // Talanta. 2016. V. 148. 2016. P. 666.
Ермаков С.С., Боржицкая А.В., Москвин Л.Н. Влияние процесса электрохимического полирования поверхности золотого электрода на чувствительость инверсионно-вольтамперометрического определения ртути(II) // Журн. аналит. химии. 2001. Т. 56. № 6. С. 610. (Ermakov S.S., Borzhitskaya A.V., Moskvin L.N. Electrochemical polishing of the surface of a gold electrode and its effect on the sensitivity of the stripping voltammetric determination of mercury(II) // J. Analyt. Chem. 2001. V. 56. № 6. P. 542.)
Nechaeva D., Shishov A., Ermakov S., Bulatov A. A paper-based analytical device for the determination of hydrogen sulfide in fuel oils based on headspace liquid-phase microextraction and cyclic voltammetry // Talanta. 2018. V. 183. 1 June 2018. P. 290.
Номенклатурные правила ИЮПАК по химии. Т. 4. Аналитическая химия / Под ред. Золотова Ю.А., Неймана Е.Я. М.: Производственно-издательский комбинат ВИНИТИ, 1985. 180 с.
Perone S.P., Birk J.R. Application of derivative techniques to anodic stripping voltammetry // Anal. Chem. 1965. V. 37. № 1. P. 9.
Jones H.C., Belew W.L., Stelzner R.W., Mueller T.R., Fisher D.J. A solid-state controlled-potential DC polarograph with cyclic scanning and calibrated first- and second-derivative scales // Anal. Chem. 1969. V. 41. № 6. P. 772.
Kim M.-H. First- and second-order derivative polarography/voltammetry for reversible, quasi-reversible, and irreversible electrode processes // J. Electrochem. Soc. 1993. V. 140. № 3. P. 712.
He Q., Liu J., Liu X., Xia Y., Li G., Deng P., Chen D. Novel electrochemical sensors based on cuprous oxide-electrochemically reduced graphene oxide nanocomposites modified electrode toward sensitive detection of sunset yellow // Molecules. 2018. V. 23. № 9. P. 2130.
Smith D.E. The enhancement of electroanalytical data by on-line fast fourier transform – data processing in electrochemistry // Anal. Chem. 1976. V. 48. № 6. P. 517A.
Surprenant H.L., Ridgway T.H., Reilley C.N. Convolution and deconvolution in the synthesis and analysis of staircase voltammograms // J. Electroanal. Chem. 1977. V. 75. № 1. P. 125.
Economou A., Fielden P.R., Packham A.J. Wiener filtering of electroanalytical data by means of fast Fourier transform // Anal. Chim. Acta. 1996. V. 319. № 1–2. P. 3.
Kumari P., Adeloju S.B. Fabrication of a novel DNA affinity biosensor based on hybridisation induced current by electrostatic repulsion of silicotungstic acid as a redox indicator // Talanta. 2019. V. 194. P. 127.
Zheng X.P., Mo J.Y., Cai P.X. Simultaneous application of spline wavelet and Riemann-Liouville transform filtration in electroanalytical chemistry // Anal. Commun. 1998. V. 35. № 2. P. 57.
Shao X. Development of wavelet transform voltammetric analyzer // Talanta. 2000. V. 50. № 6. P. 1175.
Jakubowska M. Dedicated wavelet for voltammetric signals analysis // J. Electroanal. Chem. 2007. V. 603. № 1. P. 113.
Kumar M., Kumar S., Gupta A., Ghosh A. / 2018 IEEE SENSORS. New Delhi. 28−31 Oct. 2018. P. 1.
Barker G.C., Gardner A.W. Pulse polarography // Fresenius Z. Anal. Chem. 1960. V. 173. № 1. P. 79.
Osteryoung J.G., Schreiner M.M. Recent advances in pulse voltammetry // Crit. Rev. Anal. Chem. 1988. V. 19. № sup1. P. S1.
Laborda E., González J., Molina Á. Recent advances on the theory of pulse techniques: A mini review // Electrochem. Commun. 2014. V. 43. P. 25.
Rifkin S.C., Evans D.H. Analytical evaluation of differential pulse voltammetry at stationary electrodes using computer-based instrumentation // Anal. Chem. 1976. V. 48. № 14. P. 2174.
Yeakel B.D., Burrows K.C., Hughes M.C. A Digital signal generator for rapid scan differential pulse voltammetry using commercially available instrumentation // Instrum. Sci. Technol. 2008. V. 9. № 3. P. 239.
Zachowski E.J., Wojciechowski M., Osteryoung J. The analytical application of square-wave voltammetry // Anal. Chim. Acta. 1986. V. 183. P. 47.
Barker G.C., Gardner A.W. Forty years of square-wave polarography // The Analyst. 1992. V. 117. № 12. P. 1811.
Mirceski V., Komorsky-Lovric S., Lovric M. Square-Wave Voltammetry. Berlin, Heidelberg: Springer Berlin Heidelberg, 2007. 201 p.
Bauer H.H. Alternating current polarography and tensammetry // J. Electroanal. Chem. (1959–1966). 1960. V. 1. № 5. P. 363.
Smith D.E., Bauer H.H. Recent developments in alternating current polarography // Crit. Rev. Anal. Chem. 1971. V. 2. № 2. P. 247.
Bond A.M., Heritage I.D. A systematic approach to faradaic current, charging current and phase angle measurement by digital alternating current polarography // J. Electroanal. Chem. Interfacial Electrochem. 1987. V. 222. № 1–2. P. 35.
Senaratne C., Hanck K.W. A novel instrumental approach to digital Ac voltammetry // Instrum. Sci. Technol. 2008. V. 20. № 1. P. 1.
Железцов А.В. Переменнотоковая полярография с применением амплитудно-модулированного синусоидального напряжения. Сообщение 1. Теория // Журн. аналит. химии. 1971. Т. 26. № 4. С. 644. (Zheleztsov A.V. Alternating current polarography with the use of the amplitude-modulated sinusoidal voltage. Commumication 1. The theory // Zh. Anal. Khim. 1971. V. 26. № 4. P. 644.)
Железцов А.В. Переменнотоковая полярография с применением амплитудно-модулированного синусоидального напряжения. Сообщение 2. Аппаратура // Журн. аналит. химии. 1971. Т. 26. № 4. С. 650. (Zheleztsov A.V. Alternating current polarography with the use of the amplitude-modulated sinusoidal voltage. Commumication 2. The apparatus // Zh. Anal. Khim. 1971. V. 26. № 4. P. 650.)
Железцов А.В. Переменнотоковая полярография с применением амплитудно-модулированного синусоидального напряжения. Сообщение 3. Емкостной ток // Журн. аналит. химии. 1972. Т. 27. № 8. С. 1461. (Zheleztsov A.V. Alternating current polarography with the use of the amplitude-modulated sinusoidal voltage. Commumication 3. Capacity current // Zh. Anal. Khim. 1972. V. 27. № 8. P. 1461.)
Железцов А.В. Переменнотоковая полярография с применением амплитудно-модулированного синусоидального напряжения. Сообщение 4. Линейная диффузия на капающий ртутный электрод // Журн. аналит. химии. 1973. Т. 28. № 5. С. 867. (Zheleztsov A.V., Rafikov R.K. Alternating current polarography with the use of the amplitude-modulated sinusoidal voltage. Commumication 4. Linear diffusion on a dropping mercury electrode // Zh. Anal. Khim. 1973. V. 28. № 5. P. 867.)
Brazill S.A., Bender S.E., Hebert N.E., Cullison J.K., Kristensen E.W., Kuhr W.G. Sinusoidal voltammetry: A frequency based electrochemical detection technique // J. Electroanal. Chem. 2002. V. 531. № 2. P. 119.
Vydra F., Štulík K., Juláková E. Electrochemical Stripping Analysis. Chichester: Ellis Horwood, 1976. 283 p.
Wang J. Stripping Analysis: Principles, Instrumentation, and Applications. Deerfield Beach: VCH Publi-shers, 1985. 160 p.
Brainina K., Neyman E. Electroanalytical Stripping Methods. Chemical Analysis: A Series of Monographs on Analytical Chemistry and Its Applications. 1st ed. Wiley-Interscience, 1993. 198 p.
Timofeeva D.V., Tsapko Y.V., Ermakov S.S. Stripping coulometry determination of lead and mercury at screen-printed electrodes // J. Electroanal. Chem. 2011. V. 660. № 1. P. 195.
Ермаков С.С., Яснев М.И., Аверяскина Е.О. Экспрессный способ импульсной перменно-токовой вольтамперметрии. Патент RU 2465577 C1. Заявка 2011127869/28 от 06.07.2011. Опубл. 20.10.2012.
Яснев И.М., Мустя О.В., Аверяскина Е.О., Ермаков С.С. Импульсный переменнотоковый способ амперометрических измерений. Определение пара-бензохинона и фенола // Научное приборостроение. 2012. Т. 22. № 1. С. 74.
Мошкин В.В., Хустенко Л.А. Способ коммутационной амперометрии. Патент RU 2382356 C1. Заявка 2008145948/28 от 20.11.2008. Опубл. 20.02.2010.
Belebentseva M., Navolotskaya D., Ermakov S., Moshkin V., Khustenko L. Interrupted amperometry: An ultrasensitive technique for diffusion current measuring // Electrochim. Acta. 2016. V. 191. P. 510.
Semenova E., Navolotskaya D., Ermakov S. Interrupted amperometry: The new possibilities in electrochemical measurements // Pure Appl. Chem. 2017. V. 89. № 10. P. 1459.
Семенова Е.А., Наволоцкая Д.В., Ермаков С.С., Мошкин Д.В., Хустенко Л.А. Коммутационная амперометрия на твердых электродах: Определение фенола и гидрохинона // Журн. аналит. химии. 2016. Т. 71. № 12. С. 1308. (Semenova E.A., Navolotskaya D.V., Ermakov S.S., Moshkin V.V, Khustenko L.A. Interrupted amperometry on solid electrodes: determination of yydroquinone and phenol // J. Analyt. Chem. 2017. V. 72. № 1. P. 113.)
Сонгина О.А. Амперометрическое титрование. М.: Химия, 1967. 388 с.
Гурская А.В. Новые подходы к электрохимическому определению кислорода в водных средах. Дис. … канд. хим. наук. Санкт-Петербург: Санкт-Петербургский государственный университет, 2016. 111 с.
Аналитическая химия. В 3-х т. Т. 1. Методы идентификации и определения веществ / Под ред. Москвина Л.Н. М.: Издательский центр “Академия”, 2008. 576 с.
Ермаков С.С. Способ электрохимического анализа. Патент RU 2337352 C2. Заявка 2006140707/28 от 13.11.2006. Опубл. 27.10.2008.
Meites L. End point location in controlled-potential coulometric analysis // Anal. Chem. 1959. V. 31. № 7. P. 1285.
Аверяскина Е.О., Ермаков С.С. Комбинированный безэталонный электрохимический метод определения ртути в водных растворах // Научное приборостроение. 2006. Т. 16. № 4. С. 73.
Sheremet A., Averyaskina E., Chekmeneva E., Ermakov S. Standardless electrochemical method for mercury, cadmium, lead and copper determination in aqueous solution // Electroanalysis. 2007. V. 19. № 21. P. 2222.
Ермаков С.С., Чекменева Е.Н., Москвин Л.Н. Комбинированный безэталонный электрохимический метод определения свинца в водных растворах // Журн. аналит. химии. 2007. Т. 62. № 1. С. 89. (Ermakov S.S., Chekmeneva E.N., Moskvin L.N. A combined standardless electrochemical method for determining lead in aqueous solutions // J. Analyt. Chem. 2007. V. 62. № 1. P. 89.)
Шеремет А.А., Ермаков С.С. Комбинированный безэталонный электрохимический метод определения свинца, меди и кадмия в водных растворах // Журн. прикл. химии. 2006. Т. 78. № 12. С. 1970. (Sheremet A.A., Ermakov S.S. Combined standardless electrochemical method for determination of lead(II), copper(II), and cadmium(II) in aqueous solutions // Russ. J. Appl. Chem. 2006. V. 79. № 12. P. 1947.)
Ермаков С.С., Шеремет А.А., Москвин Л.Н. Определение цинка в водных растворах комбинированным безэталонным электрохимическим методом с предварительным электролитическим отделением меди // Журн. прикл. химии. 2008. Т. 81. № 3. С. 434. (Ermakov S.S., Sheremet A.A., Moskvin L.N. Determination of zinc in aqueous solutions by a combined no-standard electrochemical method with preliminary electrolytic separation of copper // Russ. J. Appl. Chem. 2008. V. 81. № 3. P. 420.)
Цапко Ю.В., Ермаков С.С., Москвин Л.Н. Экспрессный вариант безэталонного инверсионно-вольтамперометрического определения ртути в водных растворах // Журн. аналит. химии. 2008. Т. 63. № 10. С. 1067. (Tsapko Y.V., Ermakov S.S., Moskvin L.N. A rapid version of standartless stripping voltammetry for detemination mercury in aqueous solutions // J. Analyt. Chem. 2008. V. 63. № 10. P. 971.)
Цапко Ю.В., Шеремет А.А., Ермаков С.С. Вольтамперометрия переменного тока как способ повышения чувствительности определения ионов тяжелых металлов методом инверсионной вольтамперометрии, не требующей концентрационной градуировки // Научное приборостроение. 2009. V. 19. № 2. P. 66.
Цапко Ю.В., Тумкин И.И., Ермаков С.С. Бесконтактное инверсионно-вольтамперометрическое определение мышьяка в водных растворов // Журн. прикл. химии. 2009. Т. 82. № 2. С. 268. (Tsapko Y.V., Tumkin I.I., Ermakov S.S. Determination of arsenic in aqueous solutions by no-reference inversion voltammetry // Russ. J. Appl. Chem. 2009. V. 82. № 2. P. 262.)
Чежина Н.М., Ермаков С.С. Экспреснный вариант бесконтактного инверсионно-вольтамперометрического определения свинца в водных растворах // Журн. прикл. химии. 2009. Т. 82. № 2. С. 273. (Chezhina N.M., Ermakov S.S. Fast procedure for no-reference inversion-voltammetric determination of lead in aqueous solutions // Russ. J. Appl. Chem. 2009. V. 82. № 2. P. 267.)
Наволоцкая Д.В., Ермаков С.С., Егорова Е.А., Николаев К.Г. Инверсионно-кулонометрическое определение кадмия, свинца и меди на модифицированных печатных электродах // Вестник СПбГУ. Серия 4. 2013. № 2. С. 136.
Гурская А.В., Ермаков С.С. Кулонометрический сенсор для определения кислорода // Научное приборостроение. 2012. Т. 22. № 4. С. 111.
Гурская А.В., Аверяскина Е.О., Ермаков С.С. Использование кулонометрического сенсора для автоматизации измерений концентрации кислорода в технологических водах тепловых станций // Журн. прикл. химии. 2014. Т. 87. № 11. С. 1615. (Gurskaya A.V, Averyaskina E.O., Ermakov S.S. Use of a coulometric sensor for automation of the oxygen concentration measurements in process waters of thermal power plants // Russ. J. Appl. Chem. 2014. V. 87. № 11. P. 1654.)
Гурская А.В., Ермаков С.С. Электрохимический сенсор для растворенного кислорода с проточным рабочим электродом // Журн. прикл. химии. 2015. Т. 88. № 5. С. 739. (Gurskaya A. V, Ermakov S.S. Electrochemical sensor for dissolved oxygen with a flow-through working electrode // Russ. J. Appl. Chem. 2015. V. 88. № 5. P. 782.)
Дополнительные материалы отсутствуют.
Инструменты
Журнал аналитической химии



