Журнал аналитической химии, 2019, T. 74, № 2, стр. 91-96
ОРГАНИЧЕСКИЕ РЕАГЕНТЫ И ДВУХСЛОЙНЫЕ НОСИТЕЛИ В ПОСЛЕДОВАТЕЛЬНОМ СОРБЦИОННО-СПЕКТРОСКОПИЧЕСКОМ ОПРЕДЕЛЕНИИ Ti(IV), V(V), Мo(VI) И Ni(II) ИЗ ОДНОЙ ПРОБЫ
В. П. Дедкова 1, *, О. П. Швоева 1, А. А. Гречников 1
1 Институт геохимии и аналитической химии им. В.И. Вернадского Российской академии наук
119991 Москва, ул. Косыгина, 19, Россия
* E-mail: DedVa@yandex.ru
Поступила в редакцию 08.11.2017
После доработки 18.04.2018
Принята к публикации 18.04.2018
Аннотация
Методом спектроскопии диффузного отражения изучены условия одновременного концентрирования Ti(IV), V(V), Mo(VI) и Ni(II) на двухслойном носителе и их последовательного определения с использованием органических реагентов. В качестве носителей использованы диски полиакрилонитрильного волокна, наполненного анионообменником (ПАНВ–АВ-17) или катионообменником (ПАНВ–КУ-2). Определение титана и никеля на дисках ПАНВ–КУ-2 основано на последовательном взаимодействии никеля с диметилглиоксимом (ДМГ) и титана с 2,7-дихлорхромотроповой кислотой (ДХХК). Определение ванадия и молибдена на дисках ПАНВ–АВ-17 основано на взаимодействии ванадия с 8-гидроксихинолин-5-сульфокислотой (ГОС) и 0.1 М HCl и молибдена с фенилфлуороном (ФФ). Изучены зависимости аналитических сигналов комплексов Ti–ДХХК и Ni–ДМГ на ПАНВ–КУ-2 и комплексов V–ГОС и Mo–ФФ на ПАНВ–АВ-17 от рН растворов при сорбции в динамическом режиме. Оптимальное значение рН растворов для одновременной сорбции четырех элементов равно 3.5 ± 0.1. Изучено влияние сопутствующих элементов в смеси на определение Ti, V, Mo и Ni. Приведены характеристики методик сорбционно-спектроскопического определения элементов: последовательность обработки дисков носителей растворами реагентов, условия устранения сигнала предыдущего элемента, коэффициенты градуировочных уравнений и диапазоны линейности градуировочных графиков, пределы обнаружения элементов. Определены факторы селективности и разработана методика сорбционно-спектроскопического определения Ti, V, Mo и Ni при совместном присутствии. Приведены результаты анализа модельных растворов при различном соотношении элементов; sr < 0.15.
Методы определения ионов элементов на твердом носителе в последние годы получили преимущество перед обычными фотометрическими методами так как они, как правило, более чувствительны и избирательны. Реакции на твердой фазе используют для сорбционно-спектроскопических и тест-определений элементов [1–3]. Железо(III) и молибден(VI) связывают в окрашенный комплекс с пирокатехином при рН 6.2, комплексы сорбируют на сильноосновном анионите и измеряют оптическую плотность комплексов в фазе сорбента при 520 и 400 нм соответственно [4]. Триоксифлуороны, иммобилизованные на целлюлозных матрицах, используют для тест-определения редких элементов. Фенилфлуорон на целлюлозных бумагах позволяет определять Ti, Ge, Zr, Mo, V, Nb [5]. Обычно при одновременной сорбции из раствора нескольких элементов используют их десорбцию и последующее определение методами атомно-абсорбционной спектрометрии (ААС), масс-спектрометрии с индуктивно связанной плазмой и др. Так, кремнезем, модифицированный тайроном, применен [6] для извлечения Fe, Cu, Al при рН 4 и Pb, Zn, Mn, Fe, Al, Cu при рН 7 из природных вод с последующим определением методом атомно-эмиссионной спектрометрии с индуктивно связанной плазмой. Для определения следовых количеств Co, Ni и Cu использована [7] их сорбция без хелатного агента с помощью магнитных наночастиц Fe3O4 при рН 10–12, которые затем отделяют с помощью внешнего магнитного поля; Co, Ni и Cu затем десорбируют 1 М HNO3 и определяют пламенной ААС с пределами обнаружения 0.9, 0.7 и 0.3 нг/мл соответственно.
Среди множества носителей, предложенных в качестве твердой фазы, используются и волокнистые полиакрилонитрильные материалы, наполненные ионообменниками. Тонкое волокнистое полотно, наполненное ионообменником, сочетает все положительные свойства ионообменников с удобной формой, позволяющей применять их для разделения и концентрирования элементов как в динамических, так и в статических условиях сорбции.
Волокнистые ионообменники являются весьма удобным, механически и химически стойким материалом для применения в качестве твердой фазы в сорбционно-спектроскопических и тест-методах определения. Наполненные волокнистые материалы получают промышленным способом: в процессе формования в полиакрилонитрильное волокно вводят необходимый тонкодисперсный ионообменник. Получают слабоокрашенное тонкое полиакрилонитрильное нетканое полотно, наполненное ионообменником (НИИСВ, Тверь). Степень наполнения можно варьировать в пределах 50–80 мас. %, диаметр нити волокна 30–40 мкм, диаметр частиц ионообменника 5–10 мкм. Материалы устойчивы в диапазоне от сильнокислых до слабощелочных сред, имеют хорошие кинетические и ионообменные характеристики, удобны в работе. Они легко переносятся пинцетом, не деформируются при перемешивании, нагревании в растворе, высушивании и других операциях. Волокнистые материалы, наполненные различными ионообменниками можно накладывать друг на друга в проточной ячейке или перемешивать в анализируемом растворе, выполняя одновременную сорбцию различных элементов. Таким образом удается существенно повысить экспрессность определения. С другой стороны, на одном диске носителя можно сконцентрировать 2–3 элемента с последующим последовательным определением каждого из них реакцией на твердой фазе с подходящим органическим реагентом. Выполнение сорбции двух и более элементов из одной пробы существенно снижает продолжительность анализа и расход аналита. Ранее нами предложены методики определения из одной пробы V(V) и Mo(VI) [8], V(V) и Cr(VI) [9], сорбционно-спектроскопическое и тест-определение Cr(VI), Cu(II) и Ni(II) [10, 11], Hg(II), Cd(II) и Pb(II) [12], Cr(VI), V(V), Ni(II) и Cu(II) [13].
Настоящая работа посвящена изучению возможности раздельного определения Ti((IV), V(V), Mo(VI) и Ni(II) после их одновременной сорбции из одного раствора. Использована возможность существования этих ионов в различных ионных формах: титана и никеля в катионной форме, а ванадия и молибдена в анионной. В водных растворах четырехзарядные катионы, в том числе титан, существуют в виде М4+ или МО2+. Из-за большой склонности к гидролизу и полимеризации все операции с ними проводят в кислых средах. Из разбавленных растворов соляной кислоты ионы титана не поглощаются сильноосновными анионообменниками. Никель не сорбируется на анионообменнике во всем интервале концентраций соляной кислоты. Элементы пятой группы Периодической системы (в том числе ванадий) в растворе присутствуют в анионной форме, поэтому при их разделении наиболее широко применяют анионообменники. Молибден в слабокислых и нейтральных растворах существует также преимущественно в анионной форме, на чем основано отделение молибдена от катионов, особенно многозарядных, которые сорбируются на катионообменниках [14].
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Растворы, реагенты, сорбенты. Использовали реактивы квалификации х. ч. или ч. д. а. Растворы солей металлов (0.01 М) готовили по известным методикам растворением ванадата натрия, хлорида никеля, молибдата натрия. Разбавлением получали растворы необходимой (n × 10–4 М) концентрации. Исходный раствор титана(IV) (1 мг/мл) готовили разбавлением 0.23 мл препарата хлорида титана фирмы “Мерк” (плотность 1.73 г/мл) до 100 мл 6 M HCl. Рабочий раствор (20 мкг/мл) титана(IV) получали разбавлением 1 мл исходного раствора до 50 мл 0.1 М HCl. Диметилглиоксим (0.1%-ный раствор) получали растворением 0.1 г препарата в 10 мл этанола, прибавляли 8 мл конц. NH3 и разбавляли водой до 100 мл. Раствор (0.05%-ный) 8-гидроксихинолин-5-сульфокислоты готовили растворением 50 мг реагента в 50 мл воды при добавлении 0.2 мл 1 М раствора NaOH и нагревании на водяной бане; после охлаждения до комнатной температуры разбавляли до 100 мл водой. Исходный (0.5%-ный) раствор фенилфлуорона готовили растворением 50 мг препарата в ~80 мл этанола, содержащего 1 мл 6 М HCl, при нагревании на водяной бане; после охлаждения до комнатной температуры раствор разбавляли до 100 мл этанолом. Раствор (3%-ный) 2,7-дихлорхромотроповой кислоты получали растворением 0.60 г препарата в 20 мл воды. Раствор (2%-ный) аскорбиновой кислоты готовили растворением 1 г препарата в 50 мл воды. Растворы реагентов хранили в холодильнике. Необходимую кислотность растворов перед сорбцией создавали добавлением 0.1 и 1 М растворов NaOH или HCl.
В качестве твердой фазы использовали полиакрилонитрильное волокно, наполненное тонкодисперсным сильнокислотным катионообменником КУ-2 (ПАНВ–КУ-2) или анионообменником АВ-17 (ПАНВ–АВ-17). Степень наполнения составляла 50 мас. %. Сорбенты в форме дисков диаметром 20 мм и массой ~15 мг (ПАНВ–КУ-2) и ~20 мг (ПАНВ–АВ-17) использовали в набухшем состоянии, для чего диски в течение суток выдерживали и затем хранили в дистиллированной воде. Из дисков ПАНВ–КУ-2 и ПАНВ–АВ-17 составляли двухслойный носитель.
Аппаратура. Параметры диффузного отражения определяли на колориметре Пульсар (ОКБА “Химавтоматика”, Чирчик, Узбекистан). За аналитический сигнал принимали разность коэффициентов диффузного отражения дисков (∆R = R0– RМе) после сорбции и реакции с реагентом ионов, сорбированных из контрольного и анализируемого растворов. Контрольный раствор содержал все компоненты реакции, кроме компонента, действие которого изучали; его проводили через все операции, как и исследуемый раствор. Кислотность растворов контролировали стеклянным электродом (потенциометр рН-673). Влияние условий сорбции, концентрации ионов металлов, избирательность определения изучали при комнатной температуре в динамическом режиме из объема 100 мл при скорости потока 5 мл/мин. Растворы прокачивали через ячейки с помощью перистальтического насоса РР-2-15.
Методика эксперимента. В динамическом режиме в проточную ячейку помещают послойно диск ПАНВ–КУ-2, диск ПАНВ–АВ-17 и с помощью перистальтического насоса прокачивают через них 100 мл анализируемого раствора со скоростью 5 мл/мин. После завершения сорбции диски разделяют на две ячейки и прокачивают органические реагенты с последующим измерением аналитических сигналов.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Для определения элементов методом диффузной отражательной спектроскопии выбрали органические реагенты, образующие окрашенные комплексные соединения с V(V), Mo(VI), Ni(II) и Ti(IV) на твердой фазе: 8-гидроксихинолин-5-сульфокислоту, фенилфлуорон, диметилглиоксим и 2,7-дихлорхромотроповую кислоту соответственно [15]. В качестве носителей использовали полиакрилонитрильное волокно, верхний слой которого наполнен анионообменником ПАНВ-АВ-17, нижний слой – катионообменником ПАНВ−КУ-2. В зависимости от кислотности раствора форма существования изучаемых ионов различна.
Зависимости аналитических сигналов от кислотности анализируемых растворов представлены на рис. 1. Cложность выбора оптимального рН для одновременной сорбции четырех элементов обусловлена тем, что титан хорошо сорбируется на ПАНВ–КУ-2 в кислых средах, а ванадий и молибден на ПАНВ–АВ-17 при рН > 4. Значение рН 3.5 ± 0.1 в растворах при сорбции обеспечивает получение аналитических сигналов всех четырех элементов с погрешностью <5%.
Рис. 1.
Зависимость аналитических сигналов комплексов Ti–ДХХК и Ni–ДМГ на ПАНВ–КУ-2 и V–ГОС и Mo–ФФ на ПАНВ–АВ-17 от рН анализируемых растворов при сорбции; сМе = 0.1 мкг/мл.

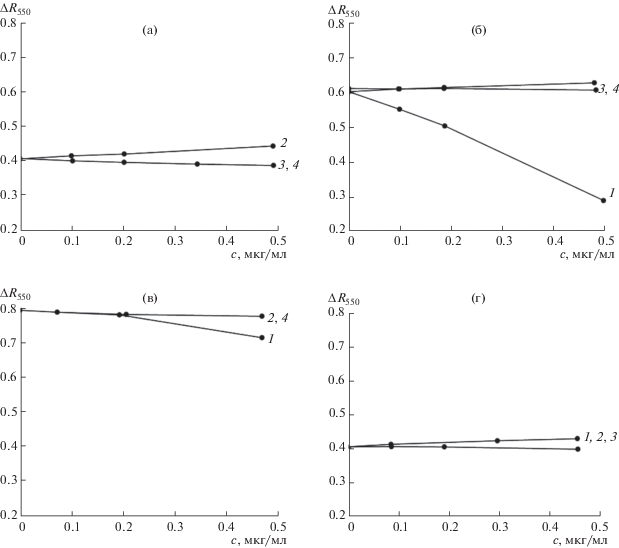
Влияние концентрации сопутствующих элементов на аналитические сигналы комплексов Ti–ДХХК, V–ГОС, Mo–ФФ и Ni–ДМГ иллюстрирует рис. 2. Сорбцию элементов осуществляли на двухслойных дисках из ПАНВ–КУ-2 и ПАНВ–АВ-17 из 100 мл раствора с рН 3.5. На определение всех трех элементов не влияет 5-кратный по массе избыток никеля. Наибольшее влияние оказывает ванадий на определение титана.
Рис. 2.
Влияние сопутствующих элементов на определение Ti с ДХХК (а), V с ГОС (б), Mo с ФФ (в) и Ni с ДМГ (г) при одновременной сорбции из 100 мл растворов с рН 3.5 на дисках ПАНВ–АВ-17 (V, Mo) и ПАНВ–КУ-2 (Ti, Ni); с определяемого элемента – 0.1 мкг/мл; с сопутствующего элемента 0.1–0.5 мкг/мл. 1 – Ti, 2 – V, 3 – Mo, 4 – Ni.
Зависимости аналитических сигналов комплексов от различных факторов изучали после сорбции элементов в динамическом режиме при скорости потока 5 мл/мин на двухслойном носителе: нижний слой – ПАНВ–КУ-2, верхний – ПАНВ–АВ-17. После сорбции слои разделяли и определяли никель и титан на ПАНВ–КУ-2, а ванадий и молибден – нa ПАНВ–АВ-17. Диск ПАНВ–КУ-2 обрабатывали растворами реагентов ДМГ и ДХХК, а диск ПАНВ–АВ-17 – растворами ГОС и 0.1 М НСl и раствором ФФ.
Установлены последовательность и режим (динамический или статический) обработки дисков растворами реагентов, время развития окраски комплексов на дисках, способы устранения аналитического сигнала предыдущего элемента. Изучены зависимости аналитических сигналов от концентрации элементов и определены коэффициенты уравнений градуировочных графиков, диапазон линейности и пределы обнаружения элементов. Результаты изучения условий сорбции и определения четырех элементов приведены в табл. 1.
Таблица 1.
Характеристики методик сорбционно-спектроскопического определения титана, никеля, ванадия и молибдена из одной пробы (V = 100 мл, сорбция при рН 3.5, скорость прокачивания раствора 5 мл/мин)
| Характеристика | ПАНВ–КУ-2 | ПАНВ–АВ-17 | ||
|---|---|---|---|---|
| Ni(II) | Тi(IV) | V(V) | Mo(VI) | |
| Последовательность обработки диска реагентом | 1 | 2 | 1 | 2 |
| Реагент для определения | ДМГ (рН 1) | ДХХК (рН 1) | ГОС (рН 1) | ФФ (рН~0,3) |
| Длина волны, нм | 550 | 530 | 600 | 550 |
| Устранение сигнала 1-го элемента | 0.1 М HCl | – | 2%-ный р-р аскорб. к-ты |
– |
| Коэффициенты уравнения ГГ* | a = 0.01 b = 5.15 r = 0.999 |
a = 0.04 b = 9.17 r = 0.993 |
a = 0.01 b = 6.83 r = 0.999 |
a = 0.09** b = 16.34 r = 0.996 |
| Диапазон линейности ГГ, мкг/мл | 0.01–0.07 | 0.005–0.035 | 0.01–0.08 | 0.003–0.03 |
| Предел обнаружения, нг/мл | 5 | 5 | 5 | 3 |
Избирательность сорбционно-спектроскопического определения Ti(IV), Ni(II), V(V) и Mo(VI) в присутствии посторонних ионов охарактеризована в табл. 2. Наибольшая избирательность присуща определению титана в присутствии меди и определению ванадия в присутствии кобальта и меди. Наименее избирательно определение элементов в присутствии железа(III).
Таблица 2.
Характеристика избирательности определения Ti(IV), Ni(II), V(V) и Mo(VI) в присутствии посторонних ионов (сМе, мкг/мл: Ti, Mo – 0.01, V – 0.05, Ni – 0.07)
| Посторонний ион | Фактор селективности | |||
|---|---|---|---|---|
| Ti(IV) | V(V) | Ni(II) | Mo(VI) | |
| Fe(III) | 10 | 2 | 10 | 2 |
| Zn(II) | 10 | 20 | 100 | 20 |
| CdII) | 10 | 10 | 100 | 50 |
| Mn(II) | 20 | 20 | 5 | 50 |
| Co(II) | 20 | 250 | 20 | 50 |
| Cu(II) | 200 | 500 | 10 | 50 |
| Cr(VI) | 20 | 2 | 100 | 5 |
На основании полученных результатов разработана методика сорбционно-спектроскопического определения Ti(IV), V(V), Ni(II) и Mo(VI) из одной пробы, основанная на одновременной сорбции элементов на двухслойном носителе и последующем их определении с помощью органических реагентов.
Выполнение определения. В проточную ячейку послойно помещают диски ПАНВ–КУ-2 и ПАНВ–АВ-17 и прокачивают через них 100 мл анализируемого раствора с рН 3.5 со скоростью 5 мл/мин. Затем диск ПАНВ–АВ-17 переносят в другую ячейку, прокачивают через него 2 мл 0.005%-ного раствора ГОС, 0.5 мл 0.1 М HCl и через 3 мин измеряют аналитический сигнал при 600 нм (RV). Диск помещают в ту же ячейку, прокачивают 1 мл 2%-ного раствора аскорбиновой кислоты, 1 мл 0.01%-ного раствора ФФ и через 5 мин измеряют аналитический сигнал при 550 нм (RMo).
Через диск ПАНВ–КУ-2 в первой ячейке прокачивают 1 мл 0.1%-ного раствора ДМГ и через 3 мин измеряют аналитический сигнал при 550 нм (RNi). После измерения диск промокают фильтром, помещают в чашку Петри, наносят 3 капли 0.1 М HCl, через ~0.5 мин 3 капли 3%-ного раствора ДХХК и через 5 мин измеряют аналитический сигнал при 530 нм (RTi).
Аналогично выполняют контрольный опыт, не содержащий определяемых ионов металлов, измеряют R0 при соответствующих длинах волн. По найденным значениям вычисляют ΔR = R0 – RMe и по уравнениям градуировочных графиков находят содержание металлов в мкг/мл: сV = (ΔRV – – 0.01)/6.83, сMo = (ΔRMo – 0.09)/16.34, сNi = = (ΔRNi – 0.01)/5.15, сTi = (ΔRTi – 0.04)/9.17. Пределы обнаружения Ni, Ti, V и Mo, оцененные по 3s-критерию, составляют 5, 5, 5 и 3 нг/мл соответственно. Получены удовлетворительные результаты анализа модельных растворов с различным соотношением Ti, V, Ni и Mo (табл. 3), sr < 0.15.
Таблица 3.
Результаты сорбционно-спектроскопического определения Ti(IV), V(V), Ni(II) и Mo (VI) при совместном присутствии из одной пробы (n = 3, P = 0.95)
| Соотношение по массе Ti : V : Ni : Mo |
Введено | Найдено (sr) | ||||||
|---|---|---|---|---|---|---|---|---|
| Ti | V | Ni | Mo | Ti | V | Ni | Mo | |
| 1 : 1 : 1 : 1 | 0.025 | 0.025 | 0.025 | 0.025 | 0.021 ± 0.006 (0.14) |
0.022 ± 0.004 (0.03) |
0.023 + 0.005 (0.10) |
0.026 ± 0.003 (0.05) |
| 2 : 3 : 4 : 1 | 0.016 | 0.024 | 0.032 | 0.008 | 0.016 ± 0.001 (0.04) |
0.022 ± 0.004 (0.08) |
0.030 ± 0.004 (0.06) |
0.010 ± 0.002 (0.09) |
| 3 : 2 : 5 : 2 | 0.033 | 0.022 | 0.055 | 0.022 | 0.032 ± 0.006 (0.09) |
0.018 ± 0.005 (0.13) |
0.052 ± 0.006 (0.05) |
0.022 ± 0.008 (0.13) |
Список литературы
Запорожец О.А. Гавер О.М., Сухан В.В. Аналитические реагенты, иммобилизованные на поверхности различных носителей // Успехи химии. 1997. Т. 66. № 7. С. 702.
Саввин С.Б., Дедкова В.П., Швоева О.П. Сорбционно-спектроскопические и тест-методы определения ионов металлов с органическими реагентами на твердой фазе ионообменников // Успехи химии. 2000. Т. 69. № 3. С. 203.
Золотов Ю.А., Иванов В.М., Амелин В.Г. Химические тест-методы анализа. М.: Едиториал УРСС, 2002. 304 с.
Lin Ying, Wu Di, Li Jingfeng, Ga Ridi. Спектрофотометрическое определение следов Fe(3+) и Мо(6+) в грунтовых водах при помощи пирокатехина в фазе смолы // Spectrosc. Spectral. Anal. 1999. V. 19. № 5. P. 694.
Амелин В.Г., Абраменкова О.И. 2,3,7-Триоксифлуороны, иммобилизованные на целлюлозных матрицах, в тест-методах определения редких элементов // Журн. аналит. химии. 2008. Т.63. № 11. С. 1217.
Дидух С.Л., Лосев В.И., Мухина А.Н., Трофимчук А.К. Применение модифицированного тайроном кремнезема для концентрирования и атомно-эмиссионно-пектрометрического с индуктивно-связанной плазмой определения металлов в природных водах // Журн. аналит. химии. 2016. Т. 71. № 11. С. 1137.
Sayed Zia Mohammadi, Hooshang Hamidian, Labeh Karimzadeh, Zahra Noeinadini. Одновременное выделение следовых количеств Co, Ni и Cu с использованием магнитных наночастиц оксида железа без хелатного агента // Журн. аналит. химии. 2013. Т. 68. № 11. С. 1067.
Швоева О.П., Дедкова В.П., Саввин С.Б. Метод двух реагентов на твердой фазе для определения ванадия (V) и молибдена (VI) при совместном присутствии // Журн. аналит. химии. 2000. Т. 55. № 6. С. 607.
Дедкова В.П., Швоева О.П., Саввин С.Б. Определение V(V) и Сr(VI) из одной пробы на одном диске волокнистого ионообменника // Журн. аналит. химии. 2009. Т. 64. № 4. С. 365.
Швоева О.П., Дедкова В.П., Саввин С.Б. Применение двухслойных носителей для сорбционно-спектроскопического определения Cr(VI), Cu(II) и Ni(II) из одной пробы в проточной системе // Журн. аналит. химии. 2001. Т. 56. № 3. С. 287.
Швоева О.П., Дедкова В.П., Саввин С.Б. Тест-метод определения Cu(II), Ni(II) и Cr(VI) из одной пробы // Журн. аналит. химии. 2001. Т. 56. № 8. С. 851.
Дедкова В.П., Швоева О.П., Саввин С.Б. Тест-метод раздельного определения Hg(II), Cd(II) и Pb(II) из одной пробы на волокнистом сорбенте ПАНВ–АВ-17 // Журн. аналит. химии. 2006. Т. 61. № 8. С. 880.
Швоева О.П., Дедкова В.П., Саввин С.Б. Сорбционно-спектроскопический метод многоэлементного анализа. Определение Cr(VI),V(V), Ni(II) и Cu(II) из одной пробы на двухслойном носителе // Журн. аналит. химии. 2010. Т. 65. № 7. С. 716.
Мархол М. Ионообменники в аналитической химии. М.: Мир, 1985. Т. 1. 264 с. Т. 2. 280 с.
Коренман И.М. Органические реагенты в неорганическом анализе. М.: Химия, 1980. 448 с.
Дополнительные материалы отсутствуют.
Инструменты
Журнал аналитической химии


