Журнал аналитической химии, 2019, T. 74, № 7-app, стр. 16-23
Применение молекулярно импринтированного полимера для концентрирования 4-нитрофенола из водных сред
А. С. Губин 1, *, П. Т. Суханов 1, Н. Ю. Санникова 1, Е. Д. Проскурякова 1, Ю. С. Фролова 1
1 Воронежский государственный университет инженерных технологий
394036 Воронеж, просп. Революции, 19, Россия
* E-mail: goubinne@mail.ru
Поступила в редакцию 01.02.2018
После доработки 03.04.2018
Принята к публикации 05.12.2018
Аннотация
Разработан способ модификации частиц Fe3O4 полимером на основе N-винилпирролидона с молекулярными отпечатками 4-нитрофенола. Обоснованы условия синтеза сорбента: соотношения сшивающего агента и функционального мономера, а также темплата и функционального мономера. Размер частиц сорбента составил около 100 нм. Предложена установка для концентрирования 4-нитрофенола из водных растворов в динамических условиях. Достигнуто 96%-ное извлечение при 100-кратном концентрировании. Изучена селективность полученного полимера. Импринтинг-фактор по отношению к 4-нитрофенолу составил 3.8.
Фенолы – широко распространенные экотоксиканты. Наиболее широко применяют фенол, нитрофенолы и алкилфенолы. Фенолы характеризуются высокой токсичностью, что обусловливает низкие допустимые уровни их содержания в природных объектах [1]. Для определения фенолов требуется стадия предварительного концентрирования. Один из современных подходов к концентрированию – применение сорбентов на основе магнитных наночастиц, что обеспечивает быстрый перенос вещества на сорбент, незначительные затраты времени на отделение раствора от сорбента и малый размер частиц.
Среди нитрофенолов наибольшее значение имеют 2-нитрофенол (2-НФ), 4-нитрофенол (4-НФ) и 2,4-динитрофенол (2,4-ДНФ). Они занесены в перечни Агентства по охране окружающей среды США [2]. Для концентрирования и извлечения нитрофенолов применяют различные подходы, включая жидкостно–жидкостную экстракцию и различные варианты твердофазной микроэкстракции. В работе [3] предложен способ мицеллярной экстракции 4-НФ. В качестве экстрагента применяли кремнийорганическое ПАВ DС193С. При рН 7 в присутствии 1.5 М Na2SO4 степень извлечения 4-НФ составила 68%. Для концентрирования 4-НФ применяли также ион-парную экстракцию [4] при рН 10 с эмульгатором цетилметиламмоний бромидом. В качестве экстрагента использовали октанол-1. После экстракции эмульсию разделяли на центрифуге при 5000 об/мин.
В последние годы для концентрирования все чаще применяют различные варианты твердофазной микроэкстракции, в частности, используют при сорбции молякулярно импринтированные полимеры (МИП) или магнитные наночастицы, покрытые МИП. В работе [5] предложен способ амперометрического определения 4-НФ с предварительным концентрированием на картридже, заполненном 100 мг МИП на основе 4-винилпиридина. Коэффициент концентрирования 4-НФ составил 97.7. Для сорбции 4-НФ, 2-НФ и 2,4-ДНФ эффективны магнитные наночастицы, покрытые полипирролом [6]. Фенолы извлекали из сточных, речных и дождевых вод со степенями извлечения нитрофенолов 84–99%.
Для получения МИП часто используют метакриловую кислоту или ее производные в качестве функционального мономера и дивинилбензол или этиленгликольдиметакрилат (ЭГДМА) в качестве сшивающего агента. Полимеры на основе N-виниламидов (N-винилпирролидон, N-винилкапролактам) являются эффективными сорбентами фенольных соединений. Использование в качестве функционального мономера 4-винилпирролидона позволило получить МИП с отпечатками 4-НФ [7]. Величина импринтиг-фактора (IF) составила 1.2. При синтезе МИП на основе акриламида величина IF составила 3.3. В работе [8] молекулярно импринтированные полимеры с опечатками 4-НФ получали радикальной сополимеризацией функциональных мономеров и ЭГДМА в абсолютизированном метаноле в течение 16 ч при 70°С. Достигнуто 85%-ное извлечение 4-НФ при IF, равном 2.0.
Основная цель настоящей работы состояла в изучении возможности синтеза МИП на основе N-винилпирролидона (НВП) с отпечатками 4-НФ методом суспензионной полимеризации и оценке основных сорбционных характеристик полученного полимера и его селективности по отношению к 4-НФ.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Приборы, реактивы и материалы. Хлорид железа(III) FeCl3 · 6Н2О (Sigma-Aldrich/Merck); сульфат железа(II) FeSO4 · 7Н2О; раствор аммиака (25 мас. %), толуол, пропанол-1, 2-НФ, 4-НФ, дибутиламин, метанол, додецилсульфонат натрия (Вектон, Россия) ч. д. а. Петролейный эфир ч. (Вектон, Россия), кислота олеиновая квалификации “для газовой хроматографии” (Sigma-Aldrich/Merck). Этиленгликольдиметакрилат (Вектон, Россия) содержал 98% основного вещества. N-винилпирролидон (Acros, США), метакрилоксипропилтриметоксисилан (МОТС) (ПФ “Техносиланы”, Россия), 2,2'-азобисизобутиронитрил (АИБН) (ООО “Кемикал Лайн”, Россия) содержали по 99% основного вещества.
Частицы Fe3O4 и полимера синтезировали в трехгорлой колбе с верхнеприводной мешалкой ES8300 (Экохим, Россия), температуру поддерживали с помощью термостатирующего блока RE 415 GLCK 1911 (LAUDA, Германия). Обработку ультразвуком при синтезе полимера осуществляли в ультразвуковой ванне Branson В1510-DTH (Branson Ultrasonics, Швейцария). Для исследования полимера применяли ИК-Фурье-спектрометр ИнфраЛЮМ ФТ-08 (Люмэкс, Россия). Удельную площадь поверхности по методу БЭТ устанавливали на анализаторе TRISTAR II 3020 (Micromeritics, США) в центре коллективного пользования (ЦКП) Белгородского государственного университета. Размер частиц сорбента определяли с помощью сканирующего электронного микроскопа JSM-6510LV (Jeol, Япония) в технопарке ЦКП Воронежского государственного университета. При динамическом концентрировании применяли перистальтический насос LOIP LS – 301 (АО “ЛОИП”, Россия). Для перемешивания при динамической сорбции применяли некоммерческую микромешалку собственной конструкции. Для спектрометрических измерений использовали спектрофотометр Shimadzu UV-1800 (Shimadzu, Япония). 2-, 4-Нитрофенолы определяли фотометрически по реакции с аммиаком [9]. Магнитные наночастицы извлекали неодимовым магнитом класса UH (рабочий диапазон температур до 180°С).
Методика эксперимента. Синтез наночастиц магнетита (Fe3O4). В трехгорлую колбу помещали 300 мл бидистиллированной воды, растворяли в ней 20.0 г FeCl3 · 6H2O и 9.6 г FeSO4 · 7H2O. Полученный раствор перемешивали при 3000 об./мин при 80°С, постепенно прибавляли 25 мл раствора NH3 и 2.5 г олеиновой кислоты. Продолжали перемешивать в течение 1.5 ч. Полученные частицы извлекали магнитом, промывали, высушивали под вакуумом, промывали толуолом и хранили в нем.
Модификация поверхности магнетита метакрилоксипропилтриметоксисиланом [10]. К 50 мл дисперсии частиц Fe3O4 в толуоле добавляли 5 мл МОТС и несколько капель дибутиламина, после чего перемешивали мешалкой в течение 48 ч при 1000 об./мин при 70°С. Частицы Fe3O4, модифицированные МОТС (Fe3O4@МОТС), выделяли из толуола петролейным эфиром и сушили под вакуумом.
Модификация поверхности частиц Fe3O4@МОТС полимером методом суспензионной полимеризации. N‑Винилпирролидон приливали к 50 мл пропанола-1 и перемешивали в течение 3 ч. Затем добавляли 10 мл толуола, сшивающий агент (ЭГДМА) и выдерживали 10 мин в ультразвукой ванне. Далее к смеси приливали суспензию, содержащую 3 г магнитных частиц Fe3O4@МОТС в толуоле, и 500 мл 0.015 М раствора додецилсульфоната натрия. Смесь переливали в колбу, добавляли инициатор полимеризации АИБН и перемешивали 30 ч при 700 об./мин и 60°С. После синтеза промывали полученные частицы, модифицированные поливинилпирролидоном, (Fe3O4@МОТС@ПВП) смесью метанол–вода (3 : 1, по объему). Количества добавляемых НВП, ЭГДМА и АИБН приведены в табл. 1. Получали серию полимеров сравнения (ПС) с соотношениями НВП : ЭГДМА: 1 : 5 (ПС-1–ПС-3), 1 : 15 (ПС-4–ПС-6) и 1 : 30 (ПС-7–ПС-9).
Таблица 1.
Сорбция 2-нитрофенола и 4-нитрофенола на полимерах сравнения и молекулярно импринтированных полимерах (n = 3, Р = 0.95, масса сорбента 0.05 г)
| Полимер | S, м2/г | Количество ЭГДМА*, ммоль | Масса АИБН, мг | Степень извлечения R, % | Коэффициент распределения, мл/г | ||
|---|---|---|---|---|---|---|---|
| 2-НФ | 4-НФ | 2-НФ, D | 4-НФ, D × 10–2 |
||||
| ПС-1 | 17 | 25 | 20 | 18 ± 2 | 43 ± 3 | 43 ± 5 | 1.5 ± 0.2 |
| ПС-2 | 28 | 25 | 50 | 18 ± 2 | 50 ± 2 | 43 ± 4 | 2.0 ± 0.2 |
| ПС-3 | 51 | 25 | 100 | 21 ± 2 | 49 ± 2 | 53 ± 6 | 1.9 ± 0.2 |
| ПС-4 | 46 | 75 | 20 | 25 ± 2 | 61 ± 3 | 67 ± 5 | 3.1 ± 0.3 |
| ПС-5 | 51 | 75 | 50 | 25 ± 2 | 68 ± 2 | 67 ± 5 | 4.2 ± 0.4 |
| ПС-6 | 39 | 75 | 100 | 25 ± 2 | 67 ± 2 | 67 ± 6 | 4.0 ± 0.4 |
| ПС-7 | 35 | 150 | 20 | 21 ± 2 | 51 ± 2 | 53 ± 6 | 2.2 ± 0.2 |
| ПС-8 | 29 | 150 | 50 | 18 ± 2 | 53 ± 3 | 43 ± 5 | 2.3 ± 0.3 |
| ПС-9 | 31 | 150 | 100 | 18 ± 2 | 51 ± 2 | 43 ± 5 | 2.2 ± 0.3 |
| ИП-1** | 107 | 75 | 50 | 21 ± 2 | 84 ± 1 | 53 ± 6 | 10.5 ± 0.7 |
| ИП-2** | 119 | 75 | 50 | 21 ± 2 | 89 ± 1 | 53 ± 6 | 16 ± 2 |
| ИП-3** | 117 | 75 | 50 | 20 ± 2 | 85 ± 1 | 50 ± 5 | 11.3 ± 0.8 |
| ИП-4** | 96 | 75 | 50 | 20 ± 2 | 78 ± 2 | 50 ± 6 | 7.1 ± 0.8 |
Молякулярно импринтированные полимеры синтезировали при соотношении НВП, ЭГДМА и АИБН как в ПС-5, который характеризовался наилучшими сорбционными характеристиками среди полимеров сравнения. Для получения полимеров с молекулярными отпечатками смесь 4-НФ и НВП приливали к 50 мл пропанола-1 и перемешивали в течение 3 ч. Далее синтез проводили, как изложено выше. Соотношения темплата (4-НФ) и функционального мономера (НВП) приведены в табл. 1. Получали полимеры с молекулярными отпечатками ИП-1–ИП-4.
Сорбция в статических условиях. 10 мл растворов фенолов с концентрациями 0.001, 0.01, 0.05, 0.1, 0.5, 1.0, 1.25, 1.5, 1.75, 2.0 мг/мл помещали в химические стаканы, добавляли 0.05 г сорбента (ПС-5 или ИП-2). Перемешивали в течение 50 мин магнитной мешалкой. После сорбции магнитом извлекали сорбент и определяли концентрацию фенола в растворе после сорбции (λmax = 405 нм). Строили зависимости величины адсорбции (а, ммоль/г) от равновесной концентрации нитрофенолов в растворе после сорбции (ср, мг/мл). Одновременно рассчитывали характеристики сорбции: степень извлечения (R, %), коэффициент распределения (D), коэффициент концентрирования (К) и импринтинг-фактор (IF) [8], а также коэффициент селективности (k) [10]. Для десорбции НФ использовали 1 мл раствора NaOH (рН 10).
Построение кинетических кривых сорбции. Cтроили зависимости степени извлечения (R, %) от времени. Готовили растворы фенолов с концентрацией 10 мкг/мл, добавляли 0.1 г сорбента ПС-5 или ИП-2, перемешивали, пробы отбирали через 5, 10, 20, 30, 40 и 50 мин.
Приготовление концентрирующего патрона для сорбции в динамических условиях. Концентрирующий патрон получали из полиэтилена средней плотности путем формования. Все элементы сваривали горячим воздухом, сварные полимерные швы герметизировали полиэтиленовой пленкой и снова обрабатывали горячим воздухом. Получался полупрозрачный концентрирующий патрон круглого сечения дисковой формы объемом 10 см3 со съемной верхней крышкой (рис. 1). Вырезали отверстие под вал микромешалки и прикрепляли входной и выходной патрубки. Внутри патрона помещали неодимовый кольцевой магнит в форме диска (7) через съемную крышку (6, выделена жирным контуром). Магнит предварительно герметизировали, покрывая всю поверхность контакта термоусадочной полиэтиленовой пленкой (8), и соединяли с валом микромешалки. Возможен вариант распечатки концентрирующего патрона с применением 3D-принтера методом термической наплавки полиэтилена высокой плотности.
Рис. 1.
Концентрирующий патрон для сорбции в динамических условиях: I – приготовление и отбор суспензии магнитного сорбента; II – заполнение сорбентом концентрирующего патрона; III – формирование слоя сорбента на магнитном диске. 1 – суспензия магнитного сорбента в химическом стакане, 2 – шприц для отбора суспензии сорбента, 3 – концентрирующий патрон, 4 – входной патрубок, 5 – выходной патрубок, 6 – съемная крышка, 7 – неодимовый магнит в форме диска, 8 – полиэтиленовая оболочка, 9 – слой магнитного сорбента, 10 – мешалка, 11 – вал мешалки, 12 – корпус мешалки. На разрезах А–А и Б–Б показана проекция входного патрубка (4).

Для проведения сорбции суспензию магнитного сорбента в воде помещали в стакан (1), отбирали шприцем (2) и через входной (4) и выходной (5) патрубки помещали в концентрирующий патрон. Медленным вращением мешалки (10) равномерно распределяли сорбент по магнитному диску (7) с образованием тонкого однородного слоя (9) по всей поверхности магнита на пленке (8).
Сорбция в динамических условиях. В концентрирующий патрон помещали 0.1 г сорбента ПС-5 или ИП-2 и пропускали раствор, содержащий 1 мкг/мл фенола, включали магнитный диск с частотой вращения 20 об./мин. Пропускали через концентрирующий патрон анализируемый раствор со скоростями 0.5, 1.0 и 2.0 мл/мин. Через определенные интервалы времени отбирали пробы и строили выходные кривые сорбции [8]. Устанавливали объем до проскока (V10%) и коэффициент концентрирования (К). Строили зависимости отношения равновесной концентрации (с) к исходной (с0) от объема пропускаемого раствора (Vпр).
Для концентрирования и определения 4-НФ через патрон пропускали 100 мл раствора с концентрацией 4-НФ 1 и 100 мкг/мл со скоростью 0.5 мл/мин. После этого концентрирующий патрон заполняли 10 мл смеси этанол–раствор NaOH с pH 10 (1 : 10, по объему). Концентрирующий патрон промывали десорбирующим раствором и определяли в нем 4-НФ.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
При сравнении ИК-Фурье спектров Fe3O4, Fe3O4@МОТС, ПС-5 и ИП-2 по максимумам поглощения идентифицировали следующие функциональные группы (рис. 2): 578 см–1 – колебания связи Fe–O, проявляются во всех спектрах; 847 см–1 – пик, соответствующий связи Si–C; группа пиков 1075–1100 см–1 характерна для Si–O; 1272 см–1 – максимум поглощения связи C–N; группа пиков 1630–1650 см–1 – колебания амидной С–O группы; группа пиков 1708–1725 см–1 – колебания карбонильных групп; колебания при 2850–2925 см–1 характеризуют наличие СН2- и СН3-групп [10, 11]. По результатам растровой электронной микроскопии размер частиц сорбента составляет 65–145 нм, отдельных частиц до 200 нм, средний размер около 100 нм (рис. 3). Наиболее мелкие частицы образуют агломераты. Удельные площади поверхности (S, м2/г) синтезированных сорбентов приведены в табл. 1.
Рис. 2.
ИК-Фурье-спектры Fe3O4 (1), Fe3O4@МОТС (2), полимера сравнения ПС-2 (3) и молекулярно импринтированного полимера ИП-5 (4).

Максимальные степени извлечения 4-НФ достигаются в случае полимера ПС-5 при соотношении НВП–ЭГДМА 1 : 15 и добавлении 50 мг АИБН (табл. 1). При синтезе МИП в присутствии 4-НФ оптимальное соотношение темплата и функционального мономера достигается на полимере ИП-2, при этом степень извлечения 4-НФ максимальна (табл. 1). Для оценки селективности извлечения рассчитывали коэффициент селективности (k) как отношение коэффициентов распределения 4-НФ и 2-НФ (k4-НФ/2-НФ) на импринтированном и неимпринтированном полимерах (табл. 2). Коэффициенты селективности для МИП больше, чем для полимера сравнения в среднем в 2.5–5 раз, величина импринтинг-фактора составляет 1.7–3.8.
Таблица 2.
Показатели селективности сорбции 4-нитрофенола
| Полимер | k4-НФ/2-НФ* | IF** |
|---|---|---|
| ПС-5 | 6.3 | – |
| ИП-1 | 19.8 | 2.5 |
| ИП-2 | 30.5 | 3.8 |
| ИП-3 | 22.6 | 2.6 |
| ИП-4 | 14.3 | 1.7 |
Для практически полного извлечения (95% и более) требуется масса сорбента ИП-2 около 0.1 г. В таких условиях при достижении равновесия извлекается 96% 4-НФ и не более 35% 2-НФ (рис. 4). При этом коэффициент концентрирования для 4-НФ составляет 100. Кинетика сорбции 4-НФ и 2-НФ на ИП-2 (масса 0.1 г) существенно различается. При интенсивном перешивании в статическом режиме уже через 5 мин извлекается около 82% 4-НФ и 17% 2-НФ (рис. 4). При сорбции на полимере сравнения степени извлечения 2-НФ и 4-НФ отличаются в меньшей степени. При сорбции на ИП-2 и ПС-5 степень извлечения 2-НФ значительно ниже, чем 4-НФ, что объясняется наличием внутримолекулярной водородной связи.
Рис. 4.
Кинетические кривые сорбции 4-нитрофенола (1) и 2-нитрофенола (2) на импринтированном полимере ИП-2.

Изотермы сорбции 4-НФ на полимере с молекулярными отпечатками ИП-2 и полимере сравнения ПС-5 существенно различаются (рис. 5). Установлено, что значение предельной сорбции 4-НФ (163 мг/г) значительно больше, чем для 2-НФ (78 мг/г). Примерно такие же значения предельной сорбции (155 мг/г) достигаются при использовании в качестве функционального мономера полииминоэтилена и сшивающего агента диэпоксиалкила [12]. Величина предельной сорбции 4-НФ меньше (57.8 и 129.1 мг/г) в случае применения в качестве сшивающего агента ЭГДМА, а в качестве функционального мономера – метакриловой кислоты [13] или 3-аминопропилтриэтоксисилана [14] соответственно. В случае полимера на основе метакриловой кислоты и глутарового альдегида в качестве сшивающего агента (модификатор β-циклодекстрин) получены более высокие значения предельной сорбции (254 мг/г) [15].
Разница в сорбции 4-НФ на МИП и полимере сравнения объясняется наличием центров специфического связывания 4-НФ. В области малых концентраций изотермы сорбции 4-НФ на ИП-2 и ПС-5 практически не отличаются. Это обусловлено тем, что специфические центры связывания 4-НФ включены в полимерную матрицу, а физическая сорбция происходит в первую очередь на неспецифических центрах. С увеличением концентрации 4-НФ начинается связывание на специфических центрах [10, 16]. Десорбция 4-НФ с ИП-2 занимает больше времени, чем 2-НФ (табл. 3). Десорбция 2-НФ и 4-НФ на ПС-2 протекает с одинаковой скоростью.
Таблица 3.
Десорбция фенолов с молекулярно импринтированного полимера ИП-2 и полимера сравнения ПС-5 (десорбент – 1 мл 1 × 10–4 М раствора NaOH)
| Фенол | Сорбент | Степень десорбции (%) за промежуток времени | |||
|---|---|---|---|---|---|
| 2 мин | 5 мин | 10 мин | 20 мин | ||
| 4-НФ | ИП-2 | 47 | 78 | 90 | 99 |
| 2-НФ | ИП-2 | 78 | 95 | 99 | – |
| 4-НФ | ПС-5 | 81 | 99 | 99 | – |
| 2-НФ | ПС-5 | 82 | 99 | 99 | – |
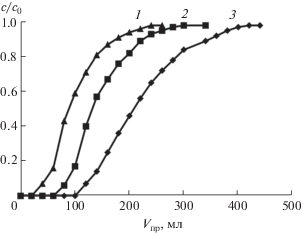
Для оценки характеристик сорбента в динамическом режиме строили выходные кривые сорбции (рис. 6). Оптимальная скорость пропускания составляет 0.5 мл/мин, При увеличении скорости пропускания происходит уменьшение диффузии, что ведет к уменьшению объема до проскока и коэффициента концентрирования (табл. 4). Дальнейшее уменьшение скорости пропускания до 0.25–0.3 мл/мин нецелесообразно, поскольку существенно увеличивается продолжительность анализа.
Рис. 6.
Выходные кривые сорбции 4-нитрофенола при различных скоростях пропускания, мл/мин: 1 – 2.0, 2 – 1.0, 3 – 0.5.
Применимость методов статического и динамического концентрирования оценивали способом введено–найдено (табл. 5). Для сорбции в статических условиях готовили 10 мл растворов с концентрациями 4-НФ 1.0 и 10.0 мкг/мл (содержащих 10 и 100 мкг 4-НФ). При динамической сорбции 100 мл раствора 4-НФ с концентрацией 1.0 мкг/мл пропускали со скоростью 0.5 мл/мин через концентрирующий патрон. Десорбцию проводили 10 мл раствора NaOH с рН 10. Погрешность определения в статических условиях не превышала 7.1%, в динамических условиях – 6.1%. Предел обнаружения составил 4.7 мкг/л.
* * *
Таким образом, изучена возможность модификации поверхности Fe3O4 молекулярно импринтированным полимером на основе НВП (функциональный мономер) и ЭГДМА (сшивающий агент), темплат – 4-НФ. Величина импринтинг-фактора при применении полученного полимера составляет 3.8. Установлено, что МИП позволяет достичь 96%-ного извлечения 4-НФ при 100-кратном концентрировании. Для бóльших объемов анализируемых растворов (объем до 100 мл) предложен способ динамического концентрирования. Коэффициент концентрирования в динамических условиях колеблется в интервале от 47 до 100 и зависит от скорости пропускания раствора через концентрирующий патрон. Погрешность фотометрического определения при сорбции в статических условиях не превышает 7.1%, в динамических условиях – 6.1%.
Список литературы
Michałowicz J., Duda W. Phenols – sources and toxicity // Polish J. Environ. Stud. 2007. V. 16. № 3. P. 347.
United States Environmental Protection Agency (US EPA), Method 8041А: Phenols by gas chromatography, US Environmental Protection Agency, 2000. https://www.epa.gov/sites/production/files/2015-12/documents/8041a.pdf. (дата обращения: март 2018).
Zain N.N.M., Abu Bakar N.K., Mohamad S., Saleh N.Md. Optimization of a greener method for removal phenol species by cloud point extraction and spectrophotometry // Spectrochim. Acta A. 2014. V. 118. P. 1121.
Moradi M., Yamini Y., Kakehmam J., Esrafili A., Ghambarian M. A new strategy to simultaneous microextraction of acidic and basic compounds // J. Chromatogr. A. 2011. V. 1218. P. 3945.
Gholivand M.B., Khodadadian M., Bahrami G. Molecularly imprinted polymer preconcentration and flow injection amperometric determination of 4-nitrophenol in water // Anal. Lett. 2015. V. 48. № 18. P. 2856.
Tahmasebi E., Yamini Y., Seidi S., Rezazadeh M. Extraction of three nitrophenols using polypyrrole-coated magnetic nanoparticles based on anion exchange process // J. Chromatogr. A. 2013. V. 1314. P. 15.
Дмитриенко С.Г., Ирха В.В., Дуйсебаева Т.Б., Михайлик Ю.В., Золотов Ю.А. Синтез и исследование сорбционных свойств полимеров с отпечатками 4-гидроксибензойной кислоты // Журн. аналит. химии. 2006. Т. 61. № 1. С. 18. (Dmitrienko S.G., Irkha V.V., Duisebaeva T.B., Mikhailik Yu.V., Zolotov Yu.A. Synthesis and study of the sorption properties of 4-hydroxybenzoic acid-imprinted polymers // J. Analyt. Chem. 2006. V. 61. № 1. Р. 14.)
Чурилина Е.В., Суханов П.Т., Ермак С.С., Коренман Я.И., Шаталов Г.В. Новые полимеры на основе N-виниламидов для концентрирования нитрофенолов из водных сред // Журн. аналит. химии. 2012. Т. 67. № 9. С. 855. (Churilina E.V., Sukhanov P.T., Ermak S.S., Korenman Ya.I., Shatalov G.V. New N-vinylamide based polymers for the preconcetration of nitrophenols from aqueous media // J. Analyt. Chem. 2012. V. 67. № 9. P. 767.)
Кушнир А.А., Суханов П.Т., Чурилина Е.В., Шаталов Г.В. Динамическая сорбция нитрофенолов из водных растворов полимерами на основе N-винилпирролидона // Журн. прикл. химии. 2014. Т. 87. № 5. С. 589. (Kushnir A.A., Sukhanov P.T., Churilina E.V., Shatalov G.V. Dynamic sorption of nitrophenols from aqueous solutions by polymers based on N-vynilpyrrolidone // Russ. J. Appl. Chem. V. 87. № 5. P. 579.)
Ji Y., Yin J., Xu Z., Zhao C., Huang H., Zhang H., Wang C. Preparation of magnetic molecularly imprinted polymer for rapid determination of bisphenol A in environmental water and milk samples // Anal. Bioanal. Chem. 2009. V. 395. P. 1125.
Mohammed A.H., Ibrahim N.A., Zainuddin N. Synthesis and monomer reactivity ratios of [3-(trimethoxysilyl) propyl methacrylate/N-vinyl pyrrolidone] copolymer // Int. J. Chem. Sci. 2016. V. 14. № 4. P. 2279.
An F.Q., Gao B.J., Feng X.Q. Binding and recognition ability of molecularly imprinted polymer toward p-nitrophenol // J. Appl. Polym. Sci. 2012. V. 125. № 4. P. 2549.
Mehdinia A., Baradaran Kayyal T., Jabbari A., Ovais Aziz Zanjani M., Ziaei E. Magnetic molecularly imprinted nanoparticles based on grafting polymerization for selective detection of 4-nitrophenol in aqueous sample // J. Chromatogr . A. 2013. V. 1283. P. 82.
Mehdinia A., Dadkhah S., Baradaran Kayyal T., Jabbari A. Design of a surface-immobilized 4-nitrophenol molecularly imprinted polymer via pre-grafting amino functional materials on magnetic nanoparticles // J. Chromatogr. A. 2014. V. 1364. P. 12.
Wilson L.D., Pratt D.Y., Kozinski J.A. Preparation and sorption studies of β-cyclodextrin–chitosan–glutaraldehyde terpolymers // J. Coll. Interface Sci. 2013. V. 393. P. 271.
Yang K., Liu Z., Mao M., Zhang X., Zhao C., Nishi N. Molecularly imprinted polyethersulfone microspheres for the binding and recognition of bisphenol A // Anal. Chim. Acta. 2005. V. 546. № 1. P. 30.
Дополнительные материалы отсутствуют.
Инструменты
Журнал аналитической химии




