Журнал аналитической химии, 2019, T. 74, № 9-app, стр. 48-56
История создания ионообменной хроматографии как метода аналитической химии
Е. В. Рыбакова *
МПО “Абакус”
127106 Москва, Гостиничный проезд, 4Б, Россия
* E-mail: rybakova_elena@list.ru
Поступила в редакцию 14.09.2018
После доработки 15.10.2018
Принята к публикации 17.03.2019
Аннотация
Рассмотрен начальный период (конец 1930-х–начало 1940-х гг.) создания ионообменной хроматографии как метода аналитической химии. Проанализированы научные работы автора метода – немецкого ученого Георга-Мария Шваба и его ближайших последователей. В представленный период времени метод носил название “неорганическая хроматография”.
Несмотря на большой объем литературы по истории хроматографии, истории ионообменной хроматографии уделялось мало внимания. Данная работа – попытка изложить историю создания ионообменной хроматографии на основе анализа работ ее автора – немецкого физико-химика Георга-Мария Шваба (Georg-Maria Schwab, 3.02.1899–23.12.1984) и его ближайших последователей. Шваб – автор множества оригинальных работ и нескольких книг по физической химии и катализу. Особенно известна его книга “Handbook of Catalysis”, вышедшая в 1941 г. и переизданная восемь раз. Дальнейшему развитию и становлению ионообменной хроматографии как метода аналитической химии (до начала 1970 гг.) будет посвящена отдельная публикация.
ГЕОРГ-МАРИЯ ШВАБ – ПИОНЕР ИОНООБМЕННОЙ ХРОМАТОГРАФИИ
Научная деятельность Шваба (фото 1) охватывает 62 года. Она отражена в почти 300 научных публикациях на различные темы: “От твердофазных реакций к неорганической хроматографии, от хлорирования на свету к строению ферментов, от гомогенной газовой кинетики до фотографического процесса, от реакции Къельдаля до преобразования параводорода”11, как пишет его ученик и коллега Дж. Блок [2]. Но для нашего исследования наиболее интересен период конца 1930 – начала 1940 гг., когда Шваб занимался хроматографией. Биографические данные Шваба представлены в статье, посвященной применению первых ионообменников [3]. Здесь мы упомянем только те факты биографии ученого, которые могли служить источниками его интереса к хроматографии или нашли отражение в его исследованиях.
В 1928 г., будучи уже доктором наук, Г.-М. Шваб был приглашен профессором Генрихом Виландом22 в Мюнхенский университет. Профессор Виланд в то время возглавлял кафедру органической химии университета в Мюнхене, заняв эту должность в 1925 г. после Р. Вильштеттера33, которого уволили за его убеждения. Как известно, Вильштеттер в некотором смысле был “злым гением” в истории хроматографии: своей необоснованной критикой метода М.С. Цвета он создавал негативное отношение к методу других исследователей. Однако, как пишет биограф М.С. Цвета Е.М. Сенченкова, упоминая о его помощи в 1931 г. своему ученику Р. Куну и его коллеге Э. Ледереру в исследованиях растительных пигментов: “Он передал им немецкий перевод книги Цвета (1910) и охотно давал различные рекомендации по освоению метода. Таким образом, Вильштеттер, хотя и со значительным опозданием, все же оценил значение открытия Цвета и, начиная с 30-х годов, стал способствовать его развитию”. Сам Виланд также применял цветовский метод, и можно сделать предположение, что именно он познакомил Шваба с хроматографией; по крайней мере, в серии работ по неорганической хроматографии, о которой мы далее пишем, Шваб неизменно выражал ему благодарность за поддержку. Кроме того, в своей первой работе серии “Неорганическая хроматография” Шваб пишет, что общался с другими химическими лабораториями Мюнхенского университета, в которых уже занимались хроматографией.
Первая статья Шваба – цель работ, название и предназначение нового метода. Первая статья Шваба “Неорганическая хроматография”, датированная 17 декабря 1936
г., была опубликована в журнале “Naturwissenschaften” в 1937 г. [4]. Статья подготовлена в дискуссионной форме и предназначена для широкой научной аудитории.
Можно предположить, что Шваб хотел привлечь внимание научного сообщества к началу
его оригинальных работ и закрепить свой приоритет в новой области – хроматографии
неорганических веществ. В самом ее начале авторы обозначают цель работ: “Большие успехи
в хроматографическом адсорбционном анализе в органической и физиологической химии
в последние годы заставили нас применить этот метод также к основной аналитической
проблеме – разделению неорганических ионов”. В статье кратко описана методика работ
и сделан вывод о пригодности этого метода для разделения катионов. В частности, авторами
был выстроен ряд удерживания катионов на колонке с оксидом алюминия в следующей последовательности
сверху вниз колонки: Sb'' Bi'' Cr'' Fe'''  Pb" Hg" Cu" Ag' Zn" Co" Cd" Ni" Mn" (ряд приведен в оригинальном написании)44. Для разделения брали водные растворы нейтральных солей (в основном нитратов). Авторы
отмечают, что “на некоторых частях этой серии ионов соседство настолько тесно, что
происходит только плохое разделение, например в парах Cr'''–Fe"\Fe'''–
Pb" Hg" Cu" Ag' Zn" Co" Cd" Ni" Mn" (ряд приведен в оригинальном написании)44. Для разделения брали водные растворы нейтральных солей (в основном нитратов). Авторы
отмечают, что “на некоторых частях этой серии ионов соседство настолько тесно, что
происходит только плохое разделение, например в парах Cr'''–Fe"\Fe'''–
 –Pb'' и особенно Co"–Cd" и Cd"–Ni". В паре Co"–Ni" разделение едва заметно”. Забегая
вперед, следует обратить внимание, что последняя проблема (сложность разделения пар
кобальт–кадмий и кадмий–никель) станет основной задачей первой серии публикаций отечественных
хроматографистов – последователей Шваба Е.Н. Гапона и Т.Б. Гапон, – посвященной применению
ионообменной хроматографии в аналитической химии [5]. Авторы обращают внимание, что ряд удерживания меняется при использовании в качестве
аналитов кислых или щелочных солей, не делая при этом никаких выводов или предположений.
–Pb'' и особенно Co"–Cd" и Cd"–Ni". В паре Co"–Ni" разделение едва заметно”. Забегая
вперед, следует обратить внимание, что последняя проблема (сложность разделения пар
кобальт–кадмий и кадмий–никель) станет основной задачей первой серии публикаций отечественных
хроматографистов – последователей Шваба Е.Н. Гапона и Т.Б. Гапон, – посвященной применению
ионообменной хроматографии в аналитической химии [5]. Авторы обращают внимание, что ряд удерживания меняется при использовании в качестве
аналитов кислых или щелочных солей, не делая при этом никаких выводов или предположений.
В этой статье Шваб называет новый метод “ионной хроматографией” и указывает на его возможности: “Практическая применимость ионной хроматографии (Ionenchromatographie) проявляется, кроме прочего, в обнаружении следовых примесей элементов …”. В качестве примера он указывает на возможность визуальной идентификации одной десятитысячной доли моля железа на фоне молярной концентрации других катионов, таких как медь или кобальт. Примечательно, что В.П. Мелешко, другой отечественный химик и в будущем известный специалист по ионному обмену, в одной из своих публикаций, посвященных ионообменной хроматографии, также отмечал высокую чувствительность визуального хроматографического определения железа на фоне катионов других металлов. Однако разделение он проводил на сульфофеноловом катионите, специально приготовленном для этих исследований [6]. Другой вариант применения этого метода, предлагаемый Швабом, – отделение неудерживаемых или слабо удерживаемых целевых катионов от сильно удерживаемых катионов примесей. Именно эти два варианта приложения ионообменных разделений в хроматографии просуществовали практически до конца 1960 гг. В заключении публикации авторы указывают, что они начали исследования разделения анионов и испытания других сорбентов на их пригодность к разделению ионов.
Серия “Неорганическая хроматография. Части I–V”. После выхода первой, вводной, статьи началась серия публикаций Шваба, подготовленных совместно с коллегами, под общим названием “Неорганическая хроматография. Части I–V” и вышедших в “Angewandte Chemie” с 1937 по 1940 гг. Первая работа серии была выполнена совместно с К. Джокерсом в 1937 г. [7]. Во введении авторы отмечают, имея в виду работы Р. Куна и Э. Ледерера, что до недавнего времени хроматография была областью разделения органических веществ. Применение хроматографии для разделения неорганических веществ, по мнению Шваба, некоторыми исследователями считалось бесперспективным, и только в одной публикации, “на которую любезно обратил наше внимание Винтерштайн55, можно увидеть, что оксиды металлов, добавленные в торф, могут быть элюированы соляной кислотой в виде фракций, “сравнимых со шкалой спектра”. Нечто, связанное с хроматографией, также показано на пермутитах”. И далее: “Но мы не обязаны этим упомянутым подготовительным работам, а только благодаря близким и плодотворным отношениям, связывающим различные направления химии в Мюнхенской лаборатории, мы поставили перед собой задачу детально изучить применимость хроматографического метода в неорганическом анализе”. Авторы ссылаются на книгу Л. Цехмейстера66 и Л. Челноки “Хроматографический адсорбционный метод” издания 1937 г. [8]. Эта книга сыграла важную роль в развитии хроматографии. Считаем нужным отметить, что именно Шваб написал на нее рецензию [9], где, в частности, указал, что она предназначена “всем, кто хочет его [метод Цвета] изучить, поскольку демонстрирует принципы, методологию и наиболее важные примеры применения таким превосходным образом”.
Вернемся к содержимому первой публикации из серии Шваба. В этой работе применялись хроматографические колонки – стеклянные трубки диаметром 4–7 мм, которые заполняли оксидом алюминия фирмы Merck, подготовленным по Брокманну. Авторы отметили, что, в отличие от органической хроматографии, в неорганической отсутствуют просветы между полосами. Основную сложность составляло количественное определение разделенных катионов. Между высотой зоны на хроматографической колонке и количеством адсорбированного на ней вещества существует только приблизительное соответствие. Авторы подробно описывают технологию экспериментов и подбор условий разделения и окрашивания зон. Техника эксперимента очень похожа на применявшуюся в то время для разделения органических веществ: трубку заполняли сорбентом в виде водной суспензии, небольшое количество образца помещали в начале колонки, которую затем промывали водой до остановки перемещения зон по колонке. На следующем этапе подходящий реагент вводили для окрашивания зон, таким образом получалась “хроматограмма”. Во всех рассматриваемых публикациях Шваба указывается порядок полос сверху вниз колонки и, если необходимо, их цвет. Удивительно точно и современно в статье звучит характеристика метода: “Неорганическая хроматография не является чисто механическим применением физических законов и аппаратных средств, но дает широкие возможности для приложения химических знаний экспериментатора и его изобретательности”. Авторы провели огромную подготовительную работу по подбору сорбентов. Было опробовано много неорганических материалов, все они “едва сорбировали и не разделяли” катионы. Безуспешно проверили также сорбционные способности органических веществ – целлюлозы и бакелита. Из всех испытанных сорбентов ни один не показал лучшие свойства по сравнению с оксидом алюминия. Элюентом служила вода, для окрашивания использовали растворы азотной кислоты, гидроксида натрия, солей аммония, сульфидов в зависимости от разделяемой и определяемой пары катионов. Например, для ионов железа и уранила использовали ферроцианид калия. Была отмечена независимость удерживания катионов от анионного состава разделяемых веществ, исключение составляли случаи образования нерастворимых осадков в процессе элюирования. Также авторами было предложено использовать комплексообразование в качестве приема разделения неразделяемых пар катионов, когда в качестве элюирующего иона использовали аммоний или тартрат. Следует отметить, что именно этот подход будет использован химиками Ман-хэттенского проекта для разделения переходных элементов в середине 1940 гг. В общей сложности было проведено хроматографирование семнадцати катионов на основном оксиде алюминия, ряд удерживания выглядел следующим образом: As3+ > Sb3+ > Bi3+ > Cr3+ = Fe3+ = Hg2+ > ${\text{UO}}_{2}^{{2 + }}$ > > Pb2+ > Cu2+ > Ag+ > Zn2+ > Co2+ = Ni2+ = Cd2+ = = Fe2+ > Ti+ > Mn2+. Ион водорода занимает положение в начале этого ряда, что было доказано экспериментально измерением рН. Из этого был сделан вывод, что на кислом оксиде алюминия можно разделить анионы, как показала следующая работа Шваба с Гретель Даттлер [10]. Колон-ку с оксидом алюминия высотой 8 см и диаметром 5.3 мм заполняли раствором азотной кислоты, затем промывали водой. Небольшое количество смеси растворов солей щелочных металлов помещали в начало колонки и промывали ее водой; катионы не удерживались, двигаясь на-много быстрее анионов. Полученный ряд удер-живания анионов выглядел так: OH– > ${\text{PO}}_{4}^{{3 - }}$ > > F– > ${\text{Fe(CN)}}_{6}^{{4 - }}$ = ${\text{CrO}}_{4}^{{2 - }}$ > ${\text{SO}}_{4}^{{2 - }}$ > ${\text{Fe(CN)}}_{6}^{{3 - }}$ = = ${\text{C}}{{{\text{r}}}_{2}}{\text{O}}_{7}^{{2 - }}$ > Cl– > ${\text{NO}}_{3}^{ - }$ > ${\text{MnO}}_{4}^{ - }$ > ${\text{ClO}}_{4}^{ - }$ > ${\text{S}}_{2}^{ - }.$ Примечательна позиция ОН− вверху этого ряда. Для окраски бесцветных зон использовали ион серебра, который мигрирует сквозь кислую колонку быстрее, чем анионы, и окрашивает зону хлорида, что помогает детектированию. В случае фторида и сульфата наблюдался белый просвет между полосами на хроматограмме.
Авторы признавали, что полноценный количественный анализ при одновременном присутствии 5–6 ионов при таком хроматографировании невозможен, поскольку наблюдается одновременная сорбция нескольких ионов в одной полосе, их взаимодействие, а самое главное – сложно подобрать универсальный окрашивающий реагент. В заключении к данной работе авторы пишут: “Таким образом, механизм анионной хроматографии представляет собой обменную адсорбцию, полностью аналогичную отношениям, наблюдаемым для катионов. Аналитическое значение этих результатов для полного кислотного анализа неизвестных смесей может быть не столь велико из-за существования многих анионов, которые не окрашены …, однако метод применим как быстрое и удобное решение отдельных вопросов”.
Понимая важность проблемы количественного определения ионов, Шваб совместно с Гретель Даттлер [11] специально уделил все внимание ее решению. Авторы отмечают, что соотношение высот полос можно использовать только для грубой количественной оценки. Большая точность (в пределах нескольких процентов) достигается при строгом соблюдении методики и использовании колонки одинакового размера. В случае разделения катионов предпочтительно наличие одного аниона (желательно сульфата). Сорбент должен быть однороден по размеру частиц, колонка тщательно заполнена. Количественный анализ применили на ряде реальных образцов (латунь и разные монеты). Образцы перед анализом растворяли в азотной кислоте. Как пишут авторы, результаты вполне соответствовали ожиданиям.
Следует отметить, что во введении к этой работе Шваб ссылается на сборник 1938 г. на немецком языке “Физические методы в аналитической химии”, где он – автор раздела “Хроматография” [12]. Этот сборник был издан в трех томах. Первый том (“Спектроскопия и радиометрический анализ”) вышел в 1933 г., в нем предлагается использовать метод радиоактивных индикаторов в качестве высокочувствительного метода изучения явлений ионного обмена и адсорбции [13]. Отметим, что этот метод будет широко применяться в исследованиях 1940 гг. в рамках Манхэттенского проекта. Второй том издан в 1936 г., третий (включает раздел “Хроматография”) – в 1938 г. Была обнаружена реферативная статья, где сообщается о задержке выхода третьего тома в связи с тем, что “использование разработанных физических методов в целях аналитической химии потребовало расширения текущих планов. Это относится к вопросам органической и неорганической хроматографии…”. А в предисловии к третьему тому его редактор В. Бёттгер77 пишет: “Нет никаких сомнений в том, что физические методы открыли совершенно новые пути для аналитика, и это развитие вряд ли достигло своего конца” [12]. В реферативной статье на второй том отмечается, что данная серия должна стать настольной книгой химика-аналитика, поскольку “дает исчерпывающий обзор инструментария, который идеально приспособлен к мышлению химика; физику, с помощью которой химик может что-то сделать без особого знания, с акцентом на химическую проблему во всех важных местах” [14].
Четвертая статья Шваба (соавтор Амалендра Нараян Гош) [15] вышла под названием “Применение хроматографии в качестве вспомогательного метода качественного анализа” и скорее всего планировалась как завершающая. Это следует из вступления, где авторы пишут, что желают обобщить и уточнить предыдущие работы. В титуле статьи указано место работы Шваба в Пирее, Греция, куда он эмигрировал из-за преследования нацистов. В данной работе авторы попытались сочетать хроматографию с групповым окрашиванием для облегчения качественного и количественного анализа. Для идентификации пользовались визуальным методом. С сульфидом аммония разделяли следующие катионы: Fe3+, Cr2+, UO2+, Zn2+, Co2+, Ni2+, Mn2+, а с дихроматом калия – ионы свинца, серебра и таллия.
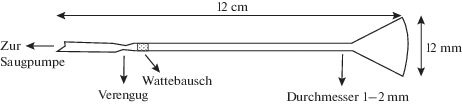
Годом позже (статья датирована 16.08.1939, но вышла в 1940 г.) была напечатана еще одна работа Шваба (совместно с А.Н. Гошем) под названием “Неорганическая хроматография как метод микроанализа” [16]. Авторы отмечают, что, перейдя от колонок диаметром 3–4 мм к колонкам диаметром 1–2 мм, добились существенного увеличения чувствительности анализа, к тому же из-за малых размеров колонок стали использовать микролитровые объемы образцов и реагентов. Как позже будет теоретически доказано, ширина колонки не оказывает влияния на разделение. В этой работе авторы впервые применили органические вещества, с оговоркой, что многие наиболее чувствительные органические реагенты не годятся для хроматографии из-за сильной сорбции на колонке или специальных условий для реакции с катионами (например, нагревания). Конструкция хроматографической колонки представлена на рис. 1.
Рис. 1.
Конструкция микроколонки для ионообменного разделения. Durchmesser – диаметр, Wattenbausch – ватный тампон, Verengung – сужение, Zug Saugpumpe – к вакуум-насосу (с немецкого) [16].
Ссылаясь на книгу Цехмейстера и Челноки [8], авторы обращают внимание, что при уменьшении диаметра колонки эффект неравномерности заполнения сорбентом проявляется все сильнее. По краям плотность меньше, чем в середине, соответственно и “сопротивление, испытываемое раствором вблизи стенки, меньше”; таким образом, “здесь адсорбируется больше катионов, чем в середине. … Для обнаружения в наших микротрубках это очень выгодно, так как, если смотреть со стороны, зоны кажутся шире…”. Авторы приводят условия разделения и визуализации девяти катионов с указанием цвета зоны и пределов обнаружения. Указаны также особенности хроматографирования пар катионов при разном соотношении концентраций, например пары железо(III)–медь(II). Микрограммовый уровень содержаний был вполне приемлем для разделения катионов этим методом. Отметим, что чувствительность этого метода достаточна, например, для определения меди в водопроводной воде. На то время, как отмечает Эттре, чувствительность этой методы была сравнима с чувствительностью капельного тест-метода [17].
Существует еще две работы 1942 г., выполненные Швабом совместно с Алисой Иссидоридис, не посвященные хроматографии, но тесно с ней связанные – в них изучено состояние соединений, адсорбированных на поверхности оксида алюминия. В частности, показано, что спектры отражения близки к спектрам основных солей, а не алюминатов, как предполагали вначале (цит. по [17]). В другой работе с тем же соавтором была обнаружена интересная реакция фотохимического взаимодействия: желтая полоса иона ${\text{UО }}_{2}^{{2 + }}$ становится коричневой при освещении белым светом, и в полосе обнаруживается пероксид водорода. Такое же явление они наблюдали на оксиде цинка в качестве адсорбента [18].
Последняя работа Шваба, полностью посвященная неорганической хроматографии (совместно с А.Н. Гошем), была опубликована в 1949 г. [19]. В конце статьи авторы пишут, что работа была на самом деле выполнена в 1938–1939 гг. в Мюнхенской лаборатории и в лаборатории Переи, со ссылкой на диссертацию Гоша. Нам удалось установить, что в 1942 г. нацисты, войдя в Грецию, лишили Шваба паспорта и запретили публиковаться в немецких журналах. В Германию он вернулся только в 1949 г. [2]. Также одной из вероятных причин появления этой публикации может быть серия публикаций американских авторов 1947 г. о применении хроматографии в Манхэттенском проекте. В этой работе Шваб и Гош пытались решить проблему разделения платиновых металлов, что было успешно сделано. Как уже было известно Швабу из первой работы с Джокерсом, ионы платиновых металлов должны располагаться между висмутом и железом. Смеси солей в виде хлоридов, приготовленные из руд, давали более десяти полос, поэтому авторы для их идентификации проводили хроматографирование отдельных чистых хлоридов. Наблюдались также большие осложнения с расположением зон вследствие гидролиза, комплексообразования и изменения валентности, особенно в случае Ru, Ir и Rh. Однако трудности были преодолены, и было показано, что ионы платиновых металлов могут быть хорошо разделены согласно ряду Ir–Pt–Pd–Rh, а также что их можно легко отделить от Cu, Ni, Zn и Pb, которые встречаются с ними в природе. Исключение составило железо. Для исследованных металлов не всегда было возможно подобрать подходящий краситель, поэтому помимо визуального определения по цвету полос выполняли идентификацию следующим образом: разрезали колонку по полосам, элюировали с сорбента раствором соляной кислоты, затем проводили термическое разложение хлоридов и по методу Дебая–Шеррера измеряли дифракцию рентгеновских лучей отдельных металлов, которые имеют различия порядка 0.04 Å. Кроме спектральных методов, применяли гравиметрический анализ фракций. Химики, позднее занимавшиеся ионообменным разделением платиновых металлов, не ссылались на эту работу Шваба [20].
Важным событием конца 1940 гг., объединившим химиков разных стан мира, работающих в области ионного обмена и аналитической химии, стало заседание Фарадеевского общества (Великобритания) в 1949 г., полностью посвященное применению хроматографии в аналитической химии. Этот форум собрал практически всех ведущих химиков в области хроматографии, присутствовал на нем с докладом о ионообменном разделении платиновых металлов и Георг-Мария Шваб. Отметим, что из 42 докладов форума 11 были посвящены ионообменной хроматографии [21].
НЕКОТОРЫЕ ПОСЛЕДОВАТЕЛИ Г.-М. ШВАБА
Ханс Эрленмейер с коллегами – комплексообразование как механизм разделения ионов. В те же годы, когда Шваб разрабатывал неорганическую ионообменную хроматографию, появились две работы Ханса Эрленмейера88 с коллегами из университета Базеля, посвященные хроматографическому разделению катионов для анализа сплавов.
В первой работе, сделанной совместно с Х. Даном [22], авторы, ссылаясь на Шваба, предлагают использовать 8-гидроксихинолин в качестве адсорбента, который также обладает способностью хроматографического разделения ионов, а кроме того, позволяет визуализировать хроматограмму. Использовали трубки длиной 5–8 см, внутренним диаметром 3 мм. В качестве сорбента применяли чистый порошковый 8-гидроксихинолин или смесь из 1–2 частей по массе кизельгура с одной частью 8-гидроксихинолина. Смесь более удобна в работе, так как “экономична, устойчива к промывке и обеспечивает лучшую “читаемость” хроматограммы”.
Подобно Швабу, который с К. Джокерсом предположил образование металл-алюминатов, Эрленмейер считает, что сорбция обусловлена образованием гидроксихинолинатов металлов, а порядок элюирования соответствует растворимости этих хелатов в воде, а также указывает, что при элюировании более “сильным” катионом полосы смещаются вниз по колонке. Элюирование проводили водой, порядок расположения зон на колонке сверху вниз был следующим: ${\text{VO}}_{3}^{ - }$ серо-черный > ${\text{WO}}_{4}^{{2 - }}$ желтый > Cu2+ зеленый > Bi3+ желтый > Ni2+ зеленый > Co2+ красный > Zn2+ желтый, интенсивная зеленая флуоресценция > > Fe3+ черный > UO2+ оранжевый. В заключении авторы полагают, что предложенный метод можно использовать для качественного (по цвету полосы) и количественного анализа при изучении некоторых сплавов. При этом авторы считали, что различия в произведениях растворимости 8-гидроксихинолинатов являются основным фактором разделения металлов на такой колонке. Однако, по мнению П.Н. Нестеренко, данная работа является первым примером комплексообразовательной жидкостной хроматографии [23].
Во второй работе [24], вышедшей в 1941 г., Х. Эрленмейер с В. Шоенауером применили в качестве сорбента виолуровую кислоту, которая образует сильно окрашенные соли со многими катионами. Именно возможность визуализации хроматограммы была основным фактором при выборе этого сорбента. Виолуровую кислоту смешивали с инертным носителем: “с диатомовой землей, сульфатом бария или, лучше всего, с крахмалом”, ее предлагалось также использовать и в чистом виде. Для разделения использовали колонки диаметром 3 и высотой 30 мм, разделяли смеси двух и более катионов. Для получения хорошо сформированных полос брали соли слабых кислот, например уксусной. При одновременном применении ацетатов K, Ca, Mg и Na образуются полосы хроматограммы: 1) К фиолетовый, 2) Ca красный, 3) Mg кирпично-красный, 4) Na красно-фиолетовый. Опять-таки ссылаясь на Шваба, авторы предлагали количественное определение по ширине полосы катиона: “Существует простая зависимость между длиной зоны и количеством примененных ионов, так что таким образом количественные определения проводятся как в макро-, так и в микрохимическом масштабе”.
Олоф Самуэльсон, “Ионообменные разделения в аналитической химии”. Шведский ученый Олоф Самуэльсон (1914–2000) – второй химик после Г.-М. Шваба, который на протяжении длительного времени занимался ионообменной хроматографией неорганических веществ и внес существенный вклад в ее развитие и популяризацию. Начиная с 1939 г. и до конца 1960-х гг. – активный период его научной деятельности в этой области; позднее Самуэльсон занялся разделением органических соединений.
Первая публикация Самуэльсона, связанная с применением ионного обмена в анализе, появилась в журнале “Zeitschrift für analytische Chemie” в 1939 г. (цит. по [20]). Она принесла Самуэльсону определенную известность, поскольку он предложил метод определения общей солевой концентрации – общей концентрации ионов в растворе солей. Метод заключается в алкалиметрическом титровании после предварительного обмена (в колонке с катионитом) катионов раствора на ионы водорода. Этим методом широко пользовались, например, для определения сульфат-иона в сульфате алюминия, нитрат-иона во взрывчатых веществах, общей концентрации оснований в кровяной сыворотке и т.п. Этот точный и экспрессный метод пригоден также для приготовления стандартных растворов в лаборатории. При этом отмечается, что растворимость солей не является обязательным условием анализа; достаточно, чтобы в воде растворялись соответствующие кислоты.
Будучи профессором химической технологии (engineering chemistry) Технического университета Чалмерса в Гётеборге, он написал монографию “Ионообменники в аналитической химии” [25]. Ее первое издание 1953 г. было переведено на русский язык и выпущено в 1955 г. под названием “Применение ионного обмена в аналитической химии”. Об этом издании в отечественном сборнике 1959 г. “Ионный обмен и его применение” пишет М.М. Сенявин – в будущем выдающийся ученый, специалист в области теории и практики ионного обмена: “Многочисленные примеры применения динамических ионообменных процессов для концентрирования и для разделения простейших смесей приведены в книге Самуэльсона”, сетуя, однако, что книга не освещает работы советских авторов.
Второе издание книги Самуэльсона (1963 г.) [26] появилось на русском языке в 1966 г. под оригинальным названием [20]. В обеих книгах отражено множество исследований автора, а также содержится обширная библиография работ других исследователей. Второе издание было существенно расширено работами автора, а также содержало информацию о вкладе советских химиков-аналитиков в эту область. В аннотации к русскому переводу отмечено: “Книга написана крупнейшим специалистом по применению ионного обмена в аналитической химии. … Значительная часть этих методов разработана самим автором. В книге использованы работы советских ученых. Книга предназначена для химиков-аналитиков, научных работников, аспирантов, преподавателей и лаборантов. Она может также служить пособием для студентов, специализирующихся по аналитической химии”. В предисловии редактора С.М. Черноброва Самуэльсон назван “пионером применения ионного обмена в неорганическом анализе”, хотя этого звания скорее заслуживает Г.-М. Шваб. Вероятно, так произошло потому, что, как верно отметил редактор, “наряду с работами многочисленных химиков в книге собраны работы самого автора, опубликованные преимущественно в малодоступных шведских журналах”. Как нами было показано, Шваб был последователен в утверждении своего приоритета и выстроил публикации как определенную стратегию, благодаря которой он закрепил свое имя как автора метода неорганической хроматографии, позже названной ионообменной.
Книги Самуэльсона представляли несомненную ценность для развития и становления ионообменной хроматографии как метода аналитической химии. Само построение и изложение материала в них сделано так, чтобы книга могла служить учебным пособием химика-аналитика. Лучше всего об этом пишет автор в предисловии ко второму изданию: “Некоторые типичные методы описаны детально для того, чтобы их мог использовать химик-аналитик, незнакомый с ионным обменом. Эти специфические примеры отобраны из числа методов, разработанных или испытанных в лаборатории автора”. Самуэльсон так очертил области применения ионного обмена и хроматографии в аналитической химии: определение общей солевой концентрации; отделение мешающих ионов противоположного знака заряда; отделение ионов от неэлектролитов; выделение следов веществ (концентрирование); разделение и селективное выделение целевых аналитов. Автор охарактеризовал особенности ионообменной хроматографии: “Ионообменная хроматография несколько сложнее, чем описанный ранее метод простого ионного обмена. При разделении смесей ионов с близкими свойствами часто требуется несколько часов или даже дней, чтобы достичь количественного разделения. Однако ионообменная хроматография легко поддается автоматизации, а поэтому может применяться даже для серийных анализов сложных смесей родственных веществ. … В органической химии ионообменная хроматография используется для разделения органических кислот, а также … для разделения аминокислот, пептидов и нуклеотидов. В настоящее время ионообменная хроматография является обычным методом в биохимических исследованиях; она используется также в качестве стандартного метода анализа в биохимической промышленности” [20].
В книге, посвященной 100-летию хроматографии, о работах Самуэльсона сказано следующее: “Он опубликовал 27 научно-исследовательских работ в период с 1939 по 1960 гг. преимущественно в скандинавских журналах, защитил диссертацию в 1944 г. … Его ранние исследования посвящены ионообменному разделению органических кислот, сахаров, альдегидов и кетонов, а также железа, алюминия от других катионов. В его двух книгах (1-я ред.1953 г., 2-я ред. 1963 г.), где описаны основы метода и его применения, цитируются все его работы до 1963 г. Его исследования после 1963 г. (около 240 статей) сосредоточены на ионообменной хроматографии органических кислот …” [27].
* * *
Таким образом, нами показано, что в период с 1936 по 1940 гг. Г.-М. Шваб с сотрудниками провел первые систематические исследования по разделению неорганических веществ методом ионообменной хроматографии и применению этого метода в неорганическом анализе. Бóльшая часть работ была посвящена катионам, одна работа посвящена разделению анионов. Для хроматографирования применяли оксид алюминия, для катионов – стандартизованный по Брокману, а для разделения анионов – промытый азотной кислотой. Данные работы показали применимость ионообменной хроматографии для разделения и количественной оценки ряда катионов и анионов. Швабом была показана возможность применения неорганической хроматографии для микроанализа. В публикации 1949 г. Шваб и Гош показали возможности ионообменной хроматографии для разделения ряда платиновых металлов. Идентификацию проводили визуально и по методу Дебая-Шеррера. Несмотря на узко практическую направленность работ и фактическое отсутствие теоретических обоснований наблюдаемых процессов, серия работ Шваба, безусловно, оказала огромное влияние на дальнейшее развитие хроматографии. Кроме того, мы показали активное участие Шваба в популяризации хроматографического метода, что прибавляет ему заслуг перед историей развития хроматографии. С работ Шваба и его коллег появилась и стала развиваться ионообменная хроматография, в первую очередь для целей анализа смесей катионов металлов и неорганических анионов. Ближайшими последователями Шваба были Эрленмейер с сотрудниками и Самуэльсон. Последний практически всю свою научную деятельность посвятил развитию и популяризации аналитической хроматографии. Следующим качественным скачком в истории ионообменной хроматографии после работ Г.-М. Шваба явились американские исследования времен Второй мировой войны. Этому этапу будет посвящена следующая публикация.
Фото 1.
Георг-Мария Шваб (Georg-Maria Schwab, 3.02.1899–23.12.1984) – немецкий физико-химик, пионер метода ионообменной хроматографии [1].

Список литературы
Traitteur H. In memoriam. Georg-Maria Schwab, 1899–1984 // J. Coll. Interface Sci. 1985. V. 106. № 1. P. 277.
Block J.H. Georg-Maria Schwab: Early endeavours in the science of catalysis / Springer Series in Surface Sciences. V. 5. Chemistry and Physics of Solid Surfaces VI / Eds. Howe R., Vanselow R. Berlin: Springer-Verlag, 1986. P. 1.
Рыбакова Е.В. Создание первых ионообменников и начало их широкого применения. // Сорбционные и хроматографические процессы. 2018. Т. 18. № 3. С. 443.
Schwab G.-M., Jochers K. Anorganische Chromatographie // Naturwissenschaften. 1937. V. 25. № 2. P. 44.
Гапон Т.Б., Гапон Е.Н. Хроматографический анализ ионов. II. Обменно-ионные хроматограммы Cu+2|Ni+2; Co+2|Ni+2 // Журн. аналит. химии. 1949. Т. 4. № 3. С. 131.
Мелешко В.П. К вопросу об обмене ионов на катионитовых смолах / Тр. Комиссии по аналит. химии АН СССР. М: Изд. АН СССР, 1955. Т. VI(IX). С. 306.
Schwab G.-M., Jockers K. Anorganische Chromatographie (I. Mitteilung). // Angewandte Chemie. 1937. V. 50. P. 546.
Zechmeister L., Cholnoky L. Die Chromatographische Adsorptionsmethode. Wien: Julius Springer, 1937. 231 p.
Schwab G.-M. Рецензия на книгу “Die Chromatographische Adsorptionsmethode”. Prof. L. Zechnieister und Dr. L. Cholnoky // Angewandte Chemie. 1938. V. 51. № 6. P. 98.
Schwab G.-M., Dattler G. Anorganische Chromatographie (II. Mitteilung) // Angewandte Chemie. 1937. V. 50. № 33. P. 691.
Schwab G.-M., Dattler G. Anorganische Chromatographie (III. Mitteilung) // Angewandte Chemie. 1938. V. 51. № 41. P. 709.
Schwab G.-M. Chromatographie / Physikalische Methoden in der analytischen Chemie. V. III: Chromatographie, Verdampfungsanalyse, Spektroskopie, Konduktometrie, Photoelektrometrie, Polarographie, Potentiometrie / Ed. Böttger W., 1938. P. 61.
Gerlach W. Peцeнзия нa “Physikalische Methoden in der analytischen Chemie”. V. I // Angewandte Chemie. 1934. V. 47. P. 11.
Thiessen. Peцeнзия нa “Physikalische Methoden in der analytischen Chemie”. V. II // Angewandte Chemie. 1937. V. 50. P. 39.
Schwab G.-M., Ghosh A.N. Anorganische Chromatographie (IV. Mitteilung) // Angewandte Chemie. 1939. V. 52. № 45. P. 666.
Schwab G.-M., Ghosh A.N. Anorganische Chromatographie (V. Mitteilung) // Angewandte Chemie. 1940. V. 53. P. 39.
75 years of chromatography – a historical dialogue / Eds. Ettre L.S., Zlatkis A. Amsterdam: Elsevier Scientific Publishing Company, 1979. V. 17.
Schwab G.-M., Issidoridis A. Über einen photochemischen Grenzflächenvorgang // Ber. Deut. Chem. Ges. 1942. V. 75. P. 1048.
Schwab G.-M., Ghosh A.N. Chromatographische Trennung und röntgenographische Identifizierung von Platinmetallen // Zeitschrift für anorganische Chemie. Mai 1949. V. 258. № 3–5. P. 323.
Самуэльсон О. Ионообменные разделения в аналитической химии. Ленинград: Химия, 1966. 416 с.
Chromatographic Analysis / Discussions of the Faraday Society. London: The Faraday Society, 1949. V. 7.
Erlenmeyer H., Dahn H. Beitrag zur chromatographischen Methode in der anorganischen Chemie // Helv. Chim. Acta. 1939. V. 22. P. 1369.
Нестеренко П.H., Джонc Ф., Полл Б. Высокоэффективная комплексообразовательная хроматография ионов металлов. М.: Техносфера, 2013. С. 18.
Erlenmeyer H., Schoenauer W. Zur Kenntnis der chromatographischen Methode in der anorganischen Chemie // Helv. Chim. Acta. 1941. V. 24. P. 878.
Samuelson O. Ion Exchangers in Analytical Chemistry. New York: John Wiley & Sons Inc., 1953. 291 p.
Samuelson O. Ion Exchange Separations in Analytical Chemistry. New York: Wiley, 1963. 474 p.
Chromatography: A Century of Discovery 1900–2000 / Eds. Gehrke Ch.W., Wixom R.L. Amsterdam: Elsevier Science B.V., 2001.
Дополнительные материалы отсутствуют.
Инструменты
Журнал аналитической химии


