Журнал аналитической химии, 2020, T. 75, № 12, стр. 1119-1128
Факторы, определяющие селективность неподвижных фаз к геометрическим изомерам жирных кислот в анализе методом газожидкостной хроматографии
А. М. Долгоносов a, *, Е. А. Зайцева a
a Институт геохимии и аналитической химии им. Вì.И. Вернадского Российской академии наук
119334 Москва, ул. Косыгина, 19, Россия
* E-mail: amdolgo@mail.ru
Поступила в редакцию 02.06.2020
После доработки 24.06.2020
Принята к публикации 03.07.2020
Аннотация
Рассмотрена весьма актуальная и сложная проблема хроматографического анализа пищевых продуктов на наличие вредных компонентов – транс-изомеров мононенасыщенных жирных кислот в присутствии избытка полезных цис-изомеров. Разделение веществ методом газожидкостной хроматографии осуществляется по двум механизмам, обеспечивающим различную селективность к геометрическим изомерам: путем адсорбции на плоской поверхности, дающей преимущество по энергии транс-изомерам, и за счет распределения в объеме фазы, приводящего к более сильному удерживанию цис-изомеров. Предложенная ранее теоретическая модель, объясняющая распределение адсорбата “поглощением” макромолекулой неподвижной фазы путем конформационной перестройки в процессе неспецифического взаимодействия, дополнена полярными взаимодействиями и водородной связью. Рассмотрены факторы, влияющие на селективность фазы к геометрическим изомерам. Проведен теоретический анализ экспериментальных данных и определены параметры неподвижных фаз, необходимые для повышения селективности разделения транс- и цис-изомеров сложных эфиров жирных кислот.
При маркировке пищевых продуктов проводят спецификацию по насыщенным, ненасыщенным компонентам жиров и отдельно по транс-изомерам мононенасыщенных жиров. Институт медицины США [1] установил, что не существует безопасного уровня потребления промышленных трансжиров из частично гидрогенизированных масел. Трансжиры, повышая уровень “плохого” холестерина, негативно влияют на целый ряд факторов риска сердечно-сосудистых заболеваний, в частности, приводят к гораздо большему риску развития ишемической болезни сердца, чем любой другой макрокомпонент. С 2003 г. Европейский союз и США придерживаются позиции по сокращению содержания трансжиров в продуктах питания [2–4].
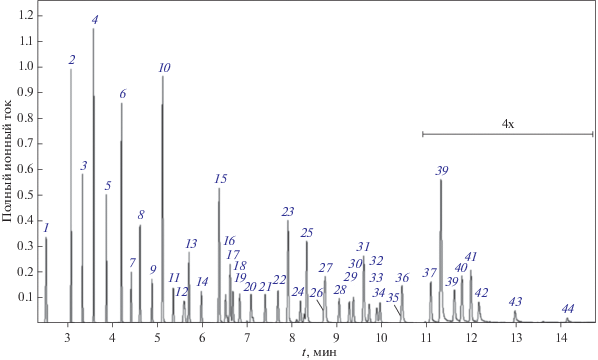
Определение методом газожидкостной хроматографии (ГЖХ) вредных трансжиров в продуктах питания весьма сложно из-за близости свойств транс- и цис-изомеров жирных кислот [5], точнее, их летучих дериватов – метиловых эфиров мононенасыщенных жирных кислот (МЭЖК), и требует особых хроматографических условий: использования очень длинных капиллярных колонок (60–100 м) и сильнополярных неподвижных фаз, состоящих, например, из цианоалкилсилоксанов [6, 7] или полиэтиленгликолей [8]. Порядок разделения изомеров МЭЖК имеет инверсный характер. В одних системах сначала выходит транс-изомер, а затем цис-изомер жирной кислоты [5–7, 9–13], в других системах порядок обратный [3, 8, 14]. В табл. 1 представлен ряд неподвижных фаз (НФ), применяемых для разделения цис- и транс-изомеров МЭЖК. Данные этой таблицы малоинформативны, тем не менее, они будут полезны при теоретическом анализе проблемы разделения изомеров МЭЖК. Более подробную информацию дает хроматограмма модельной смеси МЭЖК [13] (рис. 1), на которой видно разделение геометрических изомеров на колонке BPX-70 с содержанием 70% цианопропильных групп (ЦПГ) в полисилоксане (ПСО) (пары пиков 16, 17 и 19, 20 соответствуют изомерам МЭЖК 18 : 1 и 18 : 2 – выходят сначала транс-, затем цис-изомеры).
Таблица 1.
Коммерческие неподвижные фазы, разработанные для разделения цис- и транс-изомеров метиловых эфиров мононенасыщенных жирных кислот
| Название фазы | Состав | Порядок выхода изомеров | Литература |
|---|---|---|---|
| Supelco 2560 (SP-2560) | Бисцианопропил-полисилоксан | Транс-/цис- | [5, 7] |
| Rt-2560 | Бисцианопропил-полисилоксан | Транс-/цис- | [12] |
| BPX-70 | 70%-Бисцианопропил-30%-полифенилен-полисилоксан | Транс-/цис- | [11, 13] |
| Rtx-2330 | 90%-Бисцианопропил-10%-цианофенил полисилоксан | Транс-/цис- | [8] |
| HP-88 | 88%-Цианопропил-12%-арил полисилоксан | Транс-/цис- | [6] |
| VF-5 MS | 5%-Фенил-95%-диметил-полисилоксан | C18:1n-9 – транс-/цис-, C18:1n-12 – цис-/транс-; разделяет слабо, порядок выхода изомеров может меняться | [14] |
| Stabilwax (MXT-WAX) | ПЭГ | Цис-/транс- | [8] |
| FAMEWAX | ПЭГ | Цис-/транс- | [8] |
| Innowax column | ПЭГ | Цис-/транс- | [3] |
Рис. 1.
Хроматограмма стандартной смеси метиловых эфиров мононенасыщенных жирных кислот [13]. Условия эксперимента: колонка BPX-70 фирмы “SGE”, длина 100 м, диаметр 0.10 мм, толщина пленки 0.20 мкм, хроматограф GC-2010 с детектором GCMS-QP2010 (Shimadzu), газ-носитель – гелий с линейной скоростью 50 см/с, температурный градиент 50–250°С.
Разделяющая способность системы минимальна вблизи точки инверсии, которая обусловлена противоположными факторами; их одновременное действие делает большинство ГЖХ-систем не способными к разделению геометрических изомеров МЭЖК. Это означает, что в хроматографическом анализе смесей изомеров жирных кислот существует очень сложная проблема выбора разделяющей системы, для решения которой полезно было бы использовать теоретический анализ.
Инверсия селективности к изомерам обусловлена конкуренцией разных типов сорбции, которые проявляются в процессе удерживания молекулы аналита жидкой НФ как две стадии: адсорбция на поверхности и растворение в объеме фазы. Если взаимодействие ограничивается адсорбцией на поверхности фазы, то удерживание более плоских транс-изомеров оказывается сильнее, чем цис-изомеров (см. напр., [15]).
Вторая стадия играет заметную роль только в том случае, если при переходе молекулы от адсорбированного к растворенному состоянию энергия системы не растет [16]. В работах [17, 18] показано, что возможно не требующее затраты энергии растворение в виде “поглощения адсорбата макромолекулой”. Механизм поглощения заключается в изменении конформации макромолекулы под действием сил притяжения звеньев полимерной цепи к молекуле аналита с созданием вокруг нее полости. Степень завершения процесса зависит от продолжительности контакта молекулы аналита с отдельной молекулой поверхности фазы. Между тем, взаимодействие молекулы аналита с поверхностью фазы состоит из ряда последовательных контактов с отдельными молекулами, продолжительность которых сильно зависит от числа степеней свободы у молекулы в адсорбированном состоянии. Время одного контакта пренебрежимо мало, если молекула свободно перемещается вдоль поверхности; к росту этой величины приводят факторы, способствующие снижению числа степеней свободы движения, а в отсутствие поступательных свобод она становится равной всему периоду адсорбции, сопоставимому с временем релаксации макромолекулы. Таким образом, макромолекула способна окружить и захватить только ту молекулу аналита, которая при адсорбции теряет поступательные степени свободы.
Сорбция неплоской молекулы (например, в цис-конформации) по механизму поглощения макромолекулой энергетически выгодна из-за включения во взаимодействие с фазой тех ее электронов, которые при адсорбции оказываются удаленными от плоскости. Очевидно, что для этого нужна макромолекула, создающая гауссов клубок размером не меньше молекулы аналита. Это условие важно для ГЖХ-разделения геометрических изомеров. Поглощение макромолекулой более длинных транс-изомеров происходит в меньшей степени и поэтому удерживание цис-изомеров сильнее [18].
Итак, хроматографическое поведение геометрических изомеров зависит от механизма сорбции и имеет инверсный характер.
Настоящая работа посвящена описанию факторов, влияющих на характер сорбции, и поиску критериев выбора неподвижной фазы для хроматографического разделения геометрических изомеров МЭЖК.
ТЕОРЕТИЧЕСКАЯ ЧАСТЬ
Модель удерживания аналита включает следующие положения:
1. Поверхность полимерной фазы состоит из макромолекул, каждая из которых представляется гауссовым клубком. Реальную макромолекулу можно представить в виде цепи из свободно-сочлененных звеньев, приняв в качестве звеньев так называемые “куновские сегменты” [19].
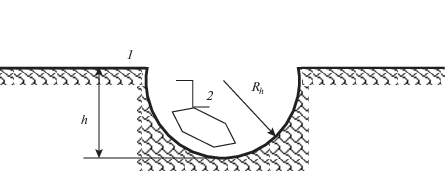
2. Взаимодействие характеризуется тремя процессами: а) адсорбцией на поверхности фазы; б) изменением ориентации звеньев макромолекулы при взаимодействии с молекулой аналита; в) образованием клубком полости вокруг молекулы (рис. 2), что ввиду свободного обмена между макромолекулами поверхности и внутренней части фазы приводит к растворению аналита (процесс поглощения аналита макромолекулой).
Рис. 2.
Модельные представления о геометрии поверхности фазы полимера 1 в месте фиксации молекулы аналита 2.
3. Возможно поглощение только тех молекул аналита, размеры которых не превышают внутренних размеров полости, создаваемой полимерным клубком.
4. При наличии поступательных степеней свободы адсорбированная молекула движется вдоль поверхности, меняя партнеров по контакту.
5. Макромолекула образует полость при условии $\tau _{A}^{'}\sim {{\tau }_{M}}$ (обозначения: $\tau _{A}^{'}( \leqslant {{\tau }_{A}})$ – длительность контакта адсорбированной молекулы с одной молекулой поверхности, ${{\tau }_{A}}$ – период адсорбции молекулы аналита, ${{\tau }_{M}}$ – длительность перестройки звеньев клубка при окружении молекулы).
6. Длительность перестройки звеньев макромолекулы вокруг молекулы аналита характеризуется временем релаксации клубка.
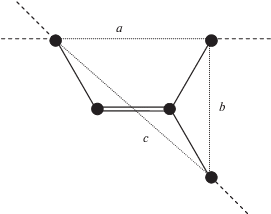
7. Описание удерживания геометрических изомеров МЭЖК имеет дополнения: а) адсорбция сопровождается образованием водородных связей; б) размеры геометрических изомеров различны: при прочих равных условиях длина цис-конформации меньше длины транс-конформации углеводорода на 0.101 нм (рис. 3).
Рис. 3.
Геометрическое построение для вычисления различия транс- и цис- конформаций мононенасыщенных углеводородов с двойной связью в средней части. Обозначения отрезков: $a = 0.284$ нм, $b = 0.260$ нм, $c = 0.385$ нм. Разность длин изомеров: $c - a = 0.101$ нм. Штриховыми линиями показаны оси молекул.
Критерий типа механизма сорбции молекул, являющийся отношением периода контакта к времени релаксации макромолекулы, $\zeta = {{\tau _{A}^{'}} \mathord{\left/ {\vphantom {{\tau _{A}^{'}} {{{\tau }_{M}}}}} \right. \kern-0em} {{{\tau }_{M}}}}{\text{,}}$ имеет вид [17]:
(1)
$\zeta \approx 0.0884{{\left( {\frac{{16\sqrt 3 {{K}_{A}}}}{{\pi {{R}_{M}}}}} \right)}^{{{{1 - s} \mathord{\left/ {\vphantom {{1 - s} 2}} \right. \kern-0em} 2}}}}{{\left( {\frac{{{{m}_{m}}}}{{{{m}_{M}}}}} \right)}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}},$(3)
${{K}_{A}} \approx \frac{{\sqrt \pi }}{{12}}\frac{{\left( {L + {{r}_{b}}} \right)\exp \left( {{{{{E}_{A}}} \mathord{\left/ {\vphantom {{{{E}_{A}}} {RT}}} \right. \kern-0em} {RT}}} \right)}}{{\sqrt {{{{{E}_{A}}} \mathord{\left/ {\vphantom {{{{E}_{A}}} {RT}}} \right. \kern-0em} {RT}}} }},$В случае если адсорбированная молекула имеет обе степени свободы ($s = 2$), то при подстановке $s = 2$ в уравнение (1) получим критерий $\zeta = 0.0884{{\left( {{{{{m}_{m}}} \mathord{\left/ {\vphantom {{{{m}_{m}}} {{{m}_{M}}}}} \right. \kern-0em} {{{m}_{M}}}}} \right)}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}} \equiv {{\zeta }_{0}}$ намного меньше 1, т.е. поглощение макромолекулой молекулы аналита, свободно передвигающейся вдоль поверхности жидкой фазы молекулы адсорбата не происходит. Механизм, характеризующийся критерием $\zeta \ll 1,$ приводящий к адсорбции молекулы на слабо искривленной (условно плоской) поверхности, назовем сорбцией типа “A” (adsorption).
Механизм сорбции, при котором молекула частично или полностью захватывается макромолекулой, способной перенести адсорбат с поверхности вглубь фазы, назовем сорбцией типа “B” (bulk sorption). Система “молекула аналита–макромолекула неподвижной фазы” моделируется полой сферой или ее сегментом, образованными звеньями макромолекулы, куда помещается молекула адсорбата (см. рис. 2). Радиус сферы (${{R}_{h}}$) определяется как разность размера клубка (${{R}_{M}}$) и ван-дер-ваальсовой толщины звеньев (${{r}_{b}}$):
Высота сферического сегмента связана с критерием $\zeta $ соотношением:
(5)
$h = \left\{ {\begin{array}{*{20}{c}} {2{{R}_{h}}\zeta ,}&{0 < \zeta \leqslant 1} \\ {2{{R}_{h}},}&{\zeta > 1} \end{array}} \right..$В зависимости от величины $\zeta $ можно говорить о разной степени искривления поверхности жидкой фазы в месте контакта с молекулой аналита: от малого прогиба (для $\zeta \ll 1$) до образования ($\zeta \sim 1$) и замыкания сферической полости вокруг молекулы ($\zeta \geqslant 1$).
Итак, для выполнения п. 5 модели требуется ограничение свободы поступательного движения адсорбата вдоль поверхности НФ. К такому ограничению приводит, например, наличие Н-связи. Необходимо выяснить: насколько значительным является этот эффект, достаточно ли для осуществления В-сорбции координации молекулы аналита по одной Н-связи или координационное число должно быть больше.
Адсорбция полярных молекул с участием Н-связи сопровождается удержанием молекулы адсорбата в той точке, где эта связь возникает. Число поступательных степеней свободы аналита на поверхности фазы прямо связано с долей ван-дер-ваальсовых взаимодействий в энергии адсорбции:
где ${{E}_{H}}$ – вклад водородных связей в энергию адсорбции. Условие $\tau _{A}^{'}\sim {{\tau }_{A}}$ требует, чтобы энергия Н-связи составляла существенную часть всей энергии адсорбции. Приняв в выражении (3) оценку $L + {{r}_{b}} \approx 0.75k{{l}_{c}},$ где $k\sim 10,$ найдем из формулы (1):(7)
$\zeta \approx {{\zeta }_{0}}{{\left( {{{{{k}^{2}}} \mathord{\left/ {\vphantom {{{{k}^{2}}} {{{N}_{c}}}}} \right. \kern-0em} {{{N}_{c}}}}} \right)}^{{{{{{E}_{H}}} \mathord{\left/ {\vphantom {{{{E}_{H}}} {2{{E}_{A}}}}} \right. \kern-0em} {2{{E}_{A}}}}}}}\exp \left( {{{{{E}_{H}}} \mathord{\left/ {\vphantom {{{{E}_{H}}} {RT}}} \right. \kern-0em} {RT}}} \right).$Ввиду малости величины ${{\zeta }_{0}}\sim {{10}^{{ - 2}}}$ для реализации В-сорбции представляет интерес уровень отношения ${\zeta \mathord{\left/ {\vphantom {\zeta {{{\zeta }_{0}}}}} \right. \kern-0em} {{{\zeta }_{0}}}}\sim {{10}^{{1.5}}}$ и выше.
Отношение энергии адсорбции к температуре ${{{{E}_{A}}} \mathord{\left/ {\vphantom {{{{E}_{A}}} {RT}}} \right. \kern-0em} {RT}}$ может быть оценено сверху из условий хроматографического эксперимента: во избежание слишком длительных экспериментов фактор удерживания не должен превышать 100 по порядку величины. Взяв логарифм фактора удерживания, получим ${{{{E}_{A}}} \mathord{\left/ {\vphantom {{{{E}_{A}}} {RT}}} \right. \kern-0em} {RT}} \leqslant 5.$ С другой стороны, логарифмируя выражение (7), получим нижнюю оценку:
(8)
$\begin{gathered} \frac{{{{E}_{H}}}}{{RT}} \approx \ln \frac{\zeta }{{{{\zeta }_{0}}}} + \frac{{{{E}_{H}}}}{{2{{E}_{A}}}}\ln \frac{{{{N}_{c}}}}{{{{k}^{2}}}} \approx \\ \approx \ln \frac{\zeta }{{{{\zeta }_{0}}}}\left( {1 + \frac{{RT}}{{2{{E}_{A}}}}\ln \frac{{{{N}_{c}}}}{{{{k}^{2}}}}} \right) \approx 3. \\ \end{gathered} $Так как ${{E}_{H}} < {{E}_{A}},$ то с учетом поправок получим интервал: $3 \leqslant {{{{E}_{H}}} \mathord{\left/ {\vphantom {{{{E}_{H}}} {RT}}} \right. \kern-0em} {RT}} \leqslant 4.$
В работе [22] получена оценка мольной энергии Н-связи через среднее число Н-связей на молекулу адсорбата ${{n}_{H}}$ в виде
(9)
${{E}_{H}} = 11.6{{n}_{H}},\,\,{{{\text{кДж}}} \mathord{\left/ {\vphantom {{{\text{кДж}}} {{\text{моль}}}}} \right. \kern-0em} {{\text{моль}}}},$Существует общее выражение для нижней границы вероятности Н-связи [23]:
(10)
${{n}_{{H12\min }}} = \frac{{\sqrt {{{Q}_{{am}}}{{Q}_{{dM}}}} + \sqrt {{{Q}_{{dm}}}{{Q}_{{aM}}}} }}{{2\sqrt {{{Q}_{m}}{{Q}_{M}}} }},$(11)
${{n}_{H}} = z{{n}_{{H12}}} \approx \frac{z}{2}{{\left( {\frac{{{{Q}_{{dM}}}}}{{{{Q}_{M}}}}} \right)}^{{{1 \mathord{\left/ {\vphantom {1 2}} \right. \kern-0em} 2}}}}.$Обобщенный заряд молекул в рассматриваемых здесь простых случаях задается формулой:
(12)
$Q = {{\left( {{{N}_{{\sigma }}} + {{N}_{{\pi }}}\sqrt 2 } \right)}^{{{3 \mathord{\left/ {\vphantom {3 4}} \right. \kern-0em} 4}}}},$(13)
${{r}_{s}} = 1.710e\sqrt {{{{{a}_{0}}} \mathord{\left/ {\vphantom {{{{a}_{0}}} {{{E}_{1}}}}} \right. \kern-0em} {{{E}_{1}}}}} $Существуют сильно гидрофильные НФ, у которых отношение ${{{{Q}_{{dM}}}} \mathord{\left/ {\vphantom {{{{Q}_{{dM}}}} {{{Q}_{M}}}}} \right. \kern-0em} {{{Q}_{M}}}}$ достаточно велико, чтобы согласно формуле (11) ${{n}_{H}}$ приближалось к верхнему пределу ${z \mathord{\left/ {\vphantom {z 2}} \right. \kern-0em} 2}.$ В случае ${{n}_{H}} \approx {z \mathord{\left/ {\vphantom {z 2}} \right. \kern-0em} 2}$ для применяемых при ГЖХ-определении жирных кислот температур 400–445 К величины ${{{{E}_{H}}} \mathord{\left/ {\vphantom {{{{E}_{H}}} {RT}}} \right. \kern-0em} {RT}}$ ≥ ≥ ${{11.6} \mathord{\left/ {\vphantom {{11.6} {3.7}}} \right. \kern-0em} {3.7}} \approx 3.1$ достигаются при $z = 2,$ т.е. при координации аналита с фазой двумя Н-связями. Поскольку аналит не имеет донорных групп, возникает требование, чтобы неподвижная фаза содержала пары донорных функциональных групп (типа гидроксильных, аминных или цианидных), расположенных не далее 0.4 нм друг от друга.
Итак, для искривления поверхности НФ под молекулой аналита в виде сферического сегмента с высотой порядка его радиуса кривизны $h \approx {{R}_{h}}$ ($\zeta \approx 0.5$), у молекулы МЭЖК должна быть возможность создавать с НФ не менее двух Н-связей. Это первое условие В-сорбции.
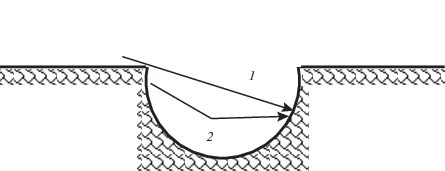
При В-сорбции, когда на поверхности фазы возникает полость высотой порядка радиуса кривизны, в которую помещается молекула (рис. 4), положение цис-изомера становится энергетически более выгодным, чем транс-изомера. Из рис. 4 видно, что параметры НФ, удовлетворяющие условию ${{L}_{{cs}}} < 2{{R}_{h}} < {{L}_{{tr}}}$ (диаметр полости больше длины цис-изомера и меньше длины транс-изомера), приводят к наилучшему разделению изомеров. Это второе условие В-сорбции. В силу статистического характера изучаемого явления получить полость с размерами в таком узком интервале крайне сложно. Тем не менее, если оставить в силе только нижний предел для диаметра полости, то эффект большей селективности НФ к цис-изомеру сохранится. При этом следует иметь в виду, что наиболее сильный эффект получим, когда диаметр полости превышает длину цис-изомера не более чем на 0.1 нм, однако он будет слабеть с ростом разности $2{{R}_{h}} - {{L}_{{tr}}}.$
Рис. 4.
Схема расположения транс- (1) и цис-конформаций (2) молекулы метилового эфира жирной кислоты с двойной связью в средней части в ямке на поверхности полимерной фазы. Стрелками показана точка крепления молекулы с помощью Н-связи.
Рассматривая энергию адсорбции изомеров как сумму вкладов полярной, неполярной энергии и водородных связей, найдем, что единственным существенным фактором, отличающим адсорбцию изомеров, является обобщенный заряд: величина ОЗ из-за эффекта экранирования сильно зависит от взаимного расположения молекулы адсорбата и макромолекулы НФ. На плоской поверхности различие электронных объемов у транс- и цис-конформаций возникает из-за инверсии положения одного атома C(sp2) относительно оси молекулы (см. рис. 3). При прочих равных условиях электрон атома водорода, связанного с таким атомом углерода, оказывается экранированным в цис-конформации, поэтому электронный объем у транс-изомера оказывается больше, чем у цис-изомера, на 1. Соответственно ОЗ цис-изомера меньше, а значит и его хроматографическое удерживание слабее, чем транс-изомера. Различие в селективности НФ с плоской поверхностью по отношению к изомерам ограничено указанной минимальной разностью электронных объемов, и с ростом длины молекул относительная селективность уменьшается. В этой связи рассмотренный механизм разделения на плоской поверхности (A-сорбция) имеет ограниченную перспективу в решении проблемы повышения селективности разделения цис- и трансжиров. Минимально необходимая степень разделения транс- и цис-изомеров длинных молекул при использовании А-сорбции достигается в хроматографической практике благодаря повышению эффективности разделяющей колонки путем ее удлинения до сотен метров [4, 9–11, 13], что сопровождается сильным увеличением продолжительности анализа.
Из рассмотрения возможных механизмов взаимодействия эфиров жирных кислот с макромолекулами НФ следует вывод о более сильном влиянии В-сорбции на селективность разделения геометрических изомеров, чем А-сорбции. Это обусловливает перспективность применения НФ, реализующих механизм В-сорбции, для определения содержания в пище трансжиров методом ГЖХ. Однако реализация эффекта В-сорбции для определения трансжиров затруднена требованием одновременного выполнения ряда условий. Во-первых, НФ должна иметь донорные группы, расположение и плотность размещения которых на поверхности допускают осуществление парной водородной связи с аналитом – сложным эфиром. Во-вторых, полимер, используемый в качестве НФ, должен создавать гауссов клубок, подходящий по размерам к размерам аналита при узком интервале отклонений.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Общая формула молекулы МЭЖК: ${{{\text{C}}}_{n}}{{{\text{H}}}_{{{\text{2}}n - {\text{1}}}}}{{{\text{O}}}_{{\text{2}}}}{\text{C}}{{{\text{H}}}_{{\text{3}}}}.$ Длина транс-изомера МЭЖК в наиболее выгодной распрямленной конформации без учета ван-дер-ваальсовых размеров (которые однократно учитываются для размеров полости) равна (нм): $\left[ {2 \times 0.11 + \left( {n + 1} \right) \times 0.15} \right] \times \sqrt {{2 \mathord{\left/ {\vphantom {2 3}} \right. \kern-0em} 3}} .$ Вычтя разность длин изомеров (0.1 нм), найдем длину цис-изомера:
Согласно формулам (2), (4) радиус полости, образуемой макромолекулой НФ равен:
Фазы, образующие с аналитом менее двух Н-связей. Рассмотрим пример полиэтиленгликоля (ПЭГ) массой 20 кДа (ПЭГ-20М). Куновский сегмент в условиях хроматографического эксперимента совпадает с мономером длиной 0.37 нм и массой 44 Да [25]. Радиус полости, образуемой звеньями ПЭГ-20М, равен 7.5 нм. Это очень большая полость, в которую могут поместиться молекулы, растянутые в транс-зигзаг, с углеродным числом 100 и более. Найдем массу ПЭГ, удовлетворяющие второму условию В-сорбции:
(16)
${{R}_{h}} \approx {{{{L}_{{cs}}}} \mathord{\left/ {\vphantom {{{{L}_{{cs}}}} 2}} \right. \kern-0em} 2}.$Подставив в выражение (16) формулы (14), (15), для массы полимера получим функцию:
Например, для МЭЖК с $n$ = 18 полость нужного радиуса создает молекула ПЭГ массой 765 Да. Однако у ПЭГ недостаточно донорных групп для образования требуемого количества (двух) Н-связей с аналитом, т.е. первое условие В-сорбции не выполняется, и поэтому в случае ПЭГ возможен только механизм А-сорбции. Ввиду инверсии селективности фаз, на которых осуществляются разные механизмы сорбции, ПЭГ-765 и близкие по массе НФ той же природы попадают в смешанную область неселективных фаз из-за низкой планарности поверхности. Гораздо лучшей поверхностью с точки зрения планарности, судя по полученным значениям радиуса кривизны, оказывается ПЭГ-20М, и ее можно использовать для варианта А-сорбции с большей селективностью к транс-изомерам.
Это теоретическое исследование объясняет селективность по отношению к геометрическим изомерам МЭЖК последних четырех фаз из табл. 1: ароматические фрагменты в VF-5 MS и Н-связывание с НФ на основе ПЭГ обеспечивают достаточную энергию межмолекулярного взаимодействия ${{E}_{A}},$ что в отсутствие фиксирующих контактов на достаточно плоской поверхности высокомолекулярных полимеров позволяет реализоваться варианту А-сорбции.
Фазы, образующие с аналитом две Н-связи. Перспективными из-за стойкости к высокой температуре представляются полисилоксановые фазы с цианопропильными группами, которые, благодаря эффектам таутомерии, являются донорами водородной связи. На рис. 5 показаны типичные варианты расположения ЦПГ в ПСО-фазах, в которых пары ЦПГ представлены в большинстве случаев, что обеспечивает регулярное образование парных Н-связей с молекулой МЭЖК, т.е. первое условие В-сорбции выполняется.
Из формулы полисилоксана со 100%-ным замещением цианопропильными группами (ПСО ЦПГ) следует выражение для массы N-звенного полимера: ${{m}_{M}} = {{m}_{2}} + {{m}_{1}}N,$ где ${{m}_{1}}$ – масса мономера (180 Да), ${{m}_{2}}$ – масса концевых остатков (162 Да). Куновский сегмент для ПСО в условиях хроматографического эксперимента соответствует двум мономерам, поэтому длина сегмента ${{l}_{c}} = 0.57$ нм, число сегментов${{N}_{c}} = {N \mathord{\left/ {\vphantom {N 2}} \right. \kern-0em} 2}.$
В табл. 2 приведены результаты расчета размера полости для ряда НФ из работы [26], представляющих собой ПСО ЦПГ.
Таблица 2.
Радиусы полости в полисилоксане со 100%-ным замещением цианопропильными группами различной молекулярной массы
| Неподвижная фаза | Число мономеров N | m1 | mM | ${{R}_{h}}$ по формуле (15) |
|---|---|---|---|---|
| A (Silar 10 C) | 22 | 180 | 4122 | 1.55 |
| B (Silar 10 C) | 56 | 180 | 10 242 | 2.68 |
| C (Silar 10 C) | 18 | 180 | 3402 | 1.37 |
| E (SP 2340) | 15 | 180 | 2862 | 1.22 |
| F (OV-275) | 12 | 166* | 2094 | 1.06 |
| G (Silar 9 CP) | 18 | 180 | 3402 | 1.37 |
| * Примечание: один из заместителей в мономере цианоэтильная группа. | ||||
Подставив формулы (14), (15) в уравнение (16) для второго условия В-сорбции, для массы ПСО ЦПГ, необходимой для того, чтобы цис-изомер МЭЖК помещался в полости НФ, запишем функцию:
В табл. 3 приведен теоретический прогноз по наиболее подходящим массам ПСО ЦПГ для разделения геометрических изомеров МЭЖК с радикалами С15…С18.
Таблица 3.
Массы полисилоксана со 100%-ным замещением цианопропильными группами, рассчитанные по формуле (17)
| Число атомов углерода кислоты n | Масса mM по формуле (17) | Ближайшая точная масса ПСО ЦПГ mM и число мономеров (N) |
|---|---|---|
| 15 | 2152 | 2142 (11) |
| 16 | 2334 | 2322 (12) |
| 17 | 2524 | 2502 (13) |
| 18 | 2722 | 2682 (14)–2862 (15) |
Таким образом, согласно теоретическому расчету оптимальными НФ для определения трансжиров в присутствии цис-изомеров являются ПСО ЦПГ с массами в диапазоне 2500–2800 Да. Полимеры с меньшими массами могут быть оптимальны для аналитов с меньшими молярными массами, однако их селективность по МЭЖК с радикалами С17, С18 заметно снизится из-за малого размера полости, не вмещающей не только транс-, но и цис-изомеры (из-за статистического разброса размеров селективность не будет резко снижаться).
Из экспериментальных данных, представленных в литературе, следует, что хорошими фазами для разделения геометрических изомеров жирных кислот С18 являются изученные в работе [26] НФ Е и F (см. табл. 2), молекулы которых содержат цепочки из 15 и 12 мономеров соответственно. Специально разработанные для определения геометрических изомеров фазы SP-2560 и Rt-2560 (см. табл. 1) по массе (2560 Да) максимально близки к теоретически найденным оптимальным значениям для разделения изомеров МЭЖК. Согласно каталогам [27–29] лучшими для разделения изомеров МЭЖК являются фазы SP-2380, SP-2560 (содержание ЦПГ 90% и выше). Колонки длиной 100 м с этими НФ разработаны специально для определения геометрических изомеров МЭЖК. В каталоге [29] указано, что разделение геометрических изомеров возможно и на колонках общего назначения с НФ SP-2330 и SP-2340, которые также являются ПСО ЦПГ с содержанием ЦПГ 80%. Однако отмечено, что разделение хуже, чем на колонках SP-2380 и SP-2560, из чего можно сделать следующие выводы: во-первых, от плотности расположения функциональных групп сильно зависит вероятность образования парных Н-связей с аналитом (теория указывает на квадратичную зависимость парной вероятности от содержания ЦПГ); во-вторых, вблизи массы 2722 Да ПСО ЦПГ обладает наилучшими параметрами для реализации картины В-сорбции, показанной на рис. 4, в применении к МЭЖК с радикалом С18. К значению 2722 наиболее близки массы макромолекул НФ с числами мономеров 14 и 15. Для молекул МЭЖК меньшей длины, определение которых также важно, нужны НФ меньшей массы в соответствии с данными табл. 3. Чем сильнее длина макромолекулы отличается от этих значений, тем ниже селективность соответствующих фаз к изомерам МЭЖК, обусловленная механизмом В-сорбции. Вывод проведенного здесь теоретического исследования о том, что оптимальными являются фазы с числами мономеров в узком интервале 13–15, хорошо согласуется с результатами, полученными экспериментально (N = 12–14).
* * *
Таким образом, изучено влияние на удерживание изомеров МЭЖК двух механизмов сорбции: адсорбции молекулы на плоской или слабо искривленной поверхности (А-сорбция) и механизма сорбции, при котором молекула частично или полностью захватывается макромолекулой, способной перенести адсорбат с поверхности вглубь фазы (В-сорбция). Сделан вывод о влиянии В‑сорбции, более сильном, чем А-сорбции, на селективность разделения геометрических изомеров, что делает перспективным применение НФ, реализующих механизм В-сорбции, для определения содержания в пище трансжиров методом ГЖХ. Трудность реализации эффекта В-сорбции для определения трансжиров связана с требованием одновременного выполнения следующих двух условий. Во-первых, НФ должна иметь донорные группы, расположение и плотность размещения которых допускают осуществление парной водородной связи со сложным эфиром. Во-вторых, полимер, используемый в качестве НФ, должен создавать гауссов клубок, подходящий по размерам к размерам аналита при небольшом интервале отклонений. В результате теоретических расчетов показано, что требуемые условия выполняются в случае использования в качестве НФ полисилоксанов с бисцианопропильными заместителями в узком интервале масс полимера 2500–2800 Да, что согласуется с опубликованными экспериментальными данными. Проведенный теоретический анализ дает возможность подбирать и разрабатывать наиболее подходящие фазы для целей ГЖХ-определения изомеров МЭЖК и для решения других подобных задач.
Работа выполнена при финансовой поддержке РФФИ (грант 18-03-00382а).
Список литературы
Libby P., Ridker P.M., Hansson G.K. Progress and challenges in translating the biology of atherosclerosis // Nature. 2011. V. 473. P. 317. https://doi.org/10.1038/nature10146
Liu A.G., Ford N.A., Hu F.B., Zelman K.M., Mozaffarian D., Kris-Etherton P.M. A healthy approach to dietary fats: Understanding the science and taking action to reduce consumer confusion // Nutr. J. 2017. V. 16. P. 53. https://doi.org/10.1186/s12937-017-0271-4
Méndez-Cid F.J., Centeno J.A., Martínez S., Carballo J. Changes in the chemical and physical characteristics of cow’s milk butter during storage: Effects of temperature and addition of salt // J. Food Compost. Anal. 2017. V. 63. P. 121. https://doi.org/10.1016/j.jfca.2017.07.032
Рудаков О.Б., Рудакова Л.В. Трансизомерные жирные кислоты: взгляд химика-аналитика // Переработка молока. 2019. № 3. С. 37.
Song, J., Park J., Jung J., Lee C., Gim, S. Y., Ka H., Lee J. Analysis of trans fat in edible oils with cooking process // Toxicol. Res. 2015. V. 31. № 3. P. 307. https://doi.org/10.5487/tr.2015.31.3.307
David F., Sandra P., Vickers Allen K. Column Selection for the Analysis of FAME. Application. USA: Agilent Technologies Inc., 2005. P. 12. https://www.agilent.com/cs/library/applications/5989-3760EN.pdf
Delmonte P., Kia A.-R.F., Hu Q., Rader J.I. Review of methods for preparation and gas chromatographic separation of trans and cis reference fatty acids // J. AOAC Int. 2009. V. 92. № 5. P. 1310. https://doi.org/10.1093/jaoac/92.5.1310
Rousova J., Konschnik J., Adams S., Sellers K., de Zeeuw J., English C. Analysis of trans-fatty acids in food products using various GC columns / Poster AOAC’S ANNUAL MEETING August 26–29, 2018. Toronto, Canada. https://www.restek.com/pdfs/aoac2018_jrfames_poster.pdf (20.05.2020).
Kiran C. Ravi, Reshma M.V., Sundaresan A. Separation of cis/trans fatty acid isomers on gas chromatography compared to the Ag-TLC method // Grasas y Aceites. 2013. V. 64. P. 95. https://doi.org/10.3989/gya.073312
Shantha N.C. Gas chromatography of fatty acids // J. Chromatogr. 1992. V. 624 P. 37.
Mjøs S.A., Pettersen J. Improved Methods for Analysis of Fatty Acid Isomers. Fyllingsdalen, Norway: SSF, 2001. 175 p.
Precht D., Molkentin, J. Fat composition of German human milk lipids // Nahrung. 1999. V. 43. № 4. P. 233.
Ecker J., Scherer M., Schmitz G., Liebisch G. A rapid GC-MS method for quantification of positional and geometric isomers of fatty acid methyl esters // J. Chromatogr. B. 2012. V. 897. P. 98. https://doi.org/10.1016/j.jchromb.2012.04.015
Dubois N., Barnathan G., Gouygou1 J.-P., Bergé J.-P. Research paper gas chromatographic behavior of fatty acid derivatives for mass spectrometry on low-polarity capillary columns // Eur. J. Lipid Sci. Technol. 2009. V. 111. P. 688.
Авгуль Н.Н., Киселев А.В., Пошкус Д.П. Адсорбция газов и паров на однородных поверхностях. М.: Химия, 1975. 384 с.
Симкин Б.Я., Шейхет И.И. Квантовохимическая и статистическая теория растворов. Вычислительные методы и их применение. М.: Химия, 1989. 256 с.
Долгоносов А.М., Прудковский А.Г. Механизм распределения в газо-жидкостной хроматографии, включающий эффект конформационной перестройки макромолекулы неподвижной фазы при контакте с молекулой адсорбата // Сорбционные и хроматографические процессы, 2010. Т. 10. № 6. С. 887.
Долгоносов А.М., Прудковский А.Г. Расчет эффекта конформационной перестройки макромолекулы неподвижной фазы при контакте с молекулой адсорбата // Сорбционные и хроматографические процессы. 2011. Т. 11. № 1. С. 23.
Гросберг А.Ю., Хохлов А.Р. Статистическая физика макромолекул. М.: Наука, 1989. 344 с.
Dolgonosov A.M. Calculation of adsorption energy and Henry law constant for nonpolar molecules on a nonpolar uniform adsorbent // J. Phys. Chem. B. 1998. V. 102. № 24. P. 4715.
Долгоносов А.М. Модель электронного газа и теория обобщенных зарядов для описания межатомных сил и адсорбции. М.: Книжный дом ЛИБРОКОМ, 2009. 176 с.
Долгоносов А.М. Представление о водородной связи, следующее из теории обобщенных зарядов // Журн. структ. химии. 2019. Т. 60. № 11. С. 1765. https://doi.org/10.26902/JSC_id46400
Долгоносов А.М. Универсальное соотношение для энергии и длины ковалентной связи, следующее из теории обобщенных зарядов // Журн. неорг. химии. 2017. Т. 62. № 3. С. 330. https://doi.org/10.7868/S0044457X17030060
Долгоносов А.М. Применение теории обобщенных зарядов для априорного расчета коэффициента поверхностного натяжения и критической температуры однородных неполярных жидкостей // Известия АН. Сер. хим. 2016. № 4. С. 952. (Dolgonosov A.M. Application of the Theory of generalized charges for a priori calculation of surface tension coefficient and critical temperature for uniform nonpolar liquids // Russ. Chem. Bull. V. 65. № 4. P. 952.)
Долгоносов А.М., Зайцева Е.А. Модель межмолекулярного взаимодействия с образованием водородной связи и ее применение для характеристики селективности хроматографических фаз на примере полиэтиленгликолей // Журн. структ. химии. 2020. Т. 61. № 9. https://doi.org/10.26902/JSC_id60676
Heckers H., Dittmar K., Melcher F.W., Kalinowski H.O. Silar 10 C, Silar 9 CP, SP-2340 and OV-275 in the gas-liquid chromatography of fatty acid methyl esters on packed columns: Chromatographic characteristics and molecular structures // J. Chromarogr. 1977. V. 13. № 5. P. 93.
https://srigc.com/cn/downloads/169/InTech-Stationary_phases.pdf (10.05.2020).
https://www.agilent.com/en/product/gc-columns/application-specific-gc-columns/select-fame-columns (10.05.2020).
http://www.supelco.com.tw/A-1%20%20%20207235% 20New.pdf (10.05.2020).
Дополнительные материалы отсутствуют.
Инструменты
Журнал аналитической химии