Журнал аналитической химии, 2020, T. 75, № 3, стр. 259-265
Определение антиоксидантной емкости объектов фармации потенциометрическим методом. Показатели точности измерений
А. В. Иванова a, *, Е. Л. Герасимова a, Е. Р. Газизуллина a, Д. С. Тимина a, Н. Л. Герасимова b, **, А. В. Собина b, Ж. В. Шалыгина a, М. П. Крашенинина b, ***
a Уральский федеральный университет имени первого Президента России Б.Н. Ельцина,
Химико-технологический институт
620002 Екатеринбург, ул. Мира, 19, Россия
b Уральский научно-исследовательский институт метрологии
620075 Екатеринбург, ул. Красноармейская, 4, Россия
* E-mail: a.v.ivanova@urfu.ru
** E-mail: lab223@uniim.ru
*** E-mail: krasheninina_m@uniim.ru
Поступила в редакцию 07.12.2018
После доработки 31.01.2019
Принята к публикации 04.10.2019
Аннотация
Исследована антиоксидантная емкость (АОЕ) водно-спиртовых настоек лекарственного растительного сырья, витаминов и витаминных комплексов. Определены показатели точности определения АОЕ указанных объектов, выполнен контроль точности результатов измерений с использованием образца аскорбиновой кислоты с известным содержанием основного компонента. Относительная погрешность измерений антиоксидантной емкости растительных и синтетических лекарственных препаратов не превышает 10%.
Антиоксидантные лекарственные препараты широко применяют в качестве основных средств терапии или как дополнительные средства коррекции при лечении атеросклероза, ишемической болезни сердца, остром нарушении мозгового кровообращения, воспалительных процессах, сахарном диабете, при широком круге заболеваний глаз и др. [1, 2]. Следует отметить, что в современной классификации лекарственных средств существует раздел: “Антигипоксанты и антиоксиданты” [3].
Применяемые в фармации природные антиоксиданты легко и органично вступают в метаболические процессы в организме и практически не дают побочных эффектов, присущих синтетическим препаратам [4]. Однако их состав невозможно регулировать, поэтому в современной терапии широкое применение нашли также различные витаминные препараты для профилактики и терапии многих системных заболеваний [5]. В связи с этим исследование лекарственных препаратов с антиоксидантными свойствами является актуальной задачей.
Существует большое число методов и подходов к определению антиоксидантов в различных объектах [6]. Согласно данным Федерального информационного фонда по обеспечению единства измерений (ФИФ ОЕИ), аттестованными методиками измерений содержаний веществ, обладающих восстановительными свойствами (т.е. характеризующихся антиоксидантной емкостью в растворах), являются, например, спектрофотометрический метод с использованием индикаторной системы на основе фенантролиновых комплексов железа, метод ВЭЖХ с УФ-детектированием, проточно-инжекционный метод с амперометрическим детектированием [7–9]. Пределы относительной погрешности при доверительной вероятности Р = 0.95 (значения расширенной неопределенности при коэффициенте охвата k = 2) указанных выше методик измерений содержания вещества колеблются от 5 до 34% в зависимости от применяемого метода, определяемого компонента (антиоксиданта) и диапазона его содержаний.
Данные подходы обладают рядом недостатков. Например, использование фенантролиновых комплексов железа возможно только в условиях кислых сред, в которых тиольные соединения (один из важнейших классов антиоксидантов) депротонированы и не вступают в химическую реакцию с комплексами железа. Применение спектрофотометрического метода ограничено для мутных и имеющих начальную окраску образцов. Общий недостаток всех перечисленных выше методов, в том числе хроматографического и амперометрического, – необходимость применения основы для сравнения – вещества с известным содержанием определяемого компонента (антиоксиданта), при этом стандартные образцы утвержденных типов с аттестованным значением массовой доли лекарственных препаратов – антиоксидантов в ФИФ ОЕИ отсутствуют. Интерпретация результатов и оценка погрешности получаемых результатов в этом случае будет затруднена. Как правило, при аттестации подобных методик измерений составляющая погрешности, связанная с неопределенностью массовой доли основного вещества в используемой основе для сравнения, не учитывается при оценке приписанной погрешности методики измерений. Это же касается и других методик измерений [10, 11], в основу которых положены методы, требующие применения в качестве основы для сравнения так называемых “чистых химических веществ” с фактически неизвестной массовой долей основного вещества. Кроме того, используемые в этих методиках средства измерений отличаются сложностью в эксплуатации и высокой стоимостью.
Окислительно-восстановительные превращения низкомолекулярных антиоксидантов, являющихся эффективными “перехватчиками” радикалов [12], сопровождаются переносом электрона. Следовательно, для их исследования целесообразно использовать электрохимические методы анализа. Электрохимические методы являются информативными, простыми, доступными и экспрессными и предполагают возможность исследования любых объектов, в том числе мутных и имеющих окраску.
В наших работах [13–15] исследованы модельные антиоксиданты, входящие в состав лекарственного растительного сырья и витаминных комплексов: полифенолы (флавоноиды и фенолкарбоновые кислоты), аскорбиновая кислота и их смеси. В данной работе исследована антиоксидантная емкость как интегральный параметр водно-спиртовых настоек лекарственного растительного сырья, поливитаминов и витаминных препаратов, определены показатели точности измерений. Использовали потенциометрический метод; в качестве модели окислителя применяли предварительно стандартизованный раствор гексацианоферрата(III) калия.
В качестве модели окислителя для потенциометрического определения антиоксидантной активности использовали окисленную форму железа в составе гексацианоферрата(III) калия [13–15]. Выбор гексацианоферрата(III) калия обусловлен тем, что это соединение удовлетворяет всем требованиям к окислителям, применяемым для корректного определения содержания антиоксидантов:
– гексацианоферрат(III) калия является окислителем средней силы (Е0 = 0.36 В), т.е. существует термодинамическая возможность протекания реакции окислителя с большинством антиоксидантов, обладающих низкими значениями потенциалов окисления. При этом отсутствует возможность взаимодействия гексацианоферрата(III) калия с соединениями, обладающими слабыми восстановительными свойствами и не относящимися к антиоксидантам;
– реакция гексацианоферрата(III) калия с антиоксидантами может быть реализована в условиях, близких к физиологическим, т.е. при pH ≈ 7 (значения условных констант устойчивости гексацианоферрата(III) калия и его восстановленной формы гексацианоферрата(II) калия при рН 7 значительно превышают значение 108);
– гексацианоферрат(III) калия является одноэлектронным акцептором электронов, его реакция с антиоксидантами протекает стехиометрично в соответствии с количеством функциональных групп, проявляющих антиоксидантные свойства, и полученные результаты выражаются в универсальных единицах измерения – моль-экв/л;
– скорость окислительно-восстановительной реакции гексацианоферрата(III) калия с антиоксидантами достаточно велика, чтобы обеспечить приемлемую продолжительность анализа (3–30 мин в зависимости от объекта исследования).
Потенциометрический метод измерений антиоксидантной емкости не требует применения стандартных образцов состава антиоксидантов. Средство измерений – рН-метр ЭКСПЕРТ-рН – выбрали, исходя из соображений соответствия измерительной задаче, достаточной точности измерений электродвижущей силы (ЭДС) и экономичности.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Средства измерений и реактивы. рН-метр ЭКСПЕРТ-рН (ООО “Эконикс-Эксперт”, Москва), зарегистрирован в Государственном реестре средств измерений (СИ) утвержденных типов (Госреестр СИ) РФ за № 29671-09, диапазон измерений ЭДС измерительным преобразователем от –2000 до +2000 мВ, предел допускаемой абсолютной погрешности измерений ЭДС ± 1.0 мВ. Использовали два экземпляра СИ (заводские №№ 1156, 1157). Электрод платиновый высокотемпературный ЭПВ-1 (ОАО “Гомельский завод измерительных приборов”, Гомель, Беларусь), зарегистрирован в Госреестре СИ РФ за № 2999-00. Электрод сравнения лабораторный ЭВЛ-1М4 (ОАО “Гомельский завод измерительных приборов”, Гомель, Беларусь), зарегистрирован в Госреестре СИ РФ за № 29896-11.
Гексацианоферрат(III) калия К3[Fe(CN)6] х. ч.; стандартный образец состава бихромата калия 1 разряда ГСО 2215-81, аттестованное значение массовой доли основного компонента 99.992%, расширенная неопределенность аттестованного значения 0.017% при коэффициенте охвата k = 2, границы абсолютной погрешности аттестованного значения ±0.019% при Р = 0.95; буферный раствор калия дигидрофосфата и натрия моногидрофосфата KH2PO4/Na2HPO4 ⋅ 12H2O с рН 7.41; аскорбиновая кислота (ОАО “Марбиофарм”, Йошкар-Ола, Россия), значение массовой доли аскорбиновой кислоты 99.63%, расширенная неопределенность приписанного значения составляет 0.25% при коэффициенте охвата k = 2 (образец для межлабораторных сличительных испытаний (МСИ) по определению показателей качества фармацевтической субстанции (кислота аскорбиновая), раунд МСИ 241-ЛА-1/2017), исследованный также с применением Государственного вторичного эталона единиц массовой доли и массовой (молярной) концентрации органических компонентов в жидких и твердых веществах и материалов на основе газовой и жидкостной хроматографии ГВЭТ 208-1-2016 [16].
Объектами исследования служили водно-спиртовые настойки боярышника (Crataegi tinctura), календулы (Calendulae tincturara), левзеи (Leuzeae extract fluid), семян лимонника (Tinctura Schizandrae chinensis), эхинацеи (Echinaceae tinctura), стручкового перца (Capsici annui tinctura), пиона уклоняющегося (Tinctura Paeoniae anomalae), родиолы розовой (Extractum Rhodiolae fluidum), валерианы (Tinctura Valerianae), мяты перечной (Tinctura Menthae piperitae). Содержание этанола в исследуемых настойках составляет 70–90%. Объем аликвоты 0.15–0.30 мл.
Также в качестве объектов исследования использовали витамины и витаминные комплексы в таблетках. Коммерческие витаминные препараты, активным компонентом которых является аскорбиновая кислота: аскорбиновая кислота в драже, аскорбиновая кислота с глюкозой и аскорбиновая кислота с декстрозой. Аскорбиновую кислоту в драже, аскорбиновую с глюкозой и аскорбиновую кислоту с декстрозой (100 мг) растворяли в воде. Общий объем каждого раствора составлял 15, 15 и 10 мл соответственно. Объем аликвоты 0.1 мл. Витаминные комплексы, составленные на основе А/С/Е-витаминов: Морской кальций, Перфектил. Морской кальций растворяли в смеси этанол–вода (1 : 1). Общий объем раствора составил 15 мл, объем аликвоты – 0.1 мл. При анализе Перфектила порошок из желатиновой капсулы растворяли в 15 мл смеси этанол–вода (1 : 2). Объем аликвоты составлял 0.05 мл.
Потенциометрический метод определения антиоксидантной емкости заключается в измерении потенциала платинового электрода после прохождения химической реакции между антиоксидантами исследуемого образца и окислителем (Е1), последующей добавке окислителя (в данной работе в качестве окислителя выбрали водный раствор гексацианоферрата(III) калия) и измерении установившегося потенциала (Е2) [13, 15]. Аналитическим сигналом служит разность потенциалов (∆Е = Е1 – Е2).
Потенциал изменяется в результате протекания химической реакции в растворе:
(1)
$n{{\left[ {{\text{Fe}}{{{\left( {{\text{CN}}} \right)}}_{6}}} \right]}^{{3 - }}}{\text{ + }}\,\,{\text{АО}} = n{{\left[ {{\text{Fe}}{{{\left( {{\text{CN}}} \right)}}_{6}}} \right]}^{{4 - }}}~ + \,\,{\text{А}}{{{\text{О}}}_{{{\text{Ox}}}}},$За счет избытка окислителя в системе после прохождения химической реакции с антиоксидантами устанавливается равновесие между окисленной и образовавшейся восстановленной формами – К3[Fe(CN)6]/К4[Fe(CN)6].
Антиоксидантную емкость в этом случае рассчитывают по формуле:
(2)
$\begin{gathered} {\text{AOЕ}} = \frac{{{{c}_{{{\text{Ox}}}}}(1 - b) - bc_{{{\text{Ox}}}}^{'}}}{{(1 - b)}}f, \\ b = {{10}^{{{{({{E}_{1}} - {{E}_{2}})nF} \mathord{\left/ {\vphantom {{({{E}_{1}} - {{E}_{2}})nF} {RT2.303}}} \right. \kern-0em} {RT2.303}}}}}, \\ \end{gathered} $Антиоксидантную емкость определяли в буферном растворе KH2PO4/Na2HPO4 ⋅ 12H2O с рН 7.4 при постоянном перемешивании. Процедура проведения измерений заключалась во внесении в электрохимическую ячейку, содержащую 0.3 ммоль/л К3[Fe(CN)6] в буферном растворе, аликвоты исследуемого образца и последующей добавке 1.5 мкмоль К3[Fe(CN)6] (0.1 мл 0.015 мМ раствора К3[Fe(CN)6]). Аликвоты образца подбирали, исходя из получаемой разницы потенциалов при введении добавки окислителя. Регистрируемая разность потенциалов должна превышать 20 мВ.
Стандартизация раствора гексацианоферрата(III) калия. Поскольку для количественного определения содержания антиоксидантов необходимо знать точное содержание окислителя, выполняли определение массовой доли К3[Fe(CN)6] методом иодометрического титрования по замещению с последующим титрованием выделившегося иода тиосульфатом натрия согласно ГОСТ 4206 [17]. Стандартизацию раствора тиосульфата натрия проводили по ГОСТ 25794.2 [18] с использованием стандартного образца состава бихромата калия 1 разряда ГСО 2215-81 с аттестованным значением массовой доли основного компонента 99.992 ± 0.019 %.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Гексацианоферрат(III) калия не относится к установочным веществам, хотя удовлетворяет большинству требований, предъявляемых к ним [19]. Массовая доля гексацианоферрата(III) калия, полученная методом иодометрического титрования по замещению с последующим титрованием выделившегося иода [17] предварительно стандартизованным тиосульфатом натрия согласно [18], составила 97.2 ± 0.6%. Данная поправка учтена в дальнейших измерениях для определения интегральной антиоксидантной емкости.
Определение антиоксидантной емкости водно-спиртовых настоек лекарственного растительного сырья, витаминных препаратов и витаминных комплексов. Описанным выше потенциометрическим методом исследовали антиоксидантную емкость водно-спиртовых настоек лекарственного растительного сырья.
На рис. 1 приведена зависимость потенциала от времени при введении 0.3 мл настойки боярышника в раствор, содержащий 0.3 ммоль/л K3[Fe(CN)6], и последующей добавке 1.5 мкмоль К3[Fe(CN)6] (0.1 мл 0.015 мМ раствора К3[Fe(CN)6]). Показатели точности полученных результатов оценены в соответствии с рекомендациями [20, 21]. Результаты определения АОЕ и оцененные показатели точности приведены в табл. 1. В табл. 2 представлены результаты определения АОЕ витаминных препаратов на основе аскорбиновой кислоты в водной среде и витаминных комплексов на основе А/С/Е-витаминов в водно-этанольной среде. Таким образом, исследовали антиоксидантную емкость водно-спиртовых настоек некоторых лекарственных растений (всего 10 видов), витаминных препаратов (3 вида) и витаминных комплексов (2 вида) потенциометрическим методом. Различия в значениях АОЕ водно-спиртовых настоек связаны с различным содержанием полифенольных соединений. Полученные значения АОЕ витаминных препаратов и витаминных комплексов коррелируют с суммарным содержанием аскорбиновой кислоты, ретинола и токоферола, заявленных производителем.
Рис. 1.
Зависимость потенциала от времени при введении 0.3 мл настойки боярышника в раствор, содержащий 0.3 ммоль/л K3[Fe(CN)6], и последующей добавке 1.5 мкмоль К3[Fe(CN)6] (0.1 мл 0.015 мМ раствора К3[Fe(CN)6]).
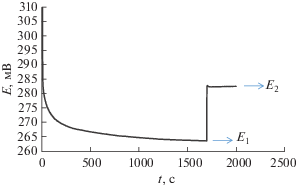
Таблица 1.
Результаты измерений и оцененные показатели точности измерений антиоксидантной емкости водно-спиртовых настоек некоторых лекарственных растений (n = 10, P = 0.95)
| Анализируемая настойка | АОЕ, ммоль-экв/л | ${{\sigma }_{r}}$, % | ${{\sigma }_{{{{R}_{L}}}}}$, % | $ \pm {{\delta }_{с}}$, % | $ \pm {{\delta }_{{}}}$, % | ±∆, ммоль-экв/л |
|---|---|---|---|---|---|---|
| Боярышника (Crataegi tinctura) | 1.06 | 5.3 | 5.3 | 3.3 | 9.9 | 0.11 |
| Календулы (Calendulae tincturara) | 0.866 | 4.2 | 4.2 | 1.8 | 8.4 | 0.073 |
| Левзеи (Leuzeae extract fluid) | 10.7 | 5.3 | 5.3 | 0.8 | 9.8 | 1.1 |
| Семян лимонника (Tinctura Schizandrae chinensis) | 0.863 | 3.1 | 3.1 | 0.7 | 6.1 | 0.052 |
| Эхинацеи (Echinaceae tinctura) | 2.59 | 4.7 | 4.7 | 1.4 | 9.2 | 0.24 |
| Стручкового перца (Capsici annui tinctura) | 0.173 | 5.1 | 5.1 | Незначима | 10 | 0.017 |
| Пиона уклоняющегося (Tinctura Paeoniae anomalae) | 3.351 | 1.0 | 1.0 | 0.1 | 2.0 | 0.067 |
| Родиолы розовой (Extractum Rhodiolae fluidum) | 27.3 | 2.2 | 2.2 | 1.4 | 4.6 | 1.3 |
| Валерианы (Tinctura Valerianae) | 0.597 | 2.4 | 2.4 | 0.3 | 4.7 | 0.028 |
| Мяты перечной (Tinctura Menthae piperitae) | 1.062 | 1.7 | 1.7 | 2.4 | 4.1 | 0.043 |
Обозначения: ${{\sigma }_{r}}$ – относительное среднеквадратичное отклонение повторяемости, %; ${{\sigma }_{{{{R}_{L}}}}}$ – относительное среднеквадратичное отклонение внутрилабораторной прецизионности, %; $ \pm {{\delta }_{с}}$ – границы относительной систематической погрешности при доверительной вероятности Р = 0.95, %; $ \pm {{\delta }_{{}}}$ – границы относительной погрешности при доверительной вероятности Р = 0.95, %; ± ∆ – границы абсолютной погрешности при доверительной вероятности Р = 0.95, ммоль-экв/л.
Таблица 2.
Результаты измерений и оцененные показатели точности измерений антиоксидантной активности витаминных препаратов и витаминных комплексов (n = 10, P = 0.95)
| Объект анализа | АОЕ, ммоль-экв/л | ${{\sigma }_{r}}$, % | ${{\sigma }_{{{{R}_{L}}}}}$, % | $ \pm {{\delta }_{с}}$, % | $ \pm {{\delta }_{{}}}$, % | ∆, ммоль-экв/л |
|---|---|---|---|---|---|---|
| АК* в драже | 3.86 | 2.8 | 2.8 | 0.4 | 5.5 | 0.21 |
| АК с глюкозой | 2.10 | 3.2 | 3.2 | 0.5 | 6.3 | 0.13 |
| Морской кальций | 0.971 | 4.9 | 4.9 | 0.4 | 9.6 | 0.093 |
| АК с декстрозой | 13.27 | 0.5 | 0.5 | 0.4 | 1.0 | 0.13 |
| Перфектил | 2.037 | 2.3 | 2.3 | 0.8 | 4.6 | 0.094 |
Контроль точности описанной потенциометрической методики измерения антиоксидантной емкости аскорбиновой кислоты. Для контроля точности описанной потенциометрической методики измеряли АОЕ аскорбиновой кислоты – образца для межлабораторных сличительных испытаний раунда МСИ 241-ЛА-1/2017 по определению показателей качества фармацевтической субстанции (кислота аскорбиновая) – с последующим пересчетом АОЕ в массовую долю аскорбиновой кислоты. Раунд МСИ 241-ЛА-1/2017 был проведен в 2017 г. аккредитованным провайдером МСИ ФГУП “УНИИМ” среди испытательных лабораторий, выполняющих контроль качества лекарственных средств. Всего в раунде приняло участие 35 лабораторий. Лаборатории определяли массовую долю аскорбиновой кислоты по титриметрическим и ВЭЖХ-методикам, изложенным в фармакопейных статьях. Значения массовой доли аскорбиновой кислоты и соответствующей ей расширенной неопределенности при коэффициенте охвата k = 2 были установлены провайдером МСИ по результатам раунда с использованием статистических подходов, изложенных в ГОСТ 13528 [22], и составили 99.63 и 0.25% соответственно.
Массовую долю аскорбиновой кислоты в образце для МСИ определяли на двух приборах два исполнителя (n = 10).
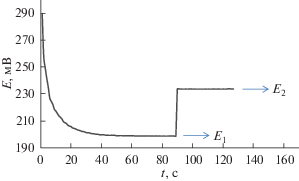
На рис. 2 представлена зависимость изменения потенциала от времени при введении 0.1 ммоль/л аскорбиновой кислоты в раствор, содержащий 0.3 ммоль/л K3[Fe(CN)6], и последующей добавке 1.5 мкмоль К3[Fe(CN)6] (0.1 мл 0.015 мМ раствор К3[Fe(CN)6]).
Рис. 2.
Зависимость потенциала от времени при введении 0.1 ммоль/л аскорбиновой кислоты в раствор, содержащий 0.3 ммоль/л K3[Fe(CN)6] и последующей добавке 1.5 мкмоль К3[Fe(CN)6] (0.1 мл 0.015 мМ раствора К3[Fe(CN)6]).
Аскорбиновая кислота при взаимодействии с гексацианоферратом(III) калия окисляется до дегидроаскорбиновой кислоты с передачей двух электронов [13–15]. Массовую доля аскорбиновой кислоты в образце определяли по формуле:
(3)
$W,~\% = {\text{АО}}{{{\text{Е}}}_{{{\text{AA}}}}}{{M}_{{1/z}}}{{V}_{{{\text{cell}}}}}\frac{{{{V}_{{{\text{cell}}}}}}}{{{{V}_{{{\text{al}}}}}}} \times {{100} \mathord{\left/ {\vphantom {{100} m}} \right. \kern-0em} m},$Массовая доля аскорбиновой кислоты в образце для МСИ, полученная по результатам пересчета АОЕ, составила 96.98%, что в пределах установленных границ относительной погрешности (см. табл. 2) хорошо согласуется со значением массовой доли аскорбиновой кислоты, установленным по результатам раунда МСИ 241-ЛА-1/2017 (99.63 ± 0.25 )%.
* * *
Таким образом, определены показатели точности потенциометрической методики измерения антиоксидантной емкости водно-спиртовых настоек лекарственных растений, витаминных препаратов и витаминных комплексов, выполнен контроль точности результатов с использованием образца аскорбиновой кислоты с известным содержанием основного компонента. Относительная погрешность измерения антиоксидантной емкости растительных и синтетических лекарственных препаратов не превышает 10%. Достигнутые показатели точности наряду с экспрессностью и простотой реализации позволяют рекомендовать потенциометрический метод измерения антиоксидантной емкости для внедрения в испытательные лаборатории, выполняющие контроль качества лекарственных препаратов по данному показателю.
Исследование выполнено при поддержке программы повышения конкурентоспособности (ППК) и Российского фонда фундаментальных исследований (проект РФФИ 19-29-08015).
Список литературы
Li C., Miao X., Li., Wang S., Liu Q., Wang Y., Sun J. Oxidative stress-related mechanisms and antioxidant therapy in diabetic retinopathy // Oxid. Med. Cell Longev. 2017. V. 11. P. 1
Окуневич И.В., Сапронов Н.С. Антиоксиданты: эффективность природных и синтетических соединений в комплексной терапии сердечно-сосудистых заболеваний // Обзоры по клинической фармакологии и лекарственной терапии. 2004. Т. 3. № 3. С. 2.
Машковский М.Д. Лекарственные средства. 16-е изд., перераб., испр. и доп. М.: Новая волна, 2012. С. 1216.
Nile S.H., Keum Y.S., Nile A.S., Jalde S.S., Patel R.V. Antioxidant, anti-inflammatory, and enzyme inhibitory activity of natural plant flavonoids and their synthesized derivatives // J. Biochem. Mol. Toxicol. 2018. V. 32. № 1. e22002.
Rembold C.M. Vitamin and antioxidant supplements do not prevent adverse cardiovascular events // Ann. Int. Med. 2013. V. 158. № 12. JC10.
Apak R., Gorinstein Sh., Böhm V., Schaich K.M., Özyürek M., Güçlü K. Methods of measurement and evaluation of natural antioxidant capacity/activity (IUPAC Technical Report) // Pure Appl. Chem. 2013. V. 85. № 5. P. 957.
Свидетельство №310354-0019/2015. Методические указания по определению массовой доли антиоксидантов в кормовых добавках методом высокоэффективной жидкостной хроматографии. № МУ А-1/035 / Федеральный информационный фонд по обеспечению единства измерений: информ.-справочный портал. М., 2019. https://fgis.gost.ru/fundmetrology/registry/16/items/298646 (03.10.2019).
Свидетельство № 08-47/275-01.00143.2008. Спектрофотометрический метод измерений антиоксидантной активности пищевых продуктов. МУ 08-47/275 / Федеральный информационный фонд по обеспечению единства измерений: информ.-справочный портал. М., 2019. https://fgis.gost.ru/fundmetrology/registry/16/items/286638 (03.10.2019).
Свидетельство № 001-130-2006 ГСИ. МВИ массовой концентрации водорастворимых антиоксидантов в биологически активных добавках, растительных экстрактах, напитках и пищевых продуктах амперометрическим способом / Федеральный информационный фонд по обеспечению единства измерений: информ.-справочный портал. М., 2019. https://fgis.gost.ru/fundmetrology/registry/16/items/292893 (03.10.2019).
Polak J., Bartoszek M. A new equation for converting the parameter EC50 into the total antioxidant capacity TEAC and vice versa // Food Chem. 2017. V. 248. P. 46.
Rodriguez-Bonilla P., Gandia-Herrero F., Matencio A., Garcia-Carmona F., Lopez-Nicolas J. Comparative study of the antioxidant capacity of four stilbenes using ORAC, ABTS(+), and FRAP techniques // Food Anal. Methods. 2017. V. 9. № 10. P. 2994.
Tinkel J., Hassanain H., Khouri S.J. Cardiovascular antioxidant therapy: a review of supplements, pharmacotherapies, and mechanisms // Cardiol. Rev. 2012. V. 20. № 7. P. 77.
Иванова А.В., Газизуллина Е.Р., Попова К.Г., Матерн А.И. Исследование антиоксидантной активности и суммарного содержания полифенолов лекарственного растительного сырья // Журн. аналит. химии. 2017. Т. 72. № 4. С. 363. (Ivanova A.V., Gerasimova E.L., Gazizullina E.R., Popova K.G., Matern A.I. Study of the antioxidant activity and total polyphenol concentration of medicinal plants // J. Analyt. Chem. 2017. V. 72. № 4. P. 363.)
Ivanova A.V., Gerasimova E.L., Brainina Kh.Z. Potentiometric study of antioxidant activity: development and prospects // Crit. Revs. Analyt. Chem. 2015. V. 45. № 4. P. 311.
Иванова А.В., Герасимова Е.Л., Кравец И.А., Матерн А.И. Потенциометрическое определение водорастворимых антиоксидантов с использованием комплексов металлов // Журн. аналит. химии. 2015. Т. 70. № 2. С. 156. (Ivanova A.V., Gerasimova E.L., Kravets I.A., Matern A.I. Potentiometric Determination of water soluble antioxidants using metal complexes // J. Analyt. Chem. 2015. V. 70. № 2. P. 173.)
Шохина О.С., Медведевских М.Ю., Крашенинина М.П., Макарова С.Г., Крылов А.И., Ткаченко И.Ю., Михеева А.Ю. Разработка Государственного вторичного эталона и стандартных образцов состава на основе жидкостной и газовой хроматографии // Стандартные образцы. 2017. Т. 13. № 1. С. 9.
ГОСТ 4206-75 Калий железосинеродистый. Технические условия (с Изменением № 1). М.: Издательство стандартов, 1993. 9 с.
ГОСТ 25794.2-83 Реактивы. Методы приготовления титрованных растворов для окислительно-восстановительного титрования. М.: Стандартинформ, 2008. 9 с.
Основы аналитической химии. Учебник для ВУ-Зов. В 2-х кн. / Под ред. Золотова Ю.А. Изд. 2‑е, перераб. и доп. М.: Высшая школа, 2002. 494 с.
РМГ 61-2010. Государственная система обеспечения единства измерений. Показатели точности, правильности, прецизионности методик количественного химического анализа. Методы оценки. М.: Стандартинформ, 2013. 62 с.
ГОСТ Р ИСО 5725-4-2002. Точность (правильность и прецизионность) методов и результатов измерений. Часть 4. Основные методы определения правильности стандартного метода измерений. М.: Стандартинформ, 2009. 36 с.
ГОСТ Р ИСО 13528-2010. Статистические методы. Применение при экспериментальной проверке компетентности посредством межлабораторных сравнительных испытаний. М.: Стандартинформ, 2012. 54 с.
Дополнительные материалы отсутствуют.
Инструменты
Журнал аналитической химии


