Журнал аналитической химии, 2021, T. 76, № 10, стр. 916-926
Сорбенты на основе диоксида титана для гидрофильной хроматографии
А. С. Попов a, Е. А. Царенко a, А. В. Чернобровкина a, *
a Московский государственный университет имени М.В. Ломоносова, химический факультет
119991 Москва, Ленинские горы, 1, стр. 3, Россия
* E-mail: chernobrovkina@analyt.chem.msu.ru
Поступила в редакцию 05.04.2021
После доработки 22.04.2021
Принята к публикации 22.04.2021
Аннотация
Получены неподвижные фазы на основе диоксида титана путем адсорбционного закрепления полиэтиленимина с последующим сшиванием 1,4-бутандиолдиглицидиловым эфиром. Хроматографические свойства сорбентов изучены с помощью теста Танака для гидрофильных неподвижных фаз и на примере разделения модельной смеси водорастворимых витаминов группы В. Показано, что варьирование количества реагентов на стадии синтеза неподвижной фазы влияет на структуру функционального слоя и тем самым позволяет получить сорбент с улучшенными хроматографическими характеристиками.
Гидрофильная хроматография (ГИХ) представляет собой современный высокоэффективный метод определения полярных веществ на полярных сорбентах [1]. Благодаря альтернативной селективности ГИХ позволяет избежать традиционных для обращенно-фазовой ВЭЖХ проблем, связанных со слабым удерживанием полярных аналитов и недостаточной эффективностью, а также обеспечивает лучшую растворимость аналитов в подвижной фазе по сравнению с нормально-фазовой (НФ) ВЭЖХ [2].
В настоящее время выбор сорбентов для работы в режиме ГИХ достаточно широк, при этом большинство существующих фаз производится на основе силикагеля [1]. Очевидно, что ограниченный рабочий диапазон рН таких фаз (3–7) существенно ограничивает возможности метода, поскольку выбор подвижной фазы также в значительной степени определяет селективность ГИХ, влияя на состояние поверхности сорбента и аналита [3]. Неорганические основные оксиды металлов, такие как диоксид титана, гидролитически существенно более устойчивы (рН 1–13), и поэтому перспективны в качестве матриц сорбентов для ГИХ.
Диоксид титана обладает иными свойствами поверхности по сравнению с силикагелем и обеспечивает высокую эффективность и другую селективность разделения полярных веществ благодаря возможности катионо-, анионо- и лигандообменных взаимодействий с аналитами. Ранние исследования хроматографических свойств оксидов металлов, в том числе и диоксида титана, в период до 1980-х годов [4–6] были посвящены решению частных прикладных вопросов, таких как экспрессное определение чистоты некоторых стероидов или определение комплексов урана в сточных технологических водах, однако влияние природы таких сорбентов на их хроматографические параметры не изучали. В 1990 г. [7] и позже появились работы, посвященные использованию диоксида титана в качестве сорбента в режиме НФ ВЭЖХ [8], а также изучению его ионообменных [9, 10] и лигандообменных [11–13] свойств. Было отмечено, что в ряде случаев разделяющая способность диоксида титана значительно превосходит таковую для силикагеля.
Первая работа по изучению хроматографических свойств диоксида титана в режиме ГИХ [14] (2008 г.) посвящена разделению нуклеотидов и их интермедиатов. Авторы подробно изучили влияние доли ацетонитрила, концентрации и природы буферного раствора в составе подвижной фазы на хроматографическое поведение аналитов. Показано, что высокое содержание ацетонитрила (больше 50%) способствует реализации механизма ГИХ, обеспечивая лучшие селективность и эффективность [15].
В это же время были опубликованы работы [16, 17], описывающие хроматографическое поведение оснований нуклеиновых кислот и производных пурина на диоксиде титана в режиме ГИХ. Подробно изучено влияние способности аналитов образовывать хелатные комплексы с поверхностью диоксида титана на их удерживание в гидрофильном режиме. Особый интерес представлял вопрос о влиянии природы органического растворителя в составе подвижной фазы. Установлено, что при использовании подвижной фазы ацетонитрил–вода только вода действует в качестве лиганда, который может конкурировать с определяемыми компонентами при содержании менее 70% ацетонитрила в элюенте. Однако при содержании ацетонитрила более 80% удерживание модельных веществ резко возрастает, поскольку содержание воды недостаточно для конкуренции с разделяемыми веществами.
В последующие годы благодаря этим первым работам [14–17] по применению диоксида титана в ГИХ решено немало прикладных задач. Так, в работе [18] предложен простой и быстрый метод определения копростанола и холестерина в образцах сточных вод без какой-либо химической обработки образцов менее чем за 10 мин на колонке с диоксидом титана с использованием подвижной фазы ацетонитрил–вода (9 : 1 по объему). Благодаря комплексному удерживанию полярных аналитов на поверхности диоксида титана за счет гидрофильных и лигандообменных взаимодействий разработана методика определения витамина В1 в фармацевтических и биогенных объектах без использования ион-парных реагентов [19]. В исследовании [20] выявлена структурная селективность диоксида титана в режиме ГИХ по отношению к моно- и диметилированным ксантинам, отсутствующая у силикагеля и оксида циркония.
Лишь единичные публикации посвящены модифицированию поверхности диоксида титана с целью улучшения хроматографических свойств материала. Так, одной из первых является работа [21] Фреда Ренье 1986 г., в которой описаны новые сорбенты на основе неорганических оксидов, покрытых полиэтиленимином (ПЭИ). Модифицирование проводили в два этапа по методике [22], адаптированной под новые матрицы: адсорбционное закрепление ПЭИ и последующее сшивание 1,4-бутандиолдиглицидиловым эфиром (1,4-БДДГЭ). Показано, что химический состав матрицы сорбента мало влияет на эксплуатационные характеристики покрытия.
Нанесение полимерного слоя на поверхность оксида титана успешно применено в работе [23], посвященной использованию капилляра с диоксидом титана, покрытым политетрагидрофураном, для микроэкстракции в онлайн-сочетании с ВЭЖХ. Такие капилляры, помимо высокой гидролитической стабильности, продемонстрировали способность обеспечивать одновременную экстракцию неполярных полициклических ароматических углеводородов, умеренно полярных кетонов и полярных фенолов, спиртов и аминов из одного и того же образца с пределами обнаружения на уровне нг/л без предварительной обработки образца.
Таким образом, диоксид титана демонстрирует иную селективность по сравнению с силикагелем благодаря возможности вступать в ионо- и лигандообменные взаимодействия. Механическая прочность и гидролитическая стабильность TiO2 позволяет работать во всем диапазоне pH подвижной фазы, что является ключевым фактором влияния на селективность и эффективность в режиме ГИХ. Именно поэтому диоксид титана представляется перспективной матрицей для получения гидрофильных сорбентов.
Цель работы – получение сорбентов путем покрытия частиц диоксида титана различным количеством полиэтиленимина с последующей сшивкой 1,4-бутандиолдиглицидиловым эфиром, установление их хроматографических характеристик в режиме ГИХ, а также оценка влияния толщины функционального слоя полиэтиленимина и количества сшивающего агента 1,4-БДДГЭ на их хроматографические свойства на примере объектов теста Танака для гидрофильных неподвижных фаз и водорастворимых витаминов.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Приборы и материалы. Использовали: рибофлавин, пиридоксина гидрохлорид, цианокобаламин, аскорбиновую кислоту, тиамин, аденозин, урацил, теобромин, теофиллин, уридин, видарабина моногидрат, 5-метилуридин, 2'-деоксиуридин, N,N,N-триметилфениламмония хлорид, тозилат натрия (>98.0%, TCI, Япония); никотинамид, кислоту никотиновую, полиэтиленимин с Mw 800, 1,4-бутандиолдиглицидиловый эфир (>98%, Sigma-Aldrich, США); толуол х. ч. (Компонент-Реактив, Россия); ацетонитрил HPLCgradientgrade (Panreac, Германия); кислоту уксусную ледяную 99.5%, кислоту ортофосфорную 85% х. ч., хлорид калия ч. д. а. (Panreac, Испания); этанол ч. д. а., ацетат аммония ч. (Лабтех, Россия); ацетон ч. д. а. (ХимМед, Россия); 1,4-диоксан ч. д. а. (Компонент-Реактив, Россия).
Для синтеза сорбентов использовали диоксид титана двух полиморфных модификаций: рутил (размер частиц <5 мкм; Sigma-Aldrich/Merck Millipore, США) и анатаз (размер частиц 5 мкм, размер пор 100 Å; Sachtopore®-NP, Sachtleben Chemie GmbH/ZirChrom Separations, Германия); силикагель Kromasil SIL (размер частиц 5.0 мкм, размер пор 100 Å; Nouryon, Швеция).
Эксперименты проводили с помощью системы ВЭЖХ, состоящей из хроматографа Dionex 3000 с двухканальным градиентным насосом, автоматической системой ввода пробы, термостатом колонок и детектором на диодной матрице. Объем вводимой пробы составлял 20 мкл, концентрации индивидуальных витаминов – от 2 до 100 мг/л, фон пробы соответствовал составу подвижной фазы. Для регистрации хроматограмм использовали программный пакет Chromeleon 7 (Thermo Fisher Scientific, США).
Для проведения синтеза применяли следующее оборудование: термостат (Memmert, Германия), вакуумный насос серии Laboport (KNF Neuberger, Германия), механическую мешалку Eurostar (IKA-Werke, Германия). В работе использовали стальные колонки размером 100 × 3 мм, которые заполняли с помощью пневмонасоса Knauer K-1900 (Knauer, Германия).
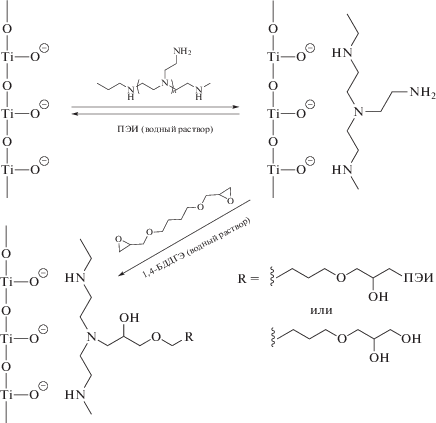
Синтез сорбентов и заполнение хроматографических колонок. Навеску диоксида титана помещали в плоскодонную колбу емк. 100 мл, добавляли полиэтиленимин, растворенный в 40 мл деионизованной воды, и перемешивали полученную суспензию на орбитальном шейкере в течение 30 мин. Полученный продукт отфильтровывали под вакуумом на стеклянном пористом фильтре, промывали деионизованной водой, после чего сушили на воздухе. Далее продукт помещали в круглодонную колбу емк. 100 мл и добавляли 1,4-БДДГЭ, растворенный в 40 мл деионизованной воды. Реакционную смесь перемешивали в течение 30 мин со скоростью 650 об/мин при 60°С. Схему синтеза иллюстрирует рис. 1. Готовый сорбент отфильтровывали под вакуумом на стеклянном пористом фильтре, промывали деионизованной водой, после чего сушили на воздухе. Количества реагентов, их соотношение и обозначения новых сорбентов приведены в табл. 1.
Таблица 1.
Условия получения новых сорбентов
| Сорбент | m(TiO2), г | m(ПЭИ), г | V(1,4-БДДГЭ), мл |
|---|---|---|---|
| T-ПЭИа-Б (T-1.0×ПЭИа-1.0×Б) | 2.00 | 2.00 | 2.0 |
| T-ПЭИа-0.1×Б | 2.00 | 2.00 | 0.2 |
| T-ПЭИа-0.3×Б | 0.6 | ||
| T-ПЭИа-0.5×Б | 1.0 | ||
| T-ПЭИа-0.7×Б | 1.4 | ||
| T-ПЭИа-1.5×Б | 3.0 | ||
| T-0.1×ПЭИа-Б | 1.50 | 0.15 | 1.5 |
| Т-0.5×ПЭИа-Б | 0.75 | ||
| T-1.5×ПЭИа-Б | 2.25 |
Сорбент на основе силикагеля (С) с идентичным функциональным слоем (С-ПЭИа-Б) синтезировали по этой же методике при массовом отношении реагентов 1 : 1.
Хроматографические колонки заполняли суспензионным способом при давлении 250–300 бар, используя в качестве подвижной фазы деионизованную воду. Для приговления суспензии сорбента на основе TiO2 использовали смесь 18 мл деионизованной воды и 2 мл 1,4-диоксана. Для приготовления суспензии сорбента С-ПЭИа-Б использовали раствор следующего состава: 10 мл 0.1 М раствора KCl, 8 мл этанола и 2 мл 1,4-диоксана.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Используя различные массовые отношения матрицы, полимера и сшивающего агента синтезировали неподвижные фазы на основе диоксида титана (Т). Хроматографические характеристики сорбентов изучали с помощью теста Танака для гидрофильных неподвижных фаз [24, 25] и на примере разделения модельной смеси водорастворимых витаминов группы В в режиме гидрофильной хроматографии.
Для анализа возможности применения сорбентов на основе диоксида титана в режиме гидрофильной хроматографии следует предварительно оценить перспективы адсорбционного модифицирования материала с точки зрения селективности и эффективности, а также определить стабильность функционального слоя полученного сорбента. Так как в режиме ГИХ доля органического растворителя в подвижной фазе достаточно высокая, адсорбционно закрепленный функциональный слой может быть неустойчив, а количество сшивающего реагента – недостаточным, что приведет к нестабильности получаемых хроматографических параметров, а также загрязнению системы. Поскольку в режиме ГИХ удерживание аналитов происходит в адсорбированном слое воды на поверхности сорбента, в этом случае можно использовать и несферические частицы без существенного снижения хроматографических характеристик [26]. В связи с этим в качестве материала для предварительных испытаний по адсорбционному модифицированию диоксида титана использовали коммерчески более доступные частицы TiO2 с полиморфной модификацией рутил.
Предварительно получили хроматографические характеристики немодифицированного материала с использованием смеси водорастворимых витаминов группы В в качестве модельных аналитов, обладающих различными физико-химическими свойствами и различающихся по гидрофильности. Информация о хроматографических условиях разделения водорастворимых витаминов в условиях ГИХ на диоксиде титана в литературе отсутствует, поэтому при выборе состава подвижной фазы варьировали рН буферного раствора в диапазоне 4–9, его концентрацию (1–100 мМ) и содержание в элюенте. Лучшие хроматографические параметры обеспечил элюент следующего состава: 20 мМ ацетатно-аммонийный буферный раствор с pH 5.8–CH3CN (10 : 90, по объему).
На рис. 2 представлены хроматограммы смеси витаминов на матрице и модифицированном сорбенте. Факторы удерживания витаминов и селективность после модифицирования увеличились благодаря созданию гидрофильного слоя и возможному экранированию лигандообменных сайтов матрицы диоксида титана, что позволило разделить смесь пяти водорастворимых витаминов за 20 мин в градиентном режиме элюирования. Таким образом, модифицирование диоксида титана позволяет регулировать селективность по полярным веществам в режиме ГИХ. Полученный сорбент стабилен в течение ~200 ч. Можно заключить, что адсорбционное закрепление функционального слоя с последующей сшивкой представляет перспективный подход для создания новых сорбентов для гидрофильной хроматографии.
Рис. 2.
(а) – Хроматограммы водорастворимых витаминов на сорбенте T (рутил). (б) – Хроматограмма модельной смеси витаминов на сорбенте T-ПЭИа-Б (рутил). Подвижная фаза: ацетонитрил–20 мМ аммонийно-ацетатный буферный раствор (ААБ) с pH 5.8 (90 : 10, по объему); скорость потока 0.3 мл/мин; УФ-детектирование при 270 нм.

Создание новых сорбентов на основе анатаза. Далее для получения новых сорбентов, отвечающих требованиям ВЭЖХ, использовали сферические частицы диоксида титана с более гидрофильной полиморфной модификацией анатаз, заявленные производителем как сорбент для ВЭЖХ. Из принципа Неймана следует, что различные полиморфные модификации диоксида титана могут обладать разными хроматографическими свойствами, поэтому необходимо предварительно оценить возможности анатаза в роли сорбента в режиме ГИХ.
При выборе оптимальных условий разделения витаминов группы В варьировали pH буферного раствора в диапазоне 3.0–11.0 с использованием подходящих буферных систем (формиатной, ацетатной, фосфатной, карбонатной), концентрацию буферного раствора и долю водной фазы в составе элюента. В кислой среде факторы удерживания никотиновой кислоты и рибофлавина на положительно заряженной неподвижной фазе слишком высоки (k = 23.11 и 60.02 соответственно), а при рН 9.0–11.0 – малы для всех витаминов. При этом тиамин не удерживается при рН 11.0, что согласуется с данными работ [19, 27]. Выбор pH водного буферного раствора осуществляли в области рН 7.0–9.0 (рис. 3). Значимого различия во временах удерживания и эффективности для витаминов при pH 7.0 и 8.0 не наблюдали, однако при pH 8.0 обеспечивается разрешение пары никотинамид/никотиновая кислота.
Рис. 3.
Диаграммы зависимости факторов удерживания и эффективности по витаминам от pH буферного раствора на сорбенте T (анатаз): 1 – никотинамид, 2 – никотиновая кислота, 3 – В6, 4 – В2, 5 – В12, 6 – В1; подвижная фаза: ацетонитрил–буферный раствор (80 : 20, по объему); скорость потока 1.0 мл/мин; УФ-детектирование при 270 нм.

В результате варьирования концентрации буферного раствора и доли водной фазы для экспрессного разделения модельной смеси витаминов выбрали элюент состава 7 мМ фосфатный буферный раствор с pH 8.0–ацетонитрил (18 : 82, по объему). Хроматограмма смеси четырех витаминов (никотинамид, В6, В2, В1) в изократическом режиме элюирования представлена на рис. 3. На колонке с анатазом (сорбент Т) обеспечиваются большие факторы удерживания аналитов, что может быть связано в том числе с различной структурной анизотропией адсорбированного на поверхности диоксида титана слоя воды, имеющего большую толщину в случае анатаза по сравнению с рутилом [28], что в ГИХ равнозначно увеличению объема неподвижной фазы.
Таким образом, выбранные условия элюирования позволили добиться приемлемого удерживания аналитов и более высокой селективности и эффективности для витаминов – до 30 000 тт/м. В результате смесь четырех витаминов (В3 амид, В6, В2, В1) удалось разделить за 5 мин без использования градиентного режима элюирования. На колонке с сорбентом Т витамины элюируются в порядке увеличения гидрофильности, что может свидетельствовать о значительном вкладе распределительного механизма в их удерживание в адсорбированном слое воды у поверхности диоксида титана.
Хроматографические свойства сорбентов T-b× ×ПЭИа-a×Б. Выше показано, что адсорбционное закрепление полимерного слоя на поверхности диоксида титана позволяет улучшить селективность и эффективность нового гидрофильного сорбента. Далее варьировали количество ПЭИ и 1,4-БДДГЭ по отношению к матрице при синтезе сорбентов с целью возможного улучшения хроматографических характеристик модифицированной таким образом неподвижной фазы. Разделение витаминов осуществляли в выбранных ранее условиях (рис. 3).
Выбор количества сшивающего агента 1,4-БДДГЭ. 1,4-БДДГЭ представляет собой молекулу, содержащую полярные эпоксидные группы, раскрывающиеся при взаимодействии с ПЭИ, и гидрофобные бутильные фрагменты. Варьируя количество 1,4-БДДГЭ, участвующего в реакции модифицирования сорбента, можно повлиять на поверхностные свойства неподвижной фазы и ее общую гидрофильность, а также установить необходимое и достаточное количество реагента для инкапсулирования адсорбированного ПЭИ с целью его надежного закрепления на матрице. Получили ряд сорбентов с массовыми соотношениями диоксид титана–1,4‑БДДГЭ, равными 1 : 0.1, 1 : 0.3, 1 : 0.5, 1 : 0.7, 1 : 1.0 и 1 : 1.5. В этой серии сорбентов соотношение матрица–адсорбционно закрепленный ПЭИ составляло 1 : 1 по массе.
Из приведенных на рис. 4 хроматограмм модельных смесей витаминов видно, что по сравнению с матрицей T селективность разделения витаминов на колонках с модифицированными сорбентами увеличилась, что обеспечило полное разрешение пары В1/В12, невозможное на колонке T. Наибольшая селективность по витаминам характерна для колонок с сорбентами T-ПЭИа-1.0×Б и T-ПЭИа-0.1×Б, наибольшая эффективность – для сорбентов T-ПЭИа-1.0×Б и T-ПЭИа-0.5×Б. Однако в случае T-ПЭИа-0.1×Б количество сшивающего реагента оказалось недостаточным для закрепления находящегося на поверхности диоксида титана слоя ПЭИ, и в процессе работы с подвижной фазой, обогащенной ацетонитрилом, плохо закрепленный адсорбционный слой ПЭИ, по-видимому, десорбировался, а эффективность колонки существенно снизилась после 11 ч эксплуатации.
Рис. 4.
Хроматограммы модельной смеси витаминов на сорбентах с различным количеством 1,4-БДДГЭ. Подвижная фаза: 7 мМ фосфатный буферный раствор с pH 8.0–ацетонитрил (15 : 85, по объему), скорость потока 1 мл/мин, УФ-детектирование при 270 нм.

Среди ряда изученных в работе неподвижных фаз сорбент T-ПЭИа-Б (с массовым соотношением реагентов TiO2–ПЭИ–1,4-БДДГЭ 1 : 1 : 1) продемонстрировал лучшую селективность и позволил разделить модельную смесь шести водорастворимых витаминов (никотинамид, никотиновая кислота, В6, В2, В1, В12) за 4 мин с эффективностью до 25000 тт/м при выбранных условиях изократического режима элюирования (рис. 4). При этом выбранное в качестве оптимального значение рН 8.0 превышает изоэлектрическую точку диоксида титана, и таким образом обеспечивается электростатическое закрепление положительно заряженного сшитого слоя ПЭИ на отрицательно заряженной поверхности матрицы.
Выбор толщины полимерного слоя полиэтиленимина. Варьирование количества ПЭИ на стадии модифицирования приводит к изменению толщины адсорбированного на матрице полимерного слоя ПЭИ. Толщина функционального слоя сорбента влияет на скорость массопереноса и установления равновесия между подвижной и неподвижной фазами и аналитами, поэтому таким образом можно влиять на эффективность. В работе получен ряд сорбентов T-b×ПЭИа-Б, где b – 0.1, 0.5, 1.0 и 1.5.
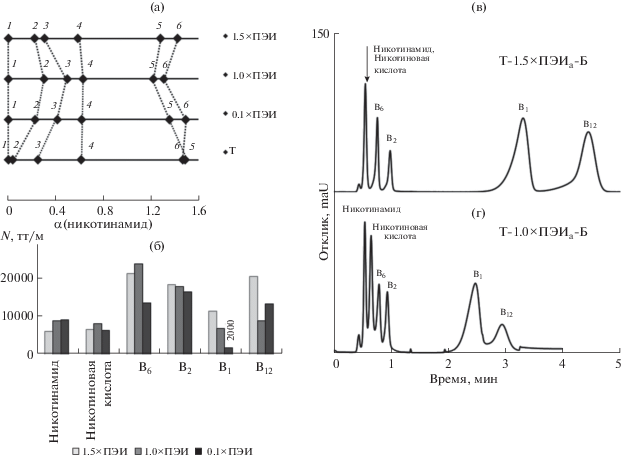
Результаты определения витаминов приведены на рис. 5. Наибольшую селективность и эффективность по витаминам наблюдали для колонок с T-1.0×ПЭИа-Б и T-0.1×ПЭИа-Б (до 24 000 тт/м). Снижение эффективности сорбента T-1.5×ПЭИа-Б, по-видимому, связано с большей толщиной функционального слоя ПЭИ на поверхности диоксида титана, что приводит к замедлению массопереноса. В процессе работы на колонке T-0.1×ПЭИа-Б наблюдали снижение эффективности и рост давления в хроматографической системе. Вероятно, 10 мас. % ПЭИ недостаточно для покрытия частиц и полного экранирования матрицы Т. На рис. 5в, 5г приведены хроматограммы модельных смесей водорастворимых витаминов на сорбентах T-1.0×ПЭИа-Б и T-1.5×ПЭИа-Б. Благодаря большей селективности на сорбенте T-1.0×ПЭИа-Б удалось разделить смесь из шести водорастворимых витаминов за 4 мин в изократическом режиме элюирования.
Рис. 5.
(а) – Шкала селективности витаминов относительно В3 амида, (б) – диаграмма эффективности по витаминам на сорбентах с различным количеством полиэтиленимина, (в) и (г) – хроматограммы модельной смеси витаминов на сорбентах с различным количеством полиэтиленимина: 1 – никотинамид, 2 – никотиновая кислота, 3 – В6, 4 – В2, 5 – В1, 6 – В12. Подвижная фаза: 7 мМ фосфатный буферный раствор с pH 8.0–ацетонитрил (15 : 85, по объему), скорость потока 1 мл/мин, УФ-детектирование при 270 нм.
В результате варьирования количества адсорбционно закрепленного на поверхности диоксида титана ПЭИ и сшивающего реагента 1,4‑БДДГЭ установили, что сорбент T-1.0×ПЭИа-1.0×Б обладает лучшими хроматографическими характеристиками, высокой эффективностью и большей селективностью при разделении водорастворимых витаминов.
Сравнение сорбентов на основе TiO2 и SiO2 в режиме гидрофильной хроматографии. Одним из главных преимуществ неподвижных фаз на основе диоксида титана является возможность обеспечить альтернативную силикагелю селективность разделения полярных аналитов благодаря иной природе материала. Сравнили хроматографические параметры силикагеля (С) и модифицированного сорбента С-ПЭИа-Б с массовым соотношением реагентов 1 : 1 по аналогии с сорбентом T-1.0×ПЭИа-1.0×Б с наилучшими характеристиками.
На рис. 6а, 6б представлены шкалы селективности по витаминам для сорбентов С, С-ПЭИа-Б, T и T-ПЭИа-Б. Для сорбента T-ПЭИа-Б факторы удерживания витаминов увеличились по сравнению с матрицей Т, а для С-ПЭИа-Б – уменьшились по сравнению с матрицей С. В случае обоих модифицированных ПЭИ сорбентов наблюдали уменьшение факторов удерживания положительно заряженного тиамина (В1) и их увеличение для никотиновой кислоты вследствие электростатического притяжения. Из представленных на рис. 6в, 6г диаграмм эффективности можно заключить, что сорбент T-ПЭИа-Б уступает по эффективности своему аналогу на основе силикагеля. Однако невысокая эффективность сорбентов на основе диоксида титана в данном случае может быть обусловлена неоптимальными условиями упаковки частиц, заметно отличающихся от силикагеля. В данном случае целесообразно сравнить селективности сорбентов на основе различных матриц до и после модифицирования. Эффективность новых сорбентов впоследствии может быть улучшена путем оптимизации условий их упаковки в хроматографические колонки.
Рис. 6.
(а) и (б) – Шкалы селективности витаминов относительно никотинамида, (в) и (г) – диаграммы эффективности по витаминам. Подвижная фаза для сорбентов на основе SiO2: 100 мМ аммонийно-ацетатный буферный раствор с pH 5.8–ацетонитрил (10 : 90, по объему); подвижная фаза для сорбентов на основе TiO2: 7 мМ фосфатный буферный раствор с pH 8.0–ацетонитрил (15 : 85, по объему); общие условия: скорость потока 1 мл/мин, УФ-детектирование при 270 нм.

Сравнение хроматографических характеристик полученных сорбентов с использованием теста Танака для гидрофильных неподвижных фаз. Для характеристики сорбентов до и после модифицирования, оценки различных типов селективности и вклада вторичных взаимодействий в удерживание определяемых веществ использовали тест Танака для гидрофильных неподвижных фаз [25] (табл. 2). Как видно из табл. 2, адсорбция и сшивка слоя ПЭИ на матрице С позволили увеличить гидрофильность, гидроксильную селективность, основность сорбента С-ПЭИа-Б и изменить селективность по отношению к заряженным соединениям с катионообменной α(СХ), обусловленной диссоциацией силанольных групп (рKа = 4.7) в условиях теста, на анионообменную α(AX), связанную с наличием положительно заряженных аммониевых групп на поверхности сорбента в результате выбранного способа модифицирования. Таким образом, данный функциональный слой эффективно экранирует матрицу, и возможности катионообменного взаимодействия полностью нивелируются.
Таблица 2.
Результаты теста Танака для гидрофильных неподвижных фаз
| Сорбент | kU | α(OH) | α(CH2) | α(AX) | α(CX) | α(Tb/Tp) | α(V/A) |
|---|---|---|---|---|---|---|---|
| С | 0.77 | 1.09 | 1.23 | 0.11 | 44.57 | 1.22 | 1.17 |
| С-ПЭИа-Б | 0.75 | 1.59 | 1.23 | 30.01 | 0.01 | 0.54 | 1.39 |
| T | 3.06 | 1.01 | 1.27 | 0.33 | 0.71 | 3.13 | 5.13 |
| T-ПЭИа-Б | 2.09 | 0.75 | 2.69 | 2.41 | 0.26 | 0.54 | 3.44 |
Аналогично сорбентам на основе силикагеля в случае модифицирования диоксида титана для Т-ПЭИа-Б возросла анионообменная селективность, а также уменьшились значения α(Tb/Tp), что свидетельствует об уменьшении кислотных свойств модифицированного сорбента по сравнению с матрицей в результате адсорбции и сшивки ПЭИ. Увеличение метиленовой селективности α(СН2), а также уменьшение гидрофильности поверхности kU и гидроксильной селективности α(ОН), вероятно, вызвано введением гидрофобных бутильных фрагментов сшивающего реагента 1,4-БДДГЭ в структуру функционального слоя, а также экранированием лигандообменных сайтов матрицы Т сшитым слоем ПЭИ. Гидрофильность T-ПЭИа-Б согласно kU почти в три раза выше, чем у прототипа на основе силикагеля, однако при этом стоит учитывать возможность лигандообменных взаимодействий диоксида титана с аналитами теста Танака, что может вносить вклад в соответствующий тип селективности и величины факторов удерживания аналитов.
Сорбент на основе силикагеля обладает бóльшими гидроксильной α(OH) и анионобменной α(AX) селективностью, при этом метиленовая α(CH2) и селективность по отношению к стереоизомерам α(V/A) более ярко выражены у T-ПЭИа-Б. Высокая стереоселективность α(V/A), характерная для матрицы Т, лишь немного снижается в результате модифицирования. Таким образом, сор-бенты на основе диоксида титана могут представлять интерес в области разделения стереоизомеров.
* * *
Впервые показано применение модифицированных частиц диоксида титана в режиме ГИХ. Установлено, что адсорбционное закрепленное ПЭИ с последующей сшивкой 1,4-БДДГЭ приводит к получению стабильных сорбентов при соотношении матрица–ПЭИ не менее 1 : 0.5 и матрица–1,4-БДДГЭ не менее 1 : 0.3. По результатам поиска условий модифицирования выявлены способы управления селективностью и эффективностью путем варьирования количества сшивающего агента 1,4-БДДГЭ и ПЭИ, а также подобраны условия определения водорастворимых витаминов на новых сорбентах. В результате получен сорбент T-1.0 × ПЭИа-1.0 × Б, позволяющий экспрессно разделить модельную смесь шести витаминов менее чем за 4 мин с эффективностью до 25 000 тт/м. Показано, что сорбенты на основе диоксида титана, полученные путем адсорбционного закрепления ПЭИ с последующей сшивкой 1,4-БДДГЭ, стабильны в течение нескольких месяцев эксплуатации и в широком диапазоне pH, проявляют иную селективность по отношению к витаминам по сравнению с аналогом на основе силикагеля, обеспечивают существенно более экспрессное разделение модельной смеси витаминов и являются потенциально эффективными сорбентами для гидрофильного режима. Отсутствие необходимости градиентного элюирования позволяет избежать процедуры уравновешивания колонки между анализами, которая часто занимает много времени в режиме ГИХ. Выбор условий модифицирования диоксида титана обеспечил получение стабильных сорбентов благодаря надежному закреплению функционального слоя в условиях эксплуатации с водно-органическими подвижными фазами, что в сочетании с гидролитической устойчивостью диоксида титана открывает новые перспективы использования метода ГИХ, а также может найти применение для создания сорбентов для твердофазной экстракции полярных веществ. Дальнейшие исследования будут направлены на улучшение эффективности путем повышения степени однородности покрытия, на поиск способов ковалентного модифицирования поверхности диоксида титана, а также оптимизации процесса упаковки.
Работа выполнена при поддержке Российского фонда фундаментальных исследований, грант № 20-03-00909.
Список литературы
Alpert A.J. Hydrophilic-interaction chromatography for the separation of peptides, nucleic acids and other polar compounds // J. Chromatogr. A. 1990. V. 499. P. 177.
Huber J.F.K., Pawlowska M., Markl P. Selection of the solid support – A crucial step for the realization of solvent generated liquid-liquid chromatography // J. Chromatogr. A. 1990. V. 500. P. 257.
Чернобровкина А.В., Смоленков А.Д., Шпигун О.А. Гидрофильная хроматография – перспективный метод определения полярных веществ // Лаборатория и производство. 2018. № 4. С. 76.
Bather J.M., Gray R.A. Relationship between chromatographic performance and surface structure of alumina microspheres // J. Chromatogr. A. 1978. V. 156. P. 21.
Jaffrezic-Renault N., Poirier-Andrade H., Trang D.H. Models for the adsorption of uranium on titanium dioxide // J. Chromatogr. A. 1980. V. 201. P. 187.
Kawahara C., Kozbur X., Gould S., Parker L. Magnesium oxide column chromatography: A novel and rapid method for steroid purification // Anal. Biochem. 1980. V. 102. P. 310.
Kawahara M., Nakamura H., Nakajima T. Titania and zirconia: possible new ceramic microparticulates for high-performance liquid chromatography // J. Chromatogr. 1990. V. 515. P. 149.
Grfin M., Kurganov A.A., Schacht S., Schüth F., Unger K.K. Comparison of an ordered mesoporous aluminosilicate, silica, alumina, titania and zirconia in normal-phase high-performance liquid chromatography // J. Chromatogr. A. 1996. V. 740. P. 1.
Tani K., Suzuki Y. Investigation of the ion-exchange behaviour of titania: Application as a packing material for ion chromatography // Chromatographia. 1997. V. 46. P. 623.
Tani K., Kubojima H. Separation of inorganic anions and cations on titania by use of acetic acid-sodium acetate and bicine-sodium hydroxide buffers // Chromatographia. 1998. V. 47. P. 655.
Tani K., Ozawa M. Investigation of chromatographic properties of titania. I. On retention behavior of hydroxyl and other substituent aliphatic carboxylic acids: Comparison with zirconia // J. Liq. Chromatogr. Rel. Technol. 1999. V.22. P. 843.
Tani K., Sumizawa T., Watanabe M., Tachibana M., Koizumi H., Kiba T. Evaluation of titania as an ion-exchanger and as a ligand-exchanger in HPLC // Chromatographia. 2002. V. 55. P. 33.
Pinkse M.W., Uitto P.M., Hilhorst M.J., Ooms B., Heck A.J. Selective isolation at the femtomole level of phosphopeptides from proteolytic digests using 2D-NanoLC-ESI-MS/MS and titanium oxide precolumns // Anal. Chem. 2004. V. 76. P. 3935.
Ting Z., Lucy C.A. Hydrophilic interaction chromatography of nucleotides and their pathway intermediates on titania // J. Chromatogr. A. 2008. V.1187. P. 87.
Ting Z., Lucy C.A. Separation of carboxylates by hydrophilic interaction liquid chromatography on titania // J. Chromatogr. A. 2010. V. 1217. P. 82.
Ozawa M., Tani K., Nomura A., Tachibana M., Koizumi H., Kiba N. Retention behavior of nucleic acid bases and purine derivatives on titania // Chromatographia. 2009. V. 70. P. 533.
Ozawa M., Tani K., Tachibana M., Koizumi H., Kiba N. Retention behavior of purine-like compounds on titania and the effect of organic modifiers content in the mobile phase // Chromatographia. 2010. V. 72. P. 313.
Moliner-Martinez Y., Herráez-Hernández R., Molins-Legua C., Campins-Falcó P. Improving analysis of apolar organic compounds by the use of a capillary titania-based column: Application to the direct determination of faecal sterols cholesterol and coprostanol in wastewater samples // J. Chromatogr. A. 2010. V. 1217. P. 4682.
Tan J., Li R., Jiang Z.T. Determination of thiamine (vitamin B1) in pharmaceutical tablets and human urine by titania-based ligand-exchange hydrophilic interaction chromatography // Anal. Methods. 2011. V. 3. P. 1568.
Abi J.M., Randon J. Chromatographic behavior of xanthines in aqueous normal phase chromatography using titania stationary phase // J. Chromatogr. A. 2011. V. 1218. P. 721.
Chicz R.M., Shi Z., Regnier F.E. Preparation and evaluation of inorganic anion-exchange sorbents not based on silica // J. Chromatogr. 1986. V. 359. P. 121.
Alpert A.J., Regnier F.E. Preparation of a porous microparticulatee anion-exchange chromatography support for proteins // J. Chromatogr. A. 1979. V. 185. P.375.
Segro S.S., Cabezas Y., Malik A. Ultra-high-stability, pH-resistant sol–gel titania poly (tetrahydrofuran) coating for capillary microextraction on-line coupled to high-performance liquid chromatography // J. Chromatogr. A. 2009. V. 1216. P. 4329.
Kawachi Y., Ikegami T., Takubo H., Ikegami Y., Miyamoto M., Tanaka N. Chromatographic characterization of hydrophilic interaction liquid chromatography stationary phases: Hydrophilicity, charge effects, structural selectivity, and separation efficiency // J. Chromato-gr. A. 2011. V. 1218. P. 5903.
Dolci M., Chromatographic Characterization of Stationary Phases for Hydrophilic Interaction Liquid Chromatography. Runcorn, Cheshire, UK: Thermo Fisher Scientific, 2013.
Buszewski B., Noga S. Hydrophilic interaction liquid chromatography (HILIC) – A powerful separation technique // Anal. Bioanal. Chem. 2012. V. 402. P. 231.
Kip C., Tosun R.B., Alpaslan S., Koçer I., Çelik E., Tuncel A. Ni(II)-decorated porous titania microspheres as a stationary phase for column chromatography applications: Highly selective purification of hemoglobin from human blood // Talanta. 2019. V. 200. P. 100.
Kavathekar R.S., English N.J., MacElroy J.M.D. Spatial distribution of adsorbed water layers at the TiO2 rutile and anatase interfaces // Chem. Phys. Lett. 2012. V. 554. P. 102.
Дополнительные материалы отсутствуют.
Инструменты
Журнал аналитической химии