Журнал аналитической химии, 2021, T. 76, № 4, стр. 324-330
Определение метамизола натрия с учетом его разложения в водных растворах методом высокоэффективной жидкостной хроматографии при изучении профилей растворения
А. В. Егорова a, *, Г. В. Мальцев b, Ю. В. Скрипинец a, О. Д. Войтюк b, С. Н. Кашуцкий b, И. В. Умецкая b, В. П. Антонович a
a Физико-химический институт им. А.В. Богатского Национальной академии наук Украины
65080 Одесса, Люстдорфская дорога, 86, Украина
b ОДО “ИНТЕРХИМ”
65080 Одесса, Люстдорфская дорога, 86, Украина
* E-mail: yegorova@interchem.com.ua
Поступила в редакцию 18.06.2020
После доработки 03.08.2020
Принята к публикации 20.08.2020
Аннотация
Разработана и валидирована методика количественного ВЭЖХ-определения метамизола натрия для изучения профилей растворения лекарственного препарата ПЕНТАЛГИН ІС®, таблетки, с учетом разложения метамизола натрия в водных растворах. При изучении профилей растворения, наряду с процессом высвобождения метамизола натрия из готовой лекарственной формы, происходит его гидролиз до продукта разложения – метиламинофеназона. Реакция разложения является мономолекулярной, поэтому на хроматограммах испытуемых растворов и растворов сравнения имеются два пика, соответствующие метамизолу и метиламинофеназону. Показано, что для корректного расчета количества метамизола натрия, перешедшего в раствор из таблетки, необходимо определять его по сумме площадей обоих пиков с учетом факторов отклика детектора.
Для подтверждения биоэквивалентности лекарственных препаратов (ЛП) проводят сравнительные фармакокинетические исследования на людях или испытания in vitro по тесту “Растворение”, которые дают возможность оценить качество и эффективность препарата, а также характеризуют скорость и степень высвобождения активного вещества из пероральных лекарственных форм в модельных условиях. При установлении эквивалентности дженерики можно сравнивать со стандартом (оригинальный препарат или ЛП, признанный в качестве препарата сравнения) не только по растворению за определенный промежуток времени (по одной точке), но и по профилю растворения, получаемому по 3−6 точкам с использованием расчетных коэффициентов подобия, рекомендуемых FDA [1]. Следует отметить, что в последние годы возросло количество публикаций по изучению качества дженериков с использованием теста “Растворение” [2–5].
Определение эквивалентности in vitro – это испытание, предназначенное для оценки эквивалентности профилей растворения в трех средах со значениями рН 1.2, 4.5 и 6.8 изучаемого и референтного ЛП. При построении профилей растворения необходимо выполнять ряд условий: количество применяемых в расчете точек должно быть не менее трех; условия испытания сравниваемых лекарственных препаратов должны быть одинаковыми; отбор проб следует проводить через одинаковые промежутки времени; после достижения уровня высвобождения 85% из обоих ЛП в расчет следует принимать все точки до этого уровня и одну следующую; коэффициент вариации для первой временной точки не должен превышать 20%, для последующих –10%. Для сравнения профилей растворения использует коэффициент различия (f1) и коэффициент подобия (f2). Для профилей, которые считаются подобными, значение f1 должно быть близко к 0, а значение f2 – к 100. Значение f1, находящееся в пределах от 0 до 15, а значение f2 – в пределах от 50 до 100, гарантирует сходство или эквивалентность двух профилей, и, следовательно, эквивалентность фармакологического действия испытуемого препарата и препарата сравнения [6].
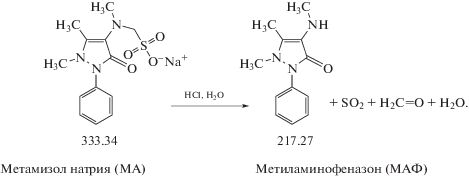
Метамизол натрия (МА известен как “анальгин”) – лекарственное средство, анальгетик и антипиретик из группы пиразолонов. Установлено, что в водных и буферных растворах происходит превращение (гидролиз) метамизола натрия до его продукта разложения метиламинофеназона (МАФ). Реакция разложения является мономолекулярной (схема 1 ) [7].
Схема 1 . Схема разложения метамизола натрия.
Влияние основных факторов на скорость разложения метамизола натрия в водных растворах и способы его стабилизации изучены методом обращенно-фазовой ВЭЖХ [8–10]. Для замедления разложения метамизола натрия в анализируемых растворах рекомендуется использовать содержание ацетонитрила на уровне 30–40% (по объему) и стабилизатора (метабисульфита натрия) 1.0–2.0 мг/мл. Стабилизация невозможна при проведении испытания “Профили растворения”.
Следует отметить, что в работе [11] по изучению профилей растворения однокомпонентного препарата метамизола натрия в 0.1 М HCl методом спектрофотометрии вопросы деградации не обсуждались.
Цель данной работы − разработка и валидация методики количественного определения метамизола натрия для изучения профилей растворения лекарственного препарата ПЕНТАЛГИН ІС® (таблетки) с учетом разложения метамизола натрия в водных растворах.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Материалы и методы. Использовали реактивы квалификации х. ч., для ВЭЖХ-анализа, бидистиллированную воду и воду для хроматографии.
Для приготовления растворов сравнения использовали вторичные рабочие стандартные образцы (РСО) парацетамола, кодеина фосфата гемигидрата, кофеин-бензоата натрия, фенобарбитала, метамизола натрия производства ОДО “ИНТЕРХИМ” (Украина).
Аппаратура. Хроматограммы регистрировали на жидкостном хроматографе Agilent 1260 Infinity 2D LC System с УФ-детектором. Использовали весы лабораторные электронные AUX220 (SHIMADZU, Япония) и магнитную мешалку ARE (VELP Scientifica, Италия). Воду для хроматографии получали с использованием системы очистки воды arium® pro UV/UF фирмы Sartorius. рН буферных растворов измеряли рН-метром серии Seven Easy фирмы “Mettler Toledo” (Швейцария). Пробоподготовку профилей растворения выполняли с использованием системы для определения степени растворения твердых дозированных форм ERWEKA тип DT 1612.
Методика определения метамизола натрия. Для изучения профилей растворения используют прибор с лопастью-мешалкой. Среды растворения – 0.1 М HCl, ацетатный буферный раствор с рН 4.5, фосфатный буферный раствор с рН 6.8 [12], температура среды 37.0 ± 0.5°С, объем – 500 мл, скорость вращения лопасти – 50 об/мин, время растворения – 45 мин.
Исследуемый раствор. В цилиндрическую посуду полуавтоматического прибора с лопастью-мешалкой помещают 1 таблетку. Через 10, 15, 30, 45 мин после начала растворения пробы автоматически отбираются и фильтруются через мембранные фильтры (0.20 мкм) в пробирки емк. 10.0 мл.
Раствор сравнения. 200.0 мг РСО парацетамола, 9.5 мг РСО кодеина фосфата гемигидрата, 50.0 мг РСО кофеин-бензоата натрия, 300.0 мг РСО метамизола натрия, 10.0 мг РСО фенобарбитала помещают в мерную колбу емк. 100.0 мл, добавляют 70 мл метанола, перемешивают в течение 15 мин, доводят объем раствора тем же растворителем до метки и перемешивают. 10.0 мл полученного раствора разбавляют до 50.0 мл соответствующей средой растворения, фильтруют через мембранный фильтр (0.20 мкм, RC). Растворы используют свежеприготовленными.
Буферный раствор. 5.44 г дигидрофосфата калия помещают в мерную колбу емк. 1000.0 мл, растворяют в 900 мл воды для хроматографии и доводят объем водой для хроматографии до метки, перемешивают. Создают значение рН раствора 5.4 добавлением 0.5 М раствора KOH.
Парацетамол, кодеин основание, кофеин, метамизол натрия и фенобарбитал определяют хроматографированием на жидкостном хроматографе с УФ-детектором при следующих условиях: колонка из нержавеющей стали размером 0.15 м × × 4.6 мм, заполненная силикагелем для хроматографии октадецилсилильным с размером частиц 5 мкм (Zorbax Eclipse XDB-C18); подвижная фаза А: буферный раствор−метанол (800 : 200, по объему); подвижная фаза Б: метанол; скорость подвижной фазы 2.0 мл/мин; температура колонки 30°С; детектирование при длине волны 210 нм; объeм инжектируемой пробы 5 мкл.
Используют следующую программу градиента:
| Время, мин | Подвижная фаза А, % (по объему) | Подвижная фаза Б, % (по объему) |
|---|---|---|
| 0–4.7 | 100 | 0 |
| 4.7–5.7 | 100 → 75 | 0 → 25 |
| 5.7−9 | 75 | 25 |
| 9−10 | 75 → 100 | 25 → 0 |
Предлагается после завершения программы градиента осуществлять переход на первоначальное соотношение подвижных фаз в течение 2 мин (время промывки колонки после анализа).
Хроматографируют раствор сравнения и исследуемый раствор. Хроматографическая система считается пригодной, если коэффициенты разделения пиков кофеина и метамизола, продукта разложения метамизола натрия и фенобарбитала на хроматограммах раствора сравнения составляют не менее 2.0.
Количество метамизола натрия (Х, %), перешедшее в раствор из таблетки в каждой временной точке пробоотбора, вычисляют по формуле:
Таким образом, при расчете количества компонента в каждой временной точке учитывается уменьшение объема раствора и убыль вещества при пробоотборе.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Специфичность методики основана на возможности достоверно определять содержание парацетамола, кодеина основания, кофеина, метамизола натрия и фенобарбитала, перешедших в раствор из таблеток, в присутствии вспомогательных веществ, что достигается путем использования внешних стандартов.
Известно, что метамизол натрия неустойчив в водных и водно-органических растворах. При изучении профилей растворения, наряду с высвобождением метамизола натрия из готовой лекарственной формы, происходит его гидролиз до продукта разложения – метиламинофеназона. Реакция разложения является мономолекулярной, поэтому на хроматограммах испытуемых растворов и растворов сравнения наблюдаются два пика, соответствующие метамизолу (tудерж ≈ ≈ 6.3 мин) и метиламинофеназону (tудерж ≈ 8.1 мин). По этой причине для корректного расчета количества метамизола натрия, перешедшего в раствор из таблетки, необходимо определять его по сумме площадей обоих пиков с учетом факторов отклика детектора.
На рис. 1–3 представлены хроматограммы исследуемых растворов на 45-ой минуте пробоотбора в различных буферных растворах.
Рис. 1.
Хроматограмма исследуемого раствора в 0.1 М HCl: 1 – парацетамол, 2 – кодеин, 3 – бензоат, 4 – кофеин, 5 – метамизол, 6 – метиламинофеназон, 7 – фенобарбитал.
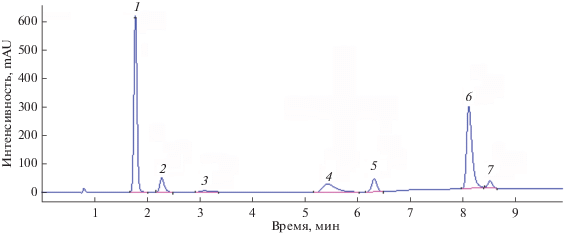
Рис. 2.
Хроматограмма испытуемого раствора в ацетатном буферном растворе c рН 4.5. Отнесение пиков см. в подписи к рис. 1.
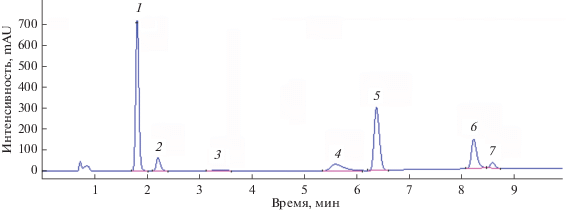
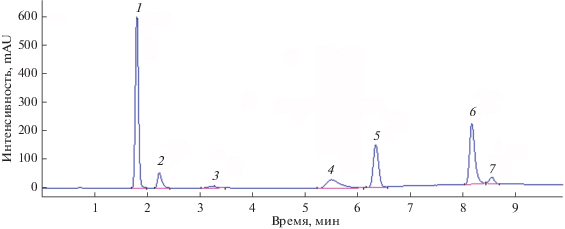
Рис. 3.
Хроматограмма исследуемого раствора в фосфатном буферном растворе с рН 6.8. Отнесение пиков см. в подписи к рис. 1.
Методика расчета фактора отклика детектора. В растворе с исходной (аналитической) концентрацией метамизола натрия (MA) n М через некоторое время происходит накопление продукта его разложения (МАФ) с концентрацией nМАФ, М и остается nМА, М метамизол натрия:
где $n$ – общая исходная (аналитическая) концентрация метамизола натрия в растворе, М; ${{n}_{{МА}}}$ – концентрация метамизола натрия в растворе после частичного разложения, М; ${{n}_{{МАФ}}}$ – концентрация продукта разложения (метиламинофеназона) в растворе, М.На хроматограмме раствора метамизола натрия имеются два пика: пик метамизола площадью АМА и пик метиламинофеназона площадью АМАФ. Площади пиков прямо пропорциональны концентрациям веществ:
где χМА – молярный фактор отклика метамизола натрия, AU, с л/моль; χМАФ – молярный фактор отклика метиламинофеназона, AU, с л/моль.Из уравнений (2) и (3) можно получить выражение для молярной концентрации метамизола натрия в растворе после частичного разложения:
(4)
${{n}_{{MA}}} = \frac{{{{\chi }_{{МАФ}}}}}{{{{\chi }_{{MA}}}}}\frac{{{{A}_{{MA}}}}}{{{{A}_{{МАФ}}}}}{{n}_{{МАФ}}} = \varphi \frac{{{{A}_{{MA}}}}}{{{{A}_{{МАФ}}}}}{{n}_{{МАФ}}},$Подставляя выражение (4) для nМА в уравнение материального баланса (1), получим:
Раствор сравнения метиламинофеназона готовят из раствора метамизола натрия с известной концентрацией nРСО МА (М) и подвергают деструкции до исчезновения пика метамизола [13]. Тогда концетрация метиламинофеназона nРСО МАФ (М) в растворе сравнения:
Концентрацию метиламинофеназона можно найти из площадей пиков метиламинофеназона на хроматограммах испытуемого раствора и раствора сравнения:
где ${{A}_{0}}$ – площадь пика метиламинофеназона на хроматограмме раствора сравнения.Подставляя выражение (7) в выражение (5), получим:
Разделив левую и правую части уравнения (8) на молярную массу метамизола натрия, получим выражение для концентрации метамизола натрия в испытуемом растворе, выраженную в г/л или в мг/мл:
Выражение (9) можно использовать для расчета молярного фактора отклика метиламинофеназона относительно метамизола натрия. Для этого выражение (9) следует представить в виде:
Для определения φ готовили серию растворов метамизола натрия различных концентраций сі и растворы поочередно хроматографировали. Затем строили зависимость, для которой на оси абсцисс откладываются значения ${{{{A}_{{M{{A}_{i}}}}}} \mathord{\left/ {\vphantom {{{{A}_{{M{{A}_{i}}}}}} {{{A}_{{MA{{Ф}_{i}}}}}}}} \right. \kern-0em} {{{A}_{{MA{{Ф}_{i}}}}}}}$ (Х), на оси ординат – значения ${{{{с}_{i}}{{A}_{0}}} \mathord{\left/ {\vphantom {{{{с}_{i}}{{A}_{0}}} {{{с}_{0}}{{A}_{{MA{{Ф}_{i}}}}}}}} \right. \kern-0em} {{{с}_{0}}{{A}_{{MA{{Ф}_{i}}}}}}}$ (Y). Полученные данные аппроксимировали прямолинейной зависимостью Y = a + bX. Значение относительного молярного фактора отклика метиламинофеназона φ определяли как угловой коэффициент этой линейной зависимости (табл. 1).
Таблица 1.
Параметры градуировочных графиков для различных сред растворения (n = 5)
| Среда растворения | Y = a + bX | r | |
|---|---|---|---|
| a | b | ||
| 0.1 М HCl | 0.969 ± 0.004 | 0.839 ± 0.047 | 0.99536 |
| Ацетатный буферный раствор c рН 4.5 | 0.952 ± 0.028 | 0.833 ± 0.007 | 0.99989 |
| Фосфатный буферный раствор c рН 6.8 | 1.128 ± 0.113 | 0.857 ± 0.015 | 0.99951 |
Рассчитанные значения относительного молярного фактора отклика метиламинофеназона φ в различных буферных растворах составили 0.839 – в 0.1 М HCl, 0.833 – в ацетатном буферном растворе c рН 4.5, 0.857 – в фосфатном буферном растворе c рН 6.8. Полученные значения φ близки между собой, но значимо отличаются от единицы.
Проверка линейности, правильности и прецизионности определения метамизола натрия в фосфатном буферном растворе с рН 6.8. Результаты проверки представлены в табл. 2–5.
Таблица 2.
Значения площадей пиков метамизола и метиламинофеназона на хроматограммах раствора сравнения
| Масса навески ${{m}_{0}}$, мг | Площадь пика метамизола на хроматограмме, ${{A}_{{0MA}}}$ | Площадь пика метиламинофеназона на хроматограмме, ${{A}_{{0MAФ}}}$ | φA0МА + A0МАФ | |
|---|---|---|---|---|
| φ = 1 | φ = 0.857 | |||
| 300.0 | 2065.97 | 1003.95 | 3069.92 | 2774.19 |
| 2050.20 | 1022.40 | 3072.60 | 2779.12 | |
| Среднее значение | 3071.26 | 2776.65 | ||
| sr, % | 0.06 | 0.13 | ||
Таблица 3.
Проверка правильности и прецизионности
| φ = 1 | φ = 0.857 | ||||
|---|---|---|---|---|---|
| введено, мг | найдено, мг | Z* | введено, мг | найдено, мг | Z* |
| 30.0 | 28.2 | 93.84 | 30.0 | 30.1 | 100.43 |
| 60.0 | 54.8 | 91.31 | 60.0 | 58.2 | 96.93 |
| 90.0 | 84.7 | 94.14 | 90.0 | 89.4 | 99.36 |
| 150.0 | 143.1 | 95.43 | 150.0 | 149.0 | 99.36 |
| 240.0 | 233.7 | 97.36 | 240.0 | 239.2 | 99.69 |
| 270.0 | 264.4 | 97.92 | 270.0 | 269.9 | 99.97 |
| 300.0 | 296.2 | 98.72 | 300.0 | 301.4 | 100.48 |
| 330.0 | 328.1 | 99.43 | 330.0 | 332.7 | 100.81 |
| 390.0 | 387.8 | 99.44 | 390.0 | 390.1 | 100.03 |
| $\overline Z $, % | 96.40 | 99.67 | |||
| s, % | 2.86 | 1.14 | |||
| ΔZ = 1.86s, % | 5.32 | 2.13 | |||
| Критерий: ${{\Delta }_{Z}} \leqslant 3$% | Не соответствует | Соответствует | |||
| $\delta = \left| {\overline {\text{Z}} {\text{ }} - 100} \right|$, % | 3.60 | 0.33 | |||
| Статистический критерий: $\delta \leqslant \frac{{{{\Delta }_{Z}}}}{{\sqrt n }} = 1.77$ | Не соответствует | Соответствует | |||
| Практический критерий: $\delta \leqslant 0.96$ | Не соответствует | Соответствует | |||
Таблица 4.
Значения нормализованных координат для проверки линейности
| φ = 1 | φ = 0.857 | ||
|---|---|---|---|
| ${{X}_{i}}$, % | ${{Y}_{i}}$, % | ${{X}_{i}}$, % | ${{Y}_{i}}$, % |
| 10.00 | 9.38 | 10.00 | 10.04 |
| 20.00 | 18.26 | 20.00 | 19.39 |
| 30.00 | 28.24 | 30.00 | 29.81 |
| 50.00 | 47.72 | 50.00 | 49.68 |
| 80.00 | 77.89 | 80.00 | 79.75 |
| 90.00 | 88.13 | 90.00 | 89.97 |
| 100.00 | 98.72 | 100.00 | 100.48 |
| 110.00 | 109.38 | 110.00 | 110.89 |
| 130.00 | 129.27 | 130.00 | 130.04 |
Таблица 5.
Значения параметров линейности и их соответствие критериям приемлемости
| Параметр | Значение | Критерий незначимости | Вывод | ||
|---|---|---|---|---|---|
| φ = 1 | φ = 0.857 | φ = 1 | φ = 0.857 | ||
| |a| | 1.73 | 0.42 | ≤1.07 | Не соответствует | Соответствует |
| b | 1.0041 | 1.0062 | |||
| |1 − b| | 0.0041 | 0.0062 | ≤0.0157 | Соответствует | Соответствует |
| S0 | 0.67 | 0.38 | ≤1.58 | Соответствует | Соответствует |
| r | 0.99989 | 0.99997 | ≥0.99932 | Соответствует | Соответствует |
| r2 | 0.99979 | 0.99993 | ≥0.96305 | Соответствует | Соответствует |
| ПО, % | 1.469 | 0.837 | ≤10.67 | Соответствует | Соответствует |
| ПКО, % | 4.408 | 2.512 | ≤32 | Соответствует | Соответствует |
Для проверки линейности вводят нормализованные координаты:
(11)
${{X}_{i}} = \frac{{{{m}_{i}}}}{{{{m}_{0}}}} \times 100\% ,\,\,\,\,{{Y}_{i}} = \frac{{\varphi {{A}_{{iMA}}} + {{A}_{{iMAФ}}}}}{{\varphi {{A}_{{0MA}}} + {{A}_{{0MAФ}}}}} \times 100\% .$Полученные несоответствия при проверке линейности и правильности (φ = 1) связаны с тем, что не были учтены относительные молярные факторы отклика метиламинофеназона. В случае учета фактора отклика детектора (φ = 0.857) валидационные характеристики методики удовлетворяют соответствующим критериям приемлемости (табл. 3–5).
* * *
Таким образом, разработана и валидирована ВЭЖХ-методика количественного определения метамизола натрия для изучения профилей растворения лекарственного препарата ПЕНТАЛГИН ІС® (таблетки) с учетом разложения метамизола натрия в водных растворах. Определены относительные молярные факторы отклика продукта разложения метамизола натрия метиламинофеназона в различных буферных растворах. На примере результатов, полученных в фосфатном буфере с рН 6.8, проведена проверка линейности, правильности и прецизионности определения метамизола натрия. Показано, что без учета фактора отклика детектора валидационные характеристики методики не удовлетворяют соответствующим критериям приемлемости.
Список литературы
U.S. Food and Drug Administration, Center for Drug Evaluation and Research. Guidance for industry: Waiver of in vivo bioavailability and bioequivalence studies for immediate-release solid oral dosage forms based on a Biopharmaceutics Classification System. 2017. www. fda.gov/downloads/Drugs/Guidance (12.26.2017).
Medina J.R., Salazar D.K., Hurtado M., Cortes A.R., Domınguez-Ramırez A.M. Comparative in vitro dissolution study of carbamazepine immediate-release products using the USP paddles method and the flow-through cell system // Saudi Pharm. J. 2014.V. 22. P. 141. https://doi.org/10.1016/j.jsps.2013.02.001
Hassouna M.E.M., Issa Y.M., Zayed A.G. A comparative study of the in-vitro dissolution profiles of paracetamol and caffeine combination in different formulations using HPLC // J. Appl. Pharm. Sci. 2012. V. 2. № 5. P. 52. https://doi.org/10.7324/JAPS.2012.2531
Шамаль Л.Л., Шохин И.Е., Ярушок Т.А., Савченко А.Ю. Тест сравнительной кинетики растворения для стратегически значимого противоопухолевого лекарственного средства – темозоломида // Разработка и регистрация лекарственных средств. 2012. Т. 2. № 3. С. 54.
Василенко Г.Ф., Раменская Г.В., Шохин И.Е., Малашенко Е.А. Оценка возможности замены исследований биоэквивалентности in vivo на изучение сравнительной кинетики эквивалентности in vitro (процедура “Биовейвер”) при определении взаимозаменяемости лекарственных средств (“Дженериков”) // Хим.-фарм. журн. 2011. Т. 2. С. 46.
Guidance on the Investigation of Bioequivalence. European Medicines Agency (EMA). Committee for Medicinal Products of Human Use (CHMP). 2010.
Мкртчян М.А. Фотометрическое исследование водных растворов метамизола натрия // Уч. зап. Ереванского гос. ун-та. 2010. Т. 2. С. 24.
Голубицкий Г.Б., Коспарной А.В., Будко Е.В., Иванов В.М., Басова Е.М. Разложение анальгина в водно-ацетонитрильных растворах // Журн. аналит. химии. 2006. Т. 61. № 10. С. 1081.
Голубицкий Г.Б., Будко Е.В., Иванов В.М. Количественный анализ таблеток “Пенталгин Н” методами градиентной и изократической высокоэффективной жидкостной хроматографии // Журн. аналит. химии. 2006. Т. 61. №1. С. 74.
Голубицкий Г.Б., Басова Е.М., Иванов В.М. Влияние нагрузки на колонку на правильность результатов анализа таблеток “Пенталгин Н” методом градиентной высокоэффективной жидкостной хроматографии // Журн. аналит. химии. 2008. Т. 63. № 3. С. 279.
Giordani M.A., de Melo E.B. Comparative study of the pharmacopeial quality and dissolution profiles of generic and other drug forms of sodium metamizole (dipyrone) sold in Brazil // Rev. Ciênc. Farm. Basica Apl. 2012. V. 33. № 3. P. 347.
Державна Фармакопея України / Державне підприємство “Науково-експертний фармакопейний центр”. 1-е вид. Доповнення 2. Харків: Державне підприємство “Науково-експертний фармакопейний центр”, 2008. 620 с.
Мелентьева Г.А. Фармацевтическая химия. М: Медицина, 1976. С. 398.
Дополнительные материалы отсутствуют.
Инструменты
Журнал аналитической химии