Журнал аналитической химии, 2022, T. 77, № 1, стр. 3-10
СПОСОБ ПРОБОПОДГОТОВКИ ПРИ ОПРЕДЕЛЕНИИ ВОДОРАСТВОРИМЫХ КРАСИТЕЛЕЙ ТРИАРИЛМЕТАНОВОГО РЯДА
А. Н. Зяблов a, *, С. А. Хальзова b, О. В. Дуванова a
a Воронежский государственный университет, химический факультет
394018 Воронеж, Университетская пл., 1, Россия
b МУП “Очистные сооружения” Борисоглебского городского округа Воронежской области
397166 Воронежская обл., Борисоглебский р-н,Борисоглебск, ул. Привольная, 2, Россия
* E-mail: alex-n-z@yandex.ru
Поступила в редакцию 19.05.2021
После доработки 14.07.2021
Принята к публикации 14.07.2021
- EDN: SVSDMO
- DOI: 10.31857/S0044450222010182
Аннотация
Предложен способ пробоподготовки при определении водорастворимых красителей триарилметанового ряда с помощью твердофазной экстракции на γ-оксиде алюминия. Спектрофотометрически определены константы протолиза функциональных групп триарилметановых красителей. Установлена зависимость извлечения красителей оксидом алюминия от рН раствора. Показано, что степень извлечения триарилметановых красителей максимальна при рН 4 и зависит от наличия ионизированных сульфогрупп и количества конденсированных бензольных колец в молекуле.
Синтетические красители находят широкое применение в различных сферах промышленности благодаря высокой красящей способности при малом количестве красителя, стабильности к нагреванию и свету, устойчивости окраски при хранении продукта, а также их низкой себестоимости по сравнению с натуральными красителями. В частности, их используют в качестве заменителей натуральных пигментов в безалкогольных напитках. Наибольшую опасность представляет превышение дозировки и применение запрещенных красителей [1], поэтому контроль содержания синтетических красителей в продуктах питания – весьма актуальная задача. Основная проблема при определении красителей в пищевых продуктах и других объектах заключается в необходимости их экстракции из сложных матриц различными сорбентами [2–11]. Твердофазная экстракция (ТФЭ) обладает широкими возможностями варьирования природы и силы специфических взаимодействий между сорбентом и сорбатом, что позволяет проводить селективное выделение целевых компонентов из пищевых матриц. Однако часто извлечение проходит неполно, поскольку не учитывается влияние рН, и происходит разрушение молекул красителя. Для повышения степени извлечения и выбора оптимальных условий твердофазной экстракции синтетических красителей необходимо изучить их кислотно-основные свойства и сорбционное поведение при изменении рН. Кроме того, анализ литературы показал отсутствие данных по величинам констант протолиза (pK) функциональных групп красителей триарилметанового ряда.
Цель настоящей работы – разработка способа извлечения красителей из водных растворов сорбентом оксидом алюминия для их спектрофотометрического определения.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Реагенты и аппаратура. Использовали красители синий патентованный V (Е131) (Roha, Индия), синий блестящий FCF (Е133) и зеленый S (Е142) (Fluka® Analytical, США) со степенью чистоты 80–85%. Исходные растворы красителей (1 г/л) готовили растворением точной навески в дистиллированной воде. Рабочие растворы (0.005 г/л) получали разбавлением исходного раствора. Для создания необходимого рН использовали 0.1 М HCl и 0.1 M раствор NaOH, стандарт-титры для рН-метрии (ЗАО НП и ИП “Уралхиминвест”, Россия).
Для экстракции синтетических красителей из водных растворов использовали твердофазный патрон, заполненный оксидом алюминия для высокоэффективной жидкостной хроматографии (γ-Al2O3, размер частиц 0.1–0.25 мм, ТУ 2163-011-51444844-2005).
Синтетические красители экстрагировали из модельных водных растворов следующим образом: 10 мл исследуемого раствора с необходимым значением рН (рН раствора доводили до нужного значения 0.1 М HCl) пропускали через патрон, заполненный оксидом алюминия массой 7 г, а затем промывали 20 мл дистиллированной воды. Красители десорбировали 20 мл 14.7 М водного раствора аммиака. Собранный элюат выпаривали досуха на водяной бане. Остаток растворяли в 10 мл дистиллированной воды для спектрофотометрического определения красителей.
Аналогично экстрагировали красители из безалкогольных напитков. Однако поскольку пищевые матрицы характеризуются высоким содержанием добавок (сахар – 300 г/л; лимонная кислота – 4 г/л и др.), затрудняющих сорбцию красителей, для устранения их влияния после сорбции сорбент промывали 1%-ным раствором уксусной кислоты. Обработка раствором уксусной кислоты способствует более полному удалению из сорбента добавок, входящих в состав безалкогольных напитков [12].
Красители определяли в водных растворах по градуировочным графикам на спектрофотометре ПЭ-5300В (ПромЭкоЛаб, Санкт-Петербург, Россия). Спектральный диапазон 325–1000 нм. Погрешность установки длины волны не более ±2 нм. Пределы абсолютной погрешности при измерении спектральных коэффициентов направленного пропускания не более ±0.5% Т. Для построения градуировочных графиков готовили стандартные растворы выбранных красителей из исходных растворов методом последовательного разбавления в диапазоне концентраций 0.001–0.02 г/л.
По полученным данным рассчитывали степень извлечения (R, %):
где с0 – концентрация определяемого вещества в растворе до экстракции, г/л; с – концентрация вещества в растворе после экстракции, г/л.Значения коэффициентов распределения красителей (D) находили по уравнению:
где V – объем анализируемого раствора, л; m – масса навески сорбента, г.Значения рН контролировали рН-метром МАРК-901 (Н. Новгород, Россия). Пределы допускаемой основной абсолютной погрешности ±0.1 ед. рН.
Методика эксперимента. Триарилметановые красители имеют хромофорную группу (хиноидное ядро), поэтому для определения констант протолиза применяли спектрофотометрический метод. Для создания необходимого значения рН раствора использовали 0.1 М HCl, 0.1 M раствор NaOH и буферные растворы, приготовленные из стандарт-титров для рН-метрии (гидротартрат калия KC4H5O6, насыщенный при 25°С с рН 3.56; гидрофталат калия C8H6O4K 0.05 моль/кг с рН 4.01; дигидрофосфат калия KH2PO4 0.025 моль/кг и гидрофосфат натрия Na2HPO4 0.025 моль/кг с рН 6.86; тетраборат натрия Na2B4O7⋅10H2O 0.01 моль/кг с рН 9.18). Затем снимали спектры поглощения индивидуальных растворов, содержащих только один вид ионов, находящихся в равновесии с недиссоциированной формой, при длине волны 640 нм. По экспериментальным данным рассчитывали константы протолиза по уравнениям (3) и (4). Если определяемая функциональная группа кислотная, то использовали уравнение (3), если основная, то уравнение (4):
где A – оптическая плотность раствора, содержащего обе ионные формы при одной и той же длине волны; Am и A1 – оптические плотности при выбранной длине волны, отвечающие полному превращению в одну из крайних ионных форм [13].В работе также использовали метод добавок [14]:
где Аx – оптическая плотность исследуемого раствора; Аx + доб – оптическая плотность исследуемого раствора с добавкой; cx – неизвестная концентрация определяемого вещества в исследуемом окрашенном растворе; cдоб – концентрация добавки в исследуемом растворе (из расчета только добавленного количества); Vдоб – объем раствора добавки, мл; Vx + a – объем окрашенного исследуемого раствора с добавкой, мл.РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
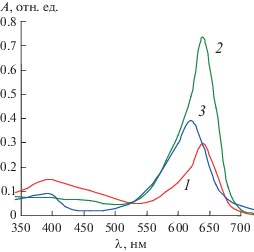
Триарилметановые красители представляют собой соли слабых оснований. При действии воды они гидролизуются. В зависимости от pH среды равновесие может быть сдвинуто либо в сторону бесцветной недиссоциированной (рН > 7), либо окрашенной диссоциированной (рН < 7) формы. Наличие окраски триарилметановых красителей обусловлено цепью сопряжения, включающей бензольные кольца, и присутствием донорно-акцепторных заместителей, вызывающих ионизацию молекулы [15, 16]. Установлено, что все ионные формы красителя Е133 (рис. 1) имеют полосы поглощения при длине волны 640 нм (табл. 1), в случае красителей Е131 и Е142 в щелочной среде происходит гипсохромное смещение полос поглощения (рис. 2, 3). Такое смещение можно объяснить перераспределением электронной плотности при отщеплении протона от гидроксильной группы, которая находится у Е131 в мета-, а у Е142 в орто-положении к центральному атому углерода. При рН < 7 наблюдается гиперхромный эффект (увеличение интенсивности поглощения), который связан с нарушением пространственной симметрии молекулы из-за протонирования сульфогрупп и перераспределением электронной плотности в хиноидном кольце [17, 18]. При увеличении рН от 7 до 10 происходит снижение интенсивности поглощения, связанное с диссоциацией второй сульфогруппы и восстановлением пространственной симметрии молекулы.
Рис. 1.
Спектры поглощения водных растворов красителя синего блестящего FCF Е133 при значениях рН 0.97 (1), 4.86 (2), 13.01 (3).

Таблица 1.
Значение λmax и коэффициента молярного поглощения (ε) красителей при разных условиях
| Краситель | Формула | рН (±0.1) | λmax, нм | ε × 10–4, л моль–1 см–1 |
|---|---|---|---|---|
| Синий патентованный V; Е131 | 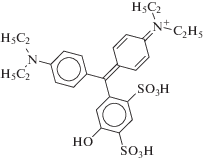 |
2.16 | 660 | 0.75 |
| 6.31 | 638 | 10.51 | ||
| 13.61 | 620 | 9.47 | ||
| Синий блестящий FCF; Е133 |  |
0.97 | 640 | 6.06 |
| 4.86 | 640 | 10.29 | ||
| 13.01 | 640 | 7.98 | ||
| Зеленый S; Е142 |  |
1.02 | 640 | 3.40 |
| 5.45 | 640 | 8.48 | ||
| 12.94 | 620 | 4.51 |
Рис. 2.
Спектры поглощения водных растворов красителя синего патентованного V Е131 при значениях рН 2.16 (1), 6.31 (2), 13.61 (3).

Рис. 3.
Спектры поглощения водных растворов красителя зеленого S Е142 при значениях рН 1.02 (1), 5.45 (2), 12.94 (3).
Диаграммы распределения ионных форм красителей представлены на рис. 4. Рассчитанные по уравнениям (3) и (4) константы протолиза синтетических красителей приведены в табл. 2.
Рис. 4.
Диаграммы распределения ионных форм триарилметановых красителей Е131 (а), Е133 (б), Е142 (в): 1 – H3R+, 2 – H2R±, 3 – НR–, 4 – R2–.

Таблица 2.
Величины рK функциональных групп триарилметановых красителей (n = 3, P = 0.95)
| Краситель | рK | Функциональная группа | Форма иона |
|---|---|---|---|
| Е 131 | 3.11 ± 0.09 | HSO3 | Переход однозарядного катиона в биполярный ион |
| 7.50 ± 0.23 | HSO3 | Переход из биполярного иона в однозарядный анион | |
| 8.49 ± 0.25 | OH | Переход из одно- в двухзарядный анион | |
| Е133 | 1.93 ± 0.06 | HSO3 | Переход однозарядного катиона в биполярный ион |
| 7.58 ± 0.23 | HSO3 | Переход из биполярного иона в однозарядный анион | |
| 9.87 ± 0.30 | HSO3 | Переход из одно- в двухзарядный анион | |
| Е142 | 1.81 ± 0.05 | HSO3 | Переход однозарядного катиона в биполярный ион |
| 7.65 ± 0.23 | HSO3 | Переход из биполярного иона в однозарядный анион | |
| 8.77 ± 0.26 | OH | Переход из одно- в двухзарядный анион |
Таким образом, все изученные триарилметановые красители в зависимости от рН находятся в водном растворе в виде однозарядных катионов, биполярных ионов или одно-двухзарядных анионов.
Оксид алюминия представляет собой полярный адсорбент с гетерогенной поверхностью, имеющий активные кислотные и основные бренстедовские, кислотные льюисовские центры. Зависимость степени извлечения красителей на оксиде алюминия от рН раствора представлена на рис. 5. На сорбцию триарилметановых красителей на поверхности оксида алюминия влияет рН среды. При уменьшении рН увеличивается число бренстедовских кислотных центров на поверхности, что приводит к росту общего положительного заряда [19, 20] и существенно отражается на сорбции красителей. По формулам (1) и (2) рассчитали степени извлечения и коэффициенты распределения красителей на оксиде алюминия. Данные представлены в табл. 3.
Рис. 5.
Зависимость степени извлечения красителей на оксиде алюминия от рН: 1 – синий патентованный V Е131, 2 – зеленый S Е142, 3 – синий блестящий FCF Е133.
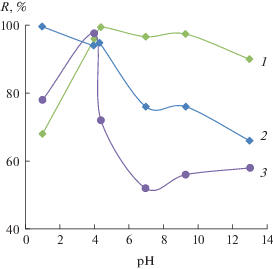
Таблица 3.
Параметры сорбции красителей на оксиде алюминия при различных значениях рН раствора (n = 3, P = 0.95)
| Краситель | рН 1 | рН 4 | рН 7 | рН 9 | sr, % | ||||
|---|---|---|---|---|---|---|---|---|---|
| R, % | D, л/г | R, % | D, л/г | R, % | D, л/г | R, % | D, л/г | ||
| Е131 | 68.0 | 0.003 | 99.4 | 0.237 | 96.6 | 0.041 | 97.4 | 0.054 | 3.3 |
| Е133 | 78.0 | 0.005 | 97.6 | 0.058 | 52.0 | 0.002 | 56.0 | 0.002 | 4.1 |
| Е142 | 99.6 | 0.356 | 94.8 | 0.026 | 76.0 | 0.005 | 76.0 | 0.005 | 3.6 |
На основании полученных данных можно предложить следующую схему процессов сорбции: в кислой области преобладают электростатические взаимодействия между положительно заряженной поверхностью оксида алюминия и биполярными ионами или анионами красителей (рис. 6а). Так, для Е142 увеличение сорбции при рН < 2 связано с взаимодействием ОН-групп с ионами алюминия по механизму комплексообразования (рис. 6б) [21, 22]. Степень извлечения красителей Е131 и Е133 максимальна при рН 4, для Е142 при рН 1–4 (табл. 3). При увеличении рН сорбция триарилметановых красителей уменьшается, что связано с перераспределением электронной плотности в структуре молекулы и уменьшением доли электростатических взаимодействий. Вблизи точки нулевого заряда (для γ-Al2O3 это рН 7.4) преобладает сорбция за счет специфических взаимодействий сопряженной π-системы красителей и гидроксильных групп поверхности (рис. 6в) [23]. Этим можно объяснить близость коэффициентов распределения красителей Е133 и Е142 при рН 7.5–9.0 (табл. 3). Сорбция красителя Е131 с увеличением рН раствора уменьшается незначительно. Вероятно, это связано с тем, что молекула этого красителя более симметричная и возможно дополнительное взаимодействие иона =N+(С2Н5)2 в водном растворе с основными центрами оксида алюминия (рис. 6г). При рН > 9 поверхность оксида алюминия заряжается отрицательно, что приводит к падению сорбции, так как в этих условиях триарилметановые красители отрицательно заряжены.
Рис. 6.
Схема процессов сорбции, протекающих на поверхности оксида алюминия на примере синего патентованного V: (а) – электростатические взаимодействия с кислотными центрами поверхности; (б) – образование координационной связи; (в) – взаимодействия сопряженной π-системы красителя и гидроксильных групп поверхности; (г) – электростатические взаимодействия с основными центрами поверхности.

Степень извлечения триарилметановых красителей при рН 2–4 зависит от наличия ионизированных сульфогрупп и количества бензольных колец. Максимальная степень извлечения триарилметановых красителей наблюдается при рН 4, когда красители в растворе находятся преимущественно в форме биполярных ионов. В этом случае сорбция осуществляется за счет электростатических взаимодействий биполярных ионов с положительно заряженной поверхностью оксида алюминия.
В отличие от методики ГОСТ [24], разработанный нами способ пробоподготовки при определении водорастворимых красителей триарилметанового ряда проще в исполнении, не требует предварительного промывания твердофазного патрона раствором уксусной кислоты, что позволяет сократить количество используемых реактивов и соответственно время пробоподготовки. Правильность определения красителей в модельных растворах с использованием предложенного способа пробоподготовки проверяли методом введено–найдено (табл. 4). Установлено, что относительное стандартное отклонение не превышает 10%.
Таблица 4.
Результаты (г/л) определения красителей в модельных растворах методом введено–найдено (n = 5, Р = 0.95)
| Объект анализа | Введено | Найдено | sr, % |
|---|---|---|---|
| Модельный раствор Е131 | 0.005 | 0.0023 ± 0.0002 | 8.7 |
| 0.05 | 0.048 ± 0.002 | 4.2 | |
| 0.1 | 0.088 ± 0.006 | 5.7 | |
| Модельный раствор Е133 | 0.01 | 0.0099 ± 0.0006 | 5.1 |
| 0.05 | 0.039 ± 0.004 | 7.7 | |
| 0.1 | 0.113 ± 0.006 | 4.4 | |
| Модельный раствор Е142 | 0.01 | 0.0088 ± 0.0007 | 5.9 |
| 0.05 | 0.052 ± 0.005 | 3.2 | |
| 0.1 | 0.097 ± 0.011 | 2.8 |
С помощью предложенного способа провели пробоподготовку безалкогольных напитков: морса “Северная ягода” (Фруктовый сад), “Соччи со вкусом малины и черники” (АкваТрайпл), “Тархун Star Bar” (ООО “ФКПЧФ Бобимэкс тм”) с последующим спектрофотометрическим определением красителей. В исследованных напитках обнаружили красители Е131 и Е133 в дозировках, не превышающих рекомендуемые 10–15 мг/мл (табл. 5).
Таблица 5.
Содержание триарилметановых красителей в безалкогольных напитках (n = 3, P = 0.95)
| Напиток | Краситель | с, мг/л | sr, % |
|---|---|---|---|
| Морс “Северная ягода” | Е131 | 1.00 ± 0.03 | 1.2 |
| “Соччи со вкусом малины и черники” | Е131 | 5.22 ± 0.16 | 6.4 |
| “Тархун Star Bar” | Е133 | 2.31 ± 0.07 | 2.8 |
Для оценки правильности спектрофотометрического определения красителей в безалкогольных напитках применяли метод добавок (табл. 6). Установили, что относительное стандартное отклонение не превышает 8%, кроме того, данный способ пробоподготовки позволяет избежать потери красителей при извлечении из безалкогольных напитков.
Таблица 6.
Результаты (мг/л) определения красителей в безалкогольных напитках методом добавок (n = 5, Р = 0.95)
| Напиток | Краситель | c красителя в соке |
сдоб | cx | sr, % |
|---|---|---|---|---|---|
| Морс “Северная ягода” | E131 | 1.00 ± 0.03 | 1.5 | 1.12 ± 0.06 | 7.8 |
| “Соччи со вкусом малины и черники” | E131 | 5.22 ± 0.16 | 10.0 | 4.81 ± 0.07 | 6.9 |
| “Тархун Star Bar” | E133 | 2.31 ± 0.07 | 5.0 | 2.13 ± 0.09 | 7.1 |
* * *
Таким образом, установлено, что использование твердофазной экстракции синтетических триарилметановых красителей оксидом алюминия при рН 4 позволяет селективно извлекать их из водных растворов при полноте сорбции >94%. При этом сорбция осуществляется за счет электростатических взаимодействий между положительно заряженной поверхностью оксида алюминия и биполярными ионами красителей, специфических взаимодействий сопряженной π-системы красителей и гидроксильных групп поверхности, взаимодействия ОН-групп с ионами алюминия по механизму комплексообразования, а также за счет взаимодействия четвертичного атома азота с основными центрами. Предложенный способ пробоподготовки апробирован при спектрофотометрическом определении красителей Е131 и Е133 в безалкогольных напитках.
Список литературы
Попович Н.А., Катаева С.Е., Мельниченко Т.И. К оценке опасности применения синтетических пищевых красителей // Современные проблемы токсикологии. 2000. № 2. С. 33.
Санникова Н.Ю., Коренман Я.И., Суханов П.Т. Экстракция синтетических пищевых красителей. Воронеж: Воронежский ЦНТИ – филиал ФГБУ “РЭА” Минэнерго России, 2012. 147 с.
Рамазанова Г.Р., Тихомирова Т.И., Апяри В.В. Сорбция пищевого красителя Желтый “Солнечный закат” FCF из водных растворов и его определение с использованием спектроскопии диффузного отражения // Журн. аналит. химии. 2015. Т. 70. № 6. С. 602. DOI 10.7868/S0044450215060146 (Ramazanova G.R., Tikhomirova T.I., Apyari V.V. Adsorption of Sunset Yellow FCF food dye from aqueous solutions and its determination by diffuse reflectance spectroscopy // J. Anal. Chem. 2015. V. 70. № 6. P. 685.)
Хальзова С.А., Зяблов А.Н., Дуванова О.В. Сорбция триарилметановых красителей полимерами с молекулярными отпечатками // Сорбционные и хроматографические процессы. 2017. Т. 17. №. 2. С. 307.
Marchese L., Bordiga S., Coluccia S., Martra G., Zecchina A. Structure of the surface sites of delta–Al2O3 as determined by high-resolution transmission electron - microscopy, computer modeling and infrared spectroscopy of adsorbed CO // J. Chem. Soc. Faraday Trans. 1993. V. 89. P. 3483. https://doi.org/10.1039/ft9938903483
Зяблов А.Н., Хальзова С.А., Селеменев В.Ф. Сорбция красных пищевых красителей полимерами с молекулярными отпечатками // Изв. вузов. Серия химия и хим. технол. 2017. Т. 60. № 7. С. 42. https://doi.org/10.6060/tcct.2017607.5595
Kucharska M., Grabka J. A review of chromatographic methods for determination of synthetic food dyes // Talanta. 2010. V. 80. № 3. P. 1045. https://doi.org/10.1016/j.talanta.2009.09.032
Trandafir I., Nour V., Ionica M.E. The liquid-chromatographic quantification of some synthetic colorants in soft drinks // Sci. Study Res.: Chem. Chem. Eng. Biotechnol. Food Industry. 2009. V. 10. № 1. P. 73.
Хальзова С.А., Кривоносова Д.А., Зяблов А.Н., Дуванова О.В. Определение синтетических красителей Е102, Е110, Е122 и Е124 в безалкогольных напитках модифицированными пьезосенсорами // Аналитика и контроль. 2017. Т. 21. № 2. С. 85. https://doi.org/10.15826/analitika.2017.21.2.006
Пацовский А.П., Рудометова Н.В., Каменцев Я.С. Электрофоретическое определение синтетических красителей в алкогольных напитках // Журн. аналит. химии. 2003. Т. 58. № 12. С. 170. (Patsovskii A.P., Rudometova N.V., Kamentsev Ya.S. Electrophoretic determination of synthetic dyes in alcoholic beverages // J. Anal. Chem. 2004. V. 59. № 2. P. 150.)
Киселева М.Г., Пименова В.В., Эллер К.И. Оптимизация условий определения синтетических красителей в пищевых продуктах методом ВЭЖХ // Журн. аналит. химии. 2003. Т. 58. № 7. С. 766. (Kiseleva M.G., Pimenova V.V., Eller K.I. Optimization of conditions for the hplc determination of synthetic dyes in food // J. Anal. Chem. 2003. V. 58. № 7. P. 685.)
Рудометова Н.В. Особенности выделения синтетических красителей из консервированных компотов // Хранение и переработка сельхозсырья. 2012. № 2. С. 47.
Альберт А., Сержент Е. Константы ионизации кислот и оснований. М.: Химия, 1964. 180 с.
Булатов М.И., Калинкин И.П. Практическое руководство по фотоколориметрическим и спектрофотометрическим методам анализа. Л.: Химия, 1976. 384 с.
Красовицкий Б.М., Болотин Б.М. Органические люминофоры. М.: Химия, 1984. 334 с.
Гордон П.Ф., Грегори П. Органическая химия красителей. М.: Мир, 1987. 344 с.
Свердлова О.В. Электронные спектры в органической химии. Л.: Химия, 1985. 248 с.
Венкатараман К. Аналитическая химия синтетических красителей. Л.: Химия, 1979. 576 с.
Танабе К. Твердые кислоты и основания. М.: Мир, 1973. 184 с.
Иконникова К.В., Саркисов Ю.С., Иконникова Л.Ф. Диагностика фазовых превращений по кислотно-основным параметрам гидроксоаквакомплексов // Материаловедение. 2005. № 5. С. 16.
Тихомирова Т.И., Кубышев С.С., Иванов А.В., Нестеренко П.Н. Сорбент на основе оксида алюминия, модифицированного тайроном // Журн. физ. химии. 2009. Т. 83. № 7. С. 1360. (Tikhomirova T.I., Kubyshev S.S., Ivanov A.V., Nesterenko P.N. Sorbent based on aluminum oxide modified with Tiron // J. Phys. Chem. A. 2009. V. 83. № 7. Р. 1208.)
Хальзова С.А. Определение синтетических красителей в жидких средах пьезоэлектрическими сенсорами, модифицированными полимерами с молекулярными отпечатками. Дис… канд. хим. наук. Воронеж: Воронежский государственный университет, 2018. 156 с.
Тихомирова Т.И., Кубышев С.С., Иванов А.В. Модифицирование поверхности оксида алюминия полифункциональными органическими реагентами // Журн. физ. химии. 2013. Т. 87. № 8. С. 1366. DOI (Tikhomirova T.I., Kubyshev S.S., Ivanov A.V. Modification of the alumina surface with polyfunctional organic reagents // J. Phys. Chem. A. 2013. V. 87. № 8. Р. 1357.)https://doi.org/10.7868/S0044453713070340
ГОСТ Р 54491-2011. Консервы фруктовые. Метод определения наличия хинолиновых, триарилметановых и азокрасителей. М.: Стандартинформ, 2012. 12 с.
Дополнительные материалы отсутствуют.
Инструменты
Журнал аналитической химии


