Журнал аналитической химии, 2022, T. 77, № 12, стр. 1138-1146
Соотношения стабильных изотопов (H, C, О) в образцах меда из разных регионов России
Д. А. Калашникова a, *, Г. В. Симонова a
a Институт мониторинга климатических и экологических систем Сибирского отделения Российской академии наук
634055 Томск, просп. Академический, 10/3, Россия
* E-mail: terrezaprk@mail.ru
Поступила в редакцию 20.01.2022
После доработки 09.02.2022
Принята к публикации 09.02.2022
- EDN: NLHCWL
- DOI: 10.31857/S0044450222120076
Аннотация
Представлены результаты анализа соотношений стабильных изотопов водорода, кислорода и углерода в образцах меда, отобранных в регионах России с различными климатическими условиями. Значения изотопного состава во всех исследуемых образцах меда варьировали для углерода от –29.5 до –24.2‰, для водорода от –116.6 до –34.5‰, для кислорода от +12.7 до +25.7‰. Показано, что величины изотопного состава углерода (δ13С), водорода (δ2Н) и кислорода (δ18О) в меде можно использовать для установления географического происхождения меда. Обнаружено, что средние величины δ2Н и δ18О в меде в значительной степени коррелируют со средними величинами δ2Н и δ18О в атмосферных осадках в регионах происхождения меда. На изотопный состав углерода влияет климат. Выявлены три зоны “изотопного ландшафта” для регионов России: самые низкие значения величин δ13С, δ2Н и δ18О характерны для сибирских образцов меда, промежуточные значения соответствовали образцам меда из европейской части России, а самые высокие значения зафиксированы для образцов меда Черноморского региона.
Мед как продукт натурального происхождения пользуется особым статусом среди потребителей не только как источник энергии, но и благодаря своим свойствам, способствующим укреплению здоровья. Однако в погоне за прибылью недобросовестные пчеловоды и продавцы подделывают натуральный мед дешевыми добавками, вводя в заблуждение потребителей, которые считают, что покупают чистый мед из определенного географического региона. Для подделки меда в основном используют замену или добавление основных компонентов меда, т.е. воды и сахара. В более сложных поддельных образцах меда могут применяться сахарные сиропы, искусственный мед, а также неправильная маркировка в отношении ботанического или географического происхождения [1]. Обычно для установления ботанического и географического происхождения меда определяют физико-химические показатели (например, диастазное число и массовую долю воды), органолептические параметры (например, аромат и вкус), а также проводят пыльцевой анализ (мелиссопалинологический анализ) [2]. Однако эти методы не позволяют обнаружить незначительные фальсификации, а в случае контроля географического происхождения они неприменимы, например, когда исследуется уже отфильтрованный мед. В последние годы изотопная масс-спектрометрия становится все более важным инструментом идентификации подлинности пищевых продуктов [3], так как этот метод позволяет выявить фальсификацию или подмену пищевых продуктов даже тогда, когда фальсифицированная продукция по своим физико-химическим свойствам оказывается идентичной оригинальному продукту. Стабильные изотопы в составе пищи являются средством регистрации условий окружающей среды в зоне происхождения продуктов питания [4], поэтому изотопный анализ биоэлементов (Н, С, О, N, S) приобретает все большее значение в определении географического происхождения продуктов питания.
Исследованию изотопного состава меда посвящено много публикаций за рубежом [5, 6]. В рамках Европейского проекта TRACE-006942 “Отслеживание продовольственных товаров в Европе” проведен анализ стабильных изотопов углерода, азота, серы и водорода в белковой фракции меда, отобранного в 20 регионах Европы [7]. Перспективность использования стабильных изотопов водорода для определения региона происхождения меда при анализе воска, отобранного из меда в сотах, проиллюстрирована в работе американских исследователей [8]. В России подобные исследования единичны [9, 10].
Цель нашего исследования заключалась в проведении комплексного изотопного анализа соотношений изотопов углерода (13C/12C), водорода (2Н/1H) и кислорода (18О/16О) в образцах меда для подтверждения региона его происхождения, опираясь на предположение, что соотношение изотопов водорода и кислорода в растительном нектаре, собранном пчелами, отражает изотопный состав воды, так как растения используют местную воду для производства нектара, изотопный состав которого затем регистрируется непосредственно в меде. Чтобы проверить эту гипотезу, была проанализирована взаимосвязь между изотопным составом образцов меда из регионов России с разными климатическими условиями и регионом происхождения, представленным изотопным составом локальных метеорных вод. Для исключения из исследования поддельных медов, фальсифицируемых добавлением сахаров, полученных из растений с С4 типом фотосинтеза, предварительно провели изотопный анализ углерода меда и его белковой фракции.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В период с 2019 по 2021 гг. отобрали 98 образцов меда, приобретенных как на медовых ярмарках, так и непосредственно на пасеках, располагающихся в регионах России (рис. 1) с различными климатическими условиями. Были отобраны монофлерные меда (липовый, рапсовый, акациевый, гречишный), разнотравный мед и мед неизвестного цветочного происхождения. Отобранные образцы меда помещали во флаконы с ограниченным свободным пространством с целью минимизации обмена с парами воды из атмосферы окружающей среды.
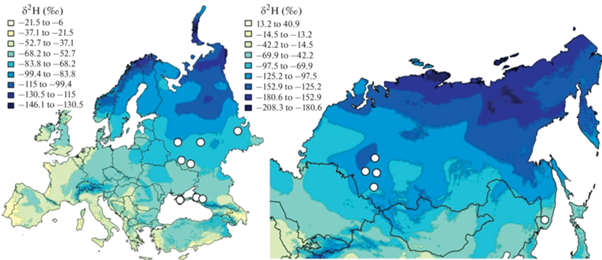
Рис. 1.
Зоны отбора образцов меда в ходе данного исследования на карте прогнозируемых среднегодовых значений изотопного состава водорода атмосферных осадков для европейской (справа) и азиатской (слева) частей России [11].
Изотопный анализ проводили методом изотопной масс-спектрометрии с использованием изотопного масс-спектрометра DELTA V Advantage (Thermo Fisher Scientific, Германия), совмещенного с элементным анализатором Flash 2000. Приборы предоставлены ТомЦКП СО РАН. Определение изотопного состава общего углерода в меде основано на мгновенном сгорании пробы в окислительно-восстановительном реакторе в потоке гелия при добавлении кислорода (180 мл/мин). Перед измерением образец меда перемешивали до однородности, взвешивали навеску массой 0.45–0.55 мг в оловянном тигле. Запакованные в тигли образцы в автоматическом режиме с помощью автосамплера попадали в окислительно-восстановительный реактор (рабочая температура 1020°С), где происходило окисление пробы до простых газов (NOx, СО2) и воды. В реакторе в потоке гелия (70 мл/мин) продукты разложения проходили через восстановленную медь, при этом оксиды азота превращались в N2, а избыток кислорода удалялся. Образовавшиеся газы проходили через ловушку для удаления воды – стеклянную полую трубку, заполненную осушителем (перхлорат магния), попадали в хроматографическую колонку, где выполнялось разделение смеси газов на CO2 и N2, которые затем поступали в масс-спектрометр через газораспределительную систему Conflo II.
Для определения величин δ2Н и δ18О навески меда массой 0.2–0.3 мг взвешивали в серебряных тиглях. Пробы сжигали в пиролитическом реакторе без подачи кислорода при 1350°С. Температуру печи устанавливали 90°C, скорость потока газа-носителя (He) составляла 70 мл/мин. Продукты пиролиза в потоке гелия попадали через хроматографическую колонку в газораспределительную систему (Conflo II) и далее в ионный источник масс-спектрометра. Результаты измерения рассчитывали автоматически с помощью программного комплекса управления прибором и обработки данных.
Изотопный состав δ измеряется в промилле (‰) и определяется по формуле:
(1)
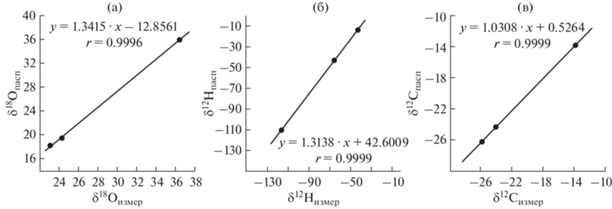
${{{{\delta }}}^{n}}X = \left[ {\frac{{{{R}_{{{\text{образец}}}}} - {{R}_{{{\text{стандарт}}}}}}}{{{{R}_{{{\text{стандарт}}}}}}}} \right] \times 1000,$Измеренные величины изотопного состава углерода, кислорода и водорода пересчитывали с использованием градуировочных графиков для определения истинного значения изотопного состава. Для получения уравнения градуировочного графика y = kx + b определяли изотопный состав углерода, кислорода и водорода в международных стандартах меда и муки Геологической службы США (USGS) [12]: USGS82 – международный стандарт тропического Вьетнамского меда со значениями δ13СVPDB= –24.31 ± 0.08‰, δ18ОVSMOW = = +19.44 ± 0.36‰ и δ2НVSMOW = –43.1 ± 3.7‰; USGS83 – международный стандарт меда из прерий Канады со значениями δ13СVPDB = –26.20 ± ± 0.08‰, δ18ОVSMOW = +18.13 ± 0.11‰ и δ2НVSMOW = = –10.5 ± 3.5‰; USGS90 – международный стандарт пшенной муки из Тосканы (Италия) со значениями δ13СVPDB = –13.78 ± 0.06‰, δ18ОVSMOW = = +35.90 ± 0.29‰ и δ2НVSMOW = –13.9 ± 2.4‰. На графиках (рис. 2) по оси Y нанесены паспортные значения изотопного состава, а по оси Х – измеренные значения. По методу наименьших квадратов определяли величину наклона линии k (“наклон”) и величину свободного члена – b “отрезок”), а также коэффициент детерминации – r.
Рис. 2.
Примеры градуировочных графиков с уравнениями для стабильных изотопов: кислорода (а), водорода (б) и углерода (в).
Воспроизводимость результатов изотопного анализа двух повторных измерений составляла: для углерода не более 0.2‰; для кислорода не более 0.6‰; для водорода не более 2‰.
Для статистической обработки данных использовали пакет “Анализ данных” в Microsoft Excel. Основная описательная статистика включала среднее значение (среднее арифметическое), стандартное отклонение (σ), минимум, максимум и размах выборки. Для анализа измеренных значений величин δ13С, δ2Н и δ18О применяли линейный регрессионный анализ.
Для обнаружения подделки меда с помощью растительных сахаров, получаемых из растений с C4 типом фотосинтеза, использовали официально принятый Ассоциацией аналитической химии метод обнаружения с применением изотопной масс-спектрометрии [13], основывающийся на сравнении величин δ13C чистого меда и экстрагированной из него белковой фракции. Методика экстрагирования белковой фракции из меда подробно описана в работе [14].
Взаимосвязь между изотопным составом водорода и кислорода метеорных вод и соотношением изотопов водорода и кислорода меда анализировали с помощью интерполированных величин δ2Н и δ18О метеорных вод, ранее полученных по сети GNIP (Global Network of Isotopes in Precipitation) для сопредельных территорий с использованием онлайн-калькулятора, размещенного на портале Waterisotopes Database [15].
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
В табл. 1 представлены измеренные средние значения величин δ13C, δ2Н и δ18О меда со стандартным отклонением и количеством образцов (N).
Таблица 1.
Результаты изотопного анализа меда из разных регионов России
| Регион | δ13СV-PDB, ‰ | δ2HV-SMOW, ‰ | δ18OV- SMOW, ‰ | ||||||
|---|---|---|---|---|---|---|---|---|---|
| среднее | σ | N | среднее | σ | N | среднее | σ | N | |
| Томская область | –27.0 | 0.7 | 39 | –97.6 | 13.8 | 9 | 18.2 | 0.9 | 8 |
| Алтайский край | –27.6 | 1.0 | 16 | –95.8 | 17.7 | 9 | 17.7 | 2.4 | 9 |
| Кемеровская область | –27.1 | 0.5 | 5 | –95.3 | 12.4 | 2 | 14.1 | 2.0 | 2 |
| Новосибирская область | –28.2 | – | 1 | –81.7 | – | 1 | 14.8 | – | 1 |
| Республика Башкортостан | –26.5 | 1.1 | 7 | –67.2 | 21.3 | 6 | 21.7 | 3.2 | 6 |
| Калужская область | –27.4 | 0.1 | 2 | –69.0 | 8.6 | 2 | 20.1 | 0.1 | 2 |
| Приморский край | –25.6 | 0.7 | 3 | –65.2 | 4.7 | 3 | 20.0 | 2.8 | 3 |
| Краснодарский край | –25.5 | 0.8 | 10 | –47.8 | 16.5 | 9 | 23.8 | 1.2 | 9 |
| Белгородская область | –25.0 | 0.1 | 2 | –41.0 | 7.3 | 2 | 25.3 | 0.6 | 2 |
| Курская область | –27.4 | – | 1 | –58.3 | – | 1 | 21.8 | – | 1 |
| Республика Адыгея | –25.7 | 1.3 | 3 | –67.7 | 17.1 | 3 | 21.7 | 3.8 | 3 |
| Республика Мордовия | –26.8 | – | 1 | –70.4 | – | 1 | 21.2 | – | 1 |
| Республика Крым | –25.2 | – | 1 | –43.2 | – | 1 | 24.8 | – | 1 |
Изотопный состав углерода. Изотопный состав углерода в меде зависит от природных условий, в которых произрастает медоносное растение, от его вида и пути фотосинтеза. Пчелы предпочитают медоносные растения с С3 типом фотосинтеза и очень редко используют растения с C4 и CAM типом фотосинтеза [16]. Диапазон значений величины δ13C составляет от −32 до −21‰ для растений с С3 типом фотосинтеза и от –19 до –10‰ для растений с С4 типом фотосинтеза. Эти различия в диапазонах значений изотопного состава углерода используют для обнаружения меда, сфальсифицированного добавлением сахарных сиропов, полученных из сахарного тростника и кукурузы (растения с С4 типом фотосинтеза) [17]. Разница в соотношении стабильных изотопов углерода между медом и его белковой фракцией позволяет выявить фальсификацию меда с использованием растительных сахаров, получаемых из растений с C4 типом фотосинтеза. Для исключения из последующих анализов поддельных медов из всех образцов меда выделили белковую фракцию и проанализировали ее изотопный состава углерода. Для чистого (неподдельного) меда значения величины δ13C варьировались от –29.5 до –24.2‰, а для его белковой фракции от −29.1 до −24.3‰. Значения величины δ13C всех образцов чистого меда <–23‰; разница величин δ13C между медом и экстрагированной из него белковой фракцией менее 1‰. В то же время для фальсифицированного меда величина δ13C варьировалась от –28.7 до –22.3‰, а диапазон значений величины δ13C для белковой фракции составил от −30.5 до −24.2‰. Разница величин δ13C между поддельным медом и экстрагированной из него белковой фракцией варьировалась от 1.1 до 2.5‰. Процент содержания сахара, полученного из растений с С4 типом фотосинтеза, составил от 6.4 до 13.1%. Таким образом, из 98 образцов меда 7 образцов оказались поддельными и были исключены из дальнейшего анализа.
Изотопный состав углерода в меде позволяет не только определить фальсификацию меда с использованием сахарных сиропов, полученных из растений с С4 типом фотосинтеза, но и выявить неправильную маркировку в отношении географического происхождения меда. Легкий изотопный состав углерода в меде можно ожидать для регионов с низкими средними температурами и более высокой влажностью воздуха, а с уменьшением влажности и ростом температуры происходит утяжеление изотопного состава углерода в растениях [18] и, как следствие, в нектаре медоносных растений и меде.
На рис. 3 представлены результаты определения изотопного состава углерода в меде из разных регионов России. Измеренные значения величины δ13С изменялись от –29.5 до –24.4‰. Наибольший разброс значений величины δ13С (3.2‰) зафиксирован в образцах Алтайского меда, что можно объяснить большим количеством разных видов меда с разными сроками сбора и, следовательно, с разными диапазонами температур атмосферного воздуха в период сбора нектара, ведущими к разным значениям величины δ13C. Также широкий разброс значений величины δ13C образцов меда из одного географического региона обусловлен разными климатическими условиями даже на небольших расстояниях. Например, в Алтайском крае на расстоянии всего в 200–300 км расположены степная зона с сухим и засушливым климатом и предгорья Алтая с более прохладным климатом. Несмотря на эти вариации мезоклимата, разница в “глобальном” климате России достаточно заметна, что и продемонстрировали вариации величины δ13С в образцах меда. Самые высокие значения, как и ожидалось, обнаружены для образцов меда из регионов с теплым морским климатом: вблизи Черного моря со значениями δ13С от –26.4 до –24.2‰ (крымский, туапсинский, краснодарский мед) и в Приморском крае (δ13С = –25.6 ± 0.7‰). Образцы меда, отобранные в регионах с умеренными климатическими условиями, имели промежуточные значения δ13С от –26.8 до –26.1‰ (Республики Башкортостан и Мордовия). Сибирский мед (алтайский, томский, кемеровский и новосибирский) показал самые низкие значения величины δ13С от –29.5 до –25.9‰. Средние значения величины δ13С приведены в табл. 1.
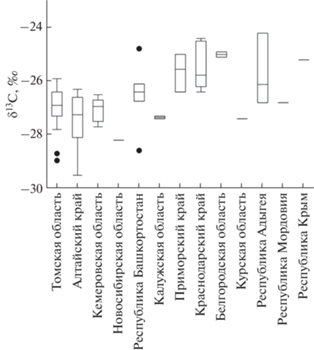
Рис. 3.
Диаграмма значений величины δ13С в меде из разных регионов России: диапазон между первым и третьим квартилем распределения заключен в рамку, вертикальные линии (“усы”) на нижнем и верхнем концах оси рамки представляют минимальные и максимальные значения, которые не считаются экстремальными значениями, вертикальная линия в рамке – среднее значение распределения; точками обозначены экстремальные значения.
Изотопный состав водорода и кислорода. Известно, что фракционирование изотопов водорода и кислорода в осадках в значительной степени зависит от климатических условий и преобладающего региона – источника атмосферной влаги [19]. Значения величин δ2H и δ18О изменяются предсказуемым образом: уменьшаются с увеличением расстояния до моря, с увеличением высоты и снижением средней температуры в конкретном регионе [20], т.е. более низкие значения величин δ2H и δ18О соответствуют высокогорным, внутренним и прохладным климатическим регионам, а более высокие значения – низкогорным, прибрежным и теплым климатическим регионам. Это связано с тем, что более легкие изотопологи воды быстрее испаряются по сравнению с более тяжелыми, которые испаряются медленнее и имеют тенденцию в большей степени выпадать в виде осадков. Результаты исследования [7] подтверждают, что эти явления, наблюдаемые в гидросфере, передаются через ассимиляцию растений. Поэтому данные о содержании стабильных изотопов кислорода и водорода можно использовать для понимания потенциальных регионов происхождения растений, а, следовательно, нектара, отобранного медоносными пчелами с растений, и, как следствие, меда.
На рис. 4 представлены результаты определения изотопного состава водорода и кислорода в меде из разных регионов России. Диапазон значений величины δ2Н во всех образцах меда колеблется от –116.6‰ (образец из Алтайского края, Красногорский район) до –34.5‰ (образец меда из Кабардинки). Самые высокие значения были обнаружены в Черноморском регионе России с теплым морским климатом (кабардинский и туапсинский меда со значениями величины δ2H –34.5 и –41.4‰ соответственно). Образцы меда, отобранные в регионах с умеренными климатическими условиями, такими как Калужская область (среднее значение величины δ2H составило –69.0 ± 8.6‰), республика Башкортостан (среднее значение величины δ2H равно –67.2 ± 21.3‰) показали промежуточные средние значения. Мед из Уссурийска (Приморский край с умеренным муссонным климатом) показал среднее значение величины δ2H –65.2 ± 4.7‰. Самые низкие значения зафиксированы для образцов из Сибирского региона: для Томской области среднее значение величины δ2H равно –97.6 ± 13.8‰, для образцов меда из Кемеровской области и Алтайского края средние значения величины δ2H составили –95.3 ± ± 12.4‰ и –95.8 ± 17.7‰ соответственно.
Рис. 4.
Диаграмма значений величин δ2Н и δ18О в меде из разных регионов России: диапазон между первым и третьим квартилем распределения заключен в рамку, вертикальные линии (“усы”) на нижнем и верхнем концах оси рамки представляют минимальные и максимальные значения, которые не считаются экстремальными значениями, вертикальная линия в рамке – среднее значение распределения; точками обозначены экстремальные значения.

Измеренные значения величины δ18O в меде варьировались от +12.7 до +25.7‰. Картина распределения значений изотопного состава кислорода в меде аналогична распределению значений изотопного состава водорода по климатическим зонам. Самое высокое среднее значение зафиксировано в Черноморском регионе (+23.4 ± ± 2.2‰), промежуточное значение (+22.0 ± 2.7‰) для Европейских регионов России, а самое низкое среднее значение – в Сибири (+17.4 ± 2.1‰).
Сравнение результатов определения изотопного состава водорода и кислорода в 48 образцах меда из нашего исследования и в 38 образцах меда, отобранных в 16 штатах США [8], показало, что для образцов американского меда диапазон значений величин δ2H (от –110 до –10‰) и δ18О (от +22 до +37‰) имеет более высокую верхнюю границу значений и шире, чем диапазон для образцов российского меда, для которого величина δ2H меняется от –116.6 до –34.5‰, а величина δ18О – от +12.7 до +25.7‰. Более тяжелый изотопный состав образцов американского меда обусловлен климатическими факторами, так как большая часть образцов американского меда была отобрана в южных штатах с субтропическим климатом, в зоне тропиков Флориды и в прибрежных районах Калифорнии со средиземноморским климатом.
Анализ взаимосвязи между изотопным составом водорода и кислорода в метеорных водах и изотопным составом меда. Измеренные значения величин δ2Н и δ18O меда сравнивали со значениями величин δ2Н и δ18O атмосферных осадков (метеорных вод), выпадающих в регионах отбора образцов меда. Величину δ2Н метеорных вод рассчитывали посредством изотопного онлайн-калькулятора, размещенного на портале Waterisotopes Database с использованием интерполированных данных значений величины δ2Н метеорных вод, полученных ранее по сети GNIP для сопредельных территорий. Анализ данных (табл. 2) демонстрирует хорошую корреляцию между соотношением изотопов водорода и кислорода в метеорной воде и меде. Коэффициент корреляции значений величины δ2Н в меде и осадках равен 0.87, а для величины δ18O – 0.83 (рис. 5).
Таблица 2.
Средние значения величин δ2H и δ18O в меде и среднегодовые интерполированные значения величин δ2Н и δ18О метеорных вод в регионах отбора образцов меда
| Регион | δ2HV-SMOW, ‰ | δ18OV-SMOW, ‰ | ||
|---|---|---|---|---|
| мед | метеорные воды | мед | метеорные воды | |
| Томская область | –97.6 ± 13.8 | –109 | 18.2 ± 0.9 | –15.1 |
| Алтайский край | –95.8 ± 17.7 | –98 | 17.7 ± 2.4 | –13.8 |
| Кемеровская область | –95.3 ± 12.4 | –100 | 14.1 ± 2.0 | –14.1 |
| Новосибирская область | –81.7 | –106 | 14.8 | –14.8 |
| Республика Башкортостан | –67.2 ± 21.3 | –71 | 21.7 ± 3.2 | –10.6 |
| Калужская область | –69.0 ± 8.6 | –77 | 21.0 ± 0.1 | –10.1 |
| Приморский край | –65.2 ± 4.7 | –54 | 20.0 ± 2.8 | –7.5 |
| Краснодарский край | –47.8 ± 16.5 | –56 | 23.8 ± 1.2 | –7.9 |
| Белгородская область | –41.0 ± 7.3 | –61 | 25.3 ± 0.6 | –8.1 |
| Курская область | –58.3 | –65 | 21.8 | –8.5 |
| Республика Адыгея | –67.7 ± 17.1 | –60 | 21.7 ± 3.8 | –9 |
| Республика Мордовия | –70.4 | –81 | 21.2 | –11.3 |
| Республика Крым | –43.2 | –60 | 24.8 | –8.8 |
Рис. 5.
Сопоставление измеренных значений величин δ2Н и δ18О меда с интерполированными данными для δ2Н и δ18О метеорных вод в регионах отбора образцов меда.
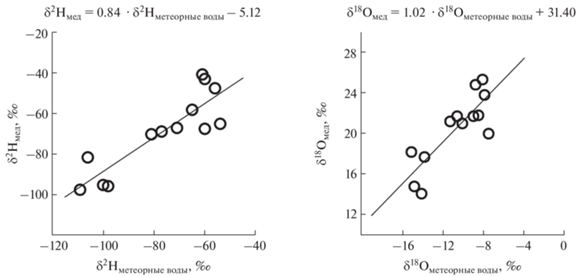
Как и предполагалось, медоносные растения фиксируют соотношения изотопов водорода и кислорода местных атмосферных осадков, и эта “запись” сохраняется в меде, хотя и с некоторой трансформацией из-за процессов фракционирования, происходящих при превращении нектара в мед.
Анализа данных по стабильным изотопам C, H и O. На рис. 6 представлены графики зависимости между изотопными составами углерода, водорода и кислорода в 48 образцах меда. Наибольшая корреляционная связь с коэффициентом корреляции 0.71 наблюдается между изотопами водорода и кислорода. Коэффициент корреляции для изотопов водорода и углерода составляет 0.68. Между изотопами кислорода и углерода коэффициент корреляции равен 0.66. Несмотря на умеренные коэффициенты корреляции, на графиках хорошо прослеживается “изотопный ландшафт”, соответствующий определенному географическому региону происхождения меда.
Рис. 6.
Взаимозависимости изотопного состава водорода, кислорода и углерода в образцах меда, отобранных в разных климатических регионах России.
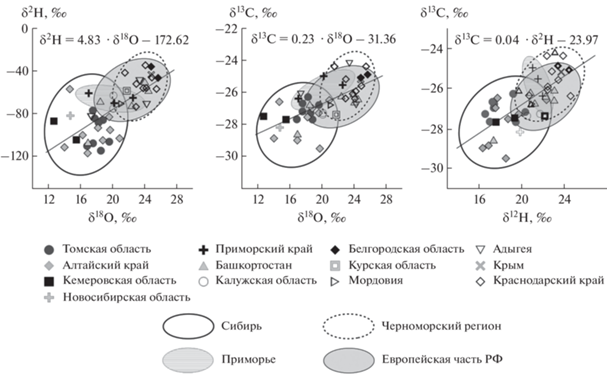
Совместное определение изотопного состава углерода, водорода и кислорода позволило выявить образцы поддельных медов по географической принадлежности. Так, гречишный мед из Республики Башкортостан (географическое происхождение указано на товарной этикетке меда), приобретенный на медовой ярмарке, показал значения изотопного состава трех элементов (δ13С = –28.6‰, δ2Н = –106.5‰ и δ18О = +17.0‰), соответствующие образцам меда из Сибирского региона. А для образца алтайского меда были определены значения изотопного состава углерода (δ13С = –26.6‰) и водорода (δ2Н = –56.9‰), соответствующие Европейскому региону России.
* * *
Определение стабильных изотопов углерода является признанным методом обнаружения фальсификации меда. Наше исследование расширило его применение, включив в него возможность определения региона происхождения меда с использованием изотопов водорода и кислорода. Продемонстрирована перспективность использования стабильных изотопов С, О, Н для определения региона происхождения меда из разных климатических зон. Показано, что не только изотопы водорода и кислорода в меде связаны с осадками и климатом, но и на изотопы углерода в меде также влияют климатические параметры. Сравнение значений изотопного состава углерода в 98 образцах Российского меда и их белковой фракции позволило выявить 7 образцов поддельного меда, сфальсифицированного сахарными сиропами, приготовленными из растений с С4 типом фотосинтеза. Однако обнаружение фальсификации меда сахарными сиропами, полученными из растений с С3 типом фотосинтеза (например, сахарная свекла), по-прежнему представляет собой серьезную проблему, поэтому необходимо совершенствовать методы, сочетающие изотопную масс-спектрометрию с газовой и жидкостной хроматографией, развивать референсную базу аутентичных продуктов пчеловодства с целью “прогнозирования” изотопных сигнатур в продуктах пчеловодства из конкретной географической зоны. Впервые совместное исследование изотопных сигнатур водорода, кислорода и углерода в образцах меда показало возможность использования изотопных данных для четкого определения трех климатических зон регионов происхождения меда в Российской Федерации: 1 зона – Черноморский регион с теплым морским климатом (δ13С = –25.6 ± 0.9‰, δ2Н = –55.2 ± ± 14.3‰ и δ18О = +23.4 ± 2.2‰); 2 зона – Европейская часть России с умеренно континентальным климатом (δ13С = –26.5 ± 1.1‰, δ2Н = –62.7 ± ± 18.1‰ и δ18О = +22.0 ± 2.7‰) и 3 зона – Сибирь с континентальным климатом (δ13С = –27.2 ± ± 0.8‰, δ2Н = –95.9 ± 14.8‰ и δ18О = +17.4 ± ± 2.1‰).
Исследование выполнено при частичной финансовой поддержке РФФИ в рамках научного проекта № 19-34-90016 и государственного задания ИМКЭС СО РАН №121031300154-1.
Авторы признательны за помощь ООO “МС-АНАЛИТИКА” в лице В.С. Файнберга за консультации при выполнении анализов и за предоставленные стандартные образцы меда для построения градуировочных графиков.
Список литературы
Fairchild G.H., Nichols J.P., Capps O. Jr. Observations on economic adulteration of high-value food products: The honey case // J. Food Distrib. Res. 2003. V. 34. P. 38.
Anklam E. A review of the analytical methods to determine the geographical and botanical origin of honey // Food Chem. 1998. V. 63. P. 549.
Longobardi F., Casiello G., Sacco D., Tedone L., Sacco A. Characterisation of the geographical origin of Italian potatoes, based on stable isotope and volatile compound analyses // Food Chem. 2011. V. 124. P. 1708.
Gremaud G., Hilkert A. Isotopic-Spectroscopic Technique: Stable Isotopic Ratio Mass Spectrometry (IRMS), Modern Techniques for Food Authentication / Ed. Sun D.-W. Elsevier, 2008. P. 269.
Tosun M. Detection of adulteration in honey samples added various sugar syrups with 13C/12C isotope ratio analysis method // Food Chem. 2013. V. 138. P. 1629.
Wang S., Guo Q., Wang L., Lin L., Shi H., Cao H., Cao B. Detection of honey adulteration with starch syrup by high performance liquid chromatography // Food Chem. 2015. V. 172. P. 669.
Schellenberg A., Chmielus S., Schlicht C., Camin F., Perini M., Bontempo L., Heinrich K., Kelly S.D., Rossmann A., Thomas F., Jamin E., Horacek M. Multielement stable isotope ratios (H, C, N, S) of honey from different European regions // Food Chem. 2010. V. 121. P. 770.
Chesson L.A., Tipple B.J., Erkkila B.R., Cerling T.E., Ehleringer J.R. B-HIVE: Beeswax hydrogen isotopes as validation of environment. Part I: Bulk honey and honeycomb stable isotope analysis // Food Chem. 2011. V. 125. P. 576.
Талибова А., Колеснов А. Оценка качества и безопасности пищевой продукции методом изотопной масс-спектрометрии // Аналитика. 2011. № 1. P. 44.
Калашникова Д.А., Симонова Г.В. Отношения стабильных изотопов 13С/12С и 15N/14N в образцах подмора пчел и в продуктах их жизнедеятельности // Журн. аналит. химии. 2021. Т. 76. № 4. С. 359. (Kalashnikova D.A., Simonova G.V. Ratios of stable isotopes 13С/12С and 15N/14N in samples of dead honey bees and beekeeping products // J. Anal. Chem. 2021. V. 76. № 4. P. 526.)
Global and regional maps of isotope ratios in precipitation. https://wateriso.utah.edu/waterisotopes/index. html (16.12.2021 г.).
Reference Materials and Calibration Services. https:// isotopes.usgs.gov/lab/referencematerials.html (22.11.2021 г.).
AOAC Official Methods of Analysis, Method 998.12: C-4 Plant Sugars in Honey. Internal Standard Stable Carbon Isotope Ratio Method, AOAC International, 1998.
Ветрова О.В., Калашникова Д.А., Мелков В.Н., Симонова Г.В. Выявление фальсификации меда сахарными сиропами методом масс-спектрометрии стабильных изотопов // Журн. аналит. химии. 2017. Т. 72. № 7. С. 645. (Vetrova O.V., Kalashnikova D.A., Melkov V.N., Simonova G.V. Detection of honey adulterations with sugar syrups by stable isotope mass spectrometry // J. Anal. Chem. 2017. V. 72. № 7. Р. 756.)
Bowen G.J. The Online Isotopes in Precipitation Calculator, version 3.1., 2017. https://wateriso.utah.edu/waterisotopes/index.html (14.12.2021 г.).
Luo D., Luo H., Dong H., Xian Y., Guo X., Wu Y. Hydrogen (2H/1H) combined with carbon (13C/12C) isotope ratios analysis to determine the adulteration of commercial honey // Food Anal. Methods. 2016. V. 9. P. 255.
Padovan G.J., Jong D.D., Rodrigues L.P., Marchini J.S. Detection of adulteration of commercial honey samples by the 13C/12C isotopic ratio // Food Chem. 2003 V. 82. P. 633.
Jonasson S., Medrano H., Flexas J. Variation in leaf longevity of Pistacia lentiscus and its relationship to sex and drought stress inferred from leaf delta δ13C // Funct. Ecol. 1997. V. 11. №. 3. P. 282.
Craig H., Isotopic variations in meteoric waters // Science. 1961. V. 133. P. 1702.
Bowen G.J., Ehleringer J.R., Chesson L.A., Stange E., Cerling T.E. Stable isotope ratios of tap water in the contiguous United States // Water Resour. Res. 2007. V. 43. Article W03419.
Дополнительные материалы отсутствуют.
Инструменты
Журнал аналитической химии


