Журнал аналитической химии, 2022, T. 77, № 5, стр. 427-432
Аналитические возможности капельно-искрового спектрометра при вводе пробы в электролитный анод
В. В. Ягов a, А. А. Жирков a, *
a Институт геохимии и аналитической химии им. В.И. Вернадского Российской академии наук
119991 Москва, ул. Косыгина, 19, Россия
* E-mail: vdomah@gmail.com
Поступила в редакцию 12.07.2021
После доработки 02.09.2021
Принята к публикации 17.09.2021
- EDN: UKCNNP
- DOI: 10.31857/S0044450222030136
Аннотация
Изучены аналитические возможности капельно-искрового спектрометра при вводе пробы в электролитный анод. Показано, что перенос вещества через границу электролитный анод–плазма происходит селективно (без коллоидного распыления), что особенно наглядно проявляется для Pb и Cd в концентрированных растворах NaCl. На примере свинца продемонстрировано влияние формы нахождения элемента в электролитном аноде на сигнал.
В последнее время публикуется все больше работ, посвященных использованию в спектральном анализе микроплазменных источников атомизации и возбуждения на основе электрических разрядов на поверхности водных растворов [1–5]. Такие источники отличаются компактностью, простотой, низким уровнем энергопотребления и расхода газов, а также возможностью проведения измерений в потоке. Устройства на основе электролитных разрядов при атмосферном давлении, описанные в работах [4, 6–8], по пределу обнаружения, воспроизводимости и диапазону определяемых содержаний почти сравнялись с атомно-эмиссионными спектрометрами с индуктивно связанной плазмой [4, 6–8].
Описано большое число систем атомизации и возбуждения на основе микроплазменного разряда с одним или двумя жидкими электродами – капельно-искровой разряд (КИР) [9], разряд при вскипании в канале [10], разряд с электролитным катодом [11], тлеющий разряд с электролитным катодом (ТРЭК) [12, 13], разряд между струями [14] и ряд других.
Начиная с первых работ по разрядам над водными растворами [11], и до недавнего времени [4] считалось, что металлы поступают в плазму только из электролитного катода, но не из электролитного анода [14]. Что касается щелочных, щелочноземельных металлов и алюминия, это мнение не опровергнуто до настоящего времени [15, 16], однако для ряда элементов (As, Ag, Bi, Cd, Hg, Pb, Sb, Se, Tl, Zn) показана возможность попадания в плазму разряда из анодного раствора [15, 17, 18], причем в ряде случаев при анодном поступлении аналита в плазму достигаются более низкие пределы обнаружения. Например, при определении кадмия и цинка при помощи тлеющего разряда с электролитным анодом (ТРЭА) Лю [15] получил пределы обнаружения в 0.05 и 0.1 нг/мл, что на два порядка лучше результатов, полученных группой Шекхара [19] с источником на основе ТРЭК. Для обладающих высокими потенциалами возбуждения селена и ртути Вебб [20] методом ТРЭК получил предел обнаружения 3 мкг/мл и 20 нг/мл соответственно, а Горска [18], используя проточный вариант ТРЭА, снизила пределы обнаружения до 3 и 0.5 нг/мл соответственно. В то же время для серебра и кадмия пределы обнаружения как в катодном [20], так и в анодном варианте [17] практически совпадают. Для свинца в случае ТРЭК предел обнаружения составляет 10 нг/мл [20], что лучше, чем для систем с ТРЭА (90 нг/мл [17] и 30 нг/мл [21]).
Цель настоящей работы – изучение аналитических возможностей источника атомизации и возбуждения на основе КИР при вводе пробы в электролитный анод. Эффекты, описанные для ТРЭА с твердым катодом [15–18, 21], воспроизведены на источнике с двумя жидкими электродами. Предложенный подход использован для расширения аналитических возможностей капельно-искрового спектрометра.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Капельно-искровой разряд возникает при сближении разноименно заряженных капель водного электролита. Опускающаяся верхняя капля, образованная вспомогательным раствором (обычно разбавленная HCl), служит для замыкания цепи, а также жидкой линзой, через которую свет попадает в оптоволоконный жгут спектрометра Maya2000 Pro. Пробу наносили в виде нижней капли объемом 20 мкл. Подробное описание прибора дано в нашей предыдущей работе [22]. Единственное отличие состояло в том, что если ранее нижняя капля с пробой всегда была заряжена отрицательно, то в настоящей работе устройство дополнено ключом, позволяющим изменять полярность. Большая часть данных относится к инверсной системе (с положительно заряженной пробой), в некоторых случаях сравнивали данные для обеих полярностей.
Растворители и реагенты. Использовали свежеприготовленную дистиллированную воду (установка очистки ДЭ-4, pH 5.8); Ca, Mg, Na, K, Pb, Hg, Ta, Cd, Ag (растворы хлоридов соответствующих металлов с концентрацией 1 мг/мл в 0.1 М HCl, ГСО, “Экоаналитика”, Россия); азотную, соляную, муравьиную, уксусную, сульфосалициловую кислоты ос. ч. (Химмед, Россия); хлорид натрия х. ч. (Химмед, Россия).
Растворы готовили непосредственно перед проведением эксперимента. Аликвотные части отбирали при помощи набора микропипеток ThermoScience (диапазоны объемов 2–20, 20–200, 100–1000 мкл, точность отбора аликвотной части ±1.5%). Для измерения массы использовали весы Extended ED Sartorius AG (Германия).
Методики исследования. Резервуар для вспомогательного раствора (жидкой линзы) заполняли 0.12 М HCl. Рабочий раствор для анодного электролита готовили, варьируя концентрацию соляной, азотной кислоты или соответствующей соли смешением концентрированного раствора с дистиллированной водой, при необходимости делая добавку рассчитанного количества органической кислоты. Аликвотную часть раствора определяемого элемента (ГСО) разбавляли рабочим раствором до требуемой концентрации, наносили полученный раствор дозатором в виде капли на металлический анод и измеряли сигнал на длинах волн, указанных в табл. 1. Аналитическим сигналом служила интегральная интенсивность свечения при соответствующей длине волны за первые 40 мс разряда.
Таблица 1.
Некоторые метрологические характеристики определения элементов методом капельно-искровой спектрометрии с электролитным анодом (n = 10, P = 0.95)
| Элемент, λ, нм | Среда | cmin, мкМ | cн, мкМ | cв, мМ | Уравнение градуировочной зависимости |
|---|---|---|---|---|---|
| Cd 228.80 | HCl 0.12 М | 1 | 10 | 0.7 | I = (2.3 ± 0.1) × 103с + 1.2 × 102 |
| Pb 405.78 | HCl 0.12 М | 3 | 5 | 5 | I = (2.85 ± 0.07) × 103c + 2.1 × 102 |
| Ag 338.29 | HNO3 0.04 M | 0.2 | 0.4 | 0.1 | I = (1.62 ± 0.04) × 105c + 4.1 × 103 |
| Tl 535.04 | HNO3 0.04 M | 6 × 10–2 | 0.1 | 0.15 | I = (3.14 ± 0.07) × 105c + 3.1 × 103 |
| Pb 405.78 | HCOOH 0.15 М | 4 × 10–2 | 0.1 | 1.5 | I = (2.91 ± 0.05) × 104c + 1.4 × 102 |
Для определения предела обнаружения использовали 3σ-критерий, а для расчета нижней и верхней границ диапазона определяемых содержаний – критерий величины относительного стандартного отклонения сходимости sr < 0.33.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
В качестве модельных использовали растворы элементов, приготовленные разбавлением соответствующих государственных стандартных образцов состава 0.12 М HCl и 0.04 М HNO3. Некоторые метрологические характеристики приведены в табл. 1.
Диапазон линейности градуировочной зависимости для свинца и таллия в минеральных кислотах составил около трех порядков величины; ограничение концентрации сверху определялось максимальной интенсивностью света, которую можно измерить в данных условиях. Для кадмия и серебра градуировочные графики имели участок насыщения. По-видимому, это связано с самопоглощением, что характерно для наиболее чувствительной в случае ТРЭА спектральной линии кадмия 228.80 нм [23]. Линейный диапазон для этих двух металлов составляет около двух порядков величины. Достигнутые пределы обнаружения для серебра согласуются с литературными данными по ТРЭА, однако для свинца и кадмия они в десятки раз выше, чем в работах [21, 24]. Различие может быть вызвано как отличием в спектральном разрешении и времени экспозиции (10 с в работе [24] против 40 мс в настоящей работе), так и ярко выраженной зависимостью интенсивности излучения металлов от состава раствора, характерной для ТРЭА [18, 21].
Интересно было сопоставить интенсивность излучения металлов в плазме КИР при анодном и катодном способе ввода пробы, зафиксировав остальные параметры неизменными. Как видно из табл. 2, в данных условиях наблюдали двадцатикратное превышение катодного сигнала индия над анодным, что согласуется с отсутствием в литературе данных об излучении индия в случае ТР-ЭА. Для свинца введение пробы в анодный раствор дает двукратный рост интенсивности свечения в сравнении катодным, для кадмия и таллия значимое различие отсутствует. Следует отметить, что эффект смены полярности сильнейшим образом зависит от состава фонового электролита. Приведенные данные касаются только 0.12 М HCl. Как показано в работе [25], при введении пробы в электролитный катод в области низких концентраций фонового электролита увеличение ионной силы раствора приводит к многократному возрастанию интенсивности линий металлов в спектре КИР и ТРЭК, причем эффект мало зависит от природы фонового электролита и металла. Для одноосновных сильных неорганических кислот область максимума интенсивности обычно приходится на концентрацию ~0.4 М [25]. Предварительные опыты, выполненные в ходе настоящей работы, показали, что при вводе пробы в электролитный анод оптимальная концентрация фонового электролита примерно на порядок ниже, однако для анода влияние природы металла и фонового электролита существенно сильнее. Из данных в табл. 2 следует, что 0.12 М HCl – это компромиссный фоновый раствор, для которого эффективность поступления металла в плазму из электролитного катода и электролитного анода одинакова для кадмия и таллия и всего в два раза отличается для свинца. Для катодного варианта 0.12 М HCl – слишком разбавленный фоновый раствор, для анодного – слишком концентрированный.
Таблица 2.
Влияние полярности на интенсивность линий Pb, Cd, Tl, In в спектре капельно-искрового разряда (фоновый электролит – 0.12 М HCl, n = 7, P = 0.95)
| Элемент, λ нм | Концентрация, мкМ | Проба на аноде | Проба на катоде |
|---|---|---|---|
| Pb 405.78 | 700 | 2500 ± 200 | 1300 ± 100 |
| Cd 228.80 | 700 | 1300 ± 100 | 1400 ± 100 |
| Tl 535.04 | 1 | 39 ± 9 | 32 ± 8 |
| In 410.17 | 200 | 130 ± 10 | 2300 ± 200 |
Очень интересным представляется тот факт, что излучение щелочных и щелочноземельных металлов, наиболее интенсивное при катодном поступлении электролита в плазму разряда, полностью отсутствует в его анодном варианте. С практической точки зрения это полезно для определения тяжелых металлов в солевых матрицах, включая и высокоминерализованные среды, являющиеся неудобным объектом для многих инструментальных методов аналитической химии. Возможности определения свинца и кадмия в насыщенном растворе хлорида натрия иллюстрируют рис. 1 и табл. 3. Как видно из приведенного на рис. 1 спектра, интенсивность D-линии натрия оказывается ниже интенсивностей наиболее чувствительных линий свинца и кадмия, несмотря на тысячекратное различие концентраций и значительное превосходство D-линии в относительной интенсивности. Фактически в факеле капельно-искрового разряда над насыщенным раствором NaCl почти нет натрия, но есть Cd и Pb, селективно поступающие в плазму. Механизм транспорта вещества через границу электролитный анод/плазма, чувствительный к природе элемента и форме его нахождения в растворе, представляется наиболее интересным аспектом изучаемого явления. Эффект пока не нашел адекватного объяснения в литературе [15, 17, 18, 21].
Рис. 1.
Спектр излучения 1 мМ свинца и кадмия в насыщенном растворе хлорида натрия в капельно-искровом разряде. Проба в анодном электролите.
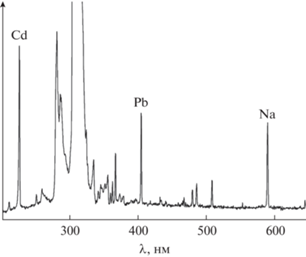
Таблица 3.
Некоторые метрологические характеристики определения свинца и кадмия в насыщенном растворе хлорида натрия при помощи капельно-искрового разряда с электролитным анодом (n = 5, P = 0.95)
| Элемент, λ, нм | cmin, мкМ | cн, мкМ | cв, мМ | Уравнение градуировочной зависимости |
|---|---|---|---|---|
| Pb 405.78 | 8 | 15 | 10 | I = (1.95 ± 0.06) × 103c + 1.8 × 102 |
| Cd 228.80 | 5 | 10 | 0.4 | I = (6.2 ± 0.3) × 103c + 3.7 × 102 |
Как видно из представленных данных, определение в насыщенном растворе хлорида натрия не просто оказывается возможным, но достигнутые при этом метрологические характеристики незначительно отличаются от таковых в 0.12 М соляной кислоте. Интересно, что коэффициент чувствительности (тангенс угла наклона градуировочной зависимости) для кадмия возрастает более чем вдвое с одновременным снижением верхней границы определяемых содержаний. Данное обстоятельство косвенно подтверждает вывод, что принципиальное значение для выхода элемента из электролитного раствора в плазму разряда имеет его форма нахождения в растворе, зависящая от pH, ионной силы, присутствия лигандов. Подобное поведение аналитов нетипично для методов атомно-эмиссионной спектроскопии, но в части зависимости от pH подтверждается данными [21, 26].
Для всестороннего рассмотрения данного явления состав и природу фонового электролита варьировали в широких пределах, используя свинец в качестве модельного аналита. Как видно из табл. 4, интенсивность линии Pb I 405.78 нм очень сильно зависит от природы и концентрации фонового электролита – разброс превышает два порядка величины. Для всех представленных растворов зависимость сигнала от концентрации фонового электролита проходит через максимум, что особенно хорошо видно для сульфосалициловой кислоты. Когда эту кислоту в оптимальной концентрации (46 мМ) наполовину нейтрализовали раствором аммиака и особенно гидроксидом натрия, сигнал снижался почти на порядок (см. последние строки в табл. 4). Можно предположить, что прочный анионный комплекс свинца – менее предпочтительная форма, чем положительно заряженный ион, что (возможно, случайно) соответствует тривиальной электростатической модели эмиссии с анода. Аналогичного снижения при переходе от соляной кислоты к ее натриевой соли не наблюдается, т.е. эффект не сводится к влиянию pH.
Таблица 4.
Влияние состава фонового электролита на интенсивность излучения 1 мМ свинца в капельно-искровом разряде с электролитным анодом (n = 4, P = = 0.95)
| Фоновый раствор | Интенсивность линии Pb 405.78 нм |
|---|---|
| Соляная кислота 4 мМ | 980 ± 90 |
| Соляная кислота 40 мМ | 1600 ± 100 |
| Соляная кислота 60 мМ | 1900 ± 100 |
| Хлорид натрия 50 мМ | 1800 ± 100 |
| Хлорид натрия 500 мМ | 2500 ± 200 |
| Хлорид натрия 5.7 М | 1200 ± 100 |
| Уксусная кислота 330 мМ | 3600 ± 400 |
| Янтарная кислота 170 мМ | 1200 ± 200 |
| Муравьиная кислота 90 мМ | 3600 ± 300 |
| Муравьиная кислота 150 мМ | 6900 ± 600 |
| Муравьиная кислота 220 мМ | 5500 ± 400 |
| Муравьиная кислота 430 мМ | 3500 ± 200 |
| Хлорид натрия 5.7 М + муравьиная кислота 220 мМ | 2800 ± 300 |
| Хлорид натрия 5.7 М + муравьиная кислота 650 мМ | 2600 ± 200 |
| Сульфосалициловая кислота 14 мМ | 1400 ± 100 |
| Сульфосалициловая кислота 46 мМ | 3300 ± 400 |
| Сульфосалициловая кислота 92 мМ | 920 ± 100 |
| Сульфосалициловая кислота 460 мМ | 40 ± 8 |
| Сульфосалициловая кислота 46 мМ + + 70 мМ NaOH | 320 ± 40 |
| Сульфосалициловая кислота 46 мМ + + 70 мМ NH3 | 550 ± 40 |
С практической точки зрения, наиболее значимый эффект в определении свинца достигается добавкой муравьиной кислоты в диапазоне концентраций несколько сотен мМ. Добавка всего 200 мМ HCOOH к насыщенному раствору хлорида натрия усиливает сигнал в два с половиной раза. Электропроводность растворов, содержащих более 50 мМ HCOOH, достаточна для зажигания КИР, что позволяет обойтись без добавки минерального электролита, обеспечивая потенциально наиболее благоприятные условия определения. Максимальная чувствительность достигнута в случае раствора, содержащего 150 мМ муравьиной кислоты. Достигнутые при этом метрологические характеристики приведены в табл. 1.
Использование оптимальной концентрации муравьиной кислоты позволяет увеличить коэффициент чувствительности определения свинца в десять раз при одновременном снижении предела обнаружения на два порядка величины за счет снижения соотношения сигнал/шум (табл. 1), что приближается к достигнутым в работах [15, 17, 21] показателям.
В заключение отметим, что КИР создает условия для широкого варьирования химического состава матрицы (фонового электролита). Обновляемость жидких поверхностей в КИР позволяет легко удалять загрязнения, оставшиеся после опытов с концентрированными растворами. Кроме того, импульсная природа КИР позволяет обойти ограничения, существующие в случае описанного в литературе стационарного ТРЭА, устойчиво горящего только над разбавленными (<0.1 М) растворами минеральных кислот [17, 24]. Так, описанные выше эксперименты с насыщенным раствором хлорида натрия и другими концентрированными растворами невозможны с использованием ТРЭА.
Работа выполнена в ГЕОХИ РАН им. В.И. Вернадского в рамках Государственного задания 0137-2019-024.
Список литературы
Cai Y., Gao X.-G., Ji Z.-N., Yu Y.-L., Wang J.-H. Nonthermal optical emission spectrometry for simultaneous and direct determination of zinc, cadmium and mercury in spray // Analyst. 2018. V. 143. P. 930.
Han B., Jiang X., Hou X., Zheng C. Miniaturized dielectric barrier discharge carbon atomic emission spectrometry with online microwave-assisted oxidation for determination of total organic carbon // Anal. Chem. 2014. V. 86. P. 6214.
Hoegg E.D., Marcus R.K., Koppenaal D.W., Irvahn J., Hager G.J., Hart G.L. Determination of uranium isotope ratios using a liquid sampling atmospheric pressure glow discharge/orbitrap mass spectrometer system // Rapid Commun. Mass Spectrom. 2017. V. 31. P. 1534.
Pohl P., Jamroz P., Swiderski K., Dzimitrowicz A., Lesniewicz A. Critical evaluation of recent achievements in low power glow discharge generated at atmospheric pressure between a flowing liquid cathode and a metallic anode for element analysis by optical emission spectrometry // Trends Anal. Chem. 2017. V. 88. P. 119.
Yang C., Chan C.-Y., He D., Liu Z., Deng Q., Zheng H., Hu S., Zhu Z. Highly sensitive determination of arsenic and antimony based on an interrupted gas flow atmospheric pressure glow discharge excitation source // Anal. Chem. 2019. V. 91. P. 1912.
Peng X., Wang Z. Ultrasensitive determination of selenium, arsenic by modified helium atmospheric pressure glow discharge optical emission spectrometry coupled with hydride generation // Anal. Chem. 2019. V. 91. P. 10073.
Cai Y., Zhang Y.-J., Wu D.-F., Yu Y.-L., Wang J.-H. Nonthermal optical emission spectrometry: Direct atomization and excitation of cadmium for highly sensitive determination // Anal. Chem. 2016. V. 88. P. 4192.
Yu J., Zhang Z., Lu Q., Sun D., Zhu S., Zhang X., Wang X., Yang W. High-sensitivity determination of K, Ca, Na, and Mg in salt mines samples by atomic emission spectrometry with a miniaturized liquid cathode glow discharge // J. Anal. Methods Chem. 2017. V. 1. № 10. Article ID 7105831.
Ягов В.В., Зуев Б.К., Коротков А.С. Электрический разряд в межэлектролитном промежутке: перспективы создания атомно-эмиссионного сенсора // Доклады РАН. 1998. Т. 359. № 2. С. 208.
Зуев Б.К., Ягов В.В., Гецина М.Л., Руденко Б.А. Разряд при вскипании в канале- новый источник атомизации и возбуждения для атомно-эмиссионного определения металлов в потоке // Журн. аналит. химии. 2002. Т. 57. № 10. С. 907. (Zuev B.K., Yagov V.V., Getsina M.L., Rudenko B.A. Discharge on boiling in channel as a new atomization and excitation source for the flow determination of metals by atomic emission spectrometry // J. Anal. Chem. 2002. V. 57. P. 907.)
Cherfalvi T., Mezei P., Apai P. Emission studies on a glow discharge in atmpspheric pressure air using water as cathode // J. Phys. D: Appl. Phys. 1993. V. 26. P. 2184.
Jamroz P., Zyrnicki W. Spectroscopic characterization of miniaturized atmospheric-pressure DC glow discharge generated in contact with flowing small size liquid cathode // Plasma Chem. Plasma Proc. 2011. V. 31. P. 681.
Paing H.W., Hall K.A., Marcus R.K. Sheathing of the liquid sampling – atmospheric pressure glow discharge microplasma from ambient atmosphere and its implication for optical emission spectroscopy // Spectrochim. Acta B. 2019. V. 155. P. 99.
Ягов В.В., Гецина М.Л., Зуев Б.К. О возможности применения разрядов со струйным электролитным катодом в качестве источников эмиссионных спектров для атомно-эмиссионного детектора в проточном анализе // Журн. аналит. химии. 2004. Т. 59. № 11. С. 1150. (Yagov V.V., Getsina M.L., Zuev B.K. Use of electrolyte jet cathode glow discharge as source of emission spectra for atomic emission detectors in flow-injection analysis // J. Anal. Chem. 2004. V. 59. P. 1037.)
Liu X., Zhu Z., He D., Zheng H., Gan Y., Belshaw N.S., Hu S., Wang Y. Highly sensitive elemental analysis of Cd and Zn by solution anode glow discharge atomic emission spectrometry // J. Anal. At. Spectrom. 2016. V. 31. P. 1089.
Jamroz P., Greda K., Dzimitrowicz A., Swiderski K., Pohl P. Sensitive determination of Cd in small-volume samples by miniaturized liquid drop anode atmospheric pressure glow discharge optical emission spectrometry // Anal. Chem. 2017. V. 89. P. 5729.
Greda K., Swiderski K., Jamroz P., Pohl P. Flowing liquid anode atmospheric pressure glow discharge as an excitation source for optical emission spectrometry with improved detectability of Ag, Cd, Hg, Pb, Tl and Zn // Anal. Chem. 2016. V. 88. P. 8812.
Gorska M., Greda K., Pohl P. On the coupling of hydride generation with flowing liquid anode atmospheric pressure glow discharge for determination of traces of As, Bi, Hg, Sb and Se by optical emission spectrometry // Talanta. 2021. V. 222. P. 121510.
Shekhar R., Karunasagar D., Ranjit M., Arunachalam J. Determination of elemental constituents in different matrix materials and flow injection studies by the electrolyte cathode glow discharge technique with a new design // Anal. Chem. 2009. V. 81. P. 8157.
Doroski T.A., King A.M., Fritz M.P., Webb M.R. Solution-cathode glow discharge-optical emission spectrometry of a new design and using a compact spectrograph // J. Anal. At. Spectrom. 2013. V. 28. P. 1090.
Swiderski K., Dzimitrowicz A., Jamroz P., Pohl P. Influence of pH and low-molecular weight organic compounds in solution on selected spectroscopic and analytical parameters of flowing liquid anode atmospheric pressure glow discharge for the optical emission spectroscopic determination of Ag, Cd and Pb // J. Anal. At. Spectrom. 2018. V. 33. P. 437.
Ягов В.В., Коротков А.С., Жирков А.А., Погонин В.И., Зуев Б.К. Портативный атомно-эмиссионный спектрометр для анализа растворов на основе капельно-искрового разряда // Журн. аналит. химии. 2019. Т. 74. С. 234.
Зайдель А.Н., Прокофьев В.К., Райский С.М. Таблицы спектральных линий. М.: Наука, 1977. 800 с.
Greda K., Gorska M., Welna M., Jamroz P., Pohl P. In-situ generation of Ag, Cd, Gh, In Tl and Zn volatile species by flowing liquid anode atmospheric pressure glow discharge operated in gaseous jet mode – evaluation of excitation processes and analytical performance // Talanta. 2019. V. 199. P. 107.
Ягов В.В., Гецина М.Л. Влияние состава фонового электролита на интенсивность линий металлов в электрических разрядах с жидким электролитным катодом // Журн. аналит. химии. 2004. Т. 59. № 1. С. 1.
Liu X., Liu Z., He D., Yao S., Zheng H., Hu S. Generation of volatile cadmium and zinc species based on solution anode glow discharge induced plasma electrochemical processes // Anal. Chem. 2017. V. 89. № 6. P. 3739.
Дополнительные материалы отсутствуют.
Инструменты
Журнал аналитической химии


