Биоорганическая химия, 2020, T. 46, № 5, стр. 557-560
Поликонденсация предшественников диоксида кремния и титана на матрицах из природных и синтетических полимеров
Ю. Н. Шкрыль 1, *, А. И. Дегтяренко 1, Т. Ю. Горпенченко 1, Т. В. Авраменко 1, В. П. Булгаков 1
1 ФГБУН “Федеральный научный центр биоразнообразия наземной биоты Восточной Азии” Дальневосточного отделения Российской академии наук
690022 Владивосток, просп. 100-летия Владивостока, 159, Россия
* E-mail: yn80@mail.ru
Поступила в редакцию 28.03.2020
После доработки 30.03.2020
Принята к публикации 31.03.2020
Аннотация
Исследована способность некоторых природных и синтетических полимеров служить в качестве катализатора и темплата для поликонденсации оксида кремния и титана из водорастворимых предшественников тетракис(2-гидроксиэтил)ортосиликата (ТГЭОС) и титан бис(аммоний лактат)дигидроксида (ТБАЛДГ). Каталитический потенциал исследованных полимеров оценивали спектрофотометрическим методом, а размер, форму и элементный состав образующихся структур определяли методами сканирующей электронной микроскопии (СЭМ) и энергодисперсионной рентгеновской спектроскопии (ЭДС). Показано, что альбумин и полиэтиленимин могут применяться для получения частиц SiO2 и TiO2 соответственно. Такие гомополимеры как поли-D- и поли-L-лилизин эффективно катализируют синтез как кремниевых, так и титановых нанокомпозитных материалов.
Наночастицы диоксида кремния и титана применяют в качестве опорных структур для полимерных трансплантов, инертных матриц для катализаторов, в системах контролируемого высвобождения биологически активных молекул, а также в прототипах новейших оптических компонентов биосенсоров [1, 2]. Разнообразные синтетические подходы, используемые для получения кремниевых и титановых нанокомпозитов часто связаны с использованием экстремальных значений температуры, pH, давления и др.
Биоминeрализация используется в природе для построения сложных скелетов организмами из двух отдаленных таксонов – диатомеями и губками. Особые белки – силикатеины и силаффины направляют формирование упорядоченных кремниевых структур на нано- и микрометровом масштабе, создавая конструкции, обладающие выдающимися физическими характеристиками [3]. Как сами белки, так и белковые и небелковые полимеры, разработанные на их основе способны катализировать биомиметический синтез нанокомпозитных материалов диоксида кремния и титана в условиях in vitro [4–6]. Однако использованию таких специализированных биополимеров в технологическом синтезе биоминералов препятствует их высокая стоимость и сложность получения.
В настоящей работе мы проверили возможность использования относительно недорогих и доступных полимеров природного и синтетического происхождения выступать в качестве катализатора и темплата для поликонденсации диоксида кремния и титана. При этом в качестве предшественников были использованы новые водорастворимые субстраты, тетракис(2-гидроксиэтил)ортосиликата (ТГЭОС) и титан бис(аммоний лактат)дигидроксида (ТБАЛДГ), которые не требуют предварительного гидролиза, отличаются высокой реакционной способностью и биосовместимостью [7, 8]. Поликонденсацию ТГЭОС (ABCR, Германия) и ТБАЛДГ (Sigma, США) в концентрации 10 мМ проводили в фосфатно-солевом буфере (pH 7.4), при комнатной температуре (24°C) в течение 16 часов при постоянном перемешивании в присутствии 10 мг/мл следующих полимеров: бычий сывороточный альбумин (БСА), пероксидаза хрена (ПХ), миоглобин лошади (МГЛ), поли-L- и поли-D-лизин (ПЛЛ и ПДЛ соответственно), разветвленный и линейный полиэтиленимин (РПЭИ и ЛПЭИ соответственно). Первичную оценку эффективности реакции проводили по возрастанию в растворе количества взвешенных частиц, что выражалось в увеличении оптической плотности при 600 нм. Морфологию и состав образованных структур определяли с помощью электронного сканирующего микроскопа Merlin (Carl Zeiss, Германия) с приставкой для энергодисперсионного микроанализа.
Такие полимеры как БСА, ПХ, МГЛ, РПЭИ и ЛПЭИ не проявляли значительной каталитической активности в отношении ТГЭОС (рис. 1). При этом наибольшая эффективность формирования SiO2 отмечена для БСА, за которым следуют ПДЛ и ПЛЛ, активность которых уменьшалась в 1.8 и 2.2 раза соответственно, по сравнению с БСА (рис. 1). В результате реакции образовались сферические частицы кремнезема, размер которых варьировал от 50 нм (ПДЛ) до 1 мкм (БСА) (рис. 2а–2в). Все синтетические полимеры были способны индуцировать поликонденсацию ТБАЛДГ, тогда как белковые матрицы оказались неактивны в отношении этого субстрата. Эффективность поликондесации в данном случае убывала в ряду ПЛЛ > > ПДЛ > РПЭИ > ЛПЭИ (рис. 1). Образовавшиеся гибридные полимер-диоксид титановые композиты представлены сферическими структурами от 30 нм (ЛПЭИ) до 200 нм (РПЭИ) (рис. 2г–2е). ЭДС-спектр показывает присутствие характеристических линий O, а также Si и Ti в соответствующих образцах (рис. 2). Это доказывает, что полученные нанокомпозитные гранулы состоят из оксидов кремния и титана. Присутствуют также пики С – материал подложки и Cr – предварительно нанесенный проводящий слой.
Рис. 1.
Сравнение эффективности поликондесации ТГЭОС и ТБАЛДГ под действием природных и синтетических полимеров. Показаны средние значения и стандартные ошибки по результатам трех экспериментов. Разные буквы над столбцами указывают значимые различия средних значений для каждого из предшественников, P < 0.05 (однофакторный дисперсионный анализ, критерий Фишера).
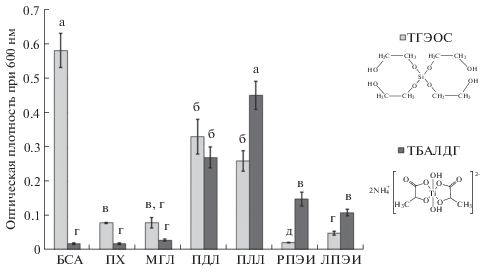
Рис. 2.
СЭМ изображение и ЭДС спектр кремниевых и титановых нанокомпозитов, полученных с различными полимерными матрицами.
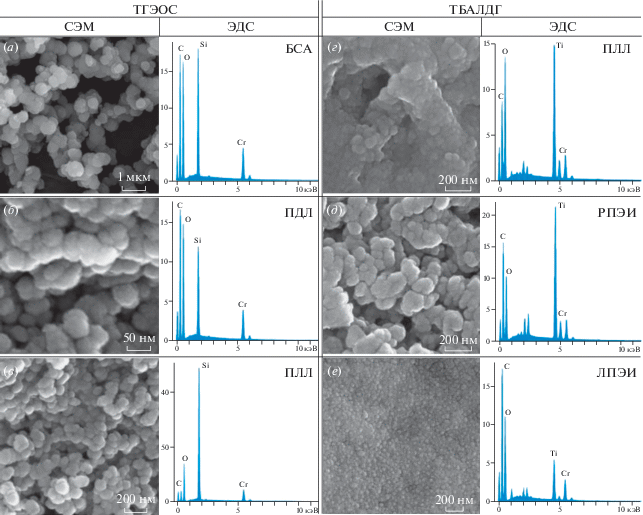
Морфология частиц, описанных в данной работе, имеет значительное сходство с частицами SiO2 и TiO2, полученными ранее с использованием биополимеров из губок и диатомей [5, 6, 9]. Такой результат может указывать на наличие универсальных фундаментальных приниципов биоминерализации и возможности их трансляции в инновационные синтетические подходы для производства биомиметических органических и неорганических гибридных материалов. Описанная способность доступных полимеров к поликонденсации оксидов кремния и титана может быть в дальнейшем испробована для получения упорядоченных наноструктур на различных поверхностях.
Список литературы
Singh P., Srivastava S., Singh S.K. // ACS Biomater. Sci. Eng. 2019. V. 5. P. 4882–4898. https://doi.org/10.1021/acsbiomaterials.9b00464
Haider A.J., Jameel Z.N., Al-Hussaini I.H.M. // Energy Procedia. 2019. V. 157. P. 17–29. https://doi.org/10.1016/j.egypro.2018.11.159
Aguilar-Camacho J.M., Doonan L., McCormack G.P. // Mol. Phylogenet. Evol. 2019. V. 131. P. 245–253. https://doi.org/10.1016/j.egypro.2018.11.159
Shkryl Y.N., Bulgakov V.P., Veremeichik G.N., Kovalchuk S.N., Kozhemyako V.B., Kamenev D.G., Semiletova I.V., Timofeeva Y.O., Shchipunov Y.A., Kulchin Y.N. // Bioprocess Biosyst. Eng. 2016. V. 39. P. 53–58. https://doi.org/10.1007/s00449-015-1488-2
Shimizu K., Morse D.E. // Methods Enzymol. 2018. V. 605. P. 429–455. https://doi.org/10.1016/bs.mie.2018.02.025
Buckle E.L., Roehrich A., Vandermoon B., Drobny G.P. // Langmuir. 2017. V. 33. P. 10 517–10 524. https://doi.org/10.1021/acs.langmuir.7b01048
Поварова Н.В., Баранов М.С., Ковальчук С.Н., Семилетова И.В., Лукьянов К.А., Кожемяко В.Б. // Биоорган. химия. 2015. Т. 41. С. 380–382. [Povarova N.V., Baranov M.S., Kovalchuk S.N., Semiletova I.V., Lukyanov K.A., Kozhemyako V.B. // Russ. J. Bioorg. Chem. 2015. V. 41. P. 338–339.] https://doi.org/10.7868/S0132342315030070
Hernández-Gordillo A., Hernández-Arana A., Campero-Celis A., Vera-Robles L.I. // RSC Adv. 2019. V. 9. P. 34 559–34 566. https://doi.org/10.1039/C9RA05923G
Шкрыль Ю.Н., Семилетова И.В., Непомнящий А.В., Ковальчук С.Н., Веремейчик Г.Н., Авраменко Т.В., Булгаков В.П., Щипунов Ю.А., Вознесенский С.С., Кожемяко В.Б. // Биоорган. химия. 2018. Т. 44. С. 465–467. [Shkryl Y.N., Semiletova I.V., Nepomnyaschiy A.V., Kovalchuk S.N., Veremeichik G.N., Avramenko T.V., Bulgakov V.P., Shchipunov Y.A., Voznesenskiy S.S., Kozhemyako V.B. // Russ. J. Bioorg. Chem. 2018. V. 44. P. 469–471.] https://doi.org/10.1134/S0132342318040188
Дополнительные материалы отсутствуют.
Инструменты
Биоорганическая химия


