Биология внутренних вод, 2019, № 2-2, стр. 28-32
Изменчивость оссификации краниального скелета сеголетков Lissotriton vulgaris (L.) (Саudata) в градиенте урбанизации
В. Л. Вершинин 1, 2, *, А. Г. Трофимов 1, 2, Е. В. Перехрест 2, Д. Л. Берзин 1
1 Институт экологии растений и животных УрО РАН
620144 Екатеринбург, ул. 8 Марта, д. 202, корп. 3, Россия
2 Уральский федеральный университет им. первого Президента России Б.Н. Ельцина
620002 Екатеринбург, ул. Мира, д. 19, Россия
* E-mail: vol_de_mar@list.ru
Поступила в редакцию 26.04.2017
После доработки 24.07.2017
Принята к публикации 20.10.2017
Аннотация
Рассмотрено влияние экологических условий на специфику процесса оссификации черепа сеголетков обыкновенного тритона Lissotriton vulgaris (Linnaeus, 1758) в зависимости от уровня урбанизации. Установлено, что степень смыкания срединного шва черепа сеголетков зависит от уровня минерализации поверхностных вод, в которых протекает развитие тритона. Аккумулирующий характер урбоценозов способствует интенсификации минерального обмена из-за обилия кальцефильных животных в местах обитания тритона и преобладания их в пищевом рационе сеголетков, он же служит сопутствующим фактором, ускоряющим формирование краниальных окостенений у животных в популяциях из селитебной части городской агломерации.
ВВЕДЕНИЕ
Известно, что у хвостатых амфибий появление и оссификация краниальных костей зависят от таксономических особенностей [19, 21, 28], межтканевых индукционных взаимодействий [5, 8] и механизма эндокринной регуляции [20, 24, 25]. При этом окостенение разных краниальных элементов в разной степени обусловлено не только уровнем тиреоидных гормонов [9, 26, 27], но и экологической спецификой местообитания, в среду которого интегрируется новая генерация в ходе онтогенеза [22].
Обыкновенный тритон Lissotriton vulgaris (L., 1758) – широко распространенный в Евразии вид, населяющий как природные, так и антропогенно измененные ландшафты, и легко осваивающий водоемы на урбанизированных территориях [11, 13, 16, 17].
Наряду с чувствительностью L. vulgaris к загрязнению и геохимическим параметрам среды [10], данный вид обладает определенной устойчивостью к антропогенным трансформациям сообществ. Известно [4], что для обыкновенного тритона важен не столько состав растительных сообществ, сколько высота и плотность травостоя, обеспечивающие благоприятные микроклиматические условия. Для уральских городов, где урбанизация, как правило, сочетается со значительным индустриальным загрязнением [1], в популяциях обыкновенного тритона, претерпевших процесс синурбизации [14], возникает ряд особенностей как адаптивного, так и негативного характера, отражающих состояние среды местообитаний [3].
Цель работы – исследование особенностей формирования краниума сеголетков L. vulgaris в градиенте урбанизации.
МАТЕРИАЛ И МЕТОДЫ ИССЛЕДОВАНИЯ
Материал собирали в 2013–2014 гг. в местообитаниях обыкновенного тритона на территории городской агломерации г. Екатеринбурга. Животных отлавливали вручную вскоре после завершения метаморфоза и достижения 56-й стадии [6]. Общее число изученных животных – 72 экз. сеголетков L. vulgaris, представленных четырьмя независимыми репрезентативными и сопоставимыми по числу животных выборками (табл. 1). Для оценки степени урбанизации использована типизация городских ландшафтов [29, 30]. В основу типизации положена степень освоенности территории человеком (плотность и этажность жилой застройки, характер использования территории, уровень загрязнения).
Таблица 1.
Доля сеголетков (% числа особей) с разным состоянием срединного шва черепа
| Состояние шва | Зона II (n = 18) |
Зона III (n = 15) |
Зона IV (n = 17) |
К (n = 22) |
|---|---|---|---|---|
| Полностью закрыт | 61.11 | 80.0 | 41.18 | 45.45 |
| Частично закрыт | 33.33 | 20.0 | 35.29 | 45.45 |
| Открыт | 5.56 | 0 | 23.53 | 9.09 |
| Длина тела, мм | $\frac{{18.38 \pm 0.26}}{{15.4--19.7}}$ | $\frac{{18.01 \pm 0.23}}{{16.3--19.4}}$ | $\frac{{18.67 \pm 0.25}}{{17.0--20.7}}$ | $\frac{{19.83 \pm 0.23}}{{18.2--22.0}}$ |
В пределах городской агломерации выделены четыре зоны, к которым приурочены места обитания амфибий: зона I – центральная часть города (амфибии не обнаружены) с многоэтажной застройкой, массивными асфальтовыми покрытиями, водоемами с сильным промышленным загрязнением, мелкими реками и ручьями, забранными в трубы; зона II – районы многоэтажной застройки с осваиваемыми территориями, пустырями, участками с открытыми почвами, малыми водоемами с высоким уровнем загрязнения; зона III – районы малоэтажной застройки, занятые домами частного сектора с садами и огородами, пустырями, парками; зона IV – лесопарковая, местообитания этой территории, главным образом, подвержены действию рекреационной нагрузки. В качестве контроля (K) использовали выборку из загородной популяции в 50 км от г. Екатеринбурга. Наличие градиента урбанизации, соответствующего настоящей типизации [30], ежегодно подтверждается гидрохимическими анализами, проводимыми в лаборатории физико-химических анализов Уральского государственного горного университета. Пробы воды отбирали в водоемах, где протекало развитие обыкновенного тритона в период размножения и в момент завершения метаморфоза. Температуру нерестовых водоемов измеряли ртутным термометром ТП–2 с ценой деления 0.5°C в первый месяц после откладки икры.
Животных отлавливали, вскрывали и фиксировали в 70%-ном спирте. Длину тела измеряли цифровым штангенциркулем Kraftool (Германия) с ценой деления 0.01 мм. В ходе камеральной обработки под бинокуляром МБС-10 исследовали содержимое желудочно-кишечного тракта сеголетков. Для изучения скелетных структур использовали стандартный протокол бинарного окрашивания хряща и кости альциановым синим и ализариновым красным соответственно [31].
При обработке результатов использовали регрессионный и дисперсионный анализы.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
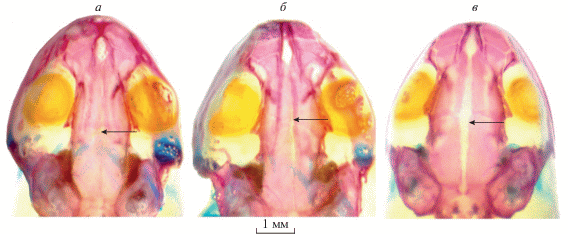
В ходе исследования особенностей формирования краниума сеголетков установлено, что для данной фазы жизненного цикла обыкновенного тритона (56-я стадия по [6]) характерны три варианта зарастания срединного шва на границе лобных и теменных костей: шов полностью закрыт; шов частично закрыт, имеется небольшая щель между костями; шов открыт (рис. 1).
Рис. 1.
Варианты зарастания срединного шва у сеголетков L. vulgaris: а – шов полностью закрыт, б – шов частично закрыт, в – шов открыт. Стрелками указан срединный шов (фото А.Г. Трофимова).
Наибольшая встречаемость варианта с полностью закрытым швом отмечена у животных из зон много- (зона II) и малоэтажной застройки (зона III) – 61.1 и 80% соответственно (табл. 1). Только в выборке из зоны III не отмечены особи с открытым швом, а наименьшая встречаемость животных с закрытым швом характерна для популяций из лесопарковой зоны и загородной популяции (41.2 и 45.5% соответственно).
Одной из особенностей пищевого рациона сеголетков в начальный период их наземной жизни на селитебной территории (зон много- и малоэтажной застройки) – преобладание в питании таких кальцефильных беспозвоночных, как моллюски, доля которых в спектре питания животных составляет 18.0 и 19.0%, против 12.5 и 2.0% в лесных и лесопарковых местообитаниях соответственно [2].
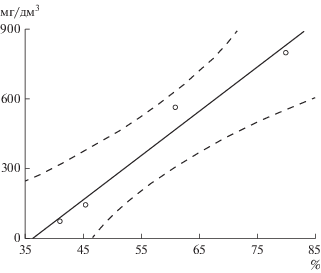
При анализе взаимосвязи минерального состава воды, особенностей содержимого желудочно-кишечного тракта сеголетков тритонов со степенью зарастания срединного шва черепа в градиенте урбанизации (табл. 2, рис. 2) выявлено наличие прямой положительной связи (r = 0.985, p = 0.015) между встречаемостью животных с полностью заросшим швом и минерализацией водной среды. На уровне тенденции отмечена положительная связь степени оссификации швов черепа со встречаемостью моллюсков в желудочно-кишечном тракте тритонов, а также с температурой и pH воды (табл. 2). Несмотря на значимые (F(3, 68) = = 11.046, p = 0.00001) различия в длине тела сеголетков из разных зон (табл. 1), достоверной связи абсолютной длины тела сеголетков с оссификацией не выявлено.
Таблица 2.
Коэффициент корреляции (R) ряда показателей с долей особей с полностью закрытым срединным швом
| Показатель | Зона II | Зона III | Зона IV | K | R |
|---|---|---|---|---|---|
| Минерализация, мг/л | 562.3 ± 31.6 (n = 8) |
793.5 ± 44.7 (n = 4) |
81.9 ± 44.7 (n = 4) |
149.3 ± 63.2 (n = 2) |
0.985 (p = 0.015) |
| рН | 8.19 ± 0.16 (n = 8) |
7.95 ± 0.22 (n = 4) |
6.75 ± 0.22 (n = 4) |
7.16 ± 0.3 (n = 2) |
0.82 (p = 0.2) |
| Среднемесячная температура мая, °С | 18.9 ± 1.0 (n = 8) |
21 ± 1.5 (n = 4) |
13.8 ± 1.5 (n = 4) |
12 ± 2 (n = 2) |
0.93 (p = 0.07) |
| Встречаемость моллюсков в ЖКТ, % числа желудков | 33.8 | 31.2 | 3.2 | 3.8 | 0.87 (p = 0.06) |
Примечание. Обозначение типов городских ландшафтов см. табл. 1. ЖКТ – желудочно-кишечный тракт, n – число измерений.
Известно, что важнейший фактор, влияющий на оссификацию скелета рыб и личинок амфибий, – уровень содержания минеральных веществ в воде. На мальках рыб установлено, что накопление кальция происходит интенсивнее в воде с высокой его концентрацией [12], в то время как ацидификация воды приводит к морфофункциональным адаптивным перестройкам проницаемости жаберного эпителия и снижению ионного транспорта [7]. Причем, прямое поглощение кальция (через жабры и кожу) превышает его потребление с пищей и у рыб [18], и у амфибий [15]. Так, у личинок лягушки-быка Lithobates catesbeianus (Shaw, 1802) с пищей поступает только 5% кальция, а вся остальная его часть – через жабры (70%) и кожу (25%). У метаморфизировавших амфибий кальций поступает только через кожу и гастроинтестинальный тракт [32]. Относительно высокие температуры также способствуют повышению степени оссификации скелета у сеголетков амфибий [23]. На основании вышеизложенного, можно предположить, что существует синергическое взаимодействие вышеупомянутых экологических факторов, которое в значительной степени определяет поступление кальция в организм и скорость зарастания срединного шва у животных в природных популяциях Lissotriton vulgaris.
Выводы. Установлено, что к моменту завершения метаморфоза состояние срединного шва крыши черепа сеголетков L. vulgaris может быть представлено тремя хорошо различимыми вариантами. В условиях селитебной части города (зон много- и малоэтажной застройки) наблюдается акселерация сеголетков L. vulgaris, выражающаяся в раннем зарастании срединного шва. Среди возможных причин наблюдаемых отличий основное значение имеет прямое влияние повышенной минерализации поверхностных вод, и в меньшей мере ‒ такие сопутствующие факторы, как увеличение доли кальцефильных организмов (раковинных гастропод) в питании сеголетков L. vulgaris, повышение температуры и рост pH водоемов селитебной части города.
Список литературы
Безуглая Э.Ю., Расторгуева Г.П., Смирнова И.В. Чем дышит промышленный город? Л.: Гидрометеоиздат, 1991. 255 с.
Берзин Д.Л., Вершинин В.Л. Особенности трофологии сеголеток обыкновенного тритона (Lissotriton vulgaris L.) на урбанизированных территориях // Вестн. Удмуртск. гос. ун-та. Сер. биол. Науки о Земле. 2016. Т. 26. Вып. 2. С. 114–120.
Вершинин В.Л. Амфибии и рептилии Урала. Екатеринбург: УрО РАН, 2007. 261 с.
Гаранин В.И., Попов А.Ю. Материалы по экологии тритонов Раифского леса (Татарская АССР) // Изв. Казан. фил. АН СССР. Сер. биол. 1958. № 6. С. 89–94.
Лебедкина Н.С. Развитие коррелятивных систем в филогенезе и онтогенезе // Морфология и эволюция животных. М.: Наука, 1986. С. 95–101.
Лиознер Л.Д. Тритоны Triturus vulgaris, Triturus cristatus // Объекты биологии развития. М.: Наука, 1975. С. 324–341.
Матей В.Е. Жабры пресноводных костистых рыб: морфофункциональная организация, адаптация, эволюция. М.: Наука, 1996. С. 1–286.
Медведева И.М. Орган обоняния амфибий и его филогенетическое значение. Л.: Наука, 1975. 260 с.
Меркулова К.М. Роль тиреоидных гормонов в регуляции онтогенеза черепа испанского тритона (Pleurodeles walti, Salamandridae, Urodela) // Вопросы герпетологии: Матер. IV съезда герпетологического общества им. А.М. Никольского. СПб.: Русская коллекция, 2011. С. 172–177.
Плисс Г.Б., Худолей В.В. Онкогенез и канцерогенные факторы у низших позвоночных и беспозвоночных животных // Экологическое прогнозирование. М.: Наука, 1979. С. 167–185.
Рузский М. Результаты исследования земноводных и пресмыкающихся в Казанской губернии и местностях с нею смежных // (Предварительный отчет Казанского общества естествознания). Приложения к протоколам заседаний общества естествоиспытателей при Императорском Казанском университете. 1894. № 139. С. 1–8.
Русанов В.В. Влияние ультрафиолетовых лучей на рост и обмен кальция у мальков карпа // Изв. ГосНИИ озер. и реч. рыб. хоз-ва. Л., 1974. Т. 92. С. 141–144.
Шарлеманъ Э.В. Заметки о фауне пресмыкающихся и земноводныхъ окрестностей Кiева // Материалы къ познанiю фауны юго-зап. Россiи. Кiев, 1917. Т. 2. С. 1–17.
Andrzejewski R., Babinska–Werka J., Gliwicz J., Goszczynski J. Synurbization processes in population of Apodemus agrarius. I. Characteristics of populations in an urbanization gradient // Acta Theriol. 1978. V. 23. P. 341–358.
Baldwin G.F., Bentley P.J. Calcium Metabolism in Bullfrog Tadpoles (Rana catesbeiana) // J. Exper. Biol. 1980. V. 88. P. 357–366.
Banks B., Laverick G. Garden ponds as amphibian breeding sites in a conurbation in the north east of England (Sunderland Tyne and Weare) // Herpetol. J. 1986. V. 1. № 2. P. 44–50.
Beebee T.J.C. Observation concerning the decline of the British amphibia // Biol. Conserv. 1973. V. 5. № 1. P. 20–24.
Berg A. Studies on the metabolism of calcium and strontium in fresh-water fish. II. Relative contribution of direct and intestinal absorption in growth conditions // Mem. Ist. Ital. Idrobiol. 1970. V. 26. P. 241–255.
Hanken J., Hall B.K. Variation and timing of the cranial ossification sequence of the Oriental fire-bellied toad, Bombina orientalis (Amphibia, Discoglossidae) // J. Morphol. 1984. V. 182. P. 245–255.
Hanken J., Hall B.K. Skull development during anuran metamorphosis. II. Role of thyroid hormone in osteogenesis // Anat. Embryol. 1988. V. 178. P. 219–227.
Gaudin A.J. The sequence of cranial ossification in the California toad, Bufo boreas (Amphibia, Anura, Bufonidae) // J. Herpetol. 1978. V. 12. P. 309–318.
Gilbert S.F. Ecological Developmental Biology: Developmental Biology Meets the Real World // Develop. Biol. 2001. V. 233. P. 1–12.
Gomez-Mestre I., Saccoccio V.L., Iijima T. et al. The shape of things to come: linking developmental plasticity to post-metamorphic morphology in anurans // J. Evol. Biol. 2010. V. 23. P. 1364–1373.
Rose C.S. An endocrine-based model for developmental and morphogenetic diversification in metamorphic and paedomorphic urodeles // J. Zool. 1996. V. 239. P. 253–284.
Rose C.S. The developmental morphology of salamander skulls // Amphibian Biology. V. 5: Osteology, Surrey Beatty and Sons, Australia: Heatwole, H. & Davies, 2003. P. 1684–1781.
Smirnov S.V., Vassilieva A.B. Bony Skull of the Smooth Newt Triturus vulgaris (Amphibia, Urodela: Salamandridae) and the Role of Thyroid Hormones in Its Ossification // Dokl. Biol. Sci. 2003. V. 388. P. 73–75.
Smirnov S.V., Vassilieva A.B. Skeletal and dental ontogeny in the smooth newt, Triturus vulgaris (Urodela: Salamandridae): role of thyroid hormone in its regulation // Rus. J. Herpetol. 2003. V. 10. № 2. P. 93–110.
Trueb L., Hanken J. Skeletal development in Xenopus laevis (Anura: Pipidae) // J. Morphol. 1992. V. 214. P. 1–41.
Vershinin V.L. Features of amphibian populations of an industrial city // Urban ecological studies in Central and Eastern Europe. Warszawa: Wydawinstwo Polskej Akademii nauk, 1990. P. 112–121.
Vershinin V.L., Vershinina S.D., Berzin D.L. et al. Long-term observation of amphibian populations inhabiting urban and forested areas in Yekaterinburg, Russia // Scientific Data. 2015. P. 1–13. https://doi.org/10.1038/sdata.2015.18
Wassersug R.J. A Procedure for Differential Staining of Cartilage and Bone in Whole Formalin–Fixed Vertebrates // Stain Technol. 1976. V. 51. № 2. P. 131–134.
Wright K. Important clinical aspects of amphibian physiology // Proceedings of the North American veterinary conference, January 7–11, 2006, Orlando, Florida. V. 20. Small Animal Edition, 2006. P. 1686–1688.
Дополнительные материалы отсутствуют.
Инструменты
Биология внутренних вод