Физиология человека, 2020, T. 46, № 2, стр. 63-75
Анализ паттернов ЭЭГ у лиц с паническими атаками
О. Е. Дик 1, *, И. А. Святогор 1, Т. Н. Резникова 2, Д. А. Федоряка 2, А. Д. Ноздрачев 1
1 ФГБУН Институт физиологии имени И.П. Павлова РАН
Санкт-Петербург, Россия
2 ФГБУН Институт мозга человека РАН
Санкт-Петербург, Россия
* E-mail: dickviola@gmail.com
Поступила в редакцию 03.03.2019
После доработки 16.04.2019
Принята к публикации 03.09.2019
Аннотация
Исследована динамика усвоения ритма фотостимуляции у лиц с паническими атаками с помощью вейвлетного и рекуррентного методов анализа реактивных паттернов электроэнцефалограмм (ЭЭГ). Количественные показатели динамики усвоения ритма предложенной частоты оценивались по нарастанию энергии вейвлетного спектра в период фотостимуляции и значениям коэффициента усвоения ритма, а также характеристикам совместной рекуррентной диаграммы светового сигнала и паттерна ЭЭГ (скорости и времени возврата траектории ЭЭГ в окрестность точки, в которой она была ранее). Эти показатели определены до и после немедикаментозного метода терапии, связанного с формированием и активацией артифициальных стабильных функциональных связей мозга (АСФС). Показано, что сеансы АСФС приводят к уменьшению асимметрии ответов затылочных долей мозга на фотостимул и снижению степени невротизации пациента с паническими атаками, что отражается в уменьшении значений коэффициента усвоения, уменьшении скорости и увеличении времени возврата. Улучшение психофизиологического состояния пациента после курса активаций АСФС подтверждено положительными изменениями, по данным психологической диагностики.
Паническая атака – комплекс симптомов, характеризующийся пароксизмальным страхом, часто сопровождающимся чувством неминуемой гибели, или тревогой и ощущением внутреннего напряжения [1–3]. Возникновение данного патологического состояния может быть связано с генетической предрасположенностью [4] или нарушениями взаимоотношений симпатической и парасимпатической систем [5], а также с изменениями уровня катехоламинов [6], серотонина [7] или γ-аминомаслянной кислоты [8]. По данным литературы, отмечается высокая распространенность панических атак: у 3% населения промышленно-развитых стран [9].
Актуальность проблемы лечения этого расстройства связана преимущественно с недостаточной эффективностью и трудностью выбора главного направления терапии: одни исследователи отдают предпочтение психофармакотерапии [10–12], а другие ведущую роль отводят психотерапии [13, 14] и психофизиологическим методам лечения [15]. В связи с этим сохраняется актуальность поиска эффективных и безопасных немедикаментозных методов терапии панических атак. К ним относится метод формирования и активации артифициальных стабильных функциональных связей (АСФС) мозга человека. В основе метода АСФС лежит внутримозговой феномен долговременной памяти, представляющий особый вид функциональных связей мозга, формирующихся в условиях активации подкорковых структур и импульсной стимуляции, и связанный с регуляторными системами мозга [16]. Преимущество метода АСФС заключается в доказанной эффективности лечения функциональных расстройств, в том числе, фобических неврозов [17–23].
Цель данной работы – количественная оценка функционального состояния нервной системы на основе анализа динамики реактивных паттернов ЭЭГ во время ритмической фотостимуляции у лиц с паническими атаками до и после сеансов АСФС.
МЕТОДИКА
В обследовании участвовали 10 пациентов в возрасте от 26 до 45 лет (в среднем 35.5 лет) с давностью заболевания в среднем 10.5 лет и диагнозом “паническое расстройство” (F 41.0), удовлетворяющим критериям МКБ-10. Малую выборку осуществляли в связи с новизной использования указанного метода для больных с паническими атаками, и рассматривали как экспериментальную. Все лица данной группы амбулаторно лечились в клинике Института мозга человека РАН. Для них были характерны жалобы на приступообразную тревогу и страх, а также вегетативные проявления в виде учащенного сердцебиения, затруднения дыхания, потливости.
Курс коррекции состоял из сеанса формирования АСФС (фотостимуляция 20 Гц, длительностью 10 с на фоне действия фармакологического препарата этимизола) и последующих 10 сеансов активаций АСФС (каждый сеанс состоял из 6 серий фотостимуляций заданной при формировании частоты без дополнительных фармакологических воздействий). Интервалы между подачей стимула составляли 1–2 мин, длительность одного сеанса активации АСФС составляла 15–20 мин. Курс составлял 4 нед. Во время проведения сеансов больные находились в комфортной позе, лежа, с закрытыми глазами. Фотостимуляцию проводили с помощью “тренажера функциональной активности мозга ТММ Мираж”, который является представителем линии приборов световой стимуляции (контрактное производство, ООО НПП “МедПАСС”, Россия); качество печатных плат соответствует требованиям ГОСТ 23 752-79 “Платы печатные. Общие технические условия”; система менеджмента качества на заводе, соответствует требованиям ISO 9001-2008. Данный прибор и его модификации активно используется для коррекции психофизиологического состояния спортсменов и здоровых лиц. Он надежно зарекомендовал себя в программах немедикаментозной коррекции в более ранних исследованиях [21–23].
До начала курса этих сеансов и после них регистрировали и анализировали биоэлектрическую активность мозга, а также проводили психологическое исследование с помощью методик СМИЛ (“Стандартизированный многофакторный метод исследования личности”), ИСАС (“Опросник иерархической структуры актуальных страхов личности”), теста Тейлор, двойной и корректурной проб.
Электрическую активность мозга регистрировали на 21-канальном электроэнцефалографе (Мицар-ЭЭГ, Россия). Активные электроды располагали по стандартной схеме 10 /20. В качестве индифферентного электрода использовали усредненный электрод Av. Данные записывались с частотой дискретизации 256 Гц и содержали безартефактные фрагменты записи в трех состояниях: до воздействия светового стимула, во время действия стимула и во время релаксации. Фотостимулятор находился на расстоянии 15 см от глаз пациента в темном помещении. Энергия лампы составляла 0.3 Дж. Действие светового стимула длилось 10 с для каждой частоты, время релаксации до включения фотовспышки другой частоты составляло 20 с. В связи с тем, что световые сигналы имеют максимальную амплитуду в затылочных долях мозга, анализировали паттерны в O1-, Oz- и O2-отведениях.
Для оценки реакции усвоения ритма в паттернах ЭЭГ применяли два метода: 1) метод непрерывного вейвлет-преобразования [24] и пакет программ Wavelet Toolbox MATLAB и 2) метод кросс-рекуррентного анализа [25] и процедуры CRP Toolbox, доступные на сайте tocsy.pik-potsdam.de/crp.php.
При первом методе в качестве базисного вейвлета использовали комплексный вейвлет Морле:
(1)
${{\psi }_{0}}(t) = {{\pi }^{{{{ - 1} \mathord{\left/ {\vphantom {{ - 1} 4}} \right. \kern-0em} 4}}}}\exp ( - 0.5{\kern 1pt} {{t}^{2}})\exp (i{{\omega }_{0}}t){\text{,}}$в котором значение параметра ω0 = 2π обеспечивает простое соотношение между масштабом вейвлет-преобразования a и действительной частотой f исследуемого сигнала [24, 26]:
(2)
$f = \frac{{{{\omega }_{{{\kern 1pt} 0}}} + \sqrt {2 + {{\omega }_{{{\kern 1pt} 0}}}} }}{{4\pi a}} \approx {1 \mathord{\left/ {\vphantom {1 a}} \right. \kern-0em} a}.$Непрерывное вейвлет-преобразование сигнала x(t) определяется функцией:
(3)
$W(a,{{t}_{0}}) = \frac{1}{{\sqrt a }}\int\limits_{ - \infty }^{ + \infty } {x(t){\text{ }}\psi {\kern 1pt} {\text{*}}\left( {\frac{{t - {{t}_{0}}}}{a}} \right)dt} ,$В силу указанной выше связи между a и f можно записать:
(4)
$\begin{gathered} W(f,{{t}_{0}}) = {{\pi }^{{{{ - 1} \mathord{\left/ {\vphantom {{ - 1} 4}} \right. \kern-0em} 4}}}}\sqrt f \int\limits_{ - \infty }^\infty {x(t)} \exp ( - 0.5{{(t - {{t}_{0}})}^{2}}{{f}^{2}}) \times \\ \times \,\,\left( {\exp ( - i2\pi (t - {{t}_{0}})f} \right)dt{\text{.}} \\ \end{gathered} $Величина квадрата модуля вейвлет-преобразования |W(f, t0)|2 задает локальный вейвлетный спектр энергии паттерна ЭЭГ в момент времени t0, т.е. мгновенное распределение энергии по частотам f. Интеграл от локального вейвлетного спектра $E(f) = \int_{{{t}_{1}}}^{{{t}_{2}}} {W{{{(f,{{t}_{0}})}}^{2}}d{{t}_{0}}} $ определяет глобальный вейвлетный спектр, т.е. интегральное распределение энергии вейвлетного спектра сигнала по частотам в интервале времени [t1, t2]. Интегрирование по частоте $E({{t}_{0}}) = \int_{{{f}_{{\text{C}}}} - \Delta f}^{{{f}_{{\text{C}}}} + \Delta f} {{{{\left| {W(f,{{t}_{0}})} \right|}}^{2}}df} $ задает энергию вейвлетного спектра в диапазоне вокруг частоты фотостимуляции fC.
Световой сигнал задавался последовательностью k импульсов, следующих с частотой fC:
(5)
$p(t) = \sum\limits_{j = 0}^{k - 1} {\frac{{0.5}}{{{{r}_{0}}\sqrt \pi }}} \exp \left( { - \frac{{{{{(t - {{t}_{j}})}}^{2}}}}{{4r_{0}^{2}}}} \right),$Вейвлет-преобразование светового сигнала находилось в виде:
(6)
$\begin{gathered} W(f,{{t}_{0}}) = {{\pi }^{{{{ - 1} \mathord{\left/ {\vphantom {{ - 1} 4}} \right. \kern-0em} 4}}}}\frac{{\sqrt f }}{{\sqrt g }}\sum\limits_{j = 0}^{k - 1} {\exp \left( { - \left( {\frac{f}{{4r_{0}^{2}}} + g} \right)} \right.{{{\left( {t{}_{j}\, - \,t{}_{0}} \right)}}^{2}}} + \\ + \,\,i\left. {\frac{{2\pi {{f}^{2}}}}{g}\left( {t{}_{j}\, - \,t{}_{0}} \right) + \frac{{{{{(2\pi {{r}_{0}})}}^{2}}{{f}^{3}}}}{g}} \right), \\ \end{gathered} $Наличие реакции усвоения по методу вейвлет-преобразования оценивали по величине коэффициента усвоения ритма (kR) в исследуемом частотном диапазоне [fС – Δ f, fС + Δ f], где Δ f = 0.5 Гц, и по нарастанию энергии вейвлетного спектра непосредственно в период фотостимуляции.
Коэффициент усвоения ритма (kR) определяли как отношение максимумов глобальных вейвлетных спектров во время (рис. 1, Б) и до действия фотостимула (рис. 1, А): kR = $ = {{{{E}_{{\max }}}{{{(f)}}_{{{\text{during}}}}}} \mathord{\left/ {\vphantom {{{{E}_{{\max }}}{{{(f)}}_{{{\text{during}}}}}} {{{E}_{{\max }}}{{{(f)}}_{{{\text{before}}}}}}}} \right. \kern-0em} {{{E}_{{\max }}}{{{(f)}}_{{{\text{before}}}}}}}.$ При этом значение коэффициента kR < 1 означало меньшее значение максимума глобального вейвлетного спектра во время фотостимуляции, по сравнению с максимумом спектра до фотостимуляции, т.е. отсутствие нарастания энергии вейвлетного спектра при действии определенного светового сигнала и отсутствие усвоения заданной частоты.
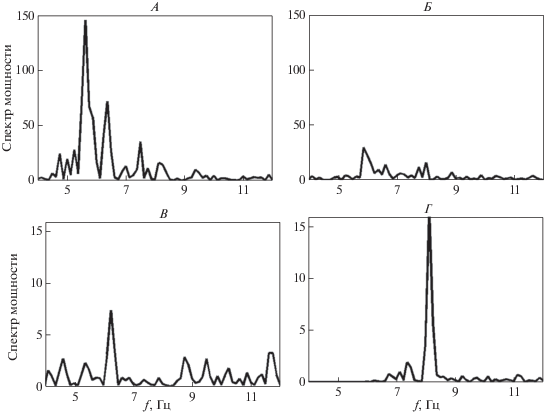
Рис. 1.
Пример наличия реакции усвоения ритма частоты 20 Гц в паттерне ЭЭГ (отведение О1). А–Б – глобальные вейвлетные спектры E(f) до и во время действия фотостимула. В – проекция локального вейвлетного спектра паттерна на плоскость (t, f). Г – нормированные интегральные распределения энергии вейвлетных спектров паттерна ЭЭГ (а) и фотостимула (б). Начало и конец фотостимуляции отмечены вертикальными стрелками.
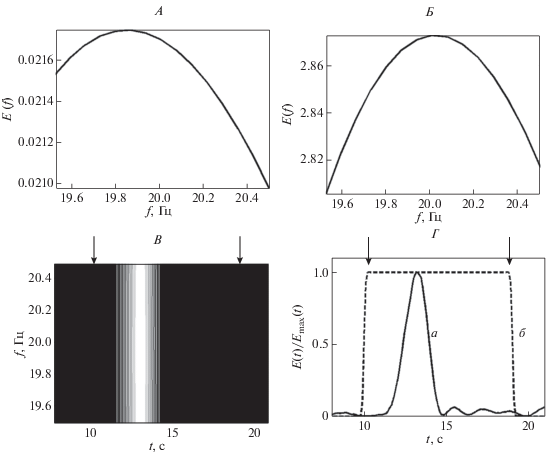
Нарастание энергии вейвлетного спектра непосредственно в период действия фотостимула показано на рис. 1, В и Г, которые иллюстрируют проекцию локального вейвлетного спектра на плоскость (t, f) (рис. 1, В) и нормированные интегральные распределения энергий вейвлетных спектров $e({{t}_{0}}) = {{E({{t}_{0}})} \mathord{\left/ {\vphantom {{E({{t}_{0}})} {{{E}_{{\max }}}({{t}_{0}})}}} \right. \kern-0em} {{{E}_{{\max }}}({{t}_{0}})}}$ паттерна ЭЭГ и светового сигнала (рис. 1, Г, а и б соответственно). Начало и конец действия фотостимула показаны на рис. 1, В и Г стрелками.
Второй метод анализа реакции усвоения ритма в паттернах ЭЭГ связан с построением совместных рекуррентных диаграмм паттерна ЭЭГ и светового сигнала. Совместная рекуррентная диаграмма представляет собой графическое представление матрицы ${{R}_{{i,j}}}(\varepsilon ) = \left\{ {\begin{array}{*{20}{c}} {1,{{y}_{i}} \approx {{y}_{j}},{{z}_{i}} \approx {{z}_{j}},} \\ {0,{{y}_{i}} \ne {{y}_{j}},{{z}_{i}} \ne {{z}_{j}}} \end{array}} \right.,$ в которой значения 1 или 0 соответствуют черной или белой точкам, при этом черная точка означает наличие рекуррентности, а белая точка – ее отсутствие. Совместная рекуррентность с точностью до ε-ошибки определяется как возврат состояния yj фазовой траектории сигнала ЭЭГ к состоянию yi и одновременный возврат состояния zj фазовой траектории светового сигнала к состоянию zi [25].
Фазовые траектории состояний z(t) и y(t) получили из исходных временны́ х рядов {x(t)} и {p(t)} методом временны́ х задержек [27]: y(t) = (x(t), x(t + d), …, x(t + (m – 1)d)), где d – временнáя задержка, m – размерность вложения (минимальная размерность пространства, в котором восстановленная траектория воспроизводит свойства исходной траектории). Оптимальная временнáя задержка d находилась на основании поиска первого минимума функции взаимной информации [28]. Оптимальную размерность вложения m определяли методом поиска минимума ближайших ложных соседей [29]. Выделение сигнала в узкой полосе частот вблизи частоты фотостимуляции позволило находить в качестве оптимальной размерности вложения значения m < 5. Величину ε-ошибки выбирали равной 1% от величины стандартного отклонения анализируемого сигнала.
Реакцию усвоения ритма в паттернах ЭЭГ методом анализа совместных рекуррентностей паттерна ЭЭГ и светового сигнала оценивали по численным показателям рекуррентных диаграмм: скорости возврата (recurrence rate) RR и времени возврата τ (рекуррентному времени, необходимому для возврата значения сигнала в ε окрестность точки, в которой оно было ранее).
Для выяснения различий между средними значениями вычисленных параметров для различных отведений в группе лиц с паническими атаками, а также для определения статистически значимых различий между средними значениями параметров, полученными до и после сеансов АСФС использовали непараметрический тест Манна-Уитни (p < 0.05).
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
По данным проведенного психологического исследования после воздействия методом АСФС были выявлены положительные изменения, которые касались эмоциональной, активирующей, когнитивной и личностной сферы. Наблюдалось существенное снижение жалоб, главным образом, на страх и тревогу, а также вегето-сосудистые реакции, улучшение состояния больного по всем клиническим параметрам – в виде снижения выраженности, развернутости и частоты приступов. Все больные отмечали значительное уменьшение или полное исчезновение приступов панических атак, снижение общей и ситуационной тревоги.
Достоверные изменения усредненных показателей проведенных психологических тестов до и после курса коррекции представлены в табл. 1.
Таблица 1.
Достоверные изменения психологических показателей у больных с паническими атаками до и после курса коррекции методом формирования и активации АСФС (n = 10)
| Показатели тестов | До курса коррекции | После курса коррекции | p |
|---|---|---|---|
| Оперативная память (двойной тест) | 3.4 ± 0.9 | 4.8 ± 0.8 | <0.05 |
| Индекс кратковременной памяти (двойной тест) | 5.1 ± 1.7 | 8 ± 1.6 | <0.05 |
| Пропускная способность зрительного анализатора (корректурная проба) | 1.1 ± 0.1 | 1.6 ± 0.2 | <0.05 |
| Суммарная тревога (тест Тейлор) | 27.7 ± 5.9 | 21.5 ± 3.3 | <0.01 |
| Общий показатель страха (ИСАС) | 126 ± 14 | 97 ± 11 | <0.05 |
| Шкала депрессивности (СМИЛ) | 80.4 ± 8 | 61.3 ± 6 | <0.05 |
| Шкала психастении (СМИЛ) | 76.2 ± 6.7 | 65.6 ± 5.1 | <0.05 |
| Шкала гипомании (СМИЛ) | 59.4 ± 5 | 50.5 ± 5.3 | <0.05 |
Как видно из табл. 1, за 10 сеансов активаций АСФС происходило достоверное снижение общего усредненного показателя страха (p < 0.05) и снижение уровня суммарной тревоги (p < 0.01), которые являлись ведущими симптомами в клинической картине болезни в исходном состоянии. Кроме того, после воздействия методом АСФС наблюдались положительные изменения пропускной способности зрительного анализатора по данным корректурной пробы и индекса кратковременной памяти по двойному тесту, что говорит о повышении уровня психической активности. По опроснику СМИЛ (стандартизованный метод исследования личности), отмечалось достоверное снижение показателей по шкалам депрессивности, психастении и гипомании (p < < 0.05), что свидетельствует о снижении внутренней напряженности, психологической депрессивности, тревожно-фобических явлений, повышении активности и коммуникабельности больных.
В фоновых паттернах ЭЭГ 69% больных с паническими атаками до сеансов активаций АСФС преобладала высокоамплитудная активность θ-диапазона (рис. 2, А), а в паттернах ЭЭГ 31% больных наблюдалась низкоамплитудная полиморфная активность в δ-, θ- и α-диапазонах (рис. 2, В). Сеансы АСФС приводили к значительному уменьшению амплитуды θ-активности (рис. 2, Б), исчезновению полиморфной активности и усилению активности в α-диапазоне (рис. 2, Г).
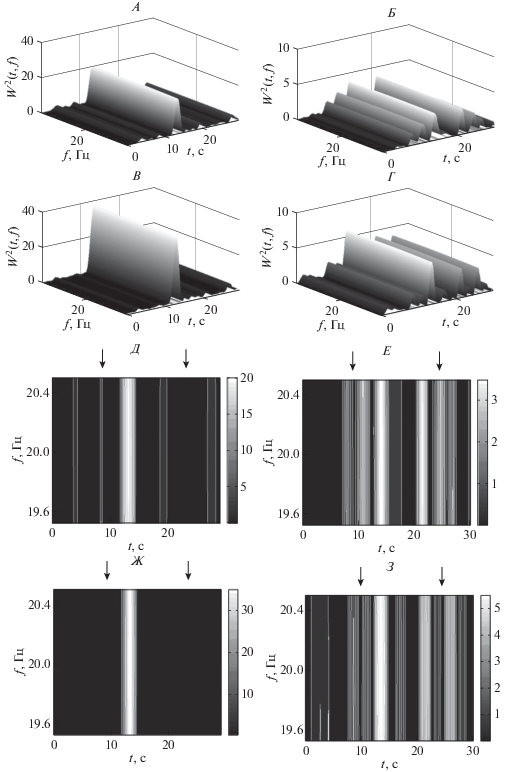
Реактивные паттерны ЭЭГ во время фотостимуляции у 9 из 10 исследуемых пациентов характеризовались асимметрией ответов затылочных долей мозга на фотостимул. Это проявлялось в различных значениях максимумов локальных вейвлетных спектров паттернов ЭЭГ, регистрируемых в О1- и О2-отведениях. Примеры локальных вейвлетных спектров паттернов ЭЭГ в этих отведениях и их проекции на плоскость (t, f) представлены на рис. 3, А, В и рис. 3, Д, Ж соответственно. Начало и конец фотостимуляции отмечены на рис. 3, Д, Ж вертикальными стрелками. Максимум локального вейвлетного спектра паттерна ЭЭГ в отведении О2 и в данном примере в 1.7 раза превышает максимум спектра в отведении О1.
Рис. 3.
Уменьшение максимумов вейвлетных спектров паттернов ЭЭГ после АСФС. А–Г – локальные вейвлетные спектры паттернов ЭЭГ: до АСФС в отведениях О1 (А) и О2 (В) и после АСФС в отведениях О1 (Б) и О2 (Г). Д–З – в таком же порядке проекции этих спектров на плоскость (t, f). Начало и конец фотостимуляции отмечены вертикальными стрелками.
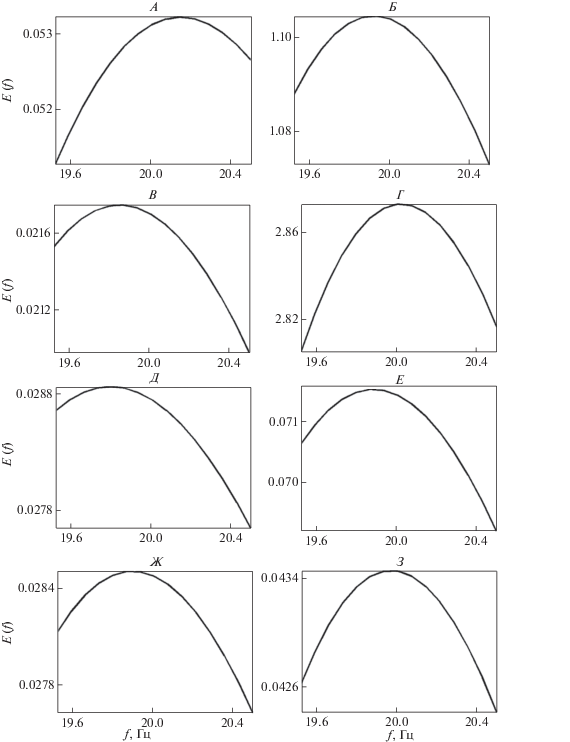
Представленные на рис. 4 глобальные вейвлетные спектры паттернов ЭЭГ, построенные в узких частотных диапазонах вблизи частоты фотостимуляции до начала действия фотостимула и во время фотостимуляции, также демонстрируют наличие асимметрии ответов затылочных долей мозга на фотостимул. Так, по данным рис. 4, А, Б, значение коэффициента усвоения ритма предложенной частоты 20 Гц kR = 20 для отведения О1 и kR = 132 для отведения О2 (данные рис. 4, В, Г). После сеансов АСФС наблюдалось уменьшение асимметрии ответов и значительное уменьшение значений коэффициента усвоения ритма данной частоты 20 Гц (kR = 2.5 для отведения О1 и kR = 1.5 для отведения О2, данные рис. 4, Д, З).
Рис. 4.
Примеры глобальных вейвлетных спектров паттернов ЭЭГ до АСФС (А–Г) и после АСФС (Д–З). А, Б, Д, Е – соответствуют отведению О1, В, Г, Ж, З – отведению О2. А, В, Д, Ж – получены до действия фотостимула, Б, Г, Е, З – во время действия фотостимула.
В табл. 2 приведены средние значения коэффициентов усвоения (kR) для реактивных паттернов ЭЭГ до и после сеансов АСФС. Значения усреднялись по числу тестируемых больных.
Таблица 2.
Усредненные значения коэффициентов усвоения (kR) ритма заданной частоты, скорости возврата (RR) и времени возврата (τ) в совместных рекуррентных диаграммах паттернов ЭЭГ и световых сигналов
| ЭЭГ пациентов (n = 9 из 10) до АСФС | ЭЭГ пациентов (n = 9 из 10) после АСФС | |||||
|---|---|---|---|---|---|---|
| частота, Гц | О1 | О2 | p | О1 | О2 | p |
| Коэффициент усвоения (kR) ритма заданной частоты | ||||||
| 6 | <1 | <1 | >0.05 | <1 | <1 | >0.05 |
| 8 | <1 | 1.1 ± 0.1 | >0.05 | <1 | <1 | >0.05 |
| 12 | 1.9 ± 0.2 | 2.7 ± 0.2 | >0.05 | <1 | <1 | >0.05 |
| 14 | 5.4 ± 0.5 | 122 ± 18 | 0.039 | 2.1 ± 02 | 3.5 ± 0.3 | >0.05 |
| 18 | 35 ± 3.7 | 147 ± 15 | 0.045 | 11 ± 1.2 | 17 ± 1.8 | >0.05 |
| 20 | 22 ± 1.9 | 101 ± 11 | 0.038 | 5.5 ± 0.5 | 7.1 ± 0.7 | >0.05 |
| Время возврата (τ) | ||||||
| 6 | 39 ± 3.1 | 33 ± 3.1 | >0.05 | 35 ± 3.3 | 31 ± 3.0 | >0.05 |
| 8 | 32 ± 3.1 | 31 ± 3.5 | >0.05 | 29 ± 2.7 | 33 ± 3.1 | >0.05 |
| 12 | 28 ± 2.7 | 24 ± 2.3 | >0.05 | 39 ± 3.9 | 41 ± 4.1 | >0.05 |
| 14 | 13 ± 1.1 | 8 ± 0.8 | 0.047 | 44 ± 4.3 | 36 ±3.5 | 0.049 |
| 18 | 7 ± 0.6 | 4 ± 0.3 | 0.041 | 25 ± 2.4 | 30 ± 2.9 | 0.036 |
| 20 | 11 ± 1.1 | 7 ± 0.6 | 0.039 | 37 ± 3.6 | 46 ± 4.5 | 0.042 |
| Скорость возврата (RR) | ||||||
| 6 | 0.05 ± 0.005 | 0.04 ± 0.004 | >0.05 | 0.06 ± 0.006 | 0.03 ± 0.003 | >0.05 |
| 8 | 0.03 ± 0.003 | 0.03 ± 0.003 | >0.05 | 0.02 ± 0.002 | 0.04 ± 0.004 | >0.05 |
| 12 | 0.08 ± 0.008 | 0.07 ± 0.007 | >0.05 | 0.05 ± 0.005 | 0.06 ± 0.006 | >0.05 |
| 14 | 0.11 ± 0.01 | 0.13 ± 0.01 | >0.05 | 0.02 ± 0.002 | 0.03 ± 0.003 | >0.05 |
| 18 | 0.13 ± 0.01 | 0.15 ± 0.01 | >0.05 | 0.03 ± 0.003 | 0.02 ± 0.002 | >0.05 |
| 20 | 0.12 ± 0.01 | 0.17 ± 0.01 | 0.037 | 0.04 ± 0.003 | 0.02 ± 0.002 | 0.048 |
Для 9 из 10 пациентов с паническими атаками значение коэффициента усвоения ритма kR < 1 для частот θ-диапазона, что означает отсутствие нарастания энергии паттерна ЭЭГ во время фотостимуляции и отсутствие усвоения ритма данного диапазона. Незначительное усвоение выявлялось для частот α-диапазона (kR = 1.9 ± 0.2 и kR = = 2.7 ± 0.2 для 12 Гц и kR = 1.1 ± 0.1 для 8 Гц). Значительное усвоение определялось для частот β-диапазона, например, kR = 22 ± 1.9 и kR = = 101 ± 11 для 20 Гц. При этом отмечалось практически пятикратное превышение значений коэффициента усвоения ритма kR для отведения О2, по сравнению со значениями для отведения О2. Таким образом, обнаружены статистически значимые различия в средних значениях коэффициента kR, вычисленных для затылочных отведений О1 и О2 (p < 0.05), что свидетельствует об асимметрии реакции усвоения ритма β-диапазона у большинства тестируемых пациентов.
После сеансов АСФС асимметрия ответов затылочных долей мозга становилась статистически незначимой (p > 0.05), а значения коэффициента усвоения ритма частот α-диапазона kR < 1, что означает отсутствие усвоения ритма α-диапазона. Усвоение ритма β-диапазона значительно уменьшалось (kR = 11 ± 1.2 для отведения О1 и kR = 17 ± 1.8 для отведения О2 для частоты 18 Гц).
Динамика изменения усвоения ритма в паттернах ЭЭГ у пациентов с паническими атаками после сеансов АСФС подтверждалась также изменением одновременных рекуррентностей (повторяемости) в совместных рекуррентных диаграммах этих паттернов и ритмических световых сигналов определенных частот. Примеры таких диаграмм до и после сеансов АСФС представлены на рис. 5, Б и Г соответственно. Эти диаграммы построены для интервала фотостимуляции частотой 20 Гц при величине временнóй задержки d = 3 и размерности вложения m = 3, величина размера окрестности ε равна 1% от величины стандартного отклонения анализируемых временны́ х рядов. На рис. 5, А, В показаны соответствующие паттерны ЭЭГ во время фотостимуляции данной частотой (а) и фотостимул (б).
Рис. 5.
Примеры паттернов ЭЭГ во время фотостимуляции частотой 20 Гц до (А) и после АСФС (В) (отведение О2). ЭЭГ – кривая а, фотостимул – кривая б. Б, Г – совместные рекуррентные диаграммы этих паттернов и световых сигналов. Д, Е – изменение скорости и времени возврата значения паттерна ЭЭГ в ε окрестность точки, в которой оно было ранее (до (а) и после (б) АСФС).
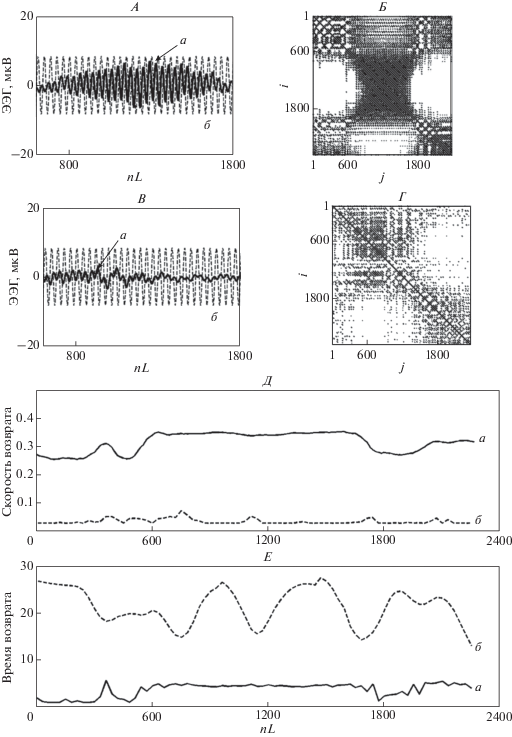
Правая диаграмма (рис. 5, Б) имеет рекуррентные структуры, cодержащие длинные диагональные линии, что свидетельствует о возникновении одновременных рекуррентностей в паттерне ЭЭГ и световом сигнале заданной частоты. Во время нарастания амплитуды ответа мозга на фотостимуляцию предложенной частоты (интервал значений nL от 600 до 1800) число одновременных рекуррентностей возрастает, что отражается в увеличении длины диагональных линий в рекуррентной диаграмме.
В отличие от этого, правая диаграмма (рис. 5, Г) содержит только короткие диагональные линии, что свидетельствует о слабой совместной рекуррентности в данном световом сигнале и анализируемом паттерне ЭЭГ.
На рис. 5, Д и Е представлена динамика изменений значений показателей рекуррентных диаграмм: скорости возврата (RR) и времени возврата (τ) значения сигнала в ε окрестность точки, в которой это значение было ранее. После сеансов АСФС наблюдается шестикратное уменьшение скорости и увеличение времени возврата, что подтверждает снижение совместной рекуррентности светового сигнала и физиологического ответа.
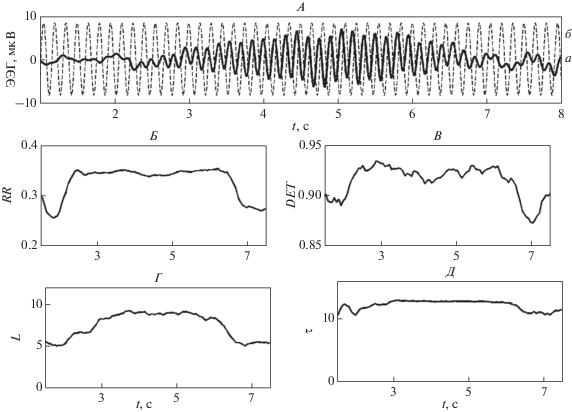
На рис. 6 вместо числа значений nL по оси абцисс отложено время, вычисленное в соответствии с правилом t = nL*dt, где dt = 1/Fs, Fs – частота дискретизации регистрируемого сигнала. Рис. 6, А показывает постепенное нарастание и спад амплитуды паттерна ЭЭГ в интервале времени от 2.3 до 6.7 с в ответ на фотостимуляцию частотой 20 Гц, которая длилась 10 с. В этом интервале происходит увеличение следующих показателей рекуррентной диаграммы: скорости возврата (RR) (рис. 6, Б), детерминизма (DET) (рис. 6, В), средней длины диагональных линий (L) (рис. 6, Г) и времени возврата (τ) (рис. 6, Д).
Рис. 6.
Паттерн ЭЭГ во время фотостимуляции (а) и световой стимул частотой 20 Гц (б) (А). Изменения во времени показателей рекуррентной диаграммы: скорости возврата (RR) (Б), детерминизма (DET) (В), средней длины диагональных линий (L) (Г) и времени возврата (τ) (Д).
Средние значения скорости (RR) и времени возврата (τ) для реактивных паттернов ЭЭГ до и после сеансов АСФС (усредненные по числу тестируемых больных) приведены в табл. 2. Данные табл. 2 свидетельствуют о повышении средних времен возврата после сеансов АСФС при фотостимуляции с частотами α- и β-диапазонов. Например, для частоты 14 Гц τ = 7 ± 0.6 (для отведения О1) и τ = 4 ± 0.3 (для отведения О2), а после сеансов АСФС значение времен возврата увеличивалось до τ = 44 ± 4.3 (для отведения О1) и τ = = 36 ± 3.5 (для отведения О2). Характерное отсутствие усвоения ритма частот θ-диапазона для тестируемых больных подтверждалось отсутствием статистически значимых изменений динамики показателей рекуррентных диаграмм во время действия фотостимула.
Значения второго показателя совместной рекуррентности (скорости возврата траектории сигнала в ε окрестность точки, в которой она была ранее) статистически не отличаются для разных затылочных отведений для всех анализируемых частот, кроме частоты 20 Гц (RR = 0.12 ± 0.01 для отведения О1 и RR = 0.17 ± 0.01 для отведения О2). Уменьшение величины RR после сеансов АСФС характерно только для частот β-диапазона (RR = = 0.12 ± 0.01 до сеансов АСФС и RR = 0.04 ± 0.003 после сеансов АСФС).
Средняя длина диагональных линий (L) также статистически значимо уменьшалась для частот именно β-диапазона. Таким образом, оба метода, используемые в работе, указывают на то, что для пациентов с паническими атаками отмечается значительная реакция усвоения ритма частот именно β-диапазона и отсутствие реакции усвоения ритма частот θ- и α-диапазона или незначительная реакция усвоения некоторых частот α-диапазона.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Как известно, выраженность перестроек электрической активности мозга в соответствии с частотой, равной или кратной частоте световых импульсов, определяется возбудимостью нейронов коры головного мозга, зависящей от соотношения синхронизирующих и десинхронизирующих процессов [30]. В связи с этим мозг здорового человека или человека с нарушениями функционального состояния центральной нервной системы по-разному реагирует на фотостимуляцию, т.е. по-разному воспроизводит ритмы частот β-, θ- или α-диапазонов [31, 32]. Например, количественные показатели реакции усвоения при нарушениях функционального состояния центральной нервной системы, связанных с сосудистой патологией мозга различной степени выраженности, статистически значимо отличаются от показателей, определенных для здорового человека [32, 33]. По мере нарастания проявлений сосудистой патологии от вегето-сосудистой дистонии к гипертонической болезни и вертебрально-базилярной недостаточности отмечается повышение показателей реакции усвоения [32].
Для здорового человека, как правило, значение коэффициента усвоения ритма меньше единицы или близко к единице, т.е. для него характерна незначительная реакция усвоения ритма световых импульсов в α-диапазоне [31, 32]. Расширение диапазона усвоения ритма в сторону θ- или β-диапазонов и межполушарная асимметрия реакции усвоения ритма связываются с возникновением невротизации пациента, т.е. с повышением уровня его психоэмоциональной возбудимости, и считаются критериями патологии при оценке реакции фотостимуляции [34, 35].
Увеличение показателей реакции усвоения ритма частот θ-диапазона показано в реактивных паттернах ЭЭГ больных с нарушениями сердечного ритма в форме фибрилляции предсердий, и по мере нарастания проявлений этих нарушений от времени существования мерцательной аритмии, т.е. при переходе от пароксизмальной формы аритмии в постоянную, значение коэффициента усвоения ритма в θ-диапазоне десятикратно возрастает, в то время как в α-диапазоне это значение существенно уменьшается, что, вероятно, связано с преобладанием процессов торможения в нервной системе этих пациентов [36].
Отсутствие или незначительность реакции усвоения ритма в диапазоне θ- и β-частот на фоне слабого усвоения α-ритма у здорового человека отражает сбалансированность процессов возбуждения и торможения и преобладание внутренней синхронизации нейронных структур при навязывании внешнего ритма [37]. Повышение показателей реакции усвоения ритмов фотостимуляции связано, как правило, с повышением неустойчивости внутренней синхронизации нейронных ансамблей и усилением их внешней синхронизации [37–40].
Формирование и активация АСФС мозга приводят к уменьшению значений коэффициента усвоения, уменьшению скорости и увеличению времени возврата траектории ЭЭГ в окрестность точки, в которой она была ранее. Также после курса активаций АСФС наблюдается улучшение психофизиологического состояния пациента, что проявляется в положительных изменениях по данным психодиагностики, улучшении субъективного состояния больного и улучшении его объективного состояния (снижение выраженности, развернутости и частоты приступов панических атак).
ЗАКЛЮЧЕНИЕ
Анализ реактивных паттернов ЭЭГ, проведенный до и после немедикаментозного метода терапии, связанного с формированием и активацией артифициальных стабильных функциональных связей мозга, продемонстрировал возможность с помощью методов вейвлетного и рекуррентного анализов достоверно выявить улучшение функционального состояния головного мозга пациентов с паническими атаками.
Психологическое исследование с помощью методик СМИЛ, ИСАС, теста Тейлор, двойной и корректурной проб позволило подтвердить достоверное снижение ведущих симптомов в клинической картине болезни в исходном состоянии, а именно уменьшение общего усредненного показателя страха и снижение уровня суммарной тревоги.
Этические нормы. Все исследования проведены в соответствии с принципами биомедицинской этики, сформулированными в Хельсинкской декларации 1964 г. и ее последующих обновлениях, и одобрены локальным биоэтическим комитетом Института мозга человека им. Н.П. Бехтеревой (протокол КПЭ ИМЧ РАН от 18 апреля 2013 г.) (Санкт-Петербург).
Информированное согласие. Каждый участник исследования представил добровольное письменное информированное согласие, подписанное им после разъяснения ему потенциальных рисков и преимуществ, а также характера предстоящего исследования.
Финансирование работы. Работа выполнена при финансовой поддержке ПФНИ государственных академий на 2013–2020 гг. (ГП-14, раздел 64).
Благодарности. Авторы благодарны Н.А. Селиверстовой за помощь в обработке результатов психофизиологических данных.
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с публикацией данной статьи.
Список литературы
Cosci F. The psychological development of panic disorder: implications for neurobiology and treatment // Rev. Bras. Psiquiatr. 2012. V. 34. Suppl. 1. P. 9.
Wilson K.A., Hayward C. A prospective evaluation of agoraphobia and depression symptoms following panic attacks in a community sample of adolescents // J. Anxiety Disord. 2005. V. 19. № 1. P. 87.
Batelaan N.M., Van Balkom A.J., Stein D.J. Evidence -based pharmacotherapy of panic disorder // Int. J. Neuropsychopharmacology. 2012. V. 15. № 3. P. 403.
Na Hae-Ran, Kang Eun-Ho, Lee Jae-Hon, Yu Bum-Hee. The genetic basis of panic disorder // J. Korean Med. Sci. 2011. V. 26. № 6. P. 701.
Вейн А.М., Дюкова Г.М., Воробьева О.В., Данилов А.Б. Панические атаки (неврологические и психофизиологические аспекты). М.: Эйдос Медиа, 2004. 408 с.
Sullivan G.M., Coplan J.D., Kent J.M., Gorman J.M. The noradrenergic system in pathological anxiety: a focus on panic with relevance to generalized anxiety and phobias // Biol. Psychiatry. 1999. V. 46. № 9. P. 1205.
Yu S.T., Kim M.K., Kim B. et al. The Effects of 5-HTR1A Polymorphism on Cingulum Connectivity in Patients with Panic Disorder // Psychiatry Investig. 2013. V. 10. № 4. P. 399.
Goddard A.W., Mason G.F., Appel M. et al. Impaired GABA neuronal response to acute benzodiazepine administration in panic disorder // Am. J. Psychiatry. 2004. V. 161. № 12. P. 2186.
Westenberg H.G., Liebowitz M.R. Overview of panic and social anxiety disorders // J. Clin. Psychiatry. 2004. V. 65. Suppl. 14. P. 22.
Иванов С.В., Андреев А.М. Хронические тревожно-фобические расстройства с явлениями стойкой агорафобии (клинико-катамнестическое исследование) // Журн. неврологии и психиатрии им. С.С. Корсакова. 1999. № 9. С. 16.
Nutt D., Feeney A., Argyropolous S. Anxiety disorders comorbid with depression: panic disorder and agoraphobia. Martin Dunitz Ltd., 2002. 110 p.
Pasquini M., Berardelli I. Anxiety levels and related pharmacological drug treatment: a memorandum for the third millennium // Ann. Ist. Super Sanità. 2009. V. 45. № 2. P. 193.
Тукаев Р.Д. Психотерапия; теории, структуры и механизмы. М.: Медицинское информационное агентство, 2007. 392 с.
Milrod B., Busch F., Leon A.C. et al. A pilot open trial of brief psychodynamic psychotherapy for panic disorder // J. Psychother. Pract. Res. 2001. V. 10. P. 239.
Бирюкова Е.В. Применение нейрофидбека у резистентных к психофармакотерапии больных с тревожными расстройствами: автореф. дис. канд. мед. наук. М., 2011. 19 с.
Смирнов В.М., Резникова Т.Н. Артифициальные стабильные функциональные связи в механизмах интрацентральной регуляции мозга человека / Ассоциативные системы мозга. Л.: Наука, 1985. С. 274.
Смирнов В.М., Бородкин Ю.С. Артифициальные стабильные функциональные связи как способ формирования матриц долгосрочной памяти у человека (к теории долгосрочной памяти) // Физиология человека. 1975. Т. 1. № 3. С. 525.
Смирнов В.М., Бородкин Ю.С. Артифициальные стабильные функциональные связи. М.: Медицина, 1979. 192 с.
Смирнов В.М., Резникова Т.Н., Губачев Ю.М. Артифициальные стабильные функциональные связи и нейрорегуляторная коррекция психовегетативных расстройств // Физиология человека. 1987. Т. 13. № 5. С. 715.
Смирнов В.М., Резникова Т.Н. Артифициальные стабильные функциональные связи как метод исследования и лечения в условиях патологического состояния // Вестн. АМН СССР. 1985. № 9. С. 18.
Резникова Т.Н., Краснов А.А., Селиверстова Н.А., Терентьева И.Ю. Исследование “внутренней картины болезни” у больных с органической и функциональной патологией ЦНС в процессе лечебных активаций методом артифициальных стабильных функциональных связей мозга человека // Вестник Клинической психологии. 2004. Т. 2. № 1. С. 84.
Селиверстова Н.А. Особенности субъективных отношений личности у больных с органической и функциональной церебральной патологией. Дис. … канд. псих. наук. Санкт Петербург, 2005. 130 с.
Семиволос В.И. Изучение особенностей внутренней картины болезни у больных рассеянным склерозом. Дис. … канд. мед. наук. Санкт Петербург, 2009. 132 с.
Torrence C., Compo G.P. A practical guide to wavelet analysis // Bulletin of the American Meteorological Society. 1998. V. 79. P. 61.
Marwan N., Romano M.C., Thiel M. et al. Recurrence plots for the analysis of complex systems // Physics Reports. 2007. V. 438. № 5. P. 237.
Павлов А.Н., Храмов А.Е., Короновский А.А. и др. Вейлет-анализ в нейродинамике // Успехи физических наук. 2012. Т. 182. № 9. С. 905.
Божокин С.В. Вейвлет-анализ динамики усвоения и забывания ритмов фотостимуляции для нестационарной электроэнцефалограммы // Журн. Технической физики. 2010. Т. 80. № 9. С. 16.
Takens F. Detecting strange attractors in turbulence. Dynamical Systems and Turbulence, Lecture Notes in Mathematics // Eds. Rand D., Young L.S. Berlin: Springer-Verlag. 1981. V. 898. P. 366.
Fraser A.M., Swinney H.L. Independent coordinates for strange attractors from mutual information // Phys. Rev. 1986. V. 33. № 2. P. 1134.
Kennel M.B., Brown R., Abarbanel H.D. Determining embedding dimension for phase-space reconstruction using a geometrical construction // Phys. Rev. A. 1992. V. 45. № 6. P. 3403.
Гриндель О.М., Сазонова О.В. Введение в клиническую ЭЭГ / Нейрофизиологические исследования в клинике. М.: Антидор, 2001. С. 13.
Dick O.E. Wavelet analysis of the human brain lability to reproduce the external rhythm // J. Chaotic Modeling and Simulation. 2013. V. 3. P. 387.
Dick O.E., Svyatogor I.A. Wavelet and multifractal estimation of the intermittent photic stimulation response in the electroencephalogram of patients with dyscirculatory encephalopathy // Neurocomputing. 2015. V. 165. № 1. P. 361.
Святогор И.А., Дик О.Е., Ноздрачев А.Д., Гусева Н.Л. Анализ изменений ЭЭГ-паттернов в ответ на ритмическую фотостимуляцию при различных нарушениях функционального состояния ЦНС // Физиология человека. 2015. Т. 41. № 3. С. 41.
Fedotchev I., Bondar A.T., Akoev I.G. Dynamic characteristics of the human resonance EEG responses to rhythmic photostimulation // Human Physiology. 2000. V. 26. № 2. P. 64.
Русинов В.С., Гриндель О.М., Болдырева Г.Н., Вакар Е.М. Биопотенциалы мозга человека. Математический анализ. М.: Медицина, 1987. 254 с.
Дик О.Е., Святогор И.А., Ноздрачев А.Д., Гусева Н.Л. Анализ реактивных паттернов ЭЭГ у лиц с фибрилляцией предсердий // Физиология человека. 2019. Т. 45. № 1. С. 49.
Федотчев А.И., Бондарь А.Т., Акоев И.Г. Резонансные ЭЭГ-реакции при ритмических световых воздействиях разной интенсивности и частоты // Журн. ВНД. 2001. Т. 51. № 1. С. 17.
Поворинский А.Г., Заболотных В.А. Пособие по клинической энцефалографии. Л.: Наука, 1987. 64 с.
Федотчев А.И., Бондарь А.Т., Матрусов С.Г. и др. Использование сигналов обратной связи от эндогенных ритмов пациента для нелекарственной коррекции функциональных расстройств // Журн. Успехи физиол. наук. 2006. Т. 37. № 4. С. 82.
Дополнительные материалы отсутствуют.
Инструменты
Физиология человека