Физиология человека, 2020, T. 46, № 5, стр. 27-36
Стимуляция работы зрительной системы с помощью когнитивной задачи в условиях виртуальной среды у пациентов с шизофренией и депрессией
С. В. Муравьева 1, *, Г. А. Моисеенко 1, А. Н. Чомский 2, Е. А. Шарыбин 2, Ю. Д. Кропотов 2, Ю. Е. Шелепин 1
1 ФГБУН Институт физиологии имени И.П. Павлова РАН
Санкт-Петербург, Россия
2 ФГБУН Институт мозга человека имени Н.П. Бехтеревой РАН
Санкт-Петербург, Россия
* E-mail: muravsvetlana@mail.ru
Поступила в редакцию 09.04.2019
После доработки 10.12.2019
Принята к публикации 20.03.2020
Аннотация
В работе описаны данные исследований, в ходе которых оценивали результат воздействия курса визуальных стимуляций с когнитивной задачей в условиях интерактивной виртуальной среды на работу магно- и парво-систем у пациентов, страдающих шизофренией и депрессией. Для демонстрации изображений использовали монитор большого углового размера, который обеспечивал более полное погружение субъектов в виртуальную среду. Для оценки эффективности методики использовали анализ амплитуды компонентов когнитивных зрительных вызванных потенциалов (ЗВП) при демонстрации изображений, различающихся по физическим признакам (пространственно-частотный спектр) для выборочной активации низкочастотных (магно) и высокочастотных (парво) каналов и по своим семантическим признакам (объекты живой и неживой природы). Было показано, что у пациентов обеих групп наблюдается снижение амплитуды компонентов вызванных потенциалов на стимулы, отфильтрованные преимущественно по высоким пространственным частотам (парво-система). Были получены данные, что у пациентов с шизофренией наблюдаются нарушения обработки зрительной информации, как на ранних, так и на поздних этапах. У пациентов с депрессией затронуты только ранние этапы обработки. После курса воздействия интерактивных виртуальных сред с когнитивной задачей у пациентов с шизофренией наблюдается улучшение обработки зрительной информации, как на ранних, так и на поздних этапах. У пациентов с депрессией – на ранних этапах обработки. У пациентов обеих групп наблюдается достоверное увеличение амплитуды компонентов когнитивных зрительных потенциалов на высоких пространственных частотах (парво-система). Таким образом, результатом применения курса воздействия является выраженная активация парво-системы, именно той системы, которая в большей степени страдает у этих пациентов.
В последние годы все большее внимание уделяется изучению нейрофизиологических механизмов, лежащих в основе когнитивных нарушений у пациентов с психоневрологической патологией. Особое место среди них занимают рассеянный склероз, шизофрения и депрессия. Актуальность обусловлена тем, что этими патологиями в первую очередь страдают молодые трудоспособные люди. А прогрессирование часто ведет к потере трудоспособности. Известно, что для этих пациентов характерными особенностями являются нарушения обработки зрительной информации, играющей ключевую роль для адаптации человека в окружающей среде. В основе нарушений лежит дисфункция магно- и парво-каналов [1–8].
Магно-каналы образуют магно-систему. Она чувствительна к низким пространственным частотам и низким контрастам и способна давать быстрый ответ на временные изменения изображения. Ее функцией является анализ изображений черного и белого цвета, динамических изменений в изображении, локализация представляющих интерес объектов и обработка информации, необходимой для ориентации в пространстве (“пространственное зрение”). Парво-каналы образуют парво-систему. Она обеспечивает детальный анализ найденных фрагментов с высоким разрешением и чувствительна к высоким пространственным частотам и высоким контрастам. Ее функцией является анализ цвета (главным образом, красного, желтого и зеленого цветов), текстуры, и распознавание мелких предметов и их деталей (“объектное зрение”).
Для пациентов, у которых нарушена работа парво-системы, характерны жалобы на нарушение восприятия деталей формы, контура и размера объекта (контуры объектов и буквы воспринимаются размытыми), на быстрое цветовое утомление, на нарушение цветового зрения. Пациенты с нарушениями в работе магно-системы предъявляют жалобы на нарушение ориентации в пространстве, нарушение восприятия направления движения объекта, нарушения ощущения положения объекта в пространстве [1].
Для оценки состояния магно- и парво-систем и когнитивных нарушений у пациентов с психоневрологической патологией уже давно используют метод зрительных вызванных потенциалов (ЗВП) [1, 6, 8–11]. Поэтому этот метод и был использован в работе с пациентами с шизофренией и депрессией.
Методика, выбранная нами для коррекции нарушений у пациентов, основана на использовании виртуальной среды [8, 9]. Виртуальная среда – это мир, созданный с помощью цифровых технологий, в основе которых лежит, главным образом, синтез изображений. Часто встречается разделение на интерактивные и неинтерактивные виртуальные среды. Неинтерактивная среда – среда, включающая видеоряд изображений, созданный для демонстрации каких-либо явлений или процессов, в которой пользователь выступает только в качестве наблюдателя и не взаимодействует с ней. Интерактивная среда – среда, которая может обеспечить чувство присутствия в пространстве, отличном от того, в котором находится наблюдатель, и может позволить взаимодействовать с данным пространством [12]. Методика с виртуальной средой, используемая нами для работы с пациентами, включает постановку цели, что приводит к включению так называемого “активного восприятия”, т.к. критерием определения активности/пассивности является факт наличия конкретной цели восприятия [9, 13, 14]. “Процесс активного восприятия начинается с постановки цели, которая затем ведет к поиску путей ее достижения. В результате этого мозг в первую очередь обрабатывает те стимулы, которые соответствуют “поисковому запросу”” [9]. Исследования с помощью интерактивной виртуальной среды с когнитивной задачей были проведены на пациентах с шизофренией и депрессией. Предварительные данные были опубликованы в книгах конференций [15, 16].
МЕТОДИКА
В исследовании принимали участие 30 пациентов с параноидной формой шизофрении (F20 по МКБ – 10) с продолжительностью заболевания от 1 до 10 лет – 17 мужчин и 13 женщин и 14 пациентов с депрессией (F32; F33 по МКБ – 10) – 8 мужчин и 6 женщин в возрасте от 21 до 34 лет. Контрольную группу составили 30 здоровых испытуемых (16 мужчин и 14 женщин в возрасте от 18 до 30 лет). У всех наблюдателей острота зрения была не менее 0.9, рефракция соответствовала норме.
Среди симптомов, которые наблюдались у большинства пациентов с шизофренией, которые участвовали в исследовании, необходимо отметить эмоциональную однообразность, гипомимичность, напряженность и настороженность, тревожность. Среди типичных симптомов шизофрении в статусе всех пациентов отмечалась амбивалентность (двойственное, противоречивое отношение субъекта к объекту, характеризующееся одновременной направленностью на один и тот же объект противоположных импульсов, возникающих внезапно и независимо от обстоятельств), симптомы “соскальзывания”. Были характерны также бредовые идеи преследования, бредовые идеи воздействия, слуховые галлюцинации (голоса). Все пациенты, которые принимали участие в исследованиях, находились в стационаре и получали антипсихотическую терапию. Для пациентов было характерно доминирование продуктивных симптомов над негативными. Нарушения мышления и поведения не определяли клиническую картину обследованных пациентов.
Группу пациентов с депрессией составили случаи депрессивного эпизода и депрессивного эпизода в рамках рекуррентной формы депрессивного расстройства. В клинической картине абсолютного большинства пациентов, участвующих в исследовании, выявляли признаки витальной депрессии с разной степенью представленности проявлений меланхолии с беспричинным пессимизмом, унынием, подавленностью, а также, витальной тоской, которую пациенты ощущали, как “душевную (чаще – загрудинную, эпигастральную) боль”. Была характерна суточная ритмика аффекта в виде отчетливого ухудшения состояния в утренние часы с улучшением в вечерние. Многие пациенты жаловались на нарушение способности к логическому мышлению, установлению последовательных связей между событиями, усвоению элементарного смысла вещей. Все пациенты с депрессией получали терапию антидепрессантами различных групп и антипсихотическими препаратами.
Среди общих симптомов, характерных для пациентов двух групп можно отметить напряженность и тревожность, эмоциональную однообразность, гипомимичность. Характерны также нарушения со стороны работы головного мозга: нарушения структурирования мышления, снижение способности к концентрации внимания и сосредоточению.
В исследованиях мы использовали интерактивную виртуальную среду, имитирующую велопрогулку по ландшафтам с различным рельефом местности, программы которые были применены в работе, описаны в статье [9]. Для имитации езды на велосипеде использовали кардиотренажер, при этом видеоряд был синхронизирован с движением испытуемого. Видео ландшафтов представляло собой видеоряд натуральных сцен, обработанных программным путем и по своим пространственно-частотным характеристикам, близким к реальным. Виртуальную среду предъявляли на жидко-кристаллическом 2D-мониторе большого углового размера: 46.7 угл. град. В задачу наблюдателя входил не только внимательный просмотр изображений, предъявляемых на экране, но и выполнение когнитивных задачи: например, акцентирование внимания на отдельных элементах видео для того, чтобы производить поиск или счет объектов с заданными пространственно-частотными характеристиками, характерными для магно- или парво-системы в равном соотношении. Объекты различались по цветам (черные, белые или цветные), размеру, расположению, могли быть стационарными или находится в движении.
Таким образом, можно было стимулировать “объектное” и “пространственное зрение” как в равной степени, так и с акцентом на определенный тип зрения. Проводили 8–10 сеансов воздействия виртуальной средой в течение десяти дней. Продолжительность сеанса – 15 мин.
Эффективность методики и контроль воздействия оценивали с помощью электрофизиологического метода (когнитивные зрительные вызванные потенциалы), описанного ранее [8, 9, 17]. Использовали сравнительный анализ амплитуды компонентов вызванных потенциалов при восприятии изображений предметов, которые были отфильтрованы по пространственным частотам с помощью цифровой вейвлетной фильтрации для выборочного воздействия на – магно- (низкочастотные) и парво- (высокочастотные) каналы зрительной системы. Оценку производили два раза: до курса воздействия и после него. Пациенту на экране монитора предъявляли визуальные стимулы, представляющие собой изображения объектов живой и неживой природы (по 50% от общего числа изображений), т.е. отличающихся по семантическим признакам. Использовали набор из 90 монохромных контурных изображений в оттенках серого цвета (45 изображений живой природы, 45 – неживой природы). Из этого набора путем цифровой фильтрации получили 180 текстовых изображений, половина из которых содержала низкочастотную часть изображения (позволяющие стимулировать магно-систему), половина – высокочастотную (позволяющие стимулировать парво-систему). Эти стимулы представляли собой изображения, подвергнутые цифровой фильтрации таким образом, что половина из них содержала только низкочастотную часть спектра пространственных частот, а другая половина – высокочастотную. Для выделения высоких пространственных частот использовали фильтр с максимальным значением пропускания на частоте 10 цикл/град, низких частот – 1 цикл/град. Фильтрацию производили путем свертки изображений с DoG-функцией (сокр. от Difference Of Gaussians) – вейвлетом, представляющим собой разность двух двумерных функций Гаусса с различной полушириной.
Таким образом, визуальные стимулы подразделяли на четыре категории: “низкочастотные” изображения живых и неживых объектов, и “высокочастотные” изображения тех же объектов (рис. 1). Каждая из этих групп содержала по 45 изображений. Средняя яркость и контраст всех изображений были одинаковы. Изображения предъявляли в случайном порядке на 100 мс с интервалом в 1 с. В задачу наблюдателя входило как можно быстрее нажать на кнопку мыши: на левую, когда видит объект живой природы и на правую, когда объект неживой природы (различение объектов по семантическим признакам).
Рис. 1.
Примеры 2-х категорий черно-белых изображений – объектов неживой (А) и живой природы (Б), отфильтрованных с помощью вейвлетного преобразования в области низких (а, в) и высоких пространственных частот (б, г).

Для регистрации вызванных потенциалов использовали энцефалограф (“Мицар”, Россия) с частотой дискретизации 250 Гц и программу WinEEG. Регистрацию электроэнцефалограммы производили с помощью электроэнцефалографической шапочки (ElectroCap, International Inc., США) с 19-ю электродами, расположенными на поверхности головы в соответствии с международной системой 10–20 в отведениях: Fp1; Fp2; F7; F3; Fz; F4; F8; T3; C3; Cz; C4, T4; T5; P3; Pz; P4; T6; O1; O2. Референтные электроды располагали на мочках ушей, а заземляющий электрод – в лобной области.
Для обработки записи ЭЭГ использовали метод, описанный в [8, 9, 17]. Эпоха анализа продолжительностью в 700 мс была разделена на четыре временных интервала: 90–160, 160–250, 250–350, 350–500 мс. Для каждого отведения в каждом временном окне находили значения амплитуды, соответствующие пикам основных компонентов вызванного потенциала (максимум для позитивных волн и минимум для негативных волн). После этого проводили статистическое сравнение значений амплитуды компонентов, полученных в ответ на предъявление различных типов стимулов. Порог статистической достоверности результатов регистрации вызванных потенциалов рассчитывался с помощью критерия Вилкоксона и составил 5%, p < 0.05.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
На первичном этапе при сравнении результатов, полученных у пациентов с шизофренией и контрольной группы и пациентов с депрессией и контрольной группы до курса воздействия интерактивной виртуальной средой с когнитивной задачей, были выявлены следующие достоверные изменения.
У пациентов с шизофренией при предъявлении изображений, содержащих высокочастотную часть спектра, было зарегистрировано достоверное снижение амплитуды компонентов ЗВП – P100 (N100) и P250 (N250) в затылочной (в отведениях O1 и O2), центральной (в отведениях C3, Cz, C4), в передней (Fp1; Fp2) и задней лобной областях (в отведениях F3; Fz; F4). Наблюдается снижение амплитуды N170 – в затылочной (в отведениях O1 и O2) и височной областях (в отведениях T5; T6), P500 – в теменной (P3; Pz; P4), центральной (C3; Cz; C4) и лобной областях (Fp1; Fp2 и F3; Fz; F4) по сравнению со здоровыми испытуемыми. От содержания изображений (объекты живой или неживой природы) этот эффект не зависел. Усредненные вызванные потенциалы у контрольной группы и пациентов с шизофренией в различных отведениях показаны на рис. 2, А, В. При сравнении соотношения амплитуд компонентов наблюдаются следующие отличия данных пациентов c шизофренией от контрольной группы. У контрольной группы амплитуда компонента P170 в теменных, в центральном (Cz) и лобных отведениях достоверно не отличается, в центральных отведениях (C3, C4) – на высоких частотах выше, чем на низких. А у пациентов наблюдается обратная картина: амплитуда этого компонента достоверно выше на низких пространственных частотах, чем на высоких. У контрольной группы амплитуда компонента N250 (P250) в затылочных, центральных и лобных отведениях на стимулы высоких частот достоверно выше, чем низких, а у пациентов достоверно не отличается. У контрольной группы амплитуда компонента P500 в теменных, центральных и лобных отведениях на стимулы высоких частот достоверно выше, чем низких. А у пациентов с шизофренией такая картина наблюдается только в центральном теменном отведении (Pz). В остальных отведениях достоверно не отличается.
Рис. 2.
Усредненные вызванные потенциалы во время выполнения инструкции по различению семантических признаков в изображениях у контрольной группы, пациентов с депрессией и пациентов с шизофренией в различных отведениях: центральное лобное отведение (Fz), центральное отведение (Сz), усреднение по двум затылочным отведениям (O1 и О2). Сплошная и пунктирная линии черного цвета – вызванные потенциалы на стимулы изображений – объектов живой и неживой природы, отфильтрованные по высоким пространственным частотам. Сплошная и пунктирная линии серого цвета – вызванные потенциалы на стимулы изображений – объектов живой и неживой природы, отфильтрованные по низким пространственным частотам. А – усредненные вызванные потенциалы контрольной группы. Б – усредненные вызванные потенциалы пациентов с депрессией. В – усредненные вызванные потенциалы пациентов с шизофренией.
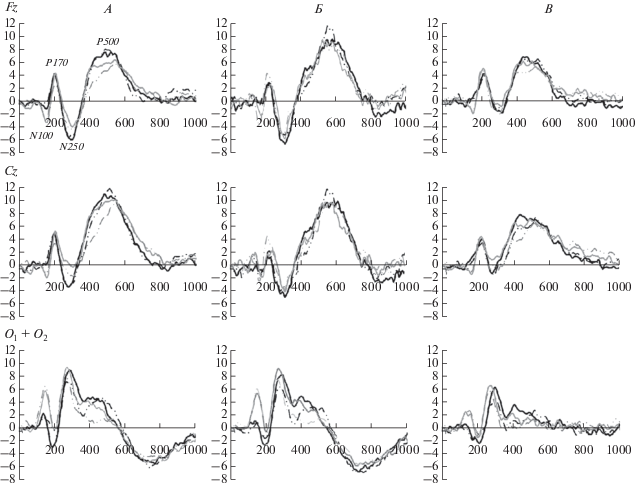
У пациентов с депрессией при предъявлении изображений, содержащих высокочастотную часть спектра, было зарегистрировано достоверное снижение амплитуды компонентов ЗВП. Амплитуда компонента P100 (N100) достоверно снижена в передней (Fp1; Fp2) и задней лобной областях (F7; F3; Fz; F4; F8), центральной (C3; Cz; C4) и теменной областях (P3; Pz; P4). От содержания изображений (объекты живой или неживой природы) этот эффект не зависел. Амплитуда компонента N170 (P170) достоверно снижена в лобной области (Fp1; Fp2) и (F7; F3; Fz; F4; F8), центральной (C3; Cz; C4) и теменной областях (P3; Pz; P4) при предъявлении изображений живой и неживой природы. Амплитуда компонента N250 достоверно снижена в передней и задней лобной, центральной и теменной областях только при предъявлении изображений живой природы. Усредненные вызванные потенциалы у контрольной группы и пациентов с депрессией в различных отведениях показаны на (рис. 2, А, Б). При сравнении соотношения амплитуд компонентов во всех вышеперечисленных областях наблюдаются следующие достоверные отличия данных пациентов с депрессией от контрольной группы. У контрольной группы амплитуда компонента P170 в теменных, лобных отведениях достоверно не отличается, в центральных отведениях – на высоких частотах выше, чем на низких. От содержания изображений (живые или неживые объекты) этот эффект не зависел. А у пациентов при предъявлении изображений неживой природы наблюдается обратная картина: амплитуда этого компонента достоверно выше на низких пространственных частотах, чем на высоких в теменных, центральных и лобных отведениях, при предъявлении изображений только живой природы в теменных отведениях. У контрольной группы амплитуда компонента N250 (P250) в затылочных, центральных и лобных отведениях на стимулы высоких частот достоверно выше, чем низких, а у пациентов – обратная картина. Соотношение амплитуд компонента P500 при предъявлении изображений высоких и низких пространственных частот у пациентов с депрессией соответствует данным контрольной группы во всех отведениях.
При анализе данных до и после курса стимуляции интерактивной виртуальной средой с когнитивной задачей были получены следующие достоверные отличия. У пациентов c шизофренией было зарегистрировано достоверное увеличение амплитуд компонентов N170 (P170) в затылочной (O1 и O2) и центральной областях (Сz), P250 (N250) в затылочной (O1 и O2) и центральной теменной (Pz) областях и P350–P500 в лобной (F3, Fz, F4), центральной (Сz, С3, С4) и теменной (P3, Pz, P4) областях при предъявлении изображений (объекты живой или неживой природы), отфильтрованных по высоким пространственным частотам. Наиболее выраженные изменения характерны для поздних компонентов P350–P500 (рис. 2, B).
У пациентов c депрессией наблюдается достоверное увеличение амплитуды компонентов: P100 в затылочно-височной (T5, T6), P170 (N170) в центральной теменной, центральной и центральной лобной областях (Pz, Сz и Fz), компонента P250 (N250) затылочно-височной (T5, T6), центральной (Сz) и лобной областях (F3, Fz, F4) в ответ на стимулы (объекты живой или неживой природы) высоких пространственных частот.
Таким образом, и у пациентов с шизофренией, и у пациентов с депрессией в указанных областях появляется достоверное отличие амплитуд компонентов ЗВП при предъявлении изображений (объекты живой или неживой природы), отфильтрованных по высоким пространственным частотам (рис. 3).
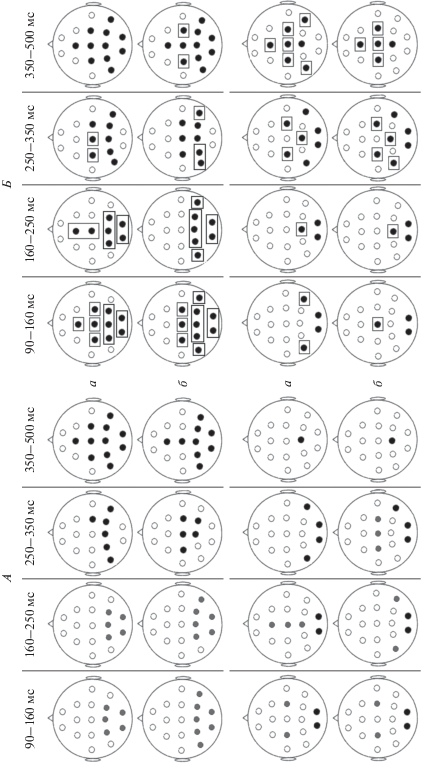
Рис. 3.
Сравнительный анализ амплитуды компонентов когнитивных ЗВП до воздействия виртуальной среды и после него. а – зависимость амплитуды от пространственной частоты изображений живых объектов, б – зависимость амплитуды от пространственной частоты изображений неживых объектов. Верхний ряд – данные пациентов с депрессией, нижний ряд – данные пациентов с шизофренией. А – до воздействия, Б – после воздействия. Серые кружки показывают области мозга, где были выявлены достоверные различия в амплитуде вызванных потенциалов, когда амплитуда в ответ на изображения низких пространственных частот выше амплитуды в ответ на изображения высоких пространственных частот. Черные кружки показывают области мозга, где были выявлены достоверные различия в амплитуде вызванных потенциалов, когда амплитуда в ответ на изображения высоких пространственных частот выше амплитуды в ответ на изображения низких пространственных частот. Прозрачные кружки показывают области мозга, где не было выявлено достоверных различий. Рамкой выделены области, которые активировались после стимуляции и стали соответствовать данным контрольной группы.
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Объем визуальной информации, поступающей непосредственно с рецепторов сетчатки глаза человека (1.2 × 108 палочек и 6.4 × 106 колбочек), очень велик. Чтобы сделать возможным обработку этой информации в реальном масштабе времени, в зрительной системе имеется ряд механизмов, позволяющих уменьшить этот объем. Анализ изображения разбивается на два этапа.
На первом этапе с помощью быстрых алгоритмов производится поиск участков изображения, которые могут содержать представляющие интерес объекты. Магно-система соответствует первому этапу анализа. Она чувствительна к низким пространственным частотам и способна давать быстрый ответ на временные изменения изображения. Ее функцией является анализ динамических изменений в изображении, локализация представляющих интерес объектов и обработка информации, необходимой для ориентации в пространстве Она обеспечивает “пространственное зрение”. На втором этапе производится детальный анализ найденных фрагментов с высоким разрешением, который осуществляет парво-система. Парво-система чувствительна к высоким пространственным частотам и обеспечивает “объектное зрение”. Ее функцией является анализ цвета (главным образом, красного, желтого и зеленого цветов), текстуры, и распознавание мелких предметов и их деталей (“объектное зрение”). Эволюционно магно-система развивалась раньше, т.к. она позволяла отличать, в первую очередь, подвижные объекты, которые могли представлять опасность для живого организма. Позже формировалась парво-система, обеспечивающая более сложные и тонкие механизмы обработки, которая позволяла детально анализировать поступающую зрительную информацию.
Большинство видов человеческой деятельности требует взаимодействия этих систем, и их функционирование часто бывает нарушено при различных патологических состояниях с нарушением адаптации. На начальных этапах развития болезни в первую очередь выходят из строя более сложные и тонкие механизмы, которые обеспечивает парво-система.
Уже много лет исследователи всего мира занимаются изучением нарушений работы зрительной системы при шизофрении. Позже были опубликованы работы, описывающие идентичные нарушения при депрессии.
Литературные данные о том, какая именно система: система магно- или парво-каналов, поражается при шизофрении, противоречивы. Большинство работ посвящено описанию нарушений работы магно-каналов [18–23], реже встречаются работы о нарушении работы парво-каналов [8, 24–26] или двух систем одновременно [26].
На основании полученных нами результатов о достоверном снижении амплитуды компонентов P100 (N100), P170 (N170), P250 (N250) в затылочной, центральной и лобной областях и P500 в затылочной, теменной, центральной и лобной областях при предъявлении изображений – объектов живой или неживой природы, отфильтрованных по высоким пространственным частотам, можно предположить, что у пациентов с параноидной формой шизофрении, продолжительностью заболевания о 1 года до 10 лет, наблюдается доминирующая дисфункция парво-каналов в зрительной системе как на ранних, так и на поздних этапах обработки зрительной информации.
Что касается депрессии, по литературным данным описание результатов применения ЗВП немногочисленны, чаще встречается описание применения слуховых вызванных потенциалов. Результаты электрофизиологических исследований при депрессивном расстройстве свидетельствуют о нарушениях обработки зрительной информации на ранних этапах. Так, в исследованиях при стимуляции изображениями эмоциональных лиц были получены данные изменений ранних компонентов ЗВП: N1, P1 и P2 в зависимости от эмоции лица по сравнению с данными контрольной группы [27, 28]. Интересной является работа, в которой авторы оценивали нейронную передачу и пластическую модуляцию в зрительном пути. Здесь использовалось сочетание метода ЗВП с высоким разрешением на шахматный паттерн и метод функциональной магниторезонансной томографии (фМРТ). Было показано снижение амплитуды (P1, N1) у пациентов с депрессией. Были выявлены генераторы электрической активности – вентральные экстракорпоральные корковые источники (парво-система) [29]. Авторы связывают эти компоненты в определенной степени с вниманием. Нейробиологические исследования показали, что при этом расстройстве наблюдаются нарушения работы парво-системы: затронуты CRF-содержащие парвоцеллюлярные нейроны паравентрикулярного ядра гипоталамуса (PVN), которые интегрируют информацию, относящуюся к стрессу [30].
В нашей работе у пациентов с депрессией были получены данные о достоверном снижении амплитуды компонентов P100 (N100) в теменной, центральной и лобной областях, P170 (N170) в теменной и центральной областях при предъявлении изображений (объекты живой или неживой природы), отфильтрованных по высоким пространственным частотам. Было получено снижение амплитуды P250 (N250) в теменной, центральной и лобной областях при предъявлении изображений – только объектов живой природы, отфильтрованных по высоким пространственным частотам. На основании полученных нами данных можно предположить, что у пациентов с депрессией наблюдается дисфункция парво-каналов в зрительной системе на ранних этапах обработки зрительной информации.
Таким образом, описанные в литературе данные при депрессии совпадают с полученными нами данными, относительно изменений в процессах ранней обработки зрительной информации, преимущественно парво-каналами.
Благодаря быстрому развитию компьютерных технологий появилась возможность применять методики с виртуальной реальностью в психотерапии пациентов с психоневрологической патологией. В настоящее время уже получены результаты, свидетельствующие об эффективности применения виртуальной реальности для лечения фобий, тревожности и депрессии.
В основе этих методик лежит так называемый поведенческий подход, согласно которому целенаправленная деятельность пациента является эффективным регулятором его эмоционального состояния. Целенаправленная деятельность или “рефлекс цели”, согласно представлениям И.П. Павлова, является ключевым в поведении человека, и ее тренировка происходит в течение всей жизни. Методика нейрореабилитации, разработанная нами, для стимуляции интерактивной виртуальной средой, включает постановку цели, что приводит к включению так называемого “активного восприятия”. Головной мозг вначале осуществляет поиск путей достижения поставленной цели, а затем выявляет только те стимулы, которые соответствуют “поисковому запросу”.
ЗАКЛЮЧЕНИЕ
При анализе результатов, после курса стимуляции интерактивной виртуальной средой с когнитивной задачей, были получены данные о влиянии курса на различные уровни обработки визуальных изображений у пациентов. Так, применение метода у пациентов с шизофренией улучшает как раннюю сенсорную обработку информации (первичное восприятие, первичную дифференциацию, принятие решений), так и позднюю обработку (глубокую обработку информации, перевод в кратковременную рабочую память). Это связано с тем, что у этих пациентов страдают как ранние, так и поздние этапы обработки зрительной информации. У пациентов с депрессией – улучшает обработку зрительной информации на ранних этапах. Это связано с тем, что у этих пациентов страдают ранние этапы обработки зрительной информации. И у пациентов с шизофренией, и у пациентов c депрессией было показано преимущественное улучшение обработки зрительной информации высокочастотных стимулов (объектное зрение), за обработку которых отвечает парво-система, которая, в первую очередь, страдает у этих пациентов.
По оценке врачей-психиатров, которые наблюдали пациентов, участвующих в выше описанном исследовании, при анализе клинических проявлений при сравнении результатов, полученных только на фоне медикаментозной терапии и терапии в сочетании с нейротехнологией с когнитивной задачей, наблюдалось более выраженное и быстрое уменьшение тревожности, патологической доминанты, улучшение структурированного мышления и эмоционального состояния пациентов.
Таким образом, комплексное воздействие интерактивной виртуальной средой с помощью видео пейзажей, которые предъявляются на экране большого углового размера в сочетании с когнитивной задачей, активируют работу магно- или парво-систем, в первую очередь парво-системы. Этот метод позволяет переключить пациента с целей, связанных с болезнью на цели, задаваемые для пациента. Вовлечение в физические нагрузки, связанные с достижением цели, обеспечивает улучшение кровообращения и всей деятельности организма и активизирует выброс в кровь биологически активных веществ.
Этические нормы. Все исследования проведены в соответствии с принципами биомедицинской этики, сформулированными в Хельсинкской декларации 1964 г. и ее последующих обновлениях, и одобрены локальным биоэтическим комитетом Института мозга человека имени Н.П. Бехтеревой РАН (Санкт-Петербург).
Информированное согласие. Каждый участник исследования представил добровольное письменное информированное согласие, подписанное им после разъяснения ему потенциальных рисков и преимуществ, а также характера предстоящего исследования.
Финансирование работы. Работа выполнена при финансовой поддержке ПФНИ государственных академий на 2013–2020 гг. (ГП-14, раздел 63).
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с публикацией данной статьи.
Список литературы
Муравьева С.В., Дешкович А.А., Шелепин Ю.Е. Магно и парво-системы человека и избирательные нарушения их работы // Рос. физиол. журн. им. И.М. Сеченова. 2008. Т. 94. № 6. С. 637.
Шошина И.И., Шелепин Ю.Е., Конкина С.А. и др. Исследование парвоцеллюлярных и магноцеллю-лярных зрительных каналов в норме и при психопатологии // Рос. физиол. журн. им. И.М. Сеченова. 2012. Т. 98. № 5. С. 657.
Шошина И.И., Шелепин Ю.Е. Контрастная чувствительность у больных шизофренией с разной длительностью заболевания // Рос. физиол. журн. им. И.М. Сеченова. 2013. Т. 99. № 8. С. 657.
Муравьева С.В., Фокин В.А., Ефимцев А.Ю., Шелепин Ю.Е. Пространственно-частотные каналы зрительной системы при рассеянном склерозе // Сенс. Сист. 2013. Т. 27. № 2. С. 130.
Муравьева С.В., Бисага Г.Н., Пронин С.В. и др. Влияние продолжительности заболевания на изменения зрительных вызванных потенциалов контрастной чувствительности у пациентов с рассеянным склерозом // Журн. высш. нервн. деятел. 2015. Т. 65. № 6. С. 711.
Муравьева С.В., Пронина М.В., Моисеенко Г.А. и др. Исследования влияния сенсомоторной нагрузки на зрительную систему пациентов с шизофренией на ранних стадиях заболевания / Материалы Всероссийского конгресса с международным участием. Современные концепции реабилитации в психоневрологии: отрицание отрицания. Санкт-Петербург, 9–11 июня 2016 г. 2016. С. 260.
Muravyova S., Moiseenko G., Pronina M. et al. Dysfunction of parvo-systems and its stimulation in patients with schizophrenia with early stage of the disease // Perception (39th European Conference on Visual Perception. Barselona). 2016. V. 45. P. 14.
Муравьева С.В., Пронина М.В., Моисеенко Г.А. и др. Исследование зрительных когнитивных вызванных потенциалов при шизофрении на ранних стадиях заболевания и их коррекция при помощи интерактивных виртуальных сред // Физиология человека. 2017. Т. 43. № 6. С. 24. Muraveva S.V., Moiseenko G.A., Pronin S.V. et al. Analysis of Visual Cognitive Impairments in Schizophrenia at the early Stages of the Disease and their Correction by Intractive Virtual Environment // Human Physiology. 2017. V. 43. № 6. P. 625.
Муравьёва С.В., Пронин С.В., Толстова Е.А., Шелепин Ю.Е. Особенности влияния экрана большого углового размера на оптимизацию целенаправленной деятельности наблюдателя в условиях интерактивной виртуальной среды // Оптический журнал. 2018. Т. 85. № 8. С. 54.
Кропотов Ю.Д., Пронина М.В, Поляков Ю.И, Пономарев В.А. Функциональные биомаркеры в диагностике психических заболеваний: когнитивные вызванные потенциалы // Физиология человека. 2013. Т. 39. № 1. С. 14. Kropotov J.D., Pronina M.V., Polyakov J.I., Ponomarev V.A. Functional biomarkers in the diagnostics of mental disorders: cognitive event-related potentials // Human Physiology. 2013. V. 39. № 1. P. 8.
Кропотов Ю.Д. Количественная ЭЭГ, когнитивные вызванные потенциалы мозга человека и нейтропенитрация / Учебник. Донецк: Издатель Заславский А.Ю., 2010. С. 512.
Schroeder R. Defining virtual worlds and virtual environments // J. Virtual Worlds Research. 2008. V. 1. № 1. P. 1.
Wexler M., Boxtel van. J. Depth perception by the active observer // Trends Cogn. Sci. 2005. V. 9. № 9. P. 431.
Freeman W.J. Comparison of brain models for active vs. passive perception // Information Sciences. 1999. V. 116. № 2–4. P. 97.
Муравьева С.В. Комплексное восстановление когнитивных функций у пациентов с тревожно-депрессивным синдромом и депрессией / Давиденковские чтения. XX Всероссийская научно-практическая конференция с международным участием. Санкт-Петербург, 27–28 сентября 2018 г. 2018. С. 274.
Муравьева С.В., Шелепин Ю.Е. Применение нейротехнологий с интерактивной виртуальной средой для коррекции когнитивных нарушений у пациентов с шизофренией и депрессией продолжительностью заболевания до 5 лет / Нейронаука для медицины и психологии. Международный Конгресс. Судак, 2018. С. 336.
Моисеенко Г.А., Шелепин Ю.Е., Хараузов А.К. и др. Классификация и распознавание изображений живой и неживой природы // Оптич. журн. 2015. Т. 82. № 10. С. 53.
Kim D., Park S. Visual perception deficits associated with the magnocellular pathway in schizophrenia // Korean. Schizophr. Res. 2011. V. 14. P. 61.
Leonard C.J., Luck S.J. The role of magnocellular signals in oculomotor attentional capture // J. Vision. 2011. V. 11. P. 1.
Rassovsky Y., Horan W.P., Lee J. et al. Pathways between early visual processing and functional outcome in schizophrenia // Psychol. Med. 2011. V. 41. № 3. P. 487.
Skottun B.C., Skoyles J.R. Visually evoked potentials, NMDA receptors and the magnocellular system in schizophrenia // Acta Neuropsychiatrica. 2012. V. 24. № 1. P. 50.
Lalor E.C., De Sanctis P., Krakowski M.I., Foxe J.J. Visual sensory processing deficits in schizophrenia: Is there anything to the magnocellular account? // Schizophr. Res. 2012. V. 139. № 1-3. P. 246.
Martinez A., Hillyard S.A., Bickel S. et al. Consequences of magnocellular dysfunction on processing attended information in schizophrenia // Cereb. Cortex. 2012. V. 22. № 6. P. 1282.
Ardekani B.A., Nierenberg J., Hoptman M.J. et al. MRI study of white matter diffusion anisotropy in schizophrenia // Neuroreport. 2003. V. 14. № 16. P. 2025.
Oribe N., Hirano Y., Kanba S. et al. Early and late stages of visual processing in individuals in prodromal state and first episode schizophrenia: An ERP study // Schizophr. Res. 2013. V. 146. № 1–3. P. 95.
Doniger G.M., Foxe J.J., Murray M.M. et al. Impaired visual object recognition and dorsal/ventral stream interaction in schizophrenia // Arch. Gen. Psychiatry. 2002. V. 59. № 11. P. 1011.
Dai Q., Feng Z., Koster E.H. Deficient distracter inhibition and enhanced facilitation for emotional stimuli in depression: An ERP study // International Journal of Psychophysiology. 2011. V. 79. № 2. P. 249.
Dai Q., Wei J., Shu X., Feng Z. Negativity bias for sad faces in depression: An event-related potential Study // Clinical Neurophysiology. 2016. V. 127. № 12. P. 3552.
Normann C., Schmitz D., Fürmaier A. et al. Long-Term Plasticity of Visually Evoked Potentials in Humans is Altered in Major Depression // Biol. Psychiatry. 2007. V. 62. № 5. P. 373.
Nestler E.J., Barrot M., DiLeone R.J. et al. Neurobiology of Depression // Neuron. 2002. V. 34. № 1. P. 13.
Дополнительные материалы отсутствуют.
Инструменты
Физиология человека


