Физиология человека, 2021, T. 47, № 6, стр. 79-87
Особенности функций систем внимания и самооценки состояния здоровья, связанные с возрастом и ишемической болезнью сердца
О. М. Разумникова 1, *, И. В. Тарасова 2, О. А. Трубникова 2
1 Новосибирский государственный технический университет
Новосибирск, Россия
2 ФГБНУ Научно-исследовательский институт
комплексных проблем сердечно-сосудистых заболеваний
Кемерово, Россия
* E-mail: razoum@mail.ru
Поступила в редакцию 03.09.2020
После доработки 28.10.2020
Принята к публикации 24.11.2020
Аннотация
Изучены особенности функций систем внимания (исполнительного контроля, бдительности и ориентационного внимания) и самооценки качества жизни при сравнении групп здоровых пожилых и молодых лиц, а также пациентов кардиологического центра. Установлено, что самооценка физического здоровья в группе здоровых пожилых была ниже, чем у молодых, но выше, чем у лиц с ишемической болезнью сердца, а психического здоровья – в двух последних группах ниже, чем в первой. Реорганизация систем внимания при ишемии головного мозга по сравнению со здоровыми лицами проявляется увеличением числа ошибок и времени селекции зрительно предъявленной информации, указывающим на ухудшение функций исполнительного контроля, меньшую бдительность и большее время реакции в системе ориентационного внимания, причем с самооценкой качества жизни в большей степени оказываются связаны функции системы бдительности, тогда как у здоровых пожилых – исполнительного контроля внимания.
Увеличение продолжительности жизни и доли людей преклонного возраста в популяции с сопутствующим повышением вероятности ухудшения состояния здоровья усиливает интерес к изучению механизмов старения. В качестве наиболее стабильно наблюдаемых изменений функций мозга в пожилом возрасте выделяют ухудшение кратковременной памяти, тормозных процессов и скорости реакции, что приводит к снижению эффективности селекции информации и гибкости мышления и поведения в целом [1]. Эти изменения способствуют развитию старческой деменции, риск которой возрастает вследствие сердечно-сосудистых заболеваний [2, 3]. Известно, что когнитивные расстройства у пациентов с сердечно-сосудистой патологией сопровождаются уменьшением мозгового кровотока [4, 5] и другими нарушениями цереброваскулярных функций и нейронной активности [6–9], которые могут усугубляться после операции коронарного шунтирования (КШ) [10, 11], снижая таким образом качество жизни прооперированных больных.
Дополнительное к возрастным изменениям деятельности мозга повреждающее влияние сердечно-сосудистой патологии вызывается атеросклеротическим ремоделированием мозговых сосудов с увеличением их жесткости и нарушением ауторегуляции мозговой перфузии, что приводит к ухудшению метаболических процессов в нейронах [6, 12–16], хотя имеются сведения и об отсутствии влияния интенсивности кровотока в средней мозговой артерии на показатели внимания и памяти [17].
Связанные с атеросклерозом ишемические процессы затрагивают, в первую очередь, фронтальные и париетальные области коры [18], однако возрастные и патологические изменения их активности различаются по своей природе [19]. Эти отделы мозга рассматриваются также как нейроанатомический субстрат организации систем внимания [20–22], причем нейронные системы передней части мозга, ответственные за торможение иррелевантной информации и выбор релевантной, нарушаются при старении в первую очередь [23–26]. Вместе с этим показано, что характеристики исполнительных функций являются лучшими предикторами качества жизни и степени развития старческой деменции [27–29]. Однако наряду с выводами о наиболее выраженных нарушениях в исполнительной системе внимания при относительной сохранности ориентационного внимания [30] имеются данные, указывающие на отсутствие возрастных различий в исполнительном контроле селекции информации [29]. Полагают, что причиной такого расхождения во мнениях может быть разная возрастная динамика изменений в отдельных субкомпонентах исполнительного контроля: процессах торможения, обновления и переключения информационных потоков [25] или его структуре [31]. Изучение возрастных особенностей показателей мозгового кровотока и внимания свидетельствует о взаимосвязи с разными формами внимания: негативной связи с селективным вниманием в группе молодых и с тонической бдительностью у пожилых [32]. В ходе выполненного недавно обзора литературы, представляющего результаты исследований систем внимания, также сделаны выводы о разных паттернах снижения их функций: бдительности при нормальном старении и исполнительного внимания на ранних фазах болезни Альцгеймера [33].
Методики субъективной оценки состояния здоровья широко используются как показатели эффективности лечения и реабилитационных мероприятий, в том числе после кардиохирургических вмешательств [34–37]. Целью настоящего исследования стало выяснение особенностей реорганизации функций систем внимания (исполнительного контроля, бдительности и ориентационного внимания) и самооценки качества жизни у здоровых пожилых и молодых лиц и у пациентов кардиологического центра. Решение этого вопроса с практической точки зрения важно для разработки нейрореабилитационных технологий восстановления когнитивных функций в постоперационный период кардиохирургических вмешательств или персонализированного когнитивного тренинга пожилых или молодых лиц.
МЕТОДИКА
В исследовании принимали участие три группы: здоровые лица молодого возраста (n = 67, средний возраст 18.8 ± 0.5 лет) (ГР1), здоровые лица пожилого возраста (n = 67, средний возраст 64.1 ± 0.6 года) (ГР2) и пациенты со стабильной ишемической болезнью сердца (ИБС), госпитализированные в Научно-исследовательский институт комплексных проблем (г. Кемерово) сердечно-сосудистых заболеваний для выполнения планового коронарного шунтирования (КШ) (n = 62, средний возраст 56.7 ± 5.5 лет) (ГР3). ГР1 была представлена студентами очного отделения Факультета гуманитарного образования, а ГР2 – пенсионерами, посещающими лекции и практические занятия Народного факультета Новосибирского государственного технического университета. Клинико-анамнестические характеристики ГР3 представлены в табл. 1.
Таблица 1.
Клинико-анамнестические показатели пациентов с ишемической болезнью сердца (ИБС) – ГР3
| Показатель | n = 62 |
|---|---|
| Длительность анамнеза ИБС, M ± σ, лет | 5.35 ± 2.50 |
| ФК по NYHA, n (%) | |
| II | 52 (84) |
| III | 10 (16) |
| Стенокардии ФК, n (%) | |
| I–II | 40 (64) |
| III | 22 (36) |
| Фракция выброса левого желудочка, M ± σ, % | 56.8 ± 9.32 |
| Поражение коронарных артерий по шкале SYNTAX, M ± σ, балл | 23.7 ± 8.63 |
| Стенозы внутренней сонной артерии <50%, n (%) | 22 (36) |
| Сахарный диабет, n (%) | 16 (26) |
Для анализа состояния исполнительной системы внимания часто используют задания с предъявлением конфликтующей или “неконгруэнтной” информации. Применение методики ANT (attention network test) позволяет определить эффективность деятельности не только исполнительной, но и ориентационной системы внимания и бдительности [38]. Целевым стимулом согласно этой методике является центральная стрелка, направление которой требуется определить в разных условиях селекции сигнала: при конгруэнтном (все пять стрелок направлены в одну сторону) или неконгруэнтном (центральная стрелка направлена в сторону, противоположную остальным) предъявлении и с предупреждающим появление целевого стимула центральным или двойным пространственно разнесенным намеком. Время предъявления всех 96 стимулов варьировало в пределах 400–1600 мс, предупреждающий намек (расположенный в центре экрана или там, где будет показан стимул) появлялся за 100 мс до целевого стимула. Регистрировали время реакции и количество ошибок для всех вариантов предъявления стимула с использованием специально разработанного программного обеспечения. На основе полученных данных вычисляли показатели функций трех систем внимания: исполнительной системы (ВРисп), бдительности (ВРбд) и ориентационного внимания (ВРор). Подробнее методика была описана ранее в работах [39, 40].
Для самооценки качества жизни использовали опросник SF-36, включающий 8 шкал: физическое функционирование (ФФ), ролевое функционирование (РФ), ощущение боли (ОБ), общее здоровье (ОЗ), жизнеспособность (ЖС), социальное функционирование (СФ), эмоциональное состояние (ЭС) и психическое здоровье (ПЗ); первые четыре шкалы представляли интегральный показатель физического здоровья (СОЗфиз), а четыре следующие – психического (СОЗпс) [41, 42]. Согласно стандартному способу оценки 100% отражали максимальный уровень показателя, 0% – минимальный.
Для статистической обработки данных использовали методы дисперсионного, факторного и кластерного анализа с применением пакета программ STATISTICA13 ru.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Анализ показателей самооценки здоровья. Дисперсионный анализ ANOVA выполняли для трех групп участников исследования и двух зависимых переменных СОЗфиз и СОЗпс или 8 зависимых переменных: показателей шкал SF-36. Был обнаружен значимый эффект фактора ГРУППА (F(2,193) = 17.51; p < 0.00001; η2 = 0.15), обусловленный меньшими значениями самооценки состояния здоровья в ГР3 по сравнению с ГР2 или ГР1 (52.6 ± 1.8; 66.5 ± 1.8 и 65.7 ± 1.8, соответственно), а также его взаимодействие с показателями восьми шкал SF-36 (F(14,1351) = 22.73; p < < 0.00001; η2 = 0.19) и интегральных показателей СОЗфиз и СОЗпс (F(2,193) = 31.56; p < 0.00001, η2 = 0.25). На рис. 1 показаны соотношения СОЗфиз и СОЗпс для трех исследованных групп, а на рис. 2 – всех шкал SF-36.
Рис. 1.
Показатели самооценки физического (С-ОЗфиз) и психического здоровья (СОЗпс) в исследованных группах. ГР1 – здоровые молодые, ГР2 – здоровые пожилые, ГР3 – пациенты с ишемической болезнью сердца (ИБС).
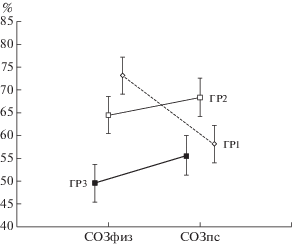
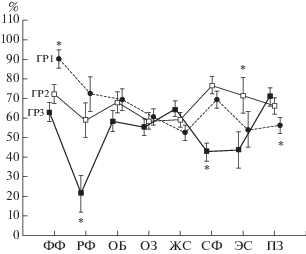
Рис. 2.
Профиль шкал SF-36 в трех исследованных группах. ФФ – физическое функционирование, РФ – ролевое функционирование, ОБ – ощущение боли, ОЗ – общее здоровье, ЖС – жизнеспособность, СФ – социальное функционирование, ЭС – эмоциональное состояние, ПЗ – психическое здоровье. Остальные обозначения см. рис. 1.
Согласно рost-hoc анализу обнаруженных эффектов ГР3 характеризовалась достоверно более низким показателем СОЗфиз по сравнению с ГР2 или ГР1 (р < 0.00002 с поправкой Бонферрони), а СОЗпс – только по сравнению с ГР2 (р < 0.0004). Следует также отметить большие значения физического, чем психического здоровья в ГР1 (р < < 0.000001) при тенденции к обратному соотношению этих компонентов в ГР2 и ГР3 (рис. 1).
Максимально низкий уровень в ГР3 отмечен для шкал “ролевое функционирование”, “социальное функционирование” и “эмоциональное состояние” (рис. 2). По первым двум шкалам ГР3 достоверно отличалась от ГР2 или ГР1 (р < < 0.0001), а по ЭС – только с ГР2. ГР1 характеризовалась значительно более высоким по сравнению с другими группами уровнем шкалы “физическое здоровье, но низким – “психическое здоровье” (р < 0.0001).
Обнаруженные возрастные различия в соотношении СОЗфиз и СОЗпс соответствуют ранее полученному такому же эффекту с привлечением других групп испытуемых [43] и при сравнении этих интегральных компонентов оценки качества жизни пациентов кардиологических клиник в Нидерландах [44, 45]. Следовательно, состояние психического здоровья можно рассматривать как устойчивый резерв поддержания сравнительно высокого качества жизни в пожилом возрасте, в том числе и при наличии сердечно-сосудистой патологии. Особенно низкие в ГР3 значения по шкалам РФ и СФ отражают возникшие в связи с заболеванием физические ограничения не только в профессиональной и повседневной деятельности, но и в социальной коммуникации. Примечательно, что наиболее существенное снижение РФ и относительная сохранность ПЗ являются устойчивой характеристикой самооценки качества жизни у пациентов разных кардиологических клиник, и применение методики SF-36 рассматривается как информативный способ определения степени улучшения состояния здоровья после операции КШ [44, 46–49].
Факторный анализ показателей самооценки состояния здоровья с использованием вращения нормализованный варимакс выполняли отдельно для каждой из трех групп. В ГР1 переменные сформировали два фактора, а в двух других – три фактора, представляющих, соответственно, 58, 67 и 73% дисперсии показателей SF-36 (табл. 2).
Таблица 2.
Факторная структура показателей самооценки состояния здоровья в группах здоровых молодых (ГР1), здоровых пожилых (ГР2) и пациентов с ИБС (ГР3)
| Шкалы SF-36 |
ГР1 | ГР2 | ГР3 | |||||
|---|---|---|---|---|---|---|---|---|
| Ф1_ПЗ | Ф2_ФЗ | Ф1_ПЗ | Ф2_ФЗ + ПЗ | Ф3_ФЗ | Ф1 | Ф2 | Ф3 | |
| ФФ | –0.030 | 0.565 | –0.035 | 0.246 | 0.765 | 0.604 | –0.567 | 0.179 |
| РФ | 0.503 | 0.508 | –0.042 | 0.804 | 0.137 | 0.013 | –0.132 | 0.872 |
| ОБ | 0.162 | 0.793 | 0.225 | 0.608 | 0.397 | 0.471 | –0.527 | 0.464 |
| ОЗ | 0.145 | 0.706 | 0.353 | 0.030 | 0.750 | 0.848 | –0.036 | 0.005 |
| ЖС | 0.673 | 0.416 | 0.679 | 0.039 | 0.442 | 0.648 | 0.106 | 0.603 |
| СФ | 0.797 | 0.005 | 0.486 | 0.678 | –0.006 | 0.151 | 0.797 | 0.087 |
| ЭС | 0.769 | –0.065 | 0.662 | 0.488 | 0.051 | 0.218 | 0.069 | 0.813 |
| ПЗ | 0.835 | 0.337 | 0.873 | 0.088 | 0.096 | 0.641 | 0.327 | 0.437 |
| Expl. Var | 2.678 | 1.995 | 2.076 | 1.785 | 1.531 | 2.205 | 1.376 | 2.230 |
| Prp. Totl | 0.335 | 0.249 | 0.259 | 0.223 | 0.191 | 0.276 | 0.172 | 0.279 |
Примечание: ФФ – физическое функционирование, РФ – ролевое функционирование, ОБ – ощущение боли, ОЗ – общее здоровье, ЖС – жизнеспособность, СФ – социальное функционирование, ЭС – эмоциональное состояние, ПЗ – психическое здоровье; жирным шрифтом выделены максимальные нагрузки в факторах Ф1–Ф3 (ФЗ – представляющих шкалы физического здоровья, ПЗ – психического).
Как видно из табл. 2, показатели SF-36 в ГР1 объединяются в два фактора, отражающих шкалы психического и физического здоровья (Ф1_ПЗ и Ф2_ФЗ), тогда как в ГР2 наряду с этими факторами (Ф1_ПЗ и Ф3_ФЗ) выделяется еще один фактор, в котором имеются нагрузки как шкал РФ и ОБ (компонентов физического здоровья), так и СФ (компонента психического здоровья). В ГР3 все выделенные факторы составлены из показателей, отражающих и физическое, и психическое состояние, причем в Ф2 показатели СФ, ФФ и ОБ имеют разный знак.
Можно предположить, что объединение шкал самооценки физического и психического здоровья в каждом из трех факторов, выделенных в ГР3, отражает эффект “дедифференциации”, который был предложен для объяснения возрастной реорганизации когнитивных функций и регионарной активности нейронных систем мозга [50–53]. Причем, этот эффект, как показывает сравнение факторной структуры показателей SF-36 в трех группах, появляется в группе пожилых и усиливается в группе пациентов, указывая на возрастающую роль психологического компонента в самооценке состояния здоровья.
Анализ показателей систем внимания также выполняли с фактором ГРУППА (3), в качестве зависимых переменных рассматривали ошибки (ОШ) или показатели времени реакции в системах внимания: исполнительной, бдительности и ориентационного внимания (ВРисп, ВРбд и ВРор, соответственно). Обнаружен достоверный эффект фактора ГРУППА для ОШ (F(2, 200) = 4.37; р = = 0.014; η2 = 0.04), обусловленный большим числом ошибок в ГР3 по сравнению с ГР1 или ГР2 (табл. 3, р = 0.06 при сравнении с ГР2 и р = 0.004 при сравнении с ГР1). Достоверные эффекты также получены для ВРисп (F(2, 200) = 5.62; р = 0.004; η2 = 0.05) и ВРор (F(2, 200) = 11.52; р = 0.00002; η2 = 0.10), и на уровне тенденции для ВРбд (F(2, 200) = 2.27; р = 0,11; η2 = 0.02). Результаты рost-hoc анализа этих эффектов представлены в табл. 3. Они указывают, что ГР3 характеризуется большим ВРисп по сравнению с ГР1 (различия между ГР2 и ГР3 также достоверны, р = 0.016); меньшим ВРбд по сравнению с ГР2; и большим ВРор по сравнению с двумя другими группами. ВРор в ГР2 было значимо меньше, чем в ГР1, р = = 0.01.
Таблица 3.
Показатели функций систем внимания в группах здоровых молодых (ГР1), здоровых пожилых (ГР2) и пациентов с ИБС (ГР3)
| Переменная | ГР1 | ГР2 | ГР3 |
|---|---|---|---|
| Ошибки (ОШ) | 1.1 ± 0.2** | 1.4 ± 0.2 | 2.0 ± 0.2 |
| ВРисп | 85.8 ± 5.7** | 104.8 ± 5.3 | 111.7 ± 5.7 |
| ВРбд | 25.5 ± 4.8 | 29.2 ± 4.6* | 15.4 ± 4.8 |
| ВРор | 24.0 ± 5.3* | 5.4 ± 5.0** | 40.0 ± 5.3 |
Примечание: ВРисп – время реакции исполнительной системы внимания, ВРбд – бдительности, ВРор – ориентационного внимания; остальные обозначения см. табл. 2; * – p < < 0.05; ** – p < 0.01 при сравнении ГР3 с группами ГР2 и ГР1.
Связанное с ишемией мозга снижение эффективности селекции информации и памяти как в дооперационный период, так и после КШ показано во многих исследованиях [40, 54–56]. Поэтому основное внимание уделяется возможностям послеоперационного восстановления когнитивных функций вследствие тренировки и активации когнитивных резервов мозга. Наблюдаемые в этом направлении положительные результаты [55, 57, 58] однако существенно различаются в зависимости от используемых методик и, соответственно, психометрических показателей когнитивных процессов, групп сравнения, а также затраченного времени тренировки и фиксации параметров.
Обнаруженные нами изменения в функциях трех систем внимания для ГР3 указывают на их реорганизацию, обусловленную не только фактором возраста (применительно к исполнительной системе внимания), но и возникшей вследствие сердечно-сосудистого заболевания ишемии головного мозга (повышение времени ориентационного внимания и снижение бдительности). Так как система ориентационного внимания имеет корковое представительство в париетальных отделах коры, а бдительности – в правом полушарии [21, 22], то следует заключить, что обнаруженные изменения селективных процессов отражают нарушения цереброваскулярных функций и нейронной активности, преимущественно в задней части правого полушария. В пользу такой гипотезы свидетельствует положительная связь показателя системы бдительности и правополушарной мощности θ-ритма [40], который рассматривается как коррелят поддерживающего внимания и исследования пространства [59, 60].
Факторный анализ показателей внимания, выполненный для каждой группы, выявил для каждой из них по два фактора, описывающих 55–61% дисперсии переменных, однако состав этих факторов, максимальную нагрузку в которых имели показатели исполнительной системы внимания или бдительности, был разным (табл. 4).
Таблица 4.
Факторная структура показателей внимания в группах пациентов с ИБС (ГР3), здоровых пожилых (ГР2) и здоровых молодых (ГР1)
| Переменная | ГР3 | ГР2 | ГР1 | |||
|---|---|---|---|---|---|---|
| Ф1_исп | Ф2_бд | Ф1_бд | Ф2_исп | Ф1_бд | Ф2_исп | |
| Ошибки | 0.681 | –0.202 | –0.654 | 0.099 | 0.103 | 0.470 |
| ВРисп | 0.771 | 0.149 | –0.308 | 0.829 | –0.182 | 0.806 |
| ВРбд | 0.176 | 0.787 | 0.715 | –0.026 | 0.751 | 0.371 |
| ВРор | 0.221 | –0.625 | 0.548 | 0.637 | 0.747 | –0.321 |
| Expl. Var | 1.139 | 1.073 | 1.334 | 1.103 | 1.165 | 1.111 |
| Prp. Totl | 0.285 | 0.268 | 0.333 | 0.276 | 0.291 | 0.278 |
Примечание: обозначения см. табл. 2 и 3.
В ГР3 в первом факторе наряду с ВРисп максимальную нагрузку имел показатель ОШ, а второй был представлен ВРбд и ВРор, причем с разным знаком. В ГР2 показатели ОШ и ВРбд составили первый фактор, а ВРисп и ВРор – второй; а в ГР1, соответственно, ВРбд и ВРор – первый и ВРисп – второй.
Согласно выделенной факторной структуре показателей селекции экспериментальных стимулов повышение ВРбд, которое в ГР3 оказывается низким по сравнению с другими группами, не обеспечивает уменьшение ошибок селекции, как это наблюдается в ГР2 (табл. 4, Ф1_бд в ГР2). Более того, увеличение времени на принятие решения (ВРисп) не приводит к снижению ОШ (табл. 4, Ф1_исп в ГР3), что указывает на низкую эффективность функций исполнительного контроля внимания при ишемии мозга.
Для выяснения особенностей соотношения функций систем внимания и самооценки состояния здоровья в группах был выполнен иерархический кластерный анализ с предварительной стандартизацией рассматриваемых переменных, использованием метода полной связи и евклидовой метрики. Учитывая тесную связь интегральных показателей физического и психического здоровья в каждой группе (0.47 < r < 0.58 при p < 0.0001), в качестве общего информативного показателя было взято их соотношение: Кфиз/пси. Полученные результаты кластеризации для каждой группы представлены на рис. 3.
Рис. 3.
Дендрограммы для показателей самооценки здоровья и функций систем внимания в группах пациентов с ишемической болезнью сердца (ИБС) (ГР3), здоровых пожилых (ГР2) и здоровых молодых (ГР1). Кфиз/пси – отношение интегрального показателя физического здоровья к психическому, ОШ – количество ошибок при тестировании систем внимания, ВРисп – время реакции исполнительной системы внимания, ВРор – ориентационной системы, ВРбд – бдительности.
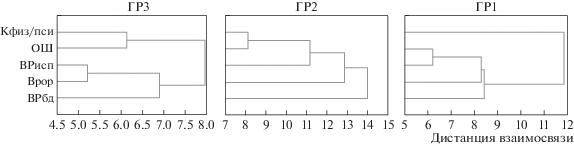
Согласно выделенному в каждой группе составу кластеров ГР3 отличается наиболее тесной связью Кфиз/пси с ВРбд, а ГР2 – с ОШ, тогда как в ГР1 ОШ и ВРисп формируют один кластер, который далее объединяется с показателями других систем внимания, и только на последнем шаге Кфиз/пси связанo с общим кластером разных функций внимания.
Следовательно, согласно полученным данным показатель функции системы бдительности оказывается наиболее тесно связанным соотношением самооценки физического и психического здоровья при ишемической болезни сердца. Этот вывод согласуется с данными о более выраженной связи мозгового кровотока и бдительности у пожилых лиц [16], которая, по-видимому, становится доминирующей при кардиологической патологии.
ЗАКЛЮЧЕНИЕ
Ухудшение самооценки состояния физического здоровья у пациентов с ИБС по сравнению с группами не только молодых, но и здоровых пожилых людей сопровождается тесной связью его показателей с состоянием психического здоровья. Реорганизация систем внимания, обусловленная ишемией головного мозга у пациентов-кандидатов на кардиохирургическое вмешательство, проявляется большим числом ошибок и временем селекции зрительно предъявленной информации, указывающим на ухудшение функций исполнительного контроля, меньшую бдительность и большee время реакции в системе ориентационного внимания, причем функции системы бдительности оказываются в большей степени связаны с самооценкой качества жизни. В молодом возрасте при самооценке здоровья выделяются факторы психического и физического здоровья, а в пожилом – происходит их “дедифференциация” с повышением интегрального компонента психического здоровья по сравнению с физическим, что сопровождается связью функций исполнительной системы внимания и соотношения этих компонентов самооценки здоровья.
Этические нормы. Все исследования проведены в соответствии с принципами биомедицинской этики, сформулированными в Хельсинкской декларации 1964 г. и ее последующих обновлениях, и одобрены локальными биоэтическими комитетами НИИ комплексных проблем сердечно-сосудистых заболеваний (Кемерово) и Новосибирского государственного технического университета (Новосибирск).
Информированное согласие. Каждый участник исследования представил добровольное письменное информированное согласие, подписанное после разъяснения ему характера предстоящего исследования.
Финансирование работы. Исследование выполнено при поддержке РФФИ (проект № 19-29-01017).
Благодарности. Авторы выражают благодарность Р.М. Суслову за разработку программного обеспечения методики для определения функций систем внимания (А.с. 2012617379 от 16.08.2012).
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с публикацией данной статьи.
Список литературы
Разумникова О.М. Закономерности старения мозга и способы активации его компенсаторных ресурсов // Успехи физиол. наук. 2015. Т. 46. № 2. С. 3.
Gorelick P.B., Counts S.E., Nyenhuis D. Vascular cognitive impairment and dementia // Biochim. Biophys. Acta. 2016. V. 1862. № 5. P. 860.
Iadecola C., Duering M., Hachinski V. et al. Vascular cognitive impairment and dementia: JACC Scientific Expert Panel // J. Am. Coll. Cardiol. 2019. V. 73. № 25. P. 3326.
Samieri C., Perier M.C., Gaye B. et al. Association of cardiovascular health level in older age with cognitive decline and incident dementia // JAMA. 2018. V. 320. № 7. P. 657.
SepehriShamloo A., Dagres N., Müssigbrodt A. et al. Atrial fibrillation and cognitive impairment: New insights and future directions // Heart Lung Circ. 2020. V. 29. № 1. P. 69.
Catchlove S.J., Macpherson H., Hughes M.E. et al. An investigation of cerebral oxygen utilization, blood flow and cognition in healthy aging // PLoS One. 2018. V. 13. № 5. P. e0197055.
Singer J., Trollor J.N., Baune B.T. et al. Arterial stiffness, the brain and cognition: a systematic review // Ageing Res. Rev. 2014. V. 15. P. 16.
Wendell C.R., Waldstein S.R., Ferrucci L. et al. Carotid atherosclerosis and prospective risk of dementia // Stroke. 2012. V. 43. № 12. P. 3319.
Xu X., Wang B., Ren C. et al. Age-related impairment of vascular structure and functions // Aging Dis. 2017. V. 8. № 5. P. 590.
Тарасова И.В., Трубникова О.А., Барбараш О.Л., Барбараш Л.С. Изменения биоэлектрической активности мозга, ассоциированные со стойкой послеоперационной когнитивной дисфункцией у пациентов, перенесших коронарное шунтирование // Сибирский научный медицинский журн. 2017. Т. 37. № 3. С. 32.
Tarasova I.V., Trubnikova O.A., Barbarash O.L. EEG and clinical factors associated with mild cognitive impairment in coronary artery disease patients // Dement. Geriatr. Cogn. Disord. 2018. V. 46. № 5–6. P. 275.
Семенютин В.Б., Асатурян Г.А., Никифорова А.А. Критические стенозы внутренних сонных артерий: церебральная ауторегуляция в ипсилатеральном бассейне // Журн. неврологии и психиатрии им. C.C. Корсакова. 2017. Т. 117. № 8. С. 76.
De la Torre J.C. Cerebral hemodynamics and vascular risk factors: setting the stage for Alzheimer’s disease // J. Alzheimers. Dis. 2012. V. 32. № 3. P. 553.
De la Torre J.C. Are major dementias triggered by poor blood flow to the brain? Theoretical considerations // J. Alzheimers Dis. 2017. V. 57. № 2. P. 353.
Highton D., Ghosh A., Tachtsidis I. et al. Monitoring cerebral autoregulation after brain injury: multimodal assessment of cerebral slow-wave oscillations using near-infrared spectroscopy // Anesth. Analg. 2015. V. 121. № 1. P. 198.
Toth P., Tarantini S., Csiszar A., Ungvari Z. Functional vascular contributions to cognitive impairment and dementia: mechanisms and consequences of cerebral autoregulatory dysfunction, endothelial impairment, and neurovascular uncoupling in aging // Am. J. Physiol. Heart Circ. Physiol. 2017. V. 312. № 1. P. H1.
Smith P.J., Browndyke J.N., Monge Z.A. et al. Longitudinal changes in regional cerebral perfusion and cognition after cardiac operation // Ann. Thorac. Surg. 2019. V. 107. № 1. P. 112.
Wählin A., Nyberg L. At the heart of cognitive functioning in aging // Trends. Cogn. Sci. 2019. V. 23. № 9. P. 717.
McAleese K.E., Walker L., Graham S. et al. Parietal white matter lesions in Alzheimer’s disease are associated with cortical neurodegenerative pathology, but not with small vessel disease // Acta Neuropathol. 2017. V. 134. № 3. P. 459.
Banich M.T., Milham M.P., Atchley R.A. et al. Prefrontal regions play a predominant role in imposing an attentional ‘set’: Evidence from fMRI // Brain. Res. Cogn. Brain. Res. 2000. V. 10. № 1–2. P. 1.
Petersen S.E., Posner M.I. The attention system of the human brain: 20 years after // Annu. Rev. Neurosci. 2012. V. 35. P. 73.
Posner M.I., Petersen S.E. The attention system of the human brain // Annu. Rev. Neurosci. 1990. V. 13. P. 25.
Gamboz N., Zamarian S., Cavallero C. Age-related differences in the attention network test (ANT) // Exp. Aging Res. 2010. V. 36. № 3. P. 287.
Luks T.L., Oliveira M., Possin K.L. et al. Atrophy in two attention networks is associated with performance on a Flanker task in neurodegenerative disease // Neuropsychologia. 2010. V. 48. № 1. P. 165.
Maldonado T., Orr J.M., Goen J.R.M., Bernard J.A. Age differences in the subcomponents of executive functioning // J. Gerontol. B. Psychol. Sci. Soc. Sci. 2020. V. 75. № 6. P. e31.
Williams R.S., Biel A.L., Wegier P. et al. Age differences in the Attention Network Test: Evidence from behavior and event related potentials // Brain Cogn. 2016. V. 102. P. 65.
Cahn-Weiner D.A., Farias S.T., Julian L. et al. Cognitive and neuroimaging predictors of instrumental activities of daily living // J. Int. Neuropsychol. Soc. 2007. V. 13. № 5. P. 747.
Clark L.R., Schiehser D.M., Weissberger G.H. et al. Specific measures of executive function predict cognitive decline in older adults // J. Int. Neuropsychological Society. 2012. V. 18. № 1. P. 118.
Davis J.C., Marra C.A., Najafzadeh M., Liu-Ambrose T. The independent contribution of executive functions to health related quality of life in older women // BMC Geriatr. 2010. V. 10. P. 16.
Zhou S., Fan J., Lee T.M.C. et al. Age-related differences in attentional networks of alerting and executive control in young, middle-aged, and older Chinese adults // Brain Cogn. 2011. V. 75. № 2. P. 205.
Bock O., Haeger M., Voelcker-Rehage C. Structure of executive functions in young and in older persons // PLoS ONE. 2019. V. 14. № 5. P. e0216149.
Bertsch K., Hagemann D., Hermes M. et al. Resting cerebral blood flow, attention, and aging // Brain Res. 2009. V. 1267. P. 77.
McDonough I.M., Wood M.M., Miller W.S., Jr. A review on the trajectory of attentional mechanisms in aging and the Alzheimer’s disease continuum through the Attention Network Test // Yale J. Biol. Med. 2019. V. 92. № 1. P. 37.
Базылев В.В., Гальцева Н.В. Результаты ранней физической реабилитации пациентов, перенесших аортокоронарное шунтирование // Клиницист. 2017. Т. 11. № 3–4. С. 34.
Никонов С.Ф., Олофинская И.Е., Багиян Л.С. Исследование качества жизни у пожилых больных после операции на сердце // Качественная клиническая практика. 2003. № 1. С. 56.
Hokkanen M., Järvinen O., Huhtala H., Tarkka M.R. A 12-year follow-up on the changes in health-related quality of life after coronary artery bypass graft surgery // Eur. J. Cardiothorac. Surg. 2014. V. 45. № 2. P. 329.
Jokinen J.J., Hippeläinen M.J., Turpeinen A.K. et al. Health-related quality of life after coronary artery bypass grafting: a review of randomized controlled trials // J. Card. Surg. 2010. V. 25. № 3. P. 309.
Fan J., McCandliss B.D., Sommer T. et al. Testing the efficiency and independence of attentional networks // J. Cogn. Neurosci. 2002. V. 14. № 3. P. 340.
Разумникова О.М., Вольф Н.В. Реорганизация связи интеллекта с характеристиками внимания и памяти при старении // Журн. высш. нерв. деят. 2017. Т. 67. № 1. С. 55.
Тарасова И.В., Вольф Н.В., Барбараш О.Л. Взаимосвязь между функционированием сети внимания и спонтанной ЭЭГ-активностью у пациентов с ишемической болезнью сердца // Сибирский научный медицинский журн. 2019. T. 39. № 2. С. 62.
Новик А.А., Ионова Т.И. Руководство по исследованию качества жизни в медицине. М.: ЗАО ОЛМА Медиа Групп, 2007. 320 с.
Ware J.E., Kosinski M.A., Gandek B.G. SF36 Health Survey: Manual and Interpretation Guide. 1993. 316 p.
Разумникова О.М., Прохорова Л.В., Яшанина А.А. Возрастные особенности взаимосвязи интеллекта и самооценки качества жизни // Успехи геронтол. 2016. Т. 29. № 2. С. 353.
Blokzijl F., Houterman S., van Straten B.H.M. et al. Quality of life after coronary bypass: a multicentre study of routinely collected health data in the Netherlands // Eur. J. Cardiothorac. Surg. 2019. V. 56. № 3. P. 526.
Verwijmeren L., Noordzij P.G., Daeter E.J. et al. Preoperative determinants of quality of life a year after coronary artery bypass grafting: a historical cohort study // J. Cardiothorac. Surg. 2018. V. 13. № 1. P. 118.
Baig K., Harling L., Papanikitas J. et al. Does coronary artery bypass grafting improve quality of life in elderly patients? // Interact. Cardiovasc. Thorac. Surg. 2013. V. 17. № 3. P. 542.
Kiebzak G.M., Pierson L.M., Campbell M., Cook J.W. Use of the SF36 general health status survey to document health-related quality of life in patients with coronary artery disease: Effect of disease and response to coronary artery bypass graft surgery // Heart Lung. 2002. V. 31. № 3. P. 207.
Lindsay G., Hanlon P., Smith L.N., Wheatley D.J. Assessment of changes in general health status using the short-form 36 questionnaire 1 year following coronary artery bypass grafting // Eur. J. Cardiothorac. Surg. 2000. V. 18. № 5. P. 557.
Pačarić S., Turk T., Erić I. et al. Assessment of the Quality of Life in patients before and after Coronary Artery Bypass Grafting (CABG): A prospective study // Int. J. Environ. Res. Public. Health. 2020. V. 17. № 4. P. 1417.
Goh J.O. Functional dedifferentiation and altered connectivity in older adults: Neural accounts of cognitive aging // Aging Dis. 2011. V. 2. № 1. P. 30.
Hertzog C., Bleckley M.K. Age differences in the structure of intelligence. Influences of information processing speed // Intelligence. 2001. V. 29. № 3. P. 191.
Koen J.D., Srokova S., Rugg M.D. Age-related neural dedifferentiation and cognition // Curr. Opin. Behav. Sci. 2020. V. 32. P. 7.
St-Laurent M., Abdi H., Bondad A., Buchsbaum B.R. Memory reactivation in healthy aging: evidence of stimulus-specific dedifferentiation // J. Neurosci. 2014. V. 34. № 12. P. 4175.
Трубникова О.А., Каган Е.С., Куприянова Т.В. и др. Нейропсихологический статус пациентов со стабильной ишемической болезнью сердца и факторы, на него влияющие // Комплексные проблемы сердечно-сосудистых заболеваний. 2017. Т. 6. № 1. С. 112.
Ajtahed S.S., Rezapour T., Etemadi S. et al. Efficacy of neurocognitive rehabilitation after coronary artery bypass graft surgery in improving Quality of Life: An interventional trial // Front. Psychol. 2019. V. 10. P. 1759.
Szwed K., Pawliszak W., Anisimowicz L. et al. Short-term outcome of attention and executive functions from aorta no-touch and traditional off-pump coronary artery bypass surgery // World J. Biol. Psychiatry. 2014. V. 15. № 5. P. 397.
De Tournay-Jetté E., Dupuis G., Denault A. et al. The benefits of cognitive training after a coronary artery bypass graft surgery // J. Behav. Med. 2012. V. 35. № 5. P. 557.
Eryomina O.V., Petrova M.M., Prokopenko S.V. et al. The effectiveness of the correction of cognitive impairment using computer-based stimulation programs for patients with coronary heart disease after coronary bypass surgery // J. Neurol. Sci. 2015. V. 358. № 1–2. P. 188.
Oken B.S., Salinsky M. Alertness and attention: basic science and electrophysiologic correlates // J. Clin. Neurophysiol. 1992. V. 9. № 4. P. 480.
Senoussi M., Moreland J.C., Busch N.A., Dugué L. Attention explores space periodically at the theta frequency // J. Vis. 2019. V. 19. № 5. P. 22.
Дополнительные материалы отсутствуют.
Инструменты
Физиология человека


