Физиология человека, 2022, T. 48, № 1, стр. 115-123
Влияние гипоксии на устойчивость показателей микроциркуляции височных областей головы человека
Л. В. Мезенцева 1, *, Е. Н. Дудник 2, Е. В. Никенина 1
1 ФГБНУ Научно-исследовательский институт нормальной физиологии
имени П.К. Анохина
Москва, Россия
2 ФГАОУ ВО Первый Московский государственный медицинский университет
имени И.М. Сеченова МЗ РФ (Сеченовский университет)
Москва, Россия
* E-mail: l.v.mezentseva@mail.ru
Поступила в редакцию 11.12.2020
После доработки 02.03.2021
Принята к публикации 30.04.2021
- EDN: VYYJBL
- DOI: 10.31857/S0131164622010106
Аннотация
Предложена новая расчетно-экспериментальная методика оценки устойчивости колебательных процессов, протекающих в системе микроциркуляции (МЦР). Методика основана на анализе устойчивости системы дифференциальных уравнений, описывающих флуктуации показателей МЦР крови симметричных височных областей головы человека. С помощью этой методики исследовали изменение показателей устойчивости МЦР симметричных височных областей головы в условиях гипоксии. В исследовании принимали участие 10 здоровых добровольцев мужского пола (возраст 18–19 лет). Состояние кратковременной гипоксии вызывали с использованием сертифицированной в РФ нормобарической установки для получения гипоксических и гипероксических газовых смесей на основе биообратной связи ReOxy Cardio (S.A. Aimediq, Люксембург) со встроенным пульсоксиметрическим датчиком (Mаsimo Rad-5, США). Синхронные измерения показателей МЦР симметричных височных областей головы в исходном состоянии и сразу после кратковременного гипоксического воздействия проводились методом лазерной допплеровской флоуметрии (ЛДФ) с помощью двухканального прибора “ЛАКК-02” НПП “ЛАЗМА” (Россия). Показано, что кратковременные гипоксические воздействия изменяют числовые значения параметров устойчивости у всех испытуемых, не выводя их за пределы границ зон устойчивости. Однако реакция на гипоксические воздействия отличалась большой индивидуальностью у разных испытуемых. Предложенная методика позволяет выполнять персонализированные оценки степени тренированности и устойчивости к гипоксическим воздействиям у различных групп испытуемых.
В настоящее время накоплен большой экспериментальный материал, содержащий эмпирические сведения о количественных характеристиках показателей перфузии и компонентов сосудистого тонуса различных органов и тканей человека и животных [1–6]. В результате этих исследований обнаружена специфичность регуляции микрокровотока парных органов, обусловленная наличием функциональной асимметрии [1, 2]. Показано наличие достоверных корреляционных взаимосвязей между показателями микроциркуляции (МЦР) симметричных сторон наблюдения как в покое [1], так и в условиях внешних воздействий [2]. Однако имеющиеся эмпирические данные об изучаемых процессах не позволяют понять системные регуляторные механизмы, лежащие в основе этих явлений. Для этого в распоряжении исследователя должна быть математическая модель изучаемого явления, а не набор разрозненных экспериментальных данных. Настоящая работа носит экспериментально-расчетный характер и направлена на математический анализ флуктуаций показателей МЦР симметричных областей головы у человека.
Цель работы – формулировка математической модели, позволяющей оценивать устойчивость системы МЦР в условиях внешних воздействий. В качестве внешнего воздействия были использованы кратковременные гипоксические нагрузки.
МЕТОДИКА
Синхронные измерения показателей МЦР у 10 здоровых добровольцев мужского пола (возраст 18–19 лет) определяли методом лазерной допплеровской флоуметрии (ЛДФ). Исследования проводили с помощью двухканального прибора “ЛАКК-02” НПП “ЛАЗМА” (Россия). Датчики ЛДФ-сигнала фиксировали на наружной поверхности симметричных височных областей головы, расположенных на 1 см латеральнее волосяного покрова. Кратковременное гипоксическое воздействие осуществляли по методике гипоксического теста на установке ReOxy Cardio (S.A. Aimediq, Люксембург) со встроенным пульсоксиметрическим датчиком (Mаsimo Rad-5, США). На лице обследуемого фиксировали плотноприлегающую ротоносовую маску, палец помещали в пульсоксиметрический датчик и предлагали спокойно дышать через маску в течение до 10 мин. Тест производили в покое, в положении сидя, на протяжении всего теста мониторировали величину насыщения артериальной крови кислородом (SpO2) и частоту сердечных сокращений (ЧСС, уд./мин), при этом автоматически фиксировались индивидуальные значения минимального уровня SpO2 и максимальной ЧСС. Концентрация кислорода во вдыхаемом воздухе составляла 11%. Во время гипоксического теста проводили измерение времени снижения SpO2 с исходного уровня (96–99%) до 80% (время десатурации, в секундах). Критериями прекращения “гипоксической фазы” теста служили снижение значения SpO2 до 80% и ниже, либо истечение 9 мин дыхания гипоксической газовой смесью. Отсчет времени производился встроенным в прибор электронным секундомером автоматически. Дополнительным критерием прекращения гипоксической фазы теста являлась выраженная тахикардия (устойчивое повышение значений ЧСС на 30% и выше от исходного уровня). Записи показателей МЦР у каждого испытуемого проводили в исходном состоянии до тестирования на гипоксию и сразу после гипоксического воздействия. Записи ЛДФ-сигнала проводили с частотой 20 Гц в течение 3 мин с интервалом отсчетов ∆t[i] = 0.05 с, что насчитывало более 3000 точек соответствующей периодограммы. Для последующего анализа в периодограмме выделяли 30 фрагментов по 100 точек в каждом фрагменте. Далее методом множественного регрессионного анализа изучали взаимосвязи между исходными значениями перфузии {x1[i] = ПМлев[i]} и {x2[i] = ПМпр[i]} и их изменениями {∆x1[i]} и {∆x2[i]}, i = 1, 2……100 слева и справа. С этой целью для каждого испытуемого рассчитывали параметры a0, a1, a2, b0, b1, b2 регрессионных уравнений:
(1)
$\left\{ \begin{gathered} \Delta x1 = a0 + a1x1 + a2x2 \hfill \\ \Delta x2 = b0 + b1x1 + b2x2. \hfill \\ \end{gathered} \right.$Значимость результатов регрессионного анализа оценивали стандартными статистическими методами. С этой целью рассчитывали стандартные значения ошибок для регрессионных коэффициентов (sa0, sa1, sa2, sb0, sb1, sb2), а также осуществляли оценку достоверности уравнений регрессии с помощью F-критерия Фишера. Полученная регрессионная модель была положена в основу математической модели, сформулированной в виде системы линейных дифференциальных уравнений:
(2)
$\left\{ \begin{gathered} {{dx1} \mathord{\left/ {\vphantom {{dx1} {dt}}} \right. \kern-0em} {dt}} = a0 + a1x1 + a2x2 \hfill \\ {{dx2} \mathord{\left/ {\vphantom {{dx2} {dt}}} \right. \kern-0em} {dt}} = b0 + b1x1 + b2x2. \hfill \\ \end{gathered} \right.$Дальнейшие исследования решений этой системы и их устойчивости проводили с использованием известных математических методов [7]. Расчеты проводили в условных (перфузионных) единицах с помощью программного обеспечения, входящего в пакеты прикладных программ Statistica и Excel for Windows (v. 6.0).
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Математическая модель. Первым этапом исследований явился расчет числовых значений коэффициентов уравнений множественной регрессии (1). Расчеты проводились в исходном состоянии и после гипоксических воздействий. Результаты регрессионного анализа подтвердили значимость регрессионных коэффициентов и адекватность выбранной регрессионной модели. Расчетные числовые значения регрессионных коэффициентов представлены в табл. 1. Закономерности изменения показателей МЦР, описываемые системой регрессионных уравнений (1), дают основание полагать, что при малых изменениях {∆x1[i]} и {∆x2[i]} (а это действительно было, поскольку интервал отсчета периодограммы ∆t[i] = 0.05 с) систему регрессионных уравнений (1) можно заменить на аналогичную систему дифференциальных уравнений (2). Эта система дифференциальных уравнений нами была положена в основу математической модели. Известно [7], что решение системы дифференциальных уравнений 1-го порядка с постоянными коэффициентами может быть получено путем сведения этой системы к одному линейному дифференциальному уравнению более высокого порядка. Поэтому путем несложных алгебраических преобразований система (2) была сведена к одному дифференциальному уравнению 2-го порядка:
(3)
$\begin{gathered} {{{{d}^{2}}x2} \mathord{\left/ {\vphantom {{{{d}^{2}}x2} {d{{t}^{2}}}}} \right. \kern-0em} {d{{t}^{2}}}} = (b2 + a1){{dx2} \mathord{\left/ {\vphantom {{dx2} {dt}}} \right. \kern-0em} {dt}} + \\ + \,\,(b1a2 - a1b2)x2 + (b1a0 - a1b0), \\ \end{gathered} $(6)
$T2 = {{(b2 + a1)} \mathord{\left/ {\vphantom {{(b2 + a1)} {(b1a2 - a1b2),}}} \right. \kern-0em} {(b1a2 - a1b2),}}$(7)
$K = {{(b1a0 - a1b0)} \mathord{\left/ {\vphantom {{(b1a0 - a1b0)} {(a1b2 - b1a2).}}} \right. \kern-0em} {(a1b2 - b1a2).}}$Таблица 1.
Числовые значения коэффициентов (a1, a2, b1, b2) регрессионной модели (1) для всех тестируемых испытуемых
| № исп | а1 | а2 | b1 | b2 | ||||
|---|---|---|---|---|---|---|---|---|
| исх | гипокс | исх | гипокс | исх | гипокс | исх | гипокс | |
| 1 | –0.31 ± 0.06 | –0.13 ± 0.04^ | 0.34 ± 0.05* | 0.11 ± 0.05*, ^ | 0.23 ± 0.04* | 0.21 ± 0.04* | –0.47 ± 0.06 | –0.39 ± 0.05 |
| 2 | –0.35 ± 0.05 | –0.43 ± 0.05 | 0.24 ± 0.03* | 0.10 ± 0.03*, ^ | 0.08 ± 0.03* | –0.16 ± 0.04* | –0.27 ± 0.05 | –0.14 ± 0.03^ |
| 3 | –0.36 ± 0.05 | –0.18 ± 0.03^ | –0.11 ± 0.03* | 0.26 ± 0.03*, ^ | 0.13 ± 0.03* | –0.04 ± 0.03^ | –0.29 ± 0.05 | –0.17 ± 0.03^ |
| 4 | –0.37 ± 0.06 | –0.48 ± 0.06^ | –0.05 ± 0.04 | 0.26 ± 0.04 | 0.07 ± 0.04 | –0.01 ± 0.05*, ^ | –0.40 ± 0.06 | –0.36 ± 0.03 |
| 5 | –0.32 ± 0.03 | –0.20 ± 0.03^ | 0.03 ± 0.04 | –0.32 ± 0.04*, ^ | –0.04 ± 0.04 | 0.05 ± 0.03 | –0.32 ± 0.05 | –0.30 ± 0.05 |
| 6 | –0.40 ± 0.06 | –0.13 ± 0.03^ | 0.05 ± 0.03 | 0.03 ± 0.03 | 0.47 ± 0.05* | 0.04 ± 0.03^ | –0.62 ± 0.05 | –0.35 ± 0.05^ |
| 7 | –0.24 ± 0.04 | –0.40 ± 0.04^ | –0.08 ± 0.02* | 0.24 ± 0.05*, ^ | –0.07 ± 0.03* | –0.03 ± 0.03 | –0.24 ± 0.05 | –0.19 ± 0.03 |
| 8 | –0.23 ± 0.05 | –0.05 ± 0.03^ | 0.10 ± 0.03* | –0.19 ± 0.03* | –0.13 ± 0.03* | 0.23 ± 0.05* | –0.09 ± 0.03 | –0.38 ± 0.06^ |
| 9 | –0.28 ± 0.05 | –0.13 ± 0.03 | 0.11 ± 0.03* | –0.07 ± 0.03* | 0.03 ± 0.03 | 0.03 ± 0.03 | –0.28 ± 0.05 | –0.33 ± 0.05 |
| 10 | –0.15 ± 0.02 | –0.32 ± 0.05^ | –0.05 ± 0.02* | 0.11 ± 0.02*, ^ | 0.24 ± 0.05* | 0.05 ± 0.03^ | –0.39 ± 0.06 | –0.30 ± 0.06 |
Решение уравнения (4), имеет вид:
(8)
$x2(t) = K + {\text{exp(}}\alpha t{\text{)[}}C1{\text{cos}}\beta t + C2{\text{sin}}\beta t{\text{]}},$(9)
${{\lambda }_{{1,2}}} = [ - T2 \pm {{\surd (T{{2}^{2}} - 4T1)]} \mathord{\left/ {\vphantom {{\surd (T{{2}^{2}} - 4T1)]} {2T1}}} \right. \kern-0em} {2T1}}$(11)
$x1(t) = {{\left( {{{dx2} \mathord{\left/ {\vphantom {{dx2} {dt}}} \right. \kern-0em} {dt}} - b0 - b2x2} \right)} \mathord{\left/ {\vphantom {{\left( {{{dx2} \mathord{\left/ {\vphantom {{dx2} {dt}}} \right. \kern-0em} {dt}} - b0 - b2x2} \right)} {b1.}}} \right. \kern-0em} {b1.}}$Устойчивость процессов кровообращения в микроциркуляторном русле. Одним из важных вопросов, возникающих при исследовании физиологических систем, является изучение механизмов обеспечения устойчивости их функционирования. Результаты настоящего исследования свидетельствуют о том, что функционирование системы МЦР в симметричных височных областях головы человека подчиняется строгим математическим закономерностям, описываемым системой линейных дифференциальных уравнений (2). Поэтому исследование условий устойчивости этой системы может быть выполнено стандартными математическими методами. Согласно критерию Гурвица [7], исследование на устойчивость системы линейных дифференциальных уравнений n-го порядка сводится к нахождению условий отрицательности действительных частей соответствующего характеристического уравнения. Применительно к нашему случаю, все корни характеристического уравнения (10) будут отрицательные и система дифференциальных уравнений (2) будет иметь устойчивые решения в том случае, если:
(13)
$T1 = {1 \mathord{\left/ {\vphantom {1 {(a1b2 - b1a2)}}} \right. \kern-0em} {(a1b2 - b1a2)}} > 0,$(14)
$T2 = {{ - \,(b2 + a1)} \mathord{\left/ {\vphantom {{ - \,(b2 + a1)} {(a1b2 - b1a2)}}} \right. \kern-0em} {(a1b2 - b1a2)}} > 0,$Влияние гипоксии на устойчивость процессов кровообращения в микроциркуляторном русле. Результаты исследований показали, что гипоксические воздействия вызывают изменения показателей МЦР как правой, так и левой стороны наблюдения, причем эти изменения отличаются ярко выраженной лево-правосторонней асимметрией и большой индивидуальностью у разных испытуемых. У 80% испытуемых гипоксические воздействия приводили к увеличению показателей перфузии слева (ПМлев); у оставшихся 20% – к уменьшению. В то же время показатели перфузии справа (ПМпр) у 50% испытуемых возрастали под влиянием гипоксии, и у 50% уменьшались.
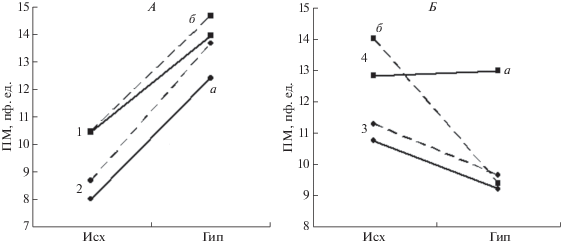
На рис. 1 приведены примеры различных типов реакции показателей перфузии на кратковременное гипоксическое воздействие. У испытуемых на рис. 1, А было одновременное возрастание ПМлев и ПМпр под влиянием кратковременной гипоксии, а на рис. 1, Б – у одного испытуемого наблюдалось одновременное снижение ПМлев и ПМпр, у другого – ПМпр резко снижалась, а ПМлев незначительно возрастала. Таким образом, реакция на кратковременное гипоксическое воздействие отличалась значительной индивидуальностью у разных испытуемых, причем важно отметить, что снижение показателей перфузии под влиянием кратковременного гипоксического воздействия было у курильщиков. Усреднение по всем испытуемым не позволяет выявить индивидуальные особенности реакции каждого из испытуемых. Среднее исходное значение перфузии слева было ПМлев(исх) = 9.44 ± 0.54 пф. ед., а после гипоксии ПМлев(гип) = 10.55 ± 0.60; исходное среднее значение перфузии справа было ПМпр(исх) = 9.91 ± 0.75 пф. ед., а после воздействия гипоксии ПМпр(гип) = 10.67 ± 0.69, достоверных изменений не выявлено.
Рис. 1.
Влияние кратковременного гипоксического воздействия на показатели перфузии левой (ПМлев) и правой (ПМпр) височных областей головы у разных испытуемых. А – испытуемые 1 и 2 с возрастанием ПМлев и ПМпр после гипоксии. Б – у исп. 3 ПМлев и ПМпр после гипоксии снижаются, у исп. 4 ПМпр резко снижается, а ПМлев незначительно возрастает. а – изменение ПМлев, б – изменение ПМпр.
Следующим этапом исследований явилось изучение количественных закономерностей флуктуаций показателей МЦР методом множественного регрессионного анализа путем оценки коэффициентов a0, a1, a2, b0, b1, b2 регрессионной модели (1). Результаты расчетов представлены в табл. 1. Из табл. 1 можно видеть, что расчетные значения коэффициентов регрессии a2 у большинства испытуемых достоверно отличаются от 0 (p < 0.05). Это свидетельствует о том, что изменения перфузии слева (∆x1 = ∆ПМлев) зависят не только от исходных значений этого показателя слева (х1 = ПМлев), но и от величины этого показателя справа (х2 = ПМправ). Аналогично для правой стороны наблюдения: расчетные значения коэффициентов регрессии b1 у большинства испытуемых достоверно отличаются от 0 (p < 0.05). Это свидетельствует о том, что изменения перфузии справа (∆x2 = ∆ПМправ) зависят не только от исходных значений этого показателя справа (х2 = = ПМправ), но также и от величины этого показателя слева (х1 = ПМлев). Таким образом, результаты регрессионного анализа свидетельствуют о том, что изменения амплитуд флуктуаций микрокровотока симметричных височных областей головы зависят от исходных значений этих показателей не только одноименной, но и противоположной стороны наблюдения.
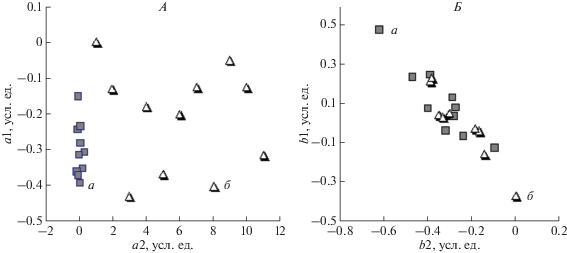
Результаты регрессионного анализа показали, что более выраженное влияние кратковременная гипоксия оказывает на регрессионные коэффициенты левой стороны измерения по сравнению с правой стороной. Это можно видеть на рис. 2, где показано изменение положения геометрических точек в фазовой плоскости регрессионных коэффициентов левой (рис. 1, А) и правой (рис. 2, Б) сторон измерения. Наличие изменений числовых значений регрессионных коэффициентов под воздействием кратковременной гипоксии можно также видеть из табл. 1, согласно которой наибольшее влияние кратковременная гипоксия оказывает на коэффициенты с левой стороны измерения. Коэффициенты a1 и a2 достоверно изменялись у 80% испытуемых, а с правой стороны достоверные изменения коэффициентов b1 и b2 наблюдались только у 40% испытуемых. Можно заключить, что под влиянием кратковременного гипоксического воздействия в системе МЦР изменяется баланс между распределением кровоснабжением правой и левой сторон измерения. Это свидетельствует в пользу предположения о том, что в механизмах ауторегуляции регионального кровообращения важную роль играет лево-правосторонняя асимметрия показателей МЦР и под влиянием внешних воздействий в системе МЦР происходит перераспределение баланса между регуляторными влияниями симметричных регионов с целью поддержания устойчивого функционирования целостной системы МЦР.
Рис. 2.
Изменения положения геометрических точек в фазовой плоскости регрессионных коэффициентов после кратковременного гипоксического воздействия. А – левой стороны измерения (a1, a2); Б – правой стороны измерения (b1, b2). а – исходное состояние; б – состояние после гипоксии.
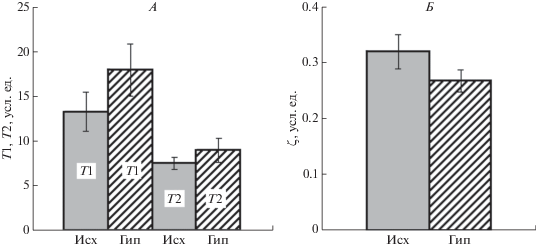
Следующим этапом исследований явилось тестирование системы МЦР испытуемых на устойчивость. С этой целью были рассчитаны числовые значения показателей устойчивости T1, T2, ζ и выполнена проверка выполнения условий (13)–(15). Результаты тестирования представлены в табл. 2, из которой можно видеть, что величины регрессионных коэффициентов у всех испытуемых как в исходном состоянии, так и сразу после кратковременного гипоксического воздействия, удовлетворяли условиям устойчивости, неустойчивых состояний не обнаружено. Результаты тестирования на устойчивость показали, что на персонифицированную оценку степени устойчивости к кратковременным гипоксическим воздействиям влияют не средние значения показателей перфузии слева и справа, а степень сбалансированности микрокровотока слева и справа, что отражено в выведенных нами объективных параметрах устойчивости (Т1, Т2, ζ). Так, у испытуемого 2 после кратковременного гипоксического воздействия показатель перфузии справа снизился (ПМпр исх = 14.03; ПМпр гип = 9.42), однако, это не говорит о снижении устойчивости системы МЦР у этого испытуемого. Показатели устойчивости Т1, Т2 и ζ у этого испытуемого, наоборот, после кратковременного гипоксического воздействия возросли, что свидетельствует о положительном влиянии такого рода воздействия на устойчивость системы МЦР этого испытуемого. Аналогичное увеличение маркеров устойчивости Т1, Т2 и ζ при снижении показателей перфузии являлось для испытуемых 7 и 8, что свидетельствует в пользу заключения о том, что на персонифицированную оценку степени устойчивости к кратковременным гипоксическим воздействиям влияют не средние значения показателей перфузии слева и справа, а степень сбалансированности микрокровотока справа и слева, отраженную в величинах маркеров устойчивости Т1, Т2, ζ. Результаты статистического анализа изменения величин маркеров устойчивости Т1, Т2, ζ показали, что в целом гипоксические воздействия имели тенденцию к увеличению устойчивости системы МЦР, что можно видеть из рис. 3. На рис. 3 представлены средние значения по всем 10 испытуемым маркеров устойчивости Т1 и Т2 (рис. 3, А) и параметра ζ, характеризующего степень выраженности колебательности флуктуаций микрокровотока в системе МЦР. Из рис. 3 можно видеть, что в среднем по всей группе испытуемых числовые значения маркеров устойчивости Т1 и Т2 под влиянием кратковременного гипоксического воздействия увеличивались одновременно с повышением степени выраженности колебательности флуктуаций микрокровотока ζ.
Таблица 2.
Числовые значения параметров {T1, T2, ζ}, определяющих устойчивость математической модели (2) в исходном состоянии и после кратковременного гипоксического воздействия, а также результаты проверки системы МЦР на устойчивость (TRUE или FALSE) для всех испытуемых
| № исп | T1 | T2 | ζ | ||||||
|---|---|---|---|---|---|---|---|---|---|
| исх | гип | T1 > 0 | исх | гип | T2 > 0 | исх | гип | ζ < 1 | |
| 1 | 14.95 | 37.47 | TRUE | 11.64 | 19.40 | TRUE | 0.39 | 0.26 | TRUE |
| 2 | 12.78 | 12.83 | TRUE | 8.01 | 7.38 | TRUE | 0.31 | 0.29 | TRUE |
| 3 | 8.54 | 24.57 | TRUE | 5.54 | 8.55 | TRUE | 0.32 | 0.17 | TRUE |
| 4 | 6.58 | 5.67 | TRUE | 5.08 | 4.76 | TRUE | 0.39 | 0.42 | TRUE |
| 5 | 9.82 | 13.25 | TRUE | 6.23 | 6.68 | TRUE | 0.32 | 0.25 | TRUE |
| 6 | 4.49 | 23.16 | TRUE | 4.55 | 11.06 | TRUE | 0.51 | 0.24 | TRUE |
| 7 | 19.19 | 12.08 | TRUE | 9.22 | 7.13 | TRUE | 0.24 | 0.30 | TRUE |
| 8 | 28.69 | 16.09 | TRUE | 9.41 | 6.93 | TRUE | 0.16 | 0.22 | TRUE |
| 9 | 13.25 | 22.80 | TRUE | 7.45 | 10.43 | TRUE | 0.28 | 0.23 | TRUE |
| 10 | 13.98 | 11.19 | TRUE | 7.56 | 6.88 | TRUE | 0.27 | 0.31 | TRUE |
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Вопросам устойчивости реакций системы кровообращения на гипоксические нагрузки посвящены многочисленные исследования в связи с широким применением гипоксических тренировок в спортивной медицине, а также немедикаментозной профилактике и реабилитации пациентов с различными заболеваниями [8–11]. Однако все эти работы носят описательный характер, т.к. не учитывают математические закономерности право-левого гемодинамического баланса системы регионарного кровообращения, обнаруженные нами в ходе настоящих исследований. Предложенная нами новая расчетно-экспериментальная методика оценки устойчивости системы МЦР к гипоксическим воздействиям, основана на анализе решений системы дифференциальных уравнений, описывающих функционирование право-левого гемодинамического баланса системы регионарного кровообращения. Проведенные исследования показали, что гипоксические воздействия изменяют числовые значения параметров устойчивости у всех испытуемых, не выводя их за пределы границ зон устойчивости. Однако реакция на гипоксические воздействия отличалась большой индивидуальностью у разных испытуемых. Это согласуется с результатами наших предыдущих исследований [8], в которых было показано, что кратковременное гипоксическое воздействие вызывает достоверно значимый ответ микроциркуляторного русла. У испытуемых было повышение эндотелиального и нейрогенного вазомоторного компонентов регуляции микрогемодинамики, причем характер микроциркуляторного “ответа” зависел от исходной чувствительности испытуемого к гипоксии и отличался большой индивидуальностью у разных испытуемых. В настоящих исследованиях нами были не только подтверждены результаты этих исследований, но и объяснены причины больших индивидуальных различий реакции показателей МЦР на гипоксические воздействия. Нами показано, что функционирование системы МЦР описывается строгими математическими уравнениями, определяющими сбалансированность кровоснабжения правого и левого микроциркуляторного русла, направленную на поддержание устойчивости всей системы. Поэтому реакция на гипоксию у одних испытуемых может характеризоваться повышением перфузии, на той или другой стороне измерения, а у других – понижением. Определяющим фактором является не величина перфузии на той или другой стороне измерения, а право-левосторонний баланс кровоснабжения симметричных регионов. Степень сбалансированности кровоснабжения симметричных регионов микроциркуляторного русла определяется параметрами математической модели, описываемой системой дифференциальных уравнений (2). Сформулированные нами критерии взаимосвязи между числовыми значениями этих параметров, выраженные в соотношениях (13)–(15), определяют условия устойчивости функционирования целостной системы МЦР. Эта система функционирует таким образом, что любое внешнее возмущающее воздействие вызывает компенсаторную реакцию, направленную на поддержание устойчивости системы. Результаты проведенных исследований показали, что гипоксические воздействия приводили к различным изменениям показателей перфузии слева и справа у разных испытуемых, но выраженность и направленность системной компенсаторной реакция на гипоксию была одинаковой для всех испытуемых. Эта реакция имела тенденцию к повышению числовых значений параметров Т1 и Т2, определяющих устойчивость системы. Таким образом, гипоксические воздействия вызывали компенсаторную реакцию, направленную на поддержание устойчивости функционирования целостной системы кровоснабжения симметричных органов. Результаты настоящих исследований подтверждают ранее сформулированный в работах С.П. Ногиной [12] принцип право-левого гемодинамического баланса, определяющий пространственно-временную организацию гемодинамической системы и выявляющий ее интегративную роль в отношении снабжаемых органов. Поддержание право-левого гемодинамического баланса является важнейшим жизнеобеспечивающим фактором устойчивости целостной гемодинамической системы и поддерживается всей иерархией вегетативной и центральной регуляции сосудов.
ВЫВОДЫ
1. Установлено, что изменения амплитуд флуктуаций микрокровотока симметричных височных областей головы зависят от исходных значений этих показателей не только с одноименной, но и с противоположной стороны наблюдения.
2. Показано, что изменения перфузии симметричных височных областей головы всегда коррелируют отрицательно с мгновенными значениями перфузии той же стороны измерения, а с мгновенными значениями перфузии противоположной стороны измерения могут быть как положительные, так и отрицательные корреляции.
3. Составлены регрессионные уравнения, описывающие взаимосвязи между синхронными изменениями показателей МЦР симметричных височных областей головы и их исходными значениями с левой и правой сторонами измерения. Показано, что числовые значения параметров уравнений регрессии a1, a2, b1, b2 могут быть использованы для оценки устойчивости функционирования системы МЦР.
4. Получены индивидуальные оценки числовых значений параметров уравнений регрессии (a1, a2, b1, b2) для каждого испытуемого в исходном состоянии и после кратковременного гипоксического воздействия, что позволяет оценить устойчивость системы МЦР испытуемых к кратковременным гипоксическим воздействиям.
5. Показано, что кратковременное гипоксическое воздействие изменяет числовые значения параметров устойчивости у всех испытуемых, не выводя их за пределы границ зон устойчивости, однако реакция на гипоксические воздействия отличается значительной индивидуальностью у разных испытуемых.
6. Предложенная методика может быть использована при проведении персонализированных оценок степени тренированности и устойчивости к гипоксическим воздействиям у различных групп испытуемых.
7. Предложенная методика позволяет определить количественные критерии, разделяющие нормальные (устойчивые) и патологические (неустойчивые) режимы функционирования системы МЦР и может найти применение в практической медицине для оценки состояния системы МЦР пациента и прогнозирования вероятности ее перехода в патологические режимы.
Этические нормы. Все исследования проведены в соответствии с принципами биомедицинской этики, сформулированными в Хельсинкской декларации 1964 г. и ее последующих обновлениях, и одобрены локальным биоэтическим комитетом Научно-исследовательского института нормальной физиологии им. П.К. Анохина (Москва).
Информированное согласие. Каждый участник исследования представил добровольное письменное информированное согласие, подписанное им после разъяснения ему потенциальных рисков и преимуществ, а также характера предстоящего исследования.
Финансирование работы. Работа выполнена за счет средств Федерального бюджета РФ в рамках выполнения Государственных заданий ФГБНУ “НИИНФ им. П.К. Анохина и Института клинической медицины им. Н.В. Склифосовского ФГАОУ ВО Первый МГМУ им. И.М. Сеченова (Сеченовский университет, Москва)
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных интересов, связанных с публикацией данной статьи.
Список литературы
Михайличенко Л.А. Показатели микроциркуляции парных органов и тканей экспериментальных животных в норме // Регионарное кровообращение и микроциркуляция. 2007. Т. 6. № 1. С. 164.
Мезенцева Л.В., Перцов С.С. Синхронные изменения показателей микроциркуляции верхних конечностей при асимметричных физически нагрузках на них // Физиология человека. 2020. Т. 46. № 6. С. 101. Mezentseva L.V., Pertsov S.S. Synchronous Changes in Microcirculation Parameters of the Upper Limbs in Asymmetric Physical Loads // Human Physiology. 2020. V. 46. № 6. P. 671.
Ладожская–Гапеенко Е.Е., Храпов К.Н. Возможности лазерной допплеровской флоуметрии с использованием ортостатической пробы в оценке функционального состояния микроциркуляции // Регионарное кровообращение и микроциркуляция. 2020. T. 19. № 3. С. 39.
Федорович А.А. Микрососудистое русло кожи человека как объект исследования // Регионарное кровообращение и микроциркуляция. 2017. Т. 16. № 4. С. 11.
Martini R., Bagno A. The wavelet analysis for the assessment of microvascular function with the laser Doppler fluxmetry over the last 20 years. Looking for hidden informations // Clin. Hemorheol. Microcirc. 2018. V. 70. № 2. P. 213.
Low D.A., Jones H., Cable N.T. et al. Historical reviews of the assessment of human cardiovascular function: interrogation and understanding of the control of skin blood flow // Eur. J. Appl. Physiol. 2020. V. 120. № 3. P. 1.
Эльсгольц Л.Э. Дифференциальные уравнения и вариационное исчисление. М.: Наука, 1969. 424 с.
Глазачев О.С., Дудник Е.Н. Особенности реактивности сосудов микроциркуляторного русла практически здоровых людей при моделировании острой умеренной гипоксии и гипероксии // Физиология человека. 2013. Т. 39. № 4. С. 74. Glazachev O.S., Dudnik E.N. Microcirculatory reactivity features in apparently heathy individuals during acute moderate hypoxia and hyperoxia modeling // Human Physiology. 2013. V. 39. № 4. P. 400.
Зеленкова И.Е., Зоткин С.В., Корнеев П.В. и др. Вариабельность гипоксической устойчивости у спортсменов различной квалификации и спортивной специализации // Спортивная медицина: наука и практика. 2016. Т. 6. № 4. С. 5.
Малеев Д.О. Определение индивидуальной устойчивости организма лыжников-гонщиков высокой квалификации к острой гипоксии // Человек. Спорт. Медицина. 2015. Т. 15. № 4. С. 19.
Mateika J.H., El-Chami M., Shaheen D., Ivers B. Intermittent hypoxia: a low-risk research tool with therapeutic value in humans // J. Appl. Physiol. 2015. V. 118. № 5. P. 520.
Мезенцева Л.В. Фундаментальные принципы системной организации мозгового кровообращения (по работам С.П. Ногиной) // Академический журн. Западной Сибири. 2018. Т. 14. № 6(77). С. 4.
Дополнительные материалы отсутствуют.
Инструменты
Физиология человека