Доклады Российской академии наук. Физика, технические науки, 2020, T. 495, № 1, стр. 26-33
САМОСБОРКА ФЛУОРЕСЦЕНТНЫХ ФОТОННО-КРИСТАЛЛИЧЕСКИХ СТРУКТУР В КАПЛЯХ БИНАРНОГО РАСТВОРИТЕЛЯ ВОДА–ГЛИЦЕРИН
О. А. Савенко 1, А. С. Степко 1, Н. Н. Шевченко 2, А. В. Кошкин 1, П. В. Лебедев-Степанов 1, 3, *
1 Федеральный научно-исследовательский центр “Кристаллография и фотоника”
Российской академии наук
Москва, Россия
2 Институт высокомолекулярных соединений Российской академии наук
Санкт-Петербург, Россия
3 Национальный исследовательский ядерный университет МИФИ
Москва, Россия
* E-mail: petrls@mail.ru
Поступила в редакцию 09.10.2020
После доработки 19.10.2020
Принята к публикации 21.10.2020
Аннотация
Впервые экспериментально исследована морфология фотонно-кристаллических структур, получаемых самосборкой флуоресцентных наночастиц-маркеров из испаряющихся капель бинарного растворителя вода–глицерин, компоненты которого существенно отличаются по вязкости и скорости испарения, будучи при этом бесконечно растворимы друг в друге при нормальных условиях. Показано, что основным разупорядочивающим самосборку фактором являются вихревые потоки Марангони, причем изменение начального соотношения концентраций компонентов бинарной смеси позволяет управлять степенью упорядочения образующейся после испарения растворителя из капли твердой фазы, распределенной на подложке. Малой начальной концентрации любого компонента бинарного растворителя отвечает наиболее упорядоченное распределение, а средним концентрациям – наиболее разупорядоченное. Рассчитаны характерные значения чисел Марангони в экспериментах. Показано, что средний радиус распределения ансамбля частиц-маркеров по подложке может служить дескриптором для описания степени упорядоченности.
Процессы самосборки ансамблей монодисперсных наночастиц, поверхность которых модифицирована фотоактивными молекулами (люминофорами), представляют интерес для многочисленных приложений (в оптической хемосенсорике, фотонике, медицинской диагностике) [1–5].
Получаемые таким образом фотонные кристаллы высокой степени упорядочения дают возможность модификации спектра излучения в широком диапазоне длин волн. Это объясняется спектральным перераспределением плотности оптических состояний, которая понижена или равна нулю в пределах фотонной запрещенной зоны, в то время как в других областях спектра она увеличивается. В связи с тем, что интенсивность спонтанного излучения молекулы люминофора зависит от распределения плотности состояний в окружающей среде, любые спектральные перераспределения этой плотности обусловливают перераспределение интенсивности в спектре люминесценции центра свечения. Таким образом, спектр люминесценции излучателя в структуре фотонного кристалла зависит от положения и ширины фотонной запрещенной зоны. Кроме того, направление фотонной запрещенной зоны также приводит к изменению частотного распределения интенсивности люминесценции, т.е. к зависимости спектра свечения от угла съемки [6].
Твердофазные массивы таких частиц, выполняющие роль матриц хемосенсоров, получают методом самосборки в испаряющейся капле раствора частиц или в мениске вертикальной пластинки, погруженной в сосуд с раствором [4, 5]. При этом важно уметь получать матрицы наночастиц разной степени упорядочения, т.е. разрыхленности, что влияет на скорость проникновения в толщу системы паров аналита.
Флуоресцентные частицы и их самособирающиеся ансамбли могут также выступать в качестве маркеров, которые визуализируют морфологию твердой фазы, получаемой в процессе кристаллизации растворенного вещества при испарении растворителя в капле раствора. При этом характер морфологии полученной твердой фазы отражает исходные свойства раствора, что применяется в медицинской диагностике. Добавление частиц-маркеров в раствор биожидкости дает возможность диагностировать заболевание, визуализируя положение частиц после высыхания капли раствора, которое зависит от свойств исходной биожидкости [7].
Для установления связи между свойствами раствора и морфологией получаемой из него твердой фазы требуется понимание процессов десольватационной самосборки (самоорганизации), приводящих к формированию твердой фазы разной степени упорядочения. В случае биологической жидкости речь идет о наиболее сложной многокомпонентной системе, свойства которой существенно меняются в процессе высыхания. Такие системы особенно сложны для моделирования и требуют накопления эмпирических данных [8, 9].
В данной работе исследовалось поведение частиц-маркеров в бинарном растворителе вода–глицерин, компоненты которого существенно различаются по вязкости и скорости испарения, будучи при этом бесконечно растворимы друг в друге при нормальных условиях. Актуальность исследования такой системы связана с ее подобием с растворами биологических жидкостей, физико-химические свойства которых, в том числе вязкость, существенно изменяются по мере испарения содержащейся в них воды – основного компонента раствора.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
В качестве флуоресцентного красителя использовали транс-4-[4-(диметиламин)стирил]-1-метилпиридиний йодид, сокращенно 4-DASPI (Sigma-Aldrich). Используемый в работе образец содержал краситель с концентрацией 3 × 10–4 моль/л и 0.057 масс. % сорбента. В качестве сорбента применялись частицы – сополимеры стирола и метакриловой кислоты П(Ст-МАК), концентрация поверхностных групп [COOH] = 2.52 мкмоль/м2, дзета-потенциал –60 мВ (синтезированы в Институте высокомолекулярных соединений РАН, [10]). В поверхностном слое частиц локализованы полимерные цепи, обогащенные звеньями метакриловой кислоты, т.е. карбоксильные группы расположены как вдоль полимерной цепи, так и на ее конце.
Гидродинамический диаметр таких частиц существенно зависит от рН, а также от присутствия заряженных фрагментов молекул, поскольку ионизованные полимерные цепи за счет сил электростатического отталкивания могут выдвигаться в дисперсионную среду. Измеренный по методу динамического светорассеяния (Photocor, Россия) диаметр частиц составил 308 нм.
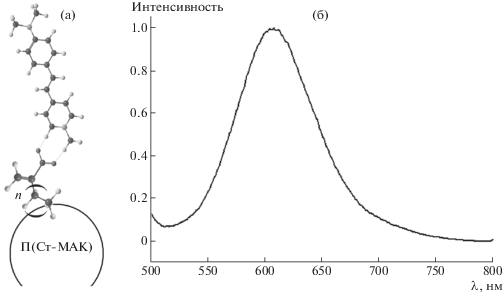
Для получения частиц, модифицированных красителем, готовили водные дисперсии полимерных частиц, в которые добавляли раствор красителя в деионизованной воде. Механизм сорбции красителя – ионно-обменный. Оптимизация структуры 4-DASPI в присутствии метакриловой кислоты, представляющей оконечность полимерной цепи, принадлежащей поверхности частицы (рис. 1а), проводилась с использованием квантово-химического метода PM3 (программа GamessUS). Спектр флуоресценции красителя (измеренный на приборе Cary Eclipse Fluorescence Spectrophotometer, Agilent Technologies, США) показан на рис. 1б. Эксперимент показал, что в бинарном растворе состава вода–глицерин не наблюдается существенного сдвига положения максимума флуоресценции красителя.
Рис. 1.
а – Схема ионно-обменной сорбции красителя 4-DASPI на карбоксильные группы частицы П(Ст-МАК); б – спектр флуоресценции 4-DASPI с максимумом на длине волны 620 нм.
Были приготовлены бинарные водно-глицериновые растворы полученных таким образом флуоресцентных частиц-меток, объемная концентрация наночастиц составляла ~0.22 об. % во всех исследуемых растворах. Растворы наносились микродозатором на предварительно очищенное – промытое поочередно водой и ацетоном – предметное стекло каплями объемом по 1 мкл. Получали не менее трех образцов капель с каждым раствором с целью последующего усреднения результатов. Потом стекло с каплями помещали в сушильный шкаф (Binder ED53, Германия), предварительно нагретый до 80°С.
Оптические и флуоресцентные изображения сухого остатка (паттерна) капель получали на сканирующем микроскопе Nikon ECLIPSE E600. Для возбуждения флуоресценции при съемке использовали ртутную лампу Nikon C-SHG1 и светофильтр Nikon B2-A.
Обработка микроскопических изображений капель проводилась с помощью программы ImageJ. Поскольку интенсивность флуоресценции с единицы площади поверхности подложки пропорциональна количеству частиц на ней, радиальные профили распределения частиц пропорциональны радиальному распределению интенсивности флуоресценции. С учетом этого, на основе анализа флуоресцентных изображений были построены профили интенсивности пространственного распределения флуоресценции, которые пропорциональны поверхностной концентрации частиц в сухом остатке высохшей капли (рис. 2).
Рис. 2.
Нормированные радиальные распределения (профили) интенсивности флуоресценции, пропорциональные относительной поверхностной концентрации распределения частиц-маркеров в твердофазном осадке круглой формы, образованном при испарении капли бинарного растворителя на стеклянной подложке при разном исходном объемном соотношении компонентов: а – 0% глицерина, 100% воды; б – 10% глицерина, 90% воды; в – 50% глицерина, 50% воды; г – 95% глицерина, 5% воды.

ОБСУЖДЕНИЕ
В работе [11] заложены основы понимания процессов в испаряющейся капле миллиметровых (капиллярных) размеров. Если имеет место эффект удержания или прилипания (pinning) контактной линии капли на подложке в процессе испарения растворителя, то внутри капли действуют потоки компенсационной природы, которые перемещают растворенные в капле частицы от центра к периферии, образуя характерное кольцевое утолщение – избыток твердой фазы на периферии капли (рис. 3а).
Рис. 3.
Формирование характерных распределений частиц гидродинамическими потоками: а – компенсационные потоки создают валик твердой фазы вдоль контактной линии, б – вихревые потоки Марангони хаотизируют распределение частиц. Направление потоков Марангони соответствует повышенному поверхностному натяжению на вершине капли по отношению к ее краю.

Кроме того, в высыхающей капле могут образовываться потоки конвективной природы, обусловленные перепадом поверхностного натяжения между верхом и краем капли (потоки Марангони). Они обусловлены зависимостью поверхностного натяжения от температуры жидкости или от концентрации сложного раствора. Процессы испарения приводят к возникновению градиента температуры на поверхности капли или к градиенту концентрации компонентов сложного растворителя вследствие того, что скорости испарения разных компонентов различаются. Потоки Марангони в испаряющейся осесимметричной капле имеют характер торообразных вихрей (рис. 3б).
Компенсационные потоки осуществляют перенос частиц к краю капли, тогда как поток Марангони приводит к разупорядочению движения частиц, размыванию пиковой концентрации твердой фазы на периферии капли. Сложение двух этих типов потока, в зависимости от их относительной интенсивности, может привести к различным морфологиям распределения частиц. Конвекция Марангони – пороговый эффект. Его наличие или отсутствие (а значит, и структура потоков) характеризуется числом Марангони.
В связи с тем, что в рассматриваемой системе вода испаряется за время, на порядки более короткое, чем глицерин, испарение бинарного растворителя имеет две четко выраженные фазы. Первая фаза – быстрая, в пределах 1 мин – испарение воды из смеси вплоть до предельно малых концентраций, величина которых определяется равновесием с водяным паром в окружающей атмосфере. Вторая фаза – длительная, несколько суток – испарение глицерина. Рост начальной концентрации глицерина от малых до средних значений в исходном растворе приводит к размыванию четко выраженной кольцевой области на краю капли. Это хорошо иллюстрирует рис. 2в по сравнению с рис. 2а.
Из общих соображений должна выполняться следующая асимптотика: если исходная примесь глицерина очень мала, то результат самосборки не может существенно отличаться от случая чистого водного растворителя (случай нулевой концентрации глицерина). При этом имеют место только небольшие по интенсивности потоки Марангони термокапиллярной природы, которые обусловливают то, что некоторое количество частиц не достигает края капли, образуя неупорядоченные массивы по всей ее поверхности. То же самое должно быть справедливо для случая существенного исходного преобладания глицерина над содержанием воды (рис. 2г).
При этом необходимо учесть, что размывание тонкой кромки частиц на краю капли может происходить за счет диффузии частиц. В случае воды испарение происходит настолько быстро, что для практически любых применяемых коллоидов диффузионные процессы не успевают заметно разбросать частицы, собираемые у контактной линии. Хотя глицерин испаряется гораздо медленнее, что увеличивает время действия броуновского движения, но и коэффициент диффузии частиц в глицерине, вследствие его большой вязкости, крайне мал – почти в 1000 раз меньше, чем в воде, так что, как показывают оценки, диффузионный процесс не скажется существенно на морфологии паттерна.
В связи с тем, что вода испаряется значительно быстрее, чем глицерин, на поверхности капли образуется область, обедненная водой. При этом, поскольку испарение с края капли с острым контактным углом происходит быстрее, чем на вершине капли, то обеднение водой больше возле контактной линии, а значит, так как поверхностное натяжение чистой воды больше, чем у глицерина, то поверхностное натяжение раствора у края капли ниже, чем наверху. Эта ситуация схематически представлена на рис. 3б. Направление закрутки потоков Марангони соответствует указанному распределению натяжения.
Интенсивность таких потоков тем больше, чем сильнее перепад поверхностного натяжения между вершиной и краем капли. Для максимума градиента нужно, чтобы перепад концентрации воды между этими точками был также максимален. Очевидно, что максимальному перепаду концентрации воды вдоль поверхности капли в бинарном растворителе отвечает обратный по знаку перепад концентрации глицерина. Из этих соображений можно заключить, что максимальные вихревые потоки возникают при максимальном значении выражения c(1 – c), т.е. при средних концентрациях бинарных компонентов (c – относительная молярная концентрация воды). В пределе малых концентраций того или иного компонента концентрационных потоков Марангони не возникает, как и должно быть для чистого растворителя.
В рассматриваемых экспериментах объемная доля глицерина изменялась в широких пределах (0–95% по объему). При нулевой концентрации глицерина пик концентрации частиц на краю капли наиболее хорошо выражен, что связано с отсутствием концентрационных потоков Марангони (рис. 2а). При исходном наличии глицерина в воде (рис. 2б–2г) пик на краю размыт в большей или меньшей степени, что связано с действием концентрационных потоков Марангони. При малых исходных концентрациях глицерина (рис. 2б), по мере испарения воды, ее концентрация падает и приближается к средним значениям – при этом потоки Марангони нарастают. При дальнейшем снижении концентрации воды потоки Марангони ослабевают и прекращаются. Когда капля становится чисто глицериновой, число Марангони уже являются докритическим, так что действуют только компенсационные потоки, которые переносят вещество к краю.
При малых начальных концентрациях глицерина средние его концентрации с максимальным потоком Марангони достигаются по мере испарения воды. Поэтому действие сильных потоков произойдет уже тогда, когда объем капли будет достаточно мал, а время действия этих потоков будет небольшим, поэтому и размытие пика на краю капли при этом невелико (рис. 2б). При несколько более высоких начальных концентрациях глицерина максимальные потоки Марангони будут достигнуты раньше и будут действовать дольше, поэтому и их размывающее действие будет сильнее, так что пик на краю может совсем не проявиться (рис. 2в). Когда воды в исходном растворе почти нет (а концентрация глицерина максимальна), имеет место другой крайний случай – вода испаряется быстро, при этом объем капли почти не меняется, и далее испаряется только глицерин. При этом время действия бинарных потоков и их интенсивность малы, так что формирование твердой фазы происходит в основном за счет радиальных компенсационных потоков с формированием выраженного краевого пика (рис. 2г).
Подчеркнем, что так как число Марангони обратно пропорционально вязкости, область максимальных значений скорости потоков Марангони смещена в сторону более высоких концентраций воды. Данные соображения качественно объясняют полученный в эксперименте результат.
Если преобладающим является поток тепла, обусловленный теплопроводностью (при этом число Пекле, которое определяет отношение интенсивности конвективного и молекулярного переноса тепла, много меньше единицы, Pe ≪ 1), то простой оценкой перепада температур на поверхности капли является величина [12]
где ΔH – теплота испарения жидкости, ${{\rho }_{S}} = m \cdot {{n}_{S}}$ – плотность насыщенного пара (m – молекулярная масса, ${{n}_{S}}$ – объемная концентрация насыщенного пара), D – коэффициент диффузии пара в окружающем воздухе, $\chi $ – относительная влажность воздуха, R и h – радиус и высота капли соответственно, $\kappa $ – температуропроводность жидкости.Термокапиллярное число Марангони определяется выражением
(2)
${\text{M}}{{{\text{a}}}_{T}} = \frac{{\Delta Th}}{{a\eta }}\left| {\frac{{d\sigma }}{{dT}}} \right|,$Концентрационное число Марангони определяется выражением
(3)
${\text{M}}{{{\text{a}}}_{C}} = \frac{{\Delta ch}}{{{{D}_{L}}\eta }}\left| {\frac{{d\sigma }}{{dc}}} \right|,$Если преобладающим является диффузионный поток, выравнивающий по всей капле концентрации компонентов бинарного растворителя (Pe ≪ 1), то в первом приближении оценкой перепада концентраций является величина, аналогичная (1):
где ${{D}_{L}}$ – коэффициент диффузии компонента в жидкости, а D – в воздухе, ${{n}_{L}}$ – объемная концентрация молекул данного сорта в жидкости. Модель испарения капли бинарного растворителя представлена в [13].Критическое значение числа Марангони – около 100 [14]. С превышением этого значения возникают конвективные потоки Марангони, компенсирующие дальнейший рост градиента температуры. Отсюда можно найти для данной капли критическое значение перепада температур, превышение которого вызывает такие потоки. Если расчет по реальным параметрам дает сверхкритическое значение числа Марангони, то можно найти величину конвективного потока, исходя из того, что наличие такого потока должно уменьшить перепад температур до критического за счет конвекции.
Определение градиента поверхностного натяжения вдоль поверхности капли позволяет вычислить граничное условие для скорости потока Марангони. Подставляя параметры индивидуальных компонентов из табл. 1, можем определить числа Марангони.
Таблица 1.
Параметры индивидуальных компонентов при 80°C
| Жидкость | ρ, кг м–3 | M, г моль–1 | p, Па | nS, м–3 | nL, м–3 | D, м2c–1 | σ, Дж м–2 | $\frac{{d\sigma }}{{dT}}$, Дж м–2K–1 | cp, Дж кг–1К–1 | ΔH, кДж кг–1 | $\frac{{d\sigma }}{{dc}}$, Дж м–2 | λ, Вт/(м К) | a = $\frac{\lambda }{{{{c}_{p}}\rho }}$ , м2c–1 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Вода | 972 | 18 | 47 400 | 9.7 × 1024 | 3.2 × 1028 | 3.5 × 10–5 | 0.0623 | –1.8 × 10–4 | 4200 | 2308 | 0.006 | 0.660 | 0.162 × 10–6 |
| Глицерин | 1224 | 92 | >100 | 2 × 1022 | 8 × 1027 | 0.7 × 10–5 | 0.0562 | –7.6 × 10–5 | 3340 | 660 | 0.294 | 0.072 × 10–6 |
Для капли объемом около 1 мкл, радиусом 1 мм и высотой 0.5 мм, можно показать, что в капле глицерина термокапиллярное число Марангони ${\text{M}}{{{\text{a}}}_{T}} \approx 3$ при перепаде температуры (1) около 0.2 K, тогда как в капле воды термокапиллярное число Марангони оценивается величиной ${\text{M}}{{{\text{a}}}_{T}} \approx 3000$ при перепаде температуры (1) около 1.7 K.
Таким образом, в рассматриваемых условиях для микролитровой капли термокапиллярное число Марангони значительно меньше критического значения этого числа, равного 100, так что потоки Марангони отсутствуют, а в капле воды той же геометрии термокапиллярные потоки существуют и имеют заметную интенсивность, приводя к перемешиванию жидкости.
С другой стороны, при достижении критического значения числа Марангони возникают конвективные потоки, направление которых таково, что эти потоки компенсируют превышение критического значения. Это позволяет оценить характерные скорости потоков для капель, которым отвечают распределения частиц, представленные на рис. 2 (см. табл. 2).
Таблица 2.
Параметры серии образцов растворов частиц-маркеров в бинарном растворителе вода–глицерин, отвечающие профилям, представленным на рис. 2
| Растворитель | Радиус капли, мм | Мольная доля воды | Средний безразмерный радиус распределения, 〈R〉 | Характерное значение Ма |
|---|---|---|---|---|
| Вода, 100% | 0.975 | 1 | 0.76 | 3000 |
| 10 об. % глицерин + 90 об. % вода | 1.05 | 0.97 | 0.59 | 10 000 |
| 50 об. % глицерин + 50 об. % вода | 1.37 | 0.80 | 0.57 | >100 000 |
| 95 об. % глицерин + 5 об. % вода | 1.25 | 0.18 | 0.67 | 3 |
На основе экспериментальных данных численно вычислялись интегралы
(5)
${{I}_{1}} = 2\pi \int\limits_0^R {rY(r)dr} = 2\pi \sum\limits_{i = 1}^N {{{r}_{i}}({{r}_{{i + 1}}} - {{r}_{i}})Y({{r}_{i}})} ,$(6)
${{I}_{2}} = 2\pi \int\limits_0^R {{{r}^{2}}Y(r)dr} = 2\pi \sum\limits_{i = 1}^N {{{r}_{i}}^{2}({{r}_{{i + 1}}} - {{r}_{i}})Y({{r}_{i}})} ,$Величины $\langle R\rangle $ с учетом погрешности были рассчитаны для капель растворов, параметры которых представлены в табл. 2, и помещены на графике рис. 4 в зависимости от исходной концентрации глицерина.
Рис. 4.
График среднего радиуса распределения частиц в сухом остатке, образованном при испарении капли, в зависимости от исходной объемной концентрации глицерина в водном растворе.
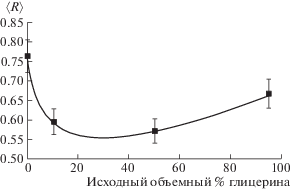
Очевидно, что безразмерная величина среднего радиуса распределения $\langle R\rangle $ может быть использована в качестве дескриптора, определяющего степень влияния потоков Марангони на формирование распределения твердой фазы.
Очевидно, что для наиболее чистых растворителей (воды и глицерина), в которых скорости потоков Марангони имеют наименьшее значение, как это следует из табл. 2, наблюдаются наибольшие значения величины $\langle R\rangle $. Этим значениям отвечает преимущественное распределение частиц по периферии капли (рис. 2а, 2г).
Ранее нами было показано, что капиллярная укладка частиц, подводимых радиальными компенсационными потоками к мениску вблизи контактной линии капли, дает наиболее плотную коллоидно-кристаллическую упаковку [15]. Потоки Марангони хаотизируют действие компенсационных потоков и ухудшают укладку частиц вблизи мениска, разрушая так называемый “эффект кофейного кольца” [11]. Поэтому наиболее упорядоченному распределению частиц отвечает более высокое значение радиуса (7), которому, как следует из табл. 2, соответствуют наименее интенсивные потоки Марангони.
ВЫВОДЫ
1. Экспериментально исследована самосборка флуоресцентных частиц-маркеров в каплях бинарных растворителей состава вода–глицерин с разной концентрацией компонентов.
2. Разработан и апробирован метод определения морфологии твердой фазы внутри капли с помощью анализа интенсивности флуоресценции частиц-маркеров.
3. Показано, что основным разупорядочивающим самосборку фактором являются потоки Марангони, разрушающие периферийное осаждение частиц. Изменение концентрации бинарного растворителя позволяет управлять степенью упорядочения твердой фазы, причем малой концентрации любого компонента отвечает наиболее упорядоченное распределение.
4. Рассчитаны характерные значения чисел Марангони, достигаемые в рассматриваемых системах.
5. Показано, что средний радиус распределения частиц может служить дескриптором для описания степени упорядоченности. Высокие значения величины $\langle R\rangle $, определяемой формулой (7), характерны для наиболее чистых растворителей.
Список литературы
Brutin D., Starov V. // Chem. Soc. Rev. 2018. V. 47. P. 558–585.
Zang D., Tarafdar S., Tarasevich Yu. et al. // Phys. Rep. 2019. V. 804. P. 1–56.
Bacchin P., Brutin D., Davaille A. et al. // Eur. Phys. J. E. 2018. V. 41: 94. P. 1–35.
Лебедев-Степанов П.В. Введение в самоорганизацию и самосборку ансамблей наночастиц. М.: НИЯУ МИФИ, 2015. 304 с.
Лебедев-Степанов П.В., Кадушников Р.М., Молчанов С.П. и др. // Российские нанотехнологии. 2013. № 3-4. С. 5–23.
Богданова М.В., Лебедев-Степанов П.В. // Кристаллография. 2017. Т. 62 (6). С. 976–980.
Trantum J.R., Wright D.W., Haselton F.R. // Langmuir. 2012. V. 28. P. 2187–2193.
Lebedev-Stepanov P.V., Buzoverya M.E., Shishpor I.V., Vlasov K.O., Potekhina Yu.P. // J. Bioinformatics and Genomics. 2018. № 1. P. 1–6.
Lebedev-Stepanov P.V., Buzoverya M.E., Vlasov K.O., Potekhina Yu.P. // J. Bioinformatics and Genomics. 2018. № 4. P. 1–5.
Yakimanskya A.V., Menshikova A.Yu., Shevchenko N.N. et al. // Polym. Adv. Technol. 2009. V. 20. P. 581–588.
Deegan R. // Nature. 1997. V. 389. P. 827–829.
Lebedev-Stepanov P.V., Vlasov K.O. Colloids and Surfaces A: Physicochem. Eng. Aspects. 2013. V. 432. P. 132–137.
Duan F., Badam V.K., Durst F., Ward C.A. // Phys. Rev. E. 2005. V. 72. P. 056303.
Lebedev-Stepanov P., Kobelev A., Efimov S. MATEC Web of Conferences. 2016. V. 84 (22). P. 1–4.
Лебедев-Степанов П.В., Громов С.П., Молчанов С.П. и др. // Российские нанотехнологии. 2011. Т. 6. № 9–10. С. 72–78.
Дополнительные материалы отсутствуют.
Инструменты
Доклады Российской академии наук. Физика, технические науки


