Доклады Российской академии наук. Химия, науки о материалах , 2021, T. 498, № 1, стр. 76-82
Масштабируемый одностадийный электрохимический синтез графеноподобного материала контролируемой морфологии
А. В. Кирьянова 1, С. Сюй 1, М. О. Галлямов 1, 2, О. О. Капитанова 1, 3, *
1 Московский государственный университет
имени М.В. Ломоносова
119991 Москва, Россия
2 Институт элементоорганических соединений
им. А.Н. Несмеянова Российской академии наук
119991 Москва, Россия
3 Московский физико-технический институт
141701 Долгопрудный, Россия
* E-mail: olesya.kapitanova@gmail.com
Поступила в редакцию 10.04.2021
После доработки 08.05.2021
Принята к публикации 03.06.2021
Аннотация
В работе впервые показан электрохимический подход к получению графеноподобных частиц с заданной морфологией. Было продемонстрировано, что параметры электрохимического синтеза позволяют контролировать степень окисленности и латеральный размер в синтезируемом графеноподобном материале.
Оксид графена (ОГ) – перспективная производная графена – является материалом нестехиометрического состава с высоким содержанием кислорода (соотношение С/O < 4), содержащегося в функциональных группах (гидроксильных, эпоксидных, карбонильных и карбоксильных) [1]. При этом синтез ОГ с различным содержанием кислорода дает возможность варьировать его физико-химические свойства в широких пределах [2]. Так, химическое или термическое восстановление кислородсодержащих групп позволяет получить восстановленный оксид графена, который обладает высокой электронной проводимостью благодаря системе π-сопряженных связей, в то время как ОГ является диэлектрическим материалом. Варьируемость свойств в широких пределах позволяет рассматривать ОГ и его производные в широком спектре применений: в газоосушительных мембранах [3, 4], мемристорах [5], проводящих добавках в аккумуляторах [6] и др.
В настоящее время наиболее распространенным способом получения оксида графена является химическое окисление графита с использованием методов Хаммерса (Hummers) и Броди (Brodie) [7], основанное на применении сильных окислителей и концентрированных кислот. При таких условиях синтеза образуются необратимые дефекты в графитовой матрице, что делает невозможным синтез графеноподобных частиц высокого структурного совершенства. Также химические методы окисления и расслаивания графита в производственных масштабах наносят значительный вред окружающей среде ввиду использования большого количества кислот.
В последнее время перспективным широкомасштабным синтетическим подходом к получению графеноподобных материалов является электрохимическое расслаивание графитового прекурсора [8]. При этом свойства получаемых частиц, например, степень окисленности, дефектности и электронная проводимость, значительно отличаются как от свойств химически синтезированного оксида графена, так и от свойств графена. Поэтому получаемый материал далее будем называть электрохимическим оксидом графена (ECGO, electrochemical graphene oxide). Данный способ имеет ряд преимуществ: не требуется дорогостоящее оборудование, есть возможность контроля процесса расслаивания электрическим полем, экологичность и масштабируемость [9]. Первые исследования с использованием электрохимического подхода заключались в окислении и расслаивании графита за счет электролиза электролитов на основе водных растворов кислот, солей и ионных жидкостей [10]. Ключевым недостатком данного способа являлись низкий выход по тонкослойным частицам (<10 слоев) и их малый латеральный размер. Следующим этапом модификации электрохимического синтеза стал двухстадийный метод, основанный на предварительной электрохимической интеркаляции графита в концентрированной серной кислоте по первой ступени с последующим окислением и расслаиванием в растворах солей [11]. Данный метод позволил значительно повысить выход по тонкослойным частицам ECGO и их латеральный размер. Однако в результате того, что расслаивание и окисление происходят во всем объеме электрода, процесс становится сложно контролируемым на второй стадии ввиду неконтролируемого расширения рабочего электрода и ухудшения его контакта с токосъемником. Это делает невозможным синтез частиц определенной морфологии (толщины, латерального размера). Актуальной разработкой электрохимического синтеза является одностадийное расслаивание графита в электролите на основе фталевой кислоты [12]. В результате механизма, заключающегося в осаждении органической кислоты на графитовом аноде в процессе электролиза, отслаивание и окисление происходят только на поверхности графита, что позволяет получать тонкослойные частицы (<3 слоев) с большим латеральным размером. Важно отметить, что данный метод не требует использования специфического оборудования и дорогостоящих прекурсоров.
В данной работе впервые представлен универсальный способ получения графеноподобных материалов, параметры которого (рабочее напряжение) определяют морфологию (толщину и латеральный размер) и окисленность частиц.
Синтез ECGO проводили в трехэлектродной электрохимической ячейке. В качестве анода использовали графитовую пластину 1.0 × 0.7 × 0.15 см3 качества “х. ч.” (Alfa Aesar, Германия), противоэлектрода – платину чистоты 99.99% (2.0 × 2.0 × × 0.05 см3), электрода сравнения – хлорсеребряный электрод ЭСр-10101 (Россия). Расстояние между рабочим и противоэлектродом составляло 2 см. Для приготовления электролита использовали 0.66 г фталевой кислоты в присутствии 1.23 г KOH и полученную смесь растворяли в 80 мл воды. Все реагенты имели качество “х. ч.” (Acros). Синтез проводили в потенциостатическом режиме при разности потенциалов в диапазоне от 2 до 10 В до полного расслаивания анода. При 2 В плотность тока составляла 1.1 мА мм–2, при 4 В – 4 мА мм–2, при 6 В – 8.4 мА мм–2, при 8 В – 12.7 мА мм–2, при 10 В – 17.8 мА мм–2 соответственно. В процессе синтеза цвет электролита постепенно менялся от прозрачного через светло-желтый и коричневый до темно-коричневого. Полученный образец ECGO подвергали ультразвуковой обработке в течение 30 мин для увеличения выхода по тонкослойным частицам. Затем полученную суспензию центрифугировали со скоростью 3000 об. мин–1 для удаления не полностью расслоившегося продукта. Для отделения частиц ECGO по латеральному размеру (нм от мкм) золь подвергали центрифугированию со скоростью 9000 об. мин–1. Завершающим этапом очистки продукта был диализ в воде в течение 10 дней.
Толщину частиц ECGO и их латеральный размер определяли методом атомно-силовой микроскопии (АСМ) с использованием сканирующего зондового микроскопа MultiMode SPM со сканирующим модулем MMAFM-2 и контроллером NanoScope-IIIa (США) в режиме “tapping mode” с кантилеверами производства NanoWorld (Швейцария).
Определение морфологии и кристаллической структуры графеноподобных частиц проводили методом просвечивающей электронной микроскопии (ПЭМ) на приборе JEM-2010 (JEOL, Япония).
Содержание дефектов и степень окисленности образцов изучали методом спектроскопии комбинационного рассеяния (КР). КР-спектры регистрировали с помощью спектрометра Renishaw InVia (Великобритания), используя аргоновый лазер с длиной волны 633 нм и мощностью 20 мВт. Анализ полученных данных проводили при помощи программного обеспечения Wire 3.4 Renishaw (Великобритания). Спектры были обработаны сверткой функций Гаусса и Лоренца для определения интенсивностей пиков G и D.
Для качественного сравнения степени окисленности частиц ECGO использовали спектрометр UVmini-1240 (Shimadzu, Япония). Нормировку спектров проводили относительно максимума поглощения в спектре образца.
Элементный состав для образцов ECGO, полученных при напряжении 6 В, определяли методом рентгеновской фотоэлектронной спектроскопии (РФЭС) с использованием спектрометра ESCALAB Xi+ (Thermo Fisher Scientific, США). Пики аппроксимировали сверткой функций Гаусса и Лоренца (pseudo-Voigt) с одновременной оптимизацией параметров фона. Оптимизацию параметров фона осуществляли по алгоритму Ширли.
На основании результатов обработки изображений АСМ (рис. 1) можно сделать вывод, что при изменении напряжения от 2 до 6 В латеральный размер частиц значительно возрастает от нанометровых до микрометровых значений, а толщина уменьшается от нескольких до одного нм. При дальнейшем повышении напряжения до 10 В размер частиц снижается до сотен нм, а толщина увеличивается вплоть до десятков нм. Также стоит отметить, что в результате значительного изменения морфологии частиц при различных напряжениях были введены их наименования. Так, при напряжении 2 В все полученные частицы имеют латеральный размер менее 200 нм, поэтому данный тип ECGO соответствует нанофракции. При 10 В кроме наночастиц также преимущественно образуются материалы с латеральным размером в диапазоне от 200 до 1000 нм, поэтому данная фракция является промежуточной. При 6 В максимален вклад микрофракции. При 4 и 8 В не наблюдалось преобладания фракции частиц определенного размера. Для данных напряжений характерна эквивалентная по массовому содержанию смесь частиц нано- и промежуточной фракций (табл. 1). Таким образом, наиболее информативными в плане распределения частиц по размерам являются результаты при 2, 6 и 10 В, позволяющие получить наибольший по величине выход частиц определенной морфологии.
Рис. 1.
Данные АСМ и результаты их обработки по толщине и латеральному размеру на основании анализа многих АСМ изображений для частиц ECGO, полученных в электролите на основе фталевой кислоты при напряжениях 2 В (левая колонка), 6 В (центральная колонка) и 10 В (правая колонка).
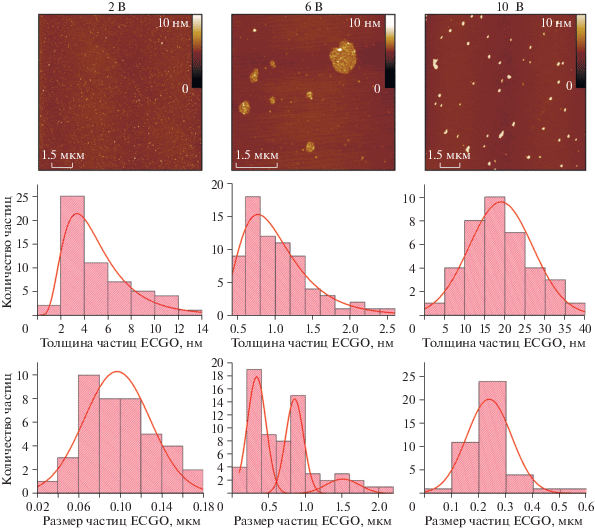
Таблица 1.
Выход частиц ECGO различной морфологии
| Напряжение, В | Выход ECGO, масс. % | Содержание нанофракции (<200 нм), мас. % | Содержание промежуточной фракции (200 нм < d < < 1000 нм), мас. % | Содержание микрофракции (>1 мкм), мас. % |
|---|---|---|---|---|
| 2 | 56 | 100 | – | – |
| 4 | 58 | 45 | 46 | 9 |
| 6 | 67 | 20 | 17 | 63 |
| 8 | 63 | 43 | 45 | 12 |
| 10 | 64 | 38 | 62 | – |
Данные изменения морфологии с ростом рабочего напряжения можно объяснить накоплением энергии упругой деформации в граничащих с электролитом графитовых слоях в процессе их окисления и, как следствие, изгибания (рис. 2). Таким образом, при подведении избыточной внешней энергии к рабочему электроду при высокой разности потенциалов за счет высокоэффективного электролиза происходит одновременное трещинообразование нескольких графитовых листов с последующей диффузией кислорода и кислородных радикалов в глубь графитового анода и дальнейшим отслаиванием частиц с большим количеством слоев.
Пренебрегая выделением тепла, можно считать, что энергия деформации может расходоваться на увеличение межслоевого расстояния между листами и трещинообразование [13]:
где Eтрещ – энергия образования трещин (∼1.26 × × 10–2 Дж м–2), ∆Eмеж – энергия изменения межслоевого пространства, Едеф – энергия упругой деформации. Значения энергии увеличения расстояния между слоями в литературе оцениваются изменением энергии разрыва ван-дер-ваальсовых связей и составляют ∼1 × 10–4 Дж м–2, что значительно ниже энергии образования трещин. Однако слабые органические кислоты, используемые в качестве электролита, препятствуют расширению межслоевого пространства, так как осаждаются на поверхности графитового анода в молекулярной форме [12]. Поэтому диффузия внутрь анода кислорода, выделяющегося в процессе электролиза, затрудняется, о чем свидетельствует отсутствие изменения объема рабочего электрода. Это подтверждает, что процесс увеличения расстояния между графитовыми слоями становится энергетически затруднен, в связи с чем вероятность процесса как образования трещин, так и окисления на поверхности анода существенно возрастает. Так, при 2 В происходит слабое окисление листов, что приводит к их небольшому изгибанию. Поэтому соответствующая энергия деформации способна приводить к образованию только низкоэнергетических трещин небольшого размера, которые и ограничивают размер получаемых частиц до 200 нм. Данной энергии деформации листа также недостаточно для значительного увеличения межслоевого пространства, и, как следствие, отслаивания однослойных частиц. Поэтому через образовавшиеся трещины электролит проникает в глубь графита, что способствует расслаиванию электрода с образованием многослойных частиц. Толщина образующихся частиц составила ∼5 нм (рис. 1, левая колонка). При 6 В энергии деформации уже достаточно для образования крупных трещин, что способствует получению микрометровых частиц. Данной энергии также достаточно, чтобы повлиять на величину межслоевого пространства, на что указывает уменьшение толщины частиц вплоть до ∼1 нм (рис. 1, центральная колонка). При 10 В происходит высоко интенсивное выделение кислорода и радикалов на его основе ввиду окисления воды, что вызывает значительное накопление энергии деформации и растрескивание графитовых листов на относительно маленькие частицы с латеральным размером до 500 нм. Данная энергия деформации листов настолько велика, что приводит к значительному повышению толщины частиц вплоть до ∼20 нм (рис. 1, правая колонка). Таким образом, напряжение 6 В является оптимальным для получения микрочастиц с минимальной толщиной и наибольшим латеральным размером, что актуально для многих технических и научных применений.После изучения различий в морфологии частиц ECGO в зависимости от условий синтеза был определен как общий выход продукта, так и выход по определенным размерам частиц (табл. 1). Как видно из данных АСМ (рис. 1), ECGO после синтеза при напряжении в 6 В имеет композитную микроструктуру, содержащую нано-, микро- и промежуточную фракции. Для оценки выхода реакции по каждому типу частиц они были разделены центрифугированием. Полученные результаты подтверждают, что использование напряжения 6 В позволяет получить максимальный выход по микрочастицам (63 мас. %). При этом содержание нанофракции ≥20 мас. % характерно для всех образцов.
По результатам ПЭМ (рис. 3а) графеноподобный продукт, полученный электрохимическим расслаиванием при напряжении 6 В, имеет наименьшую толщину частиц, при этом дифракция электронов указывает на характерную для графена гексагональную кристаллическую структуру. Согласно литературным данным [14] для графена наибольшая интенсивность дифракционной картины характеризуется (0 – 1 1 0) плоскостью. Для многослойного графена, наоборот, возрастает интенсивность для (0 – 2 1 0) плоскости. Соотношение данных интенсивностей показывает, что полученные частицы ECGO <3 слоев преимущественно, что согласуется с данными АСМ.
Рис. 3.
ПЭМ-изображения продукта, полученного при 6 В (а), и спектры комбинационного рассеяния частиц ECGO различного латерального размера, полученных при напряжениях 2 В (micro 2V PTA) и 6 В (micro 6V PTA и nano 6V PTA) (б).
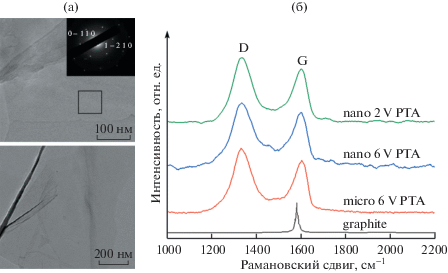
Для графита, оксида графита и оксида графена характерны разные спектры комбинационного рассеяния. Так, в спектре графита G-мода (1580 см–1) существенно выше D-моды (1350 см–1), для оксида графита и оксида графена характерны равнозначные по величине моды G (1580 см–1) и D (1350 см–1), что указывает на разрушение кристаллической структуры графита в процессе окисления (рис. 3б). В результате обработки КР-спектров (рис. 3б) было установлено, что в процессе получения ECGO с увеличением рабочего напряжения возрастает степень дефектности и окисленности полученного продукта, на что указывает рост соотношения ID/IG (табл. 2). Также при одном значении рабочего напряжения (6 В) соотношение ID/IG выше для наночастиц, чем микрочастиц, что свидетельствует о более высокой степени окисленности и большем содержании дефектов для частиц с меньшим латеральным размером.
Таблица 2.
Соотношения интенсивностей ID/IG спектров комбинационного рассеяния ECGO
| Электролит | Напряжение, В | ID/IG наночастиц | ID/IG микрочастиц |
|---|---|---|---|
| PTA | 2 | 1.2 | – |
| 6 | 1.4 | 1.2 | |
| 10 | 1.5 | – |
Согласно полученным данным (рис. 4а), для всех спектров характерен ярко выраженный пик поглощения около 275 нм, типичный для n–π*-перехода в ароматической связи С=С. Вклад адсорбционного пика ∼231 нм, который соответствует переходу π–π* одинарных связей С–С, падает для нанофракции при переходе от 6 к 2 В, а также при переходе от нано- к микрофракции для 6 В. Это указывает на более высокую окисленность и дефектность наночастиц, что согласуется с результатами КР-спектроскопии. Также отсутствие явно выраженного пика поглощения около 300 нм, характерного для переходов n–π* связей С=О, показывает, что все синтезированные образцы содержат малое количество карбонильных и карбоксильных групп, и, следовательно, характеризуются более низкой степенью окисленности в сравнении с химическим оксидом графена.
Рис. 4.
Спектры поглощения в УФ-видимой области золей на основе частиц ECGO, полученных при напряжениях 2 В и 6 В (а), и РФЭ-спектр C1s ECGO, содержащего смесь нано- и микрочастиц ECGO, полученных при 6 В (б).
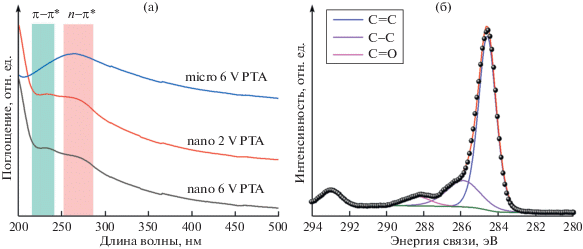
В результате разложения РФЭ-спектра на компоненты C1s-спектра (рис. 4б) можно сделать вывод, что образцы ECGO содержат атомы углерода в sp2-гибридизации (284.8 эВ), а также в виде эпоксидных/гидроксильных (286.6 эВ) и карбонильных/карбоксильных (288.8 эВ) групп. При этом для смеси микро- и нанофракций соотношение C/O ниже, чем для микрочастиц отдельно (табл. 3), что указывает на более высокую степень окисленности наночастиц. Это согласуется с результатами КР-спектроскопии и спектрофотометрии. Важно отметить, что для ECGO значения C/O значительно выше (>7), чем для оксида графена, синтезированного методом Хаммерса (С/O ∼ 2). Это указывает на низкую степень окисленности продукта, в результате чего данные частицы можно использовать в качестве проводящей добавки без дополнительного восстановления, в отличие от оксида графена, полученного химическим методом.
Таблица 3.
Соотношение С/O для ECGO на основании данных элементного РФЭС-анализа
| Электролит | Напряжение, В | Состав частиц | С/O |
|---|---|---|---|
| PTA | 6 | микро- и нано- | 7.8 |
| 6 | микро- | 8.7 |
В результате проделанной работы впервые продемонстрировано влияние параметров одностадийного электрохимического синтеза на состав и морфологию конечного графеноподобного материала. Варьирование рабочего напряжения позволило синтезировать микро- (с латеральным размером >1 мкм), наночастицы (с латеральным размером <200 нм) и композитный материал на их основе, контролировать слойность и степень окисленности полученных углеродных частиц. Оптимальная величина разности потенциалов составила 6 В. При ее приложении удалось достичь максимального выхода продукта (67 мас. %) малой толщины (1–3 нм). Это позволяет относительно недорогим способом получать графеноподобные частицы с контролируемыми физико-химическими свойствами, что значительно расширяет спектр применений ECGO.
Список литературы
Park S., Ruoff R.S. // Nat. Nanotechnol. 2009. V. 4. P. 217–224. https://doi.org/10.1038/nnano.2009.58
Wang G., Wang B., Park J., Yang J., Shen X., Yao J. // Carbon. 2009. V. 47. № 1. P. 68–72. https://doi.org/10.1016/j.carbon.2008.09.002
Petukhov D.I., Chernova E.A., Kapitanova O.O., Boytsova O.V., Valeev R.G., Chumakov A.P., Konovalov O.V., Eliseev A.A. // J. Memb. Sci. 2019. V. 577. P. 184–194. https://doi.org/10.1016/j.memsci.2019.01.041
Petukhov D.I., Kapitanova O.O., Eremina E.A., Goodi-lin E.A. // Mendeleev Commun. 2021. V. 31. № 2. P. 137–148. https://doi.org/10.1016/j.mencom.2021.03.001
Kapitanova O.O., Emelin E.V., Dorofeev S.G., Evdokimov P.V., Panin G.N., Lee Y., Lee S. // J. Mater. Sci. Technol. 2020. V. 38. P. 237–243. https://doi.org/10.1016/j.jmst.2019.07.042
Jiao X., Liu Y., Li T., Zhang C., Xu X., Kapitanova O.O., He C., Li B., Xiong S., Song J. // ACS Appl. Mater. Interfaces. 2019. V. 11. № 34. P. 30858–30864. https://doi.org/10.1021/acsami.9b08915
Nishina Y., Eigler S. // Nanoscale. 2020. V. 12. № 24. P. 12731–12740. https://doi.org/10.1039/d0nr02164d
Abdelkader A.M., Cooper A.J., Dryfe R.A.W., Kin-loch I.A. // Nanoscale. 2015. V. 7. № 16. P. 6944–6956. https://doi.org/10.1039/C4NR06942K
Ambrosi A., Pumera M. // Chem. Eur. J. 2016. V. 22. № 1. P. 153–159. https://doi.org/10.1002/chem.201503110
Liu J., Yang H., Zhen S.G., Poh C.K., Chaurasia A., Luo J., Wu X., Yeow E.K.L., Sahoo N.G., Lin J., Shen Z. // RSC Adv. 2013. V. 3. № 29. P. 11745–11750. https://doi.org/10.1039/C3RA41366G
Cao J., He P., Mohammed M.A., Zhao X., Young R.J., Derby B., Kinloch I.A., Dryfe R.A.W. // J. Am. Chem. Soc. 2017. V. 139. № 48. P. 17446–17456. https://doi.org/10.1021/jacs.7b08515
Wang H.S., Tian S.Y., Yang S.W., Wang G., You X.F., Xu L.X., Li Q.T., He P., Ding G.Q., Liu Z., Xie X.M. // Green Chem. 2018. V. 20. № 6. P. 1306–1315. https://doi.org/10.1039/C7GC03345A
Pan S., Aksay I.A. // ACS Nano. 2011. V. 5. № 5. P. 4073–4083. https://doi.org/10.1021/nn200666r
Wang J., Manga K.K., Bao Q., Loh K.P. // J. Am. Chem. Soc. 2011. V. 133. № 23. P. 8888–8891. https://doi.org/10.1021/ja203725d
Дополнительные материалы отсутствуют.
Инструменты
Доклады Российской академии наук. Химия, науки о материалах



