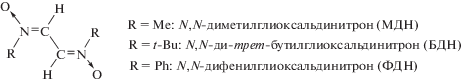Доклады Российской академии наук. Химия, науки о материалах , 2021, T. 501, № 1, стр. 5-13
Синтез и исследование теплофизических свойств полистиролов, полученных в присутствии сопряженных α-динитронов на основе глиоксаля
А. Б. Алыева 1, Е. В. Колякина 1, С. А. Стахи 1, С. С. Сологубов 1, А. В. Маркин 1, член-корреспондент РАН Д. Ф. Гришин 1, *
1 Национальный исследовательский Нижегородский государственный университет им. Н.И. Лобачевского
603950 Нижний Новгород, Россия
* E-mail: grishin@ichem.unn.ru
Поступила в редакцию 16.07.2021
После доработки 26.10.2021
Принята к публикации 01.11.2021
Аннотация
Предложен одностадийный конвергентный метод синтеза разветвленных макромолекул в присутствии сопряженных динитронов (N,N-диметилглиоксальдинитрона, N,N-ди-трет-бутилглиоксальдинитрона и N,N-дифенилглиоксальдинитрона) в условиях радикального инициирования. Установлено, что в отличие от линейных аналогов разветвленные макромолекулы полистирола, синтезированные с участием α-динитронов, характеризуются более низкими значениями температуры стеклования. Разработаны методики модификации полимеров, содержащих в своем составе алкоксиаминовые фрагменты, позволяющие повысить термостойкость синтезированных макромолекул.
В последние годы контролируемая радикальная полимеризация стала важным и надежным инструментом синтеза полимеров и макромолекулярного дизайна, органично сочетающим преимущества традиционной свободно-радикальной полимеризации и “живой” ионной полимеризации [1, 2]. При этом полимеризация с участием стабильных нитроксильных радикалов в условиях обратимого ингибирования относится к числу наиболее изученных и эффективных направлений контролируемого синтеза макромолекул (схема 1) [3, 4].
Один из вариантов проведения процесса обратимого ингибирования связан с формированием нитроксильных радикалов непосредственно в полимеризационной среде (in situ), в том числе с участием коммерчески доступных соединений, например, нитронов [4, 5]. Благодаря использованию этой методики, возможен синтез полимеров сложной топологии, включая дендритные, щетко- и звездообразные, а также гиперразветвленные [6–8], которые в ряде случаев существенно отличаются по химическим и физическим свойствам от их линейных аналогов [9].
Целью настоящей работы является синтез разветвленных полимеров на основе стирола, полученных с участием сопряженных динитронов (ДН) (рис. 1), а также сравнительный анализ теплофизических свойств указанных полимеров с их модифицированными и линейными аналогами.
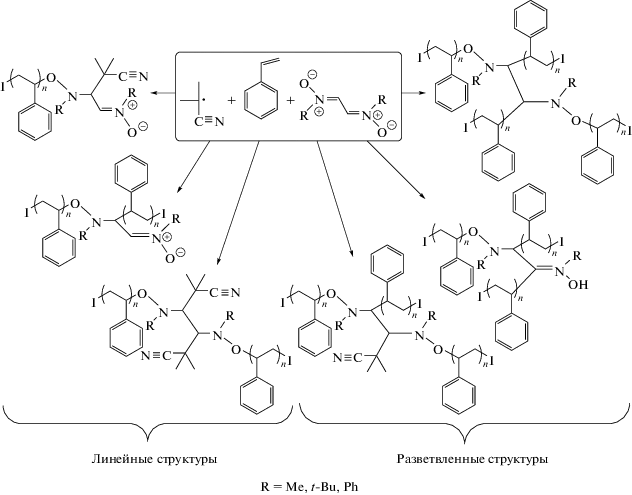
Синтез линейных и разветвленных образцов полистирола (ПС) с участием ДН проводили в широком температурном интервале 70−130°С в присутствии радикального инициатора динитрила азоизомасляной кислоты (ДАК). Подготовку образцов к полимеризации проводили в соответствии с прописью [10]. Показано, что ДН способны выступать в качестве регуляторов кинетики полимеризации и молекулярно-массовых характеристик (ММХ) полимеров. На первоначальном этапе полимеризации ДН акцептируют активные радикалы роста с образованием нитроксильных радикалов, которые в последующем выступают медиаторами полимеризации (схема 1). На возможность осуществления полимеризации в контролируемом режиме влияет не только структура ДН, но и температурные параметры процесса. Так, в случае наименее пространственно-затрудненного МДН наилучший контроль ММХ наблюдается при 130°С (табл. 1). Наличие в структуре ДН более объемных заместителей (БДН и ФДН) позволяет осуществлять процесс обратимого ингибирования и регулировать ММХ в более низкотемпературных режимах (табл. 1). Отличительной особенностью ДН является тот факт, что их структура позволяет синтезировать как линейные, так и разветвленные трех- и четырехлучевые полимеры (схема 2).
Таблица 1.
ММХ образцов ПС, синтезированных в присутствии 3 мол. % ДН и 1 мол. % ДАК, при различных температурах
| № пп | ДН | Т, °С | Время, ч | Конверсия, % | Mn × 10−3, кДа | Mw/Mn |
|---|---|---|---|---|---|---|
| 1 | МДН | 70 | 140 | 24 | 6.8 | 6.9 |
| 2 | 90 | 140 | 46 | 10.6 | 3.4 | |
| 3 | 130 | 24 | 87 | 13.5 | 1.7 | |
| 4 | БДН | 70 | 100 | 26 | 5.8 | 1.4 |
| 5 | 90 | 100 | 44 | 5.9 | 1.6 | |
| 6 | 130 | 73 | 76 | 7.4 | 2.4 | |
| 7 | ФДН | 70 | 63 | 99 | 35.4 | 2.3 |
| 8 | 90 | 80 | 80 | 14.0 | 2.1 | |
| 9 | 130 | 32 | 81 | 13.7 | 3.0 |
Для оценки конформации макромолекулы, а именно наличия разветвленной структуры, используют ряд гидродинамических параметров полимеров [11]. Наиболее распространенным из них является форм-фактор, характеризующий степень “асимметричности” макромолекулы в растворе. Форм-фактор определяется из соотношения диффузионного гидродинамического радиуса Rh − D и радиуса инерции Rg макромолекулы по формуле ρ = Rg/Rh − D. Для гауссова клубка линейного полимера в θ-растворителе ρ = 1.73, а в хорошем растворителе ρ = 2.05 [11]. В случае разветвленных структур указанный параметр уменьшается: для полидисперсных четырехлучевых звездообразных полимеров в θ-растворителе ρ = = 1.53. Увеличение числа лучей или разветвлений в макромолекуле приводит к еще большему снижению значения ρ.
Гидродинамические радиусы и Rg определяли методом светорассеяния. Рассчитанные значения форм-фактора для ПС, синтезированного с участием ДН в различных концентрациях, приведены в табл. 2. С теоретической точки зрения наиболее вероятно формирование более разветвленных структур при низкой концентрации ДН (0.5 мол. %). Действительно, в присутствии 0.5 мол. % МДН и ФДН значение форм-фактора близко к значению твердой сферы или высокоразветвленных полимеров (ρ = 0.778). Увеличение значения форм-фактора в случае избытка МДН и ФДН (3 мол. %) свидетельствует об образовании наряду с разветвленными структурами и линейных макромолекул (схема 2). В случае БДН разветвленные структуры образуются при более высокой концентрации – 3 мол. % (табл. 2). Указанный факт обусловлен стабильностью мононитроксильных радикалов (схема 3), полученных на основе БДН (1), которые способны распадаться с образованием 2-метил-2-нитрозопропана (МНП) и трет-бутилвинилнитроксилов (2) [12]. Наличие в системе МНП приводит к формированию макромолекул с линейной конформацией и увеличению значения ρ.
Таблица 2.
Гидродинамические характеристики ПС
| № | ДН (мол. %) | Mwа × 10−3, кДа | Rg, нм | Rh − D, нм | ρ = Rg/Rh − D |
|---|---|---|---|---|---|
| 1 | МДН (0.5) | 72.7 | 6.6 | 8.5 | 0.78 |
| 2 | МДН (3.0) | 38.8 | 8.4 | 6.1 | 1.38 |
| 3 | БДН (0.5) | 27.3 | 10.1 | 5.4 | 1.87 |
| 4 | БДН (1.5) | 26.0 | 8.8 | 5.4 | 1.65 |
| 5 | ФДН (0.5) | 49.6 | 9.0 | 9.0 | 0.96 |
| 6 | ФДН (3.0) | 33.1 | 9.6 | 6.5 | 1.48 |
В целом анализ гидродинамических характеристик показал, что разработанная методика синтеза ПС с участием ДН позволяет получать разветвленные трех- и четырехлучевые звездообразные полимеры.
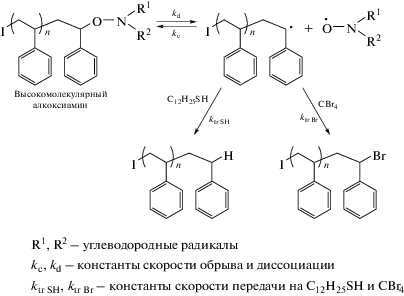
Наличие в составе полимеров, синтезируемых по механизму обратимого ингибирования, лабильных связей С–ON< может быть причиной ухудшения термической стабильности макромолекул [13]. С целью повышения стабильности полимеров нами предложена одностадийная методика модификации высокомолекулярных алкоксиаминов, синтезируемых на основе ДН, с участием CBr4 и меркаптана (C12H25SH) (схема 4). В процессе модификации происходит замена лабильного нитроксильного фрагмента на атомы брома и водорода соответственно. Энергия связи С–ON< в алкоксиамине составляет ~30 кДж моль–1, а для связей C–Br и C–H равна 293 и 435 кДж моль–1 соответственно [14, 15]. В этой связи, несомненно, следует ожидать повышения термической стабильности модифицированных макромолекул.
Экспериментальные данные подтвердили это предположение. Исследование термического поведения образцов полистирола, синтезированных в присутствии МДН и БДН, а также модифицированных полимеров проводили методом термогравиметрического анализа (ТГА) с использованием термомикровесов TG 209 F1 Netzsch Gerätebau (Германия) в атмосфере аргона в интервале температур 300–850 К. Средняя скорость нагрева тигля с веществом 5 K мин−1. Установлено, что для образцов ПС, полученных на основе БДН и модифицированных как в присутствии CBr4, так и меркаптана, потери массы наблюдаются при более высоких температурах (табл. 3).
Таблица 3.
ММХ и теплофизические свойства продуктов модификации ПС, синтезированного в присутствии 1 мол. % ДАК и 0.5 мол. % ДН
| № | ДН | Компоненты | Mn × 10–3, кДа | Mw/Mn | T10%,°С | T50%,°C | T90%,°C |
|---|---|---|---|---|---|---|---|
| 1 | МДН | Исходный | 7.1 | 1.7 | 343 | 381 | 405 |
| 2 | CBr4, C6H6 | 4.2 | 1.6 | 303 | 380 | 408 | |
| 3 | БДН | Исходный | 23.0 | 2.3 | 335 | 378 | 403 |
| 4 | CBr4, C6H6 | 14.6 | 2.9 | 358 | 390 | 413 | |
| 5 | C12H25SH, C6H6 | 17.5 | 2.4 | 363 | 393 | 416 |
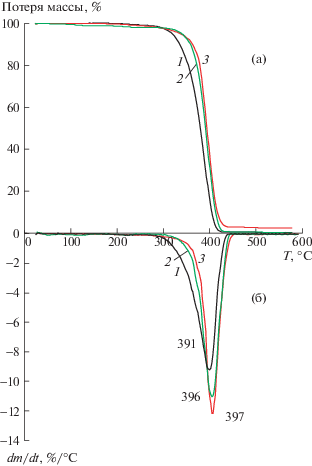
На примере образца ПС, полученного в присутствии БДН с Mn = 23 кДа, приведены полные интегральные – ТГА- (рис. 2а) и дифференциальные – ДТГ-термограммы (рис. 2б). Как следует из представленных данных, термическая стабильность ПС, модифицированного в присутствии CBr4 и меркаптана, значительно увеличилась, при этом максимальная скорость разложения ПС, синтезированного в присутствии ДН, достигалась при температуре 391°С. В случае модифицированных образцов максимальная скорость наблюдалась при более высокой температуре − 396 и 397°C.
Рис. 2.
ТГА (а) и ДТГ (б) кривые образца ПС с Mn = = 23 кДа, синтезированного в присутствии БДН (1) и модифицированного в присутствии CBr4 (2), C12H25SH (3).
При исследовании ПС, полученного в присутствии МДН, наблюдались идентичные закономерности стабилизации полимеров при их модификации в присутствии CBr4, а именно, повышение температуры 50- и 90%-й потери массы ПС (табл. 3). Однако температура 10%-й потери массы модифицированного образца значительно снижается. Вероятно, это связано с низкими значениями молекулярной массы (ММ) модифицированного продукта. Так, в работе [16] показано, что термическая стабильность полимеров зависит от ММ полимеров. Низкомолекулярные полимеры разлагаются в более широком интервале температур, при этом температура начала разложения полимера более низкая, но полное разложение достигается при более высокой температуре, по сравнению с высокомолекулярными образцами.
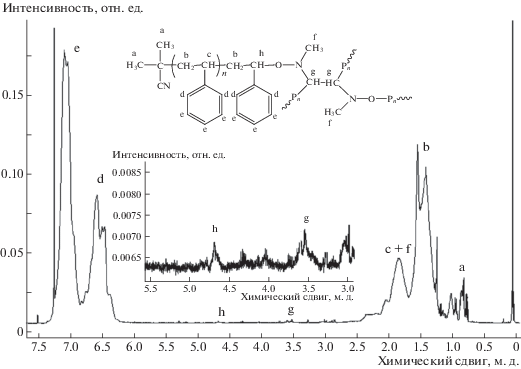
Кроме того, модификация синтезированных образцов ПС (3–7) с заменой нитроксильного фрагмента на атомы брома и водорода позволила установить структуры высокомолекулярных алкоксиаминов, синтезируемых in situ в процессе полимеризации (табл. 4). В случае ПС на основе ДН наблюдается снижение ММ образцов при модификации. Изменение ММ анализировали на основе средневесовой ММ (Mw) как наименее подверженной ошибке эксперимента. Указанный факт подтвердил образование высокомолекулярных алкоксиаминов, содержащих лабильные связи С–ON< внутри цепи. Доказательством присутствия в составе ПС алкоксиаминовых групп является наличие в спектре 1Н ЯМР образцов, синтезированных с участием исследуемых ДН, сигналов атомов водорода, связанных с алкоксиаминовым фрагментом. На рис. 3 представлен спектр 1Н ЯМР ПС, полученного в присутствии МДН. Пик (g) в области 3.5 м. д. относится к атомам водорода метинового фрагмента ДН, а сигналы (h), лежащие в области 4.5–4.7 м. д., характерны для атомов водорода метинового фрагмента стирола, непосредственно связанных с нитроксильной группой.
Таблица 4.
ММХ продуктов модификации ПС (3–7), синтезированных в присутствии 0.5 мол. % ДН и 1 мол. % ДАК. Время модификации: 90 и 110°С – 20 ч, 130°С – 7 ч
| № п.п. | Системаа | T, °C | Mw × 10−3, кДа | Mw/Mn | ∆Mw × 10−3, кДа |
|---|---|---|---|---|---|
| 1 | Исходный3, МДН, P = 24% | 90 | 9.3 | 2.5 | − |
| 2 | 3, CBr4, ТГФ | 130 | 5.5 | 1.5 | 3.8 |
| 3 | Исходный4, МДН, P = 43% | 90 | 47.2 | 4.5 | − |
| 4 | 4, CBr4, C6H6 | 130 | 30.6 | 3.6 | 17.0 |
| 5 | 4, C12H25SH, C6H6 | 130 | 36.1 | 3.5 | 11.1 |
| 6 | Исходный5, БДН, P = 44% | 90 | 14.8 | 1.7 | − |
| 7 | 5, CBr4, ТГФ | 130 | 12.5 | 1.6 | 2.3 |
| 8 | Исходный6, БДН, P = 67% | 90 | 20.5 | 1.9 | |
| 9 | 6, CBr4, C6H6 | 110 | 16.2 | 2.1 | 4.3 |
| 10 | 6, C12H25SH, C6H6 | 110 | 16.3 | 1.7 | 4.2 |
| 11 | Исходный7, ФДНб, P = 93% | 90 | 28.8 | 2.1 | − |
| 12 | 7, CBr4, C6H6 | 90 | 27.4 | 2.0 | 1.4 |
| 13 | 7, C12H25SH, C6H6 | 90 | 26.9 | 2.0 | 1.9 |
Рис. 3.
Спектр 1H ЯМР образца ПС (Mn = 3800 Да, Mw/Mn = 2.5), синтезированного в присутствии 3 мол. % МДН и 1 мол. % ДАК при Т = 90°С (на вставке – увеличенная область 3.0–5.5 м. д.). Регистрацию спектров проводили на спектрометре Agilent DD2 400 с рабочей частотой 400 МГц, растворитель CDCl3.
Отметим, что изменение значений ММ обоих осколочных фрагментов, образующихся при модификации образцов ПС различной конверсии, косвенно указывает на возможность получения звездообразных структур (табл. 4). Так, в случае МНД-содержащих ПС (3, 4) наблюдается изменение ММ обоих осколочных фрагментов (табл. 4, колонки Mw и ∆Mw, строки 2 и 4). Данный факт свидетельствует о формировании линейных полимеров на низких степенях превращения мономера и их преобразовании в ходе процесса в разветвленные структуры (схема 2). Аналогичные закономерности наблюдаются и в случае БДН-содержащего ПС – 5, 6 (табл. 4, колонки Mw и ∆Mw, строки 7 и 9).
Химический состав, строение цепи полимера, а также топология и наличие функциональных групп в составе макромолекул влияют на значения температур стеклования Тg [9, 17]. Наряду с вышеперечисленными факторами на Tg однотипных макромолекул существенное влияние оказывают и их ММХ [17]. Зависимость Tg от ММ макромолекул для узкодисперсных образцов описывается общепринятой эмпирической моделью Фокса и Флори (уравнение 1), а в случае полидисперсных полимеров − скорректированным уравнением 2 [18, 19]:
где Тg – абсолютная температура стеклования полимера данной ММ; Tg∞ – предельное значение температуры стеклования, которое достигается при бесконечно большой длине цепи; K – эмпирический параметр, связанный со свободным объемом в образце полимера [18].В связи с этим методом ДСК на приборе DSC 204 F1 Phoenix Netzsch Gerätebau (Германия) были определены значения Тg линейных и разветвленных ПС, которые синтезированы в присутствии 3 мол. % ДН и выделены на различных степенях превращения мономера (табл. 5). С целью исключения влияния ММХ на указанный параметр исследовались образцы в широком диапазоне ММ. Полученные данные представлены в табл. 5, а также на рис. 4, на котором приведены зависимости Tg от среднечисленной ММ (Mn) в различных координатах. Как и следовало ожидать, Tg для всех образцов увеличиваются с ростом Mn (рис. 4а). Причем ее значения для линейных образцов, синтезированных на ДАК, выходят на насыщение при Mn порядка 10 кДа, т.е. выше этих ММ можно считать, что термодинамические свойства ПС, в частности Tg, практически не зависят от ММ. Образцы, полученные с участием ДН с молекулярной массой до 10 кДа, характеризуются более низкими значениями Tg.
Таблица 5.
ММХ и Tg образцов ПС, синтезированных в присутствии 3 мол. % ДН и 1 мол. % ДАК
| № | ДН | T, °C | Mn × 10−3, кДа | Mw/Mn | Tg, °С | Tg∞а, °С | Kа × 10−5, К г моль−1 | Tg∞б, °С | Kб × 10−5, К г моль−1 |
|---|---|---|---|---|---|---|---|---|---|
| 1 | − | 90 | 7.0 | 2.7 | 94 | 112 | 1.28 | 110 | 1.65 |
| 2 | 8.4 | 2.3 | 95 | ||||||
| 3 | 8.9 | 3.7 | 98 | ||||||
| 4 | 9.5 | 1.8 | 99 | ||||||
| 5 | 12.4 | 2.6 | 103 | ||||||
| 6 | 17.6 | 3.7 | 105 | ||||||
| 7 | МДН | 130 | 7.5 | 3.0 | 88 | 111 | 1.73 | 105 | 1.74 |
| 8 | 9.8 | 2.7 | 92 | ||||||
| 9 | 12.5 | 1.9 | 98 | ||||||
| 10 | 13.5 | 1.7 | 97 | ||||||
| 11 | БДН | 90 | 5.4 | 1.6 | 85 | 110 | 1.43 | 107 | 1.67 |
| 12 | 6.3 | 1.6 | 86 | ||||||
| 13 | 7.1 | 1.6 | 90 | ||||||
| 14 | 7.9 | 1.6 | 93 | ||||||
| 15 | 9.2 | 1.7 | 95 | ||||||
| 16 | ФДН | 90 | 9.5 | 1.7 | 74 | 107 | 2.87 | 105 | 3.71 |
| 17 | 11.5 | 1.8 | 79 | ||||||
| 18 | 14.2 | 2.1 | 91 | ||||||
| 19 | 15.0 | 2.1 | 92 | ||||||
| 20 | 15.9 | 2.1 | 92 |
а Tg∞, K – рассчитаны по уравнению (1), бTg∞, K – рассчитаны по уравнению (2).
Рис. 4.
Зависимость Tg образцов ПС от Mn: точки – экспериментальные результаты; сплошные кривые – результаты, вычисленные по уравнению (1) (а). Зависимость Tg образцов ПС от 1/Mn (б). Условия синтеза ПС приведены в табл. 5. 1 – в отсутствие ДН, 2 – МДН, 3 – БДН, 4 – ФДН.
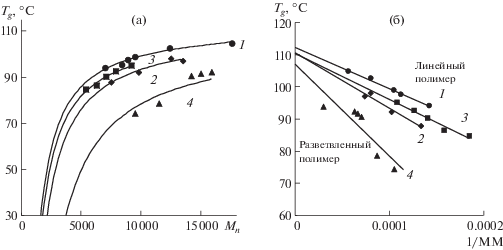
Значения Tg∞ и K определяли исходя из линейной зависимости Tg от 1/Mn или 1/(Mn × Mw)0.5 соответственно (табл. 5). Как видно из таблицы, Tg∞ как для линейных, так и разветвленных образцов лежат в интервале 107–112°С. Отметим, что значения Tg∞, рассчитанные по уравнению (2), несколько ниже по сравнению с параметрами, рассчитанными по уравнению Флори−Фокса, и более соответствуют литературным данным по температурам стеклования ПС, определенным различными методами [17, 19].
О кинетической гибкости цепи полимера можно судить по ММ, при которой кривая функции Tg = f(Mn) выходит на плато, т.е. достигается предельная температура стеклования Tg∞ [20]. Полимеры с разветвленной конформацией имеют большее количество концов цепей, следовательно, более подвижные сегменты при одной и той же ММ [20]. Так, ММ, при которой Tg∞ достигает постоянного значения для линейного ПС, синтезированного в условиях традиционной радикальной полимеризации, составляет около 10 кДа (рис 4, табл. 5). Разветвленные образцы ПС, синтезированные с участием ДН, обладают большей кинетической гибкостью цепи и, как следствие, более низкими Tg и более высокими ММ, при которых достигается Tg∞: для МДН и БДН это 13 кДа, а для ФДН – 14 кДа (рис. 4). В целом анализ Tg ПС, синтезированных с участием ДН глиоксалевого ряда, дополнительно подтверждает возможность синтеза полимеров с разветвленной структурой.
ЗАКЛЮЧЕНИЕ
Предложена методика синтеза и модификации полистирола, содержащего в своем составе алкоксиаминовые фрагменты, которая позволяет повысить термостойкость макромолекул. Сравнительный анализ теплофизических свойств линейных образцов полистирола и разветвленных макромолекул, полученных в присутствии динитронов глиоксалевого ряда, показал, что звездообразные макромолекулы характеризуются более низкими значениями температуры стеклования.
Список литературы
Grishin D.F., Grishin I.D. // Russ. Chem. Rev. 2021. V. 90. P. 231−264. https://doi.org/10.1070/RCR4964
Corrigan N., Jung K., Moad G., Hawker C.J., Matyjaszew-ski K., Boyer C. // Prog. Polym. Sci. 2020. V. 111. P. 101311. https://doi.org/10.1016/j.progpolymsci.2020.101311
Lamontagne H.R., Lessard B.H. // ACS Appl. Polym. Mater. 2020. V. 2. № 12. P. 5327–5344. https://doi.org/10.1021/acsapm.0c00888
Kolyakina E.V., Grishin D.F. // Russ. Chem. Rev. 2009. V. 78. № 6. P. 535−568. https://doi.org/10.1070/RC2009v078n06ABEH004026
Sciannamea V., Jérôme R., Detrembleur C. // Chem. Rev. 2008. V. 108. № 3. P. 1104−1126. https://doi.org/10.1021/cr0680540
Xia K., Rubaie A.J., Johnson B.P., Parker S.A., Till- man E.S. // J. Polym. Sci., Part A: Polym. Chem. 2019. V. 57. № 20. P. 2113−2120. https://doi.org/10.1002/pola.29482
Blackburn C.S., Myers K.D., Tillman E.S. // Polymer. 2015. V. 68. P. 284−292. https://doi.org/10.1016/j.polymer.2015.05.021
Kolyakina E.V., Shoipova F.H., Alyeva A.B., Grishin D.F. // Russ. Chem. Rev. 2021. V. 70. № 9. P. 1736−1745. https://doi.org/10.1007/s11172-021-3278-0
Luo X., Xie S., Huang W., Dai B., Lu Z., Yan D. // Chin. J. Polym. Sci. 2016. V. 34. № 1. P. 77–87. https://doi.org/10.1007/s10118-016-1730-7
Kolyakina E.V., Alyeva A.B., Sazonova E.V., Zakharychev E.A., Grishin D.F. // Polym. Sci., Ser. B. 2020. V. 62. № 4. P. 328−342. https://doi.org/10.1134/S1560090420040077
Burchard W. Adv. Polym. Sci. 1999. V. 143. P. 113−194. https://doi.org/10.1007/b136243
Rehorek D., Janzen E.G. // J. Prakt. Chem. 1985. V. 327. P. 968−982. https://doi.org/10.1002/prac.19853270615
Roland I., Schmidt-Naake G. // J. Anal Appl. Pyrolysis. 2001. V. 58−59. P. 143−154. https://doi.org/10.1016/S0165-2370(00)00158-3
Megiel E., Kaim A., Cyrański M. // J. Phys. Org. Chem. 2010. V. 23. № 12. P. 1146−1154. https://doi.org/10.1002/poc.1685
Bibiao J., Jianbo F., Yang Y., Qiang R., Wenyun W., Jianjun H. // Eur. Polym. J. 2006. V. 42. № 1. P. 179–187. https://doi.org/10.1016/j.eurpolymj.2005.07.016
Nishizaki H., Yoshida K. // J. Appl. Polym. Sci. 1981. V. 26. № 10. P. 3503–3504. https://doi.org/10.1002/app.1981.070261029
Smirnova N.N., Kolyakina E.V., Kulagina T.G., Gri-shin D.F. // Russ. Chem. Bull. 2013. V. 62. № 10. P. 2251–2257.https://doi.org/10.1007/s11172-013-0325-5
Fox T.G., Flory P.J. // J. App. Phys. 1950. V. 21. № 6. P. 581–591. https://doi.org/10.1063/1.1699711
Alhilfi T., Chambon P., Rannard S.P. // J. Polym. Sci. 2020. V. 58. № 10. P. 1426–1438. https://doi.org/10.1002/pol.20200143
Huang W., Gu W., Yang H., Xue X., Jiang B., Zhang D., Fang J., Chen J., Yang Y., Guo J. // Polymers. 2017. V. 9. № 1. P. 14–24. https://doi.org/10.3390/polym9010014
Дополнительные материалы отсутствуют.
Инструменты
Доклады Российской академии наук. Химия, науки о материалах