Доклады Российской академии наук. Химия, науки о материалах , 2022, T. 507, № 1, стр. 68-74
Утилизация ацетона – побочного продукта кумольного производства фенола – альдольной конденсацией на катализаторе BaSnO3
Т. В. Богдан 1, 2, *, П. А. Красников 2, А. В. Смирнов 1, 2, А. Е. Коклин 1, Н. В. Мащенко 1, В. И. Богдан 1, 2
1 Федеральное государственное бюджетное
учреждение науки Институт органической химии
им. Н.Д. Зелинского Российской академии наук
119991 Москва, Россия
2 Федеральное государственное бюджетное образовательное учреждение высшего образования “Московский государственный университет
имени М.В. Ломоносова”, Химический факультет
119991 Москва, Россия
* E-mail: chemist2014@yandex.ru
Поступила в редакцию 08.07.2022
После доработки 19.08.2022
Принята к публикации 21.09.2022
- EDN: FWUDDO
- DOI: 10.31857/S2686953522600489
Аннотация
Проведена альдольно-кротоновая конденсация ацетона в сверхкритических условиях – при температуре 300–400°С и давлении 11.0 МПа – на катализаторах BaSnO3-450 и BaSnO3-750, полученных прокаливанием BaSn(OH)6 при 450°С и 750°С соответственно. Показано, что проведение реакции в данных условиях позволяет преодолеть проблему дезактивации катализатора продуктами уплотнения и получать ценные химические вещества с высокой селективностью. При 300°С оба катализатора обладают селективностью 85–87% по изомерным окисям мезитила (продукты С6). При 400°С на катализаторе BaSnO3-450 происходит значительное изменение селективности от С6 к С9 (форонам). Данные РФА и ПЭМ указывают на полифазность образцов: станнаты бария, карбонат бария, оксид олова. Установлено, что in situ происходит перестройка структуры катализаторов, что в значительной степени влияет на их каталитические свойства и наиболее выражено для BaSnO3-450.
ВВЕДЕНИЕ
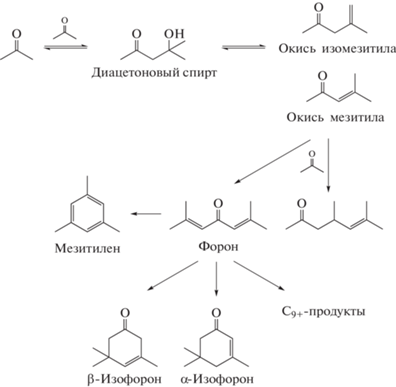
Ацетон является стехиометрическим побочным продуктом кумольного метода получения фенола. Проводя реакцию самоконденсанции ацетона (рис. 1), мы можем получить ценные для промышленности вещества: окиси мезитила и изомезитила, которые являются продуктами конденсации двух молекул ацетона (продукты С6), а также форон и изофороны, которые образуются в результате конденсации трех молекул ацетона (продукты С9). В классическом варианте альдольно-кротоновая конденсация ацетона идет в присутствии значительных количеств гомогенных катализаторов – щелочных растворов NaOH, KOH, Ca(OH)2 [1]. Реализация процесса в таком варианте создает большие экологические проблемы, связанные с утилизацией отработанных щелочных растворов. Развитие современной химической промышленности направлено на создание экологически чистых эффективных гетерогенно-каталитических процессов. В качестве альтернативного и более экологически безопасного процесса для реакции альдольно-кротоновой конденсации ацетона также используют гетерогенные катализаторы: оксид магния и смешанные оксиды Mg–Al и Mg–Zr [1]. Недостатком таких катализаторов является их быстрая дезактивация.
Рис. 1.
Схема конденсации ацетона. Продукты С6: окиси мезитила и изомезитила. Продукты С9: мезитилен, форон и изофороны. Продукты С9+: соединения с числом атомов углерода более 9, в том числе кислородсодержащие.
В настоящее время одним из подходов к решению проблемы закоксовывания гетерогенного катализатора является использование сверхкритических флюидов как в качестве реагентов, так и в качестве среды проведения реакции [2]. Критические параметры ацетона (Tкр = 235.5°С, Pкр = = 4.7 МПа) и продукта его конденсации – окиси мезитила (Tкр = 249°С, Pкр = 4.7 МПа) – при умеренных конверсиях позволяют рассматривать нахождение всей каталитической системы в сверхкритических условиях (300–400°С и 11.0 МПа). Ранее мы в работах [3–6] провели конденсацию ацетона на твердоосновных катализаторах – станнатах магния, кальция и стронция. Катализаторы показали высокую активность и стабильную работу при проведении реакции в сверхкритическом состоянии реагента, по сравнению с газовой фазой [3, 4].
В настоящей работе реакция альдольно-кротоновой конденсации ацетона проведена при температуре 300–400°С и давлении 11.0 МПа с использованием станната бария ВаSnO3 в качестве твердоосновного катализатора.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Синтез катализатора ВаSnO3. Методика синтеза образцов BaSnO3 аналогична описанной ранее для синтеза станната стронция [3]. Образцы катализатора ВаSnO3 синтезировали по следующей схеме:
На первом этапе был получен гексагидроксистаннат бария путем добавления гидроксида натрия к эквимолярным количествам солей олова и бария. Полученный осадок BaSn(OH)6 сушили на воздухе при 120°C в течение 8 ч. На второй стадии для получения метастанната бария образец BaSn(OH)6 прокаливали в муфельной печи на воздухе при температурах 450 и 750°C в течение 4 ч. Полученные образцы далее обозначены как BaSnO3-450 и BaSnO3-750.
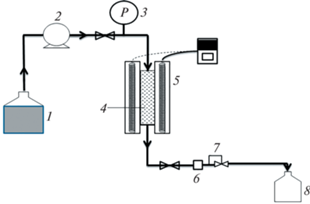
Каталитический эксперимент. Каталитический эксперимент был проведен в трубчатом реакторе проточного типа из нержавеющей стали (внутренний диаметр 4 мм). Схема каталитической установки приведена на рис. 2. Катализатор массой 0.20 г (размер частиц 0.14–0.25 мм) помещали в центр реактора, оставшийся объем заполняли кварцевым песком. Скорость подачи ацетона составляла 0.25 мл мин–1, что соответствует 59 г ч–1 г$_{{{\text{кат}}}}^{{ - 1}}$. Нагрев реактора осуществляли в токе ацетона. Продукты реакции собирали в ловушке (пробы отбирали каждые 30 мин), и далее анализировали на газовом хроматографе Хроматэк Кристалл-5000 (Россия) с капиллярной колонкой Thermo TR-5MS (США). Идентификацию продуктов проводили методом хромато-масс-спектрометрии с использование прибора Thermo Focus GC DSQ II (США) с капиллярной колонкой Thermo TR-5MS.
Рис. 2.
Схема каталитической установки: емкость с ацетоном (1), насос (2), манометр (3), реактор (4), печь (5), фильтр (6), клапан обратного давления (7), ловушка (8).
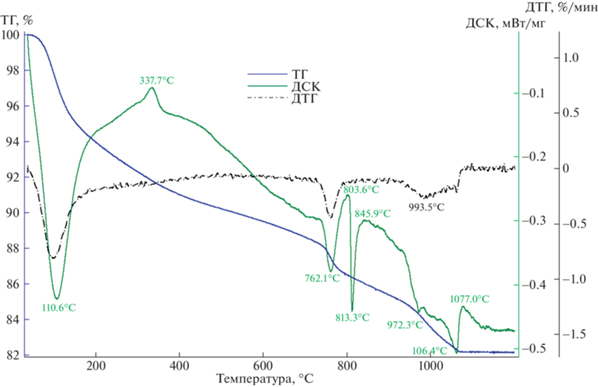
Исследование структуры катализаторов. Анализ исходного гексагидроксистанната бария BaSn(OH)6 проводили методом термогравиметрии и дифференциальной сканирующей калориметрии (ДСК) на приборе NETZSCH STA 409 PC/PG. Регистрацию кривых проводили со скоростью нагревания 10 град мин–1 в режиме непрерывного линейного нагрева.
Рентгенофазовый анализ (РФА) был выполнен на дифрактометре ДРОН-2 (CuKα-излучение, скорость вращения гониометра 2 град мин–1, диапазон съемки по 2θ от 10° до 70°).
Анализ методом просвечивающей электронной микроскопии (ПЭМ) высокого разрешения проводили на электронном микроскопе JEOL-2100F (Япония) в режимах светлого и темного полей при ускоряющем напряжении 200 кВ. Определение фазового состава катализатора проводили путем анализа данных ПЭМ, полученных в режиме дифракции и сопоставлением их со справочными данными [7].
ОБСУЖДЕНИЕ РЕЗУЛЬТАТОВ
Установлено, что конверсия ацетона для образца BaSnO3-450 выше, чем для BaSnO3-750, при этом за время наблюдения конверсия незначительно уменьшается (табл. 1). При 300°С на BaSnO3-450 конверсия составляет 10–12%, тогда как на BaSnO3-750 – порядка 5–8%. При 400°C конверсия возрастает до 46% на BaSnO3-450 и до 34% на BaSnO3-750.
Таблица 1.
Результаты каталитического эксперимента для катализаторов BaSnO3-450 и BaSnO3-750
| Время, мин | Условия | Конверсия, % | Селективность, % | ||
|---|---|---|---|---|---|
| С6а | С9б | С9+в | |||
| BaSnO3‑450 | |||||
| 60 | 300°С 11 МПа |
12 | 87 | 5 | 8 |
| 90 | 11 | 85 | 5 | 10 | |
| 120 | 10 | 85 | 5 | 10 | |
| 60 | 400°С 11 МПа |
46 | 37 | 36 | 27 |
| 90 | 45 | 42 | 37 | 21 | |
| 120 | 42 | 48 | 35 | 17 | |
| BaSnO3-750 | |||||
| 60 | 300°С 11 МПа |
7 | 87 | 5 | 8 |
| 90 | 5 | 85 | 4 | 11 | |
| 120 | 5 | 85 | 4 | 11 | |
| 60 | 400°С 11 МПа |
34 | 62 | 27 | 11 |
| 90 | 25 | 77 | 17 | 6 | |
| 120 | 20 | 77 | 16 | 7 | |
Для наглядности на рис. 3 представлены данные сравнения по селективности и конверсии ацетона на разных катализаторах при разных температурах для времени реакции 90 мин. Для образцов BaSnO3-450 и BaSnO3‑750 селективность по изомерным окисям мезитила достигает 87% при 300°C. При 400°С селективность по окиси мезитила для BaSnO3-750 снижается до 77% с увеличением селективности по форонам до 17%. При 400°C для BaSnO3‑450 заметно растет селективность по форонам – до 36%, и падает селективность по окисям мезитила.
Рис. 3.
Селективность (а) и конверсия (б) реакции альдольной конденсации ацетона на катализаторах BaSnO3-450 и BaSnO3-750 при 300 и 400°С и давлении 11.0 МПа, время реакции 90 мин.

Активность станната бария сопоставима с активностью ранее исследованного станната стронция [3] и существенно превосходит результаты, представленные в литературе. Так, при использовании одних из наиболее активных катализаторов – смешанных оксидных систем Mg–Al – удалось достичь конверсии ацетона 58–78%, однако скорость подачи ацетона была невысока – 1.2 г ч$_{{}}^{{ - 1}}$ г$_{{{\text{кат}}}}^{{ - 1}}$, а основным продуктом конденсации был изофорон [8]. Каталитические результаты для станната бария в настоящей работе получены при скорости подачи ацетона 59 г ч$_{{}}^{{ - 1}}$ г$_{{{\text{кат}}}}^{{ - 1}}$.
Синтезированный BaSn(OH)6 был охарактеризован термическими методами анализа (рис. 4). Первый пик при 110°C обусловлен потерей воды в ходе дегидратации образца. Постепенное образование метастанната бария из гидроксистанната BaSn(OH)6 происходит до температуры 802°C. При температуре 813°C происходит твердотельный фазовый переход: метастаннат бария BaSnO3 переходит в ортостаннат Ba2SnO4 с выделением фазы SnO2. Таким образом, в условиях приготовления катализатора при 750°C кристаллическая фаза метастанната бария может образоваться, а при 450°C – полностью сформироваться не может.
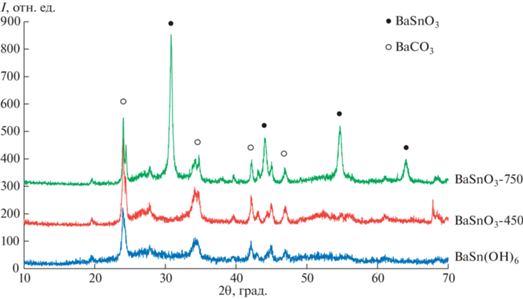
Рентгенофазовый анализ (рис. 5) для исходного BaSn(OH)6 и синтезированных образцов BaSnO3-450 и BaSnO3-750 согласуется с данными термического анализа. Для образца BaSnO3-750 установлено наличие кристаллической фазы метастанната бария, имеющего структуру перовскита. Для образца BaSnO3-450 кристаллическая фаза метастанната в объеме образца не сформировалась. Установлено, что во всех образцах присутствует фаза карбоната бария.
Рис. 5.
Дифрактограммы синтезированного образца гексагидроксистанната бария BaSn(OH)6 и катализаторов BaSnO3-450 и BaSnO3-750 до реакции.
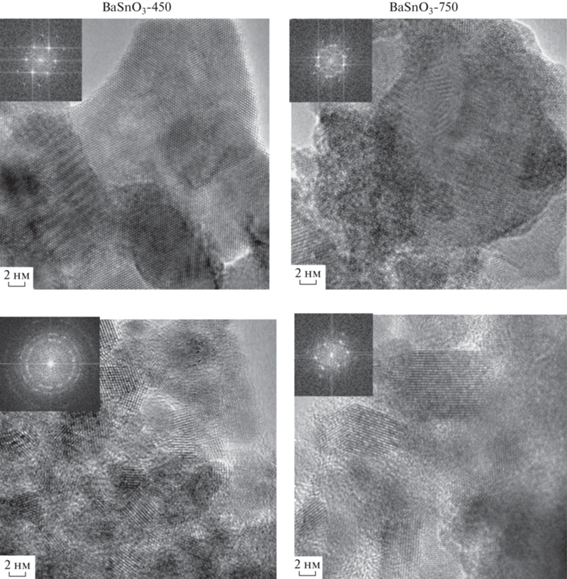
Уточнение фазового состава катализатора проводили методом ПЭМ высокого разрешения. Микрофотографии поверхности образцов BaSnO3-450 и BaSnO3-750 до и после реакции приведены на рис. 6. Несмотря на то что кристаллическая фаза метастанната бария в объеме при 450°С не образуется (см. рис. 5), анализ данных ПЭМ, полученных в режиме дифракции, для кристаллитов на поверхности образца BaSnO3-450 показали присутствие фазы BaSnO3 структурного типа перовскита. Для образца BaSnO3-750, где в объеме уже сформировалась кристаллическая фаза типа перовскита (см. данные РФА, рис. 5), данные ПЭМ показали наличие на поверхности, помимо BaSnO3, кристаллитов Ba2SnO4 и оксида олова SnO2, которые являются результатом разложения метастанната бария BaSnO3. Микрофотографии поверхности катализаторов после реакции показывают изменение поверхностной структуры катализаторов и уменьшение размеров кристаллитов (рис. 6).
ВЫВОДЫ
Станнаты бария BaSnO3-450 и BaSnO3-750, полученные прокаливанием гексагидроксистанната бария BaSn(OH)6 при 450 и 750°С соответственно, оказались активными гетерогенными катализаторами альдольно-кротоновой конденсации ацетона в сверхкритических условиях (300–400°С, 11.0 МПа). Проведение реакции в условиях, превышающих аддитивные критические параметры ацетона и основного продукта – окиси мезитила, обеспечило стабильную конверсию ацетона. При прочих равных условиях катализатор BaSnO3-450 проявляет наибольшую активность, двукратно превышающую для катализатора BaSnO3-750. Увеличение температуры реакции от 300 до 400°С приводит к четырехкратному увеличению активности катализаторов. При этом катализатор BaSnO3-750 обладает высокой селективностью по изомерным окисям мезитила 77–87%. Увеличение температуры реакции от 300 до 400°С на катализаторе BaSnO3-450 приводит к значительному изменению селективности от С6 (окиси мезитила) к С9 (форонам) и С9+. Дифракционные данные (РФА, ПЭМ) указывают на полифазность образцов: станнаты бария, карбонат бария, оксид олова. Установлено, что в процессе реакции происходит перестройка структуры катализаторов. Изменение фазового состава катализаторов in situ реакции конденсации наиболее выражено для BaSnO3-450, по сравнению с BaSnO3-750, что в значительной степени и отражается на каталитических свойствах этих станнатов.
Список литературы
Salvapati G.S., Ramanamurty K.V., Janardanarao M. // J. Mol. Catal. 1989. V. 54. № 1. P. 9–30. https://doi.org/10.1016/0304-5102(89)80134-8
Алексеев Е.С., Алентьев А.Ю., Белова А.С., Богдан В.И., Богдан Т.В., Быстрова А.В., Гафарова Э.Р., Голубе-ва Е.Н., Гребеник Е.А., Громов О.И., Даванков В.А., Злотин С.Г., Киселев М.Г., Коклин А.Е., Кононевич Ю.Н., Лажко А.Э., Лунин В.В., Любимов С.Е., Мартья-нов О.Н., Мишанин И.И., Музафаров А.М., Несте-ров Н.С., Николаев А.Ю., Опарин Р.Д., Паренаго О.О., Паренаго О.П., Покусаева Я.А., Ронова И.А., Соловьева А.Б., Темников М.Н., Тимашев П.С., Турова О.В., Филатова Е.В., Филиппов А.А., Чибиряев А.М., Шалыгин А.С. // Усп. хим. 2020. Т. 89. № 12. С. 1337–1427. https://doi.org/10.1070/RCR4932
Вещицкий Г.А., Смирнов А.В., Мащенко Н.В., Кок-лин А.Е., Богдан В.И. // Сверхкрические Флюиды: Теория и Практика. 2021. Т. 16. № 2. С. 57–62. https://doi.org/10.34984/SCFTP.2021.16.2.007
Коклин А.Е., Хасянова Г.М., Глухов Л.М., Богдан В.И. // Изв. АН. Сер. хим. 2017. Т. 66. № 3. С. 488–490. https://www.elibrary.ru/yhppvh
Богдан Т.В., Коклин А.Е., Мишин И.В., Мащенко Н.В., Смирнов А.В., Саварец А.Р., Богдан В.И. // Изв. АН. Сер. хим. 2022. № 9. С. 1930–1939.
Богдан Т.В., Коклин А.Е., Мащенко Н.В., Богдан В.И. // Журн. физ. хим. 2022. Т. 96. № 11. С. 1569–1577.
ISDD 2018. The Powder Diffraction File. International Centre for Diffraction Data, 2018.
Ma C., Liu G., Wang Z., Li Y., Zheng J., Zhang W., Jia M. // React. Kinet. Catal. Lett. 2009. V. 98. P. 149–156. https://doi.org/10.1007/s11144-009-0055-8
Дополнительные материалы отсутствуют.
Инструменты
Доклады Российской академии наук. Химия, науки о материалах