Доклады Российской академии наук. Науки о Земле, 2022, T. 504, № 2, стр. 200-204
Изменение форм нахождения меди в поверхностных водах при возрастании техногенной нагрузки
О. Ю. Дроздова 1, *, В. В. Демин 1, М. А. Макарова 2, М. М. Карпухин 1, С. А. Лапицкий 1
1 Московский государственный университет
имени М.В. Ломоносова
Москва, Россия
2 Институт геологии рудных месторождений, петрографии, минералогии и геохимии
Российской академии наук
Москва, Россия
* E-mail: drozdova@geol.msu.ru
Поступила в редакцию 24.02.2022
После доработки 03.03.2022
Принята к публикации 09.03.2022
- EDN: YXZFBP
- DOI: 10.31857/S2686739722060056
Аннотация
Экспериментально изучено изменение распределения соединений Cu по размерным фракциям при увеличении ее концентрации в незагрязненных поверхностных водах. Показано, что растворенные органические вещества природных вод, особенно гуминовые вещества, оказывают значительное влияние на формы нахождения Cu при высоком ее содержании (до 50 мг/л), определяя стабильность ее коллоидных соединений. В поверхностных водах с низким содержанием органических веществ при их загрязнении медью будут образовываться высокомолекулярные соединения Cu, что может привести к выведению Cu в донные отложения.
Важной особенностью тяжелых металлов является то, что после попадания в окружающую среду их потенциальная токсичность в значительной степени определяется формой нахождения [1]. Медь – микроэлемент, который при избыточных концентрациях в поверхностных водах является опасным токсикантом для живых организмов [2]. Кроме того, Cu может участвовать в круговороте пероксида водорода внутри водоема, играя важную роль в процессах образования ОН-радикалов в нейтральной водной среде [3, 4], что обеспечивает функцию самоочищения природных водных экосистем.
Исследования форм нахождения металлов в поверхностных водах важны не только с точки зрения их влияния на экологическую обстановку, но и для оценки путей их миграции в водных экосистемах [5]. Совершенствование научных представлений о закономерностях миграции металлов в природных ландшафтах существенно влияет на достоверность прогнозных оценок изменения состояния экосистем в условиях возрастания антропогенной нагрузки.
МЕТОДЫ ИССЛЕДОВАНИЯ
В работе рассмотрено изменение распределения соединений меди по размерным фракциям в трех не загрязненных водных объектах, расположенных на территории Мещерской низменности Владимирской области (55°49′ с.ш., 39°22′ в.д.): воды реки Сеньга, озера Сеньга и старичного оз. Ершевик. Отбор и консервация проб поверхностных вод производились в соответствии с ГОСТ Р 51592-2000. Пробы отбирали в стерильные полипропиленовые флаконы для анализа на анионы и определения металлов, а также в стеклянные емкости для определения органического углерода. Пробы для определения металлов при отборе подкисляли HNO3конц. Хранили образцы до анализа при 2–4°С.
В природных водах in situ измеряли электропроводность (кондуктометр Hanna HI 9033) и значения pH (рН-метр Hanna HI 9025). В лаборатории в водных образцах и фильтратах определяли содержание: неорганических анионов (на ионном хроматографе Dionex ICS-2000, “Thermo”), основных катионов и меди (на атомно-абсорбционном спектрофотометре ContrAA 700, “AnalytikJena Company” и на оптическом эмиссионном спектрометре с индуктивно-связанной плазмой Agilent 5110 ICP-OES), и растворенного органического углерода (РОУ) (на анализаторе LiquiTOCtrace, “Elementar”). Содержания гуминовых веществ (ГВ) в пробах определялись по реакции их связывания с красителем Толуидиновый синий [6]. В растворенной форме определялись количества катионных, анионных и нейтральных соединений меди методом ионообменной хроматографии с использованием смол: ДЭАЭ-целлюлозы (“Sigma Aldrich”) и Dowex 50 WX 8, 200–400 меш (“Serva”).
Для определения возможных изменений форм Cu при возрастании техногенной нагрузки были проведены лабораторные эксперименты по введению дополнительных количеств меди в образцы изучаемых поверхностных вод. Для этого медь в виде CuCl2 вносили в образцы исследуемых вод, так чтобы конечная концентрация металла составляла 0.5, 1, 25 и 50 мг/л. Значения рН и ионная сила в экспериментах соответствовали полученным характеристикам исследуемых вод. После наступления равновесия в системе (не менее суток после введения металла) образцы последовательно фильтровались через фильтры (“Millipore”) с различным размером пор 0.45 мкм, 30 и 10 кДа (в фильтрационных установках фирмы “Amicon”). В полученных фильтратах измеряли содержание меди и растворенного органического углерода. Все варианты экспериментов проводили в трех повторностях.
РЕЗУЛЬТАТЫ
Исследуемые воды относятся к гидрокарбонатному классу кальциевой группы [7]. Значения удельной электропроводности исследуемых природных вод находятся в диапазоне от 31 до 45 мкСм/см, а значения рН от 6.5 до 7.3. Концентрации основных неорганических анионов и катионов во всех объектах невысокие. Содержания РОУ и Cu в исследуемых водах снижаются в ряду: река Сеньга, оз. Сеньга, оз. Ершевик. Содержания Cu во всех объектах не превышают ПДК и норм ВОЗ, принятых для водных объектов.
Основные гидрохимические характеристики изучаемых природных вод представлены в табл. 1.
Таблица 1.
Основные гидрохимические характеристики изучаемых природных вод
| Показатель | р. Сеньга (n = 3) | оз. Сеньга (n = 3) | оз. Ершевик (n = 3) |
|---|---|---|---|
| pH | 6.5 ± 0.1 | 7.3 ± 0.1 | 7.0 ± 0.1 |
| æ, мкСм/см | 45 ± 5 | 31 ± 3 | 36 ± 3 |
| K, мг/л | 0.5 ± 0.1 | 1.2 ± 0.2 | 3.5 ± 0.4 |
| Na, мг/л | 2.2 ± 0.2 | 3.4 ± 0.4 | 5.9 ± 0.6 |
| Ca, мг/л | 20.0 ± 4.0 | 17.5 ±2.0 | 13.5 ± 2.0 |
| Mg, мг/л | 5.3 ± 0.7 | 4.9 ± 0.5 | 5.8 ± 0.7 |
| НСО$_{3}^{ - }$, мг/л | 7.3 ± 0.9 | 33.1 ± 2.0 | 63.4 ± 5.0 |
| Хлориды, мг/л | 0.2 ±0.1 | н.о. | 4.7 ± 0.4 |
| Сульфаты, мг/л | 0.4 ± 0.1 | 4.9 ± 0.6 | 13.3 ± 1.1 |
| Нитраты, мг/л | 0.4 ± 0.1 | н.о. | 0.5 ± 0.1 |
| РОУ, мг/л | 35.7 ± 4.0 | 27.6 ± 3.0 | 18.3 ± 2.8 |
| ГВ, мг/л | 21 ± 3 | 17 ± 3 | 11 ± 2 |
| Cu, мкг/л | 1.5 ± 0.1 | 1.6 ± 0.1 | 0.9 ± 0.05 |
Во всех исследуемых водах преобладают соединения меди <10 кДа, которые составляют 65, 75 и 96% в водах реки, оз. Сеньга и оз. Ершевик соответственно (рис. 1). Распределение Cu по различным фракциям коррелирует с распределением РОУ (рис. 2) в водах озер, где коэффициенты корреляции (R) составляют 0.96 в оз. Сеньга, 0.99 в оз. Ершевик, тогда как в водах реки эта зависимость выражена слабее (R = 0.81).
Рис. 1.
Изменения распределения Cu по размерным фракциям в исследованных водах в ходе экспериментов.
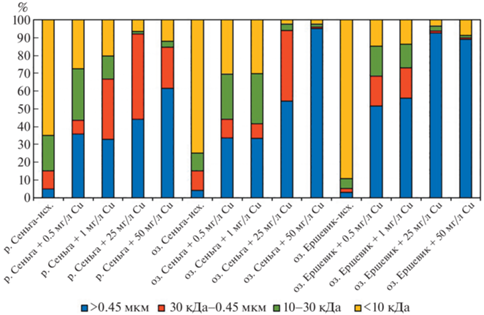
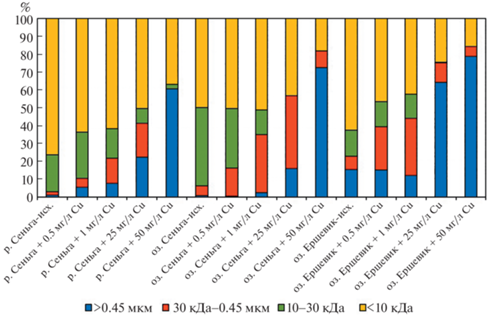
Рис. 2.
Изменения распределения РОУ по размерным фракциям в исследованных водах в ходе экспериментов.
Установлено, что в растворенной форме Cu находится во всех исследованных водах преимущественно в анионной форме (табл. 2). При этом проведенные расчеты с использованием программы физико-химического моделирования Visual MINTEQ показали, что большая часть Cu (98–99%) во всех объектах исследования представлена комплексами с органическими лигандами (L). Таким образом, большая часть Cu в исследованных водах находится в виде комплексов с органическими веществами вида [CuL]n–, которые могут быть образованы как с низкомолекулярными двух- и более основными кислотами, так и с высокомолекулярными соединениями, такими как гуминовые вещества (ГВ).
Таблица 2.
Формы меди в исследованных водах
| Объект | Форма, % | ||
|---|---|---|---|
| Катион-ная | Анион-ная | Нейтраль-ная | |
| р. Сеньга (n = 3) | 25 ± 5 | 72 ± 10 | 3 ± 1 |
| оз. Сеньга (n = 3) | 36 ± 7 | 62 ± 6 | 2 ± 1 |
| оз. Ершевик (n = 3) | 38 ± 6 | 59 ± 8 | 3 ± 1 |
Проведенные эксперименты по исследованию изменений форм Cu при увеличении техногенной нагрузки в изучаемых водных объектах показали, что введение в раствор Cu вызывает заметное увеличение доли высокомолекулярных фракций (рис. 1).
В экспериментах при добавлении 0.5 и 1 мг/л Cu увеличение размера соединений меди связано с образованием высокомолекулярных комплексов с органическими веществами, что согласуется с изменением распределения РОУ по размерным фракциям (рис. 2). Вероятнее всего, происходит образование лабильных надмолекулярных структур Cu–ГВ1∙∙∙∙∙ГВ2–Cu за счет слабых кулоновских взаимодействий [8].
При введении растворов с более высокой концентрацией Cu в систему (25 мг/л) достигалось пересыщение раствора относительно малахита, и образовывались коллоидные рентгеноаморфные частицы Cu, которые стабилизируются органическими соединениями. При этом большая стабильность коллоидов наблюдалась в водах реки и оз. Сеньга, что видно по количеству Cu и РОУ во фракции 30 кДа – 0.45 мкм. Такое отличие от вод оз. Ершевик, где большая часть Cu представлена соединениями >0.45 мкм, связано с более высоким содержанием ГВ в данных пробах (табл. 1). Известно, что ГВ могут ингибировать рост зародышей твердых фаз неорганических соединений в пересыщенных растворах и уменьшать их агрегацию за счет электростатических и стерических эффектов отталкивания, предотвращая, таким образом, осаждение коллоидов [9, 10]. Различия в результатах для вод двух озер могут быть связаны с тем, что автохтонные органические вещества, содержание которых выше в оз. Ершевик, могут способствовать агрегации и седиментации коллоидных частиц даже в присутствии стабилизирующих ГВ [11].
При внесении 50 мг/л Cu содержания ГВ в водах озер недостаточно для стабилизации коллоидов и начинают образовываться более крупные частицы, состоящие главным образом из неорганических соединений Cu, что обусловливает увеличение фракции >0.45 мкм до 91–95%. Это может способствовать выпадению меди в осадок.
ЗАКЛЮЧЕНИЕ
Таким образом, растворенные органические вещества поверхностных вод оказывают значительное влияние на формы нахождения и миграции Cu. Установлено, что стабильность коллоидных соединений Cu при высоком ее содержании в системе зависит от концентрации природного органического вещества. Низкое содержание органических соединений, особенно ГВ, в водах может способствовать быстрой коагуляции минеральных коллоидов, и соответственно, высокой скорости их седиментации. В случае значительных изменений физико-химических параметров среды и восстановительных процессов в водоеме будет происходить переход Cu и донных осадков в раствор, что может привести ко вторичному загрязнению поверхностных вод [12].
Список литературы
Голованова О.А., Маловская Е.А. Динамика загрязнения ионами тяжелых металлов поверхностных вод рек сибирского региона // Вестник Омского университета. 2016. № 3. С. 64–73.
Кашин В.К., Иванов Г.М. Медь в природных водах Забайкалья // Водные ресурсы. 2008. Т. 35. № 2. С. 239–244.
Сычев А.Я., Травин С.О., Дука Г.Г., Скурлатов Ю.И. Каталитические реакции и охрана окружающей среды. Кишинев: Штиинца, 1983.
Швыдкий В.О., Штамм Е.В., Скурлатов Ю.И., Вичутинская Е.В., Зайцева Н.И., Семеняк Л.В. Интоксикация природной водной среды как следствие разбалансировки внутриводоемных окислительно-восстановительных и свободно-радикальных процессов // Химическая физика. 2017. Т. 36. № 8. С. 23–33.
Линник П.Н., Васильчук Т.А., Линник Р.П., Игнатенко И.И. Сосуществующие формы тяжелых металлов в поверхностных водах Украины и роль органических веществ в их миграции // Методы и объекты химического анализа. 2007. Т. 2. № 2. С. 130–145.
Sheng G.-P., Zhang M.-L., Yu H.-Q. A Rapid Quantitative Method for Humic Substances Determination in Natural Waters // Analytica Chimica Acta. 2007. V. 592. P. 162–167.
Алекин О.А. Основы гидрохимии. Л.: Гидрометеоиздат, 1970. 413 с.
Tikhonov V.V., Drozdova O.Yu., Karpukhin M.M., Demin V.V. Participation of Cadmium (ll) and copper (ll) Ions in Intermolecular Forces of Humic Acids in Solutions // IOP Conf. Series: Earth and Environmental Science. 2019. V. 368. 012053. P. 1–5.
Nanja A.F., Focke W.W., Musee N. Aggregation and Dissolution of Aluminium Oxide and Copper Oxide Nanoparticles in Natural Aqueous Matrixes // SN Applied Sciences. 2020. 2: 1164. P. 16.
Philippe A., Schaumann G.E. Interactions of Dissolved Organic Matter with Natural and Engineered Inorganic Colloids: A Review// Environmental Science & Technology. 2014. 48 (16). P. 8946–8962.
Wilkinson K.J., Joz-Roland A., Buffle J. Different Roles of Pedogenic Fulvic Acids and Aquagenic Biopolymers on Colloid Aggregation and Stability in Freshwaters // Limnology and Oceanography. 1997. 42 (8). P. 1714–1724.
Даувальтер В.А. Геоэкология донных отложений озер. Мурманск: Изд-во МГТУ, 2012. 242 с.
Дополнительные материалы отсутствуют.
Инструменты
Доклады Российской академии наук. Науки о Земле


