Экология, 2022, № 4, стр. 255-288
Тритий от молекулы до биосферы. 1. Закономерности поведения в окружающей среде
Е. В. Антонова a, *, К. Л. Антонов b, c, М. Е. Васянович b, c, С. В. Панченко c
a Институт экологии растений и животных УрО РАН
620144 Екатеринбург, ул. 8 Марта, 202, Россия
b Институт промышленной экологии УрО РАН
620990 Екатеринбург, ул. С. Ковалевской, 20, Россия
c Институт проблем безопасного развития атомной энергетики РАН
115191 Москва, ул. Большая Тульская, 52, Россия
* E-mail: selena@ipae.uran.ru
Поступила в редакцию 01.02.2022
После доработки 18.03.2022
Принята к публикации 19.03.2022
- EDN: GREURA
- DOI: 10.31857/S0367059722040035
Аннотация
Бета-излучатель тритий (3H, период полураспада 12.32 ± 0.02 г.), находящийся в окружающей среде, имеет естественное и техногенное происхождение. Равновесное глобальное содержание естественного трития оценивается в (1.0–2.6) × 1018 Бк. Суммарная активность техногенного трития, который сформировался за счет испытаний ядерного и термоядерного оружия в 1945–1975 гг., штатной и аварийной работы предприятий ядерно-топливного цикла, достигает 1020 Бк. Антропогенный тритий служит уникальным маркером для обобщения данных о поведении этого радионуклида в различных компонентах окружающей среды. Это особенно актуально с учетом интенсификации в последние годы исследований и разработок в области управляемого термоядерного синтеза. Перспективные энергетические термоядерные реакторы, в которых в качестве топлива планируется использовать значительное количество 3H, могут стать дополнительным источником воздействия на биосферу. Их безопасность должна быть оценена, обоснована и в конечном итоге обеспечена технологиями и инфраструктурой. Нами проанализирована динамика числа публикаций по 3H в период с 1951 г. по 2021 г., размещенных в базах данных Google Scholar и Clarivate Analitics. Приведены основные характеристики и химические формы трития. Методология оценки содержания разных форм 3H в компонентах окружающей среды приводится с учетом межлабораторной интеркалибровки. Проанализированы пути поступления трития в окружающую среду (атмосферу, водные и наземные экосистемы) в результате штатных и аварийных выбросов и сбросов предприятий атомной промышленности. Показаны сезонные колебания активности трития с максимумом в весенний период, влияние климатических факторов и расстояния от источника выбросов на распределение 3H в пространстве. Отмечена роль почвенных органических кислот в поведении трития в экосистемах. На основании концепции о референтных видах растений и животных проведен анализ публикаций для оценки накопления разных форм 3H биотой в ходе лабораторных экспериментов и мониторинговых исследований природных экосистем. Выявлен ряд актуальных вопросов, требующих решения в самое ближайшее время.
Массовые испытания ядерного оружия в середине XX в. привели к повышению общего радиационного фона на планете [1, 2]. Уровень техногенного фона по тритию к 1954–1958 и 1961–1962 гг. достиг максимума и примерно в 100–300 раз превышал уровень природного равновесного содержания. После окончания испытаний ядерного оружия из-за естественного распада уровень техногенного трития начал снижаться – к настоящему времени в окружающей среде остается около 1.0 × 1019 Бк, что примерно в 5–10 раз больше природного содержания [2]. Современные запросы общества, направленные на поиск альтернативных источников энергии, обладающих качеством бережного (экологичного) отношения к окружающей среде, находят решение этой проблемы в развитии технологий в области ветровой, солнечной, геотермальной, водородной энергетики, биотоплива, гидроэнергетики и т.д. [3–5].
Термоядерные установки, в которых тритий используется и воспроизводится в качестве топлива, считаются одним из перспективных и безопасных источников энергии. Интерес к данному источнику не затихает с 50-х годов XX в. В настоящее время в разных странах наблюдается активное развитие этой технологии, например на Joint European Torus, Korea Superconducting Tokamak Advanced Research, Experimental Advanced Superconducting Tokamak, Spherical Tokamak Globus-M2 [6–9], а также в ходе международных проектов: Tokamak Ignitor project [10, 11], International Thermonuclear Experimental Reactor [12] и др. Ведется активная дискуссия по вопросам радиационного воздействия на окружающую среду от переработки отработавшего ядерного топлива (ОЯТ) и возможных преимуществ использования гибридных термоядерных реакторов [13]. Подчеркиваются важность и необходимость следования признанным подходам к радиационной защите живых организмов и человека, представленным в публикациях Международной комиссии по радиологической защите (МКРЗ).
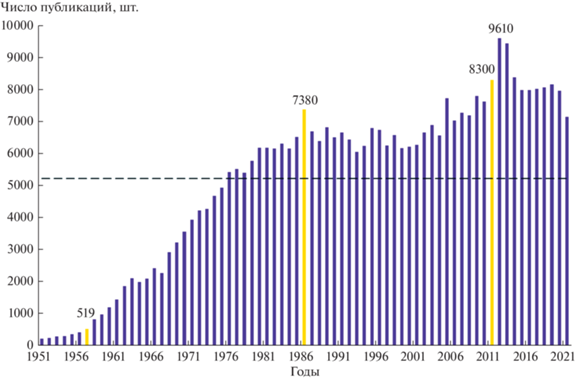
Анализ публикаций до 40-х годов ХХ в. по тритиевой тематике показал, что в Google Scholar встречаются лишь единичные работы – 50–100 за каждое десятилетие. Значительный рост числа публикаций отмечен с 1940 г. по 1950 г. (451). Динамика публикаций по тритию во всех областях знания за последние 70 лет показана на рис. 1. До середины 80-х годов XX в. наблюдался неуклонный рост числа работ по данной тематике, а 90-е годы характеризовались некоторым спадом. Начиная с 2000 г. интерес к тритиевой проблеме повысился. Отметим, что Кыштымская и Виндскейлская аварии (1957 г.) не внесли вклад в публикационную активность, в то же время наблюдался рост числа публикаций на 13.2% относительно доаварийного периода в 1986 г. (Чернобыльская авария), на 8.8% – в 2011 г. (Фукусимская авария) и на 23.7–25.6% в два последующих поставарийных года. Суммарно с 1951 г. по тритию опубликовано более 370 тыс. работ, на русском языке Google Scholar идентифицирует около 5 тыс.
Рис. 1.
Динамика числа публикаций, связанных с тритием, на основе поиска в Google Scholar: желтым цветом обозначены Кыштымская, Виндскейлская (1957), Чернобыльская (1986) и Фукусимская (2011) аварии; пунктирная линия – среднегодовой уровень публикаций с 1951 г. по 2021 г.
По данным Clarivate Analitics (рис. 2), за последние 70 лет пик публикаций по тритию (превышение среднегодового значения в 2.4–4.6 раза) также приходится на 1979–1985 гг. (31% всех публикаций), с последующим плато в 90-е годы. Начиная с 2000 г. отмечается стабильная публикационная активность (115–273 публикации в год). Всего с 1951 г. было опубликовано около 15 тыс. работ.
Рис. 2.
Динамика числа публикаций, связанных с тритием, на основе интегрального поиска в Web of Science Core Collection (1975–2021), KCI-Korean Journal Database (1980–2021), MEDLINE® (1951–2021) и SciELO Citation Index (2002–2021): желтым цветом обозначены Кыштымская, Виндскейлская (1957), Чернобыльская (1986) и Фукусимская (2011) аварии, красным – годы с кратным увеличением числа публикаций; пунктирная линия – среднегодовой уровень публикаций с 1951 г. по 2021 г.
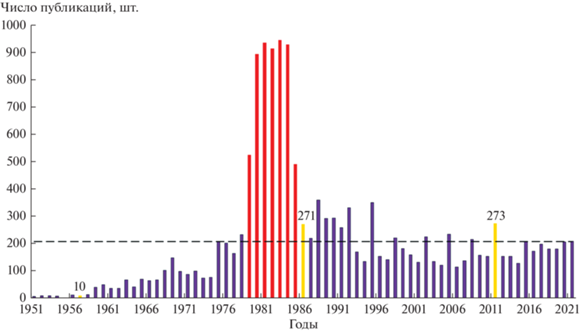
В базе данных Web of Science Core Collection (рис. 3) число публикаций по тритию в конце 70-х–начале 90-х годов XX в. превышало среднегодовой уровень (≈192). Начиная с 2000 г. отмечается невысокая публикационная активность (113–267 публикаций в год) В последние годы интерес к тритиевой тематике стабилизировался – суммарно с 1975 г. опубликовано более 9 тыс. работ. Отметим также, что после 1992 г. количество публикаций, индексированных в Clarivate Analitics (см. рис. 2) и Web of Science Core Collection (см. рис. 3), стало практически полностью совпадать. Из трех вышеуказанных баз данных наиболее наполненной является Google Scholar.
Рис. 3.
Динамика числа публикаций, связанных с тритием, на основе поиска в Web of Science Core Collection (1975–2021 гг.): желтым цветом обозначены Кыштымская, Виндскейлская (1957), Чернобыльская (1986) и Фукусимская (2011) аварии; пунктирная линия – среднегодовой уровень публикаций с 1951 г. по 2021 г.

Исходя из вышесказанного, цель настоящей работы – обобщение данных, связанных с поведением трития в разных компонентах окружающей среды (атмосфере, водных и наземных экосистемах) и поиск закономерностей накопления трития биотой.
ОБЩАЯ ХАРАКТЕРИСТИКА ТРИТИЯ
Название для изотопов водорода было предложено Х. Ури, Дж. Мерфи и Ф. Брикведде [14] в 1933 г. до открытия трития. Спустя месяц после выхода публикации тритий впервые был обнаружен М. Олифантом, П. Хартеком и Э. Резерфордом после бомбардировки дейтерия дейтронами (протоном и нейтроном, содержащими ядро дейтерия), однако выделен не был [15]. Позднее Л. Альварес и Р. Корног экспериментально обнаружили и выделили тритий, подтвердив его радиоактивные свойства [16].
Тритий (3H, или T) – радиоактивный изотоп водорода с атомным номером 1 и массовым числом 3. Атомная масса – 3.0160492777(25) а.е.м., дефект массы – 14.9498060(23) МэВ, удельная энергия связи (на нуклон) – 2.827266(1) МэВ [17]. Тритий является чистым низкоэнергетическим β-излучателем. Реакция распада имеет следующий вид:
В реакции выделяется 18.591 кэВ энергии, из которой на электрон (β-частицу) приходится в среднем 5.7 кэВ, а на электронное антинейтрино – оставшаяся часть [17, 18]. Период полураспада трития в течение 1936–2000 гг. определялся экспериментально по меньшей мере 23 раза и по современным оценкам составляет 12.32 ± 0.02 года [19]. Это означает, что в чистом виде тритий не может храниться продолжительное время, так как его исходное количество ежегодно уменьшается на 5.6%. Например, для поддержания ядерного арсенала США ежегодное производство трития составило около 2 кг (≈7 кг/год было необходимо для всех мировых военных потребителей в конце прошлого столетия) [20].
Физико-химические свойства 3H, за исключением молекулярного веса, близки к водороду. Газообразный тритий окисляется в кислороде с образованием тритиевой воды (НТО, Т2О), обменивается с атомами водорода органических соединений. Газообразный тритий легко диффундирует через преграды (особенно через пластиковые стенки). Поскольку атомы трития в 3 раза тяжелее водорода (1H), удельный вес НТО или Т2О выше, чем у H2О, следовательно, выше и температура кипения. Скорость диффузии и скорости химических реакций соединений трития часто меньше, чем у соединений водорода, что связано с “изотопным эффектом” [21]. Исследование распределения трития в клетках растения, выросшего в атмосфере тритий-содержащей воды, а также изотопное равновесие трития между водой и углеводами показали, что тритий накапливается в органическом веществе клетки с константой равновесия, равной ~1.5 [22].
Максимальная энергия электронов 18.6 кэВ при распаде 3H не позволяет им распространяться в воздухе более чем на 5 мм, а в воде (что почти эквивалентно человеческой ткани) максимальная длина трека составляет 6 мкм [18]. Поэтому эти β‑частицы не могут преодолеть даже верхний слой кожи человека и достичь клеток-мишеней для возникновения рака кожи и других типов повреждений кожи, которые находятся в базальном слое эпидермиса (20–100 мкм) и дерме (1–3 мм). Испускаемые электроны хорошо задерживаются даже простейшими преградами типа одежды или резиновых хирургических перчаток.
ОБРАЗОВАНИЕ ТРИТИЯ И ПУТИ ПОСТУПЛЕНИЯ В ОКРУЖАЮЩУЮ СРЕДУ
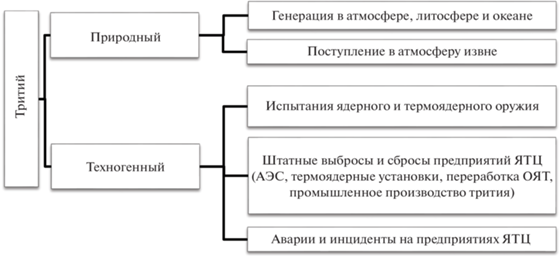
Тритий, находящийся в окружающей среде, имеет естественное и техногенное происхождение. Он образуется при ядерных реакциях, протекающих в природных условиях, а также в результате антропогенной деятельности при испытаниях ядерного и термоядерного оружия, в энергетических ядерных реакторах и перспективных термоядерных установках, а также в процессе производства трития для практического использования. Основные пути появления трития в биосфере представлены на рис. 4.
В природных условиях 3H непрерывно генерируется в верхних слоях атмосферы в результате взаимодействия протонов и нейтронов высокоэнергетического космического излучения с атомами азота, кислорода и аргона, а также поступает в атмосферу извне с космическими лучами или солнечным ветром [23]. В следовых количествах тритий может вырабатываться при реакциях захвата нейтронов 6Li в океанах и литосфере (где нейтроны образуются при спонтанном делении урана), нейтронном облучении дейтерия и нейтронных реакциях космогенных элементов (скорости реакций – 10–3 атомов трития/см2/с в литосфере; 10–6 атомов трития/см2/с в гидросфере) [24]. Однако основная часть природного 3H образуется именно в стратосфере за счет взаимодействия космического излучения с атмосферными газами. Оценки суммарной скорости образования достигают 0.5–1.5 × 1017 Бк/год [1, 2], или 0.1–1.3 атомов трития/см2/с [18, 23].
В атмосфере тритий в результате окисления и изотопного обмена конвертируется в молекулы тритиевой воды и выводится на поверхность Земли в виде осадков. Всего ~99% общего количества космогенного трития в виде тритиевой воды (НТО) вовлекается в нормальный земной круговорот воды. С учетом распада равновесное глобальное содержание трития естественного происхождения оценивается от 1.0 × 1018 до 2.6 × 1018 Бк [2, 18, 23, 25], что при удельной активности 3.57 × 1014 Бк/г соответствует примерно 2.8–7.3 кг. Из этого равновесного количества природного трития более 99% находится в водах океанов, преимущественно в виде НТО, и менее 1% в атмосфере и подземных водах [23].
Испытания ядерного и термоядерного оружия в атмосфере в 1945–1975 гг. добавили в окружающую среду (1.7–3.0) × 1020 Бк трития [2, 26], что примерно в 100–300 раз превышает уровень природного равновесного содержания. Пик выноса техногенного трития пришелся на 1954–1958 и 1961–1962 гг., вклад ядерных взрывов в вынос после 1964 г. составил менее 5% от его общего количества. Испытания привели к резкому увеличению концентрации 3H в дождевых осадках. Так, в начале 1960-х годов в северном полушарии отмечалось кратковременное 1000-кратное превышение его естественных уровней [27], в среднем концентрация трития в дождевой воде возрастала в 10–100 раз [28]. С 1963 г. временные экстремальные значения содержания трития в осадках снизились до практически естественных уровней зимой и лишь до двукратных превышений летом [23]. К настоящему времени значительная часть “бомбового” трития распалась, в окружающей среде остается около 1.0 × 1019 Бк (т.е. примерно в 5–10 раз больше природного содержания), преимущественно в океанах в очень низкой концентрации [2]. Подземные ядерные испытания, по-видимому, внесли незначительный вклад в содержание трития в атмосфере; основная его часть в форме НТО мигрировала в подземные воды.
На атомных электростанциях (АЭС) образуется около 4 кг трития в год, но не извлекается [29]. При активации нейтронами атомов 2H, 3He, 6Li и 10B тритий образуется в тех частях ядерных реакторов, где достаточны плотность потока нейтронов и концентрация упомянутых изотопных примесей-мишеней. Выход трития из топливных элементов в окружающую среду может происходить вследствие его диффузии в первичный и далее вторичный теплоноситель (в том числе из-за дефектов в оболочках топливных элементов) и неэффективности современных технологий улавливания трития, применяемых для удаления большинства радионуклидов в технологических сбросах и выбросах. Большое влияние на количество выделяемого трития оказывают конструкция системы охлаждения реактора [23] и тип реактора. Так, скорость образования и выброса трития различается для разных типов реакторов, ранжированных в порядке увеличения: высокотемпературные газоохлаждаемые реакторы (HTGR), легководные реакторы (LWR), жидкометаллические реакторы на быстрых нейтронах (LMFBR), реакторы на расплавленной соли (MSBR) и тяжеловодные реакторы (HWR). Большая часть трития была выброшена в виде НТО [30]. Для различных типов энергетических реакторов оценки выделяемой активности трития на единицу сгенерированной электрической энергии варьируют в диапазоне 1014–1016 Бк/(ГВтэ год) [2]. При этом в окружающую среду в виде газообразных выбросов и жидких сбросов поступает 1012–1015 Бк/(ГВтэ год). Совокупное поступление 3H от штатной эксплуатации энергетических установок, на долю которых приходится более 95% мировой электрогенерации, оценивается не более 2.65 × 1016 Бк/год [1, 31, 32].
Большая часть образующегося в реакторе 3H остается в топливе до тех пор, пока оно не будет переработано [23]. Как известно, в ядерном топливном цикле на этапе переработки ОЯТ уран и плутоний извлекаются из облученного топлива для повторного использования в реакторах деления. В процессе переработки эти элементы сначала удаляются из оболочки, а затем растворяются в азотной кислоте, высвобождая значительную часть трития в виде жидких отходов (в виде НТО). Некоторое количество 3H выделяется в газовой фазе, остальное иммобилизуется в оболочке в виде твердого гидрида циркония или трития, растворенного в металле [33]. Поскольку на действующих в настоящее время заводах по переработке ОЯТ нет эффективных систем удержания трития, высвобождаемая активность полностью соответствует содержанию трития в топливных элементах во время переработки, за исключением 3H, иммобилизованного в оболочке. Общий выход трития в окружающую среду от процессов переработки облученного топлива оценивается в 6.4 × 1016 Бк/год [32].
Следует отметить, что в настоящее время суммарный объем поступления трития в окружающую среду при штатной эксплуатации АЭС и заводов по переработке топлива, равный 9.05 × 1016 Бк/год (30% – реакторы и 70% – переработка ОЯТ), сопоставим с количеством его ежегодного образования в природных условиях и примерно на 1–2 порядка меньше равновесного содержания трития естественного происхождения в биосфере. С учетом распада вклад естественных и техногенных источников в накопленную активность трития в атмосфере за последние 50 лет оценен в работе [31] – основной вклад в накопление 3H в атмосфере сформирован в период испытаний ядерного оружия. Ожидается, что к 2040–2050 гг. содержание накопленного в атмосфере “бомбового” трития приблизится к уровню естественного фона. В то же время, по некоторым оценкам, глобальное содержание трития в результате антропогенной деятельности может увеличиться в 6 раз с учетом усредненной модели развития атомной энергетики [32].
Поскольку запас 3H в природе ограничен, для практического использования его нарабатывают в основном в специально оптимизированных для производства трития и других ядерных материалов реакторах путем облучения металлического лития, его сплавов или солей. В основе процесса наработки трития, как и в энергетических реакторах, лежит реакция захвата нейтронов ядрами 6Li [23]. В коммерческих целях 3H может использоваться для медицинской диагностики, радиофармпрепаратов, светящихся красок, освещения знаков, огней взлетно-посадочных полос в аэропортах, циферблатов, манометров, наручных часов и др. Однако коммерческое использование вовлекает очень малую долю производимого трития. С 1950-х годов тритий применялся главным образом для увеличения мощности ядерных боеприпасов и создания термоядерного оружия. В России наработка трития продолжается на двух промышленных реакторах “Руслан” и “Людмила” на ПО “Маяк” в Челябинской области. Там же осуществляют выделение, переработку 3H и производство тритиевых узлов ядерных зарядов [34].
Оценить масштаб поступления 3H в окружающую среду от объектов его производства можно на основе данных о его выбросах в атмосферу, например предприятия Саванна-Ривер (основного источника трития в США). Среднегодовой выброс трития составляет 4.1 × 1016 Бк и состоит примерно на 20% из HT и на 80% из HTO [35]. Общий объем жидких сбросов 3H от этого объекта не превышает 10% от выбросов в атмосферу. Таким образом, по порядку величины поступление трития при его производстве на одном предприятии сопоставимо с суммарными нормативными выбросами и сбросами АЭС и предприятий по переработке облученного топлива. По данным [36], в 2020 г. на территории России объемная активность 3H в атмосферных осадках составила 1.34 Бк/л, а в речной системе – 1.5 Бк/л.
Представленные выше оценки производства и поступления трития в окружающую среду от объектов использования атомной энергии, как правило, характеризуют нормальный (штатный) режим их работы. Аварии и инциденты на таких объектах могут быть дополнительным источником эмиссии 3H. К примеру, такие события были зарегистрированы в США в 1970–1984 гг. в Ливерморской национальной лаборатории им. Э. Лоуренса и на предприятии Саванна-Ривер [18]. Объемы выброса 3H в результате этих инцидентов ограничивались диапазоном (0.28–18) × 1015 Бк, что на 1–2 порядка ниже суммарного выхода трития в окружающую среду при нормальной эксплуатации АЭС и заводов по переработке топлива.
Еще одним важным источником образования 3H, безусловно, станут объекты новой ядерной техники (ОНЯТ) на основе управляемого термоядерного синтеза. Значительное количество трития потребуется для исследовательских термоядерных установок: например, для запуска ITER – не менее 3 кг, для запуска DEMO – от 4 до 10 кг [37]. Гипотетический тритиевый реактор потреблял бы 56 кг трития на производство 1 ГВт×год электроэнергии, тогда как всемирные запасы трития на 2003 г. составляли всего 18 кг [37]. Однако технологии широкого применения ОНЯТ для выработки энергии до сих пор находятся в стадии разработки. Оценки объемов образования и потенциального выхода трития в окружающую среду при эксплуатации ОНЯТ имеют большие неопределенности. Ожидается, например, что термоядерный реактор номинальной мощностью 1000 МВтэ способен производить 5 × 1017 Бк трития в день при равновесном уровне порядка 1019 Бк [23]. Поэтому реакторы должны быть спроектированы таким образом, чтобы предотвратить поступление трития в окружающую среду или минимизировать его выбросы до приемлемых уровней. Для установления величины приемлемых уровней выброса трития в атмосферу и водную среду необходимо проведение работ по уточнению поведения этого изотопа в окружающей среде.
ХИМИЧЕСКИЕ ФОРМЫ ТРИТИЯ
В окружающей среде тритий может существовать в следующих основных химических формах:
− тритиевая несвязанная вода (HTO, T2O, DTO);
− водная форма трития, связанная в организме или ином живом веществе, неорганически связанный тритий (TFWT – tissue free water tritium);
− органически связанный тритий (OBT – organically bound tritium) присутствует в нескольких формах: общий; обменный или лабильный, связанный с кислородом и атомами азота (E-OBT); необменный, связанный с атомами углерода (NE-OBT);
− меченные тритием биохимические субстраты (включая предшественников ДНК – дезокситимидин и дезоксицитидин);
− нерастворимые соединения и меченные тритием газы (HT, DT, T2, CH3T и др.).
Самой распространенной в природе химической формой трития (более 99%) является HTO, только 0.12% природного 3H находится в газе водорода и 0.1% в водяном паре [23]. OBT используется для описания трития, который прочно связан с органическими компонентами клеток и тканей, например с белками, полисахаридами и липидами [1]. Он более устойчив, чем HTO, поскольку является частью круговорота органических веществ. Тем не менее тритий, связанный с азотом, серой или кислородом, считается способным к обмену с водородом. Поэтому время его пребывания в молекуле будет сокращено и тесно связано с окружающими параметрами. Когда тритий связан с углеродом, предполагается, что связь более стабильна, и таким образом время пребывания в молекуле будет увеличиваться [38].
Концентрация OBT в окружающей среде относительно низка. Однако удельная активность трития в организмах, как правило, выше в 1.5–4 раза для TFWT и в 5–20 раз для OBT, чем удельная активность HTO в окружающей среде [39]. Кроме того, средние дозовые линейные энергии OBT примерно в 1.7 раза выше, чем у HTO, что приводит и к их большей радиобиологической эффективности [40]. В отличие от HTO количественные характеристики ОВТ в биосфере и его поведение мало изучены. Некоторую информацию дает оценка соотношений OBT/HTO, поскольку может указывать как на предыдущие, так и на текущие уровни воздействия трития на объекты окружающей среды [41].
Тритий, поступающий в окружающую среду в виде жидких и газообразных выбросов, потенциально может накапливаться в живых организмах [42]. Однако проблема аккумуляции трития биотой до сих пор остается дискуссионной. Выявление и понимание физико-химических форм трития и процессов, ведущих к его устойчивости в окружающей среде, объяснили бы факты накопления OBT в живых организмах [43]. Большинство опубликованных к настоящему времени исследований свидетельствует о том, что 77% отношений OBT/TFWT для наземных растений в среднем равно 1.92. В то же время 81% отношений OBT/TFWT для водных организмов меньше 1. Это значит, что причину избытка трития в наземном органическом веществе следует искать в атмосфере. Годовой максимум трития приходится на весну, а в течение вегетационного периода происходит значительное обогащение OBT/TFWT [44]. Понимание биологических эффектов тритиевой воды в низких дозах и их последствий для биоты и человека также напрямую зависит от четкого знания множества процессов на молекулярном, биофизическом и клеточном уровнях [45].
ЕДИНИЦЫ ИЗМЕРЕНИЯ
В изотопно-гидрологических исследованиях содержание или концентрацию 3H в воде принято выражать тритиевыми единицами (ТЕ): 1 ТЕ соответствует изотопному отношению 3H/1Н = 10–18. Единицы удельной (или объемной) активности (Бк/кг или Бк/л) преимущественно используются в радиационной безопасности. Соотношение между упомянутыми единицами концентрации и радиоактивности следующее: 1 ТЕ = 0.118 Бк/л, или 3.3 × 10–16 г/л [18, 46].
МЕТОДОЛОГИЯ ОЦЕНКИ СОДЕРЖАНИЯ ТРИТИЯ В ОКРУЖАЮЩЕЙ СРЕДЕ И МЕЖЛАБОРАТОРНАЯ ИНТЕРКАЛИБРОВКА
Основная проблема измерения активности 3H – низкая энергия и небольшая длина пробега бета-излучения в различных средах (максимальный пробег электронов в воздухе не превышает 5 мм, а в воде – 6 мкм). Существование разных химических форм трития является ключевым моментом для выбора методов его измерений и оценки дозовых нагрузок [47]. Сегодня методология определения содержания разных химических форм 3H в компонентах окружающей среды хорошо развита [48–57], в том числе высокочувствительных измерений для оценки малых концентраций трития [53, 58, 59]. Тем не менее в связи с обострением проблемы вывода из эксплуатации ядерных установок и развитием термоядерных технологий необходимо актуализировать имеющиеся методы измерения концентраций и запасов 3H в окружающей среде. В настоящей работе мы остановимся лишь на некоторых из методов.
Для измерения 3H в атмосфере, в которой он присутствует в виде смеси HTO и HT, используются газоразрядные пропорциональные счетчики с предварительным электролитическим обогащением [60] и ионизационные камеры [48, 61]. Для пробоподготовки при определении трития в воздухе перед жидкостным сцинтилляционным счетом в качестве осушителя для удаления HTO из воздуха используются силикагель и барборатор [62, 63]. Отбор проб паров НТО из газов можно также осуществить на основе метода фазового изотопного обмена воды. Такой способ по сравнению с барботированием через слой жидкости позволяет оценить динамику изменения концентрации НТО в анализируемом газе [64]. Это изобретение обеспечивает значительное сокращение времени отбора проб и позволяет оперативно контролировать динамику изменения концентрации трития в газовых средах [65]. Другим методом измерения трития в воздухе является система с твердотельными сцинтилляционными детекторами. Такой подход позволяет измерять общую молярную долю трития в газовом образце вне зависимости от химического состава трития в газе (HT, DT, T2 и CHxTy). Он менее чувствителен по сравнению с жидкостно-сцинтилляционным методом, однако проще и надежнее в техническом исполнении [66, 67].
Наиболее распространенным и универсальным методом измерения 3H в воде и жидких биологических средах является жидкостно-сцинтилляционная спектрометрия с обогащением и без него [39, 68–82]. Современный рынок приборов представлен широким перечнем производителей таких систем, как Perkin Elmer, Hidex system, SDEC system, Hitachi system и др. Подобных систем достаточно для определения трития в жидкой фазе на низкофоновом уровне (около 0.1 Бк/л). Подробнее принципы измерений трития на данных приборах описаны в работе [51]. Для анализа низких концентраций трития были разработаны национальные стандарты с использованием чувствительного метода жидкостно-сцинтилляционной спектрометрии [83, 84]. При наличии примеси в жидкой пробе для анализа 3H применяется метод дистилляции [83]. Еще одним сверхчувствительным методом определения трития считается ускорительная масс-спектрометрия [53, 85].
Для оценки OBT в компонентах окружающей среды и биологических объектах в мировой практике в основном используются системы для подготовки проб типа оксидайзер и жидкостно-сцинтилляционная спектрометрия [39, 81, 82, 86, 87]. Обзор методов для определения OBT [57] и результаты их валидации представлены в работе [88]. При анализе OBT возможны проблемы контаминации, воспроизводимости, длительность проведения анализа и отсутствие эталонов. Кроме того, отмечались трудности в разделении E-OBT и NE-OBT [47].
Поскольку в настоящее время уровни активности трития в окружающей среде близки к фоновым значениям, особое внимание уделено аналитической процедуре для надежного обнаружения низких уровней NE-OBT [89]. Чрезвычайно важным моментом для повышения надежности измерения OBT стала инициация процедуры межлабораторных сравнений [90]. Это способствовало снижению неопределенностей в результатах анализа OBT и обеспечению более точных данных для валидации моделей OBT [91, 92]. Ниже представлены результаты научных изысканий по оценке содержания и основных закономерностей поведения трития в различных природных средах.
МОНИТОРИНГ ТРИТИЯ В ОКРУЖАЮЩЕЙ СРЕДЕ
Тритий является одним из наиболее подвижных радионуклидов, обладает высокой миграционной способностью в природных средах и крайне слабо удерживается современными очистными барьерами, что способствует его относительно свободному поступлению в окружающую среду с жидкими сбросами и газовыми выбросами объектов использования атомной энергии. Активность 3H в жидких сбросах многократно превосходит по абсолютному значению активность всех остальных нуклидов, а в газообразных выбросах уступает только активности радиоактивных благородных газов, которые в отличие от трития химически инертны [93]. Благодаря высокой способности к миграции в окружающей среде, относительно большому периоду полураспада (12.3 года) и, следовательно, продолжительному пребыванию в атмосфере и гидросфере, тритий переносится ветром на большие расстояния, поглощается водоемами или осаждается на земную поверхность осадками и может достаточно равномерно распределяться в биосфере.
ПОВЕДЕНИЕ ТРИТИЯ В АТМОСФЕРЕ
Тритий попадает в атмосферу в результате штатных и аварийных выбросов предприятий атомной промышленности (АЭС, заводы по переработке, испытательные полигоны и т.д.). Интенсивность поступления трития в атмосферу в результате штатных выбросов оценивается разными способами. Так, расчетными методами были оценены значения интенсивности поступления трития в атмосферу с поверхности промышленных водоемов ПО “Маяк” и его объемная активность [94]. Аналогичные работы были проведены и на Балаковской АЭС. В одной из публикаций в качестве источников поступления трития в окружающую среду служили баки запаса дистиллята [95]. Обнаружена функциональная зависимость скорости поступления трития при испарении дистиллята от температуры и влажности атмосферного воздуха. Рассчитаны вероятные значения объемной активности трития в воздушном пространстве баков при постоянной скорости инфильтрации наружного воздуха для реальных условий теплого и холодного периодов года [95]. Вторая работа [96] посвящена оценке поступления трития в атмосферу из брызгальных бассейнов. Помимо описания условий формирования газоаэрозольного облака тритированной воды над поверхностью брызгальных бассейнов в разные сезоны года, была выполнена оценка накопления трития в снежном покрове в районе расположения брызгальных бассейнов [96].
Другая группа публикаций посвящена оценке основных источников поступления трития в воздушную среду в ходе испытаний ядерного оружия на территории Семипалатинского испытательного полигона (СИП). На территории полигона техногенный тритий генерировался в результате различных видов взрывов, поэтому количество, пути поступления и его перераспределение в окружающей среде в каждом случае существенно различались. Наиболее загрязненными тритием площадками СИП являются “Дегелен” и “Атомное озеро” [97]. Оценка уровня газообразных соединений трития на территории СИП показала, что он присутствует в двух формах – окисленной (НТО) и газообразной (HT). Наименьшая концентрация трития в воздушной среде отмечена в местах проведения наземных и воздушных взрывов (площадка “Опытное поле”), а максимальная – после подземных ядерных испытаний (площадка “Балапан”). Поскольку удельная активность трития в поверхностном слое почвы в этом случае достигала десятков тысяч Бк/кг, то почва может выступать в роли источника поступления HТ [98] или HTO в атмосферу [99]. Обсуждаются возможные механизмы этого явления [100] и, в частности, роль бактерий в окислении НТ. Однако вклад бактериального окисления в образование HTO в почве не превышает 10%, что составляет менее 0.1% от исходного поступления HTO в атмосферу [99].
Содержание трития в воздухе оценивается, как правило, по трем химическим формам (HTO, HT и CH3T). В ряде работ [101, 102] показано, что фоновые уровни объемной активности трития в воздухе малы и не достигают даже 1 Бк/м3: для объемной активности HTO отмечены сезонные колебания, поскольку она связана с изменениями влажности воздуха; для HT и CH3T такой закономерности не обнаружено [101]. В рамках проекта VATO было проведено многолетнее исследование поведения трития в окружающей среде, включающее почасовой сбор данных о концентрациях 3H для верификации моделей переноса и оценки его физико-химических форм [103]. Показано, что вблизи завода по переработке ОЯТ (Франция) наблюдалась высокая среднечасовая изменчивость концентраций HT (0.01–28.7 Бк/м3) и HTO (0.01–5.4 Бк/м3) в атмосфере, а также HTO в дождевой воде (1–300 Бк/л). Эти данные свидетельствуют о значительном превышении концентрации трития в осадках по сравнению с воздухом.
Значительная часть работ по мониторингу трития в атмосфере касается дождевых и снеговых осадков. Роль атмосферных осадков в распространении 3H подтверждается положительной корреляцией между выпадением трития и абсолютной влажностью атмосферы [104]. Информацию о содержании трития в осадках аккумулирует Всемирная сеть мониторинга изотопов водорода и кислорода в осадках (GNIP, https://www.iaea.org/services/ networks/gnip), созданная МАГАТЭ и ВМО в 1960 г. Анализ временны́х и пространственных изменений содержания изотопов в осадках (18О, 2Н и 3Н) позволяет использовать эти данные для гидрологических исследований в рамках инвентаризации, планирования и освоения водных ресурсов, а также для прогнозирования глобальных климатических изменений [105]. В настоящее время глобальная модель для прогнозирования концентрации трития в осадках (MGMTP) была модифицирована и значительно уточнена, поскольку охватила временно́й период с 1960 г. до наших дней [106]. В результате применения инструментов машинного обучения обнаружено, что такие масштабные циклические гидроклиматические процессы, как Североатлантическая осцилляция и Тихоокеанская декадная осцилляция, сглаживают влияние глобальных климатических изменений [105].
В ряде исследований [74, 107–114] в результате многолетних измерений трития в осадках США, Канады, Европы, Австралии и Азии показаны сезонные колебания его активности с максимумом в весенний период (так называемый феномен “весенней утечки”), достигающие семикратного превышения по сравнению с осенью и зимой [114]. В глобальной системе MGMTP сезонный цикл содержания трития в осадках смоделирован в виде простой функции косинуса с пятью параметрами [106]. Тритий в виде HTO, попадающий в атмосферу в зимний период, может внести значительный вклад в загрязнение снега, который осаждается на земную поверхность, загрязняя ее, а также подземные и поверхностные воды. Низкая скорость диффузии трития в сухом и холодном снеге ((1–2) × 10–10 м2/с) по сравнению с водой (на порядок выше) приводит к тому, что тритий накапливается в снежном покрове в течение всей зимы. Во время весеннего таяния снегов скорость диффузии вырастает до 6 раз [108].
Многолетние исследования показали, что максимальное содержание трития в осадках весной было связано со складчатостью тропопаузы, а минимальные уровни летом – с преобладающим притоком морского воздуха. В то же время из-за влияния морской влаги концентрация трития в осадках снижается по направлению к побережью и не подвержена эффекту сезонности [112]. В тех случаях, когда максимальные значения были характерны для осадков летнего периода, это указывало на стратосферный источник 3H [74]. Такое многолетнее повышение объемной активности трития в атмосферных осадках в теплый период отмечено на территории РФ [115], что связано с усилением вертикальной циркуляции воздуха в данный период года и облегчает поступление 3H из верхних слоев атмосферы, где он образуется под влиянием космического излучения, в приземный слой. В целом среднемесячная величина объемной активности трития в атмосферных осадках по территории РФ за период 2014–2019 гг. варьировала в пределах 1.1–2.4 Бк/л при среднегодовом значении 1.7 Бк/л [115]. На распределение 3H в пространстве также влияют направление ветра, количество осадков, количество выбросов в атмосферу и коэффициент атмосферной дисперсии [109, 114]. Основные закономерности пространственного распределения трития в осадках Японии после испытаний ядерного оружия в Северной Корее в 2016 г. показаны в работе [111].
Фоновые уровни удельной активности трития были исследованы в снежном покрове бассейна р. Вилюй (Республика Саха (Якутия)). Показано, что в период до аварии на АЭС Фукусима (ФАЭС-1) накопление 3Н в снежном покрове происходило в результате регионального атмосферного переноса [116], а его концентрация соответствовала референтным значениям (11.3 TE, или 1.3 × 103 Бк/м3), характерным для чистого снега Южного полюса [117]. После аварии 2011 г. содержание 3Н в этом регионе возросло почти в 3 раза [116, 118]. В то же время удельная активность трития в осадках, выпавших на расстоянии 170–220 км от ФАЭС-1, в первые две недели после аварии составила 1.5 × × 103 Бк/м3, что превышало локальный доаварийный уровень (6 TE, или 0.7 × 103 Бк/м3) в 2 раза. В течение пяти недель концентрация трития в осадках достигла доаварийных значений [119]. Внутри зоны отчуждения ФАЭС-1 в период с 2013 г. по 2014 г. следов 3H в пробах почвы не было обнаружено [120].
Чернобыльская авария 1986 г. не повлекла за собой значительного выпадения трития с осадками в городах Европы и Японии, хотя в первые дни после аварии были обнаружены значительные количества других радионуклидов [121]. В Финляндии превышение фонового уровня в 30 и сотни раз за счет чернобыльских 14С и 3Н в приземном воздухе было отмечено в данный период, но не привело к повышению содержания этих радионуклидов в растениях, дождевой воде и поверхностных водах [122]. Аналогичные данные приводятся для Польши [123]. В Югославии на станции МАГАТЭ пик активности трития в осадках наблюдался 2 мая, а в питьевых скважинах не изменился [124].
Основные эмитенты техногенного трития в окружающую среду Уральского региона и ежегодное количество штатных выбросов в период с 2002 г. показаны на рис. 5. Фактическое поступление 3Н в окружающую среду за этот период ни разу не превышало разрешенные уровни [36]. Исследования поступления 3Н на земную поверхность [36, 125–127] показали, что концентрация изотопа в дождевых осадках района воздействия ПО “Маяк” (рис. 6) и Белоярской АЭС (БАЭС) варьировала в пределах 3–4 порядков, значительно превышала уровень глобального (1 Бк/л) и техногенного (5 Бк/л) фонов, однако не достигала уровня вмешательства (7600 Бк/л), установленного для питьевой воды [128]. Максимальная объемная активность трития в снежном покрове зоны влияния ПО “Маяк” в осенне-зимний период составила 110 Бк/л и уменьшалась по мере отдаления от предприятия [129]. Аналогичные результаты по экспоненциальному снижению трития в осадках в зависимости от расстояния до источника выбросов были получены и другими авторами [104, 109, 114, 130–132]. Кроме того, в работе [130] обобщены данные многолетнего мониторинга 3Н в снеговом покрове района воздействия ПО “Маяк”, БАЭС и района падения отделяющихся частей ракет-носителей “Союз”. Содержание 3Н в районе падения отделяющихся частей ракет-носителей незначительно превышает уровень техногенного фона. В ходе экспериментальных работ и методов моделирования уточнены процессы окисления 3Н в ненасыщенном слое почвы, миграции в водоносном слое, вымывания из атмосферы каплями дождя и переноса в атмосфере [133]. Небольшой раздел посвящен тритию также в атласе ВУРСа и Карачаевского следа [134].
Рис. 5.
Выбросы трития в атмосферу (верхний ряд: 1 – разрешенный; 2 – фактический) и сбросы со сточными водами в открытую гидрографическую сеть (нижний ряд: 3 – разрешенный; 4 – фактический) предприятий атомной промышленности, которые вносят основной вклад в формирование техногенного радиационного фона wв Уральском регионе. Использованы данные ежегодников “Радиационная обстановка на территории России и сопредельных государств”, издаваемых НПО “Тайфун” в 2004–2020 гг.
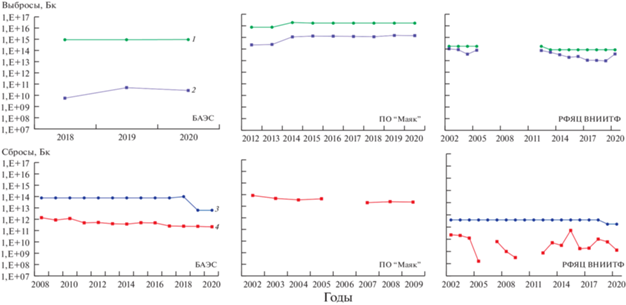
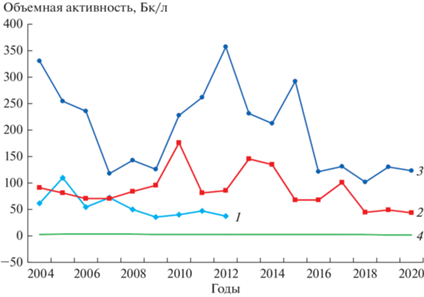
Рис. 6.
Динамика объемной активности 3H в атмосферных осадках и в р. Тече в зоне наблюдения ПО “Маяк”. Использованы данные ежегодников “Радиационная обстановка на территории России и сопредельных государств”, издаваемых НПО “Тайфун” в 2004–2020 гг.: 1 – атмосферные осадки (пос. Новогорный); 2 – р. Теча (пос. Затеченское); 3 – р. Теча (пос. Муслюмово); 4 – фоновый уровень.
Уникальные данные по содержанию трития в снеговых осадках (глубиной 245 см) были получены на станции Восток, расположенной в Антарктике [135]. Тритий в составе воды (HTO) является единственным индикатором ее возраста. Повышенный уровень трития в окружающей среде, сформировавшийся в результате испытаний ядерного оружия, дает возможность отследить его динамику в течение 100 лет [136]. Несмотря на то, что к 90-м годам XX в. содержание трития вернулось к естественным равновесным уровням, существовавшим до испытаний [112, 137], техногенные выбросы трития становятся более заметными, что может увеличить погрешность при определении возраста воды [111]. Благодаря индикаторным возможностям трития удалось датировать образцы на станции Восток, начиная с 1955 г., и оценить его максимальную активность (1414–3153 TE, или 167–372 Бк/л), соответствующую 1966–1968 гг. Из-за короткого времени пребывания воды в тропосфере тритий быстро вымывается c осадками. Кроме того, в полярных областях закачка трития из стратосферы в тропосферу может быть увеличена из-за низкого уровня тропопаузы (8 км) по сравнению со средними и экваториальными областями (14 км), а также вследствие менее интенсивной температурной инверсии в зимний период [135]. Выпадение трития в Антарктиде, видимо, происходит в результате прямого выброса стратосферного трития зимой, однако его выпадение в Арктике является результатом преобладающего весеннего нагнетания стратосферного воздуха на средних широтах, что соответствует вкладу других стратосферных индикаторов [138]. Это хорошо согласуется с данными о том, что концентрация трития в осадках Австралии [136] и Кореи [112] достигла максимума в 1963 г., что соответствует периоду интенсивных испытаний ядерного оружия.
Лесные массивы представляют собой сложные системы, в которых можно моделировать потоки переноса HTO, учитывая многообразные процессы (осаждение, дыхание растительности и почвы, испарение HTO и т.д.) и их взаимодействия в неоднородной лесной среде [139]. В этой сложной системе характер рассеивания значительно меняется из-за смены режимов потока над и под пологом леса, переноса потока НТО через границу полога, а также его неоднородности. Используя модель связанной дисперсии, была проведена оценка переноса НТО над лесом, а также внутри лесного полога и в подлеске для всего спектра метеорологических условий. На основании экспериментальных данных оценены ключевые параметры переноса HTO в зимних условиях (скорость сухого осаждения HTO в снег, коэффициент вымывания HTO снегом, скорость осаждения на сосновые иголки). Скорость повторного переноса HTO из снега в атмосферу оценивается как очень низкая. Измеренные запасы трития в снеге хорошо согласуются с результатами моделирования атмосферной дисперсии трития, полученной по данным мониторинга после случайного выброса трития в атмосферу [140].
ПОВЕДЕНИЕ ТРИТИЯ В ВОДНЫХ ЭКОСИСТЕМАХ
По аналогии с оценкой загрязнения атмосферы некоторыми изотопами в 2002 г. МАГАТЭ создало Всемирную добровольную программу наблюдения за окружающей средой – Глобальную сеть изотопов в реках (GNIR). Программа посвящена сбору, обобщению и распространению результатов изотопных анализов речных вод Земли (https://www.iaea.org/services/networks/gnir). Также МАГАТЭ разработало сайт для сотрудничества в области изотопной гидрологии, на котором сосредоточена информация по широкому спектру вопросов, связанных с водой, включая специализированные научные публикации, программное обеспечение, проекты координированных исследований, учебные материалы и межлабораторные калибровки (https://www.iaea.org/resources/ isotope-hydrology-collaboration-site).
Важным аспектом поведения трития в окружающей среде, и в частности в морских и пресноводных экосистемах, является его взаимодействие с органическими веществами. Это обусловлено сродством трития с органическим веществом, поэтому он быстро уравновешивается растворенными органическими лигандами и взвешенными твердыми частицами и отложениями. Поскольку изотопная дискриминация между 3H и H мала [141, 142], OBT и HTO должны показывать одинаковое соотношение 3H/H в стационарных условиях. Так, было показано [142], что перенос трития из HTO в OBT приводит к сохранению отношения 3H/H, которое примерно равно 1 × 10–16. Хотя ранее было высказано иное мнение [143], утверждающее, что большинство химических реакций дискриминируют включение либо трития, либо дейтерия в пользу водорода, поэтому маловероятно, что произойдет эффект концентрации.
Доказательством некоторой дискриминации между легкими и тяжелыми изотопами водорода служит отношение удельной активности ниже единицы, поскольку OBT не уравновешивалось с TFWT или HTO [144]. Отметим, что некоторая доля сорбированного трития ассоциируется с белковым материалом, который потенциально доступен для живых организмов, питающихся отложениями [145]. Так, в условиях лабораторного эксперимента изучена сорбция трития природной гуминовой кислотой в зависимости от времени экспозиции, концентрации кислоты и температуры [146]. Установлено, что примерно 10% трития входит в состав органического вещества грунта. Основным его стоком является тритиевая вода в составе капиллярной и адсорбированной форм влаги. Эти результаты хорошо согласуются с данными работы [147]. Максимальное связывание трития гуминовыми кислотами наблюдается в первые 3 дня после попадания трития в почву [148]. Способ очистки тритиевой воды был запатентован [149].
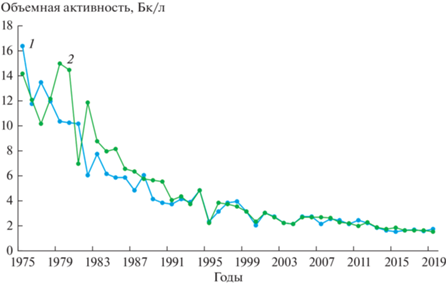
Обобщенные данные о содержании трития в речных водах по сравнению с атмосферными осадками, выпавшими на территории бывшего СССР и России за период с 1975 г., приведены в обзоре [150] и ежегодниках Росгидромета [36, 151]. Для всего периода наблюдений (рис. 7) характерно снижение среднегодовых фоновых значений объемной активности трития в атмосферных осадках, что связано с постепенным истощением стратосферного резервуара трития, сформировавшегося в период ядерных испытаний. Поскольку содержание трития в речной воде коррелирует с его концентрацией в атмосферных осадках (R2 = 0.84, p = 0.00001), для последних лет наблюдений характерна минимальная объемная активность трития в поверхностных водах. В обзорной публикации [150] рассмотрены также меридиональные закономерности распределения трития в речных водах и его сток. Показано, что в местах расположения радиационно-опасных объектов наблюдается повышенное содержание трития в природных водах. При этом при соблюдении общих правил безопасной эксплуатации предприятий атомной промышленности и разумном водопользовании сбросы трития от проектируемых АЭС могут с запасом удовлетворять требованиям, установленным в Нормах радиационной безопасности (НРБ-99/2009) [152].
В ряде работ были обобщены фоновые уровни содержания трития в открытых водоемах в районах проектируемых АЭС или их гидротехнических сооружений: Белорусской [69], Балтийской [153], Руппур (Бангладеш) [80]. Ведется мониторинг различных компонентов водных экосистем в районах: 1) действующих предприятий атомной промышленности – АЭС Циньшань на побережье Восточно-Китайского моря [132], АЭС Пакш на р. Дунай и Крскинской АЭС на р. Сава [75], АЭС Темелин на р. Влтава и р. Эльба, АЭС Дукованы на р. Дунай [154], АЭС Аско на р. Эбро [72] и прибрежной зоны восточной части Финского залива, бассейна Невы и Ладожского озера [155], Белоярской АЭС [156]; 2) остановленных и подготовленных к демонтажу АЭС: Крей-Мальвиль на левом берегу р. Роны [157], Игналинской АЭС около оз. Друкшяй, а также Балтийского моря, Куршского залива и р. Нямунас [73]. На примере Игналинской [73] и Белоярской АЭС [156, 158–160], в зоне влияния которых с 1980 г. проводится непрерывный радиоэкологический мониторинг, было показано, что после вывода из эксплуатации Игналинской АЭС концентрация 3H упала до фоновых значений [73], а на Белоярской АЭС в связи в выводом из эксплуатации второго энергоблока в 1989 г. его содержание существенно снизилось [156, 159, 160].
Кроме постановки фундаментальных задач при проведении мониторинговых исследований по содержанию трития в водных экосистемах, возможен поиск прикладных аспектов радиоэкологических работ, как это было показано в публикациях [72, 154]. В прикладных исследованиях тритий был использован в качестве радиоактивного индикатора (трейсера) миграции инфильтрата с полигонов бытовых отходов [161], для определения коэффициента продольной дисперсии и скорости вод рек [72], для датирования с целью анализа разных сценариев формирования вертикальной структуры вод Каспийского моря после крупномасштабной гравитационной конвекции в Среднем Каспии, вызванной аномальным охлаждением поверхностных вод в конце зимы 1976 г. [162], для оценки возраста и источников формирования водоносных горизонтов, используемых для водоснабжения городов [163] и т.д.
Потенциальными источниками поступление трития в экосистемы Сибирского региона являются глобальное загрязнение окружающей среды и деятельность Горно-химического (ГХК) и Сибирского химического комбинатов. Однако деятельность ГХК оказывает влияние на содержание трития в водных экосистемах р. Енисей только в ближней зоне расположения предприятия. Так, фоновые уровни содержания 3H в воде составили около 4 Бк/л, а в донных отложениях – около 2 Бк/кг [164]. С помощью трития исследован водообмен между поверхностными водами р. Большая Тель (приток Енисея) и радиоактивно загрязненными подземными горизонтами полигона “Северный” [165]. В окрестностях г. Томска также была оценена удельная активность трития в техногенной и природной воде [166].
В Уральском регионе основными источниками поступления трития в водные экосистемы являются БАЭС, ПО “Маяк” и РФЯЦ ВНИИТФ [36]. Так, в 1949–1956 гг. ПО “Маяк” осуществлял выпуск регламентных и аварийных радиоактивных отходов в открытую гидрографическую сеть р. Течи. В Теченском каскаде водохранилищ (ТКВ), который в настоящее время используется для хранения низкоактивных жидких радиоактивных отходов, современные уровни объемной активности трития варьируют в пределах 763–5935 Бк/л [167]. Содержание 3Н в верховье р. Течи, ее притоках и обводных каналах составляло 240 ± 33 Бк/л [168]. За последние 17 лет (см. рис. 6) объемная активность 3Н в реке на расстоянии 78 км (Муслюмово) и 237 км (Затеченское) от источника загрязнения изменялось от 101 до 355 Бк/л и от 43 до 175 Бк/л соответственно. По данным работы [150], диапазоны изменчивости еще шире и составили 70–585 Бк/л (Муслюмово). Удельная активность трития в водоемах комплексного назначения, расположенных в радиусе 90 км от ПО “Маяк”, варьировала от 7 до 228 Бк/л и не достигала уровня вмешательства, определенного для питьевой воды. Закономерность, характерная для атмосферных поступлений трития (снижение концентрации по мере удаления от источника выбросов), подтвердилась как для континентальных [127, 160], так и для морских [132] экосистем. В целом в настоящее время отмечается снижение содержания трития в озерах зоны влияния ПО “Маяк” в 3–16 раз по сравнению с 80-ми годами прошлого столетия [169].
Исследования, проведенные на территории Семипалатинского испытательного полигона (СИП), свидетельствуют о том, что грунты и донные отложения “Атомного озера”, сформировавшегося в результате термоядерного взрыва 1965 г., являются основным источником загрязнения тритием маловодной р. Шаган с притоком р. Ащису (левобережный приток р. Иртыш) за счет подземных вод, поступающих в русло реки [170]. Концентрация трития в соленых озерах была выше, чем в Иртыше, при этом зависимость между 2H и 18O была близка к глобальной линии метеорных вод [70]. Максимальная активность трития в весенний период на территории СИП была обнаружена в р. Шаган в 5 км от “Атомного озера” и составила 2 × 105 Бк/л [171].
Авария на ЧАЭС в 1986 г. привела к краткосрочному повышению содержания 3H в водных экосистемах [172]. В период 1992–1994 гг. изучено содержание трития в природных водах Украины, которое составило 3.5–5.2 Бк/л. Повышение концентрации 3H весной 1994 и 1995 гг. зарегистрировано в технологических водоемах и системах водообеспечения Чернобыльской АЭС – р. Припять [173]. Причинами этого явления могли быть также Хмельницкая и Ровенская АЭС, оснащенные реакторами типа ВВЭР и расположенные в бассейне этой же реки [172, 174]. Интегральный запас 3H в водоеме-охладителе ЧАЭС составил (12.1–18.6) × 1012 Бк [173].
Авария, произошедшая 11 лет назад на ФАЭС-1, привела к загрязнению морской воды 3H, концентрация которого в 6 раз превышала доаварийный уровень непосредственно около побережья [175]. Ряд исследователей указывает на роль морских течений в распространении трития в Северной части Тихого океана [60, 175–177]. Получены данные [178] по сезонной изменчивости циркуляции вод в зимне-весенний период на основе общепринятой летне-осенней циркуляции вод в Чукотском море и связанным с этой изменчивостью перемещением трития. Также было показано относительно высокое содержание трития в ядре теплого синоптического вихря Куросио [60]; за счет прибрежных течений вода, загрязненная более высокими концентрациями трития, распространилась вдоль побережья как к северу, так и к югу от ФАЭС-1 [175]. По данным [175], сразу после аварии на ФАЭС-1 прямой сброс 3H в океан составил примерно 0.05 × 1015 Бк, а по другим оценкам – (0.7 ± 0.3) × 1015 Бк [179], что значительно меньше, чем общее содержание трития в окружающей среде. В настоящий момент важность и необходимость проведения непрерывных мониторинговых исследований морских экосистем (морская вода, донные отложения и морская биота) в районе аварии на ФАЭС-1 связаны с утечками трития из резервуара с загрязненной водой, произошедшими в 2013–2014 гг. [180]. Вода в резервуаре представляет собой комбинацию восстановленных подземных вод и охлаждающей воды, которая стала загрязненной 3H, 14C, 99Tc, 125Sb, 60Co, 106Ru, 137Cs, 134Cs, 90Sr и 129I при взаимодействии с активной зоной ядерного реактора. Утечка трития широко распространилась по водонепроницаемому слою под площадкой ФАЭС-1 [181].
ПОВЕДЕНИЕ ТРИТИЯ В НАЗЕМНЫХ ЭКОСИСТЕМАХ
Загрязнение тритием компонентов наземных экосистем сопряжено с атмосферными выпадениями, проведением подземных ядерных взрывов (ПЯВ) и последующим вымыванием трития грунтовыми и поверхностными водами с выходом в верхний слой почвы [182, 183]. Вблизи открытых поверхностных водотоков и водоемов действуют оба механизма поступления трития в снежный покров (атмосферный и эманация из подстилающей поверхности почвенного покрова). В этом случае загрязнение тритием объектов окружающей среды ограничивается пределами русла водотока или водоема, и на расстоянии 200–300 м от водного объекта наблюдаются фоновые концентрации изотопа [182, 183]. На участках ПЯВ СИП было показано [184], что, если концентрация трития в приземном слое снега выше, чем в поверхностном, это свидетельствует об эманации трития из почвы. Причинами образования трития в местах проведения эксгумационных взрывов может быть процесс нейтронной активации, т.е. ядерные реакции на изотопах лития, бора и азота, присутствующих в почве, а также захват трития, изначально присутствовавшего в заряде, минеральными частицами, образующимися при конденсации из раскаленной зоны взрыва [185].
В районе СИП тритий был представлен в почве следующими формами: 3Н в поверхностно-адсорбированной воде, 3Н в межслоевой воде, гидроксильный, органически связанный, кристаллически связанный [186] и прочносвязанный [187]. Распределение прочносвязанного 3Н было изучено в местах проведения наземных и подземных ядерных испытаний СИП. Установлено, что распределение 3Н в почве специфично для каждой исследуемой площадки и зависит от мощности заряда и характера проведенного испытания [187]. На примере мирных ПЯВ “Кратон-3” и “Кратон-4” (Якутия) показано, что из зоны взрыва на поверхность земли по трещиноватой зоне разлома и ослабленной зоне вокруг боевой скважины выходят напорные подземные рассолы с радионуклидами [188–190].
В районе влияния ПО “Маяк” проведено однократное исследование миграции трития по цепочке “снег–талая вода–растение” [191]. Обнаружено отсутствие значимой зависимости между объемной активностью трития в снеге и березовом соке и ее наличие между активностью трития в талой воде и березовом соке. Аналогичные данные были получены и по г. Томску [166]. Пространственное распределение содержания трития в пробах снега и березового сока позволяет сделать вывод о том, что в начале вегетационного сезона деревья потребляют в основном талую воду. Однако березовый сок несет в себе изотопный след не только текущего, но и предшествующего года, так как в начале сезона роста деревья активно используют запасенные пластические вещества [192]. В ходе многолетних изысканий миграции трития в зоне влияния ЧАЭС по цепочке “талая вода снегового покрова–растение” было показано [193], что при постоянном поступления 3Н в окружающую среду его удельные активности в составе свободной воды и органически связанного 3Н нарастают во времени полиномиально (с порядком полинома больше 4), достигая максимума в зимне-весенний период.
Различная активность трития в составе свободной воды растений может быть обусловлена процессами их жизнедеятельности с учетом погодных условий и состава почвы, на которой произрастает растение. Так, снижение удельной активности 3Н в березовом соке происходило при повышении температуры воздуха. В то же время тритий, доходящий с талой водой до глинистого грунта, мог участвовать в замещении атомов водорода некоторых глинистых минералов. И в этом случае отмечены температурные зависимости: похолодание замедляло, а потепление ускоряло такой обмен, поэтому часть 3Н с талыми водами аккумулировалась в почве [193]. Обобщение данных по содержанию трития в поверхностной влаге почвы около хранилища низкоактивных отходов Лос-Аламосской национальной лаборатории указывает на сезонные и суточные циклы, которые положительно коррелировали с температурой окружающей среды [194]. Экспоненциальное снижение 3Н в зависимости от расстояния до источника выброса, упомянутое нами выше и характерное для распределения трития в атмосфере и водных экосистемах, показано и для березового сока [191]. Однако содержание трития в наземных экосистемах, в частности в почве, связано не столько с расстоянием до источника выброса, сколько определяется преобладающим направлением ветра во время дождя [195, 196].
Особый интерес представляет оценка концентрации OBT в почве, поскольку почва является долгосрочным резервуаром органически связанного трития [195]. Так, содержание OBT в почве импактных участков превышало HTO и было аккумулировано в верхнем 0.5 см слое. Для OBT в отличие от HTO сезонной зависимости не было обнаружено. Кроме того, концентрация OBT в почве демонстрирует меньшую пространственную изменчивость по сравнению с HTO [197].
Существует относительно хорошая корреляция между влажностью воздуха и OBT, но в свободной воде часто наблюдается более низкая концентрация трития, что связано с большим вкладом почвенной воды [196]. При этом концентрация трития во влаге почвы выше, чем в осадках [131]. По данным других исследователей [198], и на фоновых, и на импактных площадках концентрация OBT в почве превышала HTO, однако вне зоны влияния предприятий атомной промышленности отношение OBT/HTO варьировало от 2.7 до 15, а в зоне влияния оно отклонялось от ожидаемого среднего, равного 0.7. Это значение используется в моделях переноса трития в окружающей среде и, по мнению [198], должно быть пересмотрено. Таким образом, органически связанный тритий, содержащийся в почве, сохраняет следы исторических выбросов изотопа и может быть использован для построения долговременных прогнозных моделей его поведения в окружающей среде [199].
Важным аспектом поведения трития в окружающей среде является его взаимодействие с органическими веществами, в частности с гуминовыми и фульвокислотами. Для измерения возраста подземных вод и проектирования мест захоронения ядерных отходов важно понимать сорбционное поведение трития в почве. На изученных типах почвы (илистые глины, илистый песок и осадочная горная порода – лесс) коэффициент распределения 3Н не зависел от начальной удельной активности, времени адсорбции, соотношения вода/твердое вещество, pH и содержания гуминовых и фульвокислот. Относительно небольшую сорбцию трития (0.1–0.2 мл/г) почвами необходимо учитывать при изучении миграции трития в окружающей среде [200].
СКВАЖИНЫ, КОЛОДЦЫ, ПОДЗЕМНЫЕ И ПОВЕРХНОСТНЫЕ ВОДЫ
На территории бывшего СИП наиболее высокие концентрации трития, достигающие 105 Бк/л, обнаружены в некоторых пробах поверхностных и грунтовых вод [201]. В целом удельная активность дейтерия и трития в поверхностных и подземных водах СИП была типичной для современных изотопных фонов природных вод Казахстана [70]. В большинстве случаев концентрация трития в водах скважин была ниже, чем в озерах (<10 Бк/л). Уровни трития в бытовых колодезных водах незначительно превышали фоновые значения показателя для поверхностных вод [202]. Выявлены закономерности современного поступления загрязненных 3Н подземных вод в р. Шаган [203]. Экспорт трития из подземных ядерных полигонов и испарение воды являются важными детерминантами концентрации 3Н в стоячей воде СИП [70].
Содержание 3Н было также исследовано в поверхностных водах площадки боевой скважины мирного ПЯВ “Кристалл” и подземных рассолах рудника кимберлитовой трубки “Удачная” (Якутия). Максимальная объемная активность 3Н (13.4 Бк/л) установлена в подземных рассолах, что в 560 раз ниже уровня вмешательства для питьевой воды (7600 Бк/л) и в 7 раз выше регионального фона в речной воде [204]. После прекращения массовых испытаний ядерного оружия (с 1963 г.) концентрация трития в атмосфере снижалась быстрее, чем это могло бы произойти в результате естественного распада, что связано с вымыванием трития в океаны и грунтовые воды [136].
В ряде работ [160, 205, 206] приводятся результаты многолетних исследований содержания трития в питьевой воде (колодцы, скважины, сетевое водоснабжение) в районах расположения Белоярской АЭС и ПО “Маяк”. В большинстве случаев вода из скважин была чище, чем из центрального водопровода, при этом в пос. Новогорный и Касли было зарегистрировано превышение уровня техногенного и глобального фона 3Н (2.2 ± 0.7 Бк/л) до 80 раз [160]. Систематические (с 1970 г.) наблюдения за миграцией техногенных радионуклидов в подземных водах района воздействия ПО “Маяк” через систему более 480 гидрогеологических наблюдательных скважин с разной глубиной залегания показали, что источником 3Н могут быть фильтрующиеся воды из оз. Карачай, поскольку вещества, содержащие тритий, не сорбируются грунтами и поступают в водоносный горизонт. За 40 лет эксплуатации объекта поток в южном направлении распространился на 2.5–3 км и достиг р. Мишеляк [207]. В целом показана обратная зависимость между концентраций трития в питьевой воде и расстоянием от источника загрязнения и глубиной залегания воды [205]. Аналогичные результаты были получены при исследовании колодезной воды в районе воздействия АЭС Циньшань [132]. Это подтверждает возможность проникновения трития в питьевые источники в районах расположения предприятий атомной промышленности через внутригрунтовый сток [206]. При этом анализ поверхностных и грунтовых вод из дозиметрических скважин вокруг емкостей с жидкими радиоактивными отходами и хранилища для ОЯТ не выявил наличие каких-либо радионуклидов, в том числе трития, что может свидетельствовать о целостности защитных барьеров [208]. В то же время в районе расположения спецкомбината “Радон” было показано [209], что при контакте поверхностных вод с 3H-содержащими твердыми РАО в емкости хранилищ образовались жидкие тритиевые отходы активностью 105–107 Бк/кг. Это представляет потенциальную опасность для загрязнения гидрологической сети, поскольку в контрольных скважинах, расположенных в зоне строгого режима, был выявлен тритий.
В районе аварии на ФАЭС-1 относительно высокие концентрации трития были обнаружены в подземных водах (в скважинах с питьевой водой) вблизи станции [119, 210], что связано с повышенным содержанием трития в осадках после аварии [210]. При этом концентрация 3Н в осадках была ниже предельно допустимых значений ВОЗ для питьевой воды и вскоре окончательно снизилась до фонового уровня за счет перемешивания с грунтовыми водами [119, 210]. Для датирования времени попадания трития в подземные воды района воздействия ЧАЭС была разработана модель на основе соотношения 3H/3He. Она позволяет напрямую измерить время, прошедшее с момента последнего газообмена подземных вод с атмосферой с учетом максимальной скорости миграции около 200 мм/год [211]. В районе действующей АЭС в Бангладеш [80] содержание трития в подземных водах, предназначенных для питья, было ниже уровня вмешательства. Показана также сезонность в уровнях трития в районах подпитки подземных вод [112]. Наибольшая концентрация трития в почвенной влаге наблюдалась в мае и июне, когда относительная влажность была высокой [131]. В Калифорнии засуха в 2014 г. привела к снижению содержания трития в поверхностных водах, что связано с их разбавлением грунтовыми водами [110].
Фоновые концентрации стабильных изотопов (δ18О и δ2Н) и 3H были изучены в подземных водах Горного Крыма. Соотношение изотопов соответствовало локальной линии метеорных вод. Формирование подземных вод обусловлено инфильтрацией атмосферных осадков [212]. Показано также, что в водоносных зонах трещиноватости время водообмена быстро возрастает с глубиной и ниже 40–50 м уже превышает 150–400 лет [213]. Моделирование потока подземных вод и переноса трития из гипотетического реактора АЭС было проведено с использованием FEFLOW 5.0 и учетом данных мониторинга уровня воды [214]. Показано, что наибольшая активность трития в подземных водах (160 Бк/л) и напорном водоносном горизонте (0.4 Бк/л) достигается через 10 лет и не превышает безопасных уровней.
НАКОПЛЕНИЕ ТРИТИЯ БИОТОЙ
В моделях переноса трития в окружающей среде предполагается, что OBT образуется непосредственно из TFWT. Однако следует учитывать, что измеренные отношения OBT/HTO в образцах изменчивы и обычно выше ожидаемых значений. Кроме того, не совсем ясен путь передачи HTO из почвы к растению в динамике [215], хотя HTO – хорошо усваиваемая растениями форма трития [99], в том числе из влаги воздуха [216]. Вопросы об обменном и необменном OBT актуальны, и лучшее понимание связи между общим и необменным OBT, вероятно, приведет к снижению оценки дозы, уравновешивая другие неточности [217]. Также следует подчеркнуть, что в глобальном масштабе в наземной пищевой цепочке увеличения концентрации за счет выбросов НТО не происходит.
ТРИТИЙ В НАЗЕМНЫХ РАСТЕНИЯХ
В дискуссиях о будущем ядерной энергетики подчеркивается необходимость менее консервативной, но надежной оценки радиационных последствий аварийных выбросов трития. Разработка стандартной концептуальной модели аварийных выбросов 3H должна основываться на анализе баз данных экспериментов. HTO поступает в растения путем поглощения листьями (аэральный путь поступления) и корнями и превращается в обменные (E-OBT) и необменные (NE-OBT) формы OBT. Две формы (TFWT и E-OBT) описывают атмосферные поступления трития, поскольку они находятся в равновесии с влажностью атмосферы и почвы. Однако NE-OBT тесно связан с органическим веществом и обеспечивает интегрированный учет атмосферного трития во время фазы роста растительности [89]. Принято считать, что включение трития в органические вещества растений происходит главным образом за счет фотосинтеза. Некоторое количество TFWT может стать связанной с органическими компонентами растения в результате обменных реакций. При кратковременном воздействии удельная активность OBT листьев составляет лишь небольшую часть от TFWT. Эта доля снижается с уменьшением скорости фотосинтеза и степени воздействия [218].
Соотношения OBT/HTO в сельскохозяйственных культурах демонстрируют большую изменчивость в зависимости от динамически меняющихся условий [219]. Нерегулярные или пиковые выбросы трития еще больше усложняют прогноз образования OBT [220]. Это связано с тем, что перенос трития из атмосферы в растения и последующее преобразование в OBT – длительный процесс, который зависит от пространственного распределения, сезонных колебаний, изменчивых метеоусловий, характеристик растений, динамики стока [221–223]. Так, было показано [223], что концентрации OBT и TFWT значительно выше у растений, растущих с подветренной стороны от источника поступления трития, чем с наветренной, подтверждена корреляция между активностью трития в зерновых культурах и фруктах и преобладающим направлением ветра в вегетационный период, а также расстоянием до источника выброса [46, 224]. В разное время года TFWT у растений достигала пика зимой и летом, в то время как OBT непрерывно возрастала при смене сезона с весны на зиму [223]. Отметим, что испытания ядерного оружия в 1963–1965 гг. привели к максимальному загрязнению 3Н торфа Центрального Ямала, датированного этим периодом с помощью 14C [192]. В то же время в районе аварии на ФАЭС-1 следов 3H в пробах растений не было обнаружено [120]. В целом объективная оценка соотношения OBT/HTO возможна при наличии обширного набора данных, описывающих все аспекты динамически меняющихся условий, и последующего моделирования [219].
Миграция трития в растения изучается с особым интересом, поскольку фотосинтезирующие растения являются основными продуцентами наземных экосистем, основой пищевой цепочки и, таким образом, прямо или косвенно играют ключевую роль в питании человека [225]. В ходе экспериментальных исследований было показано [226], что концентрации TFWT в тканях листьев китайской капусты и редиса были значительно ниже расчетных равновесных концентраций. Кроме того, воздействие трития на ранних стадиях развития растений (фаза активного роста) приводило к высокой концентрации TFWT у китайской капусты. Аналогичные данные получены для фасоли [227]. В период между экспозицией трития и сбором урожая концентрация TFWT снижалась, поскольку увеличивался OBT [226, 228]. Однако TFWT может быть значимее OBT при оценке доз потребляемых продуктов питания, если растения подвергались воздействию HTO непосредственно перед сбором урожая [226].
Несоответствие измеренных и расчетных оценок накопления OBT было показано также при изучении динамики накопления OBT и HTO другими видами сельскохозяйственных растений (фасоль, огурцы, помидоры, кабачки, морковь, картофель, свекла, яблоки, груши, кукуруза, кормовая трава для скота) вблизи Канадских атомных объектов [198]. Обнаружено, что на фоновых участках концентрации OBT были выше, чем HTO, а соотношение OBT/HTO в растениях варьировало от 0.3 до 20. На импактной территории соотношение OBT/HTO в растениях отклонялось от ожидаемого значения 0.7 [229], при этом активность OBT в импактной почве находилась в равновесии с OBT растений. Результаты этого исследования отражают динамический характер накопления HTO и образования OBT в почве и растениях в течение вегетационного сезона, а также свидетельствуют о необходимости пересмотра некоторых параметров, используемых в моделях переноса трития в окружающей среде, поскольку смоделированные оценки накопления OBT растениями представляются завышенными. Аналогичный вывод о необходимости уточнения моделей переноса HTO от почвы к растению был сделан и другими исследователями [215]. Вывод был основан на результатах эксперимента по орошению растений водой, содержащей разные концентрации трития. Показано, что при орошении водой с низкой концентрацией трития активность TFWT и OBT зависела от атмосферного поступления трития. При высоком содержании трития зависимость от атмосферных поступлений отсутствовала: концентрация TFWT оставалась повышенной в течение всего эксперимента, а OBT в листьях увеличивалось с последующим квазиравновесием с TFWT. В работе [230] показано, что при воздействии на растения малоактивной HTO отношения OBT/HTO достигают 8.3. Аналогичные данные были получены ранее [220]. Кроме того, в кислой среде (pH 4) поглощение HTO и включение трития в OBT было выше, чем в нейтральной [227]. Отсутствие биоаккумуляции трития злаками, бодяком, недотрогой и крапивой показано в работе [231].
Распределение 3H в однолетних растениях и однолетних сегментах многолетних растений может отражать его содержание в атмосферной влаге или осадках [46]. Равновесие при поглощении TFWT листьями растений из атмосферной HTO достигается в течение 1 ч [226, 228]. Потеря TFWT растениями (например, капустой и салатом) происходит поэтапно и описывается двойной экспоненциальной функцией: первый, быстрый компонент, характеризует парообмен и транспирацию – длительность его полупериода (t1/2) равна 53 мин; второй, медленный компонент (t1/2 = 15 ч), связан с обеззараживанием тканей стебля и корня. Спустя 48 ч после кратковременного воздействия парами воды тритий в растениях не обнаруживается, при этом эффективность процесса (скорость потери HTO) на свету выше, чем в темноте [232]. Кроме того, на примере шпината показан [233] широкий диапазон изменчивости (34–117%) скорости формирования OBT из TFWT на свету и в темноте. Если предположить, что OBT формируется только в процессе фотосинтеза, то в темноте, когда скорость фотосинтеза будет менее интенсивной, должно было образоваться меньше OBT, чем на свету. Однако в этом исследовании однозначного отклика не обнаружено, что связано с иными механизмами образования OBT в темноте, например с различными метаболическими превращениями, в том числе в цикле трикарбоновых кислот.
Иные оценки были получены в модельном эксперименте по изучению миграции HTO из среды обитания в состав компонентов ивы белой (Salix alba L.) в процессе вегетации [234]. Равновесие между содержанием HTO во внешней среде и внутриклеточном соке растений устанавливалось за 1–2 недели. Длительность установления равновесия между питательной средой и TFWT подтверждена в работе [227]. При этом коэффициент фракционирования α (разделение тяжелых и легких изотопов вследствие небольшого различия массы при фазовых переходах [235]) составлял 0.88–0.94 и практически не зависел от концентрации HTO во внешней среде [234]. Равновесие по OBT устанавливалось в течение 4–11 недель, α = = 0.17–0.19 независимо от концентрации HTO во внешней среде. Вместе с тем наблюдалось изъятие радиоактивного изотопа из системы, вероятно, вследствие транспирации – коэффициент фракционирования составил 1.2. Таким образом, константа скорости формирования загрязнения 3H внутриклеточных соков растений в среднем была вдвое больше, чем константа скорости его трансформации в OBT [234]. Отметим, что воздействие HT на листья было причиной больших концентраций TFWT, но слабой трансформации в OBT [227]. Еще один важный аспект при обсуждении вопросов поглощения растениями HTO с последующим синтезом OBT связан с тем, что отдельные молекулы HTO не прикреплены к соседним молекулам легкой воды, и, следовательно, удельная активность воды не является консервативным свойством, в то время как две категории молекул движутся вместе в конвективном потоке, они ведут себя независимо в диффузионном переносе, причем движение каждого изотопа зависит от его собственного градиента концентрации [20].
В упомянутом выше проекте VATO также было проведено многолетнее изучение кинетики переноса 3H в растения с учетом вклада разных источников (воздух, дождевая вода) и определен биологический период полураспада OBT в растениях [103]. Показано, что вблизи завода по переработке ОЯТ (Франция) концентрация TFWT в растениях составила 2–62 Бк/л, а OBT – 4–20 Бк/л. Биологический период полураспада OBT в растениях для быстрого компонента составил 5 ч, а для медленного – 15 дней.
В ходе комплексных исследований СИП были использованы в качестве индикаторов содержания 3H в грунтовых водах разные экологические группы растений. Наиболее перспективными видами растений в условиях сухой степи оказались фреатофиты, имеющие глубоко проникающую корневую систему: солодка (Glycyrrhiza uralensis), чий (Achnatherum splendens) и чингиль (Halimodendron halodendron). Выявлена корреляция между концентрацией TFWT в растениях и грунтовых водах. Поскольку TFWT в заданное время отражает мгновенную активность трития в окружающей среде, метод не является точным, поскольку загрязнение тритием может быть частично разбавлено дождем перед взятием проб. Для построения долгосрочных прогнозов необходимо определение необменного OBT в растениях [236]. Такие данные были опубликованы ранее [237] и показано, что обменный OBT ведет себя как TFWT и его количество в обезвоженной органике составляет 20–57% от общего количества трития в зависимости от культуры (салат, капуста, помидоры, редис и свекла) и условий проведения эксперимента (выращивание на загрязненной тритием почве и орошение HTO). В то же время активность необменного OBT в овощах отражает интегрированные во времени концентрации HTO за несколько месяцев до отбора проб [237]. Снижение вклада OBT в общую дозу трития происходит при окислении OBT во время приготовления пищи. Так, в картофеле TFWT и OBT снизились до 46 и 54% соответственно, а в швейцарском мангольде до 22 и 57% относительно сырого продукта [238].
Обобщение экспериментальных данных по изучению поглощения трития сельскохозяйственными культурами (пшеница, рис, соя, картофель, фасоль, помидоры, редис, капуста и мандарин) показало, что формирование OBT растений зависит от стадии развития, продолжительности и условий воздействия, а его перенос в съедобные части растений может сильно различаться между культурами [222].
Путь аэрального (фолиарного) поглощения трития также очень важен для растений [239]. На примере подсолнечника Helianthus annuus установлена положительная корреляция между TFWT и НТО в воздухе, а также между значениями удельной активности OBT и TFWT. Скорость формирования OBT изменялась в пределах 0.21–0.68%/ч, индекс транслокации для H. annuus в конце экспозиции составил 27.4%. При длительном аэральном поглощении НТО отмечен неравномерный характер распределения TFWT и OBT по органам H. annuus с максимальной активностью TFWT и OBT в листьях [240]. По некоторым сведениям [222], в разное время суток формирование OBT не различается между собой. Противоположные данные были получены на пшенице [221, 241]: концентрация OBT в листьях в ночное время на 50% меньше, чем днем, а поглощение TFWT ночью также было ниже. Эти результаты хорошо согласуются с данными работы [227]: абсорбция HTO и включение трития в OBT были заметно снижены у красной фасоли в темноте. Показаны роль устьичного аппарата в процессе формирования OBT в разное время суток и циркадная динамика этого процесса [221, 242]. Основываясь на междисциплинарном подходе [242], в модели CROPTRIT были учтены источники неопределенности, связанные с изменчивостью некоторых параметров (генотип растений, погодные условия, внесение удобрений, воды и т.д.).
Особенностью корневого поступления НТО является то, что почвенная вода в активных корневых зонах представляет собой смесь просачивающихся грунтовых вод и инфильтрата дождя, что приводит к неоднородной концентрации НТО в почве. Процессы разбавления дождевой водой грунтовых и поверхностных вод необходимо учитывать при оценке 3H в транспирате [243] и годичных кольцах древесных растений [46]. Последний показатель является уникальным инструментом для ретроспективных оценок радиоактивного загрязнения окружающей среды на достаточно больших промежутках времени [192]. Содержание трития в целлюлозе годичных колец определяется глобальными, региональными и локальными факторами. Исследование, охватывающее 50-летний период наблюдений в Японии [244], выявило максимальную концентрацию OBT в годичных кольцах 1963 г., что хорошо согласуется с описываемыми выше закономерностями по атмосферным осадкам. В некоторых локациях были обнаружены вторичные пики в 1966 и 1970 г., что связано с влиянием подземных вод в некоторых горных районах. Не совсем синхронные годичные колебания содержания трития в осадках и годичных кольцах могут быть связаны с особенностями мест произрастания деревьев и колебаниями метеопараметров текущего и предыдущего сезонов [166, 192, 245]. По результатам измерений активности трития [246] было выявлено, что в пробах хвои содержится в основном OBT. В целом отмечается многолетний нисходящий тренд содержания трития в целлюлозе древесины Pinus sylvestris [245], что хорошо согласуется с уменьшением его выбросов в атмосферу [89] и поступлением с осадками, выпадающими в разных странах [106, 112, 115, 136–138], и, по-видимому, характеризует многолетнюю динамику поступления трития из стратосферы.
Концентрация OBT в семенах во время сбора урожая также зависит от времени воздействия трития на растения и может различаться до 70 раз. Максимальные значения трития характерны при воздействии на ранних стадиях развития, что соответствовало фазе быстрого роста растений. Кроме того, вклад в суммарный OBT растений был наибольшим за счет накопления OBT семенами [228]. Перемещение OBT в зерно также зависело от скорости его роста – после перехода в зерно потери OBT происходили очень медленно [241]. Через 96 ч после начала проращивания семян сосны Pinus banksiana на тритиевой воде изученные аминокислоты (глутамин, аланин, пролин и γ-аминомасляная кислота) содержали тритий, но в погибших из-за нагревания семенах 3H-аминокислоты не обнаружены. В основном 3H был локализован в цитоплазме, но на единицу площади был больше сконцентрирован в хроматине ядра [247].
Коэффициент накопления TFWT в спелых томатах и огурцах составил 0.5 (0.4–0.8) от концентрации трития в воздухе, а в листьях – 0.8 (с большим диапазоном изменчивости). При поглощении HTO из чистой почвы переход трития в TFWT для спелых плодов/воздуха составил 0.20, а листвы/воздуха – 0.45. Орошение тритиевой водой приводило к росту коэффициента концентрации TFWT в растениях до 3.2, однако OBT составил всего 9% от общего содержания трития [248]. Анализ импортированных в Японию продуктов питания (эндивий, лук-порей, корень сельдерея, шалот, спагетти, сыр камамбер) показал [249], что соотношение OBT/TFWT (0.69–3.0) было ниже указанных ранее европейскими и американскими исследовательскими группами и может быть связано с межгодовой изменчивостью накопления и трансформации трития, поэтому требует межлабораторной интеркалибровки.
Таким образом, некоторые закономерности накопления трития растениями заключаются в следующем: 1) динамический характер накопления HTO и образования OBT в растениях и почве в течение вегетационного сезона; 2) зависимость накопления HTO и соотношения OBT/НТО от концентрации трития в окружающей среде; 3) зависимость поступления трития в растения от кислотности почвы; 4) достижение устойчивого равновесия TFWT/HTO в течение одного–двух часов; 5) формирование OBT зависит от стадии развития растений, продолжительности и условий воздействия трития, а его перенос в разные части растений видоспецифичен; 6) неравномерный характер распределения TFWT и OBT по органам при длительном аэральном поглощении НТО; 7) циркадная динамика абсорбции и потери HTO, а также включения в OBT; 8) двухкомпонентный период выведения трития из организма и т.д.
ТРИТИЙ В НАСЕКОМЫХ
Для взрослых сверчков (Acheta domesticus) была определена зависимость между концентрацией общего трития в организме (0.19) и источником пищи (кресс-салат). Равновесная концентрация HTO составила 0.92 от концентрации воды, на которой он выращивался [250]. По данным [251], содержание воды в организме A. domesticus составляет около 75%. Таким образом, простые предположения о диффузионно-равновесном состоянии не подходят для описания миграции трития по пищевым цепочкам. Для моделирования процессов миграции необходимо учитывать дополнительные факторы, например скорость ассимиляции OBT и оборота TFWT, пищевые привычки и продолжительность стадий развития организмов, а также концентрации трития в окружающей среде [250].
ТРИТИЙ В НАЗЕМНЫХ ЖИВОТНЫХ
Животные являются следующим звеном пищевой цепочки после растений, которые участвуют в миграции биогенных элементов в экосистемах. Возможны два пути поступления трития в организм животных: аэральный и пероральный. В первом случае тритий, содержащийся в атмосферной влаге, поступает в организм в процессе дыхания через легкие. Во втором случае тритий может поступить в организм животного либо в виде HTO, либо с твердой пищей, содержащей TFWT и OBT.
В ходе 100-дневного эксперимента на крысах было показано [252], что 3Н в виде HTO, попавший в организм, быстро и равномерно распределялся по всему телу, но также быстро (t1/2 = 3.5 дня) выводился из него. OBT выводился медленно, при этом выявлена тканеспецифичность времени удерживания: так, максимальные концентрации 3Н отмечены в жировой ткани, мозге и мышцах, что связано с их метаболической активностью. Результаты эксперимента хорошо согласуются с данными о том, что скорость выведения у молодых животных выше, чем у пожилых. Максимальная эквивалентная доза за счет OBT для жировой ткани составила 64% от общей дозы для тканей [252]. Данные о периоде полувыведения хорошо согласуются с результатами, отмеченными для почек [253]. Для других органов эти значения были выше и зависели от дозы вводимой HTO. Накопление трития мышами (Peromyscus gossypinus) из природных экосистем, орошаемых HTO, положительно коррелировало с увеличением скорости орошения и концентрацией трития в воде. При этом получены отрицательные зависимости накопления 3Н от количества осадков, что указывает на отсутствие накопления трития биотой [254].
Молоко и кисломолочная продукция являются важными компонентами пищевого рациона человека – они содержат необходимые питательные вещества (белки, жиры, углеводы). Именно поэтому молоко – один из наиболее часто контролируемых продуктов питания вблизи источников радиоактивных выбросов [255]. Многолетние исследования почвы, растительности, продуктов питания, тканей животных и человека показали [256], что при переходе по трофическим уровням кратность снижения соотношения удельной активности свободный/связанный тритий составила для почвы относительно осадков 6–8 раз, для растительности – 3–4 раза, для человека – 1.5–2 раза, наименьшее соотношение 1.2 – для молока. Было показано [257], что при поении лактирующих коров HTO концентрация трития в компонентах молока и моче достигла максимума через 18 дней и составила 82% от HTO. Наибольшее включение трития произошло в лактозе (0.58), молочном жире (0.36) и казеине (0.27). Таким образом, в сухом веществе молока содержание трития достигало 0.45, что выше, чем в других тканях млекопитающих. Период полувыведения составил около 4 дней для быстрой компоненты и 44, 225 и 24 дня – для медленных компонент молочной воды, жира и казеина соответственно [257].
При поступлении трития в виде OBT с сеном около 97% трития концентрировалось в казеине и молочном жире [258]. Аналогичные данные указаны в работе [259]: величина перехода трития в сыворотку молока кобыл при кормлении сеном выше (20%), чем при поступлении HTO. При кормлении сеном равновесие наступало через 11 сут, а при поступлении с водой – через 25 сут. Кривые, описывающие снижение концентраций трития в молоке, можно разделить на компоненты с быстрым и медленным периодом выведения [259]. Соотношение активности трития корм/продукты животного происхождения менее изменчиво, чем коэффициент перехода (соотношение концентрация трития в молоке или тканях животных/суточное потребление нуклида), поэтому целесообразно использовать именно этот показатель [260].
ТРИТИЙ В ВОДНЫХ РАСТЕНИЯХ
Потенциальными источниками поступления трития в водные экосистемы являются штатные и аварийные выбросы предприятий атомной промышленности, а также исторически загрязненная 3H наземная биомасса, представляющая собой значительный источник OBT [261]. В некоторых работах [262] было показано, что TFWT в водных организмах уравновешивается с окружающей средой, и особенно быстро этот процесс происходит у водорослей. OBT накапливается в водных организмах гораздо медленнее, чем TFWT, и не достигает высоких концентраций. При этом некоторые виды зеленых водорослей (например, Dunaliella tertiolecta) в фазе экспоненциального роста могут накапливать OBT быстрее, чем в стационарном состоянии [262, 263]. Для Nodularia spumigena такого эффекта не наблюдалось [263]. Накопление 3Н-лизина в клетках водорослей Scenedesmus obliquus оказалось на 3–4 порядка больше, чем концентрация HTO [264].
В районе воздействия ГХК было показано, что элодея (Elodea canadensis Michx.) и рдест (Potamogeton L.) содержали тритий в концентрациях 2–8 Бк/кг сырого веса [265], при этом концентрация 3Н в воде основного русла р. Енисей составила 4–6 Бк/л, а в донных отложениях ~6 Бк/л, т.е. соотношение трития в воде, донных отложениях и живых организмах составляло около 1. Аналогичные данные были получены для камыша (Typha latifolia) около АЭС Альмарас (Испания) – соотношение TFWT/HTO варьировало от 0.3 до 1.3 (в среднем 0.74) [266]. Для нитчатых зеленых водорослей вблизи предприятий атомной промышленности Канады эта величина была выше – 1.8 (0.8–3.7) [81]. Отношение OBT/TFWT варьировало для водорослей в узких пределах (2.9–3), а отношение OBT/HTO достигло пятикратного превышения [81]. Аналогичные данные были получены в работе [86]. Значительное накопление OBT водорослями по сравнению с HTO связано с тем, что для TFWT характерен более быстрый оборот в биологических системах, чем для OBT [81]. Тритий, который уже успел включиться в органические молекулы, остается в них на долгое время. В условиях снижения концентрации HTO водоросли продолжают содержать исторически накопленный OBT по сравнению с современными уровнями HTO.
В ходе лабораторного эксперимента изучено накопление трития роголистником Ceratophyllum и ряской Lemna. Обнаружено, что основное снижение (до 70%) содержания трития в экспериментальной воде наблюдается в течение первых 48 ч после начала эксперимента [267, 268]. Оптимальными условиями для ассимиляции и трансформации 3Н водными растениями являются температура воды 25о С и отсутствие света 18 ч [164].
ТРИТИЙ В ВОДНЫХ ЖИВОТНЫХ
Существует мнение, что организмы, которые потребляют пищу, содержащую тритий, накапливают OBT быстрее и достигают более высокой концентрации трития, чем организмы, подвергшиеся воздействию только HTO. Тритий в OBT ведет себя иначе, чем в HTO, что зависит от химической формы молекулы. Однако в 80-х годах прошлого столетия ни экспериментальные исследования пищевой цепи, ни результаты изучения загрязненной окружающей среды не указывали на то, что тритий подвергается аккумуляции через пищевые цепи [262].
Современные исследования предлагают к обсуждению разнополярные результаты. Так, в районе влияния ФАЭС-1 (на примере бычка Myoxocephalus jaok, кальмара Todarodes pacificus, терпуга Pleurogrammus azonus), а также в районе влияния Ленинградской и Балтийской АЭС, АЭС Ханхикиви (на примере разных видов рыб – густера, ерш, карась, красноперка, лещ, линь, налим, окунь, осетр, плотва, судак, сырть, уклейка, чехонь, щука) было показано превышение активности трития в форме TFWT в 1.5–4 раза и активности OBT в 5–20 раз в расчете на живой вес по сравнению с его активностью в среде обитания [39]. Аналогичные данные по аккумуляции трития были получены в районе воздействия ГХК (р. Енисей). Показано, что в мышечной ткани промысловых рыб (хариус, сиг, стерлядь, тугун) концентрация 3Н составляет 12–20 Бк/кг сырого веса по сравнению с активностью в воде (4–6 Бк/л) основного русла р. Енисей [265]. В случае травоядного серебряного карася (Carassius gibelio) около 50–75% накопленного 3H находилось в мышцах – период полувыведения составил 175 дней; период полувыведения из печени, где депонировалось 30% трития [267], достигал 550 дней [164, 268]. Наибольший вклад (до 50%) в накопление трития вносят соединения холестерина [267]. В модельных экспериментах [269] было обнаружено включение 61–71% трития из HTO в OBT планктонных водорослей; в дальнейших опытах было показано, что длительный период полураспада OBT был обнаружен при различных температурных условиях.
Повышенное содержание трития в форме TFWT относительно HTO (4.3) и коэффициенты концентрации OBT/HTO были выше у пресноводных мидий (17–47) по сравнению с водорослями и рыбой [81]. Аналогичные данные были получены в районе влияния АЭС Пакш: при незначительной разнице между TFWT биоты и HTO в воде р. Дуная количество OBT в моллюсках превышало концентрацию трития в воде. У морских мидий (Mytilus edulis) тритий, содержащийся в глицине (T-Gly), показал повышенное включение в ДНК по сравнению с HTO. Около 90% начальной активности HTO выводилось из организма в течение суток, тогда как выведение T-Gly происходило медленно [270]. Аналогичные данные были получены в работе [142]. Накопление TFWT в тканях мидий (Mytilus edulis) происходило в зависимости от дозы, причем наибольшее количество свободной тритиевой воды накапливалось в кишечнике, за которым следовали жабры, мантия и мышцы [271]. Дополнительные вещества (Zn) не приводят к снижению накопления трития в организме или уменьшению его распределения в отдельных тканях мидий [148].
Накопление OBT в тканях мидий из тритиевого фитопланктона демонстрирует экологически значимый путь переноса трития даже при снижении концентрации в воде, что вносит вклад в развитие идеи о том, что OBT действует как стойкий органический поллютант [263]. Как и у наземных растений, концентрация TFWT в мидиях достигала устойчивого равновесия с HTO в течение 1–2 ч. Несовпадение расчетных данных с результатами моделирования связано с потерей OBT мидиями во время воспроизводства [272]. Меньшее накопление OBT рыбами относительно моллюсков связывают с их высокой миграционной способностью [273]. Эти результаты свидетельствуют также о неоднородном распределении OBT в водных экосистемах [81]. Для оценки переноса трития взрослой радужной форелью (Onchorrynchus mykiss) по водной пищевой цепи была предложена обновленная модель AQUATRIT. Результаты моделирования и верификация подчеркивают, что в полевых условиях основными факторами, влияющими на скорость биологической потери OBT, являются температура и доступность добычи, в то время как поглощение OBT в основном зависит от скорости роста рыбы [274]. У таких мелких организмов, как эмбрионы рыбок Danio rerio, интернализация трития (соотношение между активностью в воде и организмах) представляет собой быстрое явление, достигающее стационарного состояния в течение 24 ч после начала загрязнения при TFWT/HTO ≈ 1. Формирование OBT в организмах происходило медленно: через 24 и 96 ч после оплодотворения икры соотношение ОBТ/TFWT в эмбрионах составило около 8 и 14% соответственно [275].
Другая группа работ свидетельствует о том, что биоаккумуляции OBT не происходит. Это было показано на примере зоопланктонных организмов (Cladocera, Copepoda, Rotatoria), у которых OBT составило 2–9 Бк/л по сравнению с активностью в воде (4–6 Бк/л) основного русла р. Енисей [265]. Аналогичные данные были получены для карпа (Cyprinus carpio) – коэффициент концентрации составлял 0.8 [266], что совпадает с данными работ [143, 276, 277]. В некоторых исследованных озерах отмечалась обратная корреляция между размером тела рыбы и активностью OBT [277], что связано с замедлением роста при определенном размере и зависит от вида рыб, биоэнергетики, возраста, типа пищи, типа самой водной среды. Отметим также, что различия по коэффициенту перехода, описанные выше, могут быть обусловлены тем, что выращивание организмов было проведено в тритиевой воде с высокой удельной активностью. Однако этот эксперимент не воспроизводит накопление трития биотой в природных условиях [39].
Таким образом, для разных групп биологических объектов характерна высокая гетерогенность в накоплении разных форм трития. Для большинства организмов уровни OBT выше, чем HTO. Кроме того, анализ данных показал, что в настоящее время не во всех работах учитывается содержание OBT и, следовательно, могут быть недооценены накопление и токсическое действие трития для биоты. Такая информация необходима для точной оценки распределения трития в ходе штатных выбросов и инцидентов, а также для адекватной защиты окружающей среды и человека [263].
МЕЖДУНАРОДНЫЕ ПРОГРАММЫ ПО ОЦЕНКЕ СОДЕРЖАНИЯ ТРИТИЯ В ОКРУЖАЮЩЕЙ СРЕДЕ
К настоящему времени в открытых литературных источниках встречаются сведения о 14 программах, направленных на изучение разных аспектов поведения трития в окружающей среде, а также оценку его накопления живыми организмами и миграции по пищевым цепям (см. табл. 1). Результаты анализа данных с использованием тех или иных моделей приводятся в разных разделах статьи.
Таблица 1.
Программы и модели, направленные на оценку содержания, накопления и миграции трития в окружающей среде и биоте
| Название программы | Краткое описание | Ссылки на источник литературы |
|---|---|---|
| AQUATRIT | Оценка переноса 3H по водным пищевым цепям | [274] |
| BIOMASS TWG | Моделирование переноса 3H в окружающей среде в ситуациях длительного выброса из первичных или вторичных источников вблизи долгосрочных атмосферных и подземных источников | [278–280] |
| CROPTRIT | Динамика переноса 3H сельскохозяйственными растениями в системе “почва – растения–атмосфера” | [242] |
| CTEM+CLASS v.2.7 | Модель переноса 3H в Канадской модели наземной экосистемы с учетом феноменологии растений | [281] |
| EMRAS II | Моделирование поступления 3H в окружающую среду в результате аварийных выбросов ядерных объектов, сравнение моделей для оценки переноса 3H в водную, наземную биоту и организм человека | [85, 282] |
| FEFLOW 5.0 | Моделирование потока подземных вод и переноса 3H из гипотетического реактора АЭС с учетом данных мониторинга уровня воды | [214] |
| MARINA II | Моделирование переноса и накопления 3H в морских водах Северной Европы и морской биоте для оценки доз для биоты и человека, а также биологических эффектов этого воздействия | [283–285] |
| MGMTP | Глобальная модель для прогнозирования концентрации 3H в осадках | [106] |
| SIBYLLA | Оценка загрязнения водных объектов и доз, полученных населением в результате сбросов (выпадений, утечки, смыва) радиоактивности в гидросферу при нормальных условиях эксплуатации или авариях (на всех этапах жизненного цикла объекта использования атомной энергии) | [286] |
| TERM | Моделирование выбросов 3H в окружающую среду (атмосфера, речные и прибрежные экосистемы) | [287] |
| TOCATTA | Моделирование переноса 3H в сельскохозяйственные растения с учетом состава воздуха, дождевой и почвенной воды, а также различных процессов (фотосинтез и эвапотранспирация) | [288] |
| TRIF | Моделирование переноса 3H в сельскохозяйственные культуры и животных | [289] |
| TRANSAT | Разработка стратегий уменьшения выбросов 3H, методология оценки уровней загрязнения, улучшение обращения с отходами и совершенствование знаний в области токсичности радионуклидов и дозиметрии | [51, 290] |
| VATO | Исследование поведения 3H в окружающей среде (воздух, почва, дождевая вода, миграция в растения, оценка периода полураспада OBT в растениях) | [103] |
ЗАКЛЮЧЕНИЕ
Таким образом, учитывая относительно короткий период полураспада трития, его высокую миграционную способность, наличие нескольких физико-химических форм, сродство с органическими молекулами и включенность в обменные процессы в биосфере, современные представления о закономерностях поведения трития в окружающей среде и накопления биотой не вполне однозначны. Поскольку миграция трития в компонентах окружающей среды и биоте представляет собой сложные, длительные и многоступенчатые процессы, зависящие от пространственного распределения 3H, его суточной, сезонной и межгодовой изменчивости, метеоусловий, возрастных и видовых характеристик, динамики стока и неоднородности распределения HTO и OBT в экосистемах, остаются полностью нерешенными следующие задачи:
1. Для установления величины приемлемых уровней техногенного поступления трития в окружающую среду необходимы исследования по уточнению его поведения в круговороте воды и органических веществ в биосфере, включая количественные характеристики этих процессов.
2. Целесообразно привести к общему знаменателю (по порядку величины) предельно допустимые уровни трития в окружающей среде, используемые в настоящее время разными странами для целей нормирования.
3. Актуальна разработка концептуальных моделей аварийных выбросов трития различными предприятиями ядерного цикла. При этом необходима менее консервативная, но надежная оценка радиационных последствий аварийных выбросов трития для биоты.
4. Необходимы систематические экспериментальные данные о многолетнем накоплении трития разными референтными группами, в том числе растениями, произрастающими в природных сообществах и агроэкосистемах, и референтных животных, а также инициация процедуры запуска межлабораторных сравнений.
5. Для более точного прогнозирования дозовых нагрузок на биоту целесообразно пересмотреть некоторые параметры накопления и их значения, используемые в моделях переноса трития в окружающей среде, поскольку смоделированные оценки накопления OBT разными референтными видами демонстрируют большую изменчивость и представляются весьма консервативными.
В дальнейшем исследование будет продолжено по пути обобщения оценок дозовых нагрузок и биологических эффектов, полученных в ходе лабораторных и природных исследований действия трития для разных референтных групп.
Сбор данных проведен в рамках НИР “Развитие законодательной и нормативной базы в области использования атомной энергии, включая новые типы ядерных установок, термоядерные и гибридные системы” федерального проекта “Разработка технологий управляемого термоядерного синтеза и инновационных плазменных технологий” комплексной программы Российской Федерации “Развитие техники, технологий и научных исследований в области использования атомной энергии”, анализ и интерпретация полученных результатов – в рамках государственного задания Института экологии растений и животных УрО РАН, Института промышленной экологии УрО РАН и Института проблем безопасного развития атомной энергетики РАН. Авторы благодарят д.т.н. И.И. Линге (ИБРАЭ РАН) и д.б.н. В.Н. Позолотину (ИЭРиЖ УрО РАН) за ценные замечания и рекомендации, которые помогли значительно улучшить статью.
Авторы заявляют об отсутствии конфликта интересов.
Список литературы
Sources, effects and risks of ionizing radiation. Report 2016. NY: UNSCEAR, 2017. 512 p.
Management of waste containing tritium and carbon-14. Vienna: IAEA, 2004. 109 p.
Bartels J.R., Pate M.B., Olson N.K. An economic survey of hydrogen production from conventional and alternative energy sources // Intern. J. of Hydrogen Energy. 2010. V. 35. № 16. P. 8371–8384.
Dresselhaus M.S., Thomas I.L. Alternative energy technologies // Nature. 2001. V. 414. № 6861. P. 332–337.
Michaelides E.E.S. Alternative energy sources. Berlin: Springer, 2012. 467 p.
Reinders L. The fairy tale of nuclear fusion. Cham: Springer, 2021. 431 p.
Yukhimchuk A.A. Tritium-related activities in the Russian Federation // Fusion Science and Technology. 2020. V. 76. № 4. P. 567–577.
Zhang H.W., Lin X., Ma Z.W. et al. Systematic simulation studies on the penetration of resonant magnetic perturbations in an Experimental Advanced Superconducting Tokamak // Plasma Physics and Controlled Fusion. 2021. V. 63. № 3. P. 035011.
Kurskiev G.S., Gusev V.K., Sakharov N.V. et al. Tenfold increase in the fusion triple product caused by doubling of toroidal magnetic field in the spherical tokamak Globus-M2 // Nuclear Fusion. 2021. V. 61. № 6. P. 064 001.
Subbotin M., Rozenkevich M., Gostev A. et al. Concept design of the tritium plant on the TRINITI site for the Tokamak Ignitor Project Tasks // Fusion Science and Technology. 2020. V. 76. № 3. P. 297–303.
Rozenkevich M., Perevezentsev A., Subbotin M. et al. Optimisation of fuel cycle for IGNITOR tokamak at TRINITI in Russia: A critical review // International J. of Hydrogen Energy. 2020. V. 45. № 56. P. 32 311–32 319.
Petrov M.P., Afanasyev V.I., Chernyshev F.V. et al. 60 years of neutral particle analysis: from early tokamaks to ITER // The Europ. Physical J. H. 2021. V. 46. № 1. P. 1–5.
Линге И.И. О радиоэкологических последствиях замыкания ядерного топливного цикла // Вопросы атомной науки и техники. Серия: Термоядерный синтез. 2021. Т. 44. № 1. С. 13–17.
Urey H.C., Murphy G.M., Brickwedde F.G. A name and symbol for H2* // The J. of Chem. Physics. 1933. V. 1. № 7. P. 512–513.
Oliphant M.L.E., Kinsey B.B., Rutherford E. The transmutation of lithium by protons and by ions of the heavy isotope of hydrogen // Proceedings of the royal society of London. Ser. A. Containing papers of a mathematical and physical character. 1933. V. 141. № 845. P. 722–733.
Alvarez L.W., Cornog R. Helium and hydrogen of mass 3 // Physical Review. 1939. V. 56. № 6. P. 613.
Audi G., Wapstra A.H., Thibault C. The Ame2003 atomic mass evaluation: (II). Tables, graphs and references // Nuclear Physics A. 2003. V. 729. № 1. P. 337–676.
Okada S., Momoshima N. Overview of tritium: characteristics, sources, and problems // Health Physics. 1993. V. 65. № 6. P. 595–609.
Lucas L.L., Unterweger M.P. Comprehensive review and critical evaluation of the half-life of tritium // J. of research of the National Institute of Standards and Technology. 2000. V. 105. № 4. P. 541–549.
Zerriffi H. Tritium: The environmental, health, budgetary, and strategic effects of the Department of Energy’s decision to produce tritium. Takoma Park: IEER, 1996. 15 p.
Бучаченко А.Л., Плисс Е.М. Изотопные эффекты водорода и атомное туннелирование // Успехи химии. 2016. V. 85. № 6. P. 557–564.
Мариянац А.О., Шестаков И.А., Горшкова О.С. и др. Термодинамические изотопные эффекты трития в молекулах углеводов // Вопросы радиац. безопасности. 2017. № 1. С. 80–87.
Investigation of the environmental fate of tritium in the atmosphere. Part of the Tritium Studies Project. Ottawa: CCNS, 2009. 104 p.
Kaufman S., Libby W.F. The natural distribution of tritium // Physical Review. 1954. V. 93. № 6. P. 1337–1344.
Кесслер Г. Ядерная энергетика. М.: Энергоатомиздат, 1986. 261 с.
Ionizing radiation: sources and biological effects. New York: UNSCEAR, 1982. 43 p.
Begemann F., Libby W.F. Continental water balance, ground water inventory and storage times, surface ocean mixing rates and world-wide water circulation patterns from cosmic-ray and bomb tritium // Geochimica et Cosmochimica Acta. 1957. V. 12. № 4. P. 277–296.
Баженов В.А., Булдаков Л.А., Василенко И.Я. и др. Вредные химические вещества. Радиоактивные вещества: справочник / Под ред. Филова В.А., Ивина Б.А., Ильина Л.А. Л.: Химия, 1990. 464 с.
Kalinowski M.B. International control of tritium for nuclear nonproliferation and disarmament. Boca Raton: CRC press, 2004. 256 p.
Phillips J.E., Easterly C.E. Sources of tritium. Oak Ridge National Lab., 1980. 60 p.
Десятов Д.Д., Екидин А.А. Оценка поступления трития в окружающую среду от выбросов АЭС // Биосферная совместимость: человек, регион, технологии. 2018. № 1. С. 88–96.
Михальченко А.Г., Ивахнюк Г.К., Швецова О.В. Перспективы увеличения глобальной радиационной нагрузки от техногенного трития // Современные проблемы экологии: тезисы докладов XIV Междунар. науч.-технич. конф. / Под ред. Панарина В.М. Тула: Инновационные технологии, 2016. С. 263–264.
Environmental Health Criteria 25. Selected radionuclides – tritium, carbon-14, krypton-85, strontium-90, iodine, caesium-137, radon, plutonium. Geneva: WHO, 1983. 142 p.
Миронова Н.И. Тритий – это опасно. Челябинск: Движение за ядерную безопасность, Центр поддержки гражданских инициатив, 2001. 58 с.
Murphy C.E. Jr., Pendergast M.M. Environmental transport and cycling of tritium in the vicinity of atmospheric releases. Vienna: IAEA, 1979.
Радиационная обстановка на территории России и сопредельных государств в 2020 году / Под ред. Шершакова В.М., Булгакова В.Г., Крышева И.И. и др. Обнинск: Росгидромет, НПО “Тайфун”, 2021. 330 с.
Willms S. Tritium supply considerations. 2003. URL: https://fire.pppl.gov/fesac_dp_ts_willms.pdf).
Pastor L., Siclet F., Peron O. et al. Experimental setup for the determination of exchangeable hydrogen in environmental samples using deuterium and tritium // ICRER. Barcelona, Spain, 2014. P. 181.
Bondarenko L., Izotova A., Bolshakov V. et al. Tritium, tritium, tritium (HTO, TFWT, OBT). СПб.: Радиевый институт им. В.Г. Хлопина, 2016. 17 с.
Chen J. Radiation quality of tritium // Radiation Protection Dosimetry. 2006. V. 122. № 1–4. P. 546–548.
Kim S.B., Baglan N., Davis P.A. Current understanding of organically bound tritium (OBT) in the environment // J. of Environ. Radioact. 2013. V. 126. P. 83–91.
Adam-Guillermin C., Pereira S., Della-Vedova C. et al. Genotoxic and reprotoxic effects of tritium and external gamma irradiation on aquatic animals // Rev. Environ. Contam. Toxicol. / Ed. Whitacre D. M. NY: Springer, 2012. P. 67–103.
Eyrolle F., Ducros L., Le Dizès S. et al. An updated review on tritium in the environment // J. of Environ. Radioact. 2018. V. 181. P. 128–137.
Jean-Baptiste P., Fourré E., Baumier D. et al. Environmental OBT/TFWT ratios revisited // Fusion Science and Technology. 2011. V. 60. № 4. P. 1248–1251.
Mathur-De Vré R., Binet J. Molecular aspects of tritiated water and natural water in radiation biology // Progress in Biophysics and Molecular Biology. 1984. V. 43. № 2. P. 161–193.
Мажейка Й.В., Пятрошюс Р.И., Скуратович Ж.Л. и др. Тритий в окружающей среде Игналинской АЭС за период ее эксплуатации // Региональная экология. 2018. № 1. С. 20–30.
Baglan N., Ansoborlo E., Cossonnet C. et al. Tritium metrology within different media: focus on organically bound tritium (OBT) // Radioprotection. 2010. V. 45. № 3. P. 369–390.
Budnitz R.J. Tritium instrumentation for environmental and occupational monitoring – a review. Berkeley: Lawrence Berkeley National Laboratory, 1973. 50 p.
Clarke W.B., Jenkins W.J., Top Z. Determination of tritium by mass spectrometric measurement of 3He // The Intern. J. of Appl. Radiation and Isotopes. 1976. V. 27. № 9. P. 515–522.
Dodi E., Benco A. Radiation protection – tritium instrumentation and monitoring methods // Safety in tritium handling technology / Ed. Mannone F. Dordecht: Springer, 1993. P. 145–159.
Fitchet P., Bultel A., Markelj S. et al. Review of the different techniques to analyse tritium. TRANSAT. RIA: CEA, 2017. 34 p.
Hara M., Kawamura Y., Tanabe T. Tritium measurement. I – Tritium in gas, liquid, and solid // Tritium: Fuel of Fusion Reactors / Ed. Tanabe T. Tokyo: Springer, 2017. P. 137–164.
Love A.H., Hunt J.R., Roberts M.L. et al. Use of tritium accelerator mass spectrometry for tree ring analysis // Environ. Science & Technology. 2002. V. 36. № 13. P. 2848–2852.
Sakuma Y., Yamanishi H., Ogata Y. et al. Development of a simplified method for tritium measurement in the environmental water. Oroshi-cho, Toki: National Institute for Fusion Science, 2002. 452 p.
Zushi H. Tritium Measurement. II – Tritium in plasma // Tritium: Fuel of Fusion Reactors / Ed. Tanabe T. Tokyo: Springer, 2017. P. 165–205.
NF M60-824. Nuclear energy – measurement of radioactivity in the environment – determination of tritium activity in the environment – test method for analysis of tritium in free water and organically bound tritium in environmental matrices. 2020. 39 p.
Ware A., Allott R. Review of methods for the analysis of total tritium and organically bound tritium. Bristol: Environment Agency, 1999. 16 p.
Файзрахманов Ф.Ф., Аникин А.Я., Антоненко Г.И. и др. Измерение малых удельных активностей трития / Под ред. Романова С.А. Снежинск: РФЯЦ–ВНИИТФ, 2014. 108 с.
Pointurier F., Baglan N., Alanic G. A method for the determination of low-level organic-bound tritium activities in environmental samples // Appl. Radiation and Isotopes. 2004. V. 61. № 2. P. 293–298.
Горячев В.А., Рогачев К.А., Сойфер В.Н. Перенос трития в теплых вихрях Куросио // Океанология. 1991. Т. 31. № 4. С. 599–605.
Connan O., Hébert D., Solier L. et al. Atmospheric tritium concentrations under influence of AREVA NC La Hague reprocessing plant (France) and background levels // J. of Environ. Radioact. 2017. V. 177. P. 184–193.
Vasyanovich M.E., Ekidin A.A., Vasilyev A.V. et al. Determination of radionuclide composition of the Russian NPPs atmospheric releases and dose assessment to population // J. of Environ. Radioact. 2019. V. 208–209. Art. 106006.
Tentative method of analysis for tritium content of the atmosphere. Method 609 // Methods of Air Sampling and Analysis. NY: American Public Health Association, 1977.
Букин А.Н., Иванова А.С., Розенкевич М.Б. и др. Способ отбора проб тритированной воды методом фазового изотопного обмена // Заводская лаборатория. Диагностика материалов. 2017. Т. 83. № 7. С. 27–31.
Букин А.Н., Марунич С.А., Мосеева В.С. и др. Способ отбора проб тритированной воды из газовой среды. 2020. Патент RU 2711576 C1.
DOE handbook: Tritium handling and safe storage. Washington: U.S. Department of Energy, 2007. 149 p.
Tarancón A., Bagán H., García J.F. Plastic scintillators and related analytical procedures for radionuclide analysis // J. of Radioanal. Nucl. Chem. 2017. V. 314. № 2. P. 555–572.
Buzinny M., Panasjuk N., Tsygankov N. LSC-based approach for water analyses around the Chernobyl NPP // Advances in liquid scintillation spectrometry (LSC 2005) / Eds. Chalupnik S., Schönhofer F., Noakes J. Katowice, Arizona: University of Arizona, 2006. P. 297–303.
Журавков В.В., Позняк С.С., Скибинская А.Н. Содержание трития в гидрографической сети в районе строительства Белорусской АЭС // Журн. Белорусского гос. ун-та. Экология. 2019. № 1. С. 18–23.
Pourcelot L., Vintró L.L., Mitchell P. et al. Hydrological behaviour of tritium on the former Semipalatinsk nuclear test site (Kazakhstan) determined using stable isotope measurements // Eurasian Chemico-Technol. J. 2013. V. 15. № 4. P. 293–299.
Fons J., Tent-Petrus J., Llaurado M. Strategy for the determination of mixtures of alpha and beta emitters in water samples with a combination of rapid methods // J. of Radioanal. Nucl. Chem. 2017. V. 314. P. 797–802.
Pujol L., Sanchez-Cabeza J.A. Use of tritium to predict soluble pollutants transport in Ebro river waters (Spain) // Environ. Pollution. 2000. V. 108. № 2. P. 257–269.
Jefanova O., Mažeika J., Petrošius R. et al. The distribution of tritium in aquatic environments, Lithuania // J. of Environ. Radioact. 2018. V. 188. P. 11–17.
Janković M.M., Janković B.Ž., Todorović D.J. et al. Tritium concentration analysis in atmospheric precipitation in Serbia // J. of Environ. Science and Health. Part A. 2012. V. 47. № 5. P. 669–674.
Grahek Ž., Breznik B., Stojković I. et al. Measurement of tritium in the Sava and Danube rivers // J. of Environ. Radioact. 2016. V. 162–163. P. 56–67.
Leo W.R. Techniques for nuclear and particle physics experiments: a how-to approach. Berlin: Springer, 1994. 378 p.
Pujol L., Sanchez-Cabeza J.A. Optimisation of liquid scintillation counting conditions for rapid tritium determination in aqueous samples // J. of Radioanal. Nucl. Chem. 1999. V. 242. № 2. P. 391–398.
Stojković I., Todorović N., Nikolov J. et al. Methodology of tritium determination in aqueous samples by liquid scintillation counting techniques // Tritium: advances in research and applications / Ed. Janković M.M. NY: Nova Science Publishers, 2018. P. 99–156.
Janković M.M., Janković B.Ž., Sarap N.B. A new method for the determination of tritium originating in surface waters: symmetrical index application // Tritium: advances in research and applications / Ed. Janković M.M. NY: Nova Science Publishers, 2018. P. 213–250.
Sadhukhan R.K., Synzynys B.I. Review of tritium in Bangladesh before commissioning of NPP Rooppur // IOP Conf. Ser.: Mater. Sci. Eng. 2020. Art. 012009.
Kim S.B., Bredlaw M., Rousselle H. et al. Distribution of organically bound tritium (OBT) activity concentrations in aquatic biota from eastern Canada // J. of Environ. Radioact. 2019. V. 208–209. Art. 105997.
Clark I., Wilk M., Lacelle D. Environmental fate of tritium in soil and vegetation. Final report. Ottawa: Canadian Nuclear Safety Commission, 2010. Contract № 87055-07-0947:R388.1.
ISO 9698:2019. Water quality – tritium – test method using liquid scintillation counting. ISO, 2019. 25 p.
ISO 13168:2015. Water quality – simultaneous determination of tritium and carbon-14 activities – test method using liquid scintillation counting. ISO, 2015. 16 p.
Dogaru M., Calin M.A., Stan-Sion C. Tritium measurements by AMS and applications // J. of Radioanal. Nucl. Chem. 2011. V. 288. № 2. P. 491–498.
Kulkova M., Davidochkina A. Tritium in the environment of gulf of Finnland // Intern. J. of Chem. Engin. and Appl. 2011. V. 2. № 1. 8 p.
Nayak S.R., D’Souza R.S., Purushotham M.M. et al. Determination of organically bound tritium (OBT) concentration in fish by thermal oxidation and liquid scintillation counting method // Health Physics. 2021. V. 120. № 1. P. 1–8.
Kim M.A., Baumgärtner F. Validation of tritium measurements in biological materials // Fusion Technology. 1988. V. 14. № 2P2B. P. 1153–1156.
Baglan N., Alanic G., Le Meignen R. et al. A follow up of the decrease of non exchangeable organically bound tritium levels in the surroundings of a nuclear research center // J. of Environ. Radioact. 2011. V. 102. P. 695–702.
Baglan N., Kim S.B., Cossonnet C. et al. Organically bound tritium (OBT) behaviour and analysis: outcomes of the seminar held in Balaruc-les-Bains in May 2012 // Radioprotection. 2013. V. 48. P. 127–144.
Baglan N., Cossonnet C., Roche E. et al. Feedback of the third interlaboratory exercise organised on wheat in the framework of the OBT working group // J. of Environ. Radioact. 2018. V. 181. P. 52–61.
Kim S.-B., Roche J. Empirical insights and considerations for the OBT inter-laboratory comparison of environmental samples // J. of Environ. Radioact. 2013. V. 122. P. 79–85.
Силин И.И., Вайзер В.И., Момот О.А. Мониторинг трития в подземных водах вблизи ядерных реакторов // Разведка и охрана недр. 2012. № 7. С. 50–52.
Екидин А.А., Антонов К.Л., Жуковский М.В. Оценка загрязнения атмосферы тритием при испарении воды с поверхности промышленных водоемов // Вопросы радиац. безопасности. 2012. № 3. С. 3–10.
Екидин А.А., Васильев А.В., Васянович М.Е. и др. Анализ возможности поступления трития в атмосферу из баков запаса дистиллята (на примере Балаковской АЭС) // Вопросы радиац. безопасности. 2019. № 1. С. 16–24.
Екидин А.А., Антонов К.Л., Васильев А.В. и др. Оценка поступления трития в атмосферу из брызгальных бассейнов Балаковской АЭС в холодный период // Ядерная и радиац. безопасность. 2017. № 3. С. 35–46.
Ляхова О.Н., Лукашенко С.Н., Ларионова Н.В. и др. Сравнительная оценка основных источников поступления трития в воздушную среду на территории Семипалатинского испытательного полигона // Радиация и риск. 2014. Т. 23. № 3. С. 43–56.
Ляхова О.Н., Лукашенко С.Н., Тимонова Л.В. и др. Оценка уровня концентрации газообразных соединений трития в местах проведения ядерных испытаний на территории Семипалатинского испытательного полигона // Радиац. биология. Радиоэкология. 2020. Т. 60. № 6. С. 649–660.
Renard H., Connan O., Le Dizes S. et al. Experimental measurements of the bacterial oxidation of HT in soils: Impact over a zone influenced by an industrial release of tritium in HT form // J. of Environ. Radioact. 2022. V. 242. Art. 106779.
Lyakhova O., Lukashenko S., Larionova N. et al. Contamination mechanisms of air basin with tritium in venues of underground nuclear explosions at the former Semipalatinsk test site // J. of Environ. Radioact. 2012. V. 113. P. 98–107.
Okai T., Momoshima N., Takashima Y. Variation of atmospheric tritium concentrations in three different chemical forms in Fukuoka, Japan // J. of Radioan. and Nucl. Chem. 1999. V. 239. № 3. P. 527–531.
Momoshima N., Yamaguchi T., Toyoshima T. et al. Tritium in the Atmospheric Environment // J. of Nucl. and Radiochem. Sciences. 2007. V. 8. № 2. P. 117–120.
Maro D., Vermorel F., Rozet M. et al. The VATO project: An original methodology to study the transfer of tritium as HT and HTO in grassland ecosystem // J. of Environ. Radioact. 2017. V. 167. P. 235–248.
Simionov V., Duliu O. Atmospheric tritium dynamics around Cernavoda nuclear power plant // Romanian Reports in Physics. 2010. V. 62. № 4. P. 827–837.
Annual report. Vienna: IAEA, 2021. 191 p.
Zhang Y., Ye S., Wu J. A modified global model for predicting the tritium distribution in precipitation, 1960–2005 // Hydrological Processes. 2011. V. 25. № 15. P. 2379–2392.
Connan O., Maire D., Hébert D. et al. Tritium in precipitation on 5 sites in North-West France during the 2017–2019 period // J. of Environ. Radioact. 2020. V. 212. Art. 106129.
Galeriu D., Davis P., Workman W. Tritium profiles in snowpacks // J. of Environ. Radioact. 2010. V. 101. № 10. P. 869–874.
Chae J.-S., Lee S.-K., Kim Y. et al. Distribution of tritium in water vapour and precipitation around Wolsung nuclear power plant // Radiation Protection Dosimetry. 2011. V. 146. № 1–3. P. 330–333.
Harms P.A., Visser A., Moran J.E. et al. Distribution of tritium in precipitation and surface water in California // J. of Hydrology. 2016. V. 534. P. 63–72.
Gusyev M.A., Morgenstern U., Nishihara T. et al. Evaluating anthropogenic and environmental tritium effects using precipitation and Hokkaido snowpack at selected coastal locations in Asia // Science of the Total Environ. 2019. V. 659. P. 1307–1321.
Chae J.-S., Kim G. Seasonal and spatial variations of tritium in precipitation in Northeast Asia (Korea) over the last 20 years // J. of Hydrology. 2019. V. 574. P. 794–800.
Michel R.L., Jurgens B.C., Young M.B. Tritium deposition in precipitation in the United States, 1953–2012: Report. Reston, 2018. 19 p.
Chae J.-S., Kim G. Dispersion and removal characteristics of tritium originated from nuclear power plants in the atmosphere // J. of Environ. Radioact. 2018. V. 192. P. 524–531.
Радиационная обстановка на территории России и сопредельных государств в 2019 году / Под ред. Шершакова В.М., Булгакова В.Г., Крышева И.И. и др. Обнинск: Росгидромет, НПО “Тайфун”, 2020. 343 с.
Макаров В.Н., Торговкин Н.В. Тритий в снежном покрове бассейна р. Вилюй // Природные ресурсы Арктики и Субарктики. 2015. Т. 1. № 77. С. 50–55.
Ravoire J., Lorius C., Robert J. et al. Tritium content in a firn core from Antarctica // J. of Geophysical Research. 1970. V. 75. № 12. P. 2331–2335.
Makarov V.N. Tritium in snowpacks of Eastern Siberia // Tritium: advances in research and applications / Ed. Janković M.M. NY: Nova Science Publishers, 2018. P. 33–46.
Matsumoto T., Maruoka T., Shimoda G. et al. Tritium in Japanese precipitation following the March 2011 Fukushima Daiichi Nuclear Plant accident // Science of the Total Environment. 2013. V. 445–446. P. 365–370.
Rosenberg B.L., Ball J.E., Shozugawa K. et al. Radionuclide pollution inside the Fukushima Daiichi exclusion zone, part 1: Depth profiles of radiocesium and strontium-90 in soil // Applied Geochemistry. 2017. V. 85. P. 201–208.
Koga T., Morishima H., Niwa T. et al. Tritium precipitation in European cities and in Osaka, Japan owing to the Chernobyl nuclear accident // J. of Radiation Research. 1991. V. 32. № 3. P. 267–276.
Salonen L. Carbon-14 and tritium in air in Finland after the Chernobyl accident // Radiochimica Acta. 1987. V. 41. № 4. P. 145–148.
Florkowski T., Kuc T., Rozanski K. Influence of the Chernobyl accident on the natural levels of tritium and radiocarbon // Intern. J. of Rad. Appl. and Instrum. Part A. Applied Radiation and Isotopes. 1988. V. 39. № 1. P. 77–79.
Krajcar-Bronic I., Srdoc D., Obelic B. et al. Tritium activity in precipitation and in tap water of NW Yugoslavia after the Chernobyl accident // 4 European congress and 13 regional congress of IRPA. Austria: IRPA, 1988. P. 761–764.
Чеботина М.Я., Николин О.А., Мурашова Е.Л. Поступление трития на земную поверхность с дождевыми осадками // Водное хозяйство России: проблемы, технологии, управление. 2012. № 5. С. 77–87.
Чеботина М.Я., Николин О.А., Мурашова Е.Л. Тритий в дождевых осадках района расположения ФГУП “ПО Маяк” // Вопросы радиац. безопасности. 2009. № 3. С. 58–62.
Чеботина М.Я., Николин О.А. Радиоэкологические исследования трития в Уральском регионе / Под ред. Большакова В.Н., Васильева А.Г. Екатеринбург: УрО РАН, 2005. 90 с.
Нормы радиационной безопасности (НРБ-99/2009): Санитарно-эпидемиологические правила и нормативы (СанПиН 2.6.1.2523-09). М.: Федеральный центр гигиены и эпидемиологии Роспотребнадзора, 2009. 100 с.
Востротин В.В., Янов А.Ю., Финашов Л.В. Накопление трития в снежном покрове зоны влияния ПО “Маяк” за осенне-зимний сезон 2015–2016 гг. // Вопр. радиац. безопасности. 2017. № 3. С. 63–67.
Чеботина М.Я., Николин О.А., Смагин А.И. Тритий в снеговом покрове в зонах воздействия предприятий ядерно-топливного цикла на Урале // Водное хозяйство России: проблемы, технологии, управление. 2014. № 2. С. 102–113.
Kim C.-K., Rho B.-H., Lee K.J. Environmental tritium in the areas adjacent to Wolsong nuclear power plant // J. of Environ. Radioact. 1998. V. 41. № 2. P. 217–231.
Liang M., Ma Y., Ni S. et al. Analysis of tritium level around Qinshan NPP base // Radiation Protection (Taiyuan). 2009. V. 29. № 4. P. 255–260.
Голубев А.В. Поведение трития в окружающей среде // Вестник Мининского ун-та. 2015. № 2 (10). С. 1–7.
Израэль Ю.А. Атлас Восточно-Уральского и Карачаевского радиоактивных следов, включая прогноз до 2047 года. М.: ИГКЭ Росгидромета и РАН, Фонд “Инфосфера” – НИА-Природа, 2013. 140 с.
Hebert D. Tritium in precipitation of Vostok (Antarctica): conclusions on the tritium latitude effect // Isotopes in Environ. and Health Studies. 2011. V. 47. № 3. P. 265–272.
Tadros C.V., Hughes C.E., Crawford J. et al. Tritium in Australian precipitation: A 50 year record // J. of Hydrology. 2014. V. 513. P. 262–273.
Rozanski K., Gonfiantini R., Araguas-Araguas L. Tritium in the global atmosphere: distribution patterns and recent trends // J. of Physics G: Nuclear and Particle Physics. 1991. V. 17. P. S523–S536.
Fourré E., Jean-Baptiste P., Dapoigny A. et al. Past and recent tritium levels in Arctic and Antarctic polar caps // Earth and Planetary Science Letters. 2006. V. 245. № 1. P. 56–64.
Viner B.J., Goodlove S. Using a coupled dispersion model to estimate depletion of a tritium oxide plume by a forest // J. of Environ. Radioact. 2020. V. 220–221. Art. 106316.
Davis P.A. Tritium transfer parameters for the winter environment // J. of Environ. Radioact. 1997. V. 36. № 2. P. 177–196.
Королева В.С., Шестаков И.А., Сазонов А.Б. Изотопное равновесие дейтерия и трития между молекулами воды и углеводов // Успехи в химии и химической технологии. 2018. V. 32. № 9. С. 21–23.
Fiévet B., Pommier J., Voiseux C. et al. Transfer of tritium released into the marine environment by French nuclear facilities bordering the English Channel // Environ. Science & Technology. 2013. V. 47. № 12. P. 6696–6703.
Carsten A.L. Tritium in the environment // Advances in Radiation Biology / Eds. Lett J.T., Adler H. NY: Academic Press, 1979. V. 8. P. 419–458.
Inoue Y., Iwakura T. Tritium concentration in japanese rice // J. of Radiation Research. 1990. V. 31. № 4. P. 311–323.
Turner A., Millward G.E., Stemp M. Distribution of tritium in estuarine waters: the role of organic matter // J. Environ. Radioact. 2009. V. 100. № 10. P. 890–895.
Чеботина М.Я., Поляков Е.В., Гусева В.П. Роль природных органических веществ в миграционных процессах трития // Радиац. биология. Радиоэкология. 2019. Т. 59. № 5. С. 546–552.
Jean-Baptiste P., Fourré E. The distribution of tritium between water and suspended matter in a laboratory experiment exposing sediment to tritiated water // J. of Environ. Radioact. 2013. V. 116. P. 193–196.
Pearson H.B.C., Dallas L.J., Comber S.D.W. et al. Mixtures of tritiated water, zinc and dissolved organic carbon: Assessing interactive bioaccumulation and genotoxic effects in marine mussels, Mytilus galloprovincialis // J. of Environ. Radioact. 2018. V. 187. P. 133–143.
Поляков Е.В., Чеботина М.Я., Волков И.В. и др. Способ очистки вод, загрязненных тритием. 2019. Панент RU 2 680 507 C1.
Вакуловский С.М., Катрич И.Ю. Тритий в водных объектах на территории России в 1975–2012 годах // АНРИ. 2013. № 3. С. 38–42.
Черногаева Г.М., Журавлева Л.Р., Пешков Ю.В. и др. Обзор состояния и загрязнения окружающей среды в Российской Федерации за 2020 год / Под ред. Черногаевой Г.М. М.: Федеральная служба по гидрометеорологии и мониторингу окружающей среды (Росгидромет), 2021. 205 с.
Чионов В.Г., Носов А.В., Казаков С.В. и др. Оценка влияния трития в сбросах АЭС на радиационное состояние водных объектов // Метеорология и гидрология. 2017. № 5. С. 98–104.
Лунева Е.В. Содержание радионуклидов в поверхностных водах, донных отложениях и гидробионтах реки Неман // Биология внутренних вод. 2018. № 1. С. 100–106.
Hanslík E., Marešová D., Juranová E. et al. Comparison of balance of tritium activity in waste water from nuclear power plants and at selected monitoring sites in the Vltava river, Elbe river and Jihlava (Dyje) river catchments in the Czech Republic // J. of Environ. Manag. 2017. V. 203. P. 1137–1142.
Кулькова М.А., Лебедев С.В., Нестеров Е.М. и др. Радиоуглерод и тритий в водной системе Санкт-Петербургского региона // Изв. Российского гос. пед. ун-та им. А.И. Герцена. 2014. № 165. С. 93–97.
Чеботина М.Я. Тритий в воде Белоярского водохранилища в период работы трех энергоблоков АЭС // Водное хозяйство России: проблемы, технологии, управление. 2010. № 4. С. 58–73.
Jean-Baptiste P., Baumier D., Fourré E. et al. The distribution of tritium in the terrestrial and aquatic environments of the Creys-Malville nuclear power plant (2002–2005) // J. of Environ. Radioact. 2007. V. 94. P. 107–118.
Чеботина М.Я., Трапезников А.В., Трапезникова В.Н. и др. Радиоэкологические исследования Белоярского водохранилища. Свердловск: УрО АН СССР, 1992. 80 с.
Чеботина М.Я., Николин О.А. Тритий в экосистеме водоема-охладителя АЭС // Уральский геофизический вестник. 2003. № 1. С. 93–97.
Николин О.А. Тритий в водных экосистемах Уральского региона: Автореф. … канд. биол. наук. Пермь, 2008. 21 с.
Brunella R., Raffaele B. Tritium as a tool to assess leachate contamination: An example from conversano landfill (Southern Italy) // J. of Geochemical Exploration. 2022. Art. 106939.
Брезгунов В.С., Ферронский В.И. Природный тритий как индикатор перестройки вертикальной структуры водных масс Каспийского моря при колебаниях его уровня // Водные ресурсы. 2005. Т. 32. № 4. С. 406–409.
Stewart M.K., van der Raaij R.W. Response of the Christchurch groundwater system to exploitation: Carbon-14 and tritium study revisited // Science of the Total Environ. 2022. Art. 152730.
Bondareva L. Tritium in the freshwater ecosystem of the Yenisei river: behavior, accumulation, and transformation // Tritium: Advance in Research and Application / Ed. Janković M.M. NY: Nova Science Publishers, 2018. P. 47–98.
Bolsunovsky A.Y., Bondareva L.G. Tritium in surface waters of the Yenisei river basin // J. of Environ Radioact. 2003. V. 66. № 3. P. 285–294.
Кабанов М.В., Маркелова А.Н., Мелков В.Н. и др. Мониторинг концентрации трития в водных объектах и березовом соке в окрестностях города Томска // Экологические системы и приборы. 2012. № 1. С. 42–45.
Kostyuchenko V., Akleyev A., Popova I.Y. et al. Environmental migration of radionuclides (90Sr, 137Cs, 239Pu) in accidentally contaminated areas of the Southern Urals // Radioactive Waste / Ed. Rahman R.O.A. Intech, 2012. P. 65–98.
Казачёнок Н.Н., Попова И.Я., Мельников В.С. и др. 3Н, 90Sr, 137Cs, 239,240Pu в системе реки Теча // Вода: химия и экология. 2013. № 11. С. 10–15.
Чеботина М.Я., Николин О.А., Смагин А.И. и др. Тритий в водоемах производственного и комплексного назначения в районе ПО “Маяк” на Урале // Водное хозяйство России: проблемы, технологии, управление. 2011. № 4. С. 75–84.
Актаев М.Р., Лукашенко С.Н., Айдарханов А.О. и др. Распределение микро- и макрокомпонентов и искусственных радионуклидов в водоеме “Атомное озеро” // Радиац. биология. Радиоэкология. 2019. Т. 59. № 3. С. 311–320.
Айдарханов А.О., Лукашенко С.Н., Айдарханова А.К. и др. Радиоактивное загрязнение вод реки Шаган (по результатам 2011-го года) // Радиация и риск. 2014. Т. 23. № 4. С. 35–42.
Гудков Д.И., Кузьменко М.И. Тритий в водоемах 30-километровой зоны Чернобыльской АЭС. Киев: Наукова думка, 1996. 130–133 с.
Гудков Д.И. Тритий в пресных водах Украины и его действие на гидробионтов: Автореф. … канд. биол. наук. Киев, 1995. 24 с.
Гудков Д.И. Динамика содержания трития в пойменных водоемах р. Припять и пруде-охладителе Чернобыльской АЭС // Радиац. биология. Радиоэкология. 1999. Т. 39. № 6. С. 605–608.
Takahata N., Tomonaga Y., Kumamoto Y. et al. Direct tritium emissions to the ocean from the Fukushima Daiichi nuclear accident // Geochemical J. 2018. V. 52. № 2. P. 211–217.
Тишков В.П., Анисович К.В., Бондаренко Л.Г. и др. Исследования радиационной обстановки в районах побережья и прилегающих акваторий российского Дальнего Востока и Курило-Камчатского региона, а также северо-западной части Тихого океана в связи с аварией на японской АЭС “Фукусима-1”. Итоги экспедиций 2011, 2012 и 2014 гг. // АНРИ. 2016. № 2. С. 31–40.
Povinec P.P., Aoyama M., Biddulph D. et al. Cesium, iodine and tritium in NW Pacific waters – a comparison of the Fukushima impact with global fallout // Biogeosciences. 2013. V. 10. № 8. P. 5481–5496.
Сергеев А.Ф., Поздеев Ю., Салюк А.Н. и др. О распределении трития в циркуляции вод в Чукотском море в зимне-весенний период // Докл. АН СССР. 1990. Т. 312. № 6. С. 1472–1475.
Kaizer J., Aoyama M., Kumamoto Y. et al. Tritium and radiocarbon in the western North Pacific waters: post-Fukushima situation // J. of Environ. Radioact. 2018. V. 184–185. P. 83–94.
Shozugawa K., Hori M., Johnson T.E. et al. Landside tritium leakage over through years from Fukushima Daiichi nuclear plant and relationship between countermeasures and contaminated water // Scientific Reports. 2020. V. 10. № 1. Art. 19925.
Buesseler K.O. Opening the floodgates at Fukushima // Science. 2020. V. 369. № 6504. P. 621–622.
Турченко Д.В., Лукашенко С.Н., Айдарханов А.О. и др. Изучение содержания трития в снежном покрове горного массива Дегелен // Сборник трудов Национального ядерного центра Республики Казахстан “Актуальные вопросы радиоэкологии Казахстана” / Под ред. Лукашенко С.Н. Павлодар, Курчатов: Дом печати, 2011. С. 233–242.
Турченко Д.В., Лукашенко С.Н., Айдарханов А.О. и др. Изучение содержания трития в снежном покрове на реке Шаган // Сборник трудов Национального ядерного центра Республики Казахстан “Актуальные вопросы радиоэкологии Казахстана” / Под ред. Лукашенко С.Н. Павлодар: Дом печати, 2011. С. 329–334.
Турченко Д.В., Лукашенко С.Н., Айдарханов А.О. и др. Исследование содержания трития в снежном покрове в местах проведения подземных ядерных взрывов // Радиац. биология. Радиоэкология. 2018. Т. 58. № 2. С. 174–182.
Тимонова Л.В., Ляхова О.Н., Лукашенко С.Н. и др. Распределение трития в почве на территории “Атомного” озера Семипалатинского испытательного полигона // Почвоведение. 2020. № 3. С. 358–365.
Serzhanova Z.B., Aidarkhanova A.K., Lukashenko S.N. et al. Researching of tritium speciation in soils of “Balapan” site // J. of Environ. Radioact. 2018. V. 192. P. 621–627.
Тимонова Л.В., Ляхова О.Н., Айдарханов А.О. и др. Тритий в прочносвязанной форме в почвах Семипалатинского испытательного полигона // Журн. радиац. исслед. 2018. Т. 5. № 2. С. 126–127.
Артамонова С.Ю. Современная радиоэкологическая ситуация на объекте мирного подземного ядерного взрыва “Кратон-3” (1978 г.) в Якутии // Астраханский вестник эколог. образования. 2016. № 3 (37). С. 14–24.
Собакин П.И., Герасимов Я.Р., Чевычелов А.П. и др. Радиоэкологическая обстановка в зоне воздействия аварийного подземного ядерного взрыва “Кратон-3” в Республике Саха (Якутия) // Радиац. биология. Радиоэкология. 2014. Т. 54. № 6. С. 641‒649.
Артамонова С.Ю. Техногенные радионуклиды в природных водах районов мирных подземных ядерных взрывов “Кратон-3” и “Кратон-4” // Геоэкология. Инженерная геология. Гидрогеология. Геокриология. 2013. № 5. С. 417–428.
Востротин В.В., Янов А.Ю., Финашов Л.В. Соотношение объемной активности трития в талом снеге и березовом соке в зоне влияния Производственного объединения “Маяк” весной 2016 года // Радиац. биология. Радиоэкология. 2020. Т. 60. № 3. С. 298–304.
Калашникова Д.А., Волков Ю.В., Маркелова А.Н. и др. Радиоуглерод и тритий в объектах окружающей среды. Практическое использование этих радиоизотопов // Радиоактивность и радиоактивные элементы в среде обитания человека: Мат-лы V междун. конф. Томск: ТГУ, 2016. С. 274–277.
Коваленко О.В., Кряжич О.О. Исследование зависимостей миграции трития по цепочке “талая вода снегового покрова–растение” // Технические науки и технологии. 2016. № 3. С. 231–239.
Vold E.L. A brief review of environmental transport of tritium at the Los Alamos LLRW disposal facility. Los Alamos: Los Alamos National Lab., 1994. 15 p.
Kim S.B., Bredlaw M., Rousselle H. et al. Organically bound tritium (OBT) activity concentrations in surface soil at the Chalk River Laboratories, Canada // J. of Environ. Radioact. 2019. V. 208–209. Art. 105999.
Davis P., Leclerc E., Galeriu D. et al. Specific activity models and parameter values for tritium, 14C and 36Cl // Quantification of radionuclide transfer in terrestrial and freshwater environments for radiological assessments, IAEA–TECDOC–1616, 2009. 549 p.
Kim S.B., Workman W.J.G., Davis P.A. et al. HTO and OBT concentrations in a wetland ecosystem // Fusion Science and Technology. 2008. V. 54. № 1. P. 248–252.
Thompson P.A., Kwamena N.O.A., Ilin M. et al. Levels of tritium in soils and vegetation near Canadian nuclear facilities releasing tritium to the atmosphere: implications for environmental models // J. of Environ. Radioact. 2015. V. 140. P. 105–113.
Kim S.B., Bredlaw M., Korolevych V.Y. HTO and OBT activity concentrations in soil at the historical atmospheric HT release site (Chalk River Laboratories) // J. of Environ. Radioact. 2012. V. 103. № 1. P. 34–40.
Teng Y., Zuo R., Wang J. et al. Detection of tritium sorption on four soil materials // J. of Environ. Radioact. 2011. V. 102. № 2. P. 212–216.
Айдарханов А.О., Лукашенко С.Н., Субботин С.Б. и др. Состояние экосистемы р. Шаган и основные механизмы его формирования // Актуальные вопросы радиоэкологии Казахстана: сб. тр. Института радиационной безопасности и экологии за 2007–2009 гг. / Под ред. Лукашенко С.Н. Павлодар: Дом печати, 2010. С. 9–55.
Mitchell P.I., Vintró L.L., Omarova A. et al. Tritium in well waters, streams and atomic lakes in the East Kazakhstan oblast of the Semipalatinsk nuclear test site // J. of Radiological Protection. 2005. V. 25. № 2. P. 141–148.
Субботин С.Б., Айдарханов А.О., Дубасов Ю.В. Исследование миграции трития с подземными водами на бывшем Семипалатинском полигоне // Радиохимия. 2013. Т. 55. № 5. С. 471–478.
Артамонова С.Ю. Тритий как индикатор радиоэкологической обстановки в районе мирного подземного ядерного взрыва “Кристалл” // Астраханский вестник экологического образования. 2019. № 4. С. 4–13.
Чеботина М.Я., Николин О.А. Миграция трития от предприятий ядерного технологического цикла в источники питьевого водоснабжения на Урале // Водное хозяйство России: проблемы, технологии, управление. 2013. № 4. С. 90–100.
Чеботина М.Я., Николин О.А., Рыбаков Е.Н. Уровни содержания трития в источниках питьевого водоснабжения района БАЭС на Урале // Уральский геофизический вестник. 2011. № 1. С. 40–44.
Иваницкая М.В., Малофеева А.И. Источники поступления трития в окружающую среду // Тритий – это опасно. Челябинск: Движение за ядерную безопасность, Центр поддержки гражданских инициатив, 2001. С. 22–29.
Рыбин А.А., Рождественская Л.Н., Ряскова М.В. Измерение активности трития в поверхностных и глубинных подземных водах как эффективный инструмент контроля целостности защитных барьеров хранилищ для жидких радиоактивных отходов // Сборник трудов АО ГНЦ НИИАР. 2010. № 3. С. 57–59.
Парамонова Т.И., Польский О.Г., Каширин И.А. и др. Тритий на спецкомбинатах “Радон”, содержание в окружающей среде // Медицина труда и промышленная экология. 2006. № 10. С. 42–46.
Kashiwaya K., Muto Y., Kubo T. et al. Spatial variations of tritium concentrations in groundwater collected in the southern coastal region of Fukushima, Japan, after the nuclear accident // Scientific Reports. 2017. V. 7. № 1. Art. 12578.
Fourre E., Jean-Baptiste P., Dapoigny A. et al. Tritium/Helium-3 dating of groundwaters around Chernobyl site // Geochimica et Cosmochimica Acta. 2010. V. 74. № 12. Art. A301.
Каюкова Е.П. Формирование изотопного состава природных вод Горного Крыма под влиянием естественных процессов // Вестник СПбГУ. Сер. 7. Геология. География. 2016. № 2. С. 11–26.
Соколовский Л.Г., Поляков В.А., Соколова А.В. и др. Изотопно-гидрогеохимическое изучение подземных и поверхностных вод Западно-Сибирского артезианского бассейна и Уральской сложной гидрогеологической складчатой области // Разведка и охрана недр. 2010. № 7. С. 65–71.
Jakimavičiūtė-Maselienė V., Cidzikienė V. Modelling of tritium transport in the underground water from hypothetical reactor at the new NPP site in Lithuania // Progress in Nuclear Energy. 2015. V. 80. P. 1–6.
Ota M., Kwamena N.-O.A., Mihok S. et al. Role of soil-to-leaf tritium transfer in controlling leaf tritium dynamics: Comparison of experimental garden and tritium-transfer model results // J. of Environ. Radioact. 2017. V. 178–179. P. 212–231.
Guetat P., Boyer C., Tognelli A. et al. 50 years environmental tritium transfer review in the vicinity of French Research Centre // Fusion Science and Technology. 2011. V. 60. № 4. P. 1238–1243.
Galeriu D., Davis P., Raskob W. et al. Recent progresses in tritium radioecology and dosimetry – today and tomorrow // Fusion Science and Technology. 2008. V. 54. № 1. P. 237–242.
Belot Y., Guenot J., Caput C. et al. Incorporation of tritium into organic matter of terrestrial plants exposed to tritiated-water releases of short duration // Health Physics. 1983. V. 44. № 6. P. 666–668.
Korolevych V.Y., Kim S.B., Davis P.A. OBT/HTO ratio in agricultural produce subject to routine atmospheric releases of tritium // J. of Environ. Radioact. 2014. V. 129. P. 157–168.
Mihok S., Wilk M., Lapp A. et al. Tritium dynamics in soils and plants grown under three irrigation regimes at a tritium processing facility in Canada // J. of Environ. Radioact. 2016. V. 153. P. 176–187.
Melintescu A., Galeriu D. Uncertainty of current understanding regarding OBT formation in plants // J. of Environ. Radioact. 2017. V. 167. P. 134–149.
Galeriu D., Melintescu A., Strack S. et al. An overview of organically bound tritium experiments in plants following a short atmospheric HTO exposure // J. of Environ. Radioact. 2013. V. 118. P. 40–56.
Meng D., Wang W., Du Y. et al. Tritium distribution in typical plants around tritium laboratory in south-west of China // J. of Environ. Radioact. 2021. V. 227. P. 106 504.
Krištof R., Košenina S., Zorko B. et al. Tritium in organic matter around Krško Nuclear Power Plant // J. of Radioanal. Nucl. Chem. 2017. V. 314. № 2. P. 675–679.
Boyer C., Vichot L., Fromm M. et al. Tritium in plants: a review of current knowledge // Environ. and Experim. Botany. 2009. V. 67. № 1. P. 34–51.
Choi Y.H., Lim K.M., Lee W.Y. et al. Tritium levels in Chinese cabbage and radish plants acutely exposed to HTO vapor at different growth stages // J. of Environ. Radioact. 2005. V. 84. № 1. P. 79–94.
Cline J. Absorption and metabolism of tritium oxide and tritium gas by bean plants // Plant Physiology. 1953. V. 28. № 4. P. 717–723.
Choi Y.H., Lim K.M., Lee W.Y. et al. Tissue free water tritium and organically bound tritium in the rice plant acutely exposed to atmospheric HTO vapor under semi-outdoor conditions // J. of Environ. Radioact. 2002. V. 58. № 1. P. 67–85.
Guidelines for calculating derived release limits for radioactive material in airborne and liquid effluents for normal operation of nuclear facilities // Toronto: CSA, 2014. P. 1–14.
Mihok S., Clark I.D., Wilk M. et al. Tritium dynamics in soils and plants at a tritium processing facility in Canada // Intern. Conf. on Radioec. and Environ. Radioact. Barcelona, Spain, 2014. O-015.
Svetlik I., Fejgl M., Malátová I. et al. Enhanced activities of organically bound tritium in biota samples // Appl. Radiation and Isotopes. 2014. V. 93. P. 82–86.
Brudenell A.J.P., Collins C.D., Shaw G. Dynamics of tritiated water (HTO) uptake and loss by crops after short-term atmospheric release // J. of Environ. Radioact. 1997. V. 36. № 2. P. 197–218.
Joshi C., Patra A., Jha M. et al. Studies on foliar uptake of tritiated water on Spinach sp. during light and dark simulated conditions using environmental chamber // Radiat. Prot. and Environ. 2021. V. 44. № 3. P. 131–134.
Бобков В.М., Долін В.В. Ізотопний обмін тритію в процесі вегетації верби // Збірник наукових праць Інституту геохімії навколишнього середовища. 2016. № 25. С. 49–55.
Узиков В. Вакуумное разделение молекул воды по изотопам водорода. 2021. URL: http://www.proatom.ru/ modules.php?name=News&file=article&sid=9612 (дата обращения: 14.04.2021).
Larionova N.V., Lukashenko S.N., Lyakhova O.N. et al. Plants as indicators of tritium concentration in ground water at the Semipalatinsk test site // J. of Environ. Radioact. 2017. V. 177. P. 218–224.
Kim S.B., Korolevych V. Quantification of exchangeable and non-exchangeable organically bound tritium (OBT) in vegetation // J. of Environ. Radioact. 2013. V. 118. P. 9–14.
Kim S.B., Bredlaw M., Farrow F. Determination of changes to TFWT and OBT concentrations in potatoes and Swiss chard as a result of preparation for human consumption // J. of Environ. Radioact. 2014. V. 137. P. 18–21.
Boyer C., Gontier G., Chauveau J. et al. Environmental survey near a decommissioning nuclear facility: example of tritium monitoring in the terrestrial environment of Creys-Malville // Intern. Conf. on Radioec. and Environ. Radioact. Barcelona, Spain, 2014. O-050.
Поливкина Е.Н., Ларионова Н.В., Ляхова О.Н. Оценка аэрального поглощения НТО культурой Helianthus annuus в условиях Семипалатинского испытательного полигона // Радиация и риск. 2020. Т. 29. № 1. С. 79–89.
Diabaté S., Strack S. Organically bound tritium in wheat after short-term exposure to atmospheric tritium under laboratory conditions // J. of Environ. Radioact. 1997. V. 36. № 2. P. 157–175.
Galeriu D., Melintescu A., Lazar C. Development of CROPTRIT model: the dynamics of tritium in agricultural crops // Intern. Conf. on Radioec. and Environ. Radioact. Barcelona, Spain, 2014. O-043.
Twining J.R., Hughes C.E., Harrison J.J. et al. Biotic, temporal and spatial variability of tritium concentrations in transpirate samples collected in the vicinity of a near-surface low-level nuclear waste disposal site and nearby research reactor // J. of Environ. Radioact. 2011. V. 102. № 6. P. 551–558.
Yamada Y., Yasuike K., Komura K. Temporal variation of tritium concentration in tree-ring cellulose over the past 50 years // J. of Radioanal. Nucl. Chem. 2004. V. 262. № 3. P. 679–683.
Кабанов М.В., Маркелова А.Н., Мелков В.Н. и др. Содержание трития и радиоуглерода в природных средах в окрестностях г. Томска // Вопросы радиац. безопасности. 2013. № 4. С. 30–44.
Кабанов Д.И., Кочетков О.А., Фомин Г.В. и др. К обоснованию контроля органически связанного трития в окружающей среде ядерных установок // Вопросы атомной науки и техники. Серия: Термоядерный синтез. 2012. № 1. С. 17–22.
Durzan D.J., Mia A.J., Wang B.S.P. Effects of tritiated water on the metabolism and germination of jack pine seeds // Can. J. of Botany. 1971. V. 49. № 12. P. 2139–2149.
Dinner P.J., Gorman D.J., Spencer F.S. Tritium dynamics in vegetables: experimental results // Proceedings: tritium technology in fission, fusion, and isotopic applications. Dayton: Amer. Nucl. Society, 1980. P. 9–13.
Hisamatsu S.I., Inoue Y., Takizawa Y. Tritium concentrations in some European foods // J. of Environ. Radioact. 1989. V. 10. № 3. P. 251–255.
Van Hook R.I., Deal S.L. Tritium uptake and elimination by tissue-bound and body-water components in crickets (Acheta domesticus) // J. of Insect Physiology. 1973. V. 19. № 3. P. 681–687.
Nakagaki B.J., Defoliart G.R. Comparison of diets for mass-rearing Acheta domesticus (Orthoptera: Gryllidae) as a novelty food, and comparison of food conversion efficiency with values reported for livestock // J. of Economic Entomology. 1991. V. 84. № 3. P. 891–896.
Takeda H., Kasida Y. Biological behavior of tritium after administration of tritiated water in the rat // J. of Radiation Research. 1979. V. 20. № 2. P. 174–185.
Radwan I., Pietrzak-Flis Z., Jaworowski Z. Tritium retention in rat after administration of various doses of tritiated water // Current topics in radiation research quarterly. 1978. V. 12. № 1–4. P. 278–290.
Kelsey-Wall A., Seaman J.C., Jagoe C.H. et al. Rodents as receptor species at a tritium disposal site // J. of Environ. Radioact. 2005. V. 82. № 1. P. 95–104.
Le Goff P., Guétat P., Vichot L. et al. Tritium levels in milk in the vicinity of chronic tritium releases // J. of Environ. Radioact. 2016. V. 151. P. 282–292.
Bogen D.C., Welford G.A. “Fallout Tritium” Distribution in the Environment // Health Physics. 1976. V. 30. № 2. P. 203–208.
van den Hoek J., ten Have M.H., Gerber G.B. The meta-bolism of tritium and water in the lactating dairy cow // Health Physics. 1983. V. 44. № 2. P. 127–133.
van den Hoek J., Have M.H.J., Gerber G.B. et al. The transfer of tritium-labeled organic material from grass into cow’s milk // Radiation Research. 1985. V. 103. № 1. P. 105–113.
Байгазинов Ж.А., Лукашенко С.Н., Паницкий А.В. и др. Переход трития в кобылье молоко // Современные проблемы науки и образования. 2014. № 2. С. 498–498.
Galeriu D., Melintescu A., Beresford N.A. et al. Modelling 3H and 14C transfer to farm animals and their products under steady state conditions // J. of Environ. Radioact. 2007. V. 98. № 1. P. 205–217.
Eyrolle-Boyer F., Boyer P., Claval D. et al. Apparent enrichment of organically bound tritium in rivers explained by the heritage of our past // J. of Environ. Radioact. 2014. V. 136. P. 162–168.
Blaylock B.G., Hoffman F.O., Frank M.L. Tritium in the aquatic environment. Oak Ridge: Oak Ridge National Lab., 1986. 28 p.
Jaeschke B.C., Bradshaw C. Bioaccumulation of tritia-ted water in phytoplankton and trophic transfer of organically bound tritium to the blue mussel, Mytilus edulis // J. of Environ. Radioact. 2013. V. 115. P. 28–33.
Gogate S.S., Krishnamoorthy T.M. Uptake of tritiated lysine by fresh water alga, Scenedesmus obliquus // Indian. J. Exp. Biol. 1983. V. 21. № 9. P. 504–506.
Бондарева Л.Г. Исследование содержания трития в некоторых компонентах экосистемы р. Енисей на участке среднего течения // Радиохимия. 2015. Т. 57. № 5. С. 475–480.
Baeza A., García E., Paniagua J.M. et al. Study of the comparative dynamics of the incorporation of tissue free-water tritium (TFWT) in bulrushes (Typha latifolia) and carp (Cyprinus carpio) in the Almaraz nuclear power plant cooling reservoir // J. of Environ. Radioact. 2009. V. 100. № 3. P. 209–214.
Бондарева Л.Г. Исследования по накоплению трития некоторыми водными организмами: икра и рыба (Carassius gibelio), водные растения (Ceratophyllum и Lemna) // Радиац. биология. Радиоэкология. 2020. Т. 60. № 1. С. 71–81.
Лащенова Т.Н., Бондарева Л.Г., Федорова Н.Е. и др. Выявление путей поступления трития в пресноводные организмы при эксплуатации горно-химического комбината // Гигиена и санитария. 2017. Т. 96. № 9. С. 844–848.
Strack S., Kistner G. Biokinetic aspects of tissue-bound tritium in algae // Current topics in radiation research quarterly. 1978. V. 12. № 1–4. P. 133–141.
Jaeschke B.C., Millward G.E., Moody A.J. et al. Tissue-specific incorporation and genotoxicity of different forms of tritium in the marine mussel, Mytilus edulis // Environ. Pollution. 2011. V. 159. № 1. P. 274–280.
Jha A.N., Dogra Y., Turner A. et al. Impact of low doses of tritium on the marine mussel, Mytilus edulis: Genotoxic effects and tissue-specific bioconcentration // Mutation Research/Genetic Toxicology and Environ. Mutagenesis. 2005. V. 586. № 1. P. 47–57.
Yankovich T.L., Kim S.B., Baumgärtner F. et al. Measured and modelled tritium concentrations in freshwater Barnes mussels (Elliptio complanata) exposed to an abrupt increase in ambient tritium levels // J. of Environ. Radioact. 2011. V. 102. № 1. P. 26–34.
Janovics R., Bihari Á., Papp L. et al. Monitoring of tritium, 60Co and 137Cs in the vicinity of the warm water outlet of the Paks Nuclear Power Plant, Hungary // J. of Environ. Radioact. 2014. V. 128. P. 20–26.
Melintescu A., Galeriu D., Kim S. Tritium dynamics in large fish – a model test // Radioprotection. 2011. V. 46. № 6. P. S431–S436.
Arcanjo C., Maro D., Camilleri V. et al. Assessing tritium internalisation in zebrafish early life stages: importance of rapid isotopic exchange // J. of Environ. Radioact. 2019. V. 203. P. 30–38.
Patzer R., Moghissi A., McNelis D. Accumulation of tritium in various species of fish reared in tritiated water // Environmental behavior of radionuclides released by the nuclear industry. Vienna: IAEA, 1973. P. 403–412.
Kim S.B., Rowan D., Chen J. et al. Tritium in fish from remote lakes in northwestern Ontario, Canada // J. of Environ. Radioact. 2018. V. 195. P. 104–108.
Ould-Dada Z., Fairlie I., Read C. Transfer of radioactivity to fruit: significant radionuclides and speciation // J. of Environ. Radioact. 2001. V. 52. № 2. P. 159–174.
Modelling the environmental transport of tritium in the vicinity of long-term atmospheric and sub-surface sources. Vienna: IAEA, 2003. 284 p.
Linsley G., Torres C. The international biosphere modelling and assessment programme (BIOMASS): an overview // J. of Environ. Radioact. 2004. V. 74. № 1. P. 279–283.
Korolevych V.Y., Kim S.B. Modelling and validation of OBT formation in tomato and potato plants // Fusion Science and Technology. 2011. V. 60. № 4. P. 1288–1291.
Environmental modelling for radiation safety (EMRAS) – a summary report of the results of the EMRAS programme (2003–2007). Vienna: IAEA, 2012. 67 p.
Betti M., Aldave de las Heras L., Janssens A. et al. Results of the European Commission MARINA II study: part I – general information and effects of discharges by the nuclear industry // J. of Environ. Radioact. 2004. V. 74. № 1. P. 243–254.
MARINA II. Update of the MARINA Project on the radiological exposure of the European Community from radioactivity in North European marine waters. EC, 2003. 364 p.
MARINA II. Update of the MARINA Project on the radiological exposure of the European Community from radioactivity in North European marine waters. Executive Summary. EC, 2003. 332 p.
Krylov A.L., Nossov A.V., Kazakov S.V. SIBYLLA Code: Assessment of water bodies contamination and doses received by population due to radioactivity discharges into the hydrosphere // Intern. Conf. on Fast Reactors and Related Fuel Cycles: Next Generation Nucl. Systems for Sustainable Development (FR17). IAEA, 2017. P. 1–10.
Jeffers R.S., Parker G.T. Development, description and validation of a Tritium Environmental Release Model (TERM) // J. of Environ. Radioact. 2014. V. 127. P. 95–104.
Le Dizès S., Aulagnier C., Henner P. et al. TOCATTA: a dynamic transfer model of 3H from the atmosphere to soil-plant systems // J. of Environ. Radioact. 2013. V. 124. P. 191–204.
Higgins N.A. TRIF – an intermediate approach to environmental tritium modelling // J. of Environ. Radioact. 1997. V. 36. № 2. P. 253–267.
Liger K., Grisolia C., Cristescu I. et al. Overview of the TRANSAT (TRANSversal Actions for Tritium) project // Fusion Engin. and Design. 2018. V. 136. P. 168–172.
Дополнительные материалы отсутствуют.