Электрохимия, 2019, T. 55, № 2, стр. 239-244
Влияние электрического тока на смачиваемость водными растворами углеродсодержащих газодиффузионных электродов и изменение их емкостных характеристик
Г. А. Колягин a, *, В. Л. Корниенко a, **
a Институт химии и химической технологии СО РАН,
Федеральный исследовательский центр “Красноярский научный центр СО РАН”
660036 Красноярск, Академгородок, 50, стр.24, Россия
* E-mail: kolyagin@icct.ru
** E-mail: kvl@icct.ru
Поступила в редакцию 25.04.2018
После доработки 21.06.2018
Принята к публикации 25.07.2018
Аннотация
Исследовано влияние обработки электрическим током двухслойных газодиффузионных электродов из пористого (66–68 об. %) композиционного материала на основе ацетиленовой сажи А-437Э и политетрафторэтилена. Поляризацию проводили циклически в диапазоне 0.0 ± 2.0 В анодным (в 1 М H2SO4) и катодным (в 0.5 М КОН) токами с добавками бромистого тетрабутиламмония (ТБАБ). Установлено в обоих случаях, что увеличение количества пропущенного электричества приводит к росту объема электролитных пор и электрической емкости электродов. При анодной поляризации увеличение смачиваемости и емкости электродов происходит в большей степени, чем при катодной, но в последнем случае поверхность сажи не подвергается окислению. С увеличением количества пропущенного электричества и концентрации ТБАБ наблюдается рост омических потерь. Рассмотрены возможные причины возникновения наблюдаемых явлений.
ВВЕДЕНИЕ
Углеграфитовые материалы широко используют при изготовлении электродов для различных электрохимических устройств. С целью изменения физико-химических свойств углеграфитовые материалы подвергают обработке различными методами. Электрохимические методы обработки отличаются от термических и химических бóльшими возможностями [1]. Степень окисления или восстановления легко контролируется потенциалом, током, временем и составом электролита. Обработку можно проводить при комнатной температуре и атмосферном давлении, условия реакции могут быть очень точно воспроизведены. Электрохимические события, происходящие при поляризации электродов, весьма разнообразны и поэтому важно знать, как влияет ток на свойства композитов из углеграфитовых материалов и фторсодержащих связующих, которые в основном используют при изготовлении электродов [2].
Специальную обработку углеграфитовых материалов и электродов на их основе проводят электрическим током с различной целью: увеличение смачиваемости электродов при использовании плохо смачиваемых водными электролитами материалов [1, 3–5], функционализации поверхности [3, 6], получение на поверхности графеноподобных структур [7, 8] и самих графеновых частиц при электрохимическом расщеплении графита [9, 10], получение соединений внедрения и расширенного графита [11, 12]. А также для проведения ускоренных испытаний электродов при повышенных токах и поляризациях для оценки ресурса их работы [2], анодную обработку еще применяют для увеличения емкости электрохимических конденсаторов [1, 3, 4] и т.д.
Для обработки катодным током углеграфитовых материалов широко используют тетраалкил-аммониевые соли (ТААС). Ранее нами было показано, что при потенциалах выделения водорода в водном растворе щелочи с добавлением ТААС происходит значительное ускорение процесса затопления гидрофобизированных пористых электродов электролитом по сравнению с чистым раствором [5]. Влияние ТААС растет с увеличением молекулярного веса ионов в ряду: тетраметиламмоний, тетраэтиламмоний, тетрабутиламмоний. В данном случае полученные результаты коррелируют с правилом Траубе для поверхностно-активных веществ (ПАВ): величина межфазного натяжения на границе раздела воздух–вода уменьшается с каждой дополнительной метиленовой группой в цепи [13, 14].
ТААС являются поверхностно-активными веществами и широко используются для электрохимической интеркаляции в графит в неводных электролитах. Адсорбируясь на поверхности графеновых листов при интеркаляции, они препятствуют их повторной укладке. Образование соединений внедрения легче происходит с катионами, содержащими алкильные частицы с 4–8 атомами углерода [12]. Интеркаляция начинается при –1.5 В, относительно хлоридсеребряного электрода сравнения, и увеличивается при смещении потенциала в более катодную область. В [8] показано, что при внедрении катионов ТАА в частицы графита происходит образование стабильной поверхности из графеновых частиц. Получены графеновые частицы при интеркаляции катионов ТАА в пирографит и графитовые стержни [10]. На графитовом стержне внедрение идет лучше, чем на пирографите.
Обработка электрическим током углеродных материалов может значительно изменить их физико-химические свойства. Например, анодная поляризация повышает электрическую емкость углеродных наностенок в 30–50 раз за счет функционализации поверхности, увеличивает количество структурных дефектов и смачиваемость водным электролитом [3]. Эффективным способом повышения электрической емкости углеродных наноструктурированных материалов (нанотрубки, нанобумага) является также их γ-облучение в воде [15].
Цель данной работы – исследовать и сравнить влияние катодного и анодного токов на изменение смачиваемости и электрической емкости реальных двухслойных газодиффузионных электродов из пористых материалов на основе ацетиленовой сажи А-437Э и политетрафторэтилена (ПТФЭ). Подобные электроды, например, используют при исследовании процесса электросинтеза Н2О2 из О2 [16].
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Условия проведения экспериментов, устройство электролизера и изготовление электродов были подробно описаны ранее в [5, 16]. Электродную массу готовили совместной коагуляцией водных суспензий ПТФЭ (фторопласт-4Д) и ацетиленовой сажи А-437Э. Массу отфильтровывали, промывали водой, высушивали при 120°С до постоянного веса, размалывали на ножевой мельнице, просеивали через сито с размером ячейки 0.25 мм и прогревали при температуре 300°С в течение 1 ч. Далее из этой массы в пресс-форме формовали двухслойные электроды в виде плоских дисков толщиной 1 мм, общей пористостью 66–68 об. %. Рабочий слой содержал 10 мас. %, газоподводящий – 40 мас. % ПТФЭ. Соотношение их масс 1 : 2 соответственно. В середину газоподводящего слоя помещали никелевую сетку.
Перед экспериментами для уменьшения количества поверхностных оксидных групп, которые могли появиться на саже при спекании, электроды подвергали воздействию катодным током 0.1 А в течение 1 ч в 0.5 М водном растворе KOH при потенциалах выделения водорода. Для контроля за смачиваемостью поверхности сажи определяли электролитную пористость электродов методом гидростатического взвешивания до и после эксперимента. Электролитная пористость электродов перед обработкой током составляла ∼2 об. %.
Эксперименты проводили в стеклянной ячейке-электролизере фильтр-прессного типа при 20°С. Католит и анолит (1 М H2SO4) разделяли катионообменной мембраной МФ-4СК-100. Противоэлектрод – платиновая пластина. Все характеристики электрода, помещенного в обойму из фторопласта, рассчитывали на единицу видимой фронтальной поверхности (5 см2). Потенциал электрода контролировали на его фронтальной стороне относительно насыщенного хлоридсеребряного электрода сравнения (ЭВЛ-1М1).
Электроды поляризовали в 1 М H2SO4 циклически анодным током при скорости развертки потенциала 10 мВ/с в интервале от 0.0 до 2.0 В. То же делали при катодной обработке в интервале от 0.0 до –2.0 В в 0.5 М КОН с добавлением тетрабутиламмония бромистого (ТБАБ) в различных концентрациях. Считается, что скорость изменения поверхности углеграфитовых материалов больше при циклической развертке потенциала по сравнению с потенциостатическим режимом [17].
При пропускании катодного тока смачиваемость электрода увеличивается незначительно, поэтому обработку электрода проводили следующим образом: электрод обрабатывали в растворе с наименьшей концентрацией ТБАБ, затем в растворе с более высокой концентрацией и т.д. по несколько циклов в каждом растворе и измеряли характеристики после всех циклов в данном растворе.
Для определения электрической емкости электродов регистрировали циклические вольт-амперные кривые при скорости развертки потенциала 1–80 мВ/с в 3 М КОН в диапазоне 0.0…–0.14 В. Условия выбраны таким образом, чтобы исключить влияние псевдоемкости. Ток заряжения двойного слоя вычисляли, деля пополам абсолютное значение тока при –0.075 В, находящееся между кривыми, полученными при прямой и обратной развертке потенциала. Далее по тангенсу угла наклона прямолинейного участка зависимости плотности тока заряжения от скорости изменения потенциала (рис. 1 и 2) определяли емкость на единицу площади габаритной поверхности электрода в Ф/см2 [5]. Так как емкость двойного слоя, в общем, пропорциональна смоченной электролитом поверхности сажи [1], то по относительному увеличению емкости можно говорить о соответствующем изменении площади поверхности. Полученные результаты приведены в таблицах и на рисунках.
Рис. 1.
Зависимость плотности тока заряжения от скорости развертки потенциала, полученная на электроде после его анодной поляризации в 1 М H2SO4: 1 – до обработки, 2 – после первого цикла, 3 – после четвертого цикла. Количество пропущенного электричества приведено в табл. 1.

Рис. 2.
Зависимость плотности тока заряжения от скорости развертки потенциала, полученная на электроде после обработки катодным током в 0.5 М КОН в присутствии ТБАБ. Концентрация ТБАБ: 1 – 0.001; 2 – 0.01; 3 – 0.05; 4 – 0.2. Количество пропущенного электричества приведено в табл. 2.

РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Как видно из табл. 1 и 2, с увеличением количества пропущенного электричества растет плотность тока, но прирост уменьшается и даже становится отрицательным при катодной поляризации, что обусловлено уменьшением с каждым циклом доли несмоченных частиц сажи, увеличением омических потерь и ростом поляризации при адсорбции ТАА катионов.
Электролитная пористость электрода после анодной обработки увеличилась в 14 раз, емкость, определенная по графикам на рис. 1, а, следовательно, и смоченная электролитом поверхность сажи, увеличились в 4.7 раза (табл. 1, рис. 3). Объем всех пор в рабочем слое в расчете на единицу площади габаритной поверхности электрода ∼0.022 см3/см2, а объем пор, заполненных электролитом после обработки – ∼0.025 см3/см2. Можно предположить, что рабочий слой практически промок полностью, так как он содержит незначительное количество ПТФЭ и непосредственно соприкасается с электролитом.
Таблица 1.
Результаты обработки электрода анодным током в 1 М H2SO4
| Номер цикла обработки электрода | 0* | 1 | 2 | 3 | 4 |
|---|---|---|---|---|---|
| Плотность тока при 2.0 В, мА/см2 | – | 120 | 175 | 220 | 240 |
| Общее количество пропущенного электричества, мА ч/см2 | 0 | 1.68 | 4.34 | 7.74 | 11.61 |
| Количество пропущенного электричества в каждом цикле, мА ч/см2 | 0 | 1.68 | 2.66 | 3.40 | 3.87 |
| Увеличение емкости по сравнению с первоначальным значением, разы | 1 | 3.20 | – | – | 4.70 |
| Электролитная пористость, об. % | 1.8 | – | – | – | 25 |
Рис. 3.
Влияние количества пропущенного электричества на емкость электрода при анодной поляризации в 1 М H2SO4 (1) и катодной (2) в 0.5 М КОН. Подробности в табл. 1 и 2.
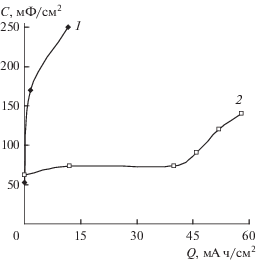
При катодной обработке через электрод пропущено, по сравнению с анодной поляризацией, почти в 5 раз больше электричества, но электролитная пористость увеличивается всего в 3.9 раза, с 2.4 до 9.4 об. %, емкость в 1.9 раза, с 74 до 140 мФ/см2 (табл. 2, рис. 3). Объем пор, заполненных электролитом ∼0.0094 см3/см2. В этом случае рабочий слой промок частично. В [5] проведена оценка удельной емкости сажи А-437А в тех же условиях – 9.2 мкФ/см2. Отсюда, исходя из полученных данных по изменению емкости, площадь смоченной поверхности увеличилась с 0.8 до 1.5 м2/см2 в расчете на площадь габаритной поверхности электрода.
Таблица 2.
Параметры обработки электрода катодным током в 0.5 М КОН с добавками ТБАБ
| № п/п | Концентрация ТБАБ, М | Количество пропущенного электричества, мА ч/см2 | Средняя плотность тока при –2.0 В, мА/см2 |
|---|---|---|---|
| 1 | 0.000 | 12 | 70 |
| 2 | 0.001 | 40 | 74 |
| 3 | 0.010 | 46 | 90 |
| 4 | 0.050 | 52 | 62 |
| 5 | 0.200 | 58 | 62 |
Из рис. 1 и 2 видно, что с увеличением количества пропущенного электричества увеличивается наклон прямолинейного участка кривых и соответственно емкость электродов (рис. 3). Это связано с увеличением смачиваемости сажи и появлением новой поверхности, что приводит к увеличению площади смоченной электролитом поверхности и, следовательно, емкости. Увеличение смачиваемости объясняется появлением на поверхности сажи кислородсодержащих функциональных групп [2–4, 6, 17–19], а также частичным разрушение фторопласта как отмечено, например, в работе [18].
Увеличение площади поверхности возможно также за счет формирования на поверхности сажевых частиц микроскопических графеноподобных структур [7, 8, 10, 12]. При анодном окислении происходит частичное раскрытие сажевых частиц с разрыхлением поверхности вследствие образования на ней малослойных графеновых структур [7]. При катодной поляризации в присутствии ТБАБ возможно незначительное внедрение катиона ТБА в сажевую частицу и разрыхление ее слоев [9, 10, 12]. Таким образом, происходит как бы увеличение шероховатости поверхности сажевых частиц.
При катодной поляризации основную роль в увеличении смачиваемости играет специфическая адсорбция тетраалкиламмониевых катионов, обладающих свойствами ПАВ, способными влиять на свойства границы раздела фаз [5, 20]. Увеличивается смачивание графитовой поверхности как в составе чисто сажевых пор, так и в конгломератах, образованных с участием ПТФЭ. После промывки и сушки электродов их первоначальная гидрофобность не восстанавливается.
При наличии в электролите ТБАБ возможно действие расклинивающего эффекта (эффект Ребиндера [13, 14]), когда молекулы ПАВ внедряются между частицами сажи и между частицами сажи и ПТФЭ, тем самым увеличивают площадь смоченной поверхности и объем микропор. ПАВ в нашем случае является катионом, проникновению которого в пористый электропроводный материал способствует катодная поляризация.
В литературе встречаются описания похожих явлений. Так, например, в [6] увеличение емкости электродов из наноструктурированного углерода (нанотрубки, колончатые структуры) в присутствии ПАВ в несколько раз объясняется увеличением поверхности, что связывается с проявлением расклинивающего эффекта Ребиндера. Происходит разрыхление поверхности углеродного материала, распад жгутов, в которые объединяются нанотрубки, расщепление углеродных “чешуек” и т.д., что приводит к увеличению поверхности, доступной для электролита. При анодной поляризации углеродных наностенок происходит увеличение емкости в 30–50 раз, а при адсорбции поверхностно активных органических веществ – только в 3–5 раз [3]. Подобное различие наблюдается и в наших исследованиях, то есть, повышение емкости и смачиваемости при анодной поляризации больше, чем при адсорбции ТАА катионов, что видно из графиков, представленных на рис. 3.
При увеличении количества пропущенного электричества, зависимости на рис. 1 и 2 отклоняются от прямолинейности с повышением скорости развертки потенциала. Увеличение электролитной пористости приводит к увеличению характерного времени подхода ионов электролита к поверхности поры, которое становится больше времени развертки потенциала. Это объясняется увеличением омических потерь как в самом электроде, так и в его электролитных порах. Увеличение омических потерь в электролитных порах связано с распространением процесса вглубь электрода и уменьшением диаметра пор, что затрудняет доступ ионов к поверхности сажи внутри электрода. При анодной поляризации хемосорбированные кислородсодержащие частицы могут частично блокировать нанопоры, что вызывает их сужение и увеличение извилистости, а также возможно их взаимодействие с ионами раствора, которое уменьшает скорость массопереноса [1, 4]. Ионы ТБАБ при адсорбции в мелких порах также могут затруднять массоперенос, особенно при больших концентрациях и высоких скоростях развертки потенциала (рис. 2).
Повышение электрического сопротивления самого композиционного материала электродов связано с ростом контактного сопротивления между частицами сажи при ее окислении [1, 19] и проявлением эффекта Ребиндера.
ЗАКЛЮЧЕНИЕ
Проведенные исследования показали, что при анодной поляризации до 2.0 В в растворе H2SO4 увеличение смачиваемости и емкости электродов из композиционного материала на основе ацетиленовой сажи и ПТФЭ происходит в большей степени, чем при катодной поляризации до –2.0 В в щелочном растворе ТБАБ. С увеличением количества пропущенного электричества и концентрации ТБАБ повышаются смачиваемость электродов, электрическая емкость и омические потери.
Приведенные в статье данные могут быть полезны для увеличения смачиваемой водными растворами поверхности композитов на основе углеграфитовых материалов и гидрофобных пластмасс, а также при анализе работы электродов под током в водных растворах. Если не желательно окисление поверхности углеродного материала при испытаниях композиционных материалов, катодная поляризация в щелочном растворе ТААС может быть альтернативой анодному окислению.
Список литературы
Tabti, Z., Berenguer, R., Ruiz-Rosas, R., Quijada, C., Morallon, E., and Cazorla-Amoros, D., Electrooxidation methods to produce pseudocapacitance-containing porous carbons, Electrochemistry, 2013, vol. 81, p. 833.
Park, J., Oh, H., Ha, T., Lee, Y.I., and Min, K., A review of the gas diffusion layer in proton exchange membrane fuel cells: Durability and degradation, Appl. Energy, 2015, vol. 155, p. 866.
Komarova, N.S., Krivenko, A.G., Stenina, E.V., Sviridova, L.N., Mironovich, K.V., Shulga, Y.M., and Krivchenko, V.A., Enhancement of the carbon nanowall film capacitance. Electron transfer Kinetics on Functionalized Surfaces, Langmuir, 2015, vol. 31, p. 7129.
Zuleta, M., Bjornbom, P., and Lundblad., A., Effects of Pore Surface Oxidation on Electrochemical and Mass-Transport Properties of Nanoporous Carbon, J. Electrochem. Soc., 2005, vol. 152, p. A270.
Колягин, Г.А. Корниенко, В.Л. Пропитка водным раствором электродов из ацетиленовой сажи со связующим политетрафторэтиленом и оценка удельной емкости ее двойного слоя. Электрохимия. 2018. Т. 54. С. 111. [Kolyagin, G.A. and Kornienko, V.L., Impregnation of Acetylene Black Electrodes with a Polytetrafluoroethylene Binder with an Aqueous Solution and Evaluation of Its Specific Double Layer Capacity, Russ. J. Electrochem., 2017, vol. 53, p. 96.]
Кривенко, А.Г., Комарова, Н.С., Свиридова, Л.Н., Стенина, Е.В. Адсорбционные характеристики электродов, содержащих наноструктурированный углерод различной морфологии. Электрохимия. 2009. Т. 45. С. 1141. [Krivenko, A.G., Komarova, N.S., Sviridova, L.N., and Stenina, E.V., Adsorption characteristics of electrodes containing nanostructured carbon of different morphology, Russ. J. Electrochem., 2009, vol. 45, p. 1064.]
Kim, T., Ham, Ch., Rhee, Ch.K., Yoon, S.-H., Tsuji, M., and Mochida, I., Morphological reason for enhancement of electrochemical double layer capacitances of various acetylene blacks by electrochemical polarization, Electrochim. Acta, 2008, vol. 53, p. 5789.
Jouikov, V. and Simonet, J., Doping of cathodically polarized glassy carbon by natural graphite. A simple procedure for overlaying different carbons with electrochemically modifiable graphene layers, Electrochim. Acta, 2015, vol. 172, p. 28.
Alanyalioglu, M., Segura, J.J., Oro-Sole, J., and Casan-Pastor, N., The synthesis of graphene sheets with controlled thickness and order using surfactant-assisted electrochemical processes, Carbon, 2012, vol. 50, p. 142.
Cooper, A.J., Wilson, N.R., Kinloch, I.A., and Dryfe, R.A.W., Single stage electrochemical exfoliation method for the production of few-layer graphene via intercalation of tetraalkylammonium cations, Carbon, 2014, vol. 66, p. 340.
Колягин, Г.А., Корниенко, В.Л., Кузнецов, Б.Н., Чесноков, Н.В. Журн. прикл. химии. 2005. Т. 78. С. 1653. [Kolyagin, G.A., Kornienko, V.L. Kuzne-tsov, B.N., and Chesnokov, N. V., Electrical Conductivity of Hydrophobized Electrodes Fabricated from Thermally Expanded Graphite and Their Activity in Electroreduction of Oxygen, Russ. J. Appl. Chem., 2005, vol. 78, p. 1625.]
De-E Liu, Guoxin Xie, Dao Guo, Ziyi Cui, Lina Si, Chunlei Wan, Wu Zou, and Jianbin Luo, Tunable lubricity of aliphatic ammonium graphite intercalation compounds at the micro/nanoscale, Carbon, 2017, vol. 115, p. 574.
Ребиндер, П.А. Поверхностные явления в дисперсных системах. Физико-химическая механика. Избранные труды. М.: Наука, 1979. 384 с. [Rebinder, P.A., Surface phenomena in disperse systems. Physico-chemical mechanics. Selected Works (in Russian), Moscow: Nauka, 1979, 384 p.]
Сумм, Б.Д., Горюнов, Ю.В. Физико-химические основы смачивания и растекания. М.: Химия, 1976. 232 с. [Summ, B.D. and Gorynov, Yu.V., Physicochemical bases of wetting and spreading, (in Russian), Moscow: Khimiya, 1976, 384 p.]
Кривенко, А.Г., Комарова, Н.С., Стенина, Е.В., Свиридова, Л.Н., Курмаз, В.А., Коткин, А.С., Мурадян, В.Е. Электрохимическое поведение электродов, содержащих наноструктурированный углерод различной морфологии в катодной области потенциалов. Электрохимия. 2006. Т. 42. С. 1164. [Krivenko, A.G., Komarova, N.S., Stenina, E.V., Svi-ridova, L.N., Kurmaz, V.A., Kotkin, A.S., and Muradyan, V.E., Electrochemical Behavior of Electrodes Containing Nanostructured Carbon of Various Morphology in the Cathodic Region of Potentials, Russ. J. Electrochem., 2006, vol. 42, p. 1047.]
Колягин, Г.А., Корниенко, В.Л. Электросинтез Н2О2 из О2 в газодиффузионных электродах для получения органических надкислот и комплекса Н2О2 с мочевиной. Электрохимия. 2015. Т. 51. С. 217. [Kolyagin, G.A. and Kornienko, V.L., Electrosynthesis of Н2О2 from O2 in gas diffusion electrodes for the preparation of organic peracids and the complex of H2O2 with urea, Russ. J. Electrochem., 2015, vol. 51, p. 185.]
Perry, M.L., Patterson, T., and Madden, T., GDL Degradation in PEFC, ECS Transactions, 2010, vol. 33, p. 1081.
Yu, S.C., Li, X.J., Liu, S., Hao, J.K., Shao, Z.G., and Yia, B.L., Study on hydrophobicity loss of the gas diffusion layer in PEMFCs by electrochemical oxidation, RSC Adv., 2014, vol. 4, p. 3852.
Kim, Y.-T. and Mitani, T., Competitive effect of carbon nanotubes oxidation on aqueous EDLC performance: Balancing hydrophilicity and conductivity, J. Power Sources, 2006, vol. 158, p. 1517.
Майрановский, С.Г. Свойства растворов тетразамещенных солей аммония. Их влияние на электродные процессы, в Электросинтез и биоэлектрохимия. (Прогресс электрохимии органических соединений), Ред. Фрумкин, А.Н., Страдынь, Я.П., Феоктистов, Л.Г., М.: Наука, 1975. С. 252–281. [Mayranovsky, S.G., Properties of solutions of tetrasubstituted ammonium salts. Their influence on electrode processes, in Electrosynthesis and bioelectrochemistry. (Progress in the electrochemistry of organic compounds) Frumkin, A.N., Stradyn, Ya.P., and Feoktistov, L.G., Eds. (in Russian), Moscow: Nauka, 1975. P. 252–281.]
Дополнительные материалы отсутствуют.


