Электрохимия, 2019, T. 55, № 3, стр. 278-285
Компакты из легированного бором синтетического алмаза: электрохимические свойства образцов с предельно высоким уровнем легирования
Ю. В. Плесков a, *, М. Д. Кротова a, Е. А. Екимов b
a Институт физической химии и электрохимии им. А.Н. Фрумкина РАН
119071 Москва, Ленинский просп., 31, Россия
b Институт физики высоких давлений им. Л.Ф. Верещагина РАН
142190 Москва, Троицк, Россия
* E-mail: pleskov33@mail.ru
Поступила в редакцию 19.06.2018
После доработки 19.06.2018
Принята к публикации 25.09.2018
Аннотация
Компакты из легированного бором алмаза с предельно высоким уровнем легирования были получены при давлении 8–9 ГПа и температурах около 2500 K из смесей графита и 5 или 7% карбида бора (B4C). Содержание бора в алмазе, оцененное по параметру решетки алмаза (соответственно, 0.3573–0.3575 и 0.3576–0.3578 нм), имеет максимальное значение около 1–3 и 3–4%. Полученные компакты демонстрируют на примере реакции анодного выделения хлора наибольшую для всех известных алмазных, алмазсодержащих и алмазоподобных электродных материалов электрохимическую активность. В согласии с найденной ранее общей закономерностью для алмазных, алмаз-содержащих и алмазоподобных материалов, и в данном случае с ростом уровня легирования, заметен некоторый рост электроактивности материала (тока реакции электроокисления ионов хлора). Показана возможность использования электродов из высоколегированных бором алмазных компактов для электроаналитического определения этилендиаминтетрауксусной кислоты в водном растворе по току ее окисления.
ВВЕДЕНИЕ
Электроды из синтетического алмаза за последние 30 лет после появления первой работы, посвященной их изучению [1], сделались привычным объектом электрохимических исследований [1–5]. Нами установлено, что электрохимическая активность алмазных, алмазсодержащих и алмазоподобных материалов повышается с ростом их электропроводности, независимо от природы этого роста. Действительно, проводимость полупроводниковых микрокристаллических алмазных CVD-пленок растет с увеличением концентрации легирующей примеси бора (акцептора) в результате повышения концентрации электронных дырок; проводимость азотированных нанокристаллического алмаза и алмазоподобного углерода – с ростом концентрации азота, по-видимому, из-за увеличения доли sp2-гибридизованного углерода, проводимость которого выше, чем sp3-гибридизованного углерода; проводимость отожженных в вакууме нелегированных алмазных CVD-пленок – с ростом температуры отжига, из-за роста количества проводящего “графитоподобного” углерода по межкристаллитным границам. Во всех этих случаях повышается электрохимическая активность: это наблюдается и для CVD-пленок [6], и для нанокристаллического алмаза [7], и для алмазоподобного углерода [8], и для нелегированных отожженных в вакууме алмазных пленок [9]. В цитированных работах электрохимическую активность электродов характеризовали в квазиобратимой окислительно-восстановительной системе ферро-феррицианид, измеряя либо непосредственно (методом электрохимического импеданса) сопротивление переноса заряда RF, обратно пропорциональное току обмена, либо разность потенциалов анодного и катодного пиков тока циклической вольтамперограммы. В частности, свойства алмазных CVD-пленок с ростом концентрации бора постепенно меняются от полупроводниковых к квазиметаллическим и, в конце концов, их электродное поведение становится квазиобратимым (коэффициент переноса α ~ 0.5, разность потенциалов анодного и катодного пиков при комнатной температуре ~60 мВ).
Недавно мы добавили к перечисленным выше алмазным электродным материалам еще один их вид, а именно компакты из сильно легированного бором синтетического алмаза [10]. В настоящей работе исследованы компакты с очень высоким уровнем легирования бором. Для полноты представленной выше картины мы исследовали влияние изменения уровня легирования компактов на их электроактивность11. Дополнительно, была изучена принципиальная возможность применения электродов-компактов для электроаналитического определения органического вещества по току его окисления (на примере этилендиаминтетрауксусной кислоты, ЭДТУ).
МЕТОДИКА ЭКСПЕРИМЕНТА
Получение образцов
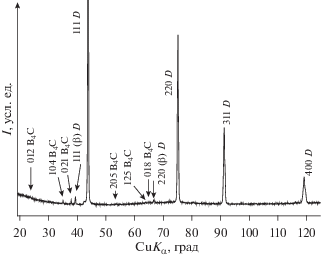
Синтез образцов осуществляли при давлениях 8–9 ГПа и температурах около 2500 K из смесей графита марки МГОСЧ (99.9999%) и карбида бора (99.4%). Смеси приготавливались перетиранием в ступке из яшмы. Параметры синтеза алмаза в системе карбид бора (B4C)–углерод были определены нами ранее [11], а подробности эксперимента при высоких давлениях и температурах представлены в работе [12]. Под давлением при температуре плавления эвтектики карбид бора–графит (около 2500 K) образуется жидкая ростовая среда, в которой растворяется графит и из которой кристаллизуется легированный бором алмаз. Согласно представлениям о строении фазовых диаграмм эвтектического типа с ограниченными твердыми растворами компонент, при температуре плавления эвтектики карбид бора–графит равновесная растворимость бора в алмазе должна быть максимальной. Продолжительность синтеза не превышала 10 с. Были получены цилиндрические компакты диаметром 3.5–4 и высотой 2.5 мм. Образцы отмывались в кипящей хлорной кислоте в течение 50 ч для удаления графита и карбида бора с поверхности образцов. На рис. 1 представлена дифрактограмма одного из образцов, полученного съемкой с торцевой поверхности компакта после кислотной обработки. Из анализа дифракционных данных следует, что алмаз и карбид бора B4C являются единственными фазами, присутствующими в образце.
Рис. 1.
Дифрактограмма, иллюстрирующая фазовый состав алмазных компактов, полученных синтезом под давлением из смесей графита и карбида бора B4C.
На рис. 2 показаны микроструктуры торцевой поверхности образца после химической обработки и поверхности излома образца после его раскалывания. С использованием микрорентгеноспектрального анализа было изучено распределение бора и углерода на поверхности излома образца. Присутствие борсодержащих включений и отсутствие пустот на изломе указывают на сохранение исходной структуры в объеме образца после химической обработки. Данное исследование указывает на формирование в образце алмазной матрицы, фаза карбида бора в которой находится в виде изолированных неудаляемых кислотной обработкой включений.
Рис. 2.
Микроструктуры поверхности образца после кислотной обработки (а) и излома образца после его раскалывания (б, в). Изображения излома в характеристическом рентгеновском излучении бора (г) и углерода (д) показывают присутствие обогащенного бором включения в алмазной матрице и относительно однородное распределение бора в алмазе.

В образцах, обозначенных Е5 и Е7, концентрация B4C в шихте составляла, соответственно, 5 и 7%; параметр решетки алмаза в образцах определялся с использованием эталона кремния NIST640C и составил для этих двух образцов значения, соответственно, 0.3573–0.3575 и 0.3576–0.3578 нм. Этим значениям параметра решетки соответствуют концентрации бора в алмазе 1–3% [или (2–5) × 1021 см–3] и 3–4%, оцененные по ранее построенной зависимости параметра решетки алмаза от содержания бора в алмазе [13]. Концентрация бора в алмазе 3–4%, как следует из работы [13], является максимальной для алмаза, синтезированного при высоких давлениях.
Электрохимические измерения
Методика измерений описана в предыдущей статье [10]. Вкратце, мы исследовали образцы в форме дисков диаметром 3.5–4 и высотой 2.5 мм. Была использована ячейка с платиновым противоэлектродом. Площадь поверхности рабочего электрода-компакта составляла ~0.1 см2. Значения потенциала в статье приводятся по отношению к хлорид-серебряному (1 М КCl) электроду сравнения (ХСЭ), а значения плотности тока и дифференциальной емкости отнесены к 1 см2 геометрической поверхности электрода. Измерения проводили в растворе индифферентного электролита (1 М KCl).
Спектры электрохимического импеданса в интервале частот переменного тока f от 1 Гц до 20 кГц измеряли с помощью анализатора спектров SOLARTRON, модель 1280B (Великобритания), а при более высоких частотах (до 200 кГц) – моста переменного тока Р-5021 (Украина). Значения элементов эквивалентной схемы получали путем сравнения экспериментально измеренных годографов импеданса с теоретически рассчитанными годографами для выбранной эквивалентной схемы, а именно схемы Эршлера–Рэндлса, в которой дифференциальная емкость заменена на элемент постоянной фазы (СРЕ). Годографы импеданса – как снятые при заданном потенциале с разверткой по частоте переменного тока f (так называемые f-sweep), так и поляризационные, снятые на фиксированной частоте при развертке потенциала Е (так называемые E-sweep) – получали с помощью анализатора спектров SOLARTRON. На нем же снимали циклические вольтамперограммы при скорости развертки потенциала 20 мВ/с.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Метод циклической вольтамперометрии
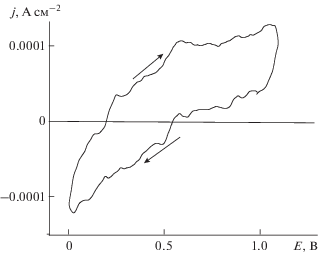
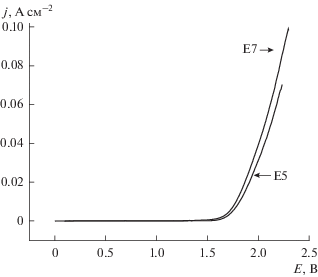
На рис. 3 приведены поляризационные потенциодинамические кривые, снятые в растворе KCl при анодной развертке потенциала для двух электродов-компактов c концентрацией бора 1–3 и 3–4%. Как и для ранее исследованных компактов [10], кривые имеют широкую область идеальной поляризуемости, за которой следует резкий подъем тока анодного выделения хлора в результате электроокисления ионов Cl–. В согласии со сформулированной выше закономерностью, и в данном случае с ростом уровня легирования заметен некоторый рост электроактивности материала (тока реакции).
Рис. 3.
Поляризационные потенциодинамические кривые, снятые в 1 М растворе KCl при анодной развертке потенциала для двух электродов-компактов c концентрацией бора 1–3% (Е5) и 3–4% (Е7).
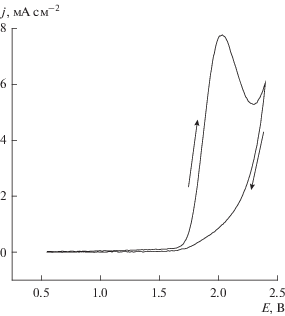
На рис. 4 показана циклическая вольтамперограмма, снятая в области идеальной поляризуемости (фоновый ток). Этот фоновый ток для сильно легированного компакта составляет 50–100 мкА см–2, что опять-таки несколько выше, чем для компактов с меньшей концентрацией бора [10]; но, в общем, он остается достаточно малым и не препятствует исследованию электрохимических процессов, протекающих в области потенциалов идеальной поляризуемости.
Метод электрохимического импеданса
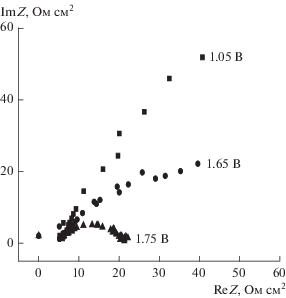
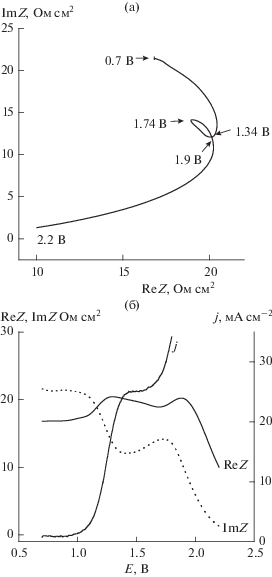
Годограф импеданса “f-sweep” приведен на рис. 5. Его форма свидетельствует о наличии в эквивалентной схеме электрода элемента постоянной фазы (СРЕ), заменяющего в эквивалентной схеме Эршлера–Рэндлса дифференциальную емкость. Действительно, в области идеальной поляризуемости это – наклонная прямая, а при потенциалах электродной реакции – приплюснутые полуокружности. Присутствие СРЕ в эквивалентной схеме вообще характерно для алмазных электродов, хотя его природа так и остается не до конца выясненной [2]. Напомним, что импеданс СРЕ равняется ZCPE = σ–1(iω)–a, где частотно-независимый множитель σ измеряется в единицах Фa Ом1 – a см–2, параметр a определяет характер частотной зависимости, ω = 2πf – круговая частота переменного тока, а i – мнимая единица.
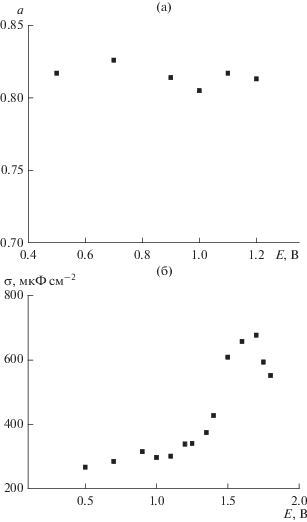
По данным рис. 5 были определены параметры эквивалентной схемы a и σ. В области идеальной поляризуемости параметр a мало зависит от потенциала (рис. 6а). Низкочастотная “емкость” (т.е., величина σ при условии a = 1) в области идеальной поляризуемости также мало зависит от потенциала, а в области выделения хлора растет (рис. 6б), что, вероятно, связано с появлением псевдоемкости электродной реакции.
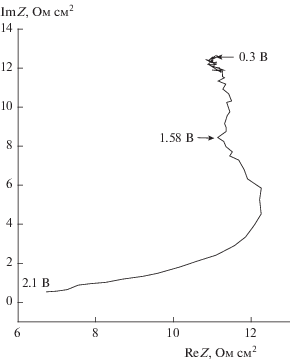
Поляризационный годограф (E-sweep, рис. 7) имеет обычный для алмазных электродов вид [10, 14]: почти вертикальная “прямая” в области идеальной поляризуемости и вертикальная “полуокружность” (искаженная благодаря наличию СРЕ) в области выделения хлора; такая форма годографа не противоречит приведенной выше поляризационной кривой (рис. 3).
Анодное окисление этилендиаминтетрауксусной кислоты
Область идеальной поляризуемости алмазных электродов простирается до весьма высоких положительных потенциалов, поэтому эти электроды хорошо подходят для исследования окисления органических веществ (в том числе трудно окисляемых) [3, 4]. Так, например, циклические вольтамперограммы анодного окисления бензола как на алмазном CVD-тонкопленочном электроде [15], так и на умеренно легированном бором алмазном компакте [16] содержат пик тока при потенциале 2 В (ХСЭ). Такова же циклическая вольтамперограмма бензола и на сильно легированном компакте (рис. 8)22. Но для выяснения возможности электроаналитического определения органического аналита мы остановились не на бензоле, а на этилендиаминтетрауксусной кислоте (ЭДТУ), потому что ее концентрацию можно удобно менять в более широких пределах.
Этилендиаминтетрауксусная кислота – распространенный умягчитель воды (а также ее загрязнитель, когда речь идет о сточных водах). В настоящей работе мы не ставим своей целью разработать метод электроанализа этилендиаминтетрауксусной кислоты, а лишь хотим продемонстрировать потенциальную пригодность алмазных электродов-компактов для этой цели; поэтому мы ограничимся исследованием концентрационной зависимости тока окисления.
На рис. 9 показаны поляризационные кривые анодного окисления ЭДТУ, снятые при различных ее концентрациях. Несмотря на относительно близкие потенциалы этой реакции и реакции окисления фона (КСl), кривые имеют достаточно хорошо выраженный максимум тока, высота которого зависит от концентрации реагента. Плотность тока в максимуме (после вычета тока фона) оказалась пропорциональной концентрации с этилендиаминтетрауксусной кислоты в пределах от 0.001 до 0.05 г-экв л–1 (рис. 10); уравнение линейной регрессии этой калибровочной кривой таково: j (мA cм–2) = 0.09115 + 192.79 с (г-экв л–1), доверительная вероятность R2 = 0.9992, чувствительность ~193 (мА л)/(г-экв см2). Отметим, что при анодном окислении ЭДТУ на алмазном CVD-тонкопленочном электроде [17] также была получена линейная калибровочная кривая с R2 = = 0.9946, но токи были меньше.
Рис. 9.
Поляризационные кривые анодного окисления ЭДТУ на электроде Е7 (1 М KCl). Концентрации ЭДТУ (г-экв л–1) указаны на кривых.
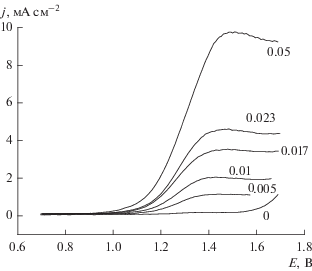
Рис. 10.
Калибровочная кривая определения ЭДТУ (1 М KCl, образец Е7): (◻) метод стандартных добавок; (◼) серия растворов различной концентрации.
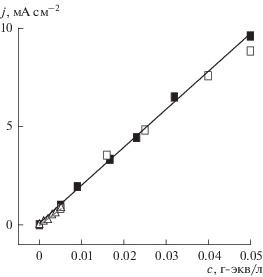
Существенно, что на рис. 10 совмещены два графика, относящиеся к двум разным способам изменения концентрации ЭДТУ в ячейке. В одном случае эту концентрацию постепенно повышали, добавляя порциями концентрированный раствор ЭДТУ (метод стандартных добавок). В другом – была заранее приготовлена серия растворов различной концентрации. Как видно, калибровочные кривые в обоих случаях практически совпадают.
Поляризационный годограф анода-компакта в растворе КСl + ЭДТУ изображен на рис. 11а. Его снимали от более положительного потенциала, чем годограф на рис. 7, поэтому на нем практически отсутствует “вертикальная прямая”, относящаяся к области идеальной поляризуемости, а осталась лишь “полуокружность”. Годограф в растворе, содержащем ЭДТУ, отличается от такового в растворе фона (рис. 7) наличием “петли” в области тока окисления ЭДТУ, которая начинается при потенциале 1.34 В, близком к потенциалу полуволны окисления ЭДТУ. В конце концов, кривая вновь выходит на “полуокружность” реакции выделения хлора при 1.9 В. Истолковать этот годограф легче с помощью вычисленных из него зависимостей компонентов импеданса Im Z и Re Z от потенциала Е, приведенных на рис. 11б вместе с кривой “ток–потенциал”. Эти зависимости Im Z и Re Z, в общем, отражают ход тока с потенциалом. Величина сопротивления (Re Z) мало зависит от потенциала до начала сильного выделения хлора (~1.85 В), где она спадает, очевидно, за счет резкого уменьшения сопротивления переноса заряда RF. Одновременно падает и емкостное сопротивление Im Z, т.к. растет связанная с реакцией псевдоемкость. Эти совместные изменения и приводят к появлению “петли” на годографе. Существенно, что форма поляризационного годографа (рис. 11а) хорошо согласуется с формой независимо снятой поляризационной кривой (рис. 3).
ЗАКЛЮЧЕНИЕ
Электрохимическая активность легированных бором алмазных электродов-компактов в реакции анодного выделения хлора несколько повышается с ростом уровня легирования материала, в согласии с найденной ранее общей для алмазных электродов закономерностью. Электрод-компакт из сильно легированного бором синтетического алмаза может служить индикаторным электродом при электроаналитическом определении этилендиаминтетрауксусной кислоты по току ее анодного окисления.
Список литературы
Плесков, Ю.В., Сахарова, А.Я., Кротова, М.Д., Буйлов, Л.Л., Спицын, Б.В. Фотоэлектрохимическое поведение полупроводникового алмаза. Электрохимия. 1987. Т. 24. С. 69–73. [Pleskov, Yu.V., Sakharova, A.Ya., Кротова, М.D., Bouilov, L.L., and Spitsyn, B.V., Photoelectrochemical behavior of semiconductor diamond, Elektrokhimiya, 1987, vol. 24, p. 69–73.]
Плесков, Ю.В. Электрохимия алмаза. Москва: Едиториал УРСС, 2003. 101 с. [Pleskov, Yu.V., Electrochemistry of Diamond, Moscow: Editorial URSS, 2003.]
Electrochemistry of Diamond, Eds. Fujishima, A., Einaga, Y., Rao, T.N., and Tryk, D.A., Tokyo: BKC & Amsterdam: Elsevier, 2005.
Synthetic Diamond Films: Preparation, Electrochemistry, Characterization and Applications, Eds. Brillas, E. and Martinez-Huitle, C.A., New York: Wiley, 2011.
Topics in Applied Physics, vol. 121, Ed. Yang, N, Springer, 2015.
Модестов, А.Д., Плесков, Ю.В., Варнин, В.П., Теремецкая, И.Г. Электроды из синтетического полупроводникового алмаза: исследование электрохимической активности в растворе окислительно-восстановительной системы. Электрохимия. 1997. Т. 33. С. 60. [Modestov, A.D., Pleskov, Yu.V., Varnin, V.P., and Teremetskaya, I.G., Synthetic Semiconductor Diamond Electrodes: A Study of Electrochemical Activity in a Redox System Solution, Russ. J. Electrochem., 1997, vol. 33, p. 55.]
Плесков, Ю.В., Кротова, М.Д., Ральченко, В.Г., Савельев, А.В., Божко, А.Д. Электрохимическое поведение азотированных нанокристаллических алмазных электродов. Электрохимия. 2007. Т. 43. С. 868. [Pleskov, Yu.V., Krotova, M.D., Ralchenko, V.G., Saveliev, A.V., and Bozhko, A.D., Electrochemical Behavior of Nitrogenated Nanocrystalline Diamond Electrodes, Russ. J. Electrochem., 2007, vol. 43, p. 837.]
Плесков, Ю.В., Кротова, М.Д., Поляков, В.И., Хомич, А.В., Руковишников, А.И., Друз, Б.Л., Зарицкий, И.М. Электрохимические свойства пленок аморфного азотсодержащего гидрогенизированного алмазоподобного углерода. Электрохимия. 2000. Т. 36. С. 1141. [Pleskov, Yu.V., Krotova, M.D., Polyakov, V.I., Khomich, A.V., Rukovishnikov, A.I., Druz, B.L., and Zaritskii, I.M., Electrochemical Properties of Amorphous Nitrogen-containing Hydrogenated Diamondlike-Carbon Films, Russ. J. Electrochem., 2007, vol. 43, p. 1008.]
Плесков, Ю.В., Кротова, М.Д., Ральченко, В.Г., Хомич, А.В., Хмельницкий, Р.А. Электроды из синтетического алмаза: фотоэлектрохимическое поведение отожженных в вакууме пленок нелегированного поликристаллического алмаза. Электрохимия. 2005. Т. 41. С. 343. [Pleskov, Yu.V., Krotova, M.D., Ralchenko, V.G., Khomich A.V., and Khmelnitskii R.A., Synthetic Diamond Electrodes: Photoelectrochemical Behavior of Vacuum-Annealed Undoped Polycrystalline Diamond Films, Russ. J. Electrochem., 2005, vol. 41, p. 304.]
Плесков, Ю.В., Кротова, М.Д., Елкин, В.В., Екимов, Е.А. Электрохимическое поведение нового электродного материала-компакта из легированного бором синтетического алмаза. Электрохимия. 2016. Т. 52. С. 3. [Pleskov Yu.V., Krotova M.D., Elkin V.V., and Ekimov E.A., Electrochemical Behavior of New Electrode Material: Compact of Boron-doped Synthetic Diamond, Russ. J. Electrochem., 2016, vol. 52, p. 1.]
Ekimov, E.A., Sidorov, V.A., and Rakhmanina, A.V., High-Pressure Synthesis and Characterization of Superconducting Boron-Doped Diamond, Sci. Technol. Adv. Mater., 2006, vol. 7, p. S2–S6.
Ekimov, E.A., Sadykov, R.A., and Gierlotka, S., A High-Pressure Cell for High Temperature Experiments in a Toroid-Type Chamber, Instrum. Exp. Tech., 2004, vol. 47, p. 276.
Brazhkin, V.V., Ekimov, E.A., Lyapin, A.G., Popova, S.V., Rakhmanina, A.V., Stishov, S.M., et al., Lattice parameters and thermal expansion of superconducting boron-doped diamonds, Phys. Rev., 2006, vol. B 74, p. 140502.
Elkin, V.V., Krotova, M.D., and Pleskov, Yu.V., Polarization complex-plane plot of impedance for two-stage charge-transfer reaction complicated with an intermediate adsorption (by example of benzene oxidation at boron-doped diamond electrode), Electrochim. Acta, 2014, vol. 144, p. 412–418.
Плесков, Ю.В., Кротова, М.Д., Елкин, В.В., Варнин, В.П., Теремецкая, И.Г. Окисление бензола на аноде из легированного бором алмаза: исследование методом электрохимического импеданса. Электрохимия. 2011. Т. 47. С. 1043. [Pleskov Yu.V., Krotova M.D., Elkin V.V., Varnin, V.P., and Teremetskaya, I.G., Benzene Oxidation at Boron_Doped Diamond Anode: an Electrochemical_Impedance Spectroscopy Study, Russ. J. Electrochem., 2011, vol. 47, p. 973.]
Pleskov, Yu.V., Krotova, M.D., Elkin, V.V., and Ekimov, E.A., Electrochemical Behaviour of Boron-doped Diamond Compacts—a New Electrode Material, Electrochim. Acta, 2016, vol. 201, p. 268.
Денисова, А.Е., Плесков, Ю.В. Электроаналитическое определение ЭДТА на тонкопленочном аноде из легированного бором поликристаллического алмаза. Электрохимия. 2008. Т. 44. С. 1166. [Denisova, A.E. and Pleskov, Yu.V., Electrooxidation of Ethylenediaminetetraacetic Acid at a Polycrystalline Boron-doped Diamond Anode, Russ. J. Electrochem., 2008, vol. 44, p. 1083.]
Дополнительные материалы отсутствуют.