Электрохимия, 2019, T. 55, № 3, стр. 294-299
Определение сульфита в вине с применением дифференциальной импульсной полярографии
Г. Сомер a, *, Ш. Калайчи a, Ю. Йилмаз a
a Университет Гази, Химический факультет
Анкара, Турция
* E-mail: gsomer@gazi.edu.tr
Поступила в редакцию 19.02.2018
После доработки 04.07.2018
Принята к публикации 25.07.2018
Аннотация
В настоящем исследовании для определения сульфита в винах разработан новый и простой метод дифференциальной импульсной полярографии. Для определения сульфита использовали его полярографический пик. Полярограммы сульфита снимали в различных электролитах при различных значениях pH в присутствии или при отсутствии вина для определения наилучших рабочих условий. Оказалось возможным определение 2 × 10–6 M сульфита при pH 4 в электролите HAc-NaAc. Данный метод применим к различным винам и пригоден для определения свободного и связанного сульфита. Полученные результаты также сравнивали с данными йодометрического метода, который использует Турецкий институт стандартизации (TSE).
ВВЕДЕНИЕ
Определение сульфита играет важную роль, поскольку его используют в некоторых пищевых продуктах в качестве консерванта. Как известно, повышенное содержание сульфита в пище создает проблемы для здоровья [1]. Таким образом, его точное определение является жизненно важным. Цель настоящего исследования представляла собой разработку нового и простого метода определения сульфита в винах. Для этой цели был разработан метод дифференциальной импульсной полярографии (ДИП), для определения сульфита использовали его полярографический пик. Результаты, получаемые этим методом, отличаются высокой воспроизводимостью, при этом оказывается возможным определение очень низких концентраций. Исследована наилучшая среда для определения сульфита в присутствии или при отсутствии вина. Используемый прибор не является дорогостоящим.
Согласно одному из косвенных методов анализа [2] для определения сульфита в воздушной среде воздух пропускали через раствор селенита в течение 10 мин, и SO2, прореагировавший с селенитом, определяли с применением дифференциальной импульсной полярографии. Содержание в воздухе более 5 мг/м3 диоксида серы классифицируется как показатель кислотного дождя.
Для определения сульфита предложено несколько методов, таких как йодометрическое титрование [3], спектрофотометрические методы [4, 5], высокоэффективная жидкостная хроматография (ВЭЖХ) [6], проточно-инжекционный анализ посредством хемилюминесценции (ПИА‑ХЛ) [7, 8] и некоторые электрохимические методы [9–11].
В одном из наших определений сульфита использована дифференциальная импульсная полярография, и определены следовые количества сульфита прямыми и косвенными методами [12]. Сульфит и тиосульфат в нефти были определены с применением дифференциальной импульсной полярографии [13]. В [14] для определения сульфита разработан новый метод электровосстановления. В спектрофотометрическом методе [15] использовано поглощение полианилина при 550 нм, поскольку оно изменяется в зависимости от концентрации сульфита. Данный метод применен для определения сульфита в вине. Проточно-инжекционный анализ также был применен [16] для определения сульфита в красном и белом вине с использованием бромкрезолового зеленого в качестве индикатора. Сульфит в вине определяли методом вольтамперометрии с линейной разверткой потенциала [17]. Определение полного содержания сульфита в вине осуществляли после окисления образца хромат-ионом [18].
МАТЕРИАЛЫ И МЕТОДЫ
Приборы
Использовали полярографический анализатор (PAR 174 A), оборудованный таймером ртутных капель PAR. Период капания электрода находился в диапазоне от 2 до 3 с (2.35 мг/с). Электролитическая ячейка Калоусека с насыщенным каломельным электродом (нас. к. э.) и жидкостным соединением была использована в трехэлектродной конфигурации. Противоэлектрод представлял собой платиновую проволоку. Полярограммы регистрировали, используя самописец Linseis (LY 1600) X-Y при продолжительности жизни капли 1 с, скорости развертки потенциала 5 мВ/с и амплитуды импульса 50 мВ.
Реагенты
Все использованные химические реагенты имели категорию ч. д. а. Для получения всех растворов использовали троекратно дистиллированную воду. Растворы 10–3 M и более разбавленные получали перед каждым применением во избежание процесса старения раствора.
Ртуть, используемую в ртутном капельном электроде, получали от компании Merck (Дармштадт, Германия). Загрязненную ртуть очищали, последовательно пропуская ее через колонки с разбавленной HNO3 (3.0 M) и водой в форме мелких капель, полученных с помощью платинового сита. Собранную ртуть сушили между листами фильтровальной бумаги. Перед использованием снимали дифференциальную импульсную полярограмму данной ртути, чтобы подтвердить отсутствие примесей. 1 М раствор ацетатного буфера (HAc/Ac) получали, добавляя 6 г NaOH, промытого дистиллированной водой для удаления образующегося карбоната, в 57 мл 1 M HAc и доводя объем до 1 л.
Получение раствора 0.2 M сульфита
Высушенный Na2SO3 (26.8 г) растворяли в 1 л деаэрированной дистиллированной воды. Для защиты сульфита от окисления воздухом и восстановления присутствующего сульфата добавляли амальгамированные ртутью гранулы цинка. Для стандартизации раствора смешивали 50.0 мл 0.048 M I2, 2.3 мл HCl и 10.0 мл ${\text{SO}}_{3}^{{2 - }};$ йод, прореагировавший с сульфитом, определяли посредством титрования избытка йода стандартизированным раствором тиосульфата в присутствии крахмала. Данный раствор стандартизировали после определенных периодов, когда на полярограмме появлялся пик цинка от восстановителя Джонса.
Получение раствора 0.1 M тиосульфата
В 1 л дистиллированной воды растворяли 26.8 г Na2S2O3. Для его стандартизации использовали KIO3. Первичный стандарт KIO3 (0.64 г) растворяли в дистиллированной воде в колбе объемом 250 мл. Отбирали 50 мл раствора, добавляли 2 г KI и 10 мл 1.0 M HCl и титровали раствором тиосульфата до светло-желтого цвета раствора. Затем добавляли 3 мл крахмала и титровали до обесцвечивания раствора.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Сульфит используют в производстве вина по многим причинам. Сладкие и свежеприготовленные вина склонны к скисанию. Сульфит защищает вино в процессе его производства от окисления кислородом воздуха. Сахар в винах такого рода может превращаться в уксусную и молочную кислоты в присутствии аэробных бактерий. При этом вкус и цвет вина изменяются. Сульфит воздействует на эти бактерии и кислород воздуха и, таким образом, защищает вино. Он улучшает вкус вина посредством удаления ацетальдегида, который образуется в процессе производства вина.
Если в процессе производства вина не использовать сульфит, качество цвета изменяется, и вино приобретает сине-фиолетовый цвет. Сульфит сохраняет цвет вина и улучшает его ценность. Для этой цели обычно используют сульфит натрия или бисульфит натрия. Это не является столь важным для белого вина. Количество сульфита в вине является показателем его качества и, таким образом, вино необходимо постоянно контролировать на содержание в нем сульфита. В настоящей работе сделана попытка разработки метода для определения содержания сульфита в разнообразных винах. Допустимое содержание сульфита в вине составляет от 200 до 400 м. д.
Предварительные эксперименты (полярографическое поведение сульфита)
Для определения сульфита в вине с применением дифференциальной импульсной полярографии должны быть выявлены оптимальные условия его определения. Для этой цели необходимо выполнить некоторые предварительные эксперименты. Устойчивость сульфита в различных средах представляет собой важный фактор, поскольку он может выступать в качестве восстановителя.
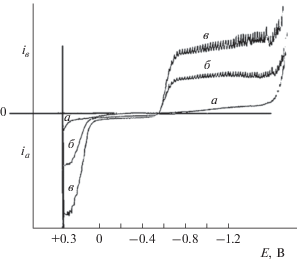
Как известно, с применением дифференциальной импульсной полярографии невозможно определить природу полярографического пика (является ли он катодным или анодным). Для этой цели должна быть применена постояннотоковая полярография. В случае постояннотоковой полярографии волна сульфит-иона наблюдается в растворах 0.1 M HAc-NaAc при различных значениях pH от 1 до 7, а также в растворах 0.1, 1, 2 и 4 M HCl. Было показано, что во всех данных электролитах фиксируется катодный пик сульфита (рис. 1), причем потенциал изменяется в направлении от положительных (+0.3 В) к отрицательным значениям, и анодная волна сульфита присутствует около +0.1 В, а катодная волна около ‒0.6 В.
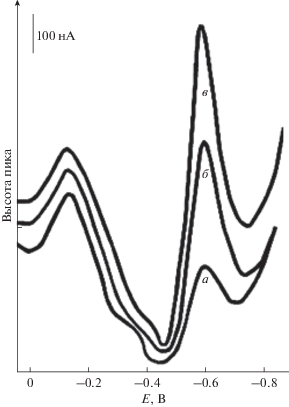
Рис. 1.
Постояннотоковая полярограмма сульфита в растворах: a – 10 мл HAc-NaAc (pH 4); б – a + 0.05 мл 0.19 M ${\text{SO}}_{3}^{{2 - }},$ в – б + 0.05 мл 0.19 M ${\text{SO}}_{3}^{{2 - }}.$
Далее необходимо установить наилучшую среду для его чувствительного определения. Для этой цели полярографический пик сульфита исследован в различных электролитах: в 4, 2, 1 и 0.1 M HCl, а также в электролите 0.1 M HAc-NaAc при значениях pH 2–6. Было обнаружено, что при определении сульфита в кислом растворе всегда возникает отрицательная ошибка, поскольку в кислом растворе сульфита образуется SO2, который выделяется из раствора при пропускании газообразного азота. Такую же ошибку авторы наблюдали в предшествующих исследованиях по определению сульфита в абрикосах [12]. Возможная реакция в кислом растворе может быть представлена следующим образом:
Поскольку в кислой среде происходит потеря сульфита в форме SO2, поведение сульфита должно быть исследовано в более основных растворах, таких как 0.1 M HAc, при значениях pH, составляющих 4, 5, 6 и 7. Согласно наблюдениям, пик был максимальным при pH 4, а при дадьнейшем увеличении значения pH высота пика уменьшалась, и пик смещался в сторону более отрицательных потенциалов; при pH выше 7 пик не наблюдался. Таким образом, для определения сульфита использовали раствор ацетатного буфера с pH 4, в котором пик наблюдался при –0.6 В. Пик сульфита, получаемый в этой среде, был наиболее высоким, и его высота не изменялась при пропускании газообразного азота в течение по меньшей мере одного часа. В этой среде оказалось возможным определение содержания сульфита порядка 1 × 10–5 ((1.12 ± 0.06) × 10–5 M).
Определение сульфита в вине
После нахождения оптимальной среды для определения сульфита его вводили в вино. Как известно, качество вина зависит от содержания в нем сульфита, дешевые вина содержат небольшое его количество, дорогие вина – более высокое. В настоящем исследовании содержание сульфита определяли в винах обоих типов. Здесь необходимо отметить, что в вине присутствует сульфит двух типов: это – свободный сульфит, который был добавлен в вино, а второй тип представляет собой серу, связанную с органическими молекулами в вине. Этот сульфит может становиться свободным при некоторых условиях, его количество также имеет значение и должно быть определено. В результате в обоих типах вина должны быть определены два типа сульфита.
Определение сульфита в дешевых винах
Здесь два типа вин (A) и (B) были исследованы в отношении содержания в них свободных и связанных сульфит-ионов.
Сульфит в дешевом вине (A) определяли в двух вариантах: во-первых, немедленно после открытия бутылки с вином и, во-вторых, после шестимесячного выдерживания бутылки с вином в открытом состоянии. Кроме того, поскольку образцы вина содержат два типа сульфита (свободный и связанный), они также были определены для каждого вина.
Определение свободного сульфита в вине (A) сразу после открытия бутылки
В 10 мл HAc (pH 4) добавляли 0.5 мл вина сразу после открытия бутылки, снимали полярограмму, а затем добавляли 0.1 мл раствора 1.3 × 10–3 M сульфита в качестве стандартного раствора. Результат составил 24 ± 4 мг в 1 л вина (доверительный интервал 90% для N = 3) (рис. 2).
Определение свободного сульфита в вине (A), выдержанном в течение 6 месяцев в открытой бутылке
2 мл вина типа (A), выдержанного в течение 6 мес. в открытой бутылке, добавляли в 8 мл буферного раствора HAc (pH 4), а затем 2 раза добавляли по 0.05 мл стандартного раствора 1.3 × × 10–3 M сульфита.
Найденное количество составляло 1.9 ± 0.3 мг в 1 л вина, показывая потерю сульфита в форме SO2 в течение времени выдерживания.
Определение общего сульфита (сумма связанного и свободного) в дешевом вине (тип A)
Содержащаяся в вине сера связана с органическими молекулами. Однако она может высвобождаться по ряду причин, что может изменить вкус и восприятие вина, а также снизить его качество. Такое вино может представлять опасность для страдающих астмой людей. Содержание сульфита этих двух типов дает представление о качестве вина. Для данного определения сначала в вино добавляли NaOH, чтобы высвободить серу, связанную с органическими молекулами. В 50 мл вина добавляли 25 мл 1 M NaOH и через 15 мин добавляли 10 мл 25% (2 M) H2SO4, доводя до значения pH 2. Снимали полярограмму в электролите HAc (pH 4) и посредством стандартной добавки сульфита можно было определить общий сульфит (связанный и свободный) (рис. 3). Результат составил 33 ± 2 мг/л (табл. 1). Такую же процедуру применяли для другого дешевого вина (B) и двух дорогих вин (C и D). Все результаты кратко представлены в табл. 2.
Рис. 3.
Определение общего (свободного и связанного) сульфита в дешевом вине (A): a – 9 мл Hac-NaAc (pH 4) + 1 мл дешевого вина (A); б – a + 1.3 × 10–3 M 0.1 мл ${\text{SO}}_{3}^{{2 - }};$ в – б + 1.3 × 10–3M 0.2 мл ${\text{SO}}_{3}^{{2 - }}.$
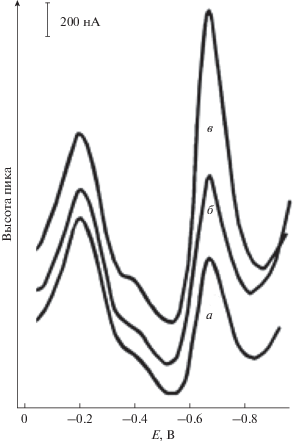
Таблица 1.
Определение содержания свободного и общего сульфита в дешевом вине (A)
| Образец A (дешевое вино) | χ, мг/л | s | $\chi \pm {{ts} \mathord{\left/ {\vphantom {{ts} {\sqrt N }}} \right. \kern-0em} {\sqrt N }},$ мг/л |
|---|---|---|---|
| Немедленно после открытия бутылки | 24 | 4 | 24 ± 4 |
| После 6-месячного выдерживания в открытой бутылке | 1.9 | 0.2 | 1.9 ± 0.3 |
| Общий сульфит (свободный и связанный) | 33 | 1 | 33 ± 2 |
Таблица 2.
Определение содержания свободного и общего сульфита в винах A, B, C и D
| Образец | Свободный сульфит, мг/л $\chi \pm {{ts} \mathord{\left/ {\vphantom {{ts} {\sqrt N }}} \right. \kern-0em} {\sqrt N }}$ | Общий сульфит, мг/л $\chi \pm {{ts} \mathord{\left/ {\vphantom {{ts} {\sqrt N }}} \right. \kern-0em} {\sqrt N }}$ |
|---|---|---|
| A (дешевое вино) | 24 ± 4 | 33 ± 2 |
| B (дешевое вино) | 23 ± 1 | 31 ± 1 |
| C (дорогое вино) | 56 ± 2 | 105 ± 8 |
| D (дорогое вино) | 110 ± 5 | 196 ± 2 |
Йодометрический метод для определения общего сульфита в вине
Чтобы сравнить результаты, полученные посредством ДИП, авторы попытались определить количество сульфита йодометрическим методом, поскольку йодометрический метод применяется некоторыми компаниями для определения сульфита в вине. Для этой цели была осуществлена следующая процедура. В 50 мл вина добавляли 25 мл 4% (1 M) NaOH, и цвет раствора становился зеленым; через 15 мин добавляли 10 мл (2 M) 25% H2SO4 и 2–3 мл 1% крахмала в качестве индикатора, значение pH составляло 2, и цвет раствора становился красным. Таким образом, в процессе титрования среда должна быть кислой, чтобы можно было наблюдать изменение цвета. Титрование осуществляли стандартизированным раствором йода до получения синего цвета. Результаты представлены в табл. 3 для сравнения с другими упомянутыми результатами. Как можно видеть, йодометрические результаты были всегда меньше, чем результаты, полученные полярографическими методами. Это может быть обусловлено потерей SO2 в течение продолжительного встряхивания, поскольку титрование должно быть осуществлено при меньших значениях pH.
Таблица 3.
Сравнение общего содержания сульфита, определенного методами йодометрии и дифференциальной импульсной полярографии
| Образец | Методы | Общий сульфит, мг/л $\chi \pm {{ts} \mathord{\left/ {\vphantom {{ts} {\sqrt N }}} \right. \kern-0em} {\sqrt N }}$ |
|---|---|---|
| A (дешевое вино) | ДИП | 33 ± 2 |
| Йодометрия | 31 ± 3 | |
| B (дешевое вино) | ДИП | 31 ± 2 |
| Йодометрия | 25 ± 8 | |
| C (дорогое вино) | ДИП | 105 ± 8 |
| Йодометрия | 84 ± 18 | |
| D (дорогое вино) | ДИП | 196 ± 2 |
| Йодометрия | 123 ± 17 |
ВЫВОДЫ
В настоящей работе определяли сульфит, добавленный в вино, и сульфит, связанный с органическими молекулами в вине. Для определения сульфита, присутствующего в вине, разработан новый чувствительный метод дифференциальной импульсной полярографии. Полученные результаты отличаются высокой воспроизводимостью, поскольку при использовании ртутного капельного электрода поверхность электрода постоянно обновляется, и поведение электрода не зависит от его предыстории. Оказалось возможным определение 2 × 10–6 M (s/N = 3) сульфита при pH 4 в электролите HAc-NaAc.
Показано, что фиксируемый полярографический пик представлял собой катодный пик сульфита для всех исследованных электролитов и значений pH.
Полученные результаты сопоставлены с данными йодометрического метода, который применяет Турецкий институт стандартизации.
Список литературы
Fazio, T. and Warner, C.R., A review of sulphites in foods: Analytical methodology and reported findings, Food Addit. Contam., 1990, vol. 7 (4), p. 433.
Somer, G. and Kocak, A., Determination of atmospheric sulfur dioxide by differential-pulse polarography using selenite, Analyst, 1993, vol. 118, p. 657.
Monnier, G. and Williams, S., Determination of sulfur dioxide, Analyst, 1972, vol. 95, p. 119
Decnop-Weever, L.G. and Kraak, J.C., Determination of sulphite in wines by gas-diffusion flow injection analysis utilizing spectrophotometric pH-detection, Anal. Chim. Acta, 1997, vol. 337, p. 125.
Cosano, J.S., Luque de Castro, M.D., and Valcarcel, M., Automatic continuous-flow determination of sulphite in the presence of a high concentration of thiosulphate Anal. Chim. Acta, 1995, vol. 302, p. 269.
Pizzoferrato, L., Di Lullo, G., and Quattrucci, E., Determination of free, bound and total sulphites in foods by indirect photometry-HPLC, Food Chem., 1998, vol. 63 (2), p. 275.
Qin, W., Zhang, Z., and Zhang, C., Reagentless chemiluminescence flow sensor for sülfite, Anal.Chim. Acta, 1998, vol. 361, p. 201.
Amatatongchai, M., Sroysee, W., Chairam, S., and Nacapricha, D., Simple flow injection for determination of sulfite by amperometric detection using glassy carbon electrode modified with carbon nanotubes–PDDA–gold nanoparticles, Talanta, vol. 133, 2015, p. 134.
Garber, R.W. and Wilson, C.E., Determination of atmospheric sulfur dioxide by differential pulse polarography, Anal. Chem., 1972, vol. 44 (8), p. 1357.
Umiker, K.J., Mora, M.J., and Cheng, I.F., Aqueous sulfur species determination using differential pulse polarography, Microchem. J., 2002, vol. 73, p. 287.
Pournaghi-Azar, M.H., and Sabzi, R.E., Electrocatalytic Oxidation of Sulfite on a Cobalt Pentacyanonitrosylferrate Film Modified Glassy Carbon Electrode, Electroanalysis, 2004, vol. 16 (10), p. 860.
Yilmaz, T.U. and Somer, G., Determination of trace sulfite by direct and indirect methods using differential pulse polarography, Analytica Chim Acta, 2007, vol. 603, p. 30.
Sid Kalal, H., Ghadiri, M., Miran Beigi, A.A., and Seyed Sadjadi, S.A., Simultaneous determination of trace amounts of sulfite and thiosulfate in petroleum and its distillates by extraction and differential pulse polarography, Anal. Chim. Acta, 2004, vol. 502 (1), p. 133.
Isaac, A., Wain, A.J., Compton, R.G., Livingstone, C., and Davis, J., A novel electroreduction strategy for the determination of sulfite, Analyst, 2004, vol. 130, p. 1343.
De Marcos, S., Alcubierre, G.J., and Castillo, J.R., Reagentless system for sulphite based on polyaniline, Anal. Chim. Acta, 2004, vol. 502 (1), p. 7.
Renard, J., Kubes, G., and Bolker, H., Polarographic determination of sulfur compounds in pulping liquors, Anal. Chem., 1975, vol. 47 (8), p. 1347.
Scampicchio, M., Lawrence, N.S., Arecchi, A., and Mannino, S., Determination of Sulfite in Wine by Linear Sweep Voltammetry, Electroanalysis, 2008, vol. 20 (4), p. 444.
Koch, M., Köppen, R., Siegel, D., Witt, A., and Nehls, I., Determination of Total Sulfite in Wine by Ion Chromatography after In-Sample Oxidation.BAM Federal Institute for Materials Research and Testing, J. Agric. Food Chem., 2010, vol. 58 (17), p. 9463.
Дополнительные материалы отсутствуют.